1. 서 론
코발트는 강자성, 경도, 내부식 및 내마모성이 뛰어나 각종 산업소재 분야에서 대체할 수 없는 전략적 금속으로 간주되고 있다. 현재 코발트 세계 공급량의 절반 가량이 리튬 배터리 제조를 위해 사용되고 있으며 나머지는 초합금, 촉매, 핵 분야등에 이용된다1). 니켈은 코발트와 비슷한 물리적 성질을 지녔으며 리튬이온 배터리(LIB), 니켈수소 배터리(NiMH) 및 니켈 카드뮴 배터리(Ni-Cd) 등에서 전극재료로 사용된다2,3,4). 최근 리튬이온 배터리 시장이 급속히 성장하면서 니켈과 코발트에 대한 수요가 폭발적으로 증가하고 있다5,6,7). 니켈과 코발트를 함유한 광석이 고갈되는 현실을 감안하면 폐배터리와 같은 2차 자원에 함유된 두 금속을 고순도로 회수할 수 있는 공정의 개발이 필요하다. 특히 니켈과 코발트와 같이 화학적 성질이 비슷한 금속을 고순도로 회수하기 위해서는 두 금속을 효율적으로 분리하는 것이 중요하다8,9).
일반적으로 수용액에서 금속이온을 분리하기 위해 용매추출과 이온교환이 널리 이용되고 있다10,11,12,13,14,15,16). 용매추출은 침출액에 용해되어 있는 금속이온을 선택적으로 분리하여 농축할 수 있는 장점이 있다. 유기인산계 추출제를 사용하여 묽은 염산 또는 황산용액에서 코발트와 니켈을 분리할 수 있는 여러 공정이 발표되었다17,18,19). 수용액의 pH가 3에서 6사이의 조건에서 두 금속을 유기인산계 추출제로 분리하기 위해서는 용액의 pH 조절이 매우 중요하며, 이러한 목적을 위해 유기인산계 추출제를 비누화시켜 사용한다.
최근 친환경적 용매로 각광받고 있는 이온성액체의 가장 큰 장점은 양이온과 음이온의 구조를 사용 목적에 따라 선택적으로 합성하여 사용할 수 있다는 점이다. 또한 낮은 휘발성, 높은 이온 전도성, 전기화학적 안정성, 열적 안정성 등의 우수한 특성을 지니고 있다20,21). 유기인산계 추출제인 D2EHPA, PC88A, Cyanex 272의 음이온을 Aliquat 336의 염소이온으로 치환시킨 이온성액체는 상용화 추출제로 제조가 가능하므로 기존의 이온성액체에 비해 경제성이 우수하다. 또한 금속이온뿐만 아니라 수소이온도 추출되므로 비누화를 하지 않아도 용액의 pH를 조절할 수 있는 장점이 있다22,23,24). 수용액에서 SCN-은 니켈보다는 코발트와 착물을 형성하려는 경향이 강하므로 두 금속이온의 분리에 이용이 가능하다25). 이러한 특성을 활용해 Aliquat 336의 염소이온을 SCN-으로 치환하면 코발트와 니켈이 혼합된 용액에서 코발트를 선택적으로 추출할 수 있다26).
본 논문에서는 유기인산 추출제와 Aliquat 336을 반응시켜 합성한 이온성액체를 추출제로 사용하여 묽은 염산용액에서 코발트와 니켈의 분리를 위한 추출실험을 수행했다. 이러한 목적을 위해 유기인산계 추출제로 D2EHPA, PC88A, Cyanex 272, Cyanex 301을 선택하여 Aliquat 336과 반응시켜 이온성액체로 사용했다. 이러한 이온성액체에 TBP를 첨가하는 경우 코발트와 니켈의 추출 및 분리에 미치는 영향에 대해서도 조사했다. 또한 Aliquat 336의 염소이온을 SCN-으로 치환한 이온성액체(ALi-SCN)를 사용하여 두 금속의 분리를 조사했다. 유기인산계 추출제로 합성한 이온성액체중 Cyanex 301로 합성한 이온성액체의 경우 두 금속의 선택도는 추출조건에 의존하였다. 이에 반해 ALi-SCN로 추출하면 코발트가 선택적으로 추출되어 두 금속을 분리하는 것이 가능했다. 코발트와 니켈의 분리에 미치는 SCN-의 영향을 조사하기 위해 수상에 NH4SCN을 첨가한 다음 Aliquat 336으로 추출하여 ALi-SCN의 실험결과와 비교했다.
2. 실험 재료 및 방법
2.1. 실험재료
본 연구를 위해 시약급 염화코발트(CoCl2, Junsei Chemical Co., Japan, 99%)와 염화니켈(Yakuri pure chemicals co., Ltd., Japan, 99%)을 2차 증류수에 용해시켜 두 금속의 혼합용액을 제조했다. 혼합용액에서 코발트와 니켈의 농도는 모두 100 ppm으로 고정했다. 또한 염산(Daejung chemicals & metals Co. Ltd., Korea., 35%)과 수산화나트륨용액(Duksan Co. Ltd., Korea., 93%)을 사용해 용액의 pH를 조절했다.
이온성액체를 제조하기 위해 유기인산 추출제인 Cyanex 272(Cytec Inc., Canada., 85%), PC88A(Daihachi Chem. Inc., 95%), D2EHPA(Daihachi Chem. Inc., 95%), Cyanex 301(Cytec Inc., Canada., 70%)과 Aliquat 336(BASF Co. Ltd., 93%)을 문헌에 보고된 방법으로 각각 반응시켰다27,28). 또한 이온성액체인 Aliquat 336을 NH4SCN(Daejung chemicals & metals Co. Ltd., Korea., 99%)과 반응시켜 Aliquat 336의 음이온을 SCN-으로 치환했다26). 용매추출시 제 3상이 형성되는 것을 억제하기 위해 개질제로 10%의 decanol (Daejung Chemical & Metals Co., Ltd., 98%)을 유기상에 첨가했고 희석제로는 등유(Daejung chemicals & metals Co. Ltd., Korea., 100%)를 사용했다. 본 연구에서 사용된 추출제 및 희석제는 시약급으로 정제하지 않고 그대로 사용했다.
2.2. 실험방법
코발트와 니켈이 혼합된 수상 20 ml와 추출제 20 ml를 50 ml 광구병에 넣고 상온에서 wrist action shaker(model 75, USA)를 이용하여 30분간 교반했다. 교반이 끝난 후 분액여두로 수상과 유기상을 분리 했고, 이 때 수상의 평형 pH는 pH미터(Fisher Accumet pH model 620)로 측정했다. 또한 수상에 존재하는 금속의 농도는 유도결합 플라즈마 원자방출분광기(Inductively Coupled Plasma-Optical Emission Spectometer)로 측정했다. 추출 후 두 상의 부피에 변화가 없다고 가정하여 금속의 추출률(Extraction percentage)과 분리인자(Separation factor)를 각각 다음 식으로 계산했다29).
|
$$\mathrm{Extraction}\;\mathrm{percentage}\;=\frac{\mathrm{Mass}\;\mathrm{of}\;\mathrm{metal}\;\mathrm{in}\;\mathrm{the}\;\mathrm{organic}\;\mathrm{phase}\;\mathrm{after}\;\mathrm{extraction}}{\mathrm{initial}\;\mathrm{mass}\;\mathrm{of}\;\mathrm{metal}\;\mathrm{in}\;\mathrm{the}\;\mathrm{aqueous}\;\mathrm{phase}\;\mathrm{before}\;\mathrm{extraction}}\times100$$
|
(1)
|
|
$$\mathrm{Separation}\;\mathrm{factor}\;=\frac{{\mathrm D}_{\mathrm A}}{{\mathrm D}_{\mathrm B}}$$
|
(2)
|
분리인자에서 상대적으로 추출률이 높은 금속의 분배계수(Distribution coefficient)를 DA, 추출률이 낮은 금속의 분배계수(Distribution coefficient)를 DB로 나타냈다.
3. 결과 및 고찰
3.1. 평형 pH가 두 금속의 분리에 미치는 영향
D2EHPA, PC88A, Cyanex 272를 Aliquat 336과 반응시켜 합성한 이온성액체인 ALi-D2, ALi-PC, ALi-CY272을 추출제로 사용했을 때, 평형 pH에 따른 두 금속의 추출 거동을 조사하기 위해 수상의 초기 pH를 3에서 5로 변화시켰다. 이 때 추출제의 농도는 0.1 M로 고정했으며 실험결과를 Fig. 1에, 평형 pH를 Table 1에 나타냈다. 추출실험 후 수상의 평형 pH는 초기 pH보다 증가했는데, 이는 이온성액체가 금속이온뿐만 아니라 수소이온도 동시에 추출했다는 것을 의미한다. pH가 3에서 5인 염산용액에서 코발트와 니켈이온은 양이온 형태로 존재한다. 따라서 이온성액체에 의한 금속이온과 수소이온의 추출반응을 다음과 같이 나타낼 수 있다22,23,30,31).
|
$${\mathrm{MCl}}_{2\mathrm{aq}}+2{\mathrm R}_4{\mathrm{NA}}_{\mathrm{org}}=2{\mathrm R}_4{\mathrm{NCl}}_{\mathrm{org}}+{\mathrm{MA}}_{2\mathrm{org}}$$
|
(3)
|
|
$${\mathrm R}_4{\mathrm{NA}}_{\mathrm{org}}+{\mathrm H^+}_{\mathrm{aq}}+{\mathrm{Cl}^-}_{\mathrm{aq}}={\mathrm R}_4\mathrm{NA}\cdot{\mathrm{HCl}}_{\mathrm{org}}$$
|
(4)
|
상기 식에서 M2+는 금속이온을, R4NA는 이온성액체를, R4NCl는 Aliquat 336을 나타낸다. 식 (3)을 보면 이온성액체가 금속이온을 추출했을 때 이온성액체의 일부가 Aliquat 336으로 전환되는 것을 알 수 있다. 유기상에 추출된 금속을 탈거한 다음 유기상을 탄산수소나트륨수용액과 접촉시키면 식 (5)반응에 의해 이온성액체가 재생될 수 있다.
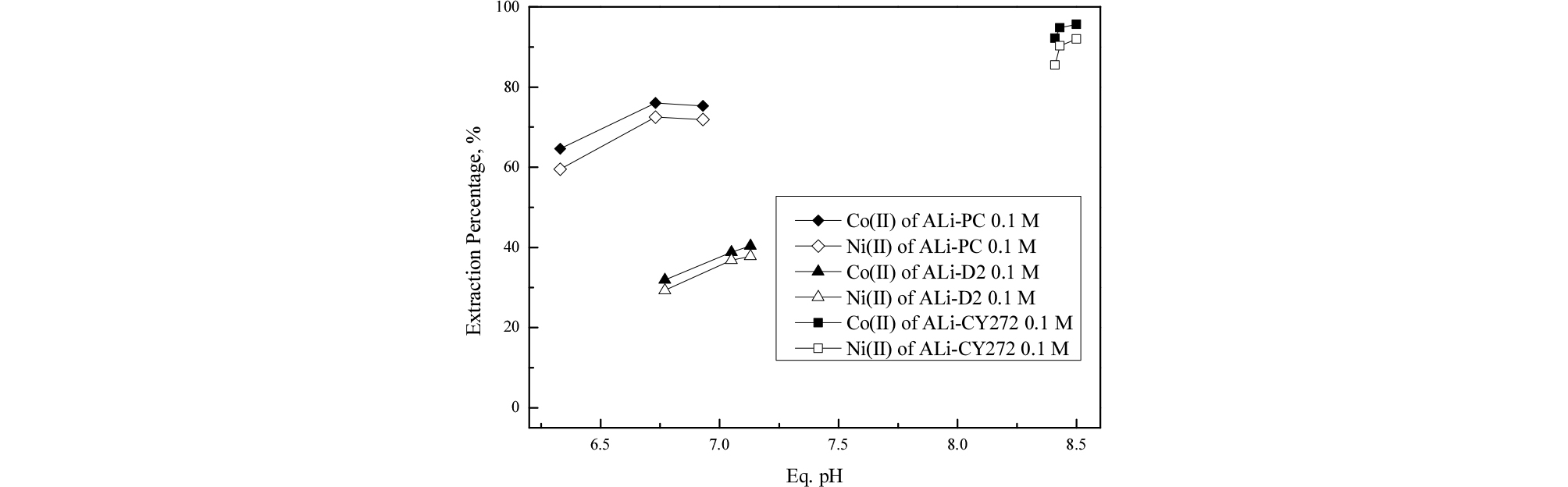
Fig. 1.
Effect of equilibrium pH on the extraction of Co(II) and Ni(II) from HCl solution with ILs ([Ionic liquid] = 0.1 M, [Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
Table 1.
Variation in the equilibrium pH of aqueous phase after extraction with initial pH
|
Initial pH
|
ALi-Cy272
|
ALi-PC
|
ALi-D2
|
|
3
|
8.41
|
6.77
|
6.33
|
|
4
|
8.43
|
7.05
|
6.73
|
|
5
|
8.50
|
7.13
|
6.93
|
|
$${\mathrm R}_4\mathrm{NA}\cdot{\mathrm{HCl}}_{\mathrm{org}}+{\mathrm{NaHCO}}_{3\mathrm{aq}}={\mathrm R}_4{\mathrm{NA}}_{\mathrm{org}}+{\mathrm{NaCl}}_{\mathrm{aq}}+{\mathrm H}_2\mathrm O+{\mathrm{CO}}_2$$
|
(5)
|
본 논문에서 사용한 유기인산 추출제로 제조한 이온성액체는 평형 pH가 증가할수록 두 금속의 추출률이 증가했고 코발트의 추출률이 니켈보다 약간 높았다. 두 금속의 추출률과 평형 pH는 ALi-CY272 > ALi-PC > ALi-D2 순서로 높았다. 평형 pH의 변화폭은 이온성액체의 음이온인 유기인산의 작용기와 관계된다. 본 논문에서 사용한 유기인산 추출제는 약산이므로 수소화되려는 경향이 강하다. 유기인산 음이온의 염기도는 유기인산의 산해리도에 반비례하며 각각의 pKa값을 Table 2에 나타냈다32,33). 해리상수는 Cyanex272 < PC88A < D2EHPA 순으로 높으며, 이는 평형 pH의 결과와 잘 일치한다34).
Table 2.
pKa values of organophosporus acids32,33)
|
D2EHPA
|
PC88A
|
Cyanex272
|
|
pKa
|
3.24
|
4.51
|
6.37
|
0.5 M ALi-CY301를 사용해 용액의 pH에 따른 두 금속의 추출거동을 조사해 Fig. 2에 나타냈다. 평형 pH가 증가함에 따라 코발트의 추출률이 직선적으로 증가했으며, 평형 pH 6 이상의 조건에서는 니켈의 추출률이 코발트보다 높았다. 초기 pH가 3과 4인 조건에서 코발트와 니켈의 분리 가능성을 조사하기 위해 ALi-CY301의 농도를 0.01 M에서 0.1 M 까지 변화시켜 실험한 결과를 Fig. 3에 나타냈다. 혼합용액의 초기 pH가 3인 조건에서 두 금속의 추출률은 비슷하다. 그러나 용액의 초기 pH가 4인 조건에서는 니켈이 코발트보다 잘 추출되었다. 용액의 pH 및 ALi- CY301의 농도에 따른 두 금속의 분리인자의 변화를 Table 3에 나타냈다. 전반적으로 두 금속의 분리인자는 초기 pH 4의 조건에서 높았으며 ALi-CY301의 농도가 0.01 M조건에서 분리인자가 28.5로 가장 높았다. 일반적으로 유기인산 추출제에 의한 코발트와 니켈의 분리에서 Versatic acid 10을 제외하면 대부분 코발트가 선택적으로 추출된다. 따라서 본 논문의 실험결과와 같이 니켈을 선택적으로 추출할 수 있는 Cyanex301으로 제조한 이온성액체는 향후 두 금속을 분리하는 경우 니켈의 선택적 추출에 응용이 가능하다.
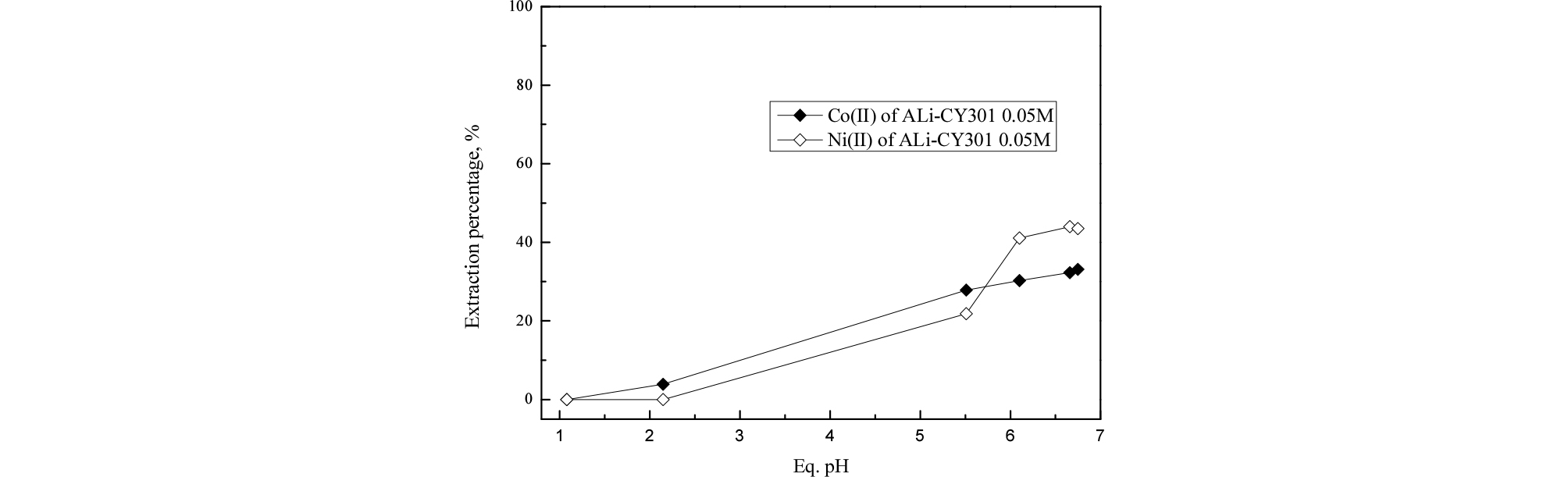
Fig. 2.
Effect of equilibrium pH on the extraction of Co(II) and Ni(II) from HCl solution with ALi-CY301 ([ALi-CY301] = 0.05 M, [Co(II)] = 100 ppm, [Ni (II)] = 100 ppm).
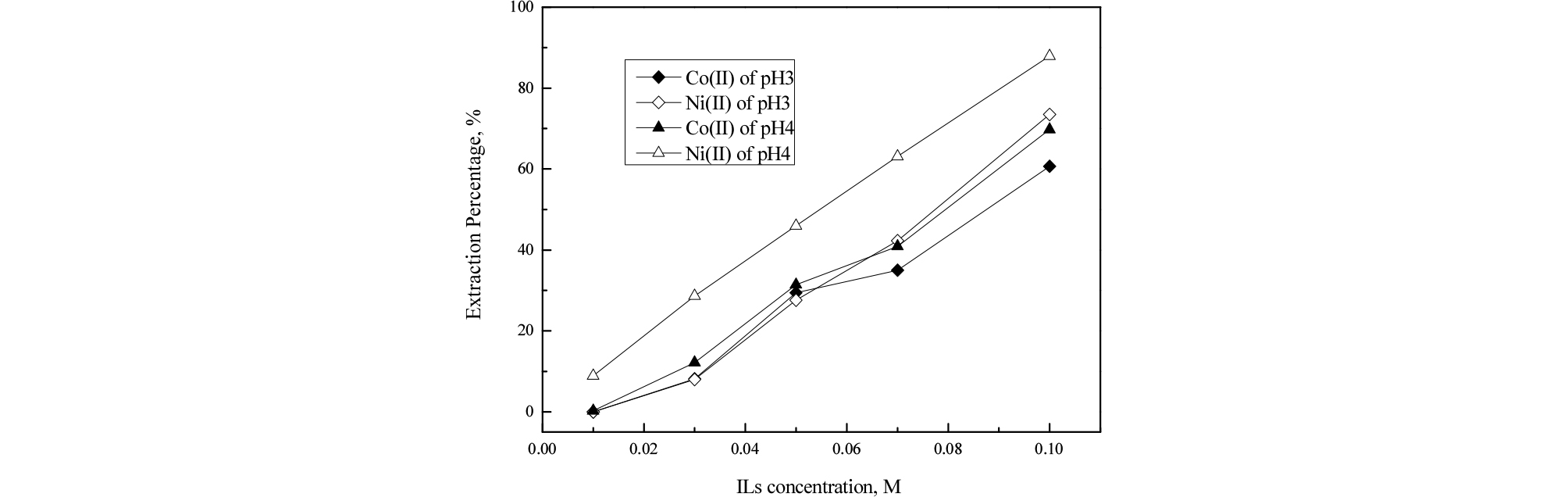
Fig. 3.
Variation in the extraction percentage of Co(II) and Ni(II) from HCl solution with ALi-CY301 concentration ([ALi-CY301] = 0.01 – 0.1 M, [Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
Table 3.
Effect of ALi-CY301 concentration on the separation factor between Co(II) and Ni(II) at initial pH 3 and 4
|
Separation factor
|
|
[ALi-cy301], M
|
pH 3 (Co/Ni)
|
pH 4 (Ni/Co)
|
|
0.01
|
-
|
28.54
|
|
0.03
|
1.03
|
2.87
|
|
0.05
|
1.09
|
1.86
|
|
0.07
|
0.74
|
2.48
|
|
0.1
|
0.56
|
3.15
|
3.2. TBP 농도의 영향
기존 연구에 의하면 유기인산계 추출제와 Aliquat 336으로 합성한 이온성액체에 TBP를 첨가하면 코발트보다 니켈의 추출특성이 향상된다23). 따라서 본 논문에서 합성한 이온성액체에 TBP를 첨가하여 두 금속의 추출 및 분리거동에 미치는 영향을 조사했다. 이를 위해 수상의 초기 pH를 4, 추출제 농도를 0.1 M로 고정했고 TBP 농도를 0.1 M에서 0.5 M까지 변화시켜 실험한 결과를 Fig. 4에 나타냈다. 실험결과 TBP의 농도에 관계없이 두 금속의 추출률은 비슷했다. ALi-PC의 경우에는 TBP를 첨가하지 않은 경우에 비해 코발트와 니켈의 추출률이 각각 18%, 28% 가량 증가했으며, ALi-D2의 경우에는 각각 25%, 12% 감소했다. ALi-PC와 ALi-D2의 경우 TBP를 첨가하면 니켈이 선택적으로 추출되면서 두 금속의 분리인자가 증가했으며, 이는 기존 실험결과와 잘 일치한다23).
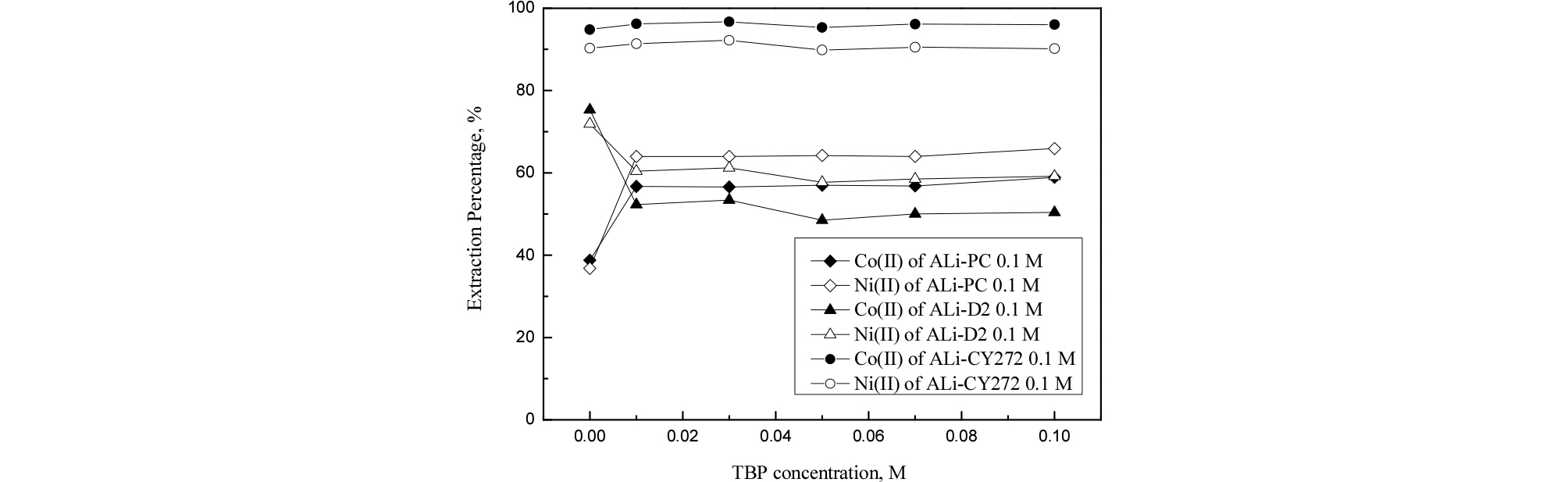
Fig. 4.
Effect of TBP concentration on the extraction of Co (II) and Ni(II) from HCl solution with ILs (Initial pH = 4, [Ionic liquid] = 0.1 M, [Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
3.3. ALi-SCN에 의한 코발트와 니켈의 분리
3.3.1. 평형 pH 및 이온성액체 농도 영향
이온성액체 ALi-SCN을 사용해 코발트와 니켈의 추출거동을 조사했다. 수상의 초기 pH를 1에서 6까지 변화시켜 0.1 M의 ALi-SCN로 추출 실험한 결과를 Fig. 5에 나타냈다. 실험결과 니켈은 전혀 추출되지 않는 반면 코발트는 선택적으로 추출되어 두 금속을 분리하는 것이 가능했다. 또한 ALi-CY272, ALi-CY301, ALi-PC, ALi-D2로 추출한 결과와 달리 ALi-SCN을 사용한 경우 평형 pH는 초기 pH보다 감소했다. 이는 ALi-SCN이 수소이온을 거의 추출하지 않는다는 것을 의미한다. 이온성액체를 추출제로 사용하면 이온성액체의 음이온이 수상으로 이온교환된다. 특히 ALi-SCN을 염산용액과 접촉시키면 염소이온이 SCN-에 비해 전하밀도가 크므로 이온교환된다. 이러한 조건에서 코발트이온은 수상으로 이동한 SCN-과 음이온성 착물을 형성하여 유기상으로 추출될 수 있다. ALi- SCN에 의한 코발트의 추출반응을 다음과 같이 나타낼 수 있다.
|
$${\mathrm{Co}^{2+}}_{\mathrm{aq}}\;+\;2{\mathrm{Cl}^-}_{\mathrm{aq}}\;+\;4{\mathrm R}_4\mathrm N\times{\mathrm{SCN}}_{\mathrm{org}}\;=\;{({\mathrm R}_4\mathrm N)}_2\mathrm{Co}{(\mathrm{SCN})}_{4\mathrm{org}}+2{\mathrm R}_4\mathrm N\times{\mathrm{Cl}}_{\mathrm{org}}$$
|
(6)
|
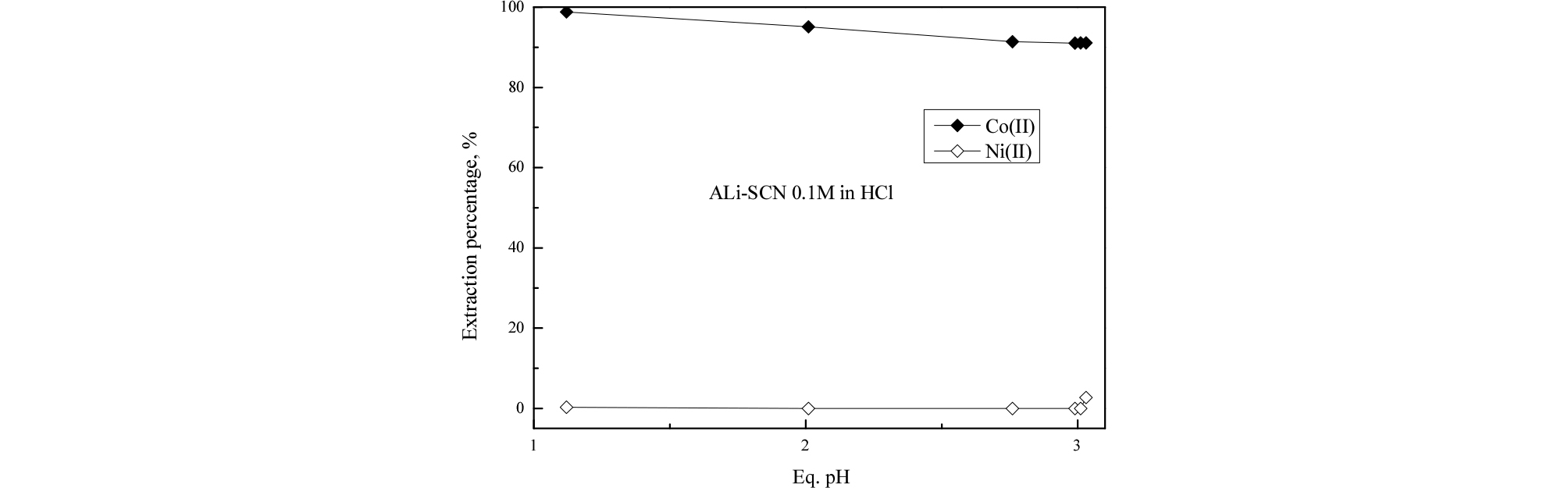
Fig. 5.
Effect of equilibrium pH on the extraction of Co(II) and Ni(II) from HCl solution with 0.1 M ALi-SCN ([Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
SCN-과 코발트 및 니켈의 착물형성상수를 Table 4에 나타냈다35,36). 표를 보면 니켈에 비해 코발트이온이 SCN-와 착물을 형성하려는 경향이 강하다는 것을 알 수 있으며, 이는 본 연구에서 코발트가 선택적으로 추출된 결과와 잘 일치한다.
Table 4.
Complex formation constants of Co(II) and Ni(II) with Cl- and SCN- at 25°C35,36)
|
Reaction
|
log K
|
|
Co2+ + Cl- = CoCl+ |
0.22
|
|
Co2+ + 2Cl- = CoCl2 |
-3.95
|
|
Co2+ + 3Cl- = CoCl3- |
-3.02
|
|
Co2+ + 4Cl- = CoCl42- |
-9.06
|
|
Ni2+ + Cl- = NiCl+ |
-1.29
|
|
Co2+ + SCN- = [CoSCN]+ |
2.5
|
|
Co2+ + 2 SCN- = [Co(SCN)2]
|
1.8
|
|
Co2+ + 3 SCN- = [Co(SCN)3]- |
4.0
|
|
Co2+ + 4 SCN- = [Co(SCN)4]2- |
3.9
|
|
Ni2+ + SCN- = [NiSCN]+ |
2.2
|
|
Ni2+ + 2 SCN- = [Ni(SCN)2]
|
2.4
|
|
Ni2+ + 3 SCN- = [Ni(SCN)3]- |
2.6
|
|
Ni2+ + 4 SCN- = [Ni(SCN)4]2- |
2.1
|
혼합용액의 초기 pH를 2로 고정시키고 ALi-SCN의 농도를 0.01에서 0.16 M로 변화시켜 추출실험한 결과를 Fig. 6에 나타냈다. 상기 이온성액체의 농도범위에서 니켈은 전혀 추출되지 않았으나, 이온성액체의 농도가 증가함에 따라 코발트의 추출률은 증가했으며 추출제 농도 0.16 M 조건에서 두 금속의 완전한 분리가 가능했다.
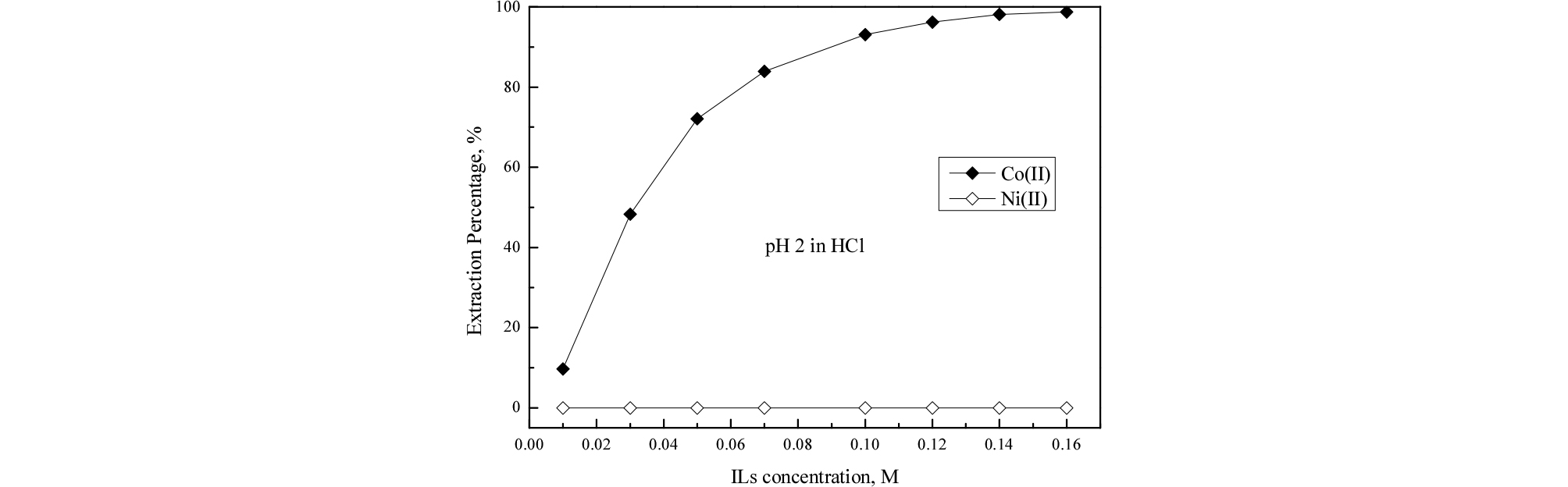
Fig. 6.
Variation in the extraction percentage of Co(II) and Ni(II) from HCl solution with ALi-SCN concentration ([ALi-SCN] = 0.01 - 0.16 M, [Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
3.3.2. NH4SCN의 영향
식 (6)에 의하면 ALi-SCN를 추출제로 사용시 수상으로 이동한 SCN-이 코발트이온과 음이온성 착물을 형성해 다시 유기상으로 추출된다. 따라서 SCN-이 코발트와 니켈의 추출에 미치는 영향을 알아보기 위한 추가 실험을 수행했다. 코발트와 니켈이 함유된 염산용액에 NH4SCN을 첨가한 용액과 첨가하지 않은 용액에 대하여 각각 0.1 M Aliquat 336으로 추출 실험을 수행했으며 실험결과를 Fig. 7에 나타냈다. 두 용액의 초기 pH는 1에서 6까지 변화시켰다. NH4SCN을 첨가하지 않은 염산용액에서 코발트와 니켈 모두 Aliquat 336에 추출되지 않았다. 이는 상기 pH범위에서 코발트가 음이온을 형성하는데 필요한 염소이온의 양이 충분하지 않기 때문이다. 그러나 0.1 M의 NH4SCN이 함유된 혼합용액에서는 코발트가 SCN과 음이온성 착물을 형성해 Aliquat 336에 선택적으로 추출됐고 니켈은 미량 추출됐다. 이와 같이 니켈의 추출률이 낮은 것은 니켈이 SCN-과 착물을 형성하려는 경향이 작고 니켈의 착물이 Ni(SCN)4(H2O)22-로 존재하기 때문이다26). 즉, 니켈 착물에 두개의 물분자가 존재하므로 유기상에 용해되려는 경향이 낮아 추출이 잘 일어나지 않는다.
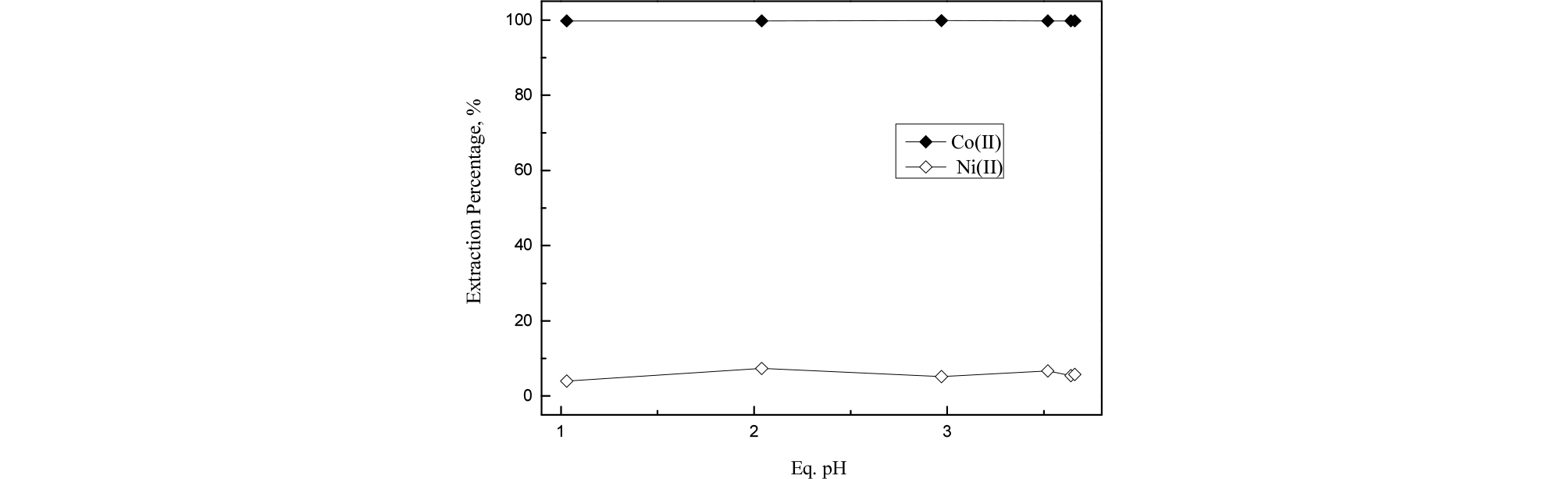
Fig. 7.
Effect of equilibrium pH on the extraction of Co(II) and Ni(II) by 0.1 M Aliquat 336 from HCl solution containing 0.1 M NH4SCN ([Co(II)] = 100 ppm, [Ni(II)] = 100 ppm).
코발트와 니켈의 혼합용액에 NH4SCN을 첨가한 다음 Aliquat 336으로 추출시 코발트의 추출반응을 다음과 같이 나타낼 수 있다25).
|
$${\mathrm{Co}^{2+}}_{\mathrm{aq}}\;+\;4{\mathrm{SCN}^-}_{\mathrm{aq}}\;=\;\mathrm{Co}{{(\mathrm{SCN})}_4^{2-}}_{\mathrm{aq}}$$
|
(7)
|
|
$$\mathrm{Co}{{(\mathrm{SCN})}_4^{2-}}_{\mathrm{aq}}\;+\;2{\mathrm R}_4{\mathrm{NCl}}_{\mathrm{org}}\;=\;\;{({\mathrm R}_4\mathrm N)}_2\mathrm{Co}{(\mathrm{SCN})}_{2\mathrm{org}}+2{\mathrm{Cl}^-}_{\mathrm{org}}$$
|
(8)
|
Aliquat 336의 염소이온을 SCN-로 치환한 ALi-SCN의 경우, 평형 pH가 증가함에 따라 코발트의 추출율이 약간 감소했다. 그러나 수상에 NH4SCN을 첨가하고 Aliquat 336으로 추출한 경우에는 평형 pH에 무관하게 코발트가 모두 추출되었다. 이는 3.3.1절에서 SCN-이 염소이온과 이온교환되어 코발트와 착물을 형성했던 것과 달리, SCN-이 수상에서 코발트 이온과 직접 착물을 형성해 Aliquat 336의 염소이온과 이온교환 반응에 의해 유기상으로 추출되기 때문이다.
ALi-SCN을 사용한경우 SCN-이온이 염소 이온과 이온교환되어 코발트와 착물을 형성하여 유기상으로 추출되었으나, 수상에 NH4SCN을 첨가한 다음 Aliquat 336으로 추출실험시 수상에서 미량의 니켈이 SCN-이온과 착물을 형성하여 코발트와 같이 유기상으로 추출된 결과를 보인다. 따라서 묽은 염산용액에서 코발트와 니켈의 분리를 위해서는 ALi-SCN로 용매추출하는 것이 NH4SCN을 첨가한 다음 Aliquat 336으로 추출하는 것보다 효율적이다.
4. 결 론
묽은 염산용액에서 이온성액체에 의한 코발트와 니켈의 분리를 위해 이온성액체의 종류와 농도 및 수상의 초기 pH를 변화 시켜 추출실험을 수행했다. 유기인산으로 제조한 이온성액체(ALi-D2, ALi-PC, ALi-CY272)로 코발트와 니켈을 추출 실험한 결과 평형 pH는 초기 pH 보다 높았다. 또한 코발트의 추출률이 니켈의 추출률보다 높은 경향을 보였으며 코발트와 니켈이 동시 추출되므로 두 금속의 분리가 어렵다. 또 다른 유기인산 이온성 액체 ALi- CY301의 경우 초기 pH와 이온성액체의 농도에 따라 코발트와 니켈의 선택도가 변화했다. 또한 상기 이온성액체에 TBP를 첨가하면 두 금속의 분리 특성이 약간 향상 됐고 니켈의 추출률이 증가했다. Aliquat 336의 염소이온을 SCN-으로 치환한 ALi-SCN을 추출제로 사용하면 코발트만 선택적으로 추출하는 것이 가능했고 다른 이온성액체와 달리 평형 pH는 초기 pH보다 감소했다. 수상에 NH4SCN을 첨가하여 Aliquat 336으로 추출하면 평형 pH에 무관하게 코발트가 모두 추출되었으나 미량의 니켈이 함께 추출됐다. 따라서 묽은 염산용액에서 ALi-SCN을 추출제로 사용하면 코발트만을 선택적으로 추출하여 두 금속을 분리하는 것이 가능하다.
Acknowledgements
본 연구는 2020년도 산업통상자원부 및 산업기술평가관리원(KEIT) 연구비 지원에 의한 연구결과(과제번호 20 011183)이며 이에 감사드립니다.
References
Shedd, K. B., McCullough, E. A., Bleiwas, D. I., 2017 : Global trends affecting the supply security of cobalt, Mining engineering, pp.37-42.
Wang, X., Gaustad, G., Babbitt, C. W., 2016 : Targeting high value metals in lithium-ion battery recycling via shredding and size-based separation, Waste Management, 51, pp.204-213.
Fernandes, A., Afonso, J. C., Dutra, A. J. B., 2012 : Hydrometallurgical route to recover nickel, cobalt and cadmium from spent Ni-Cd batteries, Journal of Power Sources, 220, pp.286-291.
Liu, C., Deng, Y., Chen, J., et al., 2017 : An Integrated Process to Recover NiMH Battery Anode Alloy with Selective Leaching and Multi-stage Extraction, Industrial & Engineering Chemistry Research.
Wang, L. Y., Lee, M. S., 2017 : Separation of Co(II) and Ni(II) from chloride leach solution of nickel laterite ore by solvent extraction with Cyanex 301, International Journal of Mineral Processing, 166, pp.45-52.
Silveira, G. T. R., Chang, S. Y. 2010 : Cell phone recycling experiences in the United States and potential recycling options in Brazil, Waste Management, 30, pp. 2278-2291.
Bertuol, D. A., Bernardes, A. M., Tenorio, J. A. S., 2006 : Spent NiMH batteries: Characterization and metal recovery through mechanical processing, Journal of Power Sources, 160, pp.1465-1470.
Lisbona, D., Snee, T., 2011 : A review of hazards associated with primary lithium and lithium-ion batteries, Process Safety and Environmental Protection, 89, pp.434-442.
Gupta, B., Deep, A., Singh, V., et al., 2003 : Recovery of cobalt, nickel, and copper from sea nodules by their extraction with alkylphosphines, Hydrometallurgy, 70, pp. 121-129.
Cheng, C. Y., 2006 : Solvent extraction of nickel and cobalt with synergistic systems consisting of carboxylic acid and aliphatic hydroxyoxime, Hydrometallurgy, 84, pp.109-117.
Virolainen, S., Fini, M. F., Laitinen, A., et al., 2017 : Solvent extraction fractionation of Li-ion battery leachate containing Li, Ni, and Co, Seperation and Purification Technology, 179, pp.274-282.
Zhang, P., Yokoyama, T., Itabashi, O., et al., 1998 : Hydrometallurgical process for recovery of metal values from spent lithium-ion secondary batteries, Hydrometallurgy, 47, pp.259-271.
Nan, J., Han, D., Zuo, X., 2005 : Recovery of metal values from spent lithium-ion batteries with chemical deposition and solvent extraction, Journal of Power Sources, 152, pp.278-284.
Castillo, S., Ansart, F., Laberty-Robert, C., et al., 2002 : Advances in the recovering of spent lithium battery compounds, Journal of Power Sources, 112, pp.247-254.
Contestabile, M., Panero, S., Scrosati, B., 2001 : A laboratory-scale lithium-ion battery recycling process, Journal of Power Sources, 92, pp.65-69.
Badawy, S. M., Nayl, A. A., El Khashab, R. A., et al., 2014 : Cobalt separation from waste mobile phone batteries using selective precipitation and chelating resin, J Mater Cycles Waste Manag, 16, pp.739-746.
Devi, N.B., Nathsarma, K. C., Chakravortty, V., 1998 : Separation and recovery of cobalt(II) and nickel(II) from sulphate solutions using sodium salts of D2EHPA, PC 88A and Cyanex 272, Hydrometallurgy, 49, pp.47-61.
Georgi-Maschler, T., Friedrich, B., Weyhe, R., et al., 2012 : Development of a recycling process for Li-ion batteries, Journal of Power Sources, 207, pp.173-182.
Zante, G., Masmoudi, A., Barillon, R., et al., 2020 : Separation of lithium, cobalt and nickel from spent lithium-ion batteries using TBP and imidazolium-based ionic liquids, Journal of Industrial and Engineering Chemistry, 82, pp. 269-277 (2020).
Plechkova, N. V., Seddon, K. R., 2008 : Applications of ionic liquids in the chemical industry, The Royal Society of Chemistry, 37, pp.123-150.
Oh, C. G., Son, S. H., Lee, M. S., 2019 : Solvent Extraction of Tb(III) from Chloride Solution using Organophosphorous Extractant, its Mixture and Ionic Liquids with Amines, J. of Korean Inst. of Resources Recycling, 28(1), pp.40-46.
Padhan, E., Sarangi, K., 2017 : Recovery of Nd and Pr from NdFeB magnet leachates with bi-functional ionic liquids based on Aliquat 336 and Cyanex 272, Hydrometallurgy, 167, pp.134-140.
Tran, T. T., Azra, N., Iqbal, M., et al., 2020 : Synthesis of succinimide based ionic liquids and comparison of extraction behavior of Co(II) and Ni(II) with bi-functional ionic liquids synthesized by Aliquat336 and organophosphorus acids, Separation and Purification Technology, 238, 116496.
Tran, T. T., Lee, M. S., 2020 : Separation of Mo(VI), V(V), Ni(II), Al(III) from synthetic hydrochloric acidic leaching solution of spent catalysts by solvent extraction with ionic liquid, Separation and Purification Technology, 247, 117005.
Clifford, W. E., McClaine, L. A., George, J. B. H., et al., 1965 : Remval of metal contaminants from nickel-containing, U.S. Patent Office, 3194652.
J. S. Preston., 1982 : Solvent Extraction of Cobalt(l1) and Nickel(l1) by a Quaternary Ammonium Thiocyanate, Separation Science and Technology, 17(15), pp.1697-1718.
Rybka, P., Regel-rosocka, M., 2012 : Nickel(II) and Cobalt (II) Extraction from Chloride Solutions with Quaternary Phosphonium Salts, Separation Science and Technology, 47, pp.1296-1302.
Sun, X., Ji, Y., Hu, F., et al., 2010 : The inner synergistic effect of bifunctional ionic liquid extractant for solvent extraction, Talanta, 81, pp.1877-1883.
Baek, J. W., Lee, M. S., 2017 : Separation of Rhenium (VII) and Vanadium(V) from concentrated HCl solution by solvent extraction with Alamine 336 and LIX 63, Korean J. Met. Mater, 55(1), pp.31-38
Liu, Y., Jeon, H. S., Lee, M. S., 2014 : Solvent extraction of Pr and Nd from chloride solution by the mixtures of Cyanex 272 and amine extractants, Hydrometallurgy, 150, pp.61-67.
Wang, L.Y., Lee, M. S., 2017 : Recovery of Co(II) and Ni(II) from chloride leach solution of nickel laterite ore by solvent extraction with a mixture of Cyanex 301 and TBP, Journal of Molecular Liquids, 240, pp.345-350.
Moyer, B. A., 2013 : Ion Exchange and Solvent Extraction Volume 21, Supramolecular Aspects of Solvent Extraction, p.293, 1st Edition, CRC Press, United States.
Wang, X., Li, W., Meng, S., et al., 2006 : The extraction of rare earths using mixtures of acidic phosphorus-based reagents or their thio-analogues, J Chem Technol Biotechnol, 81, pp.761-766.
Das, D., Juvekar, V. A., Rupawate, V. H., et al., 2015 : Effect of the nature of organophosphorous acid moiety on co-extraction of U(VI) and mineral acid from aqueous solutions using D2EHPA, PC88A and Cyanex 272, Hydrometallurgy, 152, pp.129-138.
Lee, M. S., Oh, Y. J., 2004 : Estimation of Thermodynamic Properties and Ionic Equilibria of Cobalt Chloride Solution at 298K, Materials Transactions, 45(4) pp.1317-1321.
Hogfeldt, E., 1982 : Stability Constants of Metal-Ion Complexes, Part A : Inorganic Ligands, p.87-88, Vol. 21, Pergamon Press, Oxford, NewYork, Toronto, Sydney, Paris, Frankfurt.











