1. 서 론
2. 구연산(Citric acid) 회수 기술 분석
2.1. 침전(Precipitation)
2.2. 용매추출(Solvent extraction)
2.3. 이온교환수지(Ion exchange resin)
2.4. Electro-Membrane
3. 결 론
1. 서 론
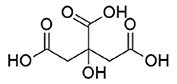
구연산(Citric acid: C6H8O7) 일명 시트르산은 유기산의 일종으로 식품산업, 화장품, 의약품 뿐만 아니라 환경 친화적인 청소제 및 금속의 에칭제, 도금약품 등에서도 광범위하게 사용되고 있고 수요도 매년 꾸준히 증가하고 있다. Global Citric Acid Market Outlook1)에 의하면 2022년 구연산의 시장규모는 약 2.59 million tons이며 2028년에는 3.29 million tons으로 증가하리라 예상하고 있다. 구연산은 주로 화학적 합성이나 미생물 발효를 통해 생산이 가능하나 화학적 합성을 통해 생산되는 구연산은 고순도와 고농축 제품으로 제조가 가능하지만 고가의 제조 비용 및 환경에 유해한 약품 사용 등으로 인하여 생산이 제한적으로 이루어지고 있어 대부분은 미생물의 발효 산물을 이용하여 정제․회수되고 있다2,3,4,5). 구연산의 경우 황산이나 염산 등의 독성이 있는 무기산에 비해 다음과 같은 특성이 있어 금속 침출 분야에 많은 응용이 기대되고 있다6). (1) 구연산은 3개의 카르복실산 그룹(pKa1 = 3.09, pKa2 = 4.75, pKa3 = 6.40)으로 구성된 삼양성자산(triprotic acid : H3A)으로 1몰의 구연산은 잠재적으로 3몰의 H+를 방출할 수 있다. 따라서 강한 산도와 아울러 강력한 킬레이트 복합체 형성에 기여할 수 있어 금속 이온과의 착물 형성을 촉진시킬 수 있다. Table 1에 구연산의 산분해 반응(Acidolysis reaction)과 금속 착체형성 반응(Complexolysis reaction)에 대해 나타내었다.
Table 1.
Reactions involved in acidolysis and complexolysis mechanisms for metal recovery
(2) 다가 전이 금속에 대하여 적당한 환원제 역할을 할 수 있어 강 무기산에 비하여 비교적 낮은 산 농도와 일반적인 침출 조건에서도 상대적으로 높은 침출 효율을 얻을 수 있다. (3) 유해가스 배출이 없고, 생태계에 부정적인 영향을 주지 않는 환경친화적인 침출제 역할을 할 수 있고, 미반응된 산은 침출 반응 중이나 반응 후에 쉽게 분해될 수 있다. 따라서 구연산은 금속 에칭제나 도금공정의 착화제로 현재 일부 사용되고 있고 최근에는 디스플레이 패널 제작공정 중 은(Ag) 에칭액으로 기존 사용하여 왔던 인산계 에천트(etchant)를 대신하여 대체 사용도 기대되고 있다. 또한 구연산의 친환경성 때문에 광석이나 폐리튬전지에서 Li, Co, Ni 등의 유가금속을 회수하기 위한 친환경 침출제로 활용하기 위한 연구가 활발히 진행중에 있다7,8,9,10,11). 또한 구연산 등 유기산을 생성하는 균주를 직접 침출과정에 적용하여 유가금속 성분을 용출시키는 미생물 침출(Bioleaching)에 대한 관심도 증가하고 있다12,13,14,15).
이와 같이 향후 다양한 분야에서 구연산의 사용이 예상됨에 따라 구연산의 고순도 생산 기술뿐 만 아니라 다량 발생이 예상되는 구연산 폐액의 재활용 기술 분야에도 관심을 기울여야 할 시점이다. 현재 구연산 폐수의 경우 대부분 혐기성 분해(anaerobic digestion)처리 후 한외여과(ultrafiltration)나 나노여과(nanofiltration)를 거쳐 단순 폐기 처리하고 있으며, 고가의 처리 비용 등 여러 가지 문제점이 지적되고 있다16).
본 연구에서는 현재 상용화 되었거나 또는 실용화를 위한 연구 중에 있는 다양한 구연산의 정제 및 회수 기술들을 분석하여 향후 다량 사용으로 인해 발생이 예상되는 구연산 함유 폐액의 친환경 재활용 기술개발의 기초를 마련하고자 하였다.
2. 구연산(Citric acid) 회수 기술 분석
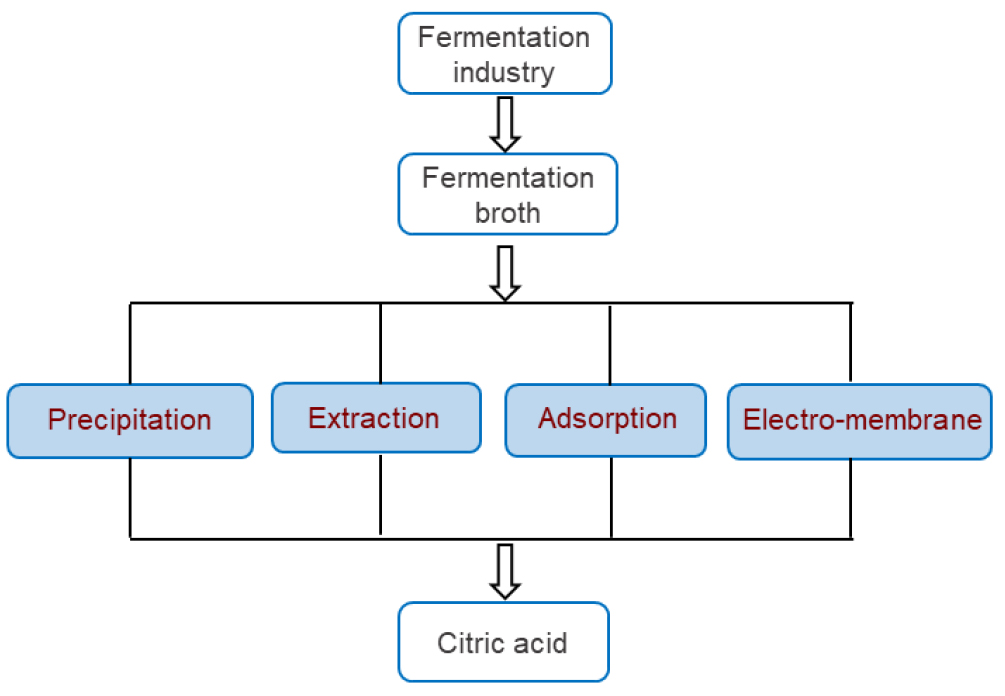
구연산은 90% 이상이 미생물 발효(fermentation)에 의해 회수되고 있다. 가장 많이 사용되는 미생물은 곰팡이류인 Aspergillus niger이며 주로 당밀(molasses) 이나 액화옥수수가루 등의 저가 원료를 주로 사용하고 있다. 또한 효모 계열의 Yarrowia lipolytica도 사용되고 있다. Aspergillus niger의 발효작용을 통하여 생성된 저농도의 조구연산(조산 : crude acid)의 경우는 일반적으로 농도 및 순도가 낮기 때문에 정제공정을 거쳐서 고농도 및 고순도의 구연산으로 회수하고 있다17,18,19). 조구연산용액 에서 고순도 정제산으로 회수하는 정제 비용이 총 생산 비용의 30~40%를 차지한다고 알려져 있다. Fig. 1에 미생물 발효액에서 구연산을 회수할 수 있는 방법들에 대해 나타내었다. 미생물 발효를 거쳐 생성된 발효액(조구연산 용액)으로부터 침전(precipitation)이나 추출(extraction), 흡착(adsorption), 전기분리막(electro-membrane) 등을 사용하여 정제산으로 회수하고 있다. 이러한 정제 방법중에서 현재는 침전법이 주로 사용되고 있으나 회수 과정에서의 고 에너지 비용, 복잡한 공정, 환경에 유해한 시약의 과도한 사용 등으로 인하여 보다 경제적이고 환경 친화적이며 지속 가능한 방향으로 기술 혁신이 요구되고 있다.
Table 2에 현재 상용화된 기술과 실용화를 위해 연구되고 있는 여러 기술들에 대한 장․단점을 비교하였다.
Table 2.
Comparison of citric acid recovery methods (adapted Ref. 4)
2.1. 침전(Precipitation)
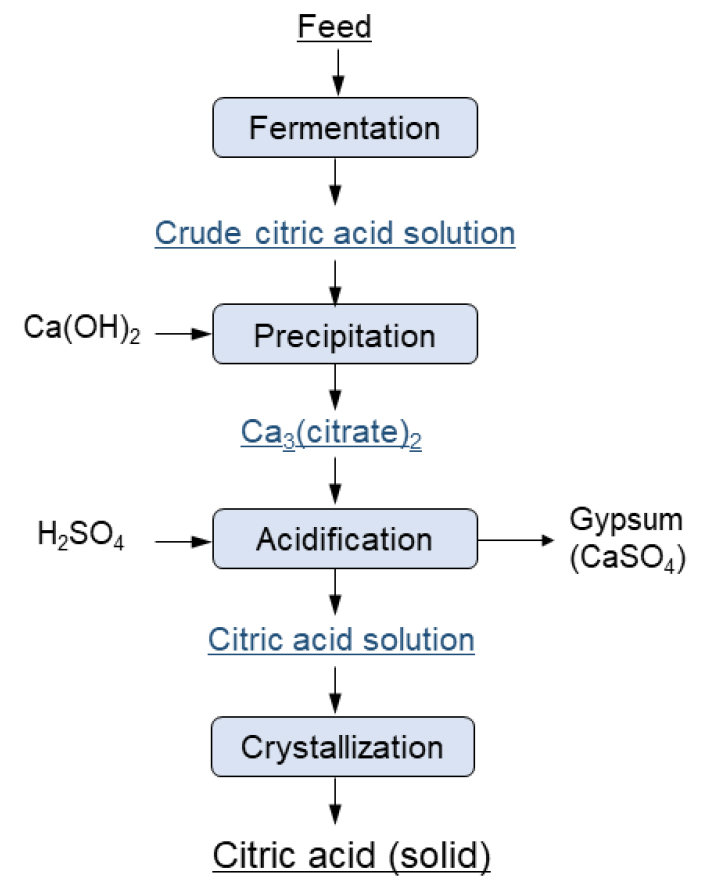
침전 기술은 구연산 생산에서 가장 널리 사용되는 회수 방법 중 하나이다. 이 기술은 고온(85~90°C)의 석회(lime)를 사용하여 발효액에 존재하는 구연산을 구연산염(칼슘, 칼륨 또는 나트륨)의 형태로 침전시키는 것이다. 이후 생성된 불용성 구연산염을 여과에 의해 분리한 다음 세척과정을 거쳐 당 및 기타 발효 배지 성분과 같은 불순물을 제거한다. 이후 현탁액을 황산(H2SO4)으로 처리를 한 후에 구연산용액을 황산칼슘(CaSO4, gypsum)과 분리하여 회수한다. 이후에 고순도 제품을 얻기 위해서는 수지 나 활성탄을 사용한 흡착, 증발, 결정화 및 건조와 같은 후속 단계가 필요하다. 이에 대한 공정 개략도를 Fig. 2에 나타내었다.
침전 공정의 첫 번째 단계는 수산화칼슘(Ca(OH)2) 또는 석회(CaO)를 첨가하여 가용성 구연산을 불용성의 구연산칼슘으로 전환하는 단계이다(식 (1)).
두 번째 단계는 황산(H2SO4)을 첨가하여 구연산칼슘과 반응시켜 가용성의 구연산과 불용성의 황산칼슘(CaSO4 : gypsum)이 생성되는 단계이다(식 (2)).
상기 반응에서 구연산 1 kg 처리시 0.58 kg의 수산화칼슘과 0.76 kg의 황산이 필요하다. 그리고 마지막에 1.3 kg의 황산칼슘이 생성되고 대략 18 L의 물이 소비된다. 황산칼슘 침전을 위해 사용되는 황산, 수산화칼슘 등의 화학약품은 전체 구연산 생산 공정비용의 11.4%를 차지하며 또한 침전 후 발생되는 황산칼슘의 폐기 비용은 환경비용의 85%를 차지한다고 알려져 있다20). 침전반응에 영향을 미치는 요인으로는 구연산의 농도, 온도, 반응시간, pH 및 석회의 첨가 속도 등이다. 고순도 및 조대한 결정을 얻기 위해서는 석회(CaO)를 함유한 용액(180~250 kg/m3)을 90°C 이상에서 그리고 pH는 7.0 이하에서 서서히 첨가해야 한다. 이 경우 용액 속 구연산의 농도는 15% 이상이어야 하며, 중화 과정은 보통 120~150분 정도 유지한다. 구연산칼슘을 여과한 후에 농축 황산(60~70%)과 반응시켜 구연산용액 과 침전물로 황산칼슘을 얻는다. 황산칼슘을 여과하여 제거하면 25~30%의 구연산용액이 얻어진다. 여과액은 잔류 불순물을 제거하기 위해 활성탄으로 처리하거나 이온교환컬럼을 통해 정제할 수 있다. 정제된 용액은 40°C 이하에서 진공증발 농축기에서 농축․결정화된다. 이후 건조 과정을 거쳐 무수 또는 일수화물의 구연산으로 회수가 가능하다. 이러한 방법에 의해 회수되는 구연산의 회수율은 64.8~92.9% 정도로 알려져 있다21). 이러한 침전 방법은 투자비와 공정비용이 많이 소요된다. 또한 다량의 화학약품 및 공정수가 사용되며 마지막 단계에서는 다량의 폐기물(폐액 및 석고)가 발생된다는 단점이 있다22). 이러한 단점에도 불구하고 이 기술은 복잡한 기술과 장비가 필요하지 않고 공정의 특성이 잘 알려져 있으며 기술 구현 및 사용이 용이하기 때문에 구연산 회수에 널리 사용되고 있다.
2.2. 용매추출(Solvent extraction)
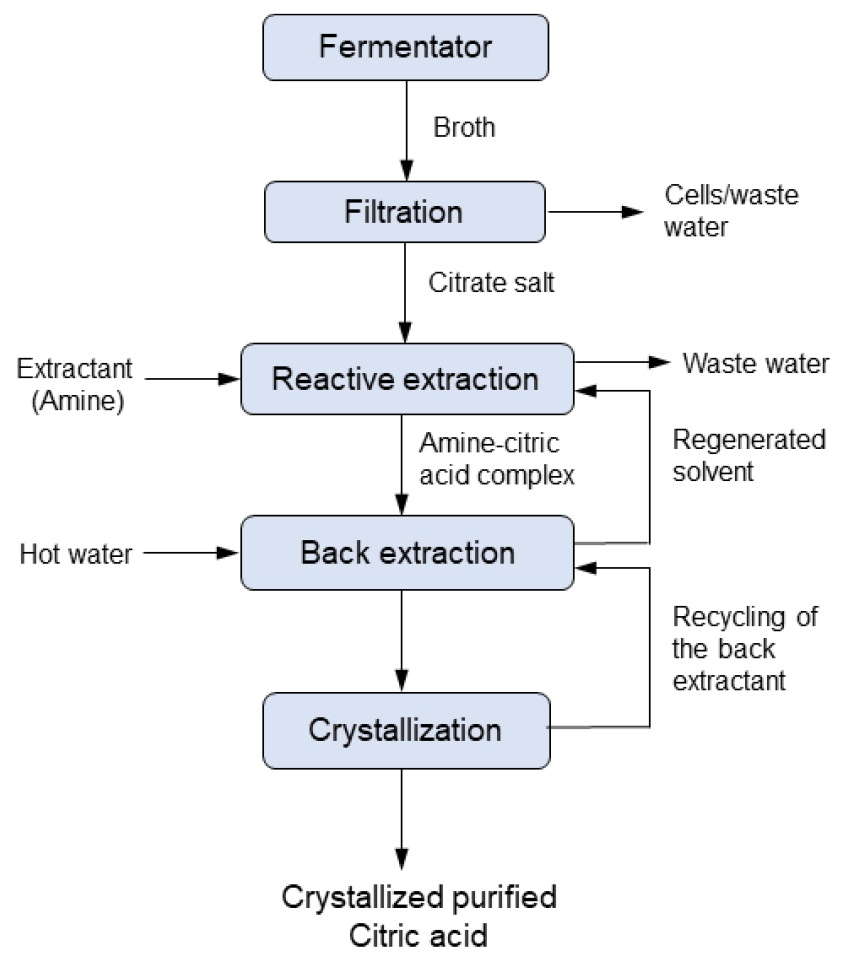
고전적인 침전법은 대규모 산업 공정에서 가장 많이 사용되는 기술이지만 구연산 분리를 위해 용매추출(액체-액체 추출) 기술도 개발되었다. 용매추출 시스템은 유기용매가 함유된 유기상과 구연산이 함유된 수용액상으로 구성되며, 적절한 용매가 존재할 경우 수용액상의 citrate 성분이 유기상으로 이동되어 추출된다. 구연산의 회수에 이상적인 용매로는 추출용량이 크고 불순물의 혼입을 최소화해야 한다. 각 용매는 특정 평형 분배계수(distribution coefficient)를 갖고 있으며, 이는 평형상태에서 추출된 산과 수용액중에 남아 있은 산 농도의 비율로 정의된다. 초기에는 장쇄 알코올(long-chain alcohols)및 케톤(ketones), 부탄올과 같은 용매가 일부 사용되었다. 기존 용매를 사용한 용매추출에서는 추출 효율이 낮기 때문에 반응성 추출(reactive extraction)이 연구되었다23,24,25). 반응성 추출은 반응성이 강한 추출제와의 구연산과의 유기착화합물을 형성시켜 분리하는 방식이다. 이 기술은 추출(extraction)과 역추출(back extraction) 공정으로 구분할 수 있다. 추출단계에서는 추출제와 구연산 사이의 유기착화합물이 형성되는 추출반응이 일어나고 이후에 추출용매중의 유기착화합물을 다시 수상으로 이동시키는 역추출 반응이 진행된다. 역추출 반응이 완료되면 추출용매는 재생되어 추출공정으로 다시 보내진다. Fig. 3에 반응성 추출에 의한 구연산 회수에 대한 공정 개략도를 나타내었다. 추출제는 추출률이 너무 낮으면 안되고 또한 재생이 어렵거나 너무 강한 착화합물 형성으로 역추출이 어려우면 안된다. 반응성 추출에 사용되는 추출제로는 탄소에 결합된 산소를 가진 추출제, 유기인화합물(organophosphorous compound) 추출제 그리고 고분자 지방족 아민계(high molecular weight aliphatic amines) 추출제로 구분할 수 있다. TOPO(trioctyl phosphine oxide)와 TBP(tributylphosphate) 등의 유기인화합물 추출제는 추출 능력은 다소 떨어지지만 미생물에 대한 독성이 낮아 발효액에서 카르복실산 추출하는데 일부 사용이 되었다. 그러나 최근에는 우수한 추출능력과 재생 용이성 등으로 인하여 아민계 추출제가 더 적합한 것으로 평가하고 있다. 아민계 추출제 중에서도 1차(primary) 아민의 경우는 물에 대한 용해성 문제가 있고, 2차(secondary) 아민은 추출 후에 재생이 다소 어렵다는 단점이 있다. 따라서 3차 아민(tertiary amine)계 추출제가 주로 사용되고 있으며, TOA(tri-octylamine) 및 Alamine®336(tri-octyl/dodecyl amine)가 대표적인 3차 아민계 추출제이다26,27,28,29). 한편 추출 공정비용을 낮추고 물리화학적 특성을 개선하기 위하여 혼합 추출제를 사용하거나 추출제를 희석제와 혼합하여 사용할 수 있다. 예를 들어 3차 아민은 추출 과정에서 높은 점도와 부식성 및 표면 장력을 나타내기 때문에 유기 용매를 희석제로 사용한다. 희석제는 활성 및 비활성의 두 가지 범주로 나눌 수 있다. 활성 희석제는 염소화 탄화수소, 식물성 기름, 등유와 같이 추출된 착화물의 용해도를 증가시키는 여러 작용기를 갖는 극성 물질이다. 비활성 희석제는 알칸, 벤젠, 알킬 성분이 치환된 방향족을 포함하는 비극성 물질이며 착화물에 대해 매우 낮은 용해도를 나타낸다. Thakre 등은25) 저농도 용액에서 구연산의 반응성 추출에 대해 연구하였다. 추출제로 TBP, TOA 및 Aliquat®336를 사용하고 희석제로 부틸 아세테이트, 데칸올 및 벤젠을 사용하여 추출 실험을 실시한 결과 20%(v/v) TOA + 부틸 아세테이트 시스템을 사용할 경우 최대 추출률(95.5%)을 보였다고 발표하였다. Keshav 등은30) 30%(v/v) TOA 에 4종의 비독성 희석제를 사용하여 구연산 추출 회수 연구를 진행 하였는데, 연구 결과 구연산 추출률은 쌀겨유(95%), 콩기름(94%), 참기름(94%), 해바라기유(93%) 순이라 발표하였다. Liu 등은31) 기존의 반응 추출법 보다 환경친화적인 깊은 공융 용매(Deep Eutectic Solvents : DESs)를 사용한 새로운 추출방법을 제안하였다. 10가지 서로 다른 디알킬 아미드(dialkyl amides)를 추출제로 사용하고 이소스테아릴 알코올(isostearyl alcohol)을 희석제로 사용하여 발효액에서 구연산을 추출․분리하기 위한 연구를 실시하였다. 수소 결합 수용체(hydrogen bond acceptor)로 아미드(amide: C10H21NO)와 수소 결합 공여체(hydrogen bond donor)로 구연산이 반응하여 소수성(hydrophobic) DESs가 형성되는데 30°C에서 20분간 반응하여 고순도(99.8%)의 구연산을 75% 추출이 가능하였다. 또한 반응후에 온도를 상승(75°C)시켜 용이하게 추출제 재생도 가능하다고 하였다. Rongjie 등은32) 구연산 용액을 유기 용매와 혼합한 후에 혼합물을 진공 증발시킴으로써 구연산은 유기상에 농축시키고 대부분의 무기염 및 기타 불순물은 수용액상에 남도록 한 후에 유기용매에 물을 첨가하여 구연산을 수용액상으로 회수하는 방법을 제안하였다. 50 wt.%의 구연산을 함유한 용액을 트리옥틸 암모늄, 옥타데카놀 및 등유로 구성된 유기용매 혼합물로 반응시 99.0%의 구연산을 99.0% 순도로 얻을 수 있었다.
이와 같이 반응성 추출 기술은 고전적인 침전 기술과 비교하여 시약 재사용 가능성, 고형 폐기물 생성 감소, 에너지 소비 감소, 천연 및 무독성 희석제 사용 가능성 등으로 침전법 보다는 친환경 공정이라 할 수 있다. 그러나 이 기술은 추출제 및 희석제의 가격으로 인하여 경제성이 다소 문제로 지적되고 있고 또한 유기성 용매의 독성, 휘발성 및 가연성으로 인하여 실제 적용 가능성이 제한될 수 있다는 단점이 있다. 따라서 보다 경제적이고 환경친화적 공정 개발을 위해서는 새로운 추출제나 공정 개발 등 아직 연구해야 할 부분이 많다고 할 수 있다.
2.3. 이온교환수지(Ion exchange resin)
이온교환수지는 3차원 구조의 폴리머 모체(Matrix)에 이온교환반응기(functional group)를 결합시켜 특정 이온물질을 가역적으로 교환 할 수 있는 특성이 있어 물질의 분리․정제에 많이 이용된다. 전하, 극성 등의 물리화학적 특성에 따라 구연산 이온과 상호 작용하여 이온교환수지에 흡착할 수 있다. 이후, 흡착물질은 탈리제(용리액)를 통과시켜 탈착시켜 순수한 용액으로 얻을 수 있다. 이온교환수지는 고체 미립자 물질로 반응기의 고정층 컬럼에 충진하여 연속적으로 흡착 반응을 수행할 수 있다. 이러한 흡착기술은 기존 추출 기술에 비해 조작이 간단하고 용매 손실이 적다는 장점이 있으나 수지의 오염 및 수명이 단축 된다는 문제가 있다. 고흡착 용량과 선택성은 공정의 효율성을 높이는 데 필요한 중요한 요소이며 이 외에도 물 이나 에탄올 등 친환경 용매로 쉽게 용리되어 재생되어야 한다. 일반적으로 구연산 회수에는 3차 및 4차 아민 또는 피리딘이 함침된 고분자 염기성 음이온 교환 수지가 구연산에 대한 친화성과 선택성이 우수하여 사용되고 있다. P. Gluszcz 등은33) 구연산 회수를 위하여 18가지 다른 이온 교환 수지에 대하여 조사했는데, 약염기성 음이온 교환 수지인 Amberlite®IRA-67이 가장 흡착 용량이 우수하다고 발표하였다. Van den Bergh 등은34) 구연산 회수를 위하여 3종의 수지(PVP: Poly(4-vinylpyridine), Amberlite®IRA-900 및 Amberlite®IRA-67)에 대한 성능을 비교하였다. 연구 결과 PVP 수지가 저 pH뿐만 아니라 황산염이 함유된 중성 pH 용액에서도 고흡착 용량(0.9 g/g)을 보이고 구연산에 대한 선택성도 우수하며 또한 메탄올이나 에탄올을 사용하여 효과적으로 재생이 가능하다고 발표하였다. C. Jacinto 등은35) 약염기성 음이온교환수지인 Dowex™Marathon™WBA와 강염기성인 Dowex™Marathon™MBA를 사용하여 모의 발효용액에서 구연산 회수에 대한 연구를 실시하였다. 연구 결과 강염기성 이온교환수지 보다 흡착용량이 약 2.3배 정도 개선되며 특히 낮은 pH(≈1.5)에서 구연산의 회수율이 최대를 보였다고 하였다. 이 경우에 흡착용량은 약 0.46 g/g이었고, 92% 순도로 85% 정도의 구연산을 회수할 수 있다는 연구 결과를 발표하였다. 한편, Wu 등은36)고정흡착제로 3차 PVP 수지를 사용하고 모의 이동층(Simulated moving bed: SMB) 기술을 이용하여 구연산을 회수율을 향상시킬 수 있는 공정을 제안하였다. 파일럿 규모(최대 유속 150 mL/분)의 연구를 통해 약 97.2%의 구연산 회수가 가능하고 회수된 구연산 순도는 99.8%라고 발표하였다. Delgado 등은37)상업용 수지(Reillex® 425)를 사용하고 메탄올을 용리제로 사용하여 동일한 SMB 기술을 사용하여 연구를 수행하였다. 이들의 연구 결과에 의하면 수지의 흡착 용량은 0.57 g/g이었고, 99% 이상의 순도로 95% 이상의 회수율로 구연산 회수가 가능하다고 발표하였다. Wang 등은38) 침전, 반응 추출 그리고 이온교환수지를 사용하는 3가지 공정에 대한 경제적, 환경적 영향에 대해 비교 연구를 하였다. 연구 결과, 이온교환수지를 사용할 경우 산성화, 부영양화, 생태 독성 및 지구 온난화 가능성이 낮아 가장 환경친화형 기술이라고 제안하였다. 또한 6,400 kg/h 규모의 구연산을 생산할 경우, 공정 운영비용의 경우는 흡착(6,100만 달러)이 용매추출(5,400만 달러)보다 높으나 침전(7,000만 달러)보다는 낮았고, 총투자액은 침전 3,510만불, 용매추출 3,260만불, 흡착의 경우는 4,150만불 정도로 추산하였다. 따라서 이온교환수지를 활용한 흡착기술은 침전이나 용매추출 기술 보다는 친환경 기술이라고 할 수 있고 또한 에너지비용과 화학약품 소모를 줄일 수는 있지만 수지의 재생과 주기적인 교체에 따른 비용이 부담으로 작용하고 있다.
2.4. Electro-Membrane
기존 구연산 등의 유기산 회수 기술은 일반적으로 추가 농축 단계가 필요하고, 위해한 폐기물을 생성하고 고가의 용매를 필요로 하며, 에너지 비용이 높다는 단점이 있다. 이러한 문제를 해결하기 위해 친환경 공정인 전기막 분리 공정에 대한 많은 관심과 개발이 진행되고 있다39,40).
2.4.1. 전기투석(Electro-dailysis : ED)
전기투석은 Fig. 4와 같이 주로 희석실, 농축실 및 전극실을 포함한 3실로 구성되어 있고, 양극과 음극 사이에는 음이온 및 양이온 교환막이 배열되어 있다. 양극과 음극사이에 전기장을 걸어줄 경우, 양이온 및 음이온이 양이온교환막 및 음이온교환막을 통해 선택적으로 투과하여 탈염이나 물질 농축에 사용되는 기술이다. 이러한 전기투석 공정은 부산물이 거의 발생하지 않고 재사용시 화학적 처리가 필요치 않기 때문에 환경 친화형 공정이며 에너지 효율 측면에서도 장점을 가지고 있다. 또한 운영의 용이성 및 유연성, 연속공정이 가능하고 최근에는 우수한 이온선택성 및 내열성 그리고 내화학성이 우수한 이온교환막의 개발로 인하여 다양한 조건의 환경에서 조업이 가능하게 되었다. 전기투석 기술은 생화학분야에 널리 응용되고 있으며 해수담수화 처리 분야는 물론 폐수처리 분야에 응용되면서 공업용수의 재순환 및 도금폐수 처리 분야에 적용이 되고 있고, 최근에는 황산나트륨 및 황산리튬의 농축 및 회수에도 응용되고 있다41,42).
S. Novalic 등은43) 전기투석을 사용하여 구연산의 농축 거동을 연구하였다. 용액의 pH, feed 농도 그리고 온도 변화에 따른 영향을 조사하였다. 연구결과 낮은 pH에서는 물질 전달이 느리기 때문에 pH를 7.5 부근으로 조절하는 것이 유리하고, 5~20 wt%의 낮은 feed 농도는 물질 전달에 큰 영향을 미치지 않는다고 하였다. 또한 1 kg Citric acid를 분리하기 위한 에너지 소모량은 약 6.1 × 103~7.2 ×103 kW라고 하였다. R. Nikbakht 등도44) 전기투석을 사용하여 구연산 회수에 관한 연구에서 공정 변수로 pH, 전압, 유량, 온도 및 feed 농도의 영향에 대해 고찰하였다. 연구 결과 pH 증가는 구연산 용액의 전기 저항을 감소시켜 셀 성능을 향상 시키고, 전압 증가와 유속 감소는 각각 구동력과 체류 시간의 향상으로 인하여 셀 성능이 개선된다는 것을 확인하였다. 구연산 회수에 최적의 운전 조건으로 pH 7.5, 전압 20 V, 온도 55°C 그리고 유속은 4 mL/min가 적절하다고 제시하였다. A. Chandra 등은45) 전기투석시 feed 용액에 NaCl, CaCl2 또는 FeCl3와 같은 강한 전해질이 혼합될 경우에 구연산 회수율이 최대 40%까지 감소되며 또한 농도 분극 및 fouling 현상으로 인하여 막에 금속 및 유기 분자의 흡착 가능성이 있어 미세여과법 이나 활성탄 또는 수지(resin)에 의한 흡착법 등으로 부유 고체 물질이나 금속 이온의 제거를 위한 전처리가 필요하다고 강조하였다.
2.4.2. BPED(Bipolar Membrane Electrodialysis)
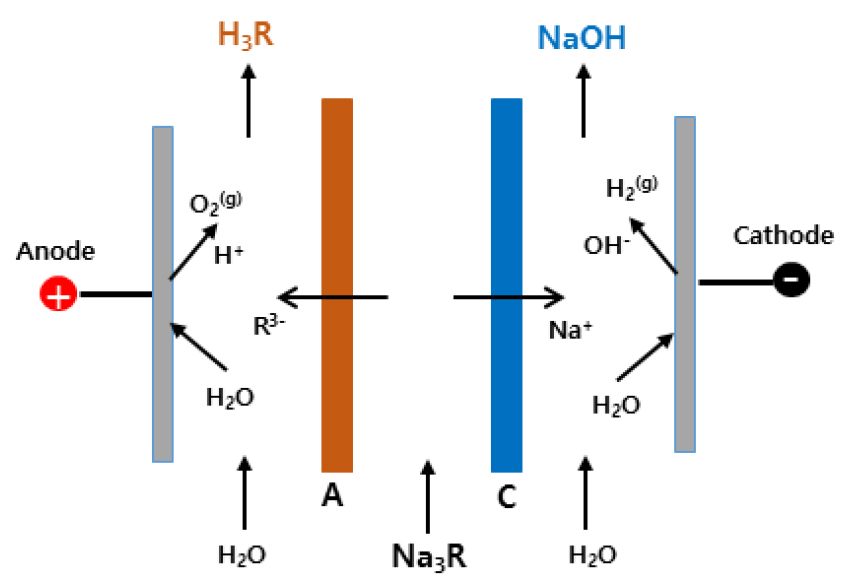
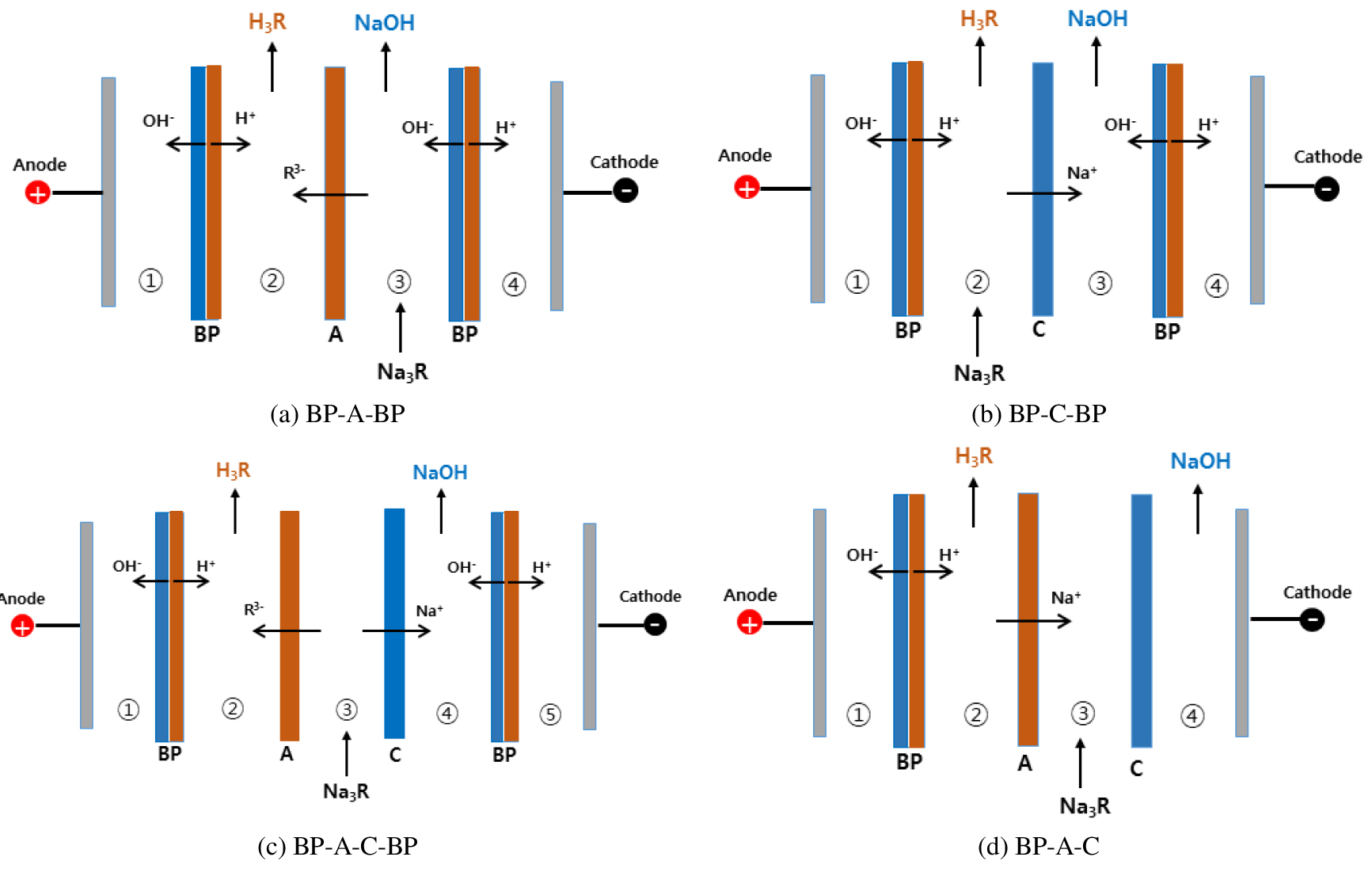
바이폴라 전기투석(BPED, Bipolar Membrane Electrodialysis)은 양이온과 음이온교환막으로만 구성된 탈염용 전기투석 공정에 물(H2O)을 분해하여 수소이온(H+)과 수산화이온(OH-)을 생성할 수 있는 바이폴라막을 추가한 공정이다. 바이폴라막은 양이온교환막 과 이온교환막이 하나로 결합된 특수한 형태의 이온교환막이다. 바이폴라막의 양이온교환층이 음극을, 음이온교환층이 양극을 향하도록 배열한 후 전류를 공급하면 바이폴라막 내부의 전이영역(transition region)에서 물분자가 수소이온(H+)과 수산화이온(OH-)으로 분해된다. 양이온교환막(C), 바이폴라막(BP), 음이온교환막(A)이 차례로 배열된 BPED 스택에 전류를 공급하면 양이온교환막을 통해 이동한 양이온(Na+)은 바이폴라막에서 생성된 OH-이온과 결합하여 염기(NaOH)를 생성하고, 음이온교환막을 통해 이동한 유기 음이온(R3-)은 바이폴라막에서 분해된 H+와 결합하여 유기산(H3R)을 생성함으로서 결과적으로 유기염(Na3R)으로 부터 유기산과 염기를 생산할 수 있다. 염으로부터 산과 염기를 제조하는 BPED 공정은 산(acid)회수실, 염기(base)회수실 및 탈염실로 구성된 3실(3-compartment) 구조를 갖는 것이 일반적이나 염의 종류 및 목적에 따라 2실(2-compartment) 구조도 가능하다. 많은 연구자들이 바이폴라 전기투석법의 Cell 구조 배열에 따른 산 및 염기의 회수 효율에 대한 영향을 고찰하였다. Cell 구조는 Fig. 5와 같이 양이온교환막(C), 바이폴라막(BP), 음이온교환막(A)을 여러가지 형태로 배열하여 구성을 할 수 있는데 대표적인 구조 및 특성은 다음과 같다.
1) BP-A-BP 구조(Fig. 3a) : 2개의 BP막 사이에 1개의 음이온교환막(A)으로 구성된 2실 형태의 구조이며, 초기 투입 염용액(Na3R)이 ③번실로 투입되면 양이온(Na+) 과 음이온(R3-)으로 해리되고 음이온이 ②번실로 이동되어 BP막에서 물분해로 인해 발생된 H+ 이온과 결합하여 순수한 산(H3R)이 생성된다. ③실에서는 Na+이온과 BP막에서 나오는 OH-와 결합하여 알칼리(NaOH)가 생성되는데 일부 초기 투입된 염(Na3R)이 잔존하게 되어 순수한 NaOH용액으로 회수는 어렵다. 음이온으로 citrate ion일 경우에는 낮은 이동도 때문에 오히려 바이폴라막에서 생성된 OH- 이온이 우선적으로 음이온교환막을 통해 이동하기 때문에 반응초기 전류효율이 낮고(20% 이하) 산 농축이 어렵다.
2) BP-C-BP 구조(Fig. 3b) : 2개의 BP막 사이에 양이온교환막(C)이 배열된 2실 형태의 구조이며, 초기 염용액(Na3R)이 ②번실로 투입되면 양이온(Na+)은 양이온교환막(C)을 통해 ③번실로 이동하여 BP막에서 물분해에 의해 나오는 OH- 이온과 결합하여 순수한 알칼리(NaOH)가 생성되고, ②번실에는 일부 잔존 염(Na3R)과 생성된 산(H3R)이 동시에 혼합상태로 존재하여 산의 순도가 떨어질 수 있다. 주로 약산과 약알칼리의 염으로부터 유기산과 유기염을 회수하는데 사용한다.
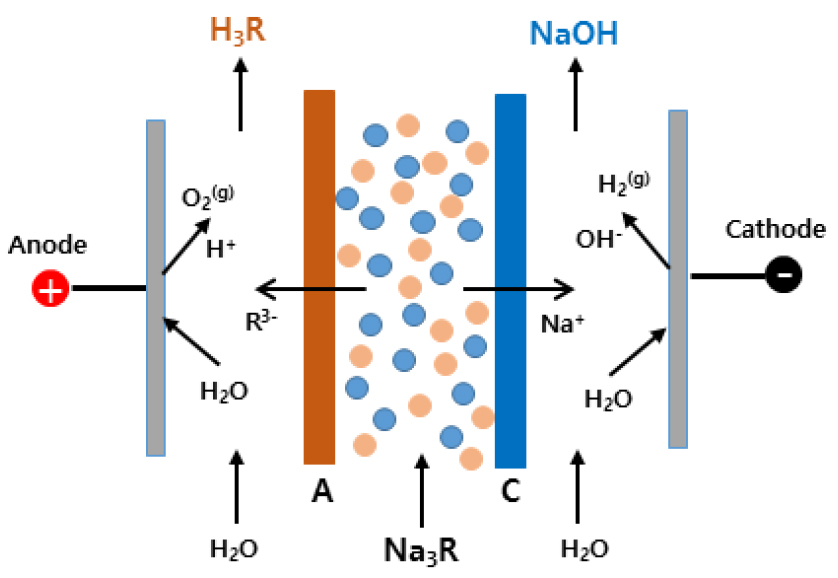
3) BP-A-C-BP 구조(Fig. 3c) : 2개의 BP막 사이에 1개의 양이온교환막(C)과 1개의 음이온교환막(A)이 배열된 3실 형태의 구조이다. 염용액(Na3R)이 ③번실로 투입되면 음이온(R3-)은 ②번실로 이동하여 순수한 산(H3R)이 생성되고 양이온(Na+)은 ④번실로 이동하여 순수한 염기(NaOH)를 생성한다. 주로 고순도의 산 및 염기를 동시에 회수하기 위한 공정에 적용한다. 이 경우 양이온교환막이 생성된 산(H3R)과 그리고 음이온교환막은 생성된 염기(NaOH)와 직접 접촉을 하지 않기 때문에 이온교환막의 내구성이 증가한다는 장점이 있다.
4) BP-A-C 구조(Fig. 3d) : 1개의 BP막과 1개의 음이온교환막(A) 및 1개의 양이온교환막(C)으로 배열되어 전체 4개의 챔버로 구성되어 있다. 염용액(Na3R)은 ③번실로 투입되며 일정한 전기장에서 Na3R가 분해되어 음이온(R-)은 음이온교환막(A)을 통해 ②번실로 이동하여 BP막에서 물 분해로 인해 발생된 H3O+이온과 결합하여 산(H3R)를 생성한다. ④번실에서는 NaOH용액을 얻을 수 있으며, ①번실과 ④번실은 전극실이다.
이와 관련된 연구개발 동향을 살펴보면 다음과 같다. S. Novalic 등은46) 3실 BPED 셀을 사용하여 구연산나트륨(Na3R)에서 구연산(H3R)과 NaOH로 전환하는 연구를 실시하였다. 모의 용액을 사용하여 300~1,000 A/m2 사이에서 전류밀도 변화에 따른 전류효율, 전환율 및 에너지 소모 등을 조사하였다. 또한 염기 농도(1.0N~3.5N)와 산 농도(20~60%)를 조절하면서 공정 거동에 미치는 영향을 조사하였고, 생성물에 함유된 불순물 및 물 이동율을 측정하였고 회수 산 농도를 증가시키기 위한 연구도 실시하였다. 연구 결과, 에너지 비용과 막 가격이 공정의 경제성에 가장 큰 영향을 미친다고 하였다. 이어서 발표한 연구에서 S. Novalic 등은47) 약 200 kg/kmol 이상의 분자량을 갖는 유기산을 3실 배열의 BPED를 사용할 경우에는 물질 전달이 낮아 전환율이 감소하고, 에너지 소모도 상대적으로 높아 ED와 2실(BP-C-BP) 시스템으로 구성된 복합공정을 제시하였다. 복합공정(ED: 440 A/m2 + 2실 BMED(500 A/m2)과 3실 BPED(440 A/m2)를 비교한 결과 Specific energy consumption이 각각 5.9 × 106 과 7.9 × 106으로 복합공정의 통하여 에너지 비용을 절감할 수 있다고 제안하였다. P. Pinacci 등은48) 3종류(BP-C-A-BP, BP-A-BP, BP-C-BP)의 셀을 사용하여 파일럿 실험을 통해 셀 구조 및 공정 변수에 대한 효과를 비교하였다. 이때 사용한 BP막은 Tokuyama사에서 제조한 BP-l, 음이온막은 AHA-2 그리고 양이온막으로는 CMB를 각각 사용하였다. 3실(BP-A-C-BP) 셀의 경우 염기와 산이 각각 양이온막과 음이온막을 통해 분리되어 산 및 염기가 1.8N까지 농축되었고, 전류효율은 60%를 보였으며 전류밀도(90~150 A/m2)가 낮아 대면적의 막 사용이 필요하다고 하였다. 2실(BP-A-BP) 셀의 경우는 음이온교환막을 통한 citrate 이온의 낮은 이동도로 인하여 초기에 전류효율이 20% 이하까지 감소되어 산 농축이 어렵다고 하였다. 한편 양이온교환막을 사용한 2실(BP-C-BP) 셀의 경우는 Na+가 양이온교환막을 통해 쉽게 이동함으로써 염기 및 산으로 비교적 원활하게 전환되어 2N sodium citrate로부터 염 및 산으로 전환율은 90% 이상, 전류밀도는 700~1,000 A/m2, 전류효율은 75%로 가장 만족할 만한 결과를 얻었다. 또한 Neosepta CMB(Tokuyama), FKB(Fuma Tech), Selemion CMV(Ashai Glass) 등 3종의 양이온교환막 효과를 분석하기 위해 전류밀도 800 A/m2에서 정전류 실험을 통해 분석한 결과, 모든 막에서 산/염기 전환율은 92% 이상이었고, 2.1~2.2 N 농도의 구연산 회수가 가능하다고 하였다. 이때 구연산용액중의 염 잔류량은 8% 정도 이고, 산 생성 속도는 대략 1.2 kg/h·m2이었다. 가성소다의 경우는 1.8 N 농도까지 재농축이 가능하며 막 종류에 관계없이 전류효율은 약 75% 이었고 잔류 산 오염은 200 ppm 미만이라고 발표하였다. 또한 연속식 조업으로는 최대 80%의 산/염기 전환율을 얻을 수 있으나 회분식 조업을 할 경우에는 전환율을 92%까지 증가시킬 수 있다고 하였다. 그러나 회분식 공정의 경우는 보다 높은 에너지 공급과 대면적의 막이 필요하며 급격한 전압 변화 현상으로 인하여 유체역학적 설계가 중요하다고 강조 하였다. Xu T 등도 3종류의 셀 구성에 대해 연구를 실시하였다49,50). A-C-BP-A-C(유형I), BP-C-BP(유형 II), BP-A-C-BP(유형 III)로 구분하여 셀 전압, BP 전압강하, 전류효율 및 에너지 소비 면에서 비교하였다. 셀 전압의 크기는 유형 II < 유형 I < 유형 III 이었고, BP 전압강하는 유형 II > 유형 I≈유형 III의 순서를 나타내었다. 전류효율의 경우는 유형 II > 유형 I > 유형 III이었고, 에너지 소모는 유형 I < 유형 II < 유형 III의 순서를 나타내었다. 결과적으로 에너지 소모, 전류효율 및 생성된 구연산의 농도를 종합적으로 고려할 때 유형 II(BP-C-BP)가 가장 유리한 셀 구성이라고 제안하였다. 이어서 Xu, T. 등은51) 2실 BP–C–BP로 구성된 공정 실험에서 구연산나트륨(Na3Cit) 농도와 황산나트륨(Na2SO4)농도의 영향에 대한 연구를 실시한 결과 에너지 소모, 전류 효율 및 산 농도를 고려할 할 경우 구연산나트륨의 경우 0.5~1.0 M, 황산나트륨의 경우 0.25~1.5 M이 최적 농도 범위라고 제시하였다. 0.5 M Na3Cit + 0.5 M Na2SO4 및 1 M Na3Cit + 0.5 M Na2SO4의 경우에 200분 반응후에 최대 30 g/L의 구연산을 회수할 수 있었다. 따라서 구연산나트륨에서 구연산 회수시에는 2실 BP-C-BP 셀을 사용하는 것이 바람직하다고 제안하였다. Igliński B. 등은52) BP-A-C 셀 구조에 대하여 전류밀도 및 염 용액 농도에 따라 구연산의 회수율에 미치는 영향을 조사하였다. 산과 염기의 평균 회수율은 저전류밀도(52 mA/cm2)에서 더 높게 나타났으며, 초기 염 농도가 1.4 mol/dm3인 경우 전류밀도 78 mA/cm2에서 최대값을 보였다. 또한 에너지 소모(kWh/kg)면에서 BP-A-C 구조가 다른 구조보다 가장 낮다고 제시하였고, 구연산나트륨염에서 구연산 1수화물 1 kg을 얻는 데 필요한 에너지 비용을 계산하였다. C. Huang 등은53) 유기산 회수에 응용되는 전기투석 기술의 종류(ED, EED, BPED, EDI 등)에 대하여 특징을 설명하고, 2실(BP-C-BP)구조를 사용할 경우에 전류밀도 1,000 A/m2, 전류효율 70%, 그리고 회수산 농도는 30 g/L 정도 가능하며, 1 kg 구연산 생성시 에너지 소모가 약 2-5 kWh 라고 하였다. Y. Wang 등은54) BP-A, BP-A-C, BP-C 구조에 따른 스택 전압 강하, 산 회수율, 전류 효율 및 에너지 소모에 대하여 평가하였다. 초기 염농도는 0.13 mol/dm3이고 전류밀도는 10 mA/cm2로 조절하여 실험을 실시한 결과. 전압 강하의 경우는 UBP-A-C > UBP-A > UBP-C 이었고, 회수된 구연산 농도는 CBP-C > CBP-A-C> CBP-A 이었으며 전류효율은 ηBP-C >ηBP-A-C >ηBP-A 순서를 보였다. 에너지 소모의 경우는 EBP-A > EBP-A-C > EBP-C 순서를 나타내 종합적으로 고찰한 결과 BP-C 구조가 가장 적합하다고 분석하였다. Sun, X. 등은55) 2실(BP-C-BP) 구조 BPED를 사용하여 구연산 회수에 대한 연구를 하였다. 전류밀도, 초기 sodium citrate 농도 및 cell 구조 영향 등에 대해 고찰하였다. 초기 sodium citrate 농도가 3.3 wt%인 경우 전류밀도 40 mA/cm2에서 97.1%의 구연산 회수율을 얻었다. 이 경우 전류밀도의 증가가 구연산 회수율을 향상시키는 효과적인 방법이 될 수 있으나 과도하게 높은 전류 밀도에서는 H+ 이온과 물 분자가 염기실로 이동이 가속화되어 오히려 구연산의 회수율을 감소시키고 에너지 소모를 증가시킬 수 있다고 발표 하였다.
2.4.3. EDI(ED/IEX Hybride system)
기존의 ED(또는 BPED) 공정에 유기산 등의 회수 효율을 증가시키기 위하여 농축실이나 희석실에 이온교환수지(Ion exchange resin)를 충진시켜 전류효율을 개선하기 위해 하이브리드 공정이 개발 되었다. 이 기술은 전기탈이온(Electrodeionization, EDI) 원리를 응용한 것으로 일반적인 공정 개략도는 Fig. 6과 같다. EDI 스택은 희석실, 농축실 및 전극실로 구성되고 희석실에는 양이온과 음이온 교환수지가 혼합된 혼합이온교환수지로 충진되어 있다. 전기장 하에서 이러한 혼합이온교환수지가 벌크 용액에서 이온교환막으로 이온 성분의 이동을 향상시켜 결과적으로 희석실에서는 이온의 농도가 감소하고, 농축실에서는 농도가 증가하여 정제 또는 농축 두 가지 공정 모두에 적용할 수 있다. EDI 공정에서 이온 전달은 거의 전적으로 이온교환수지를 통해 이루어지며 물 저항률의 영향을 받지 않는다. 전기장의 영향으로 용액 속의 양이온은 음극으로, 음이온은 양극으로 끌린다. 이 과정에서 혼합이온교환수지층이 전도성 매체로 작용한다. 희석실내서 이온이 용액을 통한 전류 전달을 수용하기에 충분하지 않을 경우, 물 분해 반응이 일어나 H+ 및 OH-가 혼합이온교환수지를 지속적으로 재생시킬 수 있다. 따라서 EDI 장치는 연속 재생이 가능하며 완전한 탈이온화가 가능하다는 장점이 있다.
Widiasa, I.N. 등은56) 발효액으로부터 구연산을 회수하기 위해 EDI 시스템에 대해 연구하였다. 희석실내에 혼합이온교환수지를 충진하여 연구한 결과 희석실을 통한 전류 전달이 거의 전적으로 혼합 이온교환수지에 의해 매개되며, 이 경우 feed용액의 이온 농도 변화는 전기저항에 큰 영향을 미치지 않는다고 발표하였다. 또한 희석실에서 H+ 및 OH- 이온의 생성으로 인하여 전기저항이 상당히 감소된다고 발표하였다. K. Zhang 등은57) 유기산의 일종인 타르타르산(주석산 : tartaric acid)을 회수하기 위하여 3실 BPED의 산실(acid chamber)에 강산성 이온교환수지를 충진하고 셀 전압, 전류 효율 그리고 수지 충진 전후의 타르타르산 회수율 및 에너지 소모 등에 대하여 조사하였다. 연구 결과 이온교환수지를 충진할 경우 산실내의 이온의 이동도가 증가되어 전기저항이 감소되어 고전류밀도하에서 저에너지 비용으로 고순도의 타르타르산의 회수 가능성을 확인하였다고 발표하였다. A. Rehouma 등은58) 아세트산 회수를 위하여 2실(BP-A-BP) BPED 구조의 희석실에 음이온교환수지를 충진시키고 저농도의 아세트산 폐액을 보다 순수한 물질로 농축시키고자 하였다. 연구 결과 희석실내에 이온교환수지를 충진시킴으로써 이온 이동성이 개선되고 전기저항이 감소되어 에너지 소모를 효과적으로 개선할 수 있다고 발표하였다. 한편, 산 회수율을 최대 90%까지 증가시킬 수 있지만 이 값을 초과하면 에너지 소모가 급격히 증가하기 때문에 회수율과 에너지 소모 사이의 적절한 분석을 통해 최적 조건의 선택이 필요하고, 이온교환수지는 별도의 재생 공정이 필요 없이 재사용이 가능하다고 발표하였다. Sun, X. 등은55) 2실(BP-C-BP) 구조에 구연산의 회수율을 높이기 위해 염기실(BC) 또는/및 산실(AC)에 이온교환수지를 충진한 셀을 사용하여 연구를 하였다. 원료용액으로 구연산나트륨(Na3Cit) 용액을 산실에 투입하고 염기실에는 Na2SO4 용액 대신에 정제수(H2O)를 투입하여 구연산(H3Cit) 및 염기(NaOH)을 회수에 관한 연구를 실시하였다. 산실에 양이온교환수지를 충진할 경우에는 셀 전압을 낮추고 에너지 소모를 크게 줄일 수 있었다. 또한 염기실에는 혼합이온교환수지를 충진하고 전해질로 탈이온수를 사용함으로써 순수한 NaOH 용액을 동시에 얻을 수 있었다. 한편 구연산나트륨의 초기 농도가 증가하면 전기장의 영향하에서 물 투과가 증가하고 동시에 Na+ 이온의 이동도 촉진시킬 수 있다고 하였다. 결과적으로 이온교환수지가 충진된 BPED를 사용함으로써 구연산의 회수율 개선 및 에너지 비용 감소에 효과적이라고 제안하였다. M. Jaouadi 등은59) 묽은 아세트산 용액을 사용하여 BPED/IEX 하이브리드 시스템을 통한 물질 전달의 반응단계를 규명하고자 이온 교환막을 통한 전달, 수용액 내 전달, 이온교환수지 베드 내 전달, 바이폴라막 내 물 해리 등으로 구분하고 이러한 물질전달 메커니즘 이해를 통하여 필요한 순도 또는 농도의 함수로서 에너지 소비를 최소화할 수 있는 방안에 대하여 고찰하였다. 다양한 유형의 이온교환수지를 사용한 BPED/IEX 하이브리드 연속 파일럿 실험을 통해 각 반응 단계에서의 에너지 소비를 평가하여 전체 에너지 비용을 줄일 수 있는 방안에 대하여 연구하였다.
3. 결 론
다양한 응용 분야에서 구연산에 대한 수요의 증가로 인하여 효율적인 생산을 위한 새로운 방법들이 개발되어 왔다. 그동안은 주로 침전 기술을 위주로 하여 용매추출 및 이온교환수지, 전기막 분리 기술 등이 꾸준히 개발되고 일부는 상용화되었다. 그러나 기존 회수 공정은 여전히 해결해야 할 문제점이 많이 남아 있다. 침전 및 용매추출 기술은 많은 양의 화학 물질과 에너지가 필요하고 또한 다량의 고형 폐기물이나 폐액 등이 발생되어 공정비용의 상승뿐 만 아니라 환경 문제를 야기시킬 수 있다. 이온교환수지에 의한 흡착 기술은 흡착제의 수명이 짧고 흡착 용량이 낮다는 단점이 있다. 전기투석 등 전기분리막 공정은 폐액이나 폐염 등을 배출 하지 않는 저에너지 공정 기술로 기존 방법들을 대체할 수 있는 환경친화형 기술로 주목을 받고 있다. 그러나 이 방법의 경우는 농도분극(concentration polarization)과 파울링(fouling) 현상이 여전히 해결해야 할 문제이다. 농도 분극은 막과 원료 용액의 이온 이동도 차이에 의하여 농축실의 막 표면에서 이온이 축적되는 반면에 희석실의 막 표면에서는 이온 고갈 현상에 의해 발생되어 결과적으로 전기막 분리 공정의 전류효율을 감소시키는 요인으로 작용한다. 파울링 현상은 막 표면 이나 막 기공 내에 콜로이드 물질이나 유기물들이 축적되어 나타나는 현상으로 역시 생산 효율을 저하 시키는 요인이 된다. 파울링 및 농도 분극은 불가피하지만 어느 정도 제어가 가능하다. 적절한 전처리 방법을 거쳐 원료용액의 불순물 농도를 감소시키거나, 공정운영의 최적화와 내구성 및 투과성이 우수한 분리막을 개발할 경우에 향후 전기분리막 공정이 구연산 등의 유기산 회수 공정에 많이 적용될 것으로 기대된다.