1. 서 론
SCR(Selective Catalytic Reduction) 성능의 탈질촉매는 화력발전소, 소각장 등에서 발생하는 배출가스 중 대기오염물질인 NOX를 환원제인 암모니아, 요소와 반응시켜 인체와 환경에 무해한 N2, H2O로 변환시키는데 사용되는 촉매로써, 조성이 TiO2 70~80 %, WO3 5~12 %, V2O5 1~5 %인 V2O5-WO3/TiO2 type 촉매가 주로 사용되고 있다1). 이러한 탈질촉매는 현장에 설치된 후, 사용시간이 경과함에 따라 효율이 점차 감소되기 때문에 일반적으로 20,000 시간을 주기로 재생하거나 새로운 촉매로 교체하여야 한다. 교체된 사용 후 폐촉매는 조성에 따라 일반 또는 지정폐기물로 분류되어 매립처리 되고 있으며 2014년 기준 연간 11,000 톤의 폐촉매가 발생되었고, 이 중 9,600 톤이 매립되고, 1,400 톤만이 재활용되었다2).
탈질 폐촉매의 재활용에 관한 연구는 탈질 촉매 원료가격 중 50 % 이상을 차지하는 텅스텐, 바나듐의 회수에 관한 연구가 주로 진행되었다. 대표적인 재활용연구로는 탈질 폐촉매를 황산으로 침출 후, 침출액으로부터 용매추출법을 이용한 바나듐을 회수하는 연구, 탈질 폐촉매를 탄산나트륨(Na2CO3)을 이용하여 배소처리 후, 수침출에 의한 텅스텐과 바나듐을 회수하는 연구, 탈질 폐촉매를 수산화나트륨(NaOH)과 혼합 후, 가압침출하여 텅스텐(Tungsten, W)과 바나듐(Vanadium, V)을 회수하는 연구 등이 실행되었다. 이렇듯 탈질촉매의 재활용 연구는 대부분 W과 V 회수연구에 집중되어 진행되었다3,4,5).
탈질촉매의 70 % 이상을 차지하는 TiO2는 대표적 백색 안료로써 백색도, 굴절율, 은폐력, 착색력이 우수하며, 열적, 화학적으로도 안정하여 플라스틱, 도료, 고무, 제지산업에서 특성향상 첨가제로 널리 이용되고 있다6). 또한, 탈질 폐촉매에서 텅스텐, 바나듐 회수를 위해서도 처리 후 발생되는 대량의 잔사(residue)에 대해 환경적으로 적절한 TiO2의 회수공정 개발이 요구되고 있는 실정이다.
따라서 본 연구에서는 탈질 폐촉매로부터 W, V 회수를 위해 소다배소(Na2CO3) 후 수침출을 실시한 잔사로부터, TiO2를 회수하기 위해 황산을 이용한 산침출과 침출액의 가수분해 침전반응을 실시하여 TiO2 성분의 회수율과 회수된 TiO2에 대한 순도 및 형상을 평가하였다.
2. 실험원료 및 방법
본 연구에서 사용한 실험원료는 탈질폐촉매로부터 W, V을 회수하기 위해 소다배소처리 후, 수침출을 진행한 수침출 잔사를 이용하였다. 구체적으로는 삼천포발전소에서 발생한 폐촉매를 대상으로 탄산나트륨(Na2CO3, Junsei Chemicals, 99 %, Japan)과 폐촉매를 질량비로 2:1로 혼합 후 1000 ℃, 1 시간 배소처리 하였고, 소다배소된 폐촉매를 Rod mill을 이용하여 분쇄 후 sieving을 통해 325 mesh를 통과한 분말을 준비하였다. 준비된 시료에 대한 수침출은 온도 70 ℃, 교반속도 500 rpm, 고액비 100 g/L의 조건으로 1 시간 수침출 후, 고액 분리하였다. 분리된 잔사는 흡착성분의 제거를 위하여 3차 증류수를 이용하여 3회 세척한 후, 105 ℃, 24 시간 건조하였으며 건조된 시료를 본 연구의 실험원료로 사용하였다.
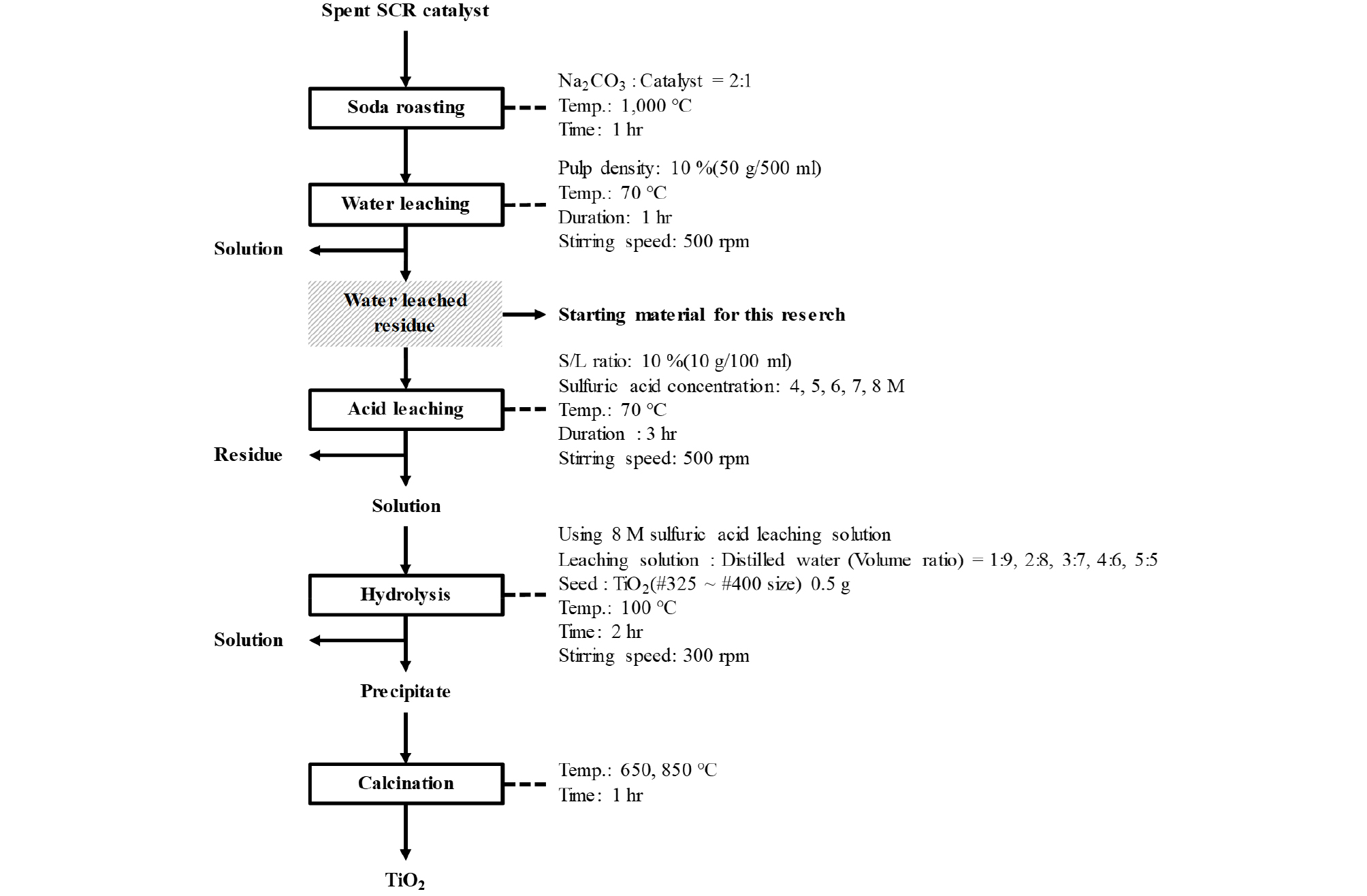
수침출 잔사로부터 Ti 성분의 침출은 황산을 이용하여 온도 70 ℃, 교반속도 500 rpm, 침출시간 3 시간, 슬러리 농도 100 g/L 조건으로 황산 농도를 4~8 M 구간에서 변화시키면서 진행하였다. 침출액으로부터 Ti 성분의 회수를 위하여 가수분해 침전반응을 진행하였다. 가수분해 침전반응은 침출액과 증류수를 부피비로 1:9~5:5로 변화시키면서 혼합액 100 ml를 준비한 후, 100 ℃, 교반속도 300 rpm 조건으로 침전반응을 유도하였다. 또한 동일한 실험 조건에서 TiO2 결정생성 촉진을 위한 Seed (Titanium(IV) oxide, Anatase 98%, DAEJUNG) 첨가 유무에 따른 Ti의 침전율 변화를 확인하였다. 가수분해 실험 후 필터(aspirator, Qualitative filter paper, Whatman)를 사용하여 고액 분리를 실시하였다. 분리된 고상의 침전물은 증류수로 3회 반복하여 세척한 후, 105 ℃, 24 시간 건조 후 전기로(Electric furnace, Kanathal Super, Korea Furnace Development Co. Ltd., Korea)에서 650, 850 ℃, 1 시간 열처리하여 결정성을 향상시켰다. 본 연구에서의 출발원료 준비과정과 TiO2 회수를 위한 전체 공정을 Fig. 1로 정리하였다.
액 중 원소 농도분석은 유도결합플라즈마 분광기(ICP, Inductively Coupled Plasma Spectrometer, OPTIMA 7300 DV, Perkinelmer, USA)을 이용하여 분석하였으며, 침출율은 식 (1)을 이용하여 계산하였다.
| $$L_M(\%)=\frac{W_A}{W_A+W_B}\times100$$ | (1) |
여기서 LM은 원소의 침출율을, WA는 고액 분리 후 여과액의 원소 함량, WB는 고액 분리 후 침출잔사의 원소 함량을 나타낸다. 잔사의 원소함량은 chemical digestion method를 이용하여 완전용해 후 분석하였다. 고상의 성상은 고분해능 X-선 회절기(HRXRD, High Resolution X-ray Diffractometer, X`pert-Pro MPD, PANalytical, Netherlands)을 이용하여 분석하였고, 조성은 X선 형광분석기(XRF, X-ray Fluorescence, S2 ranger, Bruker, USA)를 이용하여 분석하였다. 또한 가수분해 침전법으로 회수한 TiO2의 형상학적 분석은 고분해능 주사전자현미경(UHR-SEM, Ultra High Resolution Scanning Electron Microscope, Hitachi, Japan)으로 확인하였다.
3. 결과 및 고찰
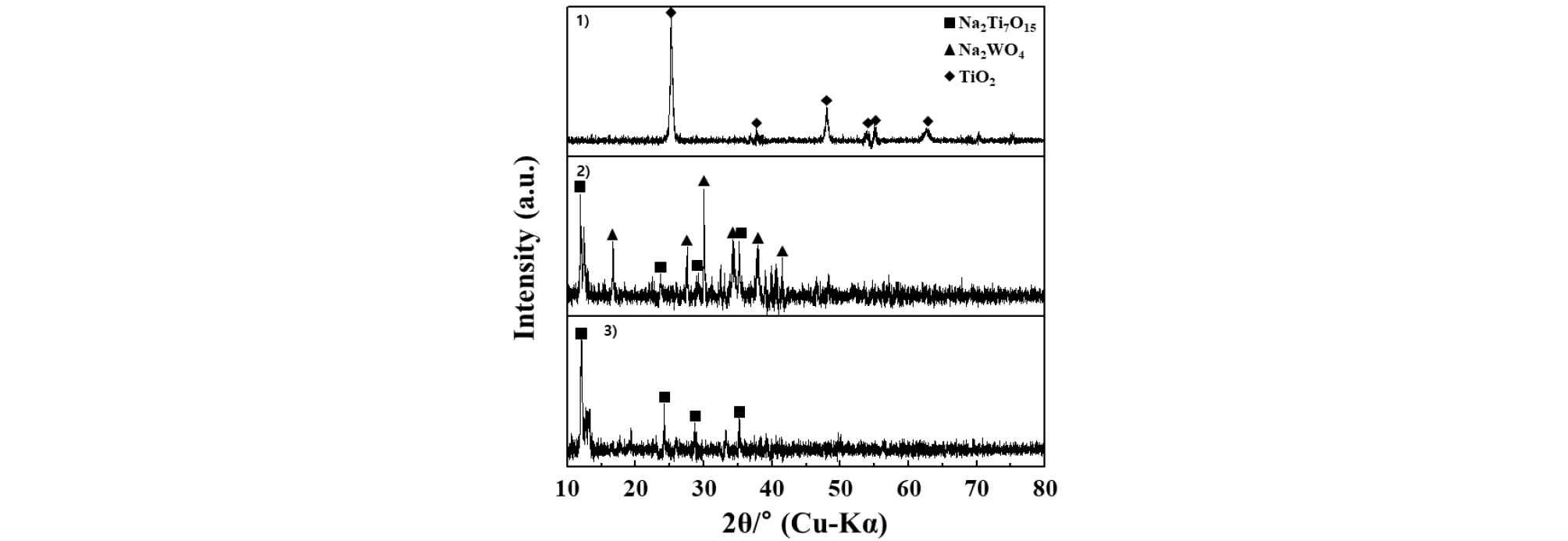
탈질 폐촉매와 W, V를 회수한 수침출 잔사에 대한 조성을 XRF를 이용하여 분석하였다(Table 1). 수침출에 의해 W, V 성분의 대부분이 제거되었으며, Na2O 성분의 증가로 인해 TiO2 성분이 상대적으로 감소하였다. 이러한 Na2O의 증가와 TiO2 성분의 상대적 감소는 TiO2 성분의 Na2Ti7O15로의 변화에 의한 결과로 해석되었다(Fig. 2).
Table 1.
XRF result of Spent SCR catalyst and its water-leaching residue after soda roasting treatment
3.1. 황산침출
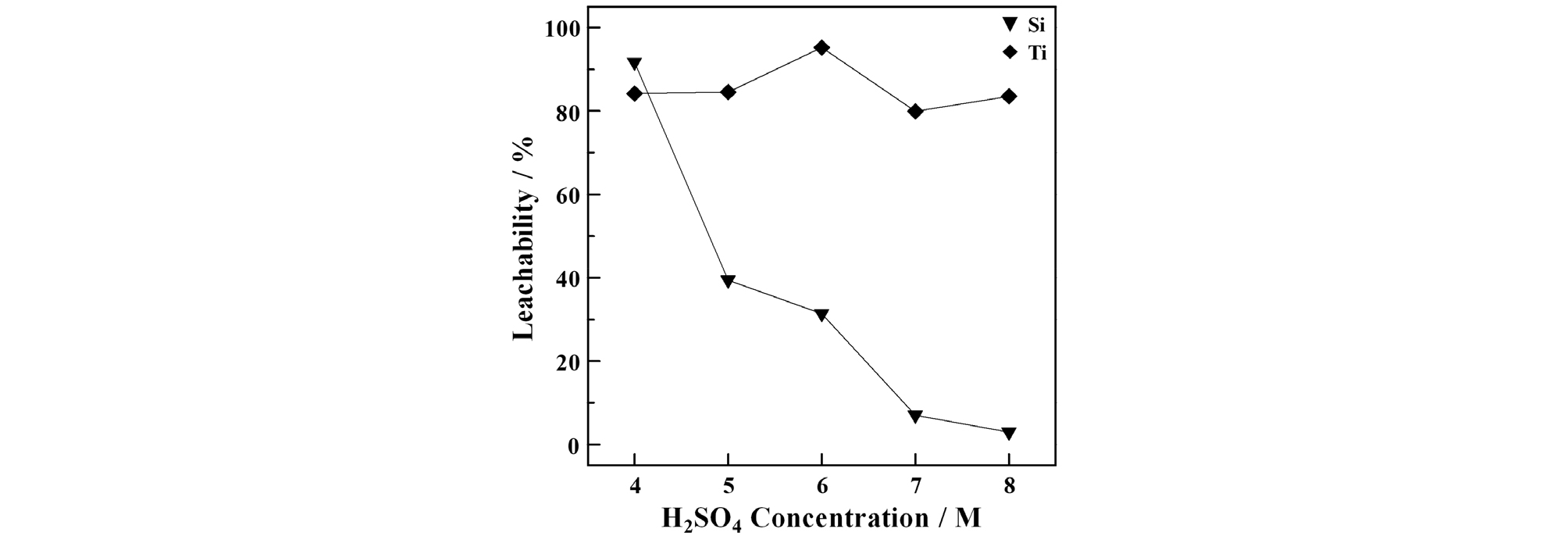
침출 실험은 수침출잔사에 대해 슬러리 농도(100 g/L), 침출온도(70 ℃), 침출시간(3 hrs), 교반속도(500 rpm)를 고정하였으며, 황산 농도의 변화에 따른 Ti, Si의 침출율을 관찰하기 위해 농도를 4, 5, 6, 7, 8 M로 변화시키면서 실험을 진행하였다(Fig. 3).
Fig. 3에서 보이는 바와 같이 Ti의 침출율은 전구간에서 약 80 % 이상을 나타내었다. 황산농도 6 M 까지는 산농도 증가에 비례하여 다소 증가하지만(6 M, Ti 침출율 95.2 %), 이 후 감소하는 경향을 확인하였다. 이는 황산농도 증가에 따른 고-액 계면에서의 침출액의 확산이 감소된 결과로 판단된다. 반면에 Si의 침출율은 황산농도 증가에 반비례하여 급속하게 감소하였다. 4 M에서는 91.7 %의 침출율이 8 M 조건에서는 3.0 %까지 감소되었다. 이러한 현상은 수침출 잔사에 존재하는 Si가 Na 화합물인 규산나트륨(Na2SiO3)으로 존재하고, 이것이 황산과 반응하여 이온상태가 아닌 액 중 콜로이드상의 SiO2 미립자로 전환됨에 따라 액 중 Si의 농도가 감소한 것으로 해석되며, 이와 관련된 반응을 식 (2)로 표시하였다7).
| $${\mathrm{Na}}_2{\mathrm{SiO}}_3+{\mathrm H}_2{\mathrm{SO}}_4+{\mathrm H}_2\mathrm O={\mathrm{SiO}}_2\cdot2{\mathrm H}_2\mathrm O+{\mathrm{Na}}_2{\mathrm{SO}}_4$$ | (2) |
Ti 회수를 위한 침출액은, 침출율이 최대인 황산 6 M의 경우 액 중 다량의 Si 성분이 존재하고 이는 가수분해 침전반응에 의해 Ti 성분과 공침이 일어날 가능성이 높아서 회수된 TiO2의 순도를 저감시킬 가능성이 높기 때문에 침출율은 다소 낮지만 액 중 Si 성분이 극히 낮게 존재하는 황산 8 M 침출액을 사용하였다.
3.2. 가수분해 침전반응
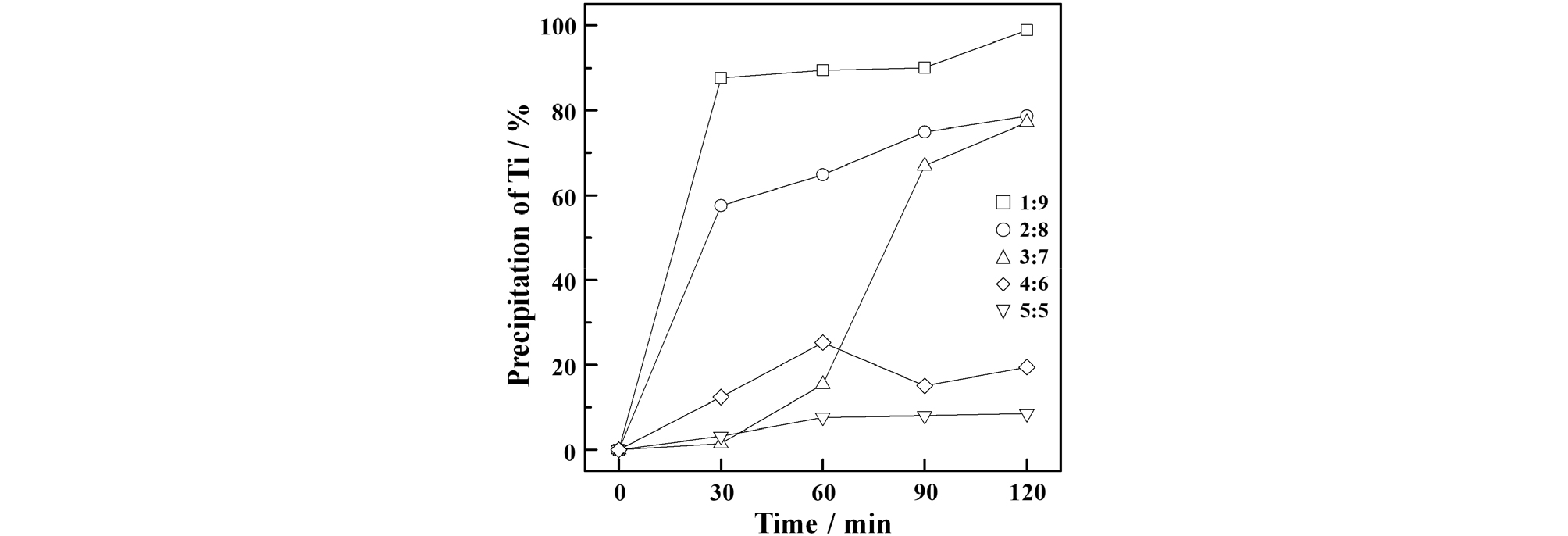
황산침출액으로부터 Ti 성분의 가수분해 침전반응을 위해 8 M 침출액과 증류수를 부피비로 1:9, 2:8, 3:7, 4:6, 5:5의 비율로 혼합하여 각각 100 ml를 각각 준비하였다. 준비된 혼합용액을 100 ℃에서 교반속도 300 rpm조건에서 0~2 시간까지 반응을 진행한 후, 고-액 분리하여 액 중 잔류 Ti 성분을 정량분석하여 가수분해 침전회수율을 측정하였다(Fig. 4). 액 중 Ti 농도가 낮을수록 회수율 상승속도가 빠르게 나타났으며, 혼합비 4:6, 5:5에서는 2 시간까지 회수율이 최대 20 % 정도로 낮게 측정되었다. 침출용액에서 Ti 성분의 가수분해 침전반응은, 황산침출 시 생성된 TiSO4 성분이 물과 반응하여 수화 TiO2와 황산이 생성되고, 연속적으로 재용해반응이 반복적으로 일어난 결과로 판단된다8,9,10).
| $${\mathrm{TiOSO}}_4+{\mathrm{nH}}_2\mathrm O={\mathrm{TiO}}_2\cdot(\mathrm n-1){\mathrm H}_2\mathrm O+{\mathrm H}_2{\mathrm{SO}}_4$$ | (3) |
식 (3)에 나타낸 반응은, 액 중 TiOSO4의 농도가 높을 경우 Ti 성분은 의 결합구조로 존재하고, 이러한 결합구조의 생성물은 용해도가 높은 것으로 알려져 있다. 그러나 TiOSO4의 농도가 낮으면 Ti 성분은 단량체 형태로 존재하게 되며 가수분해 조건 하에서 의 결합구조를 가진 침전물을 형성하게 되고, 그 결과 생성된 화합물은 고농도 TiOSO4 상에서 생성된 화합물보다 용해도가 낮으며 용액 내 과포화상태의 3TiO2·4H2O로 침전된 결과로 판단된다11).
또한, Ti 농도가 높을수록 침전회수율이 낮게 나타난 이유는 침전반응 시 단량체의 핵생성에 많은 양의 활성화에너지가 요구되기 때문이라고 해석된다. 따라서 고농도 Ti 함유 용액의 침전회수율을 향상시키기 위해 Ti seed를 첨가하여 침전반응을 진행하였다. 사용한 seed는 고순도 TiO2 분말을 #325~#400 입도로 사분(sieving)하여 각각의 100 ml 혼합용액에 0.2 g 첨가하여 가수분해 침전반응을 진행하였다.
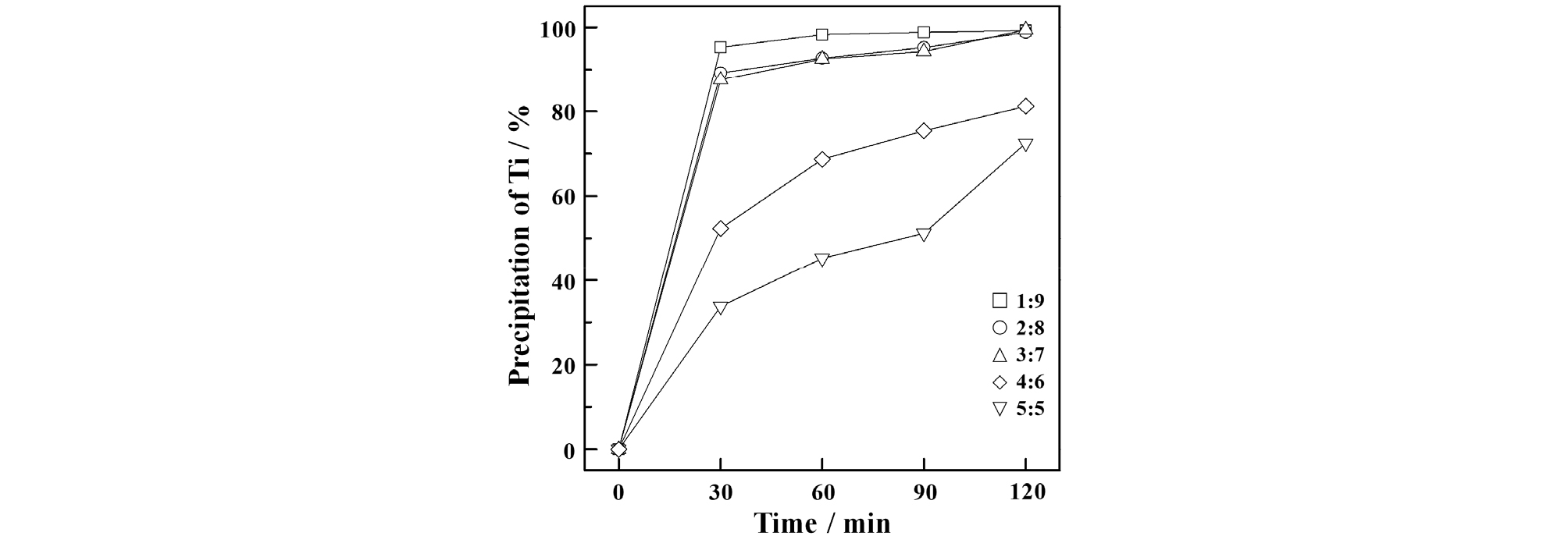
Fig. 5에서 보는 바와 같이 모든 혼합조건에서 TiO2 침전율이 향상되었다. 특히 1:9~3:7 혼합용액에서는 2 시간 이내에 침전반응이 완료되어 98.8~99.8 %의 회수율을 달성하였고, 4:6, 5:5의 혼합조건에서는 2 시간 반응에 각각 81.2 %, 72.5 %의 침전율로 다소 낮게 나타났지만 회수율 변화경향을 보면 가수분해 침전반응이 아직 진행 중에있는 것으로 판단되며, 이는 침전반응을 2 시간 이상으로 진행할 경우 침전회수율 향상을 기대할 수 있다고 판단된다.
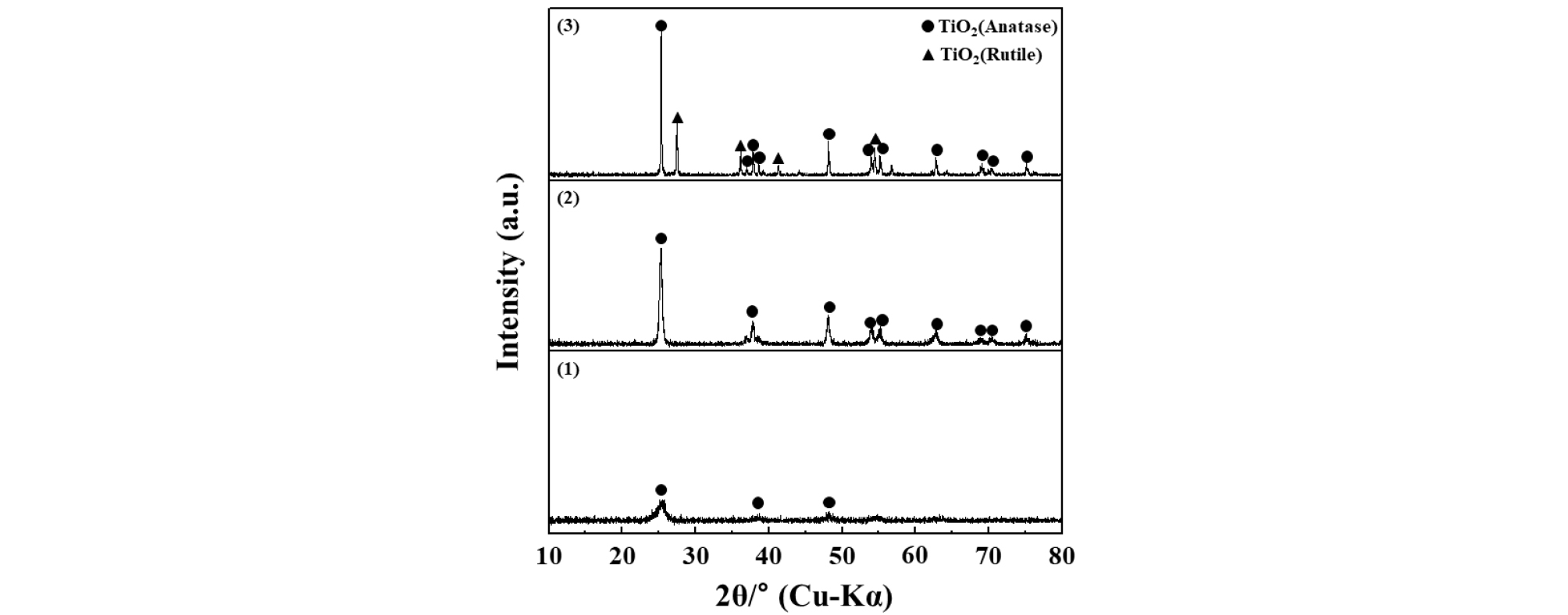
침전 회수된 TiO2는 결정수의 제거와 결정성 향상을 위해 650, 850 ℃로 각각 1 시간 열처리하여 성상을 조사하였다. 침전물의 XRD 분석 결과(Fig. 6), 열처리 전 침전물은 회절피크의 강도가 낮고, broad하여 결정립의 크기가 작고 결정성이 다소 낮은 성상으로 분석되었다. 반면에 열처리를 통해 결정성 향상과 상변화를 확인할 수 있었다. 650 ℃, 1 hr의 열처리 결과 Anatase 결정의 TiO2 로 존재함이 확인되었다. 한편, 850 ℃, 1 hr 열처리한 경우 일부 TiO2가 Rutile 결정으로 전이되는 것이 확인되었다.
생성된 TiO2 분말의 형상을 SEM으로 분석한 결과(Fig. 7), TiO2 입자크기는 열처리 온도에 상관없이 0.5 μm 정도로 거의 균일하였고, 응집상태로 존재하였다. 열처리 온도에 따라 응집체 표면의 toughness가 변화하였고 이는 열처리 온도가 높을수록 소결체로 변화한 결과라고 판단된다11). 또한, 850 ℃로 열처리한 분말에 존재하는 Rutile 결정의 TiO2는 형상분석만으로는 구분할 수 없었다.
4. 결 론
탈질폐촉매로부터 W, V 성분을 회수한 수침출 잔사로부터 Ti 성분을 회수하기 위하여 황산침출과 침출액의 가수분해 침전반응을 진행하였다.
Ti의 침출율은 황산 농도 6 M까지는 산농도 증가에 비례하여 다소 증가 하지만 그 이상의 조건에서는 다시 감소하는 경향을 나타내었다. 반면에 Si의 침출율의 경우는 산 농도에 반비례하여 급속히 감소하는 경향을 나타내었다. 이는 침출액 농도 증가에 따른 반응계면 에서의 침출액의 확산속도 감소와 액 중 콜로이드상의 SiO2 미립자 생성의 결과로 판단된다. 침출액으로부터 TiO2의 가수분해 침전반응은 황산 침출 시 생성된 TiSO4 성분의 수화 TiO2로의 전환과 황산에 의한 반복적 재용해반응의 결과로 해석된다. 침전반응에 의한 Ti 성분의 회수율은 액 중 Ti 농도에 반비례하였고, 회수율 향상을 위한 seed 첨가효과로 1:9~ 3:7 혼합용액에서는 2 시간 이내에 99 % 이상의 TiO2 회수가 가능하였다.
침전회수된 TiO2는 결정립 크기가 작고 결정성이 낮은 성상으로 존재하였으며, 650 ℃ 열처리를 통해 Anatase 결정의 TiO2로 전환되었다. 또한 850 ℃ 조건에서는 일부 Rutile 결정의 TiO2가 공존하였으며, 두 조건 모두 입자의 크기가 0.5 μm 정도로 균일하였으며 열처리 온도에 따라 응집체의 표면소결상태가 다소 변화됨을 확인할 수 있었다.