1. 서 론
리튬이온배터리는 높은 에너지 및 전력 밀도와 같은 우수한 전기화학적 성능을 지녀 수요가 증가하고 있다1,2,3). 전 세계적으로 폐리튬이온배터리의 양은 2030년까지 1,100 만톤 이상에 도달할 것으로 예측된다4). 또한 폐리튬이온배터리는 토양과 지하수를 오염시킬 수 있는 코발트, 망간, 니켈과 같은 중금속으로 구성되어 있기 때문에 폐리튬이온배터리를 부적절하게 처리하면 여러 환경문제가 일어날 수 있다5,6). 따라서 환경오염문제를 방지하면서 폐리튬이온배터리에 함유된 유가금속을 효율적으로 회수할 수 있는 공정개발이 필요하다7,8,9,10).
리튬이온 배터리는 5~20% 코발트, 5~10% 니켈, 5~7% 리튬, 15% 유기화학물질 및 7% 플라스틱 및 미량의 구리, 알루미늄과 철이 함유되어 유가금속을 회수하기 위해 다양한 연구가 진행되고 있다11,12,13). 일반적으로 폐리튬이온 배터리의 금속 회수공정은 전처리, 금속 추출 및 정제로 나눌 수 있다. 특히 최근에는 고온제련과 습식제련의 융합에 의한 회수공정이 전체공정에서 핵심적인 역할을 하고 있다14). 먼저 폐리튬이온 배터리에서 플라스틱을 제거한 다음 유가금속인 코발트, 니켈 및 구리를 농축하기 위해 용용환원처리를 통해 금속합금으로 회수한다15). 이와 같이 회수한 금속합금을 무기산 용액으로 침출시킨 다음 용매추출, 침전 및 이온교환을 통해 금속이온을 분리한다16,17,18,19). 이때 침출과정에서 유가금속의 회수율을 높이기 위해서 산화제를 첨가하거나 고농도의 산을 필요로 한다20).
본 연구에서는 폐리튬이온 배터리에 함유되어 있는 유가금속인 코발트, 니켈 및 구리의 회수를 위한 습식제련의 전처리로 용융환원된 금속합금의 염산용액에 의한 침출을 조사하였다. 표준환원전위가 수소이온보다 높은 구리의 경우 산화제를 첨가하지 않으면 침출되지 않는다21,22). 따라서 산화제로 과산화수소를 첨가했으며, 염산과 과산화수소의 농도, 반응온도 및 시간, 광액밀도를 변화시켜 목적금속인 코발트, 니켈 및 구리를 99% 이상 침출할 수 있는 조건을 조사하였다.
2. 실험재료 및 실험방법
본 실험에 사용한 금속합금시료는 국내 제련업체로부터 제공받았으며, 금속 조성비를 Table 1에 나타냈다. 침출액으로 시약급 염산(Daejung chemicals & metals Co. Ltd., Korea., 35%)을 희석하여 농도를 조절한 후 사용했다. 산화제로는 과산화수소(H2O2, Daejung Chemical. Co., Korea., 30%)를 염산과 혼합하여 사용했다. 침출실험시 광액밀도의 영향에 대한 실험을 제외하고는 침출용액의 부피에 대한 금속의 중량비를 45 g/L로 조절 하였으며, 디지털 가열식 자력 교반기(WiseStir MSH-20D, Daihan Scientific Co., Korea)를 사용하여 반응온도 및 시간을 조절하였다. 일정 농도의 염산용액을 반응온도까지 가열한 다음, 시료와 과산화수소를 반응 플라스크에 첨가시켜 침출실험을 진행했다. 모든 실험에서 교반속도는 300 rpm으로 조절했고, 침출반응 후 여과를 통해 잔사와 용액을 분리하였다. 침출후 여과한 용액중 금속 농도는 유도결합 플라즈마 원자방출 분광기(Inductively Coupled Plasma-Optical Emission Spectometer)로 분석했으며, 금속의 침출률은 다음 식으로 계산했다.
여기서 VM 과 CM은 침출 용액에서 금속 이온의 부피와 농도이고, MO는 침출실험 전 시료에 함유된 금속 질량이다.
Table 1.
Composition of the metallic alloys produced by smelting reduction of spent lithium-ion batteries
|
Wt%
|
Co
|
Ni
|
Cu
|
Mn
|
Fe
|
Al
|
Si
|
|
%
|
12.9
|
61.99
|
22.33
|
1.58
|
0.498
|
0.0024
|
0.34
|
3. 결과 및 고찰
3.1. 염산 농도에 따른 금속의 침출 거동
염산농도가 금속합금에 함유된 금속의 침출에 미치는 영향을 조사하기 위해 염산농도를 1에서 3 M까지 변화시켜 실험을 수행했다. 이때 과산화수소의 농도는 10%, 45 g/L의 광액밀도, 60°C에서 300 rpm의 교반속도로 90분동안 반응을 진행시켰다. 실험결과인 Fig. 1을 보면 1 M의 염산용액에서 니켈은 대부분 침출되었으나 코발트와 구리의 침출률은 각각 82.0, 17.6%로 낮았다. 염산농도가 2 M이상인 조건에서는 규소를 제외한 다른 금속이 대부분 침출되었다. 규소가 침출되면 수용액에서 실리케이트로 존재하는데 실리케이트를 수용액에서 제거하는 것이 어려우므로 규소의 침출률이 낮은 것이 후속 분리정제단계에 유리하다. 따라서 염산 2 M이 본 시료인 합금의 침출에 적합하다. 염산과 과산화수소의 혼합용액에서 2가 금속(M)의 침출반응을 다음과 같이 나타낼 수 있다23).
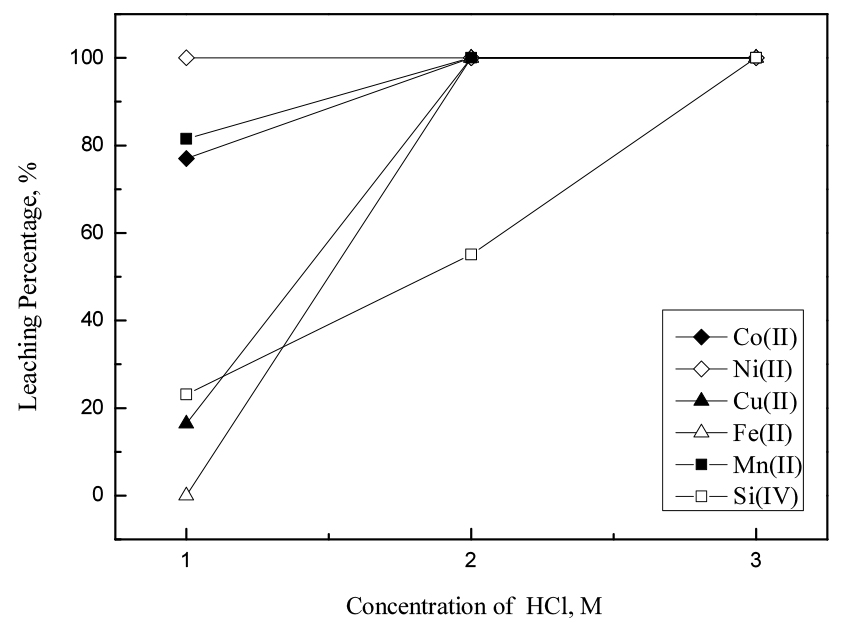
Fig. 1.
Effect of HCl concentration on the leaching of metals from the smelting reduced metallic alloys (Concentration of H2O2 : 10%(v/v), temperature : 60℃, stirring speed : 300 rpm, time : 90 min, pulp density : 45 g/L).
3.2. 과산화수소 농도에 따른 금속의 침출거동
과산화수소의 농도가 금속합금에 함유된 금속들의 침출에 미치는 영향을 조사하기 위해 염산농도 2 M의 조건에서 과산화수소 농도를 5- 15%로 조절하여 실험한 결과를 Fig. 2에 나타냈다. 반응 조건은 45 g/L의 광액밀도, 60°C의 온도에서 300 rpm 교반속도로 90분 동안 반응을 진행시켰다. 10% 이상의 과산화수소를 첨가하면 규소를 제외한 모든 금속이 침출되었으나, 5%의 과산화수소에서 코발트와 구리는 각각 78.1%, 79.4%의 침출률을 나타냈고 니켈은 99% 이상 침출되었다. 이러한 결과는 니켈의 경우 표준환원전위가 수소이온보다 낮지만 구리이온은 수소이온보다 높기 때문에 구리를 침출시키기 위해서는 산화제가 필요한 것과 잘 일치한다21,22). 과산화수소농도가 10%인 조건에서 유가금속의 침출이 가능하지만, 산화제의 농도를 감소시킬 수 있는 조건을 조사하기 위해 과산화수소의 농도를 5%와 10%로 변화시켜 반응온도, 반응시간 및 광액밀도에 따른 금속침출률을 조사하였다.
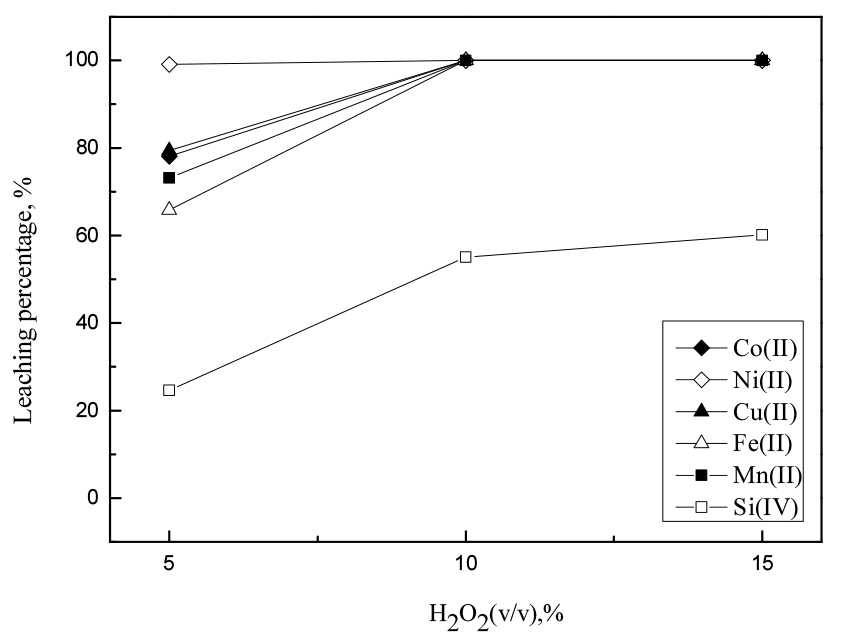
Fig. 2.
Effect of H2O2 concentration on the leaching of metals from the smelting reduced metallic alloys (Concentration of HCl : 2 M, temperature : 60℃, stirring speed : 300 rpm, time : 90 min, pulp density : 45 g/L).
3.3. 반응온도에 따른 추출거동
5% 과산화수소 농도조건에서 반응온도에 따른 침출률을 조사하기 위해 염산농도를 2 M, 45 g/L의 광액밀도, 반응시간을 90분으로 조절한 다음 반응온도를 20에서 80°C로 변화시켜 실험한 결과를 Fig. 3에 나타냈다. 반응온도가 증가함에 따라 모든 금속의 침출률이 증가하였지만 80°C에서 코발트, 니켈 및 구리는 각각 81.1, 99.9, 83.2%로 침출률이 소폭 증가하여 상기 세 금속이 99% 이상 침출되지 않았다. 10%의 과산화수소에서 반응온도의 영향을 알아보기 위해 5%의 실험조건과 동일하게 실험을 진행하여 실험한 결과를 Fig. 4에 나타냈다. 반응온도 20°C에서는 철과 규소의 경우 각각 97.6, 40.7% 침출률을 보이고 나머지 금속들은 99% 이상의 침출률을 달성했다. 40°C 이상의 온도에서 철도 모두 용해되었으며 규소의 경우는 반응온도에 따라 침출률이 점차 증가하여 80°C에서 58.1%의 침출률을 보였다. 본 논문의 온도범위에서 규소를 제외한 다른 금속의 경우 반응온도 40°C에서 모두 용해시키는 것이 가능했다.
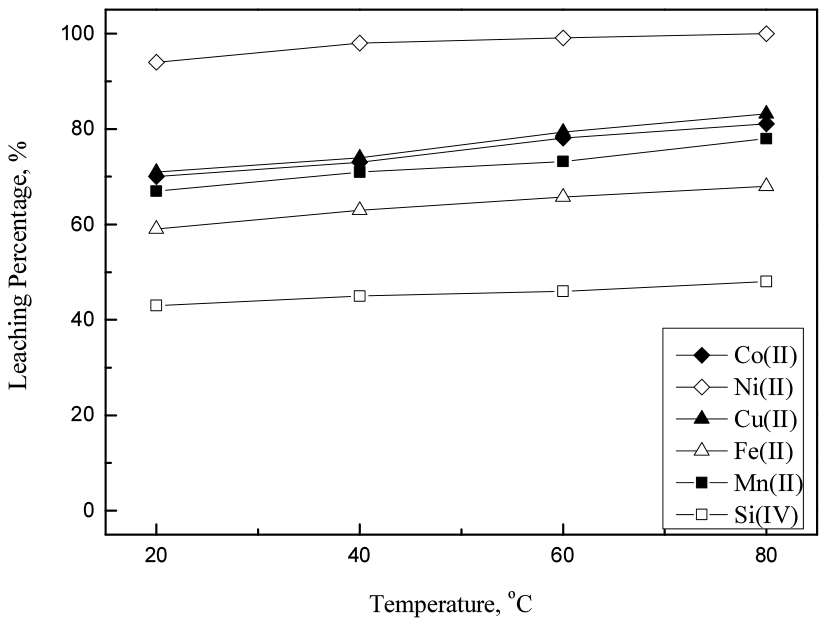
Fig. 3.
Effect of reaction temperature on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 5% H2O2 (stirring speed : 300 rpm, time : 90 min, pulp density : 45 g/L).
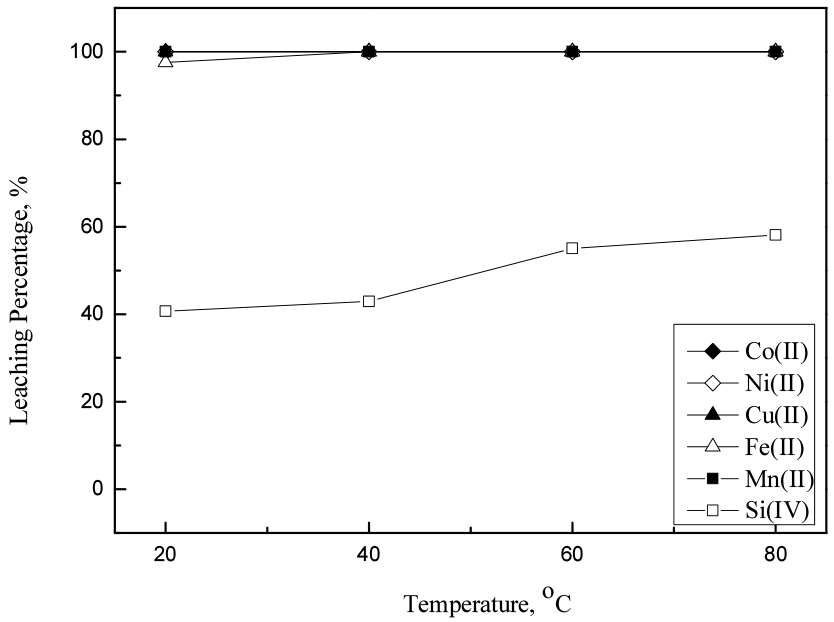
Fig. 4.
Effect of reaction temperature on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 10% H2O2 (stirring speed : 300 rpm, time : 90min, pulp density : 45 g/L).
3.4. 반응시간의 영향
3.3절의 연구결과에 따르면 5%와 10% 과산화수소 농도조건에서 반응온도는 금속의 침출에 큰 영향을 미치지 않았다. 반응시간이 침출에 미치는 영향을 파악하기 위하여 2 M의 염산농도에서, 60°C 반응온도, 45 g/L의 광액밀도에서 반응시간을 변화시켜 실험한 결과를 Figs. 5와 6에 나타냈다. 과산화수소의 농도가 5%에서의 실험결과인 Fig. 5를 보면 반응시간이 증가함에 따라 120분 이상에서 니켈이 99% 이상 침출되었지만, 코발트와 구리는 각각 81.0과 85.2%만 침출되었다. 반면 과산화수소 농도가 10%에서의 결과인 Fig. 6을 보면 반응시간 30분까지 침출률이 급격히 증가하여 90분에서 규소을 제외한 모든 금속이 99% 이상 침출되었다. 이 결과로부터 5%의 과산화수소 농도를 사용하는 경우 니켈을 제외한 코발트와 구리의 완전 침출이 어렵고, 10% 과산화수소를 첨가하면 2 M의 염산농도, 90분의 반응시간 및 60°C의 반응온도에서 목적금속을 99%의 이상 침출하는 것이 가능한 것을 알 수 있다.
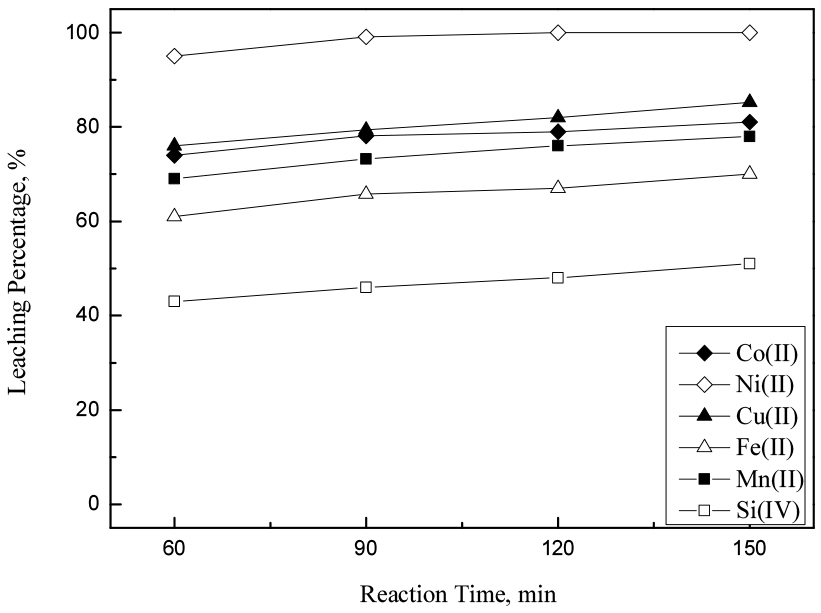
Fig. 5.
Effect of reaction time on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 5% H2O2 (stirring speed : 300 rpm, temperature : 60°C, pulp density : 45 g/L).
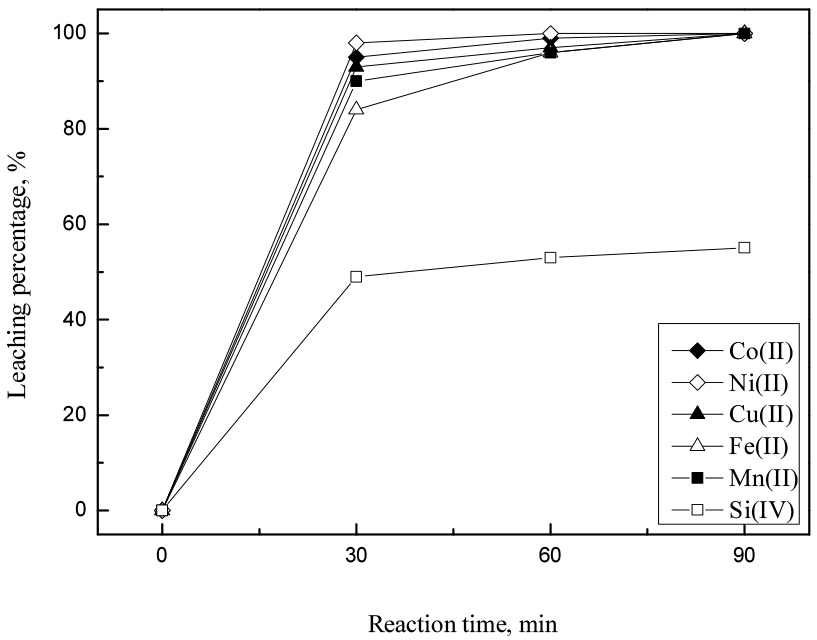
Fig. 6.
Effect of reaction time on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 10% H2O2 (stirring speed : 300 rpm, temperature : 60°C, pulp density : 45 g/L).
3.5. 광액밀도에 따른 추출거동
광액밀도가 변하면 실제 침출반응에 참여하는 염산과 과산화수소의 화학당량비가 변하므로 금속의 침출률에 큰 영향을 미친다. 즉 5%의 과산화수소 농도 조건에서 광액밀도를 감소시키면 코발트와 구리가 99%이상 침출될 수 있을 것으로 예상된다. 5%의 과산화수소 농도조건에서 반응시간을 150분으로 조절하고 광액밀도를 30에서 60 g/L로 변화시켜 실험한 결과를 Fig. 7에 나타냈다. 또한 10%의 과산화수소 농도조건에서는 반응시간을 90분으로 조절하고 광액밀도를 40에서 100 g/L로 변화시켜 실험한 결과를 Fig. 8에 나타냈다. Fig. 7에서 광액밀도가 증가할수록 모든 금속의 침출률이 감소했으며 30 g/L의 광액밀도에서 규소를 제외한 모든 금속이 99% 이상 침출되었다. Fig. 8을 보면 50 g/L 의 광액밀도에서 구리의 침출률이 96%으로 감소하기 시작하여 이후 60 g/L에서 니켈과 망간을 제외한 다른 금속들의 침출률이 감소하였다. 70 g/L 이상의 조건에서는 니켈의 침출률이 감소하기 시작하여 100 g/L의 광액밀도에서 76.3%의 침출률을 보였다.
상기 실험자료로부터 염산농도 2 M에서 과산화수소 농도가 각각 5%와 10% 인 조건에서 규소를 제외한 다른 금속을 99%이상 침출할 수 있는 조건은 다음과 같다.
1) 5% 과산화수소 : 60°C의 반응 온도, 150분의 반응시간, 30 g/L의 광액밀도
2) 10% 과산화수소 : 60°C의 반응온도, 90분의 반응시간, 45 g/L의 광액밀도
1)과 2)를 비교하면 5%의 과산화수소의 경우 150분의 반응시간으로 2)에 비하여 60분가량 더 길다. 하지만 1)조건의 경우 과산화수소 농도가 2)조건의 절반이므로 가격이 비싼 산화제의 양을 줄일 수 있다. 또한 광액밀도로 비교하면 1)에서는 30 g/L, 2)에서는 45 g/L로 과산화수소의 농도가 두배인데 반해 용해가능한 금속질량비는 1.5배 이다. 따라서 침출공정의 경제성을 고려하면 1)조건이 더 효율적이다.
폐리튬전지를 고온에서 용융환원시 철과 실리콘의 환원율은 환원온도에 비례한다. 따라서 니켈과 코발트의 금속환원율을 높이기 위해 환원온도를 상승시키면 환원금속중 철과 실리콘의 함량이 증가한다. 실리콘을 염산으로 침출하면 실리케이트로 존재하며, 철은 3가 이온으로 존재한다. 염산침출액에 함유된 코발트와 니켈의 분리를 위한 용매추출 예비실험결과 철이온과 실리케이트의 농도는 후속 코발트와 니켈의 분리에 큰 영향을 미치지 않았다.
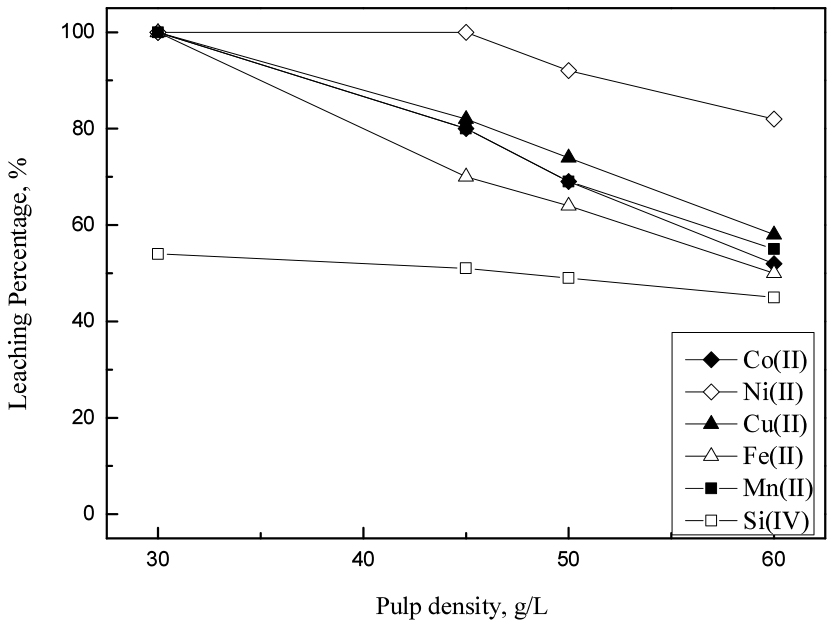
Fig. 7.
Effect of pulp density on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 5% H2O2 (stirring speed : 300 rpm, temperature : 60°C, time : 150 min).
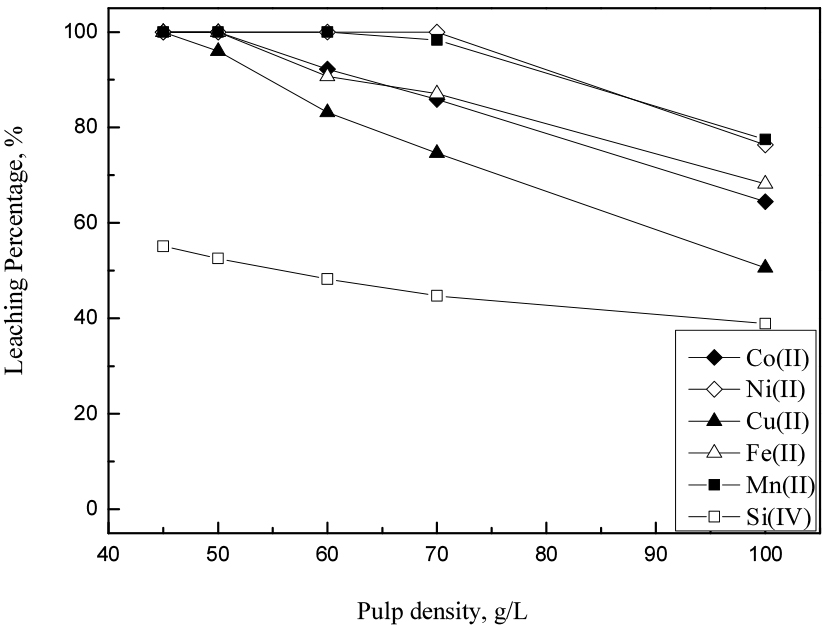
Fig. 8.
Effect of pulp density on the leaching of metals from the smelting reduced metallic alloys by the mixture of 2 M HCl and 10% H2O2 (stirring speed : 300 rpm, temperature : 60°C, time : 150 min).
4. 결 론
폐리튬이온 배터리를 용융환원처리한 금속합금상에 함유된 코발트, 니켈 및 구리를 회수하기 위한 습식공정 개발을 위해 염산용액에 의한 침출을 조사하였다. 본 논문에서 시료로 사용한 금속합금상은 상기 세 목적금속외에 철, 망간과 규소를 함유했다. 구리를 침출시키기 위해 산화제로 과산화수소를 염산용액에 첨가해서 침출용액으로 사용했다. 본 논문에서는 염산농도를 1에서 3 M까지, 과산화수소의 농도는 5에서 15%로 변화시켜 반응시간, 반응온도 및 광액밀도에 따른 금속의 침출률을 조사했다. 금속합금에 함유된 성분중 규소를 제외한 코발트, 니켈, 구리, 망간과 철은 염산농도 2 M의 조건에서 과산화수소 농도와 광액밀도를 조절하여 모두 침출하는 것이 가능했다. 침출액중 과산화수소의 농도와 광액밀도를 감안하면 2 M의 염산용액과 5%의 과산화수소의 혼합용액으로 60°C, 150분의 반응시간, 30 g/L의 광액밀도로 침출하는 것이 경제성이 우수하며 규소를 제외한 모든 금속이 99% 이상 침출되었다.
Acknowledgements
본 연구는 2021년도 산업통상자원부 및 산업기술평가관리원(KEIT) 연구비 지원에 의한 연구결과(과제번호 20011183)이며 이에 감사드립니다.
References
Dia, Y., Xu, Z., Hua, D., et al., 2020 : Theoretical-molar Fe
3+ recovering lithium from spent LiFePO
4 batteries: an acid-free, efficient, and selective process, Journal of Hazardous Materials, 396, 122707.
10.1016/j.jhazmat.2020.12270732353734Sun, Y., Zhu, M., Yao, Y., et al., 2020 : A novel approach for the selective extraction of Li
+ from the leaching solution of spent lithium-ion batteries using benzo-15-crown-5 ether as extractant, Separation and Purification Technology, 237, 116325.
10.1016/j.seppur.2019.116325Chen, S., Wang, Z., Yan, W., 2020 : Identification and characteristic analysis of powder ejected from a lithium ion battery during thermal runaway at elevated temperatures, Journal of Hazardous Materials, 400, 123169.
10.1016/j.jhazmat.2020.12316932574883Li, J., Lai, Y., Zhu, X.., et al., 2020 : Pyrolysis kinetics and reaction mechanism of the electrode materials during the spent LiCoO
2 batteries recovery process, Journal of Hazardous Materials, 398, 122955.
10.1016/j.jhazmat.2020.12295532474320Yadav, P., Jie, C. J., Tan, S., et al., 2020 : Recycling of cathode from spent lithium iron phosphate batteries, Journal of Hazardous Materials, 399, 123068.
10.1016/j.jhazmat.2020.12306832521319Winslow, K. M., Laux, S. J., Rownsend, T. G., 2018 : A review on the growing concern and potential management strategies of waste lithium-ion batteries, Resources, Conservation & Recycling, 129, pp.263-277.
10.1016/j.resconrec.2017.11.001Yang, J., Gu, F., Guo, J., 2020 : Environmental feasibility of secondary use of electric vehicle lithium-ion batteries in communication base stations, Resources, Conservation & Recycling, 156, 104713.
10.1016/j.resconrec.2020.104713Fernandes, A., Afonso, J. C., Dutra, A. J. B., 2012 : Hydrometallurgical route to recover nickel, cobalt and cadmium from spent Ni-Cd batteries, Journal of Power Sources, 220, pp.286-291.
10.1016/j.jpowsour.2012.08.011Wang, X., Gaustad, G., Babbitt, C. W., 2016 : Targeting high value metals in lithium-ion battery recycling via shredding and size-based separation, Waste Management, 51, pp.204-213.
10.1016/j.wasman.2015.10.02626577459Liu, C., Deng, Y., Chen, J., et al., 2017 : An Integrated Process to Recover NiMH Battery Anode Alloy with Selective Leaching and Multi-stage Extraction, Industrial & Engineering Chemistry Research.
Pindar, S., Dhawan, N., 2020 : Recycling of mixed discarded lithium-ion batteries via microwave processing route, Sustainable Materials and Technologies, 25, e00157.
10.1016/j.susmat.2020.e00157Silveira, G. T. R., Chang, S. Y. 2010 : Cell phone recycling experiences in the United States and potential recycling options in Brazil, Waste Management, 30, pp.2278-2291.
10.1016/j.wasman.2010.05.01120554440Bertuol, D. A., Bernardes, A. M., Tenorio, J. A. S., 2006 : Spent NiMH batteries: Characterization and metal recovery through mechanical processing, Journal of Power Sources, 160, pp.1465-1470.
10.1016/j.jpowsour.2006.02.091Hageluken, C., 2006 : Recycling of Electronic Scrap at Umicore’s Integrated Metals Smelter and Refinery, World of Metallurgy - ERZMETALL, 59, pp.154-161.
Lisbona, D., Snee, T., 2011 : A review of hazards associated with primary lithium and lithium-ion batteries, Process Safety and Environmental Protection, 89, pp.434-442.
10.1016/j.psep.2011.06.022Li, L., Ge, J., Chen, R., et al., 2010 : Environmental friendly leaching reagent for cobalt and lithium recovery from spent lithium-ion batteries, Waste Management. 30, pp.2615-2621.
10.1016/j.wasman.2010.08.00820817431Aaltonen, M., Peng, C., P.Wilson, B., et al., 2017 : Leaching ofMetals from Spent Lithium-Ion Batteries, Recycling, 2(20), pp.1-9.
10.3390/recycling2040020Peng, C., Hamuyuni, J., P.Wilson, B., et al., 2018 : Selective reductive leaching of cobalt and lithium from industrially crushed waste Li-ion batteries in sulfuric acid system, Waste Management, 76, pp.582-590.
10.1016/j.wasman.2018.02.05229510945Chen, X., Chen, Y., Zhou, T., 2015 : Hydrometallurgical recovery of metal values from sulfuric acid leaching liquor of spent lithium-ion batteries, Waste Management, 38, pp.349-356.
10.1016/j.wasman.2014.12.02325619126Chen, L., Tang, X., Zhang, Y., et al., 2011 : Process for the recovery of cobalt oxalate from spent lithium-ion batteries, Hydrometallurgy, 108(1-2), pp.80-86.
10.1016/j.hydromet.2011.02.010Moon, H. S., Song, S. J., Tran, T. T., et al., 2021 : Leaching of Cobalt and Nickel from Metallic Mixtures by Inorganic and Organic Acid Solutions, Resources Recycling, 30(2), pp.53-60.
Rybka, P., Regel-Rosocka, M., 2012 : Nickel and Cobalt Extraction from Chloride Solutions with Quaternary Phosphonium Salts, Separation Science and Technology, 47(9), pp.1296-1302.
10.1080/01496395.2012.672532Tran, T. T., Moon, H. S., Lee, M. S., 2020 : Separation of Cobalt, Nickel, and Copper from Synthetic Metallic Alloy by Selective Dissolution with Acid Solutions Containing Oxidizing Agent, Mineral Processing and Extractive Metallurgy Review, pp.1-13.
10.1080/08827508.2020.1858079











