1. 서 론
2. 백금족 금속의 생산량과 리사이클링
3. 백금족 금속의 제련
3.1. 황화광으로부터 백금족 금속의 추출
3.2. 비철금속 제련공정에서의 백금족 금속 회수
4. 백금족 금속의 리사이클링 기술
4.1. 건식법에 의한 백금족 금속의 농축
4.2. 백금족 금속의 침출과 환원
4.3. 백금족 금속의 분리와 정제
4.4. 폐촉매의 리사이클링
5. 종 합
1. 서 론
백금족 금속(Platinum Group Metals, PGMs)은 백금(Pt), 팔라듐(Pd), 로듐(Rh), 이리듐(Ir), 루테늄(Ru), 오스뮴(Os)의 6가지 원소이다. 여기에 금(Au), 은(Ag)을 더하여 8 원소를 귀금속이라 한다. 유럽에 백금이 알려진 것은 스페인의 군인이면서 탐험가, 천문학자인 우로아(Antonio de Ulloa)가 1735년에 남비 콜럼비아의 초코(Choco)지방에 있는 핀토(Pinto) 강변에서 은과 비슷한 백색 금속인 백금을 발견하여 본국에 보고하면서 알려지게 되었다. 그 기록에 백금은 ‘핀토강가의 보잘것 없는 은(platina del Pinto)’으로 불리어 원소명인 ‘Platinum’의 어원이 되었다1).
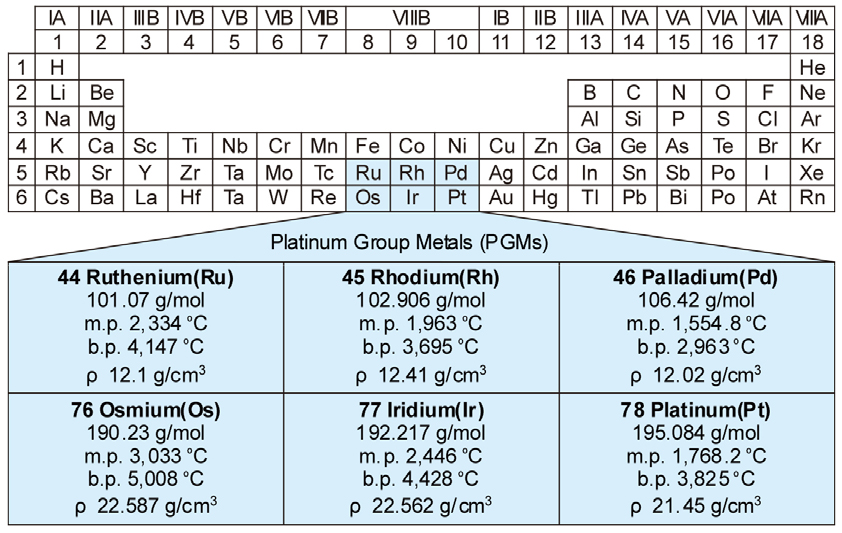
Fig. 1에는 백금족 금속의 물성을 주기율표와 함께 비교하여 나타내었다2). 백금족 금속에는 Pd, Rh, Ru과 같이 비중이 약 12 g/cm3인 경백금족과 Pt, Ir, Os과 같이 비중이 약 22 g/cm3인 중백금족으로 구분할 수 있다3). 백금족 금속은 융점이 높고, 내열성, 내식성이 우수하며, 특이한 촉매 특성을 가지는 등 전기, 화학, 및 물리적 성질이 우수하여 장신구, 치과재료, 석유화학 촉매, 자동차용 촉매, 도가니, 전기전자부품 등 다양한 분야에서 이용되고 있다. 최근에는 초고순도(5N), 고기능성이 요구되는 고밀도 자성재료, 고온 형상기억 소재, 연료전지용 전극 촉매, 정밀센서, BT분야에서 제암제 원료와 같이 첨단 미래산업으로의 응용이 확대되고 있다. 백금족 금속이 사용되는 부품에서 백금족 금속을 대체할 만한 소재가 아직 개발되지 않아 향후 그 수요가 꾸준히 증가할 것으로 예상된다4). 다만 Os은 산소와 반응하기 쉽고, 분말인 경우는 상온에서도 유독한 산화물이 되므로 합금원소 이외에는 그다지 사용되지 않는 금속이다5). Table 1에는 백금족 금속의 주요 용도를 나타내었다6,7).
Table 1.
Application of PGMs in products
이러한 백금족 금속은 희소금속으로 생산량이 제한되어 있을 뿐만 아니라, 1차 공급원인 광산이 극히 한정된 국가의 특정 지역에 편재되어 있다. 백금족 금속 중에서 가장 생산량이 많은 Pd의 연간 생산량도 300 톤이 되지 않는 수준이다. 따라서 자원의 안정적인 공급을 위해서 신뢰성 높은 자원 버퍼를 구축하고 장기적인 순환이용을 할 수 있는 공급선을 확보하는 것이 매우 중요하다. 한편 백금족 금속의 새로운 리사이클링 기술을 개발하기 위해서는 제련기술을 이해하는 것이 필요하다. 특히 백금족 금속이 단체로 존재하는 경우도 있으나 촉매와 같이 담채에 포함되어 있거나 다른 금속들과 혼합되어있는 경우 백금족 금속의 제련 및 정련 기술을 응용할 수 있을 것이다. 따라서 본 논문에서는 백금족 금속의 제련기술과 함께 폐촉매의 리사이클링 기술에 대해 보고한다.
2. 백금족 금속의 생산량과 리사이클링
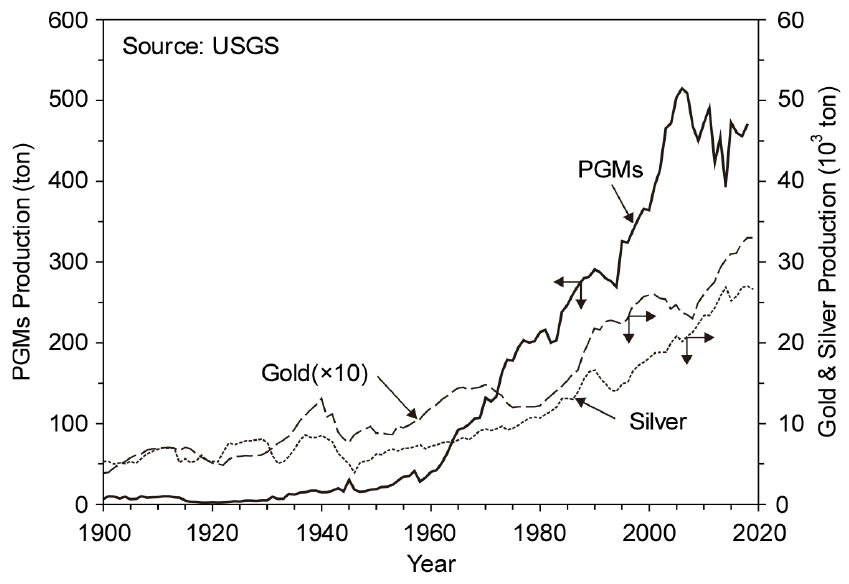
Fig. 2에는 백금족 금속과 금, 은 1차 지금(광산에서 채굴되어 생산된 것)의 년간 생산량 변화를 비교하여 나타내었다8). 전체적으로는 은의 생산량이 가장 많으며, 금은 은의 약 1/10, 백금족 금속은 금의 약 1/50 정도인 것을 알 수 있다. 백금족 금속의 생산량은 일반 금속들에 비하여 변동폭이 큰 편이지만 1960년대에 들어서서 생산량이 큰 폭으로 증가한 것을 알 수 있다. 특히 백금족 금속의 광산 생산량은 1962년까지는 년간 50 톤 미만이었으나, 그 이후 급격하게 증가하기 시작하여 1968년부터 100 톤을 초과하였으며, 1994년부터 현저하게 증가하여 2006년에는 515 톤으로 최댓값을 나타내었으나 2018년에는 471 톤을 생산하였다.
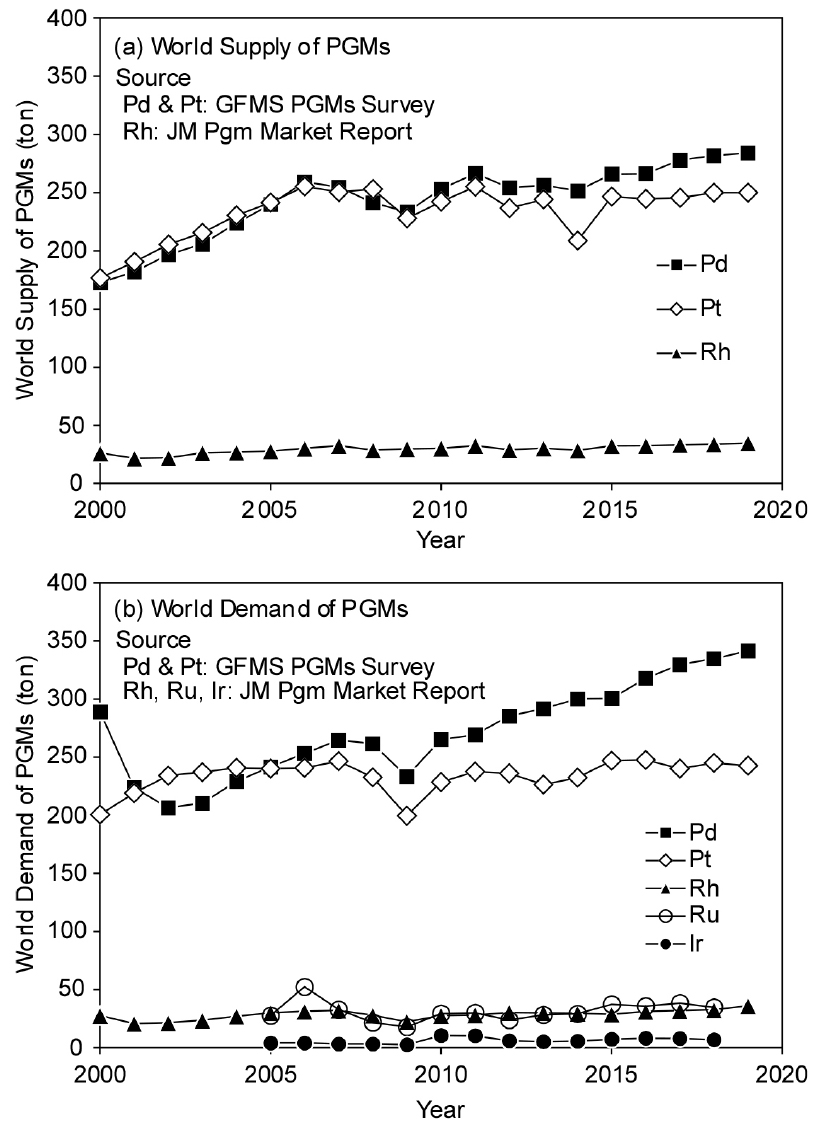
Fig. 3에는 백금족 금속 중 생산량이 많은 Pd, Pt, Rh의 공급량과 수요량의 변화를 나타내었다9,10,11). 백금족 금속의 공급원으로는 광산과 스크랩으로 구분할 수 있다. Pd과 Pt의 공급량은 1994년부터 현저하게 증가하기 시작하였으나, 2006년부터는 큰 폭의 변화는 없다. 최근(2018년)의 Pd과 Pt의 공급량은 각각 279 톤, 238 톤 수준이지만, Rh의 공급량은 2016년 기준으로 33.9 톤 수준에 불과하다. 한편 Pd 수요의 대부분은 촉매이며, 2010년부터 꾸준히 증가하는 추세에 있고, 수요가 공급량보다 많은 편이다. Pt의 수요는 촉매와 보석 및 장식용이지만, 공급량과 마찬가지로 최근에는 큰 변동이 없지만, 광산 공급량 감소분을 자동차 폐촉매 스크랩의 리사이클링에 의한 공급량 증가가 상쇄하여 오히려 공급 과잉인 상태에 있다. Rh도 대부분은 촉매에 사용되고 있고, 일부 화학산업이나 유리산업에 사용되지만, 최근의 수요는 30 톤에 못 미치는 수준이며 오히려 공급량이 많은 실정이다.
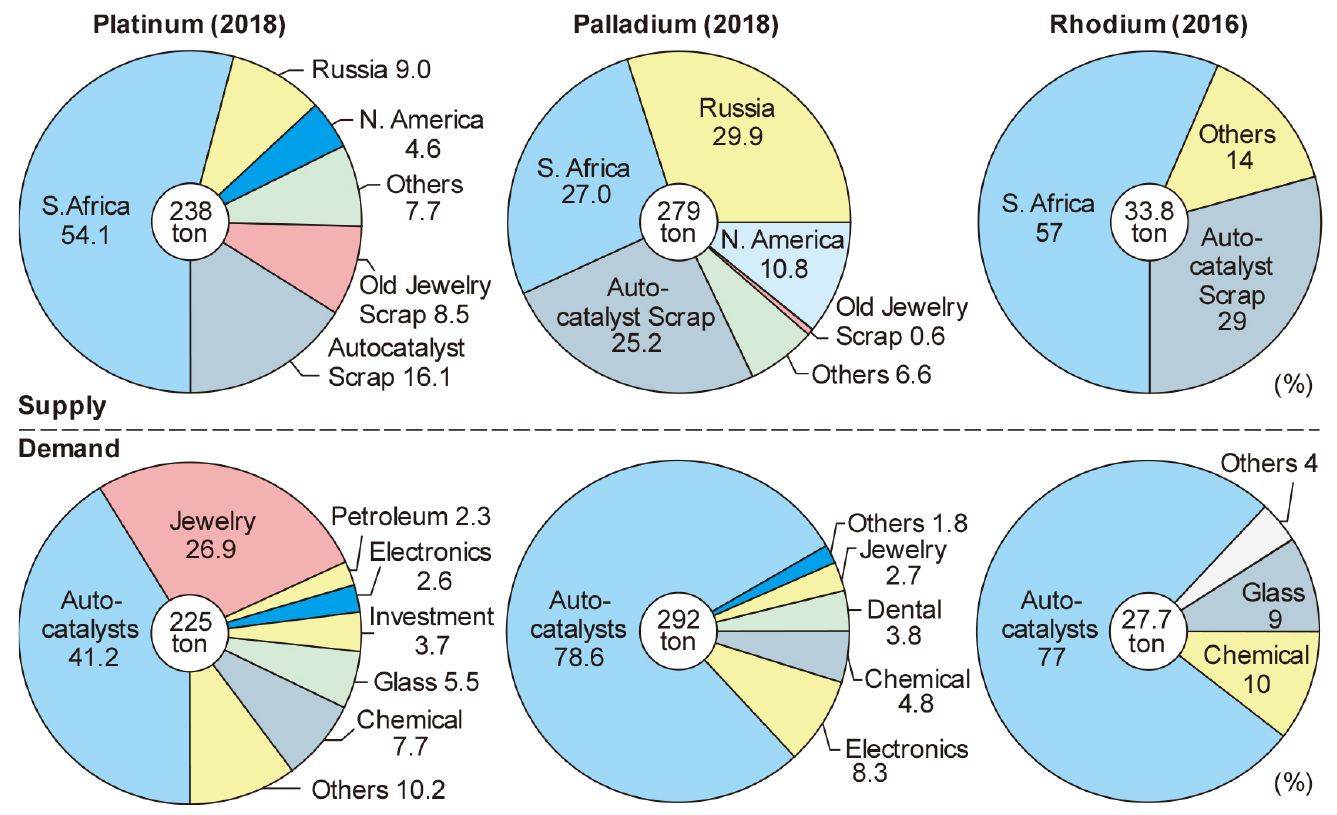
Fig. 4에는 2018년 기준 Pt, Pd, Rh(2016년)의 공급원에 따른 공급량과 용도를 비교하여 나타내었다11). 2018년 기준의 전 세계 Pt 생산량은 238 톤이며, 공급원은 광산과 스크랩으로 구분할 수 있다. 광산 생산량의 70 % 이상을, 그리고 전체 공급량의 약 54 %는 남아프리카공화국에서 생산되고 있으며, 러시아에서 약 9 %가 생산되어 지역적 편재가 매우 심한 것을 알 수 있다. 또 자동차의 폐촉매로부터 약 16 %, 중고 보석/장식품 등에서도 약 8.5 %의 Pt이 공급되고 있다. Pd의 전 세계 생산량은 279 톤이지만 광산에서 생산된 것은 약 68 %이며, 나머지는 폐촉매, 장신구, 기타 등으로부터 리사이클링한 것이다. 그러나 Rh은 Pt, Pd 보다 생산량이 훨씬 작으며, 2016년 기준 전 세계 생산량은 33.8 톤에 불과하며, 자동차의 폐촉매를 리사이클링하여 생산된 9.8 톤(29 %)을 제외하면 광산에서 생산된 것은 24 톤(57 %)에 불과하다. 루테늄과 이리듐에 대해서는 생산량이 알려져 있지 않다. 수급상황에 따라 국가별 비축물량이 방출되므로 연간 수요에 대해서만 알려져 있다. 루테늄과 이리듐의 2011년 기준 전 세계 년간 수요는 각각 25.2 톤과 9.4 톤에 불과하다. 이러한 백금족 금속의 대부분은 자동차용 촉매로 사용되고 있으므로, 이의 리사이클링이 중요한 것을 알 수 있다.
3. 백금족 금속의 제련
3.1. 황화광으로부터 백금족 금속의 추출
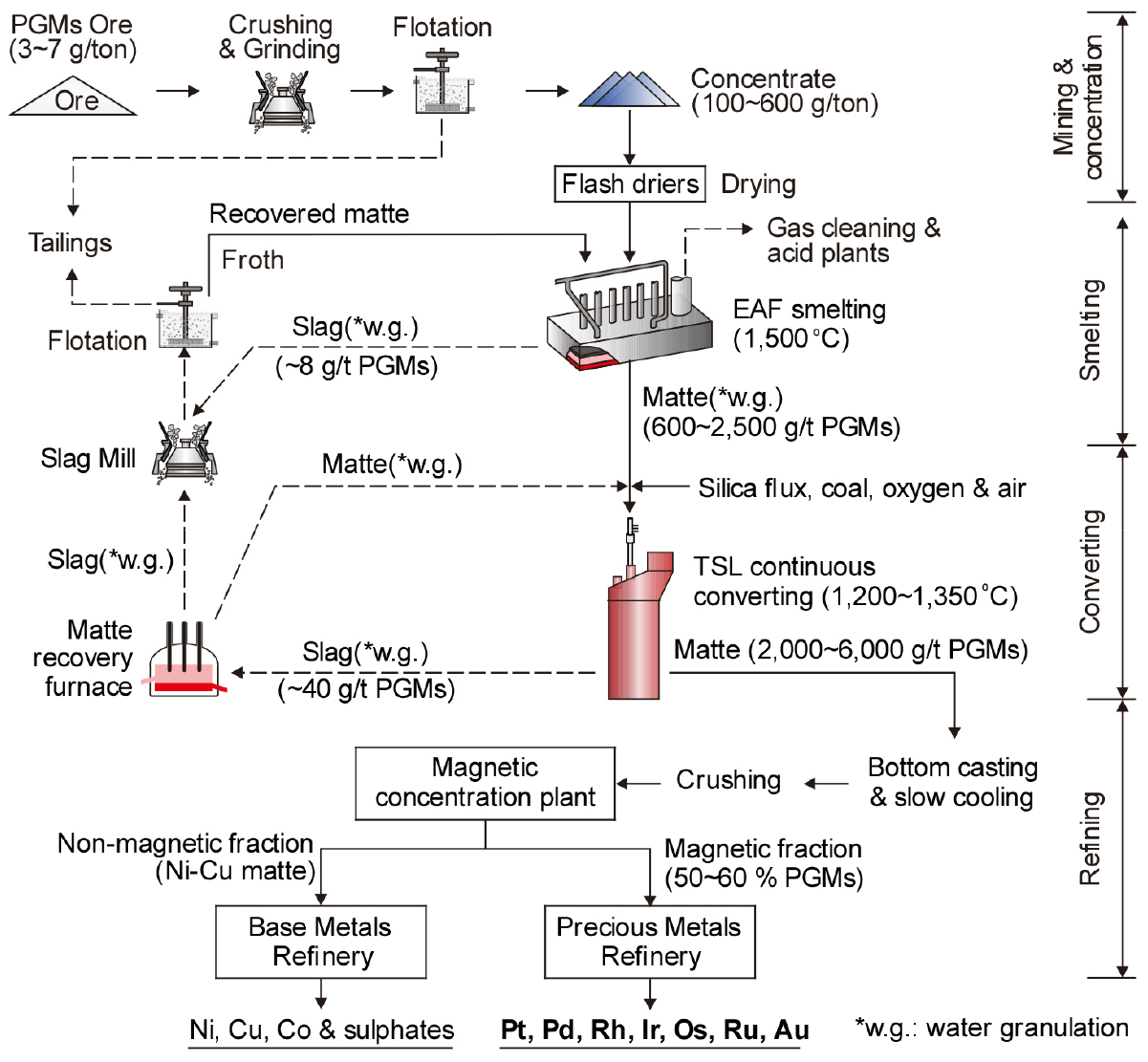
백금족 금속의 주요 광석은 감람암질의 1 차 광상이 2 차적인 풍화작용을 받아서 발생한 사백금이나 남아프리카 및 캐나다의 백금족 금속을 함유한 황화광(Cu 및 Ni 황화광) 등이다. 따라서 백금족 금속의 제련은 광석이나 제련소에 따라 서로 다른 프로세스를 적용하고 있다. Fig. 5에는 남아프리카공화국(Anglo American Platinum)에서 니켈과 구리의 황화광으로부터 백금족 금속을 추출하는 공정도를 재구성하여 나타내었다12,13). 황화광을 사용하므로 정광(백금족 금속 100~600 ppm 함유)을 전기로에서 정련하여 맥석 등의 불순물을 제거하며, 백금족 금속은 황화물인 매트상으로 분배되어 600~2,500 ppm 정도의 백금족 금속을 함유하는 전기로 매트가 얻어진다12).
백금족 금속을 함유하는 전기로 매트는 PS(Peirce-Smith) 전로로 옮겨 산화반응에 의해 매트 중의 철 성분과 유황을 각각 산화철과 SOx로 제거하므로 전기로 매트 중의 PGM은 더욱더 농축된다. 이러한 전로 제련공정에서는 2,000~6,000 ppm의 백금족 금속을 함유하는 전로 매트라 불리는 황화물(Ni3S2-Cu2S-FeS, Ni ~50 wt%, Cu ~30 wt%, S ~20 wt%)이 얻어진다. 전로 공정에서 나온 매트 중의 Ni, Cu, Co 등은 침출시켜 회수하고, 백금족 금속은 침출 잔사를 다시 침출하고 정제하여 얻는다. 따라서 남아공 등에서는 주산물로 백금족 금속을 생산하고 부산물로 Ni, Cu, Co 등을 회수하고 있다. 러시아에서는 니켈 제련의 부산물로 백금족 금속을 생산하고 있다.
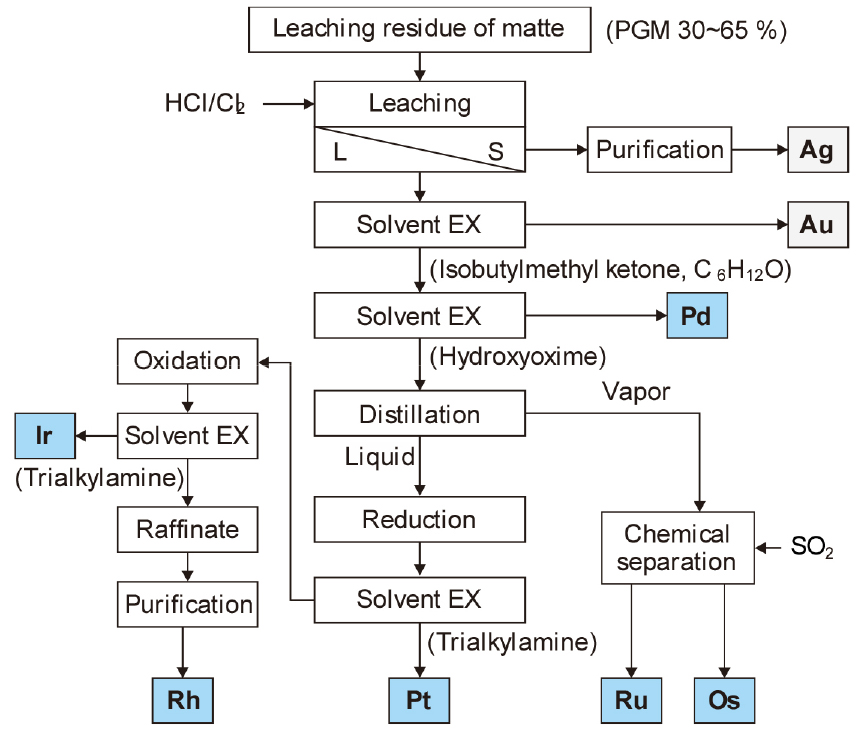
습식공정에서는 고농도로 농축된 전로 매트를 산으로 침출하여 Ni, Cu, Co 등의 비한 금속(base metal)을 분리하고, 남은 잔사로부터 백금족 금속을 분리하여 추출한다. 백금족 금속의 습식제련은 품위나 불순물 원소에 따라 제련소 마다 다양한 방법을 적용하고 있다. Fig. 6에는 남아프리카 Amplats사의 귀금속 제련 공정을 나타내었다12). 그림에 나타낸 바와 같이 귀금속 제련에서는 침전분리법, 이온교환법, 용매추출법, 휘발법, 전해법 등 다양한 분리 방법을 이용하고 있다. 이와 같이 백금족 금속의 습식제련에서는 장시간에 걸친 다단계의 처리 공정을 거쳐 각각의 금속이 얻어진다.
3.2. 비철금속 제련공정에서의 백금족 금속 회수
귀금속이 함유된 전자부품, 리드프레임, 전자기판 등을 Cu나 Pb 정광(concentrate)의 건식제련 공정에 투입하여 유가금속을 회수하기도 한다. 스크랩이나 광석 및 플럭스 중의 백금족 금속은 조동이나 조연 중에 분배되며, 전해정제를 하는 과정에서 발생하는 침전물인 양극 슬라임(anode slime) 중에 농축된다. 양극 슬라임을 배소-고온용융-전기분해 공정으로 처리하여 귀금속을 회수하며, 전해 슬라임법이라고도 한다.
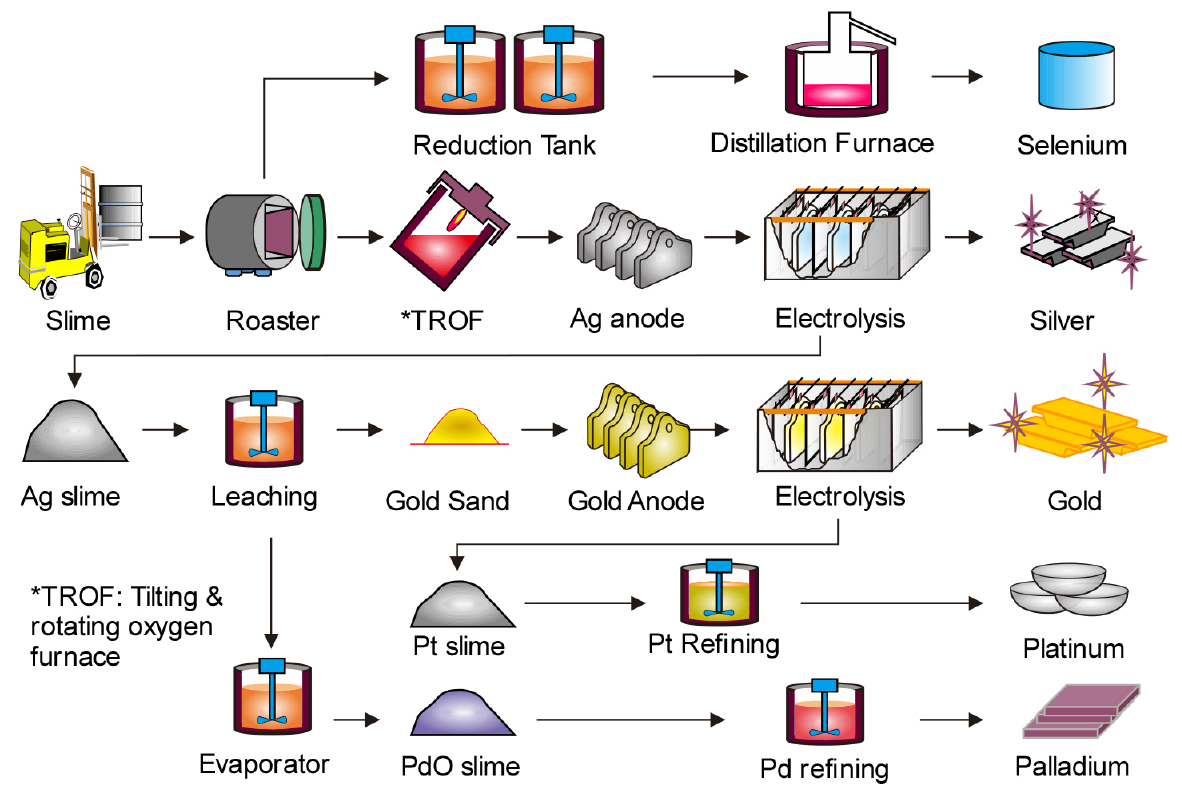
Fig. 7에는 LS-Nikko 동제련에서 양극 슬라임으로부터 Ag, Au와 함께 Pt와 Pd를 회수하는 공정의 예를 나타내었다14). 양극 슬라임 중의 Se은 SO2 가스 분위기 중에서 400~600 °C로 가열하여 증기압이 높은 SeO2의 형태로 휘발 제거한다. Se을 제거한 슬라임을 1,100~1,200 °C로 가열하여 소다회, 붕사 등과 함께 산화·용융시켜 Pb를 슬래그로 제거하고 Ag와 귀금속을 환원시킨다. 귀금속을 함유하는 은 합금은 양극판으로 주조한 후에 전기분해하여 순은과 귀금속이 함유된 양극 슬라임을 얻는다. 이 Ag 슬라임(Au, Pt, Pd 등 함유)을 침출하여 Pd를 분리한 후, Au 양극판으로 주조하고 전기분해에 의해 고순도의 Au를 얻고, 이 과정에서 발생한 Pt 슬라임과 Ag 슬라임의 침출잔사를 별도로 처리하여 Pt과 Pd을 얻고 있다.
4. 백금족 금속의 리사이클링 기술
4.1. 건식법에 의한 백금족 금속의 농축
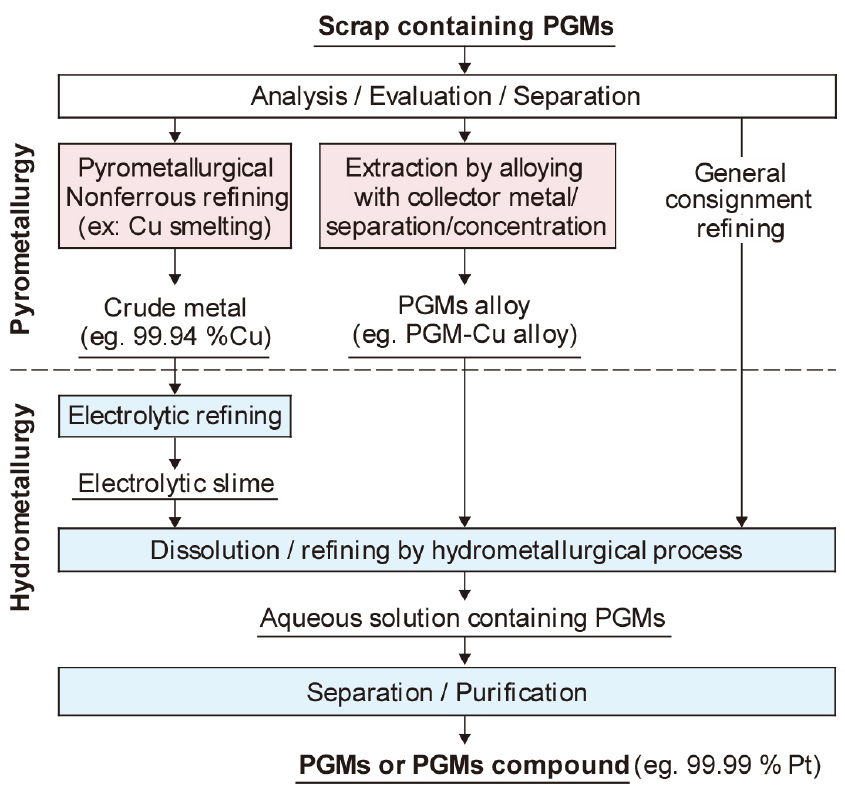
백금족 금속의 리사이클링 기술에는 건식법과 습식법이 있다. Fig. 8에는 백금족 금속을 함유한 스크랩을 처리하는 주요 공정을 나타내었다15). 자동차용 촉매, 석유화학용 촉매, 세라믹에 몰딩되어 있는 반도체 칩 등은 건식법으로 처리하기도 하지만, 스크랩으로부터 백금족 금속을 농축하는 1 단계 공정에서는 건식법을 사용하고, 백금족 금속의 종류별 분리와 정제는 습식법을 이용하는 것이 일반적이다.
Fig. 8에서와 같이 스크랩으로부터 백금족 금속을 회수하는 경우, 비철금속 제련공정에서 처리하는 경우와 전용로에서 처리하는 방법으로 구분할 수 있다. 전자는 백금족 금속을 함유하는 스크랩 등을 용련공정(구리나 납제련)에서 조금속에 포집시킨 후, 전해 정련시 발생하는 anode slime으로부터 Fig. 7과 같이 백금족 금속 등을 회수한다. 이 방법은 높은 실수율로 백금족 금속을 리사이클링할 수 있으나, 공장입지에 제약이 있으며, 백금족 금속을 회수하기까지 많은 시간이 소요되어 경제적이지 못한 측면이 있다. 후자는 백금족 금속 함유 스크랩을 별도의 전기로 등에서 용융시켜 구리나 철 등의 포집 금속에 농축시키는 방법이다. 특히 자동차용 폐촉매 등과 같이 품위가 일정한 다량의 스크랩을 지속적으로 확보할 수 있으면 전용로에서 처리하는 경우가 많다. 전용로에서는 백금족 금속을 포집 금속(Fe, Cu, Ni, Pb, Sn 등)이나 합금, 황화물을 추출제로 이용하여 농축시켜 품위를 높인다.
한편, Pt은 염산 용액에 잘 용해되지 않으며, 용해시키기 위해서는 강력한 산화제가 필요하다. 그러나 Pt을 함유하는 폐기물을 활성 금속 증기와 반응시켜 염산과 쉽게 반응할 수 있도록 한 예가 보고되어 있다. Okabe 등은 Mg이나 Ca 증기와 Pt 함유 스크랩을 반응시킨 후, 금속 염화물을 이용하여 염화 처리한 후에 염산으로 용해하는 방법을 제안하였다16,17,18). 특히 활성 금속과 백금족 금속을 합금화 처리한 후, 염화 처리하면 염소계 수용액에 쉽게 용해되는 것으로 알려져 있다. 이때 염화 처리제로는 CuCl2나 FeCl3 등이 적당한 것으로 알려져 있다19).
4.2. 백금족 금속의 침출과 환원
백금족 금속의 분리와 회수는 원료를 수용액 상태로 만들어 정제하는 경우가 대부분이다. 건식법으로 처리하는 경우에도 포집금속과 합금화시킨 후 침출 등의 공정을 거쳐서 회수하는 경우가 대부분이다. 특히 2차 자원으로부터 백금족 금속을 회수하는 공정에서, 백금족 금속의 침출 비용이 전체 공정의 경제성에 큰 영향을 미치므로 출발 물질에 적합한 침출 용액을 선택하는 것이 중요하다20). 침출액의 선정은 원료 중 귀금속의 종류, 조성, 형태, 회수와 정제 공정에서의 적합도 등에 의해 결정되며, Table 2에 침출액의 종류에 따른 백금족 금속의 용해성을 비교하여 나타내었다21).
Table 2.
Corrosion of the PGMs under various conditions in different solutions
| Reagent | Pt | Pd | Rh | Ir | Ru | Os | *STS |
| HNO3 aq. | △ | ○ | × | × | × | × | × |
| Aqua regia | ○ | ○ | △ | △ | △ | △ | ○ |
| HCl(aq.)+Cl2(g) | ○ | ○ | △ | △ | △ | △ | ○ |
| H2SO4 aq. | × | ○ | △ | × | × | ○ | ○ |
| Alkali cyanide+Oxidizing agent | ○ | ○ | - | - | - | - | × |
고체 원료는 질산, 염산, 황산 등이나 알칼리, 시안화소다 용액을 이용하여 최대한으로 침출한다. 특히 백금족 금속의 용해는 질산이나 왕수를 사용하는 경우가 많다. 왕수는 염산과 질산의 혼합 산으로, 강력한 산화력을 가지는 염화나이트로실(nitrosyl chloride, NOCl)을 형성하여 백금족 금속을 용해한다. 질산을 사용하지 않을 때는 염산 용액을 가열하여 산화제로 염소가스를 이용하여 용해하는 것도 가능하다22). 식 (1), (2), (3)에는 Pt을 용해하여 염화물 착체를 만드는 반응식의 예를 나타내었다20).
그리고 염산 용액에 과산화수소를 첨가하여 생성된 염소가스나 차아염소산(hypochlorous acid, HClO)의 산화 작용으로 백금족 금속의 침출이 진행되기도 한다20).
벌크 상태의 Rh, Ru, Ir 등은 왕수에 잘 용해되지 않지만, 매우 미세한 분말이나 합금화되어 분산된 상태에서는 NaCl과 염소가스 기류 중에서 가열하면 가용성 염을 형성한다. 또 Rh의 경우 산성 황산칼륨으로 가열하면 가용성의 Rh2(SO4)3를 생성하면서 용해된다22).
한편 Pt의 환원은 아연분말이나 포름산염(formate)을 사용한다.
또 염화백금산을 알칼리로 중화하여 포름산염을 첨가하여 회수하기도 한다.
그리고 염화백금산 용액에 염화암모늄을 첨가하면 염화백금산 암모늄의 침전이 생성되며, 이것을 하소하여 Pt을 얻을 수도 있다.
4.3. 백금족 금속의 분리와 정제
회수된 백금족 금속의 분리와 정제는 주로 습식법을 이용하고 있으며, 몇 가지 방법을 조합하여 정제한다. 기본적으로는 침전분리법, 이온교환수지법, 용매추출법, 전해채취법, 산화증류법을 필요에 따라 조합한 복합 프로세스로 정제한다.
4.3.1. 침전분리법
백금족 금속의 침전분리는 회수한 유가물 원료로부터 백금족 금속을 산이나 알칼리 용액으로 침출·용해한 후에 목적 백금족 금속의 용해도가 작은 염으로 침전시켜 정제하는 방법이다. 실제로는 1 회의 조작으로 목적으로 하는 순도를 얻을 수 없으므로 용해-침전분리를 반복한다. 그러나 이러한 조작은 수작업이며 회분식이므로 주요한 분리정제의 단위조작은 용매추출이나 이온교환법으로 바뀌고 있다. Table 3에 정제에 이용되는 침전분리법을 정리하여 나타내었다.
Table 3.
Precipitation methods for refining of PGMs
4.3.2. 용매추출법
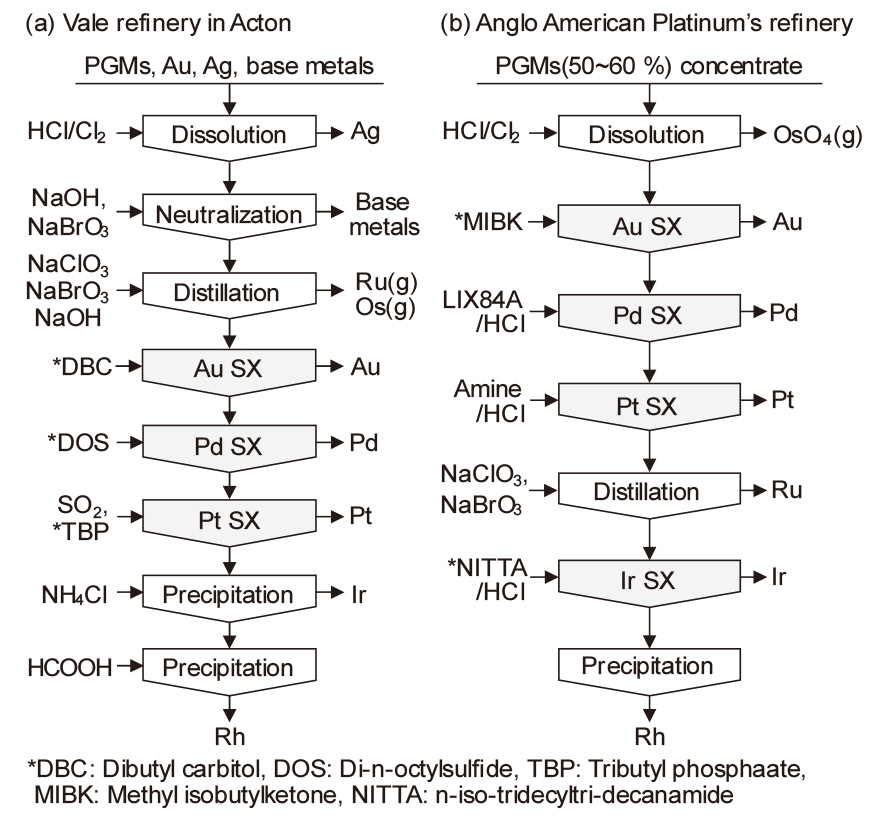
백금족 금속은 화학적 성질이 유사하여 침전분리법을 적용하면 수없이 반복해야 하므로 처리 공정이 길고 회수정제 비용이나 처리 기간도 매우 길다. 따라서 자동화와 연속조작이 가능한 용매추출법이 공업적으로 응용되고 있으며, 많은 연구들이 수행되었다23). 대표적인 용매추출 프로세스로서는 Vale(Acton), Johnson Matthey, Alglo American Platinum 등이 있다. Fig. 9에 공업적으로 적용되고 있는 용매추출 프로세스를 비교하여 나타내었다24).
Fig. 9(a)는 Vale refinery에서 적용하는 것으로, 정광, anode slime, 폐촉매, 전자 스크랩 등에서 백금족 금속을 분리정제할 때 적용하고 있다. 우선 염소가스와 염산용액으로 고체 원료를 용해하고, 이 단계에서 Ag는 AgCl로 침전분리 한다. 그리고 NaOH를 첨가하여 중화에 의해 base metal을 분리한다. 산화제를 첨가하여 Os은 OsO4, Ru는 RuO4로 증류하여 회수한다. 증류한 후의 용액에 HCl을 첨가하여 Au를 DBC(Dibutyl carbitol)로 추출한다. 추출된 Au는 옥살산(oxalic acid)에 의해 역추출되어 직접 Au 분말로 환원된다. 그후 Pd는 DOS(Di-n-octylsulfide)에 의해 추출하고, 암모니아 용액으로 역추출 한다. TBP(tributyl phosphate)를 이용하여 Pt를 추출한 후에 NH4Cl을 첨가하여 (NH4)2IrCl6로 Ir을 침전분리하고 Rh를 회수한다.
한편 Fig. 9(b)의 Anglo American Platinium의 공정은 Johnson Matthey와 거의 유사한 공정이며, Vale와 마찬가지로 시료의 용해는 염소가스와 염산용액을 이용한다. 이 공정에서 Os는 OsO4로서 기체로 분리되며, Ag는 용해 잔사로 회수한다. Au는 MIBK(methyl isobutyl ketone)에 의해 추출하고 옥살산으로 환원시켜 회수한다. 뒤이어 Pd는 LIX84A에 의해 추출되고 6 M 염산으로 역추출한다. Ir을 3가로 환원한 후에 Pt를 아민(amine)으로 추출하고 11 M 염산으로 역추출한다. 그리고 Ru을 증류하여 제거하고, 용액에 남은 Ir과 Rh를 수산화물 침전으로 회수한다. 수산화물을 고농도 염산으로 다시 용해한 후에 Ir을 NITTA(n-iso-tridecyltri-decanamide)에 의해 추출하고, 묽은 염산으로 Ir을 역추출한다. 마지막으로 라피네이트로부터 Rh를 회수한다25).
4.4. 폐촉매의 리사이클링
4.4.1. 폐촉매
백금족 금속의 용도는 다양하지만, 그 고유한 특성을 이용하여 촉매로 가장 많이 사용되고 있다. Table 1에 나타낸 바와 같이 Os을 제외한 나머지 백금족 금속은 촉매로 이용되고 있는 것을 알 수 있다. 따라서 다양한 폐촉매로부터 백금족 금속을 회수하기 위한 많은 연구들이 수행되었다26,27,28,29,30,31,32).
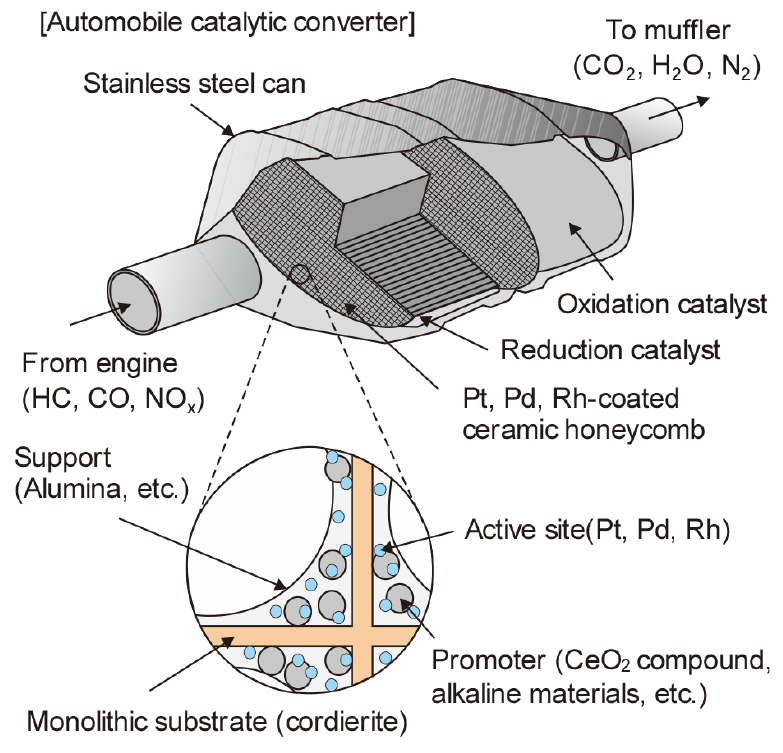
촉매의 조성은 매우 다양하지만 가장 기본이 되는 구조는 Fig. 10과 같다. 일반적으로 담채(support)는 하니컴 구조를 가지는 코디에라이트(cordierite, 2MgO·Al2O3·5SiO2)를 사용한다. 그 내부에 고온에서 높은 표면적을 유지할 수 있는 다공질 산화물(Al2O3)이나 촉매반응을 촉진하는 산화물(CeO2, ZrO2)이 도포되어 있다. 이러한 산화물 위에 백금족 금속의 미립자가 담지되어 있다. 기본적인 구조는 이와 같지만, 다단계의 코팅처리를 하여 다층으로 만들거나, 상류부와 하류부의 위치에 따라 다르게 코팅하기도 한다. 촉매 중 백금족 금속의 양은 차종이나 촉매에 따라 다르지만, 자동차 1 대당 수~10 g 정도로 예상하고 있다.
4.4.2. 폐촉매의 습식처리
백금족 금속은 화학적으로 안정하므로 수용액 중으로 용해하기 위해서는 산화제 및 착화제가 필요하다. 특히 Rh 등이 고농도의 금속상으로 존재할 때는 산화제와 착화제가 있어도 거의 용해되지 않는 것으로 알려져 있다. 이것은 이러한 금속의 용해반응 속도가 느리고 표면이 산소와 결합하여 부동태화되기 때문인 것으로 알려져 있다. 그리고 산 등을 다량으로 사용하므로 폐액 처리 등의 문제도 있다.
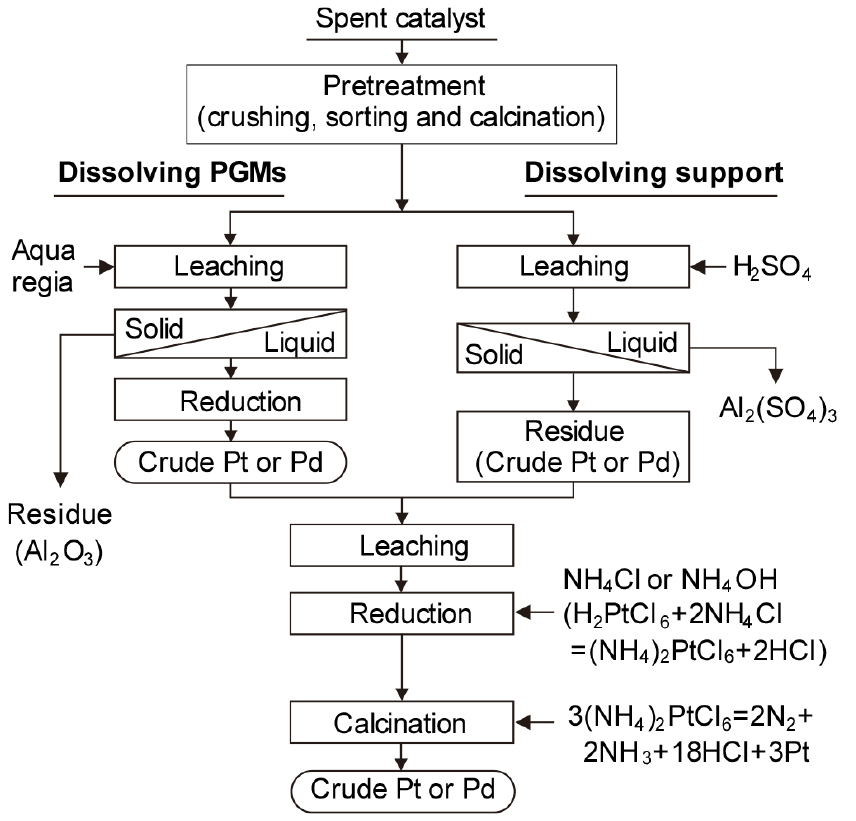
한편, 상기한 문제점은 있으나 폐촉매의 수급량이 작을 때는 건식법보다 습식법을 적용하고 있다. 다만 습식법의 경우 고가인 백금족 금속의 회수율 향상과 분리·정제 기술의 개발이 관건이다. 귀금속 함유 폐촉매를 습식으로 처리하는 방법은 Fig. 11에 나타낸 것처럼 귀금속 용해법과 담체 용해법으로 구분할 수 있다27).
(1) 백금족 금속 용해법
다공성 담체에 분산되어 있는 백금족 금속의 효과적인 침출을 위해 담체를 미분쇄하여 다음과 같은 방법으로 침출한다.
① 왕수나 HCl/산화제(NaClO3, NaOCl, Cl2 가스)에 의한 백금족의 직접 침출
② Autoclave를 이용하는 NaCN 또는 I2에 의한 직접 침출
다만 침출 후 잔사로 남는 다공성 알루미나 잔사 중에 백금족 금속의 침출액이 흡수되어 손실되는 문제점이 있다. 이러한 손실량은 침출액의 약 1~2 %로 비교적 적은 양이지만 백금족 금속이 고가이므로 상당한 손실이 된다27).
(2) 담체 용해법
백금족 금속 용해법과 마찬가지로 담체를 미분쇄하고 소성한다. 석유화학 폐촉매의 경우 알루미나 담체는 H2SO4에 용해되지만, 담지된 백금족 금속들은 용해되지 않는 특성을 이용하여 폐촉매의 알루미나 담체를 H2SO4로 용해하여 불용성인 백금족을 농축, 회수한다. 이 방법은 백금족 금속의 회수율 향상과 담체의 활용도 측면에서 보다 경제적인 공정이 될 수 있는 것으로 알려져 있다.
4.4.3. 폐촉매의 건식처리
자동차용 폐촉매 등은 품위가 일정하고 다량의 스크랩을 지속적으로 확보할 수 있으므로 건식법을 이용하여 처리하고 있다. 다만 금속별 분리와 정제는 습식법을 이용하고 있다. 건식처리법에는 Fe를 포집 금속으로 사용하는 Multimetco사의 플라즈마 아크 용융법과 Cu를 포집 금속으로 사용하는 일본 PGM사의 Roes법이 있다.
(1) 플라즈마 아크 용융법
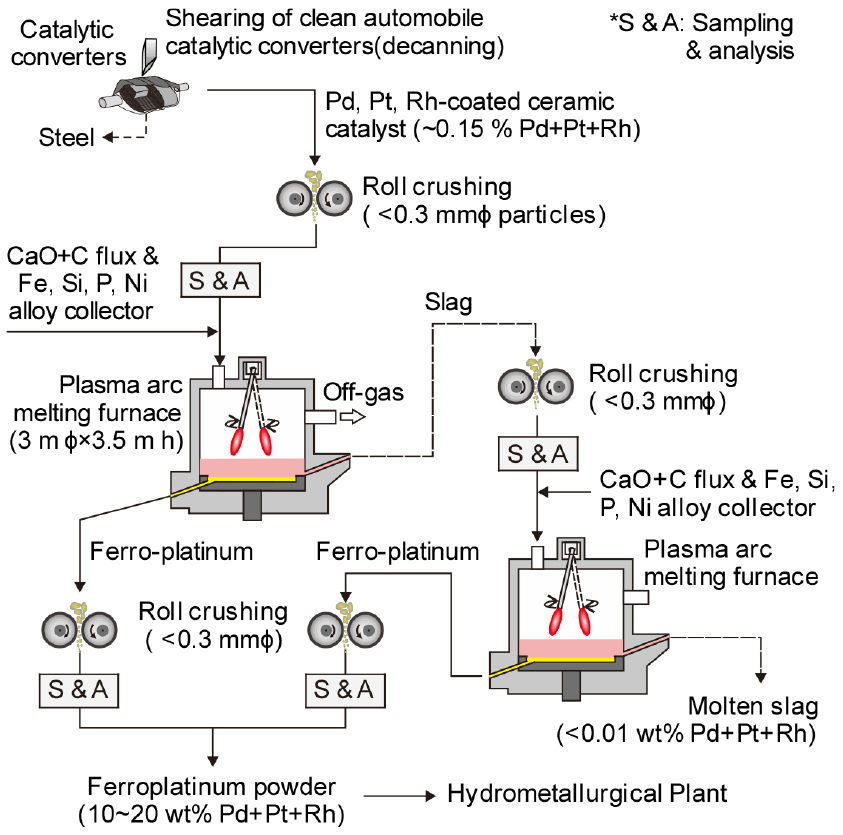
Fig. 12에는 자동차용 배가스 폐촉매를 플라즈마 아크로 용융하여 백금족 금속을 회수하는 건식처리 공정33)을 재구성하여 모식적으로 나타내었다. 미국의 Multimetco사와 우리나라의 희성피엠텍에서 이 방법을 적용하고 있다. 우선 철제 외피를 절단하여 분리한 폐촉매를 롤 크러셔 등으로 0.3 mm 이하로 파쇄하고, 시료를 채취하여 분석한다. 파쇄한 폐촉매를 CaO+C 플럭스 및 철계 포집 금속과 함께 플라즈마 아크 1차 용융로에 장입하며, 백금족 금속을 포집 금속인 Fe 중으로 분리한다. 노 내를 균일하게 가열하기 위해 텅스텐제 음극을 10~15 rpm으로 회전시키면서 1,500~1,600 °C에서 조업하는 것으로 알려져 있다. 주기적으로 출탕한 포집 금속은 냉각한 후에 다시 파쇄하여 습식 회수 공정으로 보낸다. 이때 생성되는 슬래그는 연속적으로 출탕하여 냉각, 파쇄 공정을 거처서 플라즈마 아크 2차 용융로에 장입하여 1차 용융로와 동일하게 작업한다. 습식처리에 의한 정련 공정에서 Pt, Rh, Pd으로 분리, 정제한다34).
(2) Rose법
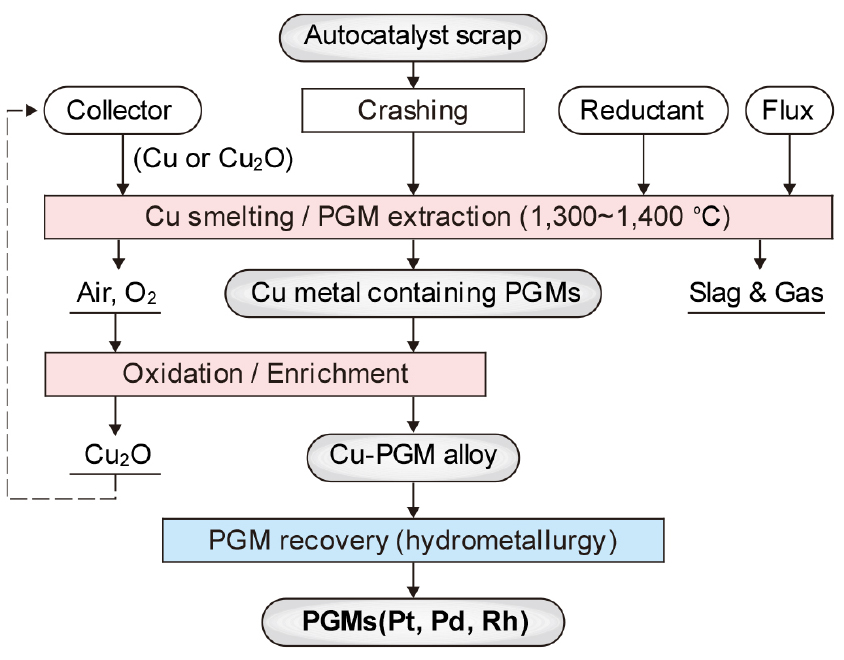
Rose법은 일본 PGM사가 개발한 방법으로, 플라즈마 아크 용융법과 달리 구리를 포집 금속으로 사용하여 자동차용 배가스 촉매로부터 백금족 금속을 리사이클링하는 방법이며, Fig. 13에 공정도를 나타내었다35). 촉매의 세라믹 담채인 코디라이트(Cordierite, 2MgO·2Al2O3·5SiO2) 등 비교적 융점이 높은(1,300 °C~) 산화물 중에 분산되어 있는 백금족 금속을 높은 효율로 리사이클링하는 방법이다. 기본적으로는 제련공정을 활용하는 방법과 마찬가지로 구리합금을 포집 금속으로 사용한다. 다만 산화동(Cu2O)도 포집 금속으로 이용하여 슬래그의 융점을 낮추고, 포집 합금을 직접 산화시켜 백금족 금속을 농축하는 점이 기존의 동제련을 활용하는 방법과 다른 점이다. 특히 이 방법은 동제련 등에서 부산물로 회수하는 방법에 비하여 단기간에 귀금속을 회수할 수 있는 특징이 있다15).
5. 종 합
백금족 금속은 대표적인 희소금속으로 극히 한정된 국가의 특정 지역에 편재되어 향후 공급 리스크가 발생할 것으로 예상되고 있다. 따라서 백금족 금속의 안정적인 공급을 위해서는 리사이클링이 필수적이다. 백금족 금속의 연간 생산량은 500 톤 미만이며, Pd과 Pt을 제외한 나머지 백금족 금속의 생산량은 수십 톤 미만이다. 백금족 금속의 최대 용도는 촉매이므로, 폐촉매의 리사이클링이 중요하다. 백금족 금속은 건식제련에 의한 농축과 습식제련에 의한 분리 및 회수에 의해 생산되고 있으며, 폐촉매 등으로부터 백금족의 회수도 건식에 의한 포집 금속으로의 농축과 습식에 의한 분리 및 정제 방법을 적용하고 있다. 그러나 폐촉매 등의 2차 자원 수급량에 따라 습식에 의한 처리도 이루어지고 있다. 폐촉매를 비롯한 2차 자원 중 백금족 금속의 함유량이 낮고, 수용액으로의 용해가 쉽지 않으므로, 백금족 금속을 쉽게 용해할 수 있는 새로운 농축 방법에 대해서도 많은 연구가 이루어지고 있다. 향후 2차 자원으로부터 백금족 금속 회수를 위한 새로운 농축 기술의 개발이 필요할 것이다.