1. 서 론
2. 실험재료 및 방법
3. 결과 및 고찰
3.1. PAM에 의한 규소(IV)의 선택적 흡착
3.2. 탄산나트륨에 의한 니켈(II) 침전
3.3. 옥살산나트륨에 의한 니켈(II) 침전
4. 결 론
1. 서 론
리튬이온배터리는 현재 가장 널리 사용되는 이차전지로 전기자동차 시장이 확대됨에 따라 사용량이 급격히 증가하고 있다1). 그러나 리튬이온 배터리는 장기간의 충방전 과정에서 전극표면의 과성장과 활물질에서 층구조의 차단 및 리튬이온의 지속적인 손실로 인해 리튬이온배터리의 평균 수명은 2-4년에 불과하다2,3). 따라서 세계적으로 폐리튬이온배터리의 발생량은 2030년까지 1,100만톤 이상이 될것으로 예상된다4). 또한 폐리튬이온배터리에 포함된 니켈은 배터리 제조뿐만 아니라 일부 신소재 및 합금제조에 사용되므로 폐리튬이온배터리에서 니켈을 회수하는 것은 소재공급 측면에서 중요하다5,6).
일반적으로 폐리튬이온배터리에서 유가금속을 회수하기 위해 건식제련법과 습식제련법이 함께 사용된다. 먼저 건식제련은 고온에서 용융환원처리를 통해 일부 금속 산화물을 합금으로 환원시켜 회수하고, 여기서 얻어진 합금은 습식제련을 통해 분리된다7,8). 폐리튬이온배터리를 용융환원시켜 얻은 합금상에는 코발트, 니켈, 구리 및 비교적 미량의 철, 망간, 규소가 함유되어 있다9). 이를 30 g/L 광액농도에서 2 M HCl과 5% H2O2 혼합용액에서 60°C로 150분간 침출하면 완전히 용해시킬 수 있다10). 침출용액에서 용매추출을 통해 철(III), 구리(II) 및 코발트(II)를 분리하고, 침전으로 망간(II)을 분리하면 여과액에는 니켈(II)과 미량의 규소(IV)가 남는다. 염산침출액과 여과액에서 금속이온의 농도를 Table 1에 정리했다. 이때 여과액의 pH는 3이며 규소(IV)가 함유되어 있으므로 고순도 니켈 화합물을 회수하기 위해서는 반드시 정제과정이 필요하다. 니켈(II)과 규소(IV)를 분리할 목적으로 용매추출을 적용하면 규소(IV)와 니켈(II)이 동시에 추출되므로 분리가 어렵다. 따라서 규소(IV)를 선택적으로 제거하거나 또는 니켈(II)을 선택적으로 침전시켜 고순도 니켈화합물을 회수해야 한다. 문헌에 따르면 규소(IV)는 polyacrylamide(PAM)에 흡착되고, 니켈(II)은 탄산염 및 옥살산염 화합물로 침전된다11,12,13,14).
Table 1.
The chemical composition of HCl leaching solution of reduction smelted metallic alloys from spent LIBs and final raffinate after separation of Co(II), Cu(II), Fe(III) and Mn(II) (Leaching Conditions ; 2 M HCl, 60°C, 300 rpm, 90 min, pulp density : 30 g/L, H2O2 : 5%(v/v))
| Metals | Co(II), mg/L | Ni(II) , mg/L | Cu(II) , mg/L | Fe(III) , mg/L | Mn(II) , mg/L | Si(IV) , mg/L |
| Leaching solution | 3870.0 | 18597.0 | 6699.0 | 474.0 | 149.4 | 66.7 |
| Final raffinate | 0 | 18597.0 | 0 | 0 | 0 | 37.4 |
따라서 본 연구에서는 염산용액에서 PAM을 사용해 규소(IV)를 선택적으로 제거하기 위해 용액의 초기 pH와 PAM 농도를 변화시켜 규소(IV)의 제거율을 조사했다. 또한 탄산나트륨과 옥살산나트륨을 침전제로 첨가해 니켈(II)과 규소(IV)의 혼합용액에서 초기 pH 및 침전제 농도가 침전에 미치는 영향을 조사했다.
2. 실험재료 및 방법
용융환원된 폐리튬이온배터리의 염산침출액에서 용매추출 및 침전에 의해 철(III), 구리(II), 코발트(II) 및 망간(II)을 분리한 여과액의 니켈(II)과 규소(IV) 농도는 각각 18597.0 mg/L와 37.4 mg/L였다. 본 연구에서는 실험을 위해 실제 여과액의 조성을 모사한 합성용액을 제조했다. 합성용액은 시약급 염화니켈(NiCl2·6H2O, Yakuri pure chemicals co., Ltd., Japan, 99%)을 2차 증류수에 용해시킨 다음 규산나트륨용액(Na2SiO4, Daejung chemicals & metals Co. Ltd., Korea)을 첨가해 제조했으며, 용액의 pH는 염산(Daejung chemicals & metals Co. Ltd., Korea., 35%)으로 조절했다. 합성용액에서 규소(IV)의 선택적인 제거를 위해 Polyacrylamide granular(PAM, Acros Organics Co., 99.9%)를 사용했고, 니켈(II)의 선택적인 침전을 위한 침전제로는 탄산나트륨(Na2CO3, Yakuri pure chemicals Co., Ltd., Japan, 99.7%)과 옥살산나트륨(Na2C2O4, Oriental chemical industries., Korea, 99%)을 사용했다.
규소(IV)의 흡착실험은 디지털 가열식 자력교반기(WiseStir MSH-20D, Daihan Scientific Co., Korea)를 사용해 반응온도(60°C)와 교반속도(300 rpm)를 조절했고 합성용액에 PAM을 첨가한 다음 3시간 동안 교반했다. 니켈(II) 침전실험은 상온에서 20 mL 합성용액에 각각 탄산나트륨과 옥살산나트륨을 첨가해 1시간동안 300 rpm으로 교반했다. 두 실험 모두 여과지(ADVANTEC NO. 2, 110 mm, Toyo roshi kaisha, Ltd.)를 사용해 침전물과 여과액을 분리했으며, 침전물을 80°C의 오븐에서 24시간 건조시킨 다음 XRD(EMPYREAN, PANalytical, Germany)와 FE-SEM(S-4800, Hitachi, Japan)으로 분석했다. 그리고 여과액의 금속농도를 ICP-OES(Arcos, Spectro, Germany)로 측정했으며, 규소(IV)의 제거율과 니켈(II)의 침전율을 다음 식으로 구했다.
여기서 m0 와 mf 는 흡착 및 침전 전후 용액에서 금속이온의 질량을 나타낸다.
3. 결과 및 고찰
3.1. PAM에 의한 규소(IV)의 선택적 흡착
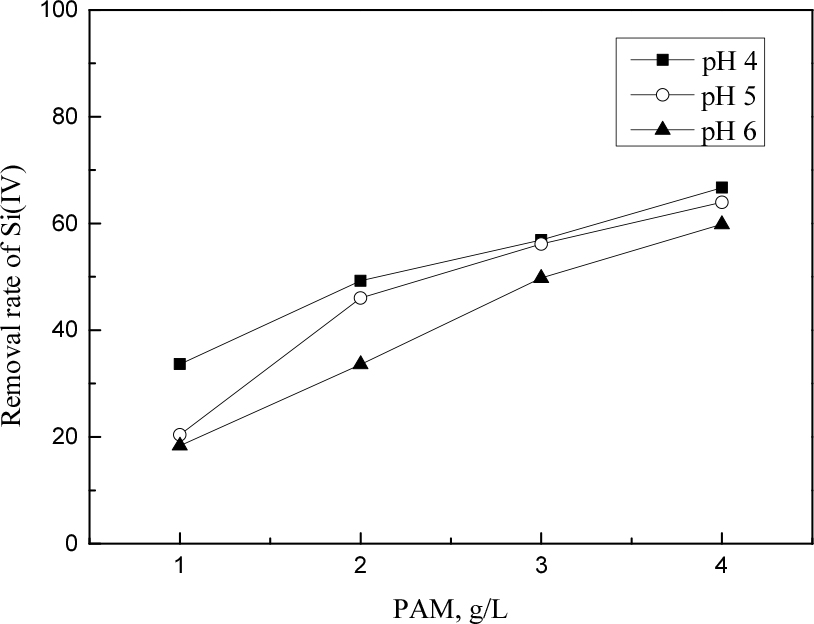
아크릴아미드 단량체는 PAM 합성에 사용되며 수분 흡수성이 뛰어나고 물에 용해되면 겔을 형성한다. PAM은 음용수에서 염화제2철 및 염화알루미늄과 같은 3가 금속염을 흡착해 제거하는 용도로 사용되며, 문헌에 따르면 규소(IV)를 흡착해 선택적으로 제거할 수 있는 것으로 알려져 있다11,15,16). 아크릴아미드에 의한 규소(IV)의 흡착은 폴리아미드 그룹과 규산염 표면의 수산기(-OH) 사이에 다중 수소 결합을 형성함으로써 발생한다17). 따라서 본 연구에서는 염산합성용액에서 규소(IV)를 제거하기 위해 PAM을 사용했으며 용액의 pH는 니켈(II)이 석출되지 않도록 각각 4, 5, 6으로 조절했다. 또한 PAM의 농도를 1에서 4 g/L까지 변화시켰으며, 이 때 반응온도는 60°C, 반응시간은 3시간 그리고 교반속도를 300 rpm으로 고정했고11), 실험결과를 Fig. 1에 나타냈다.
합성용액에서 pH가 4에서 6으로 증가함에 따라 모든 PAM 농도에서 규소(IV)의 제거율이 향상되었다. 본 조건에서 니켈(II)은 PAM에 전혀 흡착되지 않았으므로 그림에 나타내지 않았다. PAM에 의한 규소(IV)의 흡착 및 응집은 규소(IV) 표면의 수산기와의 반응을 통해 발생하므로 비교적 수산화이온 농도가 높은 pH 6조건에서 규소(IV)의 제거율이 높은 것으로 판단된다.
다음으로 pH가 6인 조건에서 PAM 농도가 1에서 4 g/L로 증가함에 따라 규소(IV)의 제거율은 18.3에서 59.8%로 증가했다. 따라서 PAM의 농도를 높이면, 규소(IV)의 제거율을 증가시킬 수 있다. 그러나 PAM은 수용액에 첨가시 물 또는 규소(IV)를 흡착해 고분자를 형성함으로써 용액의 점도를 증가시킨다. 따라서 4 g/L보다 많은 양을 첨가할 경우 용액의 점도가 급격히 상승해 규소(IV)가 흡착된 PAM을 용액으로부터 분리하기 어려웠으며, 또한 높은 점도는 후속공정에서 니켈 화합물 합성에 악영향을 미칠 수 있다. 따라서 PAM은 고순도 니켈용액을 회수하기 위한 규소(IV)의 흡착제로 적합하지 않다고 생각된다.
3.2. 탄산나트륨에 의한 니켈(II) 침전
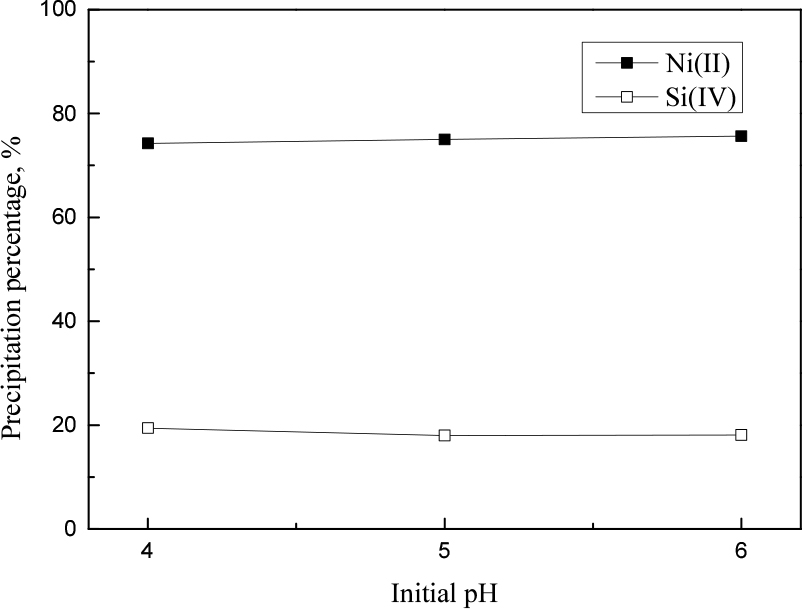
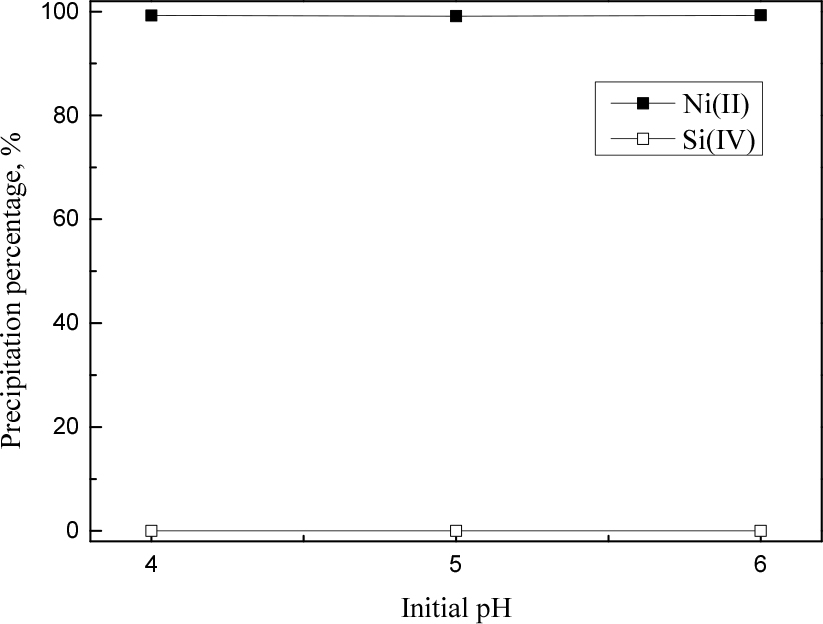
규소(IV)와 니켈(II)이 혼합된 용액에서 니켈(II)을 선택적으로 침전시켜 고순도 니켈화합물을 제조할 수 있는 조건을 조사하기 위해 침전제로 탄산나트륨과 옥살산나트륨을 사용해 침전실험을 수행했다. 탄산나트륨에 의한 니켈(II) 침전시 pH의 영향을 알아보기 위해 pH를 4, 5, 6으로 변화시켰으며, 탄산나트륨은 니켈(II)과 1:1의 몰비로 첨가했다. 실험결과를 Fig. 2에 나타냈으며 탄산나트륨에 의한 니켈의 침전반응을 아래 식에 나타냈다.
실험결과 모든 pH 조건에서 규소(IV)보다 니켈(II)이 선택적으로 침전되었다. pH는 니켈(II)의 침전에 거의 영향을 미치지 않았으며, 니켈(II)과 규소(IV)의 침전율은 평균 75%와 18%였다. 탄산나트륨 첨가시 용액의 pH가 증가하여 NiCO3와 Ni(OH)2가 동시에 침전된다. 이 때 침전물 Ni2CO3(OH)3의 수산기와 Si(OH)4의 수산기 사이에서 상호작용을 통해 수소결합을 형성함으로써 규소(IV)가 공침된다18). 따라서 탄산나트륨으로는 니켈(II)의 선택적인 침전이 어렵다.
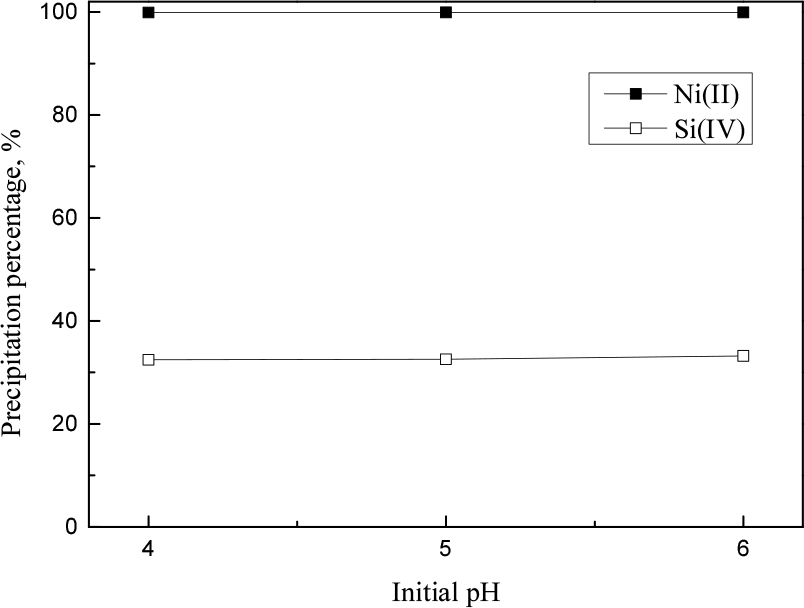
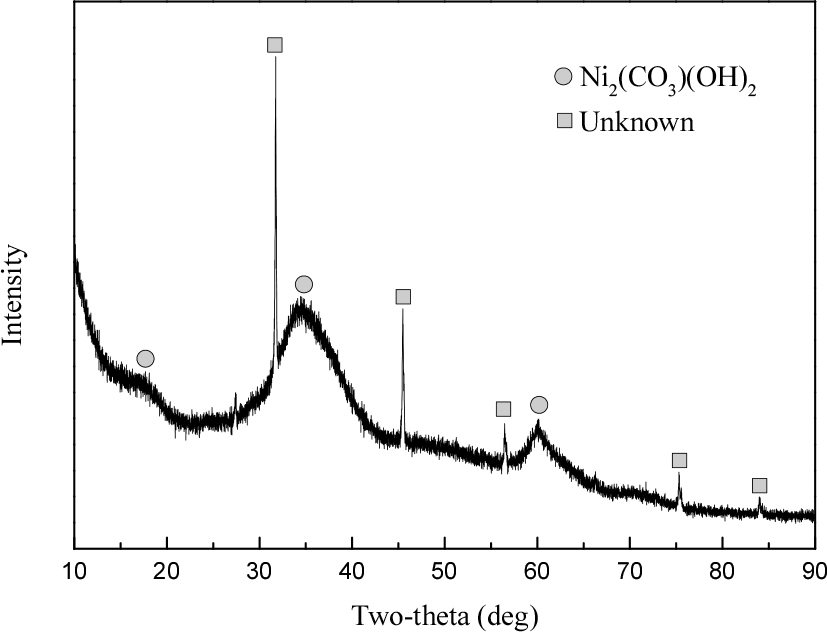
다음으로 니켈(II)의 침전율을 증가시키기 위해 탄산나트륨을 1.5배 몰비로 첨가한 결과를 Fig. 3에 나타냈다. 니켈(II)과 탄산나트륨의 몰비가 1.5일 때 니켈(II)과 규소(II)의 침전율은 각각 평균 99%와 32%로 증가했다. 이는 식 (2)와 비교했을 때 니켈(II)을 완전히 침전시키기 위해서는 과량의 탄산나트륨이 필요하다는 것을 의미한다. 따라서 실험을 통해 얻은 탄산나트륨과 니켈(II)의 최적 몰비는 1.5였으며, 이 때 ICP-OES로 측정한 여액에서 규소(II)의 농도는 25.4 mg/L였다. 이는 11.9 mg/L의 규소(IV)가 공침 되었음을 의미하며, 이로부터 계산된 침전물에서 니켈(II)화합물의 순도는 99.88%였다. 그리고 여기서 얻은 침전물은 건조 후에 FE-SEM과 XRD로 분석해 결과를 각각 Figs. 4와 5에 나타냈다. 탄산니켈분말은 형광초록색을 띠었으며, 입자크기는 균질했다. XRD 분석결과 비정질 Ni2CO3(OH)2 상과 미상의 상이 측정되었으며, 미상의 상은 규소 화합물로 추정된다. 또한 결정질의 탄산니켈분말을 얻기 위해서는 반응온도를 높여줄 필요가 있을 것으로 판단된다.
3.3. 옥살산나트륨에 의한 니켈(II) 침전
탄산나트륨에 의한 니켈(II)의 침전시 용액에 함유된 미량의 규소(IV)가 공침되며, 이는 니켈 화합물의 순도를 떨어뜨린다. 따라서 침전제로 탄산나트륨 대신 옥살산나트륨을 사용해 침전실험을 수행했다. 옥살산나트륨에 의한 침전실험 역시 탄산나트륨 침전실험과 동일하게 수행되었으며, 옥살산나트륨과 니켈(II)의 몰비를 1:1로 고정해 pH에 따른 침전율 변화를 Fig. 6에 나타냈다. 또한 옥살산 나트륨에 의한 니켈(II)의 침전반응을 식 (3)에 나타냈다.
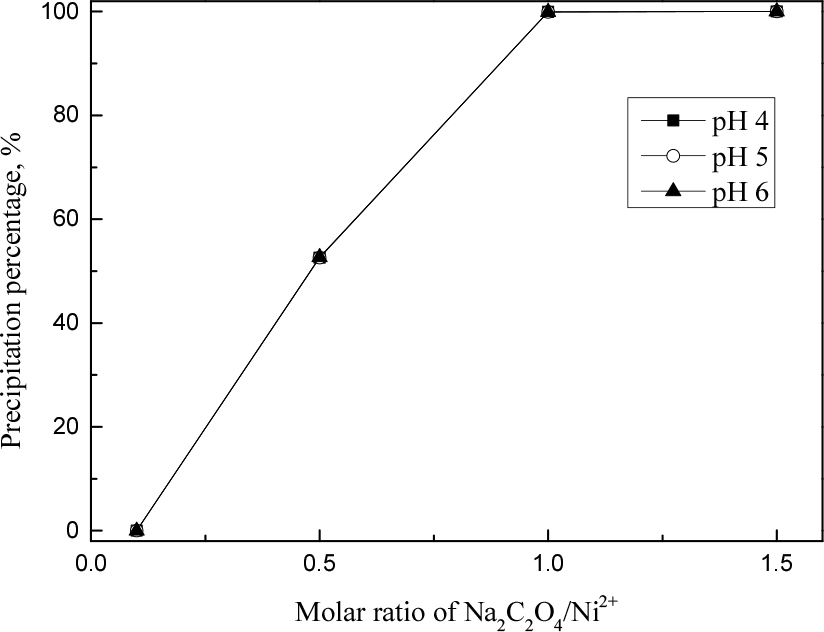
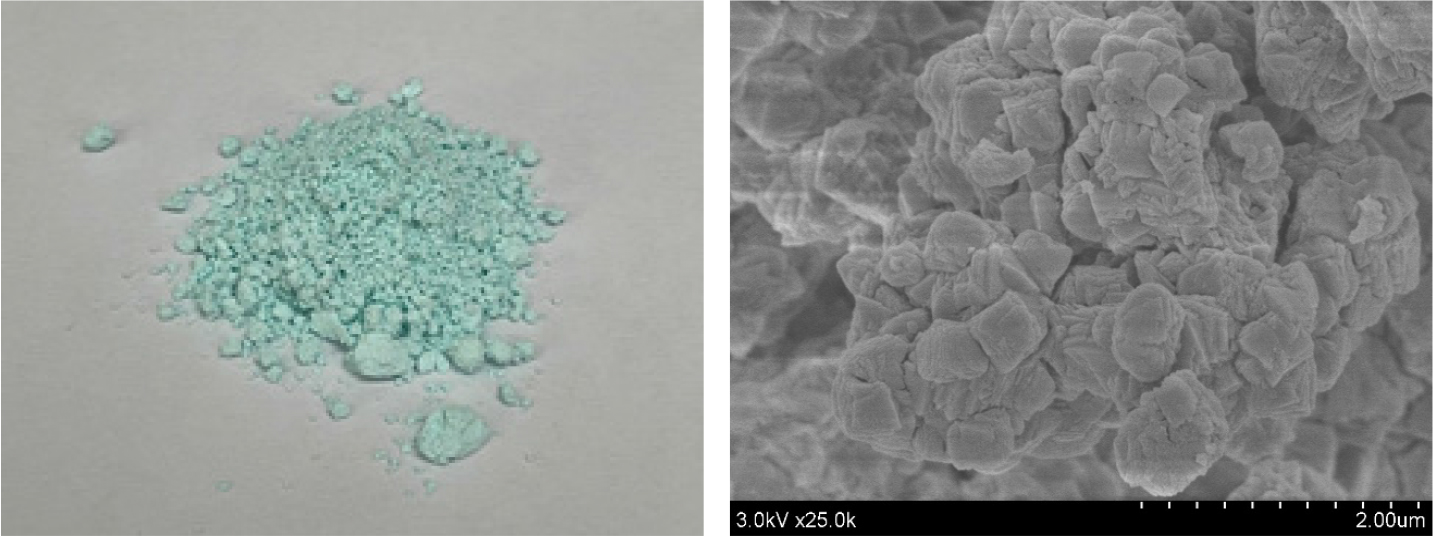
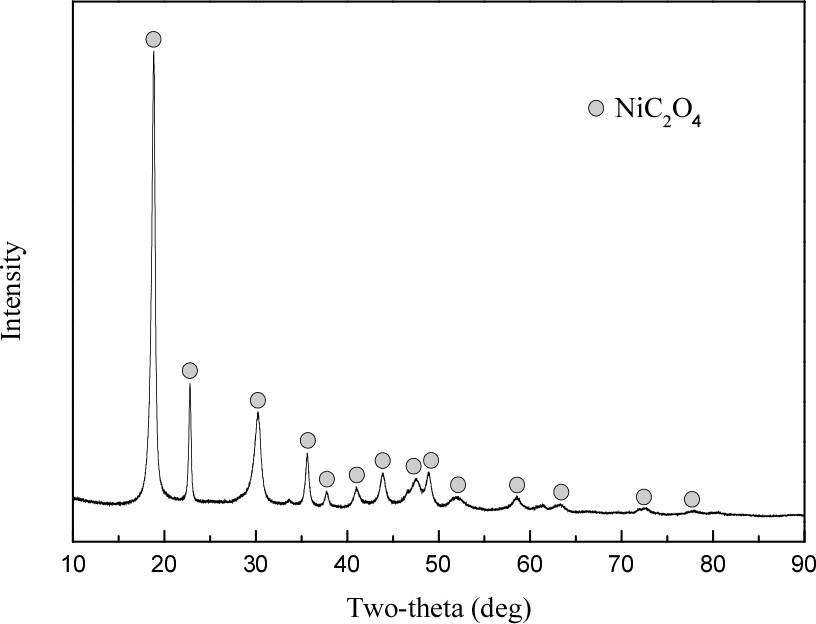
Fig. 6에서 옥살산나트륨에 의한 니켈(II) 침전은 pH의 영향을 받지 않았으며, 옥살산나트륨과 니켈(II)의 몰비 1:1 조건에서도 니켈(II)은 완전히 침전되었다. 이는 옥살레이트가 bidentate ligand이기 때문이다. 모든 조건에서 니켈(II)이 선택적으로 침전되었고 규소(IV)는 전혀 침전되지 않았다. 옥살산나트륨은 탄산나트륨에 비해 용액의 pH변화에 거의 영향을 미치지 않아 Ni2C2O4의 형태로 침전된다. 따라서 니켈화합물에 수산기가 없으므로 규소(II)가 공침되지 않는다고 생각된다. 따라서 최적의 옥살산나트륨과 니켈(II)의 몰비를 조사하기 위해 몰비를 0.1에서 1.5까지 변화시켜 실험을 수행했고, 결과를 Fig. 7에 나타냈다. 실험결과 모든 pH에서 몰비에 따른 니켈(II)의 침전율이 동일했으며, 니켈(II)을 완전히 침전시키기 위한 최적의 몰비는 1로 식 (3)과 일치했다. 이때 여과액의 ICP-OES 분석결과로부터 계산된 니켈옥살산염의 순도는 99.99% 이상이었다. 탄산나트륨과 비교했을 때 옥살산나트륨을 침전제로 사용시 니켈(II)에 대한 선택성이 매우 우수했으며, 이는 초고순도 니켈원료의 제조에 적합한 침전제로 생각된다. 여기서 얻어진 침전물에 대해 FE-SEM과 XRD 분석을 실시했으며, 결과를 Figs. 8과 9에 나타냈다. 니켈옥살산염은 연한 청록색을 띠었으며, 탄산니켈분말과 비교해 입자크기가 더 크다. XRD 분석결과 단일상의 니켈옥살산염(NiC2O4)이 관찰되었으며, 옥살산나트륨의 경우 상온에서 니켈과 결정질을 형성할 수 있는 것으로 판단된다.
4. 결 론
고온에서 폐리튬이온배터리를 용융환원처리하면 코발트, 니켈, 구리, 철, 망간 및 규소가 함유된 합금상이 얻어진다. 이러한 합금을 염산으로 침출한 용액에서 용매추출로 코발트(II), 구리(II), 철(III)을 분리한 다음 침전으로 망간(II)을 분리하면 여과액에는 니켈(II)과 미량의 규소(IV)가 남는다. 여과액으로부터 고순도 니켈화합물을 회수하기 위해서는 반드시 규소(IV)를 제거해야 하며, PAM을 통해 규소(IV)의 선택적인 흡착이 가능하다. 그러나 PAM은 용액의 점도를 증가시켜 규소(IV)가 흡착된 PAM과 용액의 분리가 어렵다. 니켈(II)의 침전제로 탄산나트륨을 니켈(II)과의 몰비 1.5로 첨가시 용액의 pH가 4-6사이의 조건에서 니켈(II)은 완전히 침전되었으나 일부 규소(IV)가 공침되어 침전물의 순도를 감소시켰다. 이에 반해 옥살산나트륨을 첨가한 경우 옥살산나트륨과 니켈(II)의 몰비가 1일 때, 니켈(II)은 모두 침전된 반면 규소(IV)는 전혀 침전되지 않아 결정상의 순도 99.99%이상을 지닌 니켈옥살산염을 회수하였다.