1. 서 론
2. 실험 재료 및 방법
3. 실험 결과 및 고찰
3.1. Cyanex 301의 추출 특성
3.2. Cyanex 301에 의한 Co, Ni의 추출(extraction) 거동
3.3. Cyanex 301에 추출된 유기상에서 Co, Ni, Mn, Mg의 세정(scrubbing) 거동
3.4. 세정 후 유기상에서 Co, Ni의 탈거(stripping) 거동
4. 결 론
1. 서 론
니켈과 코발트는 리튬과 함께 리튬이차전지 핵심 소재로 양극재 제조에 사용되고 있으며1), 현재는 대부분 광석으로부터 니켈 및 코발트를 생산하여 공급하고 있다. 향후 전기차 시장이 급격히 확대됨에 따라 수요 대비 공급이 부족하리라 예상되고 있어 폐리튬배터리 및 페로니켈 제조 시 발생하는 공정 부산물 등에 함유되어 있는 니켈 및 코발트 회수에 대한 관심이 매우 높아지고 있다2,3,4,5,6,7,8). 이러한 폐배터리나 공정 부산물에는 철, 구리, 망간 등 불순물과 코발트와 니켈이 함유되어 있어 고순도로 코발트와 니켈을 분리․회수하여 리튬이차전지 전구체용으로 재사용하고자 하는 노력이 지속되고 있다5,6,7). 기존에는 코발트 및 니켈을 각각 단일염으로 회수하기 위한 연구가 주로 진행되어 왔으나 최근에는 이차전지용 양극활물질로 활용하기 위해서 2~3성분계 혼합염 형태로 회수하여 활용하고자 하는 시도가 관심을 끌고 있다9).
일반적으로 철, 망간, 마그네슘 등이 불순물로 함유되어 있는 침출용액에서 코발트와 니켈을 분리․회수하기 위해서는 철이나 망간을 사전에 제거한 후에 Cyanex 272나 PC88A, Versatic acid 10 등을 사용하여 용매추출 기술로 분리하고 있다10,11). 이 경우 다단공정으로 인하여 공정이 복잡하고 강산 침출액을 중화시켜 적절한 산도 조절을 위하여 알칼리 약품의 다량 투입이 불가피 하며 이로 인한 나트륨, 마그네슘이나 칼슘 등이 불순물로 다량 혼입되는 현상이 발생하고 있다. 이러한 불순물 제거에 대한 공정비용이 증가 요인으로 작용하고 있어 이에 대한 개선 연구가 필요하다고 할 수 있다12,13,14). 따라서 본 연구에서는 공정부산물이나 폐자원에서 발생되는 침출액으로부터 망간, 마그네슘 등의 불순물과의 분리성이 우수하고, 침출액의 중화처리 없이 강산성 용액에서 코발트와 니켈을 효과적으로 분리 추출할 수 있는 공정 개발을 하고자 하였다15,16). 추출제로 Cyanex 301(bis-2,4,4-trimethyl pentyldithiophosphinic acid)을 사용하고자 하였으며, Cyanex 301의 경우 황(S)이 함유된 추출제로 Mihaylov 등과 P.E. Tsakiridis 및 S.L. Agatzini 등이 니켈 및 코발트 분리․회수 시에 불순물(Mn, Mg 등)과의 분리 거동에 대해 연구 결과가 보고되어 있다. 그리고 현재 Inco-Goro공정에서 니켈 및 코발트를 회수 시 사용되고 있다고 보고되고 있다17,18,19,20).
본 연구에서는 망간, 마그네슘, 리튬 등이 불순물로 함유되어 있는 용액에서 Cyanex 301을 추출제로 사용하여 각 금속성분의 추출 및 세정 그리고 탈거 거동을 조사하여 코발트 및 니켈 성분을 고순도의 단독염 또는 2성분계 혼합염의 형태로 회수 가능성에 대하여 기초 연구를 실시하였다.
2. 실험 재료 및 방법
본 실험에서 사용한 침출액으로는 공정부산물이나 폐자원에서 침출하여 얻을 수 있는 성분들로 구성된 모의용액을 제조하여 사용하였다. 용액의 구성 성분으로는 코발트, 니켈, 망간, 리튬, 마그네슘이 함유된 황산계 모의 용액을 사용하였으며, 침출액 제조를 위해 0.5 M 황산에 각각의 시약을 용해하였으며 이에 대한 용액 조성을 Table 1에 나타내었다. 실험에 사용된 시약으로는 CoSO4·7H2O (98.0%, DAEJUNG), NiSO4·6H2O(98.5%, DAEJUNG), FeSO4·7H2O(98.5~102.5%, JUNSEI), MnSO4·H2O(99%, SIGMA-ALDRICH), Li2SO4·H2O(99%, JUNSEI), MgSO4· 7H2O(99%, JUNSEI), H2SO4(95%, DAEJUNG)을 사용하였다. 추출제로 사용된 Cyanex 301(75~80%, Cytec Indus. Co.)은 제조사로부터 구입한 후 정제 없이 사용하였으며, 유기상 제조 시 희석제로는 시약급 등유(Exxol D 80, Exxon mobil chem.)를 사용하였다.
추출 실험으로는 특정 농도의 유기상과 수상을 일정한 비율로 혼합하여 교반시키면서 10 M NaOH 수용액 및 10 M H2SO4 용액을 사용하여 평형 pH를 조절하였다. 그 후 20분 간 반응시킨 후, 분액여두(Separatory Funnel)을 사용하여 정치하고 상분리가 된 수상을 여과하여 ICP-AES (PerkinElmer/Optima-4300DV)를 이용하여 금속이온 성분을 분석 하였으며, 세정 및 탈거 실험도 추출 실험과 유사한 방법으로 실시하였다.
그리고 금속이온을 분석한 후 다음 식 (1)에서 식 (4)에 의해 추출율(E : Extraction %), 세정율(Scrubbing %), 탈거율(Stripping %), 분배계수(D : Distribution Coefficient) 그리고 분리계수(β : Separation Factor)값을 계산하였다.
3. 실험 결과 및 고찰
3.1. Cyanex 301의 추출 특성
Cyanex 301에 의한 금속이온과의 추출반응식은 식 (5)와 같다. 여기서 M은 금속 성분, R은 2,4,4-trimethylpentyl group을 나타낸다. Cyanex 301은 pKa값이 2.61로 작은 값을 나타내기 때문에 강산 용액에서도 금속 추출이 가능하다는 장점이 있다21).
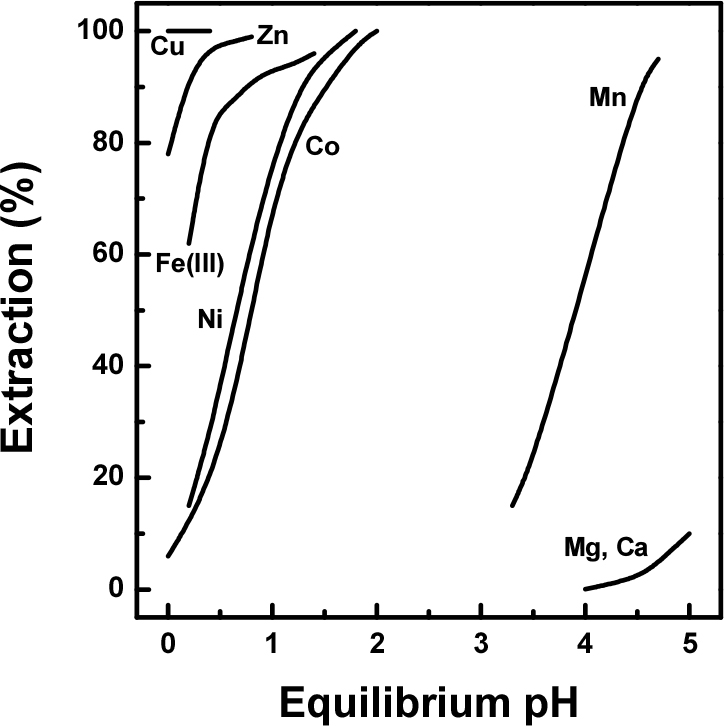
Cyanex 301에 의한 pH 변화에 따른 금속이온에 대한 추출곡선을 Fig. 1에 나타내었다22). 추출제로 사용한 Cyanex 301의 경우 황을 함유하고 있기 때문에 황성분과 강한 반응에 의해 추출이 된다. 따라서 황과의 결합력이 강한 구리, 아연 및 철(III) 성분의 경우는 니켈 및 코발트 보다 낮은 pH에서 쉽게 추출 된다는 것을 알 수 있고, 상대적으로 높은 pH 영역에서 추출되는 마그네슘, 망간, 칼슘 등과는 선택적 추출이 가능하다는 것을 알 수 있다.
참고로 각 금속과 황과의 용해도적 값을 Table 2에 나타내었다. 표에서 알 수 있듯이 Co(II), Ni(II) 및 Fe(II)에 비하여 Cu(II), Zn(II) 및 Fe(III)의 경우는 황과의 안정한 화합물을 형성하여 우선 추출이 진행되는데 반면에 추출된 유기상에서 탈거가 어렵기 때문에 사전에 침전 제거를 하는 것이 바람직하다. 한편 코발트 및 니켈의 경우도 강산성 용액에서도 추출 반응이 쉽게 일어나기 때문에 타 추출제의 경우와 비교 시 pH 조절에 따른 NaOH 등의 비용 절감 효과가 있다. 그리고 반응 속도가 빠르고, 추출반응 후 상 분리 속도도 빠르며, 추출제의 용해에 따른 손실이 매우 작다는 장점이 있다15,16).
Table 2.
Solubility product (KSP) constants at 25°C
| Compound | KSP |
| CuS | 8.0 × 10-37 |
| ZnS | 7.0 × 10-26 |
| CoS | 5.0 × 10-22 |
| NiS | 3.0 × 10-21 |
| FeS | 6.0 × 10-19 |
| Fe2S3 | 1.31 × 10-88 |
| CaS | 8 × 10-6 |
| MnS | 7.0 × 10-16 |
| MgS | No data |
| Li2S | No data |
3.2. Cyanex 301에 의한 Co, Ni의 추출(extraction) 거동
최근 리튬이차전지 수요의 급증에 따라 발생되는 이차전지 제조 중에 발생되는 공정 부산물 혹은 폐리튬이차전지로부터 코발트, 니켈, 리튬 등의 유가 금속을 회수하기 위해 공정 개발이 이루어지고 있고, D2EHPA, PC88A, Versatic acid 10 등의 추출제를 사용하여 불순물과 유가 금속을 분리 회수하는 공정이 개발, 일부 상용화 되어 공정 운영 중에 있다. 기존의 용매추출 공정에서는 철, 구리, 망간 등의 불순물을 우선 제거하고, 코발트, 니켈, 리튬 순으로 회수하는 공정이 일반적인데, 폐리튬이차전지 Black powder를 황산으로 침출한 용액에서 코발트와 니켈을 우선 회수하기 위해 Cyanex 301을 사용한 공정 기초실험을 진행하였다.
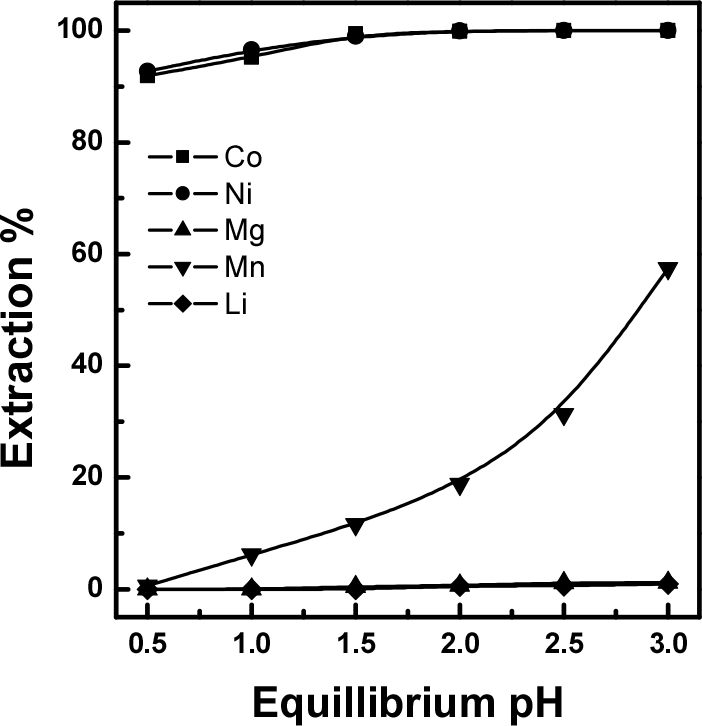
Table 1의 조성을 가지는 용액을 사용하여 추출 상비(A/O) 1.0, 25°C, 10 v/v% Cyanex 301 조건에서 5 성분의 추출 거동을 살펴보았다. 이에 대한 실험 결과를 Fig. 2에 나타내었으며, 코발트와 니켈의 경우 평형 pH 0.5에서 91% 정도의 추출율을 보였고, 평형 pH 2.0 이상 에서는 99.9% 이상 추출되는 경향을 보였다. 마그네슘과 리튬의 경우에는 pH 1.0이하에서는 추출되지 않았으며, pH 3.0 까지 증가시켜도 1.2% 이하의 낮은 추출율을 보였다. 한편, 망간의 경우는 pH 증가에 따라 추출율 증가하는 경향을 보여 평형 pH 0.5에서는 0.6%, pH 3.0에서는 57% 정도 추출되었다. 추출율이 낮은 마그네슘과 리튬을 제외하고 코발트와 망간, 니켈과 망간 사이의 분리계수를 Table 3에 나타내었다. 표에서 알 수 있듯이 평형 pH 2.0에서 분리계수가 가장 높았다. 따라서 코발트, 니켈과 불순물인 망간과의 분리성을 고려할 경우에는 각 금속의 추출율을 고려할 경우 pH 2.0 이하에서 추출하는 것이 바람직할 것으로 사료된다.
Table 3.
Metal extraction characteristics for the system of [Co, Ni, Mg, Mn, Li]-Cyanex 301 for the contact time of 10 minutes at 25°C
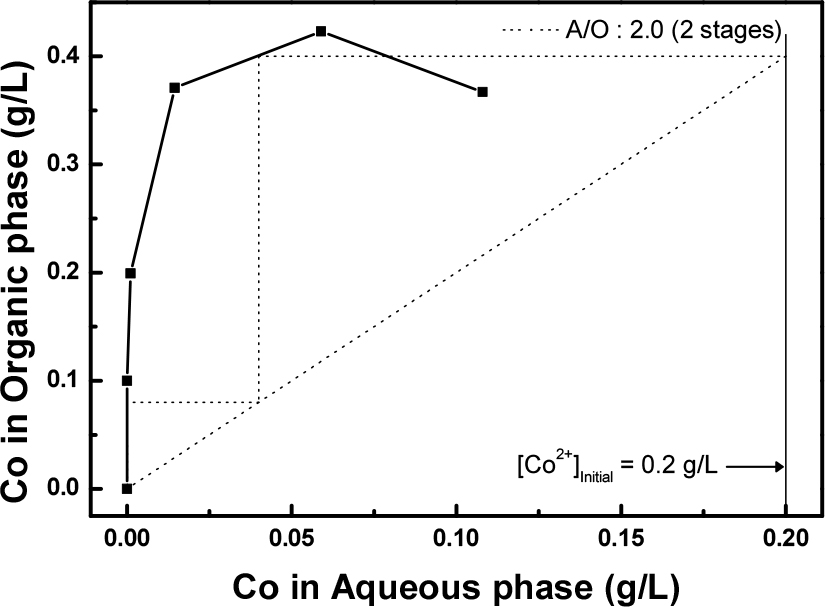
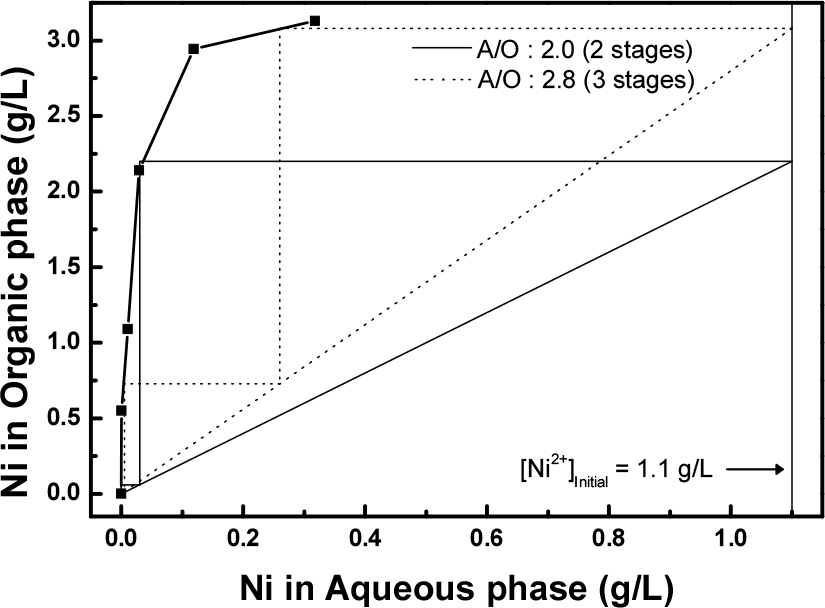
한편, 상비에 따른 코발트와 니켈의 추출 거동을 살펴보기 위해 평형 pH 1.5 에서 추출 상비(A/O)를 0.5~4.0으로 조절하여 실험을 진행하였으며, 이에 대한 결과를 Figs. 3, 4에 나타내었다. Fig. 3는 코발트 그리고 Fig. 4는 니켈의 McCabe-Thiele diagram을 나타낸 그림이다. 그림으로 부터 추출 상비(A/O) 2.0, 2단 추출을 통하여 코발트와 니켈을 99.9% 이상 동시 추출이 가능하다는 것을 알 수 있었고, 니켈의 경우 추출 상비(A/O) 2.8에서 3 g/L 이상으로 농축 가능함을 확인하였다.
3.3. Cyanex 301에 추출된 유기상에서 Co, Ni, Mn, Mg의 세정(scrubbing) 거동
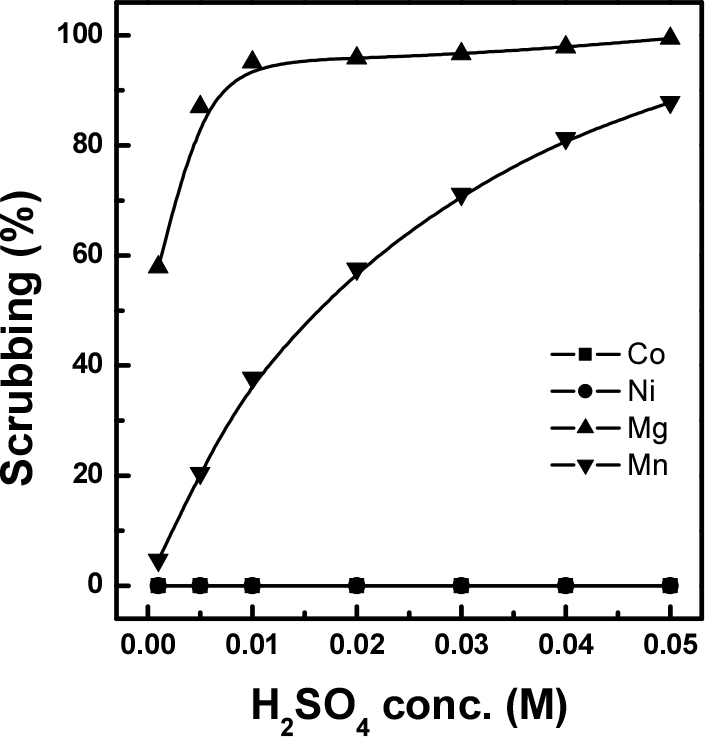
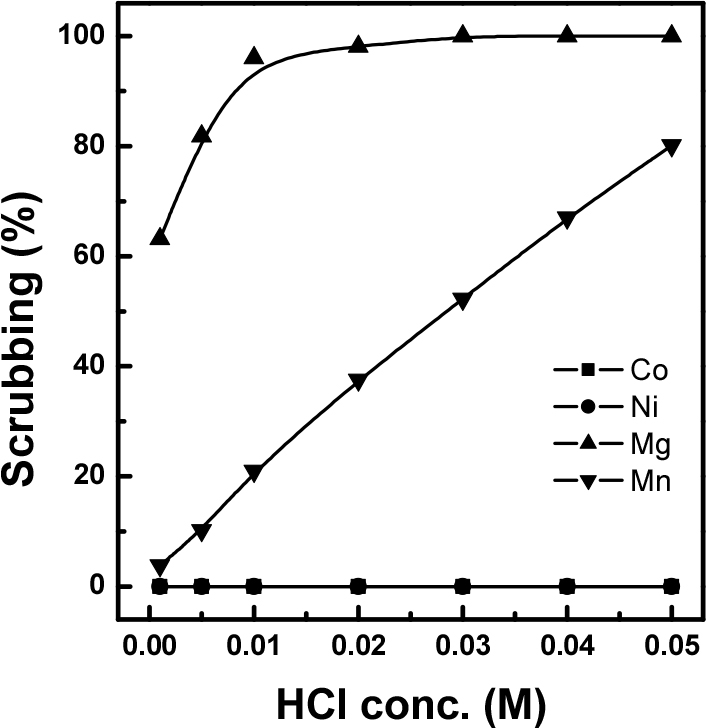
추출 단계에서 코발트, 니켈과 함께 공추출 된 망간, 마그네슘을 제거하기 위해 황산, 염산을 사용하여 세정 실험을 진행하였다. 평형 pH 1.5, A/O 1.0 조건에서 추출하였으며, 추출 후 유기상 중 금속이온 농도는 199.86 mg/L Co, 1,089.22 mg/L Ni, 22 mg/L Mg, 28.93 mg/L Mn이며 Li은 추출되지 않았다. 세정 상비(O/A) 1.0, 25°C에서 0.001~0.05 M의 황산, 염산을 사용하여 세정 실험을 실시하여 그 결과를 Fig. 5에 나타내었다. 그림에서 코발트와 니켈의 경우는 해당 실험 조건에서는 세정되지 않고 그대로 유기상 중에 남아있었다. 상대적으로 적은 양이 추출되었던 마그네슘의 경우 0.01 M 이상의 황산용액에서 약 95% 내외의 세정율을 보였다. 망간의 경우는 황산의 농도가 증가함에 따라 세정율이 급격히 증가하는 경향을 보였고 0.05 M황산 용액에서 약 88 %의 세정율을 보였다. 한편, 염산용액을 세정액으로 사용한 실험 결과를 Fig. 6에 나타내었는데, 황산을 사용한 세정 실험과 유사하게 0.001 M 염산용액을 사용할 경우에는 마그네슘이 약 63% 세정되었고, 염산의 농도가 증가함에 따라 세정율이 증가하여 0.05 M 염산을 세정제로 사용하였을 때에는 100% 세정되었다. 한편, 망간은 0.001 M 염산에서는 3.8% 정도의 낮은 세정율을 보이다가 염산의 농도가 증가함에 따라 세정율이 꾸준히 증가하여 0.05 M 염산을 사용한 경우 약 80% 세정되었다. 따라서 5성분 용액에서 Cyanex 301에 의해 추출되지 않는 리튬을 제외하고 마그네슘, 망간과 같은 불순물들은 황산 및 염산을 사용하여 쉽게 세정이 가능하다는 것을 알 수 있었다.
3.4. 세정 후 유기상에서 Co, Ni의 탈거(stripping) 거동
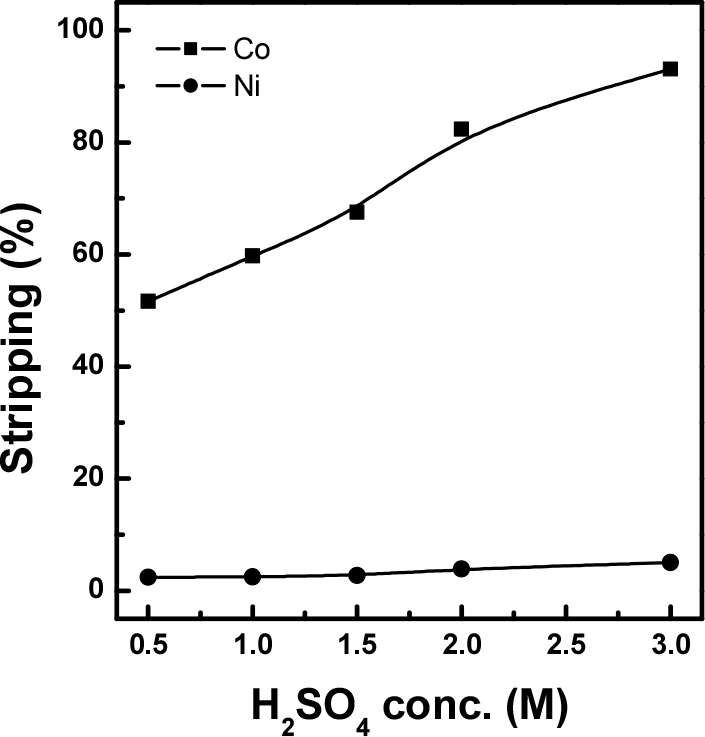
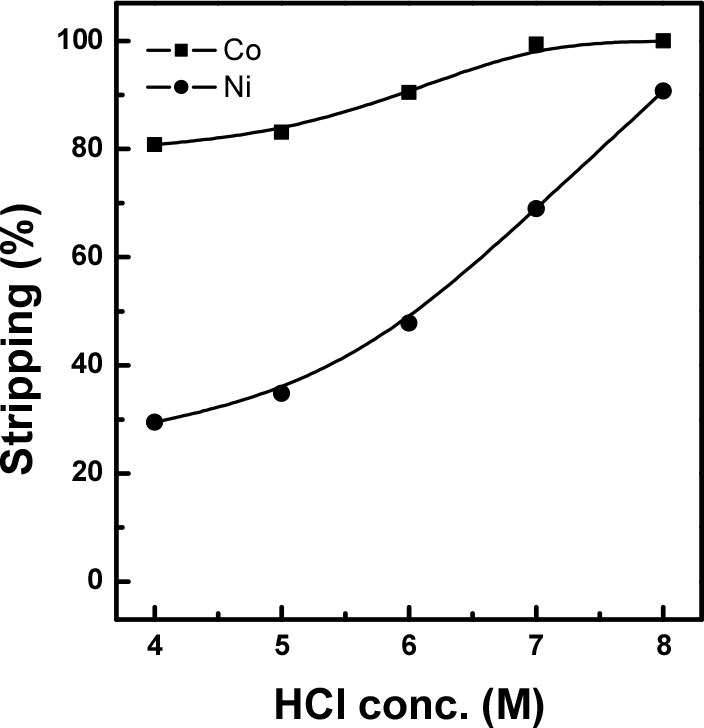
Cyanex 301에 의해 추출한 후 세정공정을 거쳐 망간 및 마그네슘을 제거한 유기상에서 코발트와 니켈을 회수하기 위한 탈거 실험을 진행하였다. 유기상으로는 평형 pH 1.5, 상비(A/O) 1.0 에서 추출한 유기상을 각각 0.05 M 황산으로 세정한 용액을 사용하였다. 추출 후 유기상에는 199.86 mg/L Co, 1,094.72 mg/L Ni, 3.5~5.7 mg/L Mn이 함유되어 있었다. 이 유기상을 탈거 상비(O/A) 1.0, 25°C 조건에서 황산의 경우 0.5~3.0 M, 염산의 경우는 4.0~8.0 M을 사용하여 탈거 실험을 실시하였다. 황산을 사용한 탈거 실험 결과를 Fig. 7에 나타내었으며, 황산 농도가 증가함에 따라 코발트의 탈거율은 크게 증가하여 3.0 M H2SO4을 사용한 경우 93%의 탈거율을 보인 반면, 니켈은 0.5M 황산 사용 시 2.4%의 낮은 탈거율을 보였고 황산 농도가 3.0 M에서도 5% 내외의 탈거율을 보여 탈거 효과가 미미하였다. Fig. 8는 염산을 사용한 탈거 실험 결과이다. 그림으로부터 코발트의 경우 4.0 M HCl을 사용하였을 때 80%의 탈거율을 보이고, 염산 농도의 증가에 따라 탈거율도 증가하여 8.0 M HCl을 사용한 경우 전량 탈거 되었다. 한편, 니켈의 경우도 염산 농도 증가에 따라 탈거율이 증가하여, 8.0 M HCl을 사용한 경우에는 90% 이상 탈거 되어 염산을 사용할 경우에는 코발트와 니켈이 동시 탈거가 가능함을 확인하였다. 따라서 Cyanex 301로 코발트 및 니켈을 동시 추출한 후에 황산을 탈거제로 사용할 경우에는 코발트는 효과적으로 탈거할 수 있으나 니켈의 탈거율이 낮아 두 성분을 분리하여 회수는 가능하나 니켈의 탈거가 어렵다는 단점이 있다. 이 경우에 C. Bourget 등에 의하면 황산에 의한 낮은 탈거율을 개선하기 위해 아민계 추출제인 Aliquat 336과 Cyanex 301을 혼합하여 사용하는 등의 방법을 통하여 탈거율을 일부 개선시킨 연구 결과가 있으며, TBP를 혼합한 니켈 탈거 개선 연구도 진행되고 있다16). 한편, 탈거제로 염산을 사용할 경우에는 코발트, 니켈을 동시에 빠르게 탈거 한 후에 후속 공정에서 Alamine 336 등에 의해 코발트와 니켈을 쉽게 분리하여 순수한 물질로 회수가 가능하다23). 그러나 이 경우 코발트와 니켈을 동시 탈거하여 2성분계 혼합염의 형태로 회수할 경우에도 혼합염의 형태로 이차전지 양극활물질의 전구체용으로 사용을 고려할 수 있다. 따라서 Cyanex 301에 의해 추출된 코발트와 니켈의 탈거는 염산을 탈거제로 사용하는 것이 효과적 일 것으로 사료된다.
4. 결 론
본 연구에서는 코발트, 니켈과 불순물(Fe, Mg, Mg, Li) 혼합 용액에서 Cyanex 301을 사용하여 코발트, 니켈을 회수하기 위한 기초 실험을 실시하였으며, 다음과 같은 결론을 얻을 수 있었다.
코발트, 니켈과 불순물로 마그네슘, 망간, 리튬이 함유되어 있는 용액의 경우 마그네슘과 리튬은 미량 추출되거나 추출되지 않았다. 망간의 경우 일부 공추출 되었으나, 평형 pH 1.5 부근에서 코발트, 니켈은 99% 이상 추출되고, 망간은 약 11% 추출되어 분리가 가능하였다. McCabe- Thiele diagram을 통해 추출 상비(A/O) 2.0, 2단 추출을 통해 코발트와 니켈을 99.9% 이상 동시 추출이 가능함을 확인하였다. 코발트, 니켈 추출 후 불순물 제거를 위해 황산, 염산을 사용하였으며, 0.05 M H2SO4 사용 시 마그네슘은 99%, 망간은 88%은 세정되어 제거하였다. 0.05 M HCl의 경우 마그네슘은 99.9%, 망간은 80%이상 제거하여, 황산과 염산 모두 불순물에 대한 세정율이 높았다. 3.0 M H2SO4을 사용하여 탈거 할 경우 코발트는 93% 탈거된 반면, 니켈은 5% 탈거되었으며, 8 M HCl을 사용한 경우 코발트는 99.9%, 니켈 90% 이상 탈거되었다. 탈거 공정에서 코발트와 니켈을 분리하여 회수하기 위해서는 황산을 사용하는 것이 유리하며, 동시 회수를 위해서는 염산을 사용하는 것이 바람직하다.