1. 서 론
1.1. 주요 아연 함유 산업부산물의 특성
2. 습식 아연 회수 연구 동향
2.1. 강산(무기산) 활용 아연 함유 산업부산물 침출 연구 동향 분석
2.2. 약산(유기산) 활용 아연 함유 산업부산물 침출 연구 동향 분석
2.3. 알칼리 활용 아연 함유 산업부산물 침출 연구 동향 분석
2.4. 기타 용매 활용 아연 함유 산업부산물 침출 연구 동향 분석
2.5. ZnFe2O4의 침출 메커니즘 및 구조 변화 기술 분석
2.6. 아연 회수 후 용액 정제 및 철 분리 기술
3. 결 론
4. 기술적 제언
1. 서 론
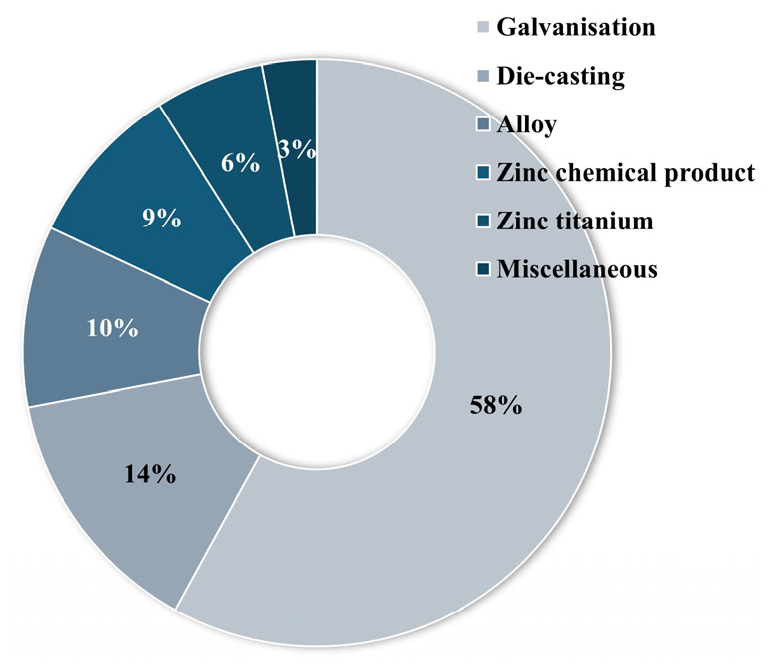
4대 비철금속 중 하나인 아연(Zinc, Zn)은 현대 산업 전반에 필수적인 금속 원소로, 철강의 아연도금(Galvanizing), 배터리 제조(특히, 알칼라인 및 아연-공기 전지), 황화아연 형광체, 합금 제조(브라스, 다이캐스팅용 Zn-Al 합금), 의약 및 화장품 첨가제, 농업용 미량 원소 비료 등 다양한 용도로 활용되고 있다. 특히, 전 세계 아연 소비의 약 50% 이상이 철강 표면 부식 방지를 위한 도금용으로 사용되며, 이는 제강 산업과 아연 수요가 밀접히 연관되어 있음을 의미한다. Fig. 1에 아연의 주요 용도에 대하여 나타내었다1).
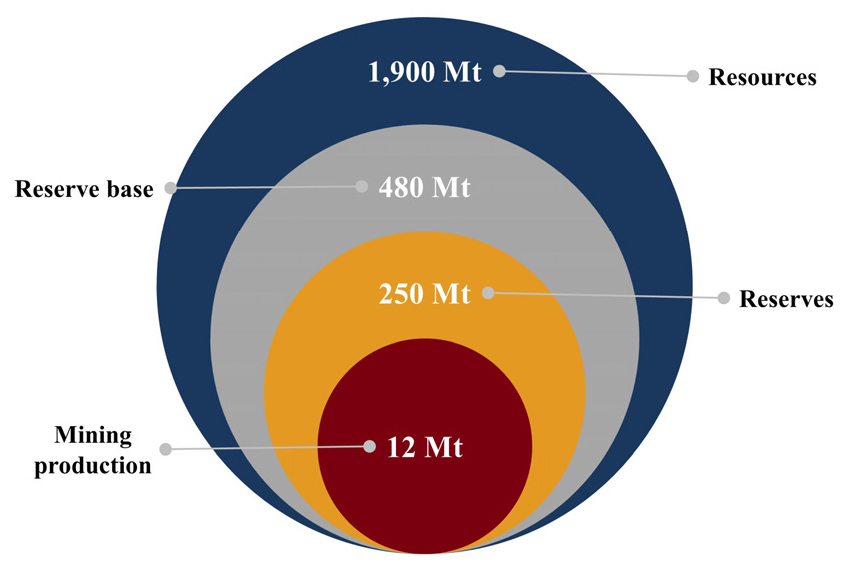
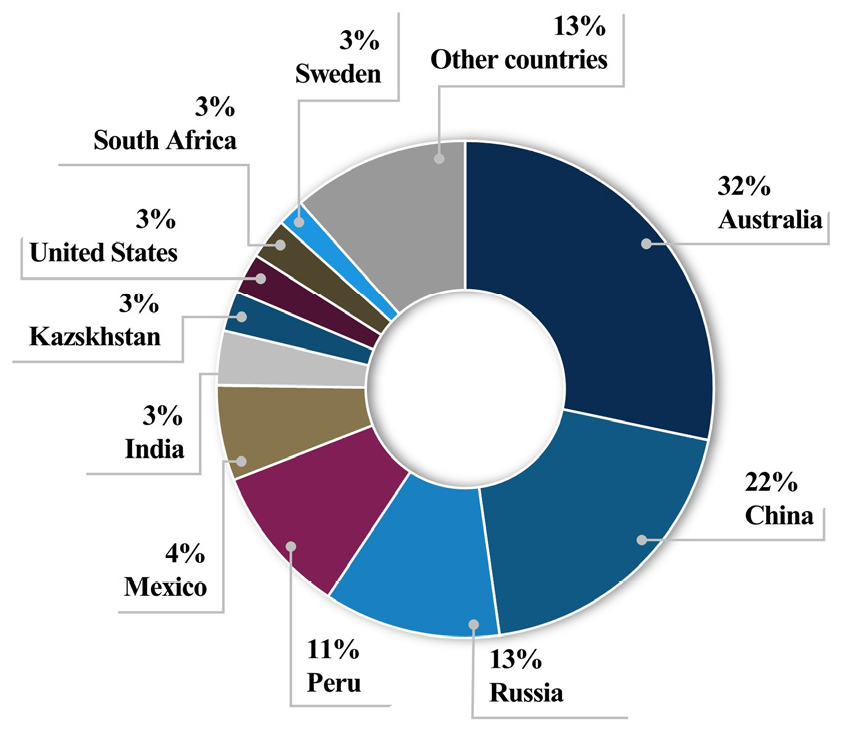
아연의 공급은 주로 황화아연(Sphalerite, ZnS)으로, 전통적으로 고온 배소(Roasting) 공정을 거쳐 아연 산화물로 전환된다. 채광이 가능한 아연 매장량(Reserves)은 2023년 기준 약 2억 5,000만 톤 이상으로 추정되며, 주요 국가로는 오스트레일리아, 중국, 러시아, 멕시코 등이 있으며 이들 국가가 전 세계 매장량의 약 57%를 차지한다. 2023년 전 세계 아연 광석 채굴량은 연간 약 1,200만 톤 이상(Zn metal 기준)으로 보고되었으며, 이 중 중국이 약 33%로 세계 최대 생산국이자 소비국으로서 기능하고 있다. Fig. 2와 Fig. 3 그리고 Table 1에 아연 매장량 현황과 주요 국가의 생산량을 나타내었다2,3,4,5,6). 또한, 전 세계 아연 생산량 중 약 13%는 2차 자원(재활용 아연)으로부터 공급되고 있으며, 그 비중은 점차 증가하는 추세이다. 이러한 재활용 아연은 전기로 또는 도금 부산물, 산업 스크랩 등 다양한 2차 자원으로부터 회수된다.
Table 1.
World mine production of zinc, by country, 20233)
한편, 이러한 아연의 산업적 활용과는 별개로 제강・비철금속 공정의 부산물로부터의 아연 손실은 자원적 측면에서 큰 문제가 되고 있다. 대표적인 아연 함유 산업부산물은 주로 제철・제강 공정, 아연도금 공정, 비철금속 제련 공정 등에서 다량 발생하며, 대표적인 형태로는 전기로 제강 분진(Electric Arc Furnace Dust, EAFD), 아연도금 슬러지(Galvanizing Sludge), 아연 회수 후 슬러지(Residues), 아연 소광 분진(Zinc Smelting Dust, ZSD) 등이 있다. 이 중 EAFD는 1,600℃의 고온 전기로 제강 공정에서 고철을 녹일 때 발생하는 대표적 부산물로, 일반적으로 전체 철강 생산량의 약 1–2%에 해당하는 양이 발생하며, 아연 함량은 10–40% 수준으로 높은 편이다. 국내에서는 연간 약 40만 톤의 EAFD가 발생하는 것으로 추정되며, 세계적으로는 연간 700–1,000만 톤 규모에 달한다7,8).
또한, 비철금속 제련 공정(예 : 아연 제련소, 납-아연 합금 제련소)에서도 EAFD 또는 로 회분(Furnace Ash) 형태로 아연이 포함된 고체 잔사가 발생하며, 아연 함량이 20–60% 이상일 수 있다. 이들 부산물은 자원적으로 높은 가치를 가지나, 동시에 납, 카드뮴, 및 크롬 등 중금속이 동반되어 있어 환경 규제 하에서 폐기물로 분류되고 있다. 이에 따라 아연 함유 산업부산물의 발생량을 단순 폐기 처리하지 않고, 금속 회수 및 재자원화하는 기술개발이 중요 과제로 대두되고 있으며, 각국은 이를 기반으로 한 순환 경제 체계(Circular Economy) 전환을 적극 추진하고 있다. 최근에는 이를 2차 아연 자원(Secondary Zinc Resources)으로 분류하고 많은 연구자들이 회수 기술에 대한 개발이 활발히 이루어지고 있으며, 다양한 연구가 총설 형식으로 보고되고 있다7,9,10,11,12).
아연 함유 산업부산물을 처리하고 자원화하는 기술은 크게 건식 공정(Pyrometallurgy)13,14,15,16,17)과 습식 공정(Hydrometallurgy)18,19,20)으로 나뉜다. Waelz 공정, 전기 용해, 플라즈마 제련 등의 고온 처리 기반 건식공정 기술은 주로 높은 처리 속도와 대규모 처리에 유리하며, 아연을 휘발시켜 산화아연(ZnO) 형태로 회수한다. 그러나 고온 공정으로 인해 막대한 에너지 소비가 수반되며, 불순물과의 동반 휘발 가능성 및 복잡한 부산물 처리 과정, CO2 배출 및 슬래그 문제 등을 해결해야 한다는 단점이 있다. 이러한 건식공정의 한계를 극복하고, 낮은 에너지 소비와 높은 선택성 및 순도를 요구하는 최근의 추세에 따라 습식공정 기술의 중요성이 재조명되고 있다.
습식공정은 산(Acid) 또는 염기(Base) 수용액을 이용해 부산물 내의 특정 금속 성분(예: 아연)만을 선택적으로 침출(Leaching)하여 용액 상태로 분리한 후, 침전(Precipitation), 용매추출(Solvent Extraction), 이온 교환(Ion Exchange), 전해 채취(Electrowinning) 등의 후속 정제 과정을 통해 고순도의 최종 제품을 회수하는 일련의 기술을 포괄한다. 습식공정에서 가장 핵심이 되는 요소는 아연의 최대 회수율 달성과 동시에 철 성분의 최소 용해를 위한 침출제의 종류와 반응 조건이다. 아연 회수에 사용되는 침출제는 크게 무기산(황산, 염산), 유기산(카복실산, 옥살산 등), 알칼리(수산화나트륨 등) 그리고 특수 침출제(FeCl3, Deep Eutectic Solvent 등)로 분류되고 있다. 이러한 습식공정은 조업 온도가 낮아 에너지 효율이 높으며, 최종 회수되는 아연의 순도가 높아 고부가 가치 창출에 유리하다. 특히, 부산물 내 다양한 금속 성분을 분리하고 정제하는 데 있어 정밀한 제어가 가능하며, 회수 잔류물인 철 성분을 제강 공정에 재활용할 수 있도록 환경친화적인 형태로 남길 수 있다는 점에서 큰 강점을 갖는다.
본 총설 논문에서는 EAFD 및 ZSD를 포함한 다양한 아연 함유 산업부산물로부터 국내・외 학술지에 발표된 최신 연구 동향을 종합적으로 분석하여 정리하고자 한다. 특히, 유・무기산 또는 알칼리성 침출제를 활용한 습식 공법에 따른 아연 회수 및 철 분리 기술을 정리하고, 침출제 종류, 조건, 회수율, 반응 메커니즘 등을 비교 분석함으로써 향후 고효율・친환경 아연 회수 공정 설계의 방향을 제시하고자 하였다.
1.1. 주요 아연 함유 산업부산물의 특성
아연을 함유하는 대표적인 산업부산물은 전기로 제강 분진인 EAFD와 아연 소광 분진인 ZSD로 나뉜다. 이들은 산업 공정 중 집진장치에 의해 수집되는 미세 분말 형태의 부산물로, 다양한 중금속을 포함하고 있으며 화학적・물리적 특성에 따라 처리 공정 설계에 중요한 영향을 미친다. Table 2에 아연 함유 산업부산물의 발생 출처별 주요 특징을 정리하여 나타내었으며, Table 3에 EAFD와 ZSD의 일반적인 함량을 나타내었다.
Table 2.
Characteristics of Zinc-Bearing Industrial By-products by Source
Table 3.
General contents of EAFD and ZSD
| EAFD | ZSD | |||
| Elements | Composition | Elements | Composition | Composition [21] |
| Zn | 10–40% | Zn | 30–80% | 77.4 |
| Fe | 20–40% | Fe | 5–15% | 12.4 |
| Pb, Cd, Cr, Mn, etc. | small amount | Pb, Cl, S, K, Na, etc. | small amount | 10.2 |
1.1.1. 전기로 제강 분진(EAFD)
제강 분진은 전기로에서 고철(Steel Scrap)을 재용해하여 철강을 제조하는 과정 중에 발생하는 미세한 고체 입자 형태의 부산물이다. 이는 철강산업에서 대표적인 고체 폐기물 중 하나로, 강철 용융 과정에서 금속 성분, 불순물, 첨가제가 고온에서 기화되거나 미세 분말 형태로 비산되어 배가스를 따라 이동한 뒤, 집진장치(예: 백필터, 사이클론 등)를 통해 포집되어 형성된다.
EAFD는 일반적으로 회색 또는 흑색의 미세한 분진 형태로 존재하며, 입자크기는 수 마이크로미터 이하로 매우 작다. 화학 조성은 철(Fe)과 아연(Zn)을 주요 성분으로 포함하고 있으며, 이외에도 납(Pb), 크롬(Cr), 니켈(Ni), 망간(Mn), 칼슘(Ca), 염소(Cl) 등의 다양한 금속 및 비금속 원소가 혼합되어 있다. 특히 아연(Zn)은 아연도금 강판(Scrap Galvanized Steel)과 같은 스크랩 소재에서 기원하며, 고온에서 휘발된 후 산화아연 형태로 분진 내에 포함된다. 전 세계적으로 발생하는 EAFD의 양은 매년 수백만 톤에 달하며, 철강 생산량 증가와 함께 꾸준히 증가하는 추세이다.
EAF 공정은 전통적인 고로 방식에 비해 에너지 효율이 높고 탄소 배출량이 적다는 장점이 있어, 친환경 제강 기술로 주목받고 있지만, EAFD의 처리 문제는 여전히 해결해야 할 과제로 남아있다. 그 이유는 EAFD가 단순 폐기물이 아니라, 유해물질과 유가금속을 동시에 포함한 복합 물질이기 때문이다. 실제로 EAFD는 미국 환경보호청 및 유럽연합에서 유해 폐기물로 분류되는 경우가 많으며, 이를 매립하거나 단순 소각하는 경우 환경오염을 유발할 수 있다.
그러나 역설적으로, EAFD는 산업적으로 매우 가치 있는 2차 금속 자원(Secondary Metal Resource)으로 간주되기도 한다. 특히 아연은 비철금속 산업에서 중요한 소재이며, 제강 분진 내 산화아연 함량은 10–40%에 이를 수 있다. 따라서 EAFD로부터 아연 및 철을 회수하고, 유해 성분을 안정화 또는 제거하는 다양한 재활용・자원화 기술이 개발되고 있으며, 이는 순환 경제 및 자원 고갈 대응 전략과 밀접한 관련을 지닌다.
1.1.2. 아연 소광더스트(Zinc Smelting Dust, ZSD)
ZSD는 아연 제련 공정(특히 Roasting 및 Sintering)에서 고온 휘발 공정을 통해 아연이 함유된 폐기물로부터 아연을 회수하는 과정에서 생성되는 산화아연 기반의 미세 입자상 부산물이다. 주로 제강 분진, 도금 슬러지, 아연 함유 폐촉매 등과 같은 이차 자원을 원료로 하여, 약 1,000–1,200℃의 고온에서 환원 및 휘발 처리하는 과정에서 생성된다. 휘발된 아연 증기는 배가스 라인을 따라 이동하며, 산소와 반응해 산화아연 형태로 산화되고, 냉각기 또는 백필터 등 집진장치를 통해 포집되어 최종적으로 아연 소광 더스트로 수거된다.
이러한 ZSD는 본질적으로 회수 대상 금속(Zn)을 포함한 농축 미세 분진이며, 물리적으로는 회백색 또는 백색의 파우더 형태이고, ZSD는 다량의 ZnO, ZnSO4, ZnCl2 등을 포함하고 있으며, 일부는 ZnFe2O4 또는 기타 난침출성 화합물로 존재한다. 원료 성분 및 공정 조건에 따라 성분비는 차이를 보이나, 일반적으로 30–80% 수준의 산화아연을 포함하고 있어 2차 자원으로서 높은 산업적 가치를 지닌다. 그러나 동시에 납(Pb), 카드뮴(Cd), 염소(Cl) 등 환경 유해 요소도 동반되어 있기 때문에, 유해 폐기물로 분류될 수 있는 잠재적 위험성도 함께 지닌다.
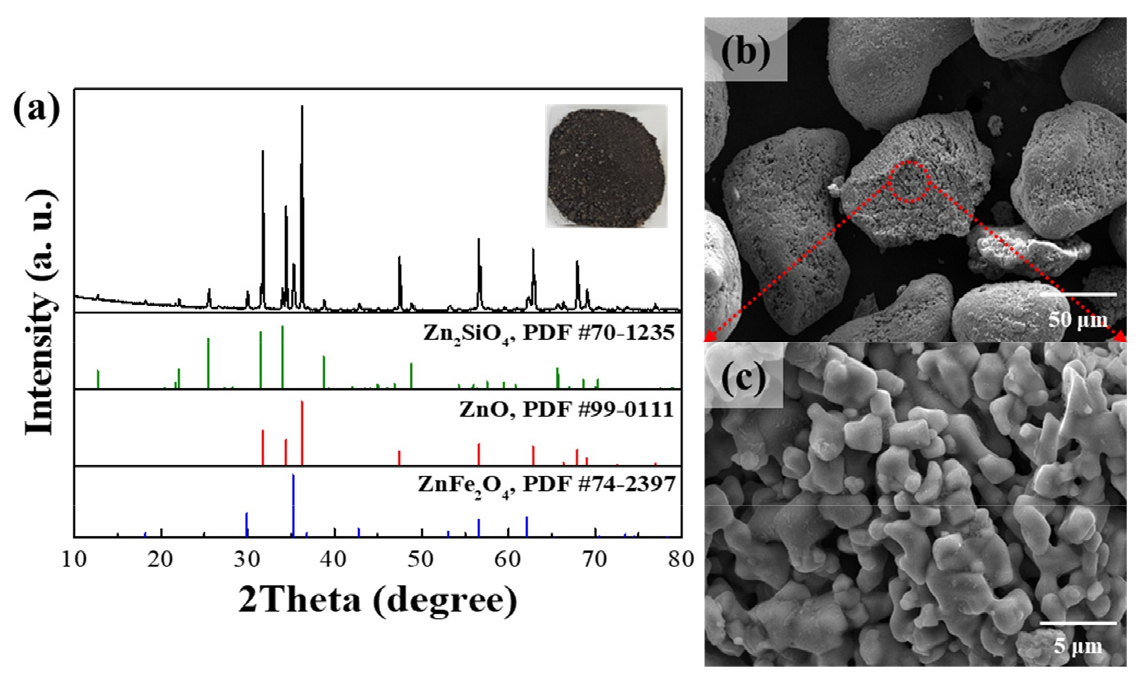
이에 Kim et al.21)의 연구에서는 국내 제련소에서 발생한 ZSD의 화학적 성분과 결정상을 자세히 나타내었으며, 아연은 약 77%, 철은 약 12% 그리고 규소(Si), 납, 황(S)과 같은 불순물들이 포함되어 있었다. 또한, 결정상은 알려진 것과 같이 ZnO, ZnFe2O4, Zn2SiO4 등의 결정상이 혼합되어 있었으며, 이러한 특성은 Table 3 및 Fig. 4에 나타내었다.
ZSD의 생성은 아연을 회수하기 위한 필연적인 부산물이며, 이의 생성 원인은 아연이 높은 증기압과 휘발성을 가지고 있기 때문이다. 도금된 강철 스크랩이나 기타 아연 함유물의 고온 처리 시 아연은 용융 상태로부터 쉽게 증발하고, 이후 산화되어 포집된다. 이러한 물리화학적 성질은 아연 회수에 유리한 동시에, 다단계의 후처리 및 정제 과정이 필수적으로 발생하여 이는 공정적 복잡성을 야기한다.
따라서 ZSD는 단순한 폐기물이 아니라, 아연 회수를 통해 경제적 가치를 창출할 수 있는 전략적 2차 자원으로 재인식되고 있으며, 이를 고순도 산화아연 또는 금속 아연으로 정제하기 위한 기술개발이 활발히 진행 중이다. 동시에 납・염소 등의 유해 성분을 제거하거나 저감할 수 있는 친환경 공정의 도입이 필수적인 과제로 대두되고 있다. 이러한 맥락에서 ZSD는 순환 경제와 지속 가능한 금속 자원 관리 측면에서 중대한 위치를 차지하는 산업부산물로 평가된다.
1.1.3. 물리적/광물학적 특성
EAFD와 ZSD는 물리적 특성에서는 모두 미세 분말이며, 광물학적으로는 다양한 금속 산화물 결정상을 포함하지만, EAFD는 스피넬 구조(ZnFe2O4 등)의 난용성 복합 광물이 주로 존재하는 반면, ZSD는 산화아연 결정이 주성분으로 비교적 회수가 용이한 특성을 보인다. 이에 따라 처리 방법, 회수 효율, 정제공정에 큰 차이를 유발하게 된다.
EAFD는 일반적으로 입자크기 0.1–10 μm 범위의 분말 형태로 존재하며, 구형(Spherical), 다면체(Polyhedral), 결정상(Crystalline), 유리상(Glassy) 등 다양한 입자 형태를 보인다. 색상은 보통 회색에서 암회색이며, 입도분포는 넓고 응집된 입자(Agglomerate)를 포함하기도 한다. 비표면적이 넓고, 미세한 입자 때문에 반응성이 높은 특성을 지닌다. 특히 아연은 자유 산화아연으로 존재하거나 Franklinite와 같이 스피넬(Spinel) 구조의 고용체로 존재할 수 있다. 이러한 스피넬 구조는 화학적으로 안정하여 습식공정에서 아연 회수를 어렵게 만들기도 한다. 또한 염소(Cl), 황(S), 플루오린(F) 등 휘발성 성분은 복합염 형태로 존재하거나 미세 입자의 표면에 흡착된 형태로 나타난다.
ZSD는 아연 제련 공정에서 발생하는 미세 산화물로, 주로 산화아연 결정이 높은 비율(30–80%)로 포함된 분말이다. 입자는 대부분 수 μm 이하의 구형(Spherical) 또는 복합 응집체(Agglomerated Clusters) 형태이며, 표면적이 넓고, 색상은 백색에서 회백색이다. 상대적으로 낮은 비중(약 1.5–2.5 g/cm3)을 가지며, 흡습성이 있어 장기간 노출 시 응집되기 쉽다. 또한, 휘발 금속(Pb, Cd 등)은 아연과 유사한 증기압을 가지므로, 분진 내 공존하며 유해 성분으로 작용한다. 염소 및 알칼리 성분은 산화아연 결정 표면에 혼입되거나 염화물 형태로 존재하여 정제 과정에서 제거 대상이 된다.
2. 습식 아연 회수 연구 동향
아연이 함유된 산업부산물로부터의 회수 기술 중, 습식공정은 다양한 침출제 조성과 조건 설정에 따라 매우 다양한 경로로 발전해 왔다. 이러한 습식공정은 침출, 분리, 정제 및 회수 등의 단계를 포함한다. 특히 침출 단계에서는 아연 함유 산업부산물에 함유된 유가금속을 회수하기 위한 과정으로 후속 분리 및 정제공정의 기초적 물성을 형성하기 때문에 재활용 공정에서 가장 중요한 부분을 차지한다. 이러한 침출 공정은 다양한 방법으로 많은 연구자들이 연구를 수행하고 있다. 사용되고 있는 침출제는 무기산, 유기산, 알칼리, 그리고 특수 화합물 기반 시스템으로 나뉘며, 각 계열은 반응 메커니즘과 금속 선택성에서 고유한 특징을 지닌다.
2.1. 강산(무기산) 활용 아연 함유 산업부산물 침출 연구 동향 분석
무기산 침출은 가장 전통적인 아연 회수 방식으로 현재까지도 가장 널리 적용되고 있는 기술적 방법이다. 대표적으로 황산(H2SO4), 염산(HCl), 질산(HNO3)이 사용된다. 이러한 무기산은 강산으로서 높은 효율의 침출 효과와 경제성의 이유로 유가금속을 회수하는 공정에 많이 사용되고 있다. Table 4에 무기산을 침출제로 사용하여 아연 함유 산업부산물에 대하여 아연 및 철 성분을 침출하는 연구 동향에 대하여 나타내었다.
Table 4.
Research trends on Zn/Fe leaching from Zinc-containing Industrial by-products using strong (inorganic) acids
| Material used | Leaching Conditions | Leaching Rate (%) | Reference |
|
Zinc ferrite residue (Zn 18.12%, Fe 29.81%) |
•H2SO4 : 200 g/L •L/S ratio : 10 mL/g •Temp. 90℃, Time 5 h |
- LZn : 98.3% - LFe : 92.72% | [32] |
|
Zinc-bearing dust (Zn 44.77%, Fe 17.45%) |
•Ultrasonic power : 600 W •Ascorbic acid : 0.08 mol/L •H2SO4 : 2 mol/L •L/S ratio : 7 mL/g •Temp. 90℃, Time 30 min |
- LZn : 98.96% - LZn : 88.59%, only H2SO4 - LFe : ~ 10% | [31] |
|
EAF slag (Fe2O3 17.45%) |
•H2SO4 & HCl 4 M •oxidant H2O2 & KMnO4 •Temp. 50℃, 75 μm |
- H2SO4 : 48.2% - HCl : LFe 36.8% | [33] |
|
Zinc oxide bearing (Zn 41.37%, Fe 2.05%) |
•Ultrasonic power : 500 W •H2SO4 : 140 g/L •L/S ratio : 5 •Temp. 25℃, 100 rpm, 30 min |
- LZn : 91.16% - LZn : 85.36%, only H2SO4 - Residues : ZnFe2O4, Zn2SiO4, ZnS | [34] |
|
Zinc-leached residue (Zn 20%, Fe 26%) |
•H2SO4 : 140 g/L •Reductant galena (PbS) •Galena:ZnFe2O4 = 1:1 •Particle size : 43-48 μm •Temp. 85℃, 90 min |
- LZn : 67%, LFe : 69% - LZn : 87%, LFe : 97% (Galena) | [35] |
|
EAF flue (Zn 42.7%, Fe 27.0%) |
•H2SO4 : 20% solution •L/S ratio : 50-200 g/L •Temp. 80℃, 2 h, 400 rpm | - LZn : 60% (50 g/L) | [27] |
| EAFD (Zn 33.16%, Fe 17.89%) |
•HNO3 : 1.5 M •HCl : 1.2 M •Aqua regia : 10% •L/S ratio : 100 g/L •Room Temp., 168 h, 400 rpm |
- HCl & Aqua regia LZn : > 75%, Fe : < 5% - HNO3 LZn : > 75%, LFe : < 20% | [36] |
|
In-bearing zinc dust (Zn 23.4%, Fe 30.9%) Sphalerite (Zn 47.27%, Fe 14.44%) |
•H2SO4 : 150 g/L •Reductant sphalerite •Zn dust : sphalerite = 0.95 •Particle size : 58-74 μm •Temp. 90℃, 4 h |
- LZn : 96.1%, - LFe : 92.8% | [37] |
|
Zinc ferrite & EAF (Zn 7.8%, Fe 37.3%) |
•FeCl3・6H2O decomposition agent •Temp:150℃ (ZnFe2O4), 200℃ (EAF dust), hydrothermal reaction •time : 2-10 h •RF/Z FeCl3・6H2O:ZnFe2O4 = 15:20 •NaOH leaching solution |
- Zinc ferrite LZn : 97.2%, LFe : ~ 0% - EAF dust LZn : 94.5%, LFe : trace - separation efficient SZn 99.2%, SFe 99.5% | [38] |
|
Zinc leach residue (Zn 9.87%, Fe 4.93%) |
•H2SO4 : pH 1.5 •Oxidant : H2O2, MnO2 •L/S ratio : 7 •Temp. 75℃, 120 min |
- LZn : 96%, LFe : 70% - LZn : 90%, LFe : 5% (H2O2) - LZn : 80%, LFe : 0.4% (MnO2) | [39] |
| BOF sludge (Zn 2.57%, Fe 61.4%) |
•H2SO4 : 0.1-1.0 M •L/S ratio : 10 •Temp. 80℃, Time 15 min, 300 rpm | - LZn : 70% | [26] |
| EAFD (Zn 8%, Fe 45%) steel-making waste (Zn 14%, Fe 52%) |
•H2SO4 : 0.3 M •microwave, 260℃, 100 min |
- LZn : > 92% - LZn : > 99% (H2O2) - Residues 90% hematite | [24] |
| EAFD (ZnO 25.29%, Fe2O3 24.78%, D50=19.3 μm) |
•H2SO4 : 3 N •L/S ratio : 10% •Temp. 60℃, Time 1.6 h, 700 rpm |
- LZn : 80.6% - LFe : 44.6% | [40] |
| EAFD (Zn 29.1%, Fe 24.0%) |
•H2SO4, HCl, HNO3, 0.001-2.2 mol/L •Temp. 50℃, Time 90 min, 900 rpm |
- 0.1 M, 50℃ LZn : 72% - H2SO4 > HNO3 > HCl, | [41] |
|
Synthetic zinc ferrite (Zn 28.0%, Fe 50.3%) TF sludge (Zn 14.1%, Fe 52.1%) |
•HCl : 0.3 M •microwave, 260℃, 100 min •L/S ratio : 50 ml/g |
- Zinc ferrite LZn : 93%, LFe : 1.7% - Steel-making dust LZn : 99%, LFe : 22% | [8] |
| EAFD (Zn 8.08%, Fe 45.24%) TF sludge (Zn 9.15%, Fe 52.50%) |
•H2SO4 : 0.1 M, 3 M •L/S ratio : 5 •Temp. 80℃, Time 6 h |
- H2SO4 : 0.1 M LZn : ~ 30%, LFe : low - H2SO4 : 3 M LZn : ~ 100%, LFe : > 90% | [23] |
| EAFD (Zn 20.9%, Fe 27.8%) |
•H2SO4 : 0.4 M •L/S ratio : 0.4 •Temp. 80℃, Time 60 min | - LZn : 67%, LFe : < 10% | [42] |
|
EAF Steelmaking Dust (Zn 17.05%, Fe 27.23%) |
•I) H2SO4 : 1 M, 80℃, 60 min •II) H2SO4 : 0.1 M, 60℃, L/S=50 |
- I) LZn : 95%, LFe : 66% - II) LZn : 95%, LFe : 5% | [43] |
| EAFD (Zn 20.9%, Fe 27.8%) |
•H2SO4 : 0.4 M with Autoclave •L/S ratio : 0.4 &1.2 •100-250℃, 1-41 bar •60 min, 700 rpm |
- 100℃ & 1.0 bar LZn : 77.5%, LFe : 22.8% - 150℃ & 4.1 bar LZn : 84%, LFe : ↓ - 250℃ & 41 bar LZn : 56.7%, LFe : 8.5 | [25] |
|
Residue of EAFD (Zn 16%, Fe 30%) Carbon steel EAFD (Zn 7.4%, Fe 38.6%) Residue of Roasted ZS (Zn 56%, Fe 17%) |
•FeCl3・6H2O decomposition agent •Temp. 150℃, time 4-8 h •RF/Z FeCl3・6H2O:ZnFe2O4 = 10:1 |
- Residue of EAFD CZn 16→0.03%, CFe 30→42% - Carbon steel EAFD CZn 7.4→0.17%, CFe 38.6→52% - Residue of Roasted ZS CZn 56→2%, CFe 17→52.3% | [29] |
| EAFD (Zn 15.9%, Fe 37.7%) EAFD2 (Zn 26.7%, Fe 32.3%) |
•HCl : 2 M •Temp. 90℃, Time 2 h |
- LZn : > 90% - LFe : Relatively low | [28] |
| EAFD (Zn 22%, Fe 12%) |
•H2SO4 : 0.1 M, 2.0 M •L/S ratio : 10 •Temp. 30℃, Time 24 h, 1,000 rpm |
- H2SO4 : 0.1 M LZn : 90%, LFe : < 40% - H2SO4 : 2.0 M LZn : ~ 90%, LFe : ~ 90% | [22] |
황산 침출은 가장 보편적인 아연 회수 기술로 상당히 오래전부터 적용하여 관련 연구가 다양이 진행되고 있다. 특히 산화아연 기반 화합물의 용해에 매우 효과적이다. Cruells et al.22)은 0.1–2.0 M 황산을 이용하여 EAFD를 침출한 기초 연구를 수행하였으며, 비교적 낮은 온도인 약 30℃에서 90% 이상의 아연 침출율을 보고하였다. 본 연구의 중요한 발견은 아연은 반응 초기에 대부분 용출되는 반면, 철은 낮은 산 농도에서는 비교적 침출율이 낮아(약 40% 미만) Zn/Fe 선택성이 확보된다는 점이다. 이는 산업적으로 철 성분을 잔사로 남기고 아연 성분을 용액상에서 회수하는 데 유리한 핵심 조건임을 제시하였다22).
황산 기반 침출 기술을 한 단계 발전시킨 연구는 Langova et al.23)과 Langova & Matysek24)이다. Langova et al.23)은 상압 조건에서 황산 농도(0.1–3.0 M), 온도(20–80℃) 및 시간에 따른 침출 거동을 체계적으로 분석하였다. 아연은 낮은 농도에서도 비교적 빠르게 용출되지만, ZnFe2O4와 같은 스피넬 구조는 고농도・고온 조건에서만 침출된다는 사실을 규명하였다23). 이어진 고압 침출 연구에서는 수열 조건(260℃, 100분)에서 EAFD의 ZnFe2O4가 거의 완전히 분해되며 아연 회수율이 99%에 도달함을 확인하였다. 또한 Fe(III)를 α-Fe2O3(Hematite)로 수열반응을 통하여 침전시키는 기술을 결합함으로써 철 성분 제거까지 단일 공정에서 수행할 수 있음을 보였다24).
한편, Havlik et al.25)은 0.4 M 황산을 이용한 오토클레이브 기반의 압력 침출에서 a/d(Acid to EAFD ratio), 온도(100–250℃), 압력(1–41 bar)의 영향성을 검증하였다. 특히 150℃에서 84%의 아연 회수율을 달성하며 철 침출을 최소화할 수 있는 최적의 조건을 찾았으며, 관련 반응식은 하기와 같이 나타내었다. 해당 연구에서는 온도의 영향은 ZnFe2O4 결정 구조의 분해에는 한계가 있으나 Fe2+/Fe3+의 산화환원 상평형을 변화시켜 선택적 침출 조건을 형성할 수 있음을 제시하였다25). 최근 황산 침출에 관한 연구 흐름은 공정 최적화 및 정제 단계를 결합하는 방향으로 확장되고 있다. Trung et al.26)은 BOF 슬러지에서 아연은 1 M 황산에서 70% 침출되는 반면 철은 용액에서 pH 변화에 따라 빠르게 침전할 수 있음을 보였고, Rudnik27)은 H2O2–NH3 혼합 산화・침전법을 황산 침출액의 정제 단계에 적용하여 Fe2+/Fe3+ 상태를 제어하고 전해 회수 효율을 극대화할 수 있음을 확인하였다. 이 연구는 침출–정제–전해의 통합 공정이 산업적으로 실용화할 수 있음을 보여준 대표적인 사례이다26,27).
염산을 이용한 침출 연구에서는 ZnO, ZnCO3뿐만 아니라 ZnFe2O4와 같은 스피넬 구조에 대해서도 높은 반응성을 보여 황산 기반 침출보다 넓은 적용성을 가진 침출제로 평가된다. Baik & Fray28)의 연구에서는 1–2 M 농도의 염산에서 ZnFe2O4가 포함된 EAFD를 침출하여, 고온(90℃)에서 아연 침출율이 90% 이상 도달하고 비교적 철 침출율은 낮음을 확인하였다. 이 연구의 특징은 염산 침출 후 아연 전기분해 공정을 결합함으로써 염산 전해액을 재생하는 “폐쇄형 염산 순환 공정”을 구현한 점이다28).
한편, Langova et al.8)의 연구에서는 합성 ZnFe2O4 및 제강 슬러지(Tandem Furnace Sludge)로부터 아연을 선택적으로 침출하기 위한 염산 기반 습식공정을 고온・고압 조건에서 수행하였다. ZnFe2O4는 스피넬 구조로 매우 안정하여 일반적인 산 침출로는 분해가 어렵기 때문에, 본 연구에서는 0.3 M 염산 용액을 이용해 260℃, 100분 조건으로 마이크로웨이브 가열 방식의 반응을 도입하였다. 그 결과, 합성 ZnFe2O4에서는 약 93%, 실제 제강 슬러지에서는 약 99%의 아연 침출률을 기록하였으며, 철 성분은 대부분 고형으로 잔존해 침출액 내 농도가 매우 낮게 유지되었다. 침출 후 잔사에는 Fe2O3 (Hematite)의 안정한 산화물 형태로 존재하였다. 아연은 ZnCl2로 용해되는 반면, 철은 일시적으로 FeCl3로 침출된 후 수열 조건에서 역반응을 통해 Fe2O3로 재침전되는 반응 메커니즘이 제시되었으며, 관련 반응식은 하기에 나타내었다. 이 과정에서 Cl-은 아연 이온과의 착화합물 형성에 핵심적인 역할을 하며, 철과의 선택적 분리를 가능케 한다. 이러한 선택적 염산 침출 공정은 아연 회수율을 극대화하면서도 철 성분 동반 침출을 최소화할 수 있는 기술적 우위를 가지며, 잔사의 재활용 가능성 또한 확보할 수 있어 제강 부산물 처리 분야에서 산업적 활용 가능성이 높은 접근법으로 평가된다8).
염화계 침출의 진전은 Leclerc et al.29)의 연구에서 나타난다. 이 연구에서는 FeCl3・6H2O를 침출제로 사용하여 ZnFe2O4의 O2-와 Cl- 사이의 이온 교환 반응을 유도함으로써 ZnFe2O4 격자를 직접 분해하였다. 관련 반응식은 하기와 같이 나타내었으며, 그 결과 아연은 용액상 ZnCl2로 완전히 전환되었고, 철은 α-Fe2O3 형태로 침전 고화되었다. 특히 합성 ZnFe2O4에서 150℃ 및 4시간 조건으로 아연 성분을 거의 100% 용출에 성공했으며, 실제 EAFD에서도 ZnFe2O4 분해를 통해 높은 회수율을 확보하였다. 본 연구는 기존 황산 침출에서 구조적 한계 물질로 간주되었던 ZnFe2O4를 효과적으로 분리할 수 있는 접근법이었다29).
염산 기반 침출의 산업적 확장 가능성을 보여준 연구로는 Dreisinger et al.30)에서 언급한 UBC–Chaparral 공정이 있다. 이 공정은 다양한 침출제 및 정제 방법을 제시하였으며, 하기에 관련 내용 반응식을 나타내었다. 초기에는 NH3-(NH4)2CO3로 ZnO 및 ZnCO3를 침출한 뒤, 남은 ZnFe2O4는 염산으로 최종 침출하여 아연을 회수하는 하이브리드 방식으로 납, 카드뮴, 구리 등의 중금속을 시멘테이션으로 제거하고 잔사는 EPA(Environmental Protection Agency) 기준을 충족하는 비유해성 물질로 전환할 수 있음을 증명하였다30).
또한, Wan et al.31)은 아연 함유 폐분진으로부터의 아연 회수를 극대화하기 위해 황산–염산 혼합산 침출에 아스코르브산(Ascorbic acid)를 환원제로 도입한 초음파 보조 공정을 제안하였다. ZnFe2O4 구조는 일반적인 산 침출 조건에서 화학적으로 매우 안정하나, Wan et al.이 제시한 연구에서는 아스코르브산의 전자 공여를 통해 Fe3+를 Fe2+로 환원시킴으로써 스피넬 구조의 안정성을 저하시켜 아연 이온(Zn2+)의 용출을 유도하였다. 실제로, 2 M 농도의 혼합산 조건에서 초음파(25 kHz, 200 W)를 병용하고 아스코르브산을 첨가한 경우, 아연 침출률은 90.3%에 도달하였으며 이는 무첨가 조건 대비 약 18% 향상된 수치였다. 반응속도론 분석 결과, 활성화 에너지는 33.89 kJ/mol로 낮아졌으며, 반응은 확산 지배 단계에서 화학 반응 지배 단계로 전환되는 것으로 확인되었다. 침출 메커니즘 상 아연은 Zn2+로 용출되고, 철은 Fe3+에서 Fe2+로 환원되어 용출되며, 이는 XRD와 SEM 분석에서도 ZnFe2O4의 분해와 표면 다공화 증가를 통해 확인되었다. 이러한 환원성 유기산 기반의 침출 공정은 비유독성 환원제를 활용하여 고효율 아연 회수와 철의 선택적 억제를 동시에 달성할 수 있는 친환경 공정으로 평가할 수 있다31).
무기산 기반 침출은 높은 아연 회수율, 공정 단순성, 침출제 비용의 저렴함 등 여러 장점을 지닌다. 특히 황산 계열 공정은 전해 아연 산업과의 궁합이 뛰어나 대규모 적용 가능성이 높다. 반면, 고농도 황산 및 고온・고압 조건에서는 철 및 망간 등 불순물의 용출이 증가하고, 이에 따라 정제 단계가 복잡해질 수 있다. 또한, 염산 기반 공정은 ZnFe2O4와 같은 난용성 스피넬 구조까지 분해할 수 있어 침출 효율이 매우 높지만, 염화물 부식 문제, 염소계 오염물 관리, 장비 소재 비용 증가 등의 제약이 존재한다. 더불어 Zn2SiO4 및 Ca–Zn–Fe 복합 산화물 등 일부 광물상은 무기산 침출에 대한 반응성이 낮아, 환원 전처리 또는 플라즈마・기계화학적 공정과의 결합이 필요한 경우도 있다. 그럼에도 불구하고 최근의 연구들은 무기산 침출에 산화제/환원제 결합(H2O2, SO2, Fe2+ 재산화 제어), 초음파・마이크로파 보조, 전해액 재생・순환 공정 결합, 철 침전물의 고부가 가치화 등이 가능함을 입증하고 있다. 이는 무기산 기반 침출 기술이 향후 더 높은 경제성과 환경성을 가진 형태로 진화할 수 있음을 보여준다.
무기산 기반 침출 연구는 지난 30여 년간 지속적으로 발전하며, 초기 단순 선택 침출–산 농도 평가 연구에서 출발하여, 고압 침출・이온 교환 기반 구조 분해・정제–전해 결합형 통합 공정과 같은 고도화된 기술로 확장되어 왔다. 황산 기반 공정은 경제성・실용성 측면에서 강점을 가지며, 염산 기반 공정은 난용성 스피넬 구조에 대한 분해 성능이 탁월하다. 향후 기술적 과제는 ZnFe2O4 및 Zn2SiO4 등 난처리 광물상에 대한 해결, 철 성분 동시 용출 억제, 침출제 재사용성 확보 및 공정 경제성 향상 등이 될 것이다.
2.2. 약산(유기산) 활용 아연 함유 산업부산물 침출 연구 동향 분석
최근 환경친화성과 금속 선택성 확보 측면에서 유기산을 활용한 침출 공정이 활발히 연구되고 있다. 유기산은 생분해성, 낮은 부식성, 중금속 착화합물 형성능 등에서 장점을 가지며, 특히 아연과 철이 공존하는 산업부산물에서 선택적 아연 침출에 효과적일 수 있다. 대표적인 유기산 침출제로는 구연산(Citric acid), 말릭산(Malic acid), 옥살산(Oxalic acid), 타타르산(Tartaric acid) 등이 있으며, 침출 메커니즘은 pH 조절, 착물 형성, 환원성 등에 기반한다. Table 5에 유기산을 침출제로 사용하여 아연 함유 산업부산물에 대하여 아연 및 철 성분을 침출하는 연구 동향에 대하여 나타내었다.
Table 5.
Research trends on Zn/Fe leaching from Zinc-contained Industrial by-products using weak (organic) acids
| Material used | Leaching Conditions | Leaching Rate (%) | Reference |
| EAFD |
•Sodium citrate & H2SO4 - 0.5 M, 25 g/L, 500 rpm, 3 h - pressure & ambient temperature |
- Sodium citrate LZn : 59%, LFe : 2-3 % - H2SO4 LZn : 96%, LFe : < 40% | [45] |
| EAFD (Zn 24.7%, Fe 31.6%) |
•Sodium citrate •Oxalic acid •L/S ratio : 40 mL/g •Room temp, 3 h, 500 rpm |
- Sodium citrate LZn : 50%, LFe : < 5% - Oxalic acid LZn : 40%, LFe : < 10% | [44] |
|
Zinc plant residue (Zn 7.98%, Fe 5.44%) |
•Oxalic acid : 50 g/L •L/S ratio : 25 mL/g •Temp. 80℃, 400 rpm, 120 min |
- LZn : ≤ 10% - LFe : 82.5% | [47] |
|
Blast furnace dust (Zn 0.6%, Fe 36.2%) |
•Various acids (6 kinds), 1 mol/L - Malonic, Acrylic, Citric, Acetic, Oxalic, Benzoic acid •Temp. ambient, 24 h, L/S ratio=10 |
- Malonic LZn : 93.9%, LFe : 16.9% - Acrylic LZn : 83.1%, LFe : 8.5% - Citric LZn : 82.6%, LFe : 32.2% - Acetic LZn : 58.1%, LFe : 2.7% - Oxalic LZn : 18.5%, LFe : 31.2% - Benzoic LZn : 37.0%, LFe : 0.1% | [48] |
|
5 EAFD (Zn 7.4-28%, Fe 16-44%) |
•1st step : HNTA2- leaching - 1M, R.T., pH 8, 1hr, HNTA2-/ZnO=8 •2nd step : FeCl3・6H2O - 150℃, 8 h, FeCl3・6H2O/ZnFe2O4=10 |
- HNTA2- leaching LZn : 60-90%, LFe : < 3% - 1st + 2nd step LZn : 99.9% | [49] |
침출 효율 및 선택성에 대한 기초 연구로서 Borda & Torres44)은 EAFD로부터 아연을 선택적으로 침출하기 위해 구연산나트륨(Sodium Citrate) 및 옥살산을 이용하였으며, 각각 0.5 M 이하의 저농도로 적용하여 반응 온도와 시간에 따른 침출 거동을 비교하였다. 두 유기산 침출제 모두 대기압 및 실온에서 약 50%의 금속 침출율을 보였으며, 안정상인 ZnFe2O4 및 Fe2O3 성분은 상기 조건에서는 분해되지 않음을 보고하였다44). 또한 연이은 Borda et al.45)의 논문에서는 유기산계 침출제인 구연산염과 황산에 대한 용출 성능과 반응 속도를 비교하여 보고하였다45). 구연산염으로 침출 시 산화물인 산화아연에 대하여서는 자발적인 반응으로 빠르게 용해되고 Fe는 2-3%의 침출율을 나타내어 비철금속에 대한 선택성을 보였다. ZnFe2O4 경우 안정한 스피넬 구조로 황산을 이용한 고온 처리 시 분해 가능하다고 하였으며, Zn/Fe 성분의 동반 침출이 일어났다고 하였다. 관련 반응에 대한 반응식을 하기와 같이 나타내었다.
Gargul et al.46)의 연구에서는 구연산을 침출제로 사용하여 아연 침출 효율을 최대화하고 철 침출 효율을 최소화하여 선택성 계수를 극대화하는 실험을 수행하였으며 관련 반응식은 다음과 같다. 구연산 농도 0.5 M, 50℃ 및 1시간의 조건에서 아연 침출율은 최대 61.0%이고, 철 침출율은 3.8%을 보고하였다46).
반면, Yildirim et al.47)의 연구에서는 옥살산을 침출제로 사용하여 아연을 고형상에 잔존시키고 선택적으로 철을 용액상으로 침출하는 공정을 제안하였다. 관련 반응식은 하기와 같다. 최적 침출의 결과는 50 g/L 옥살산 농도로 80℃ 및 2시간 조건에서 철 침출율은 최대 82.5%이고, 아연 침출율은 10% 미만으로 보고하였다47).
Steer et al.48)은 6가지 카복실산(Carboxylic acid)인 말론산(Malonic acid, CH2(COOH)2), 아크릴산(Acrylic acid, CH2=CHCOOH), 구연산(Citric acid, C6H8O7), 아세트산(Acetic acid, CH3COOH), 옥살산(Oxalic acid, C2H2O4) 벤조산(Benzoic acid, C6H5COOH)를 침출제로 사용하여, 고로 습식 집진 슬러리(Blast Furnace Dust Slurry, BFDS)의 침출 특성을 비교하였다. BFDS의 주요 성분은 Table 5에 나타내었으며, 각 침출제에 대한 아연과 철 성분에 대한 침출율을 Table 6에 정리하였다. 또한, 관련 반응식은 하기와 같이 나타내었다. 특히 유기산–비수용성 용매 혼합 시스템(Acrylic acid + Methylbenzene 혼합 용액)은 철의 침출률을 0.1% 미만으로 억제하면서도 아연은 85% 수준으로 회수할 수 있어, 극도로 높은 선택성을 보인다고 보고하였다48).
Table 6.
Extraction of zinc and iron using a variety carboxylic acid at 1 mol/L
Borda et al.44)의 연구에서는 유기산 침출 후의 잔사에 대한 SEM-EDS 분석 결과, 대부분의 철은 산화철 형태로 잔존하며, 납 및 크롬 등의 중금속은 침출되지 않고 고형상태로 남아 안정성을 보였다. 이는 유기산 침출이 침출액의 중금속 오염을 최소화하면서 고상에 고정시키는 기능도 수행할 수 있음을 시사한다. 유기산 침출은 고온・고압이 필요하지 않으며, 환경 친화적인 침출 환경을 제공할 수 있으나, 다음과 같은 공정화 도전 과제를 갖는다.
•유기산 가격: 산업용 옥살산 또는 구연산은 무기산 대비 단가가 높아 재생 및 회수 기술이 병행되어야 함.
•느린 반응 속도: ZnFe2O4 구조에 대해서는 침출 반응 속도가 느리며, 충분한 시간 확보 및 반응 조건 제어가 요구됨.
•침출 후 정제공정: 유기산 착화합물은 금속 이온과 강하게 결합하기 때문에 후속 금속 회수 단계(예: 전해, 용매추출 등)에서 복잡성을 유발할 수 있음.
유기산 기반 침출은 선택성과 환경친화성 측면에서 아연 회수 공정의 유력한 대안으로 간주된다. 특히 ZnFe2O4와 같은 복합 산화물에 대해서는 환원제 병용 시스템을 구성하거나 특수 용매와의 병합을 통해 고효율 침출이 가능하며, 다양한 아연 함유 부산물에 대한 적용성이 지속적으로 확대되고 있다. 향후 공정 연속화와 유기산의 재생・회수 기술 확보가 상용화를 위한 핵심 요소가 될 것으로 예상된다.
2.3. 알칼리 활용 아연 함유 산업부산물 침출 연구 동향 분석
알칼리 침출은 산성 조건에 비해 철, 납, 구리 등 다수의 중금속을 침출하지 않고 아연만을 선택적으로 침출할 수 있는 특성이 있어, 높은 선택성과 공정 후처리의 간편성에서 주목받고 있다. 일반적으로 NaOH 또는 KOH가 침출제로 사용되며, 침출 메커니즘은 ZnO 또는 Zn(OH)2와 같은 아연화합물이 알칼리 수용액과 반응하여 [Zn(OH)4]2- 착이온으로 용해되는 원리를 기반으로 한다. 알칼리 침출은 ZnO, Zn(OH)2, ZnCO3와 같이 산화형 또는 염기성 아연화합물에 대해 우수한 침출 성능을 보인다. 그러나 ZnFe2O4, Zn2SiO4와 같은 스피넬계 또는 복합 산화물 구조에서는 침출이 거의 이루어지지 않는다. 이는 강한 Zn-O 및 Zn-Fe 격자 결합 에너지로 인해 알칼리 조건 하에서 격자 파괴가 일어나기 어렵기 때문이다. 관련된 반응식을 하기와 같이 나타내었으며, Table 7에 알칼리를 침출제로 사용하여 아연 함유 산업부산물에 대하여 아연 및 철 성분을 침출하는 연구 동향에 대하여 나타내었다.
Table 7.
Research trends on Zn/Fe leaching from Zinc-contained Industrial by-products using alkali
| Material used | Leaching Conditions | Leaching Rate (%) | Reference |
| EAFD (Zn 24.5%, Fe 43.8%) |
•NaOH 8 M •L/S ratio : 40 •Temp. 80℃, 800 rpm •Pretreatment C roasting 1,200℃ |
- LZn : 60.5% - C roasting RFe : 89.87% | [55] |
| EAFD (Zn 25.9%, Fe 18.0%) |
•Na2CO3, NaHCO3, NaOH (1-7 M) •4 h, 500 rpm •L/S ratio : 20, 80, 120 mL/g •Temp. : 20℃, 40℃, 60℃ |
- NaOH (3 M, 60℃) LZn : 92.92% - Na2CO3 : 56% - NaHCO3 : 45% | [53] |
| EAFD (Zn 33.0%, Fe 21.85%) |
•Pretreatment water leaching 60℃ •NaOH 6 M •L/S ratio : 40 •Temp. 80℃, Time 2 h, 400 rpm | - LZn : 88% | [54] |
|
Zinc Ferrite (high purity) |
•NaOH 6 M •Reductant Fe powder •Planetary Ball Mill - stainless steel ball 25 : 1, 4-6 h - Fe : ZnFe2O4 = 2:1) •Temp. 90℃, 2-4 h |
- Direct alkaline leaching LZn : < 2% - Mechanical activation LZn : 13% - Mechanochemical reduction LZn : > 70% | [52] |
| EAFD (Zn 12.2%, Fe 37.1%) |
•Conventional leaching - NaOH 6 M, 90℃, 4 h •Pressure leaching - 200℃ •Microwave pretreatment leaching •Ultra-sonic leaching |
- Conventional leaching LZn : 74% - Pressure leaching LZn : 74% - Microwave leaching LZn : 60.4% - Ultra-sonic leaching LZn : 55.9% | [51] |
| EAFD (Zn 33.0%, Fe 26.0%) |
•NaOH 10M •L/S ratio : 7 •Temp. 95℃, Time 2 h, 600 rpm | - LZn : 85% | [51] |
| EAFD (Zn 13.6%, Fe 29.8%) |
•NaOH 3M •Percent solid 0.2%, 10%, 20% •Temp. 95℃, Time 2 h, 850 rpm |
- Percent solid LZn : 85% (0.2%) LZn : 70% (10%), 56% (20%) | [56] |
| EAFD (Zn 20.5%, Fe 21%) |
•Chloride wash : 90 water •Lime leaching : acetic acid •Zinc leaching : NH3-(NH4)2CO3 | - LZn : 55-60% | [30] |
Orhan, G.50)은 EAFD로부터 아연과 납을 회수하기 위한 알칼리 침출 및 시멘테이션 공정을 제안하였다. 연구에서는 10 M 농도의 수산화나트륨을 사용하여 95℃에서 2시간 반응시킴으로써 아연 85%, 납 90%의 침출 효율을 달성함을 보고하였다. 침출 후 잔사는 ZnFe2O4와 Fe3O4와 같은 안정한 산화물 광물상을 포함하고 있었으며, 이는 XRD 분석을 통해 확인되었고 ZnFe2O4의 구조적 안정성이 침출 효율을 제한하는 주요 원인임을 시사한다. 이후 침출액 내 불순물 금속 제거를 위해 아연 분말을 이용한 시멘테이션 공정을 적용하였으며, 50℃에서 3시간 동안 진행된 반응에서 납 96%, 구리 76%, 카드뮴 89%의 제거 효율이 보고하였다50).
이은 Dutra et al.51)의 연구에서는 EAFD로부터 아연을 선택적으로 회수하기 위한 알칼리 침출 공정을 다양한 침출 조건 및 공정 방식으로 비교・분석하였다. 침출제는 수산화나트륨(NaOH)을 사용하였으며, 침출 조건은 농도 2–6 M, 온도 25–200℃, 반응 시간 최대 240분, 공정 방식은 일반 가열 교반, 오토클레이브 고압 침출, 마이크로웨이브 전처리, 초음파 교반 등으로 다양하게 설정되었다. 실험 결과, 6 M NaOH 용액에서 90℃, 240분 침출 시 아연 침출률은 최대 74%에 달하였으며, 철의 침출은 0.3% 이하로 매우 낮아 뛰어난 선택성을 보였다. 오토클레이브 방식의 고온 고압 조건에서도 유사한 수준의 아연 회수가 가능했으나, 일부 아연이 재침전되는 부반응 가능성이 제기되었고, 마이크로웨이브 전처리 방식은 sintering 효과로 인해 오히려 침출 효율이 저해되었다. 초음파 교반 조건에서는 최대 아연 침출률이 55.9%로 제한적이었다. XRD 분석에서는 침출 전 ZnO와 ZnFe2O4, Fe3O4 등이 관찰되었으며, 침출 후 ZnO는 제거되었지만 ZnFe2O4는 잔사에 잔존하여 아연 페라이트의 높은 구조적 안정성이 알칼리 침출 반응의 제한 요인임을 확인하였다51).
Zhang et al.52)의 연구에서는 아연 페라이트로부터의 아연 회수를 효율적으로 향상시키기 위해 금속철을 이용한 기계화학적 환원 전처리와 알칼리 침출법을 연계한 하이브리드 공정을 제안하였다. ZnFe2O4는 일반적으로 알칼리 용액에서 매우 안정적이며, 직접적인 NaOH 침출로는 아연 침출률이 2% 이하로 매우 낮다. 이에 저자들은 고에너지 볼밀을 이용해 ZnFe2O4와 금속철을 Fe:ZnFe2O4 몰비 2:1 조건에서 6시간 동안 기계화학적 공동 분쇄(mechanochemical milling)한 후, 6 M NaOH (90℃) 용액에서 침출을 수행하였다. 그 결과 아연 회수율은 70% 이상으로 증가하였다. XRD 분석 결과, 금속철과의 공분쇄에 따라 ZnFe2O4의 회절피크 강도가 감소하고, 결정 구조가 점차 비정질화되며 준안정(metastable) 상태로 전이되는 것이 확인되었다. 또한 XPS 분석에서는 Fe3+→ Fe2+로의 환원이 관찰되었으며, 이는 ZnFe2O4의 구조 내 산화철의 화학적 안정성을 약화시켜 침출 반응성을 높인 주요 요인이라 해석하였다52).
Al-Makhadmeh et al.53)의 연구에서는 요르단 지역의 전기로 제강 더스트로부터 아연을 선택적으로 회수하기 위해, 수산화나트륨(NaOH), 탄산나트륨(Na2CO3), 중탄산나트륨(NaHCO3)을 침출제로 활용하여 그 효과를 보고하였다. 분석 결과, EAFD는 Franklinite(ZnFe2O4), Magnetite, Wustite, Zincite(ZnO) 등 다양한 금속 산화물을 포함하고 있었으며, 아연 함량은 28.8%, 철 함량은 25.1%로 구성되어 있었다. 침출 실험은 다양한 농도(1–6 M)의 NaOH 용액을 사용하여 20–60℃의 온도 조건에서 수행되었으며, 6 M NaOH를 60℃에서 적용한 조건에서는 아연 침출률이 최대 92.9%에 도달하였다. 반면, Na2CO3 및 NaHCO3는 반응성이 낮아 아연 침출률이 56% 이하로 제한되었다. XRD 분석에 따르면, 침출 후 ZnO는 대부분 제거되었으나, ZnFe2O4는 여전히 잔사로 남아 구조적 안정성에 따른 침출 한계를 드러냈다. 또한, 활성화 에너지 분석 결과 15.7 kJ/mol로 산정되어, NaOH를 이용한 침출이 반응속도론적으로도 우수함을 확인하였다. 본 연구는 NaOH를 활용한 알칼리 침출이 아연 회수에 있어 높은 선택성과 환경친화적 장점을 가지며, 특히 ZnFe2O4와 같은 안정한 스피넬 구조를 효과적으로 처리하기 위해 고온 및 고농도 조건의 적용이 필수적임을 강조하였다53).
이와 별도로 Palimaka et al.54)은 폴란드 제강소에서 얻은 아연 함량이 약 33% 그리고 철 함량이 약 22% 함유된 EAFD를 사용하였으며, 먼저 수침출을 통하여 침출제 소모를 줄이고 전기분해 중 유해한 염소 방출 위험을 방지하기 위하여 전처리 공정을 실시하였으며, 6 M NaOH를 이용하여 80℃, Liquid/Solid=40의 조건에서 88.0%의 최대 아연 추출 효율을 달성하였다고 하였다. 이후 아연 금속판을 이용한 시멘테이션을 통해 납을 제거하고 전기분해를 통하여 순도 99.88%의 아연 스펀지형 분말 형태로 회수하였다고 하였다54). Siame et al.55)은 잠비아 UMCIL(Universal Mining & Chemical Industries Ltd) 제철소에서 발생하는 EAFD를 처리하여 철(약 43.8%)과 아연(약 24.5%)을 회수하고자 습・건식공정을 도입하였다. 습식공정은 아연을 회수하고자 8 M NaOH를 이용하여 80℃에서 약 60.5% 침출하였고, 이은 1,200℃ 탄소 환원배소에서 잔사 내 철 함량을 최대 89.87%까지 높여, EAF 공정의 원료로 재활용 가능하다고 보고하였다55).
알칼리 침출은 pH 제어가 용이하고, 침출액의 부식성이 낮아 설비 내구성이 뛰어나며, 특히 정제 및 고형화 공정이 단순하다는 점에서 산업적으로 유리하다. 다만 ZnFe2O4 구조의 침출에는 한계가 있으며, 고온에서의 반응성 증진이 필수적이다. 아울러 NaOH 가격 및 재생 공정, 침출 후 용액 내 나트륨 농도 조절 등의 공정 최적화 문제가 존재한다. 알칼리 침출은 아연 및 일부 희소금속의 선택적 회수에 효과적이며, 침출액 정제와 고형 잔사 안정성 측면에서 산업적 장점을 지닌다. 그러나 ZnFe2O4와 같은 난용성 구조에 대한 반응성은 낮으며, 전처리 기술 및 보조 에너지 도입을 통한 고도화가 요구된다. 공정 단순성과 친환경성이 요구되는 응용 분야에서의 활용 가능성이 높아, 다양한 복합 부산물에 대한 확대 적용이 기대된다.
2.4. 기타 용매 활용 아연 함유 산업부산물 침출 연구 동향 분석
최근 친환경 침출제 개발에 관한 관심이 급증함에 따라, 전통적인 산・알칼리 용매를 대체할 수 있는 심층융점용매(Deep Eutectic Solvent, DES) 기반 침출 기술이 주목받고 있다57,58,59). DES는 수소결합 공여체(Hydrogen bond donor, HBD)와 수소결합 수용체(Hydrogen bond acceptor, HBA)의 혼합으로 형성되는 저융점 용매로, 제조가 간단하고 생분해성이 높으며 금속 이온에 대한 높은 용해 특성을 지닌다. 대표적인 DES 조합인 콜린 클로라이드(ChCl) + 우레아(Urea), ChCl + 옥살산, ChCl + 구연산 등은 아연, 구리, 철 희토류 금속 등 다양한 금속 산화물에 대해 우수한 침출 성능을 나타낸다. 특히 아연 침출의 경우, 유기산 기반 DES가 Zn2+ 이온과 착화합물을 형성하며 선택적 용해를 유도한다.
Zhang et al.58)의 연구에서는 ChCl과 Urea 기반의 DES를 활용하여 선택적으로 아연을 침출하고자 하였으며, liquid-solid=15:1, 교반 속도 400 rpm, 침출 온도 90℃ 그리고 침출 시간은 600분의 조건에서 아연의 침출율은 약 87%로 침출되었다. 이때, 철 성분은 거의 침출되지 않았고 Fe2O3 형태로 회수되었다고 보고하였다.
이러한 DES 침출 연구에서는 침출 효율을 높이기 위해 초음파, 마이크로웨이브, 전기화학 보조 기술이 병용되기도 하며, 이러한 방식은 고점도 DES의 반응 확산 속도 문제를 개선하는 데 기여한다. 또한 DES는 침출 후 금속을 분리한 뒤에도 재사용 가능하다는 점에서 경제성과 환경친화성을 모두 확보할 수 있는 침출 시스템으로 주목받고 있다. 본 연구는 DES가 폐금속의 자원화뿐 아니라 폐수・독성 부산물의 최소화를 통해 지속 가능한 금속 회수 공정의 핵심 용매로 발전할 수 있음을 시사한다.
2.5. ZnFe2O4의 침출 메커니즘 및 구조 변화 기술 분석
ZnFe2O4은 EAFD 및 ZSD에 존재하는 가장 침출이 어려운 주요 아연화합물이다. 이는 스피넬 구조로 매우 안정하며, 일반적인 산이나 알칼리 조건에서는 분해되지 않는다. 따라서 ZnFe2O4의 침출 효율을 높이기 위해서는 구조적인 변형이나 환원 전처리가 필수적으로 요구된다.
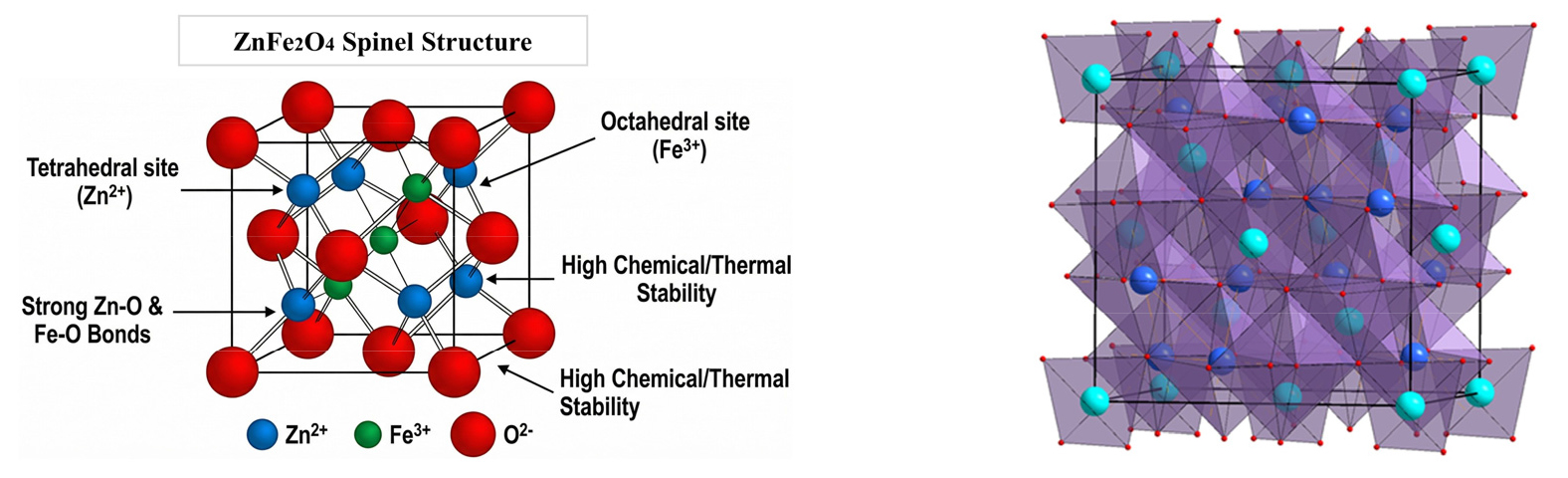
Fig. 5에 나타낸 ZnFe2O4의 구조적 특징을 살펴보면 ZnFe2O4는 정방정계 스피넬 구조를 가지며, Zn2+는 사면체 자리(Tetrahedral site), Fe3+는 팔면체 자리(Octahedral site)를 점유하고 있으며, Zn2+–O 및 Fe3+–O 간 결합 에너지가 강하여, 화학적/열적 안정성이 매우 높다. 일반적인 침출제(염산 및 황산 등)에서는 ZnO와 PbO는 쉽게 용출되지만, ZnFe2O4는 거의 침출되지 않고 잔사에 남는다. XRD에서는 강한 (311), (400), (511) 회절 피크가 나타나며, 침출 전후에도 이 구조가 유지되는 경우가 많다. 침출 저해 요인으로는 표면 수동화(Passivation)로 침출 과정 중 표면에 Fe(OH)3, SiO2, PbSO4 등이 형성되어 침출이 진행되지 않는다. 또한, 불균일한 입자크기 및 내부 결함으로 내부 ZnFe2O4가 침출제에 접근하지 못하는 경향이 있어 Fe3+의 높은 산화상태인 Fe3+–O 결합은 강력하여 구조를 깨기 어렵다. 이러한 문제점의 해결 방안으로 구조 변화 및 전처리 기술을 통한 환원 전처리, 기계화학적 분쇄, 플라즈마 및 열처리 전처리, 초음파 및 마이크로파 보조 침출 기술 등이 제안되고 있다60,61,62,63).
2.6. 아연 회수 후 용액 정제 및 철 분리 기술
습식 침출 후 용액에는 아연 이온(Zn2+) 외에도 철(Fe2+/Fe3+), 납(Pb2+), 카드뮴(Cd2+), 알루미늄(Al3+), 칼슘(Ca2+) 등의 이온이 함께 용출되는 경우가 많다. 따라서 순수한 아연화합물 또는 금속 아연을 회수하기 위해서는 선택적 정제 및 분리 공정이 필수적이다. 이러한 해결 방법으로는 침출액의 pH 조절, 침전제 첨가 등을 통해 아연 이외의 불순물 이온을 선택적으로 침전시킬 수 있는 침전법, 전위차를 활용해 아연보다 환원전위가 낮은 금속 이온(Pb2+, Cu2+, Cd2+)을 아연 분말로 환원하여 침전시키는 시멘테이션법(Cementation), 유기용매와 추출제를 이용하여 Zn2+ 또는 불순물 이온을 선택적으로 추출하는 용매 추출법 등이 제시되고 있다.
3. 결 론
본 총설 논문은 전기로 제강 분진(EAFD) 및 아연 소광 더스트(ZSD)와 같은 아연 함유 산업부산물로부터 아연을 선택적으로 회수하고, 철 등 공존 금속과의 분리를 위한 습식공정 기술들을 체계적으로 검토하였다. 다양한 침출제(황산, 염산, 유기산, 알칼리, DES 등)와 전처리 기술(환원, 기계 화학, 플라즈마 등)의 적용 사례들을 비교 분석함으로써, 현재 기술의 한계와 가능성을 다음과 같이 도출할 수 있었다.
ZnFe2O4는 침출 효율이 낮은 대표적인 아연 보유 광물이며, 구조 변화를 유도하지 않으면 침출 효율이 30% 이하로 제한되는 문제가 발생한다. 무기산 침출제는 경제성이 우수하나 선택성이 낮고, 후단 정제에서 복잡한 정제공정을 수반하며, 유기산 및 알칼리성 침출제는 선택성은 높지만, 반응 속도가 느려 공정 시간이 증가하게 된다.
이에 환원 전처리를 통해 ZnFe2O4의 격자 구조를 불안정화하여 아연 침출율을 70% 이상으로 끌어올릴 수 있었으며, 특히 철 분말, 아스코르브산 기반의 환원 기술 등이 효과적인 것으로 보고되었다. 침출 후 용액의 정제 및 회수는 침전법, 시멘테이션, 용매추출, 전해 회수 기술 등이 있으며, 이는 각각의 장단점을 바탕으로 공정 통합 설계가 중요하다. 최근 연구 동향은 DES 기반 침출, 플라즈마 보조 전처리, 자동화 모듈 설계로 확장되고 있으며, 이는 고효율・친환경 공정으로의 전환을 위한 핵심 기술 요소로 주목받고 있다.
4. 기술적 제언
아연 함유 산업부산물의 습식 침출 및 금속 회수에 관한 기술은 환경 규제 강화와 자원 순환의 요구에 따라 지속적으로 진화하고 있다. 그러나 아직까지도 ZnFe2O4와 같은 난침출성 구조, 철 이온과의 분리 한계, 비경제적인 전처리 등이 해결되지 않은 과제로 남아있다. 이에 아연 함유 산업부산물의 재활용을 위하여서는 최신 기술을 접목한 지속적인 연구가 필요하다. 이러한 기술들은 물질수지 및 공정분석을 통한 경제성으로 이어져 종합적으로 평가되고 산업적으로 활용되어야 한다. 결국 아연 함유 산업부산물 재활용 기술은 경제성, 환경성 그리고 효율성을 극대화하는 것이 중요하며, 이는 지속 가능한 발전과 순환자원 활용에 크게 기여할 것으로 판단된다.
본 연구에서는 상기 분석한 데이터를 바탕으로 향후 주목할 연구 방향과 기술적 제언을 다음과 같이 정리하며, 전반적인 아연 함유 산업부산물에 대한 자원 순환 체계 구축을 통하여 효율적인 관련 산업의 발전을 촉진하는데 큰 기여를 할 것으로 기대된다.