1. 서 론
2. 실험방법
3. 결과 및 고찰
3.1. MEA의 열분해 특성 및 조성 변화
3.2. 열처리 및 침출 조건에 따른 백금 회수 거동
3.3. 사이클론 전해채취에 의한 백금 회수 및 특성 분석
4. 결 론
1. 서 론
연료전지(Polymer Electrolyte Membrane Fuel Cell, PEMFC)는 청정에너지 전환의 핵심 장치로, 미래 저탄소 사회 구현에 중추적 역할을 담당하고 있다. PEMFC의 촉매 전극(Membrane Electrode Assembly, MEA)은 고가의 백금(Pt) 촉매가 다량 사용되는 구조로 되어 있으나, 운전 중 성능 저하와 수명 한계로 인해 대량의 폐촉매가 발생한다1). 이에 따라, 사용 후 MEA로부터 백금을 고효율로 회수하여 재활용하는 것은 자원 순환 및 경제성, 환경 보전의 측면에서 매우 중요하다.
현재 백금 회수에는 습식 및 건식 제련법이 모두 적용되고 있다. 습식법에서는 폐촉매를 산에 침출하는 방식이 일반적이며, 특히 열처리를 병행한 후 염산 침출을 통해 백금의 회수율을 높이는 연구가 활발하다2,3). 일부 공정에서는 별도의 열처리 없이 왕수를 이용해 백금을 직접 침출하는 사례도 있으나, 강한 산화 환경에 따른 환경·설비 부담이 크고, 후처리 공정이 복잡하다는 단점이 존재한다. 건식제련법은 고온에서 슬라임 형태로 백금을 분리하지만, 에너지 소모 및 환경 부담이 크다.
폐 MEA는 이온전도성 고분자인 나피온(Nafion)과 접착제 등 유기물이 다량 포함되어 있어, 이들 유기물이 침출 반응의 장애물로 작용한다4,5). 실제로 유기물 존재 시 백금 표면 피막 형성, 침출제 소모 증가, 침출액 내 불순물 유입 등으로 침출 효율이 크게 저하된다. 최근 리튬이온 배터리 등 타 전자폐기물의 금속 회수 분야에서도 유기물 사전 제거가 금속 침출율 향상에 결정적 역할을 하는 것으로 밝혀지고 있다6). 따라서 백금 회수 공정에서도 유기물의 효과적 제거는 필수적인 단계라 할 수 있다. 현재까지 상용화된 전처리 공정은 없으나, 연구 단계에서는 폐 연료전지 스택으로부터 MEA를 선별하고 백금 침출 효율을 개선하기 위하여 (1) 나피온 등 유기물 제거를 위한 열처리, (2) 나피온을 선택적으로 용해할 수 있는 화학적 처리, (3) GDL(Gas Diffusion Layer)과 MEA의 물리적 분리 등의 방법이 대표적으로 적용되고 있다.
본 연구에서는 무산소 조건에서의 열분해(thermal decomposition) 전처리를 도입하여, 유기물을 효과적으로 제거한 후 염산 침출을 적용하는 공정을 탐구하였다. 무산소 열분해는 백금의 산화와 불필요한 부반응을 억제하면서도, 나피온 등 유기물을 효율적으로 분해할 수 있는 장점이 있다7). 또한, 저온에서도 처리가 가능하여 에너지 절감 및 CO2 저감 효과도 기대된다. 열분해 후 MEA는 표면이 친수성으로 변환되어, 침출 공정에서 용매와의 접촉 효율 및 교반성이 향상되고, 이에 따라 백금 침출율도 증진된다8).
한편, 백금이 침출된 용액으로부터의 고순도 회수는 자원화의 완결 단계로 매우 중요하다. 이를 위해 본 연구는 사이클론 전해채취(cyclone electrodeposition) 공정을 적용하였다. 사이클론 전해채취는 기존 단순 전해채취에 비해 유체 흐름이 개선되고, 전극 표면에 백금이 더 균일하게 성장하는 특징이 있다9). 본 연구에서는 전해조건을 최적화하여, 침출액 내 백금 이온을 효과적으로 금속 백금으로 환원·회수하였다.
나아가, 이렇게 회수된 백금을 실제 수전해용 전극(hydrogen evolution electrode)으로 제조하고, 상용 백금 전극과의 전기화학적 성능을 직접 비교·평가하였다. 수전해 반응(HER, Hydrogen Evolution Reaction) 실험을 통해, 회수 백금 전극의 촉매 활성, 전류밀도, 내구성 등 주요 특성을 분석하였으며, 실질적인 재자원화 및 친환경 촉매 활용 가능성을 검증하였다.
구체적으로, 본 연구에서는 열중량분석(TGA)을 통해 유기물 분해 및 고정탄소 제거 온도 영역을 규명하였고, 다양한 열처리 조건에서의 백금 침출 효율을 체계적으로 평가하였다. 침출 전후 시료의 미세구조 및 표면 특성 변화는 TEM, XPS, 접촉각 분석 등을 활용해 정밀 분석하였으며, 전해채취된 백금의 물성(SEM, XRD, XPS)과 전기화학적 성능(CV, ECSA 등)도 종합적으로 비교하였다. 이를 통해, 무산소 열분해-습식침출-전해회수-전극 제조로 이어지는 백금 재활용의 전 주기적 최적화 전략을 제시하고자 한다.
2. 실험방법
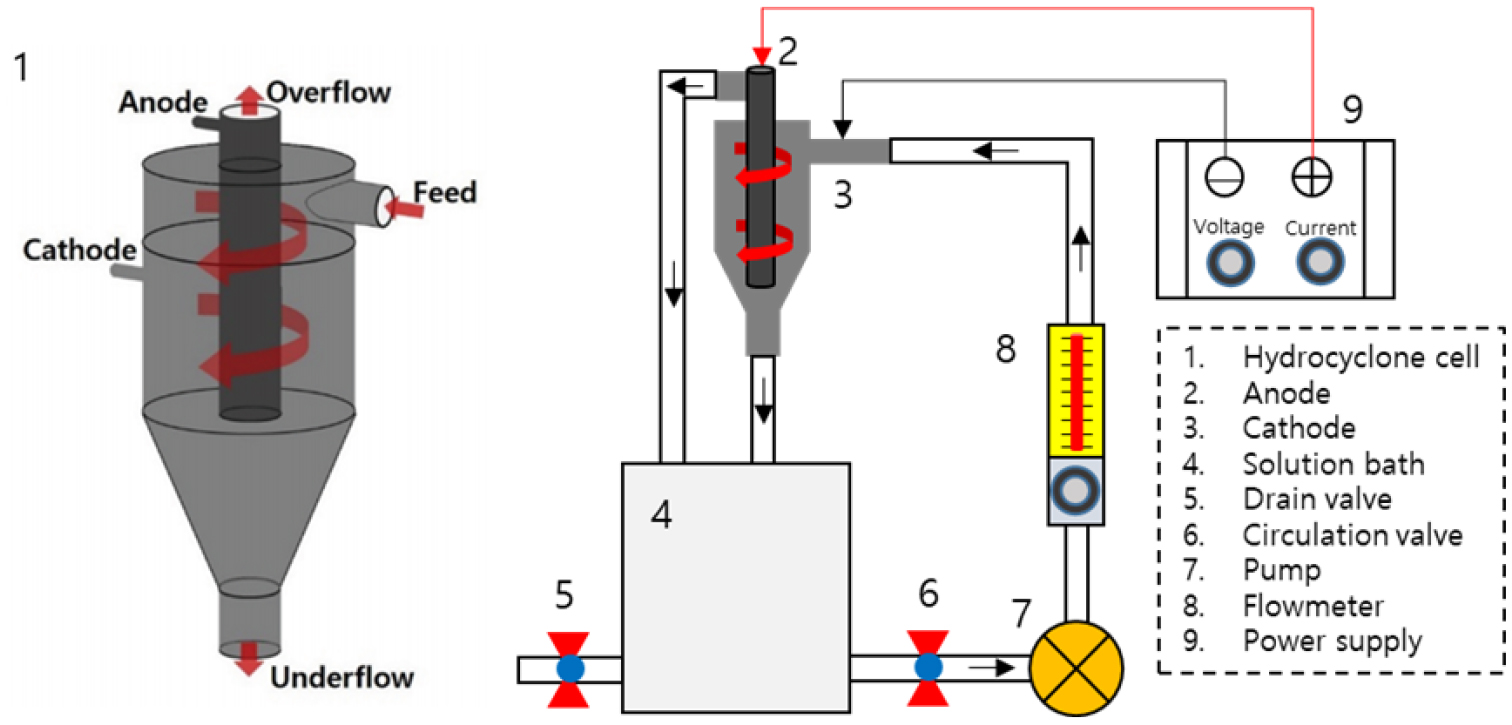
본 연구에 사용된 MEA 시료는 연료전지 제조공정에서 발생한 불량품을 수집하여 이용하였으며, Nafion 멤브레인과 백금 촉매층으로 이루어진 다층 구조를 갖는다. 시료는 실험에 앞서 균질화를 위해 적정 크기로 절단 및 분쇄 과정을 거쳤다. 실험에 사용된 주요 시약은 염산(HCl), 질산(HNO3), 과산화수소(H2O2), 차아염소산나트륨(NaClO) 등으로, 모두 상용 제품을 사용하였다. 시료의 열적 안정성 평가와 유기물 제거 최적 온도 탐색을 위해 열중량분석(TGA, [PerkinElmer TGA 400])을 수행하였으며, TGA 결과에 따라 질소 분위기 하에서 전기로를 이용해 무산소 열분해 열처리(승온속도 10°C/min, 목표온도 1000°C, 유지시간 4시간)를 진행하였다. 열처리된 MEA 시료는 침출 실험에 사용되었으며, 침출은 100 mL 플라스크 반응기에 시료를 투입한 후, 광액농도 2.5~15.0 g/L, 교반속도 150~300 rpm, 염산 농도 4~10 M, 산화제(H2O2, NaClO) 종류 및 농도, 반응 온도 50~90°C 등 다양한 조건에서 항온교반기를 활용하여 수행하였다. 침출 반응이 완료된 후에는 여과를 통해 침출액과 잔사를 분리하였고, 침출액 중 백금 및 기타 금속 함량은 유도결합플라즈마 방출분광분석기(ICP-OES, [Thermo Scientific iCAP 7000 Series])로 정량 분석하였다. 고상 시료의 결정상은 X선 회절분석(XRD, [Rigaku SmartLab SE])으로, 표면 화학상은 X선 광전자분광분석(XPS, [Thermo Fisher Scientific ESCALAB 250 Xi])으로, 나노구조 및 미세표면 형태는 투과전자현미경(TEM, [Hitachi HT7700])을 통해 각각 분석하였다. 한편, 침출액으로부터 백금을 회수하기 위해 자체 설계한 사이클론 전해조(Fig. 1)를 이용하였고, 전해조건은 유량 5 L/min 및 10 L/min, 전류 3.9 A, 전해시간 180분으로 고정하였다. 전해 종료 후 전극에 석출된 백금 고상은 세척·건조 후 특성 분석과 촉매 성능 평가에 사용하였다. 전기화학적 성능 평가는 수소 발생 반응(HER) 조건에서 3전극 셀로 실시하였으며, 작동전극으로는 Rotating Disk Electrode(glassy carbon, active area 0.2 cm2), 상대전극으로 graphite rod, 기준전극으로 Hg/HgO(1 M KOH)을 사용하였다. 촉매 잉크는 회수 백금(20 mg), 에탄올(900 μL), 5 wt% Nafion 용액(100 μL)을 혼합하여 15분간 초음파 분산한 후, 5 μL를 작동 전극 표면에 1회 드롭 후 건조하여 사용하였다. 실험 전 RDE를 1600 rpm으로 회전시켜 용존 산소를 충분히 제거하였으며, 전해질로는 N2로 퍼지된 1 M KOH 용액을 사용하였다. 모든 전기화학 실험은 cyclic voltammetry(scan rate 5 mV/s)로 수행하였고, 측정 결과를 바탕으로 백금 촉매의 전기화학적 활성과 수소발생 반응 특성을 평가하였다.
3. 결과 및 고찰
3.1. MEA의 열분해 특성 및 조성 변화
본 연구에서는 연료전지 MEA 시료를 대상으로 무산소 열분해, 산 침출, 전해회수 및 재자원화에 이르는 일련의 공정을 설계하고, 각 단계별 공정 조건과 물질 특성 변화가 백금 회수 효율 및 촉매 재활용 가능성에 미치는 영향을 체계적으로 분석하였다. 특히, 열처리(무산소 열분해) 단계에서 MEA 내 유기성분 및 탄소질의 제거 특성을 규명하고, 이후 침출 거동 및 회수 백금의 물성 변화와 전기화학적 성능 평가에 이르기까지 전체 공정 흐름을 순차적으로 검토하였다.
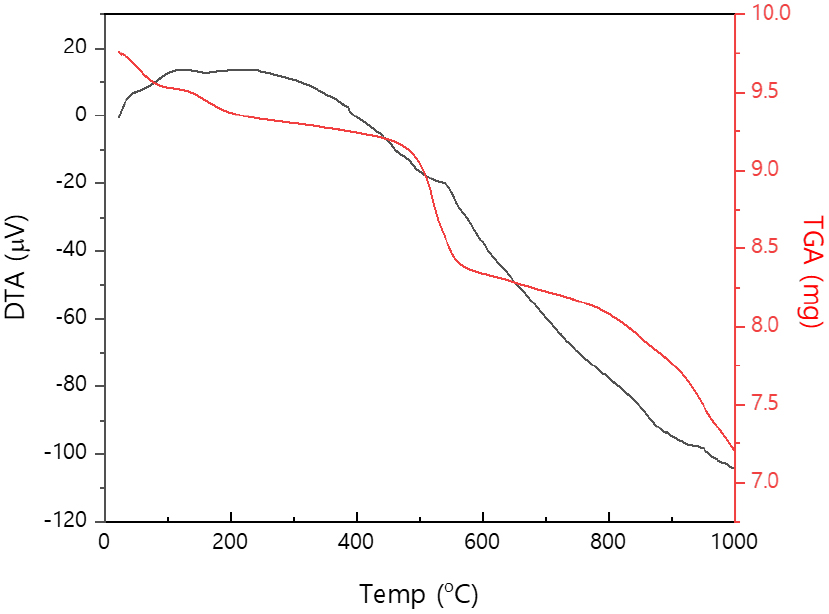
먼저, MEA 시료의 열분해 특성을 정량적으로 분석하기 위하여 TGA(열중량분석) 및 DTA(미분열분석)를 실시하였다(Fig. 2). Fig. 2는 아르곤 가스 분위기(무산소 조건)에서 승온하며 측정한 TGA 및 DTA 결과를 보여준다. 시료의 조성은 수분 3.54%, 휘발성분 10.95%, 회분 23.84%, 고정탄소 61.67%로 분석되었으며, 발열량은 5655 cal/g로 나타났다. TGA 곡선(적색선)에 따르면, 100°C 이하에서 시료 내 잔류 수분 증발로 인한 소폭의 무게 감소가 나타나고, 200~400°C 구간에서는 휘발성 유기물이 분해되어 추가적인 중량 감소가 진행된다. 특히, 500~550°C 부근에서 시료의 무게 변화가 매우 뚜렷하게 관찰되어, 이 영역에서 나피온, 접착제 등 주요 유기물질이 열분해를 통해 효과적으로 제거되는 것으로 해석된다8,10). 600°C 이상에서는 고정탄소의 점진적 분해가 진행되며, 800~900°C 이후에는 주로 무기물(백금, 회분 등)만이 잔류하게 된다. DTA 곡선(흑색선) 역시 500~600°C에서 뚜렷한 발열 피크가 관찰되어, 이 구간에서 주요 분해 반응이 집중적으로 일어남을 시사한다.
이와 같은 TGA/DTA 분석 결과를 바탕으로, 무산소 분위기에서 500~600°C 이상에서의 열분해가 MEA 내 유기물 및 고정탄소 성분을 효과적으로 제거하는 데 적정 조건임을 확인하였다. 이러한 최적 열처리 구간의 도출은 이후 백금 침출 실험에서 전처리 조건 선정의 근거가 되었으며, 전체 공정의 효율 및 백금 회수율을 극대화하는 데 중요한 기초 자료로 활용되었다.
3.2. 열처리 및 침출 조건에 따른 백금 회수 거동
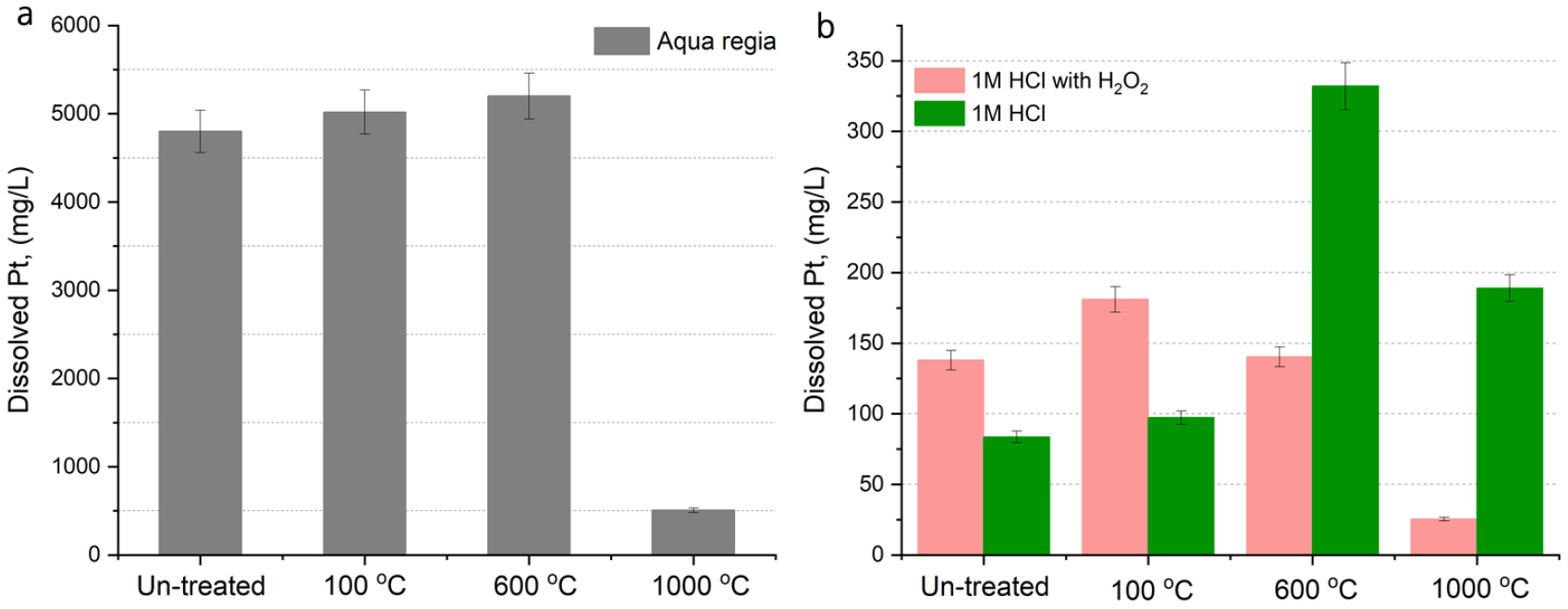
Fig. 3은 MEA 시료를 다양한 열처리 온도(무처리, 100°C, 600°C, 1000°C)에서 처리한 뒤, 서로 다른 침출 조건에서의 백금 용출량을 정량적으로 비교한 결과이다.
Fig. 3(a) 그래프는 각 열처리 시료를 왕수(aqua regia, HCl:HNO3=3:1, v/v)로 상온에서 3시간 동안 침출하여 백금 용해량을 측정한 결과를 나타낸다. 무처리, 100°C, 600°C 조건에서는 각각 4800, 5020, 5200 mg/kg 수준의 백금이 침출되어, 열처리 온도가 증가할수록 소폭의 증가 경향이 관찰되었다. 그러나 1000°C에서 열처리한 시료는 백금 침출량이 508 mg/kg으로 현저하게 감소하였다. 이러한 결과는 고온 열처리 과정에서 Pt가 안정한 산화물 상(PtO 또는 PtO2)으로 전환되어 왕수에 대한 용해성이 급격히 저하된 데 기인한다. 특히 백금 산화물은 열역학적으로 안정하여, 왕수 조건에서도 쉽게 용해되지 않는 것으로 보고된 바 있다11). 비록 본 연구의 열처리가 무산소(Ar) 분위기에서 진행되었으나, MEA 내 나피온 및 접착제와 같은 고분자 유기물의 분해 과정에서 –SO3H, -CF2, -COOH 등 산소를 함유한 관능기가 분해되며 CO2, H2O, SO2와 같은 산화성 기체가 발생한다. 다음 식 (1), (2), (3), (4)과 같이 산화성 종이 Pt와 반응하여 PtOx 상을 형성한 것으로 판단된다.
Fig. 3(b) 그래프는 동일한 열처리 조건에서, 1 M 염산+과산화수소(H2O2), 그리고 1 M 염산 단독을 이용해 침출을 실시한 결과이다. 두 조건 모두 왕수를 사용했을 때보다 침출된 백금의 양이 훨씬 적었으며, 1 M 염산만 사용한 경우 특히 600°C 이상 열처리된 시료에서 백금 침출량이 상대적으로 크게 증가하는 현상이 관찰되었다(600°C, 약 320 mg/kg). 반면, 1000°C 이상 열처리에서는 두 조건 모두에서 침출량이 크게 감소했다. 이는 고온 열처리에 의해 Pt가 결정성 산화물로 전환되고, 일반적인 산 침출 조건에서는 용해성이 급격히 저하되기 때문으로 해석된다12). 또한, 모든 조건에서 왕수 침출 시 약 5000 mg/kg 수준의 백금이 용해된 반면, 1 M 염산 침출에서는 약 300 mg/kg 내외로 큰 차이를 보였다. 왕수는 HCl 단독 용액 대비 Pt 침출에 효과적인데, 이는 (i) 높은 Cl- 농도로 인해 [PtCl6]2-와 같은 안정한 염화착이온 형성이 용이하며, (ii) HNO3로부터 생성되는 NOCl, Cl2 등 강력한 산화종이 Pt를 고차 산화 상태로 전환시키기 때문이다. 따라서 Pt의 용해는 단순한 Cl- 농도의 영향이 아니라, 강한 산화제의 존재와 염화 착이온 안정화 효과가 상호 작용한 결과라 할 수 있다.
결과적으로, 600°C 이하의 적정 온도에서 열처리하면 MEA 내 백금의 침출성이 유지되거나 오히려 증가할 수 있으나, 과도한 고온 열처리는 백금의 화학적 불용화를 초래하여 침출 효율을 크게 저해함을 알 수 있다.
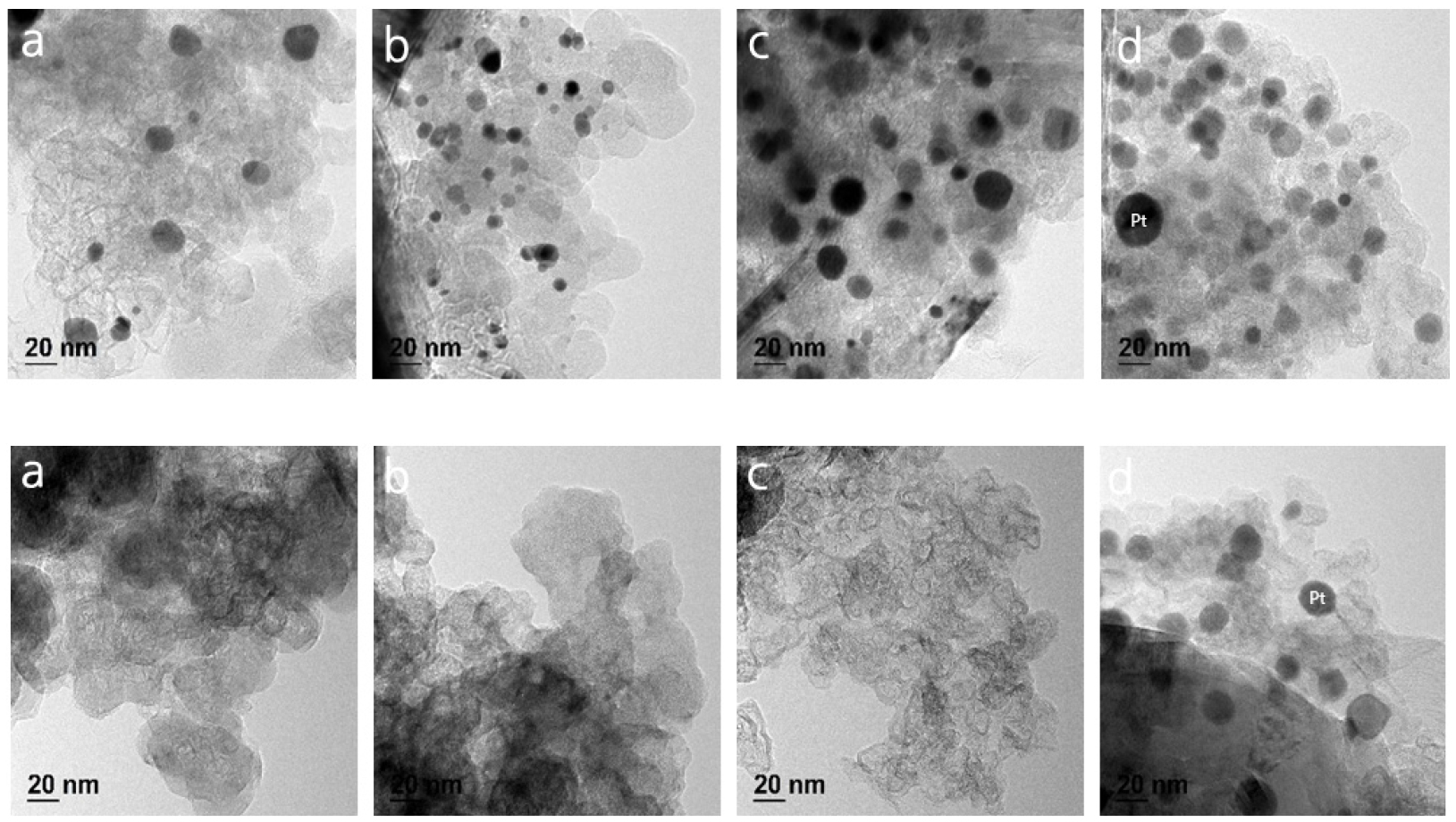
Fig. 4는 왕수 침출 전후, 서로 다른 열처리 조건(무처리, 100°C, 600°C, 1000°C)에서 준비된 MEA 시료의 TEM 이미지를 비교한 결과이다. 침출 전(상단 a~d)에서는 모든 조건에서 백금(Pt) 입자가 명확하게 관찰되고, 일부 고온 시료에서는 입자 크기의 성장과 응집이 확인된다. 침출 후(하단 a~d)에서는 무처리, 100°C, 600°C 조건에서 백금 입자가 거의 소실되어 효과적으로 침출이 이루어진 반면, 1000°C 열처리 시료에서는 백금 입자가 여전히 시료 내에 뚜렷하게 잔존함을 확인할 수 있다.
이러한 현상은 열처리 온도에 따른 백금의 산화 상태 변화, 그리고 각 산화물의 침출 반응의 자발성에 직접적으로 기인한다. 금속 백금(Pt)이 염산과 산화제(예: 산소)와 반응하는 경우, 다음 식 (5) 같은 침출 반응이 일어나며 ΔG°는 -184 kJ/mol로 매우 자발적이다.
고온 열처리 과정에서 Pt가 일가 산화물(PtO)로 전환될 수 있으며, 이 경우도 염산과 다음 식 (6)와 같은 반응을 한다.
ΔG°가 음수로, 이 반응 또한 열역학적으로 자발적이다. 실제로 PtO 형태라면 침출 과정에서 PtCl2로 쉽게 용해되므로 백금이 시료 내에 남아 있지 않아야 한다. 그러나, 본 연구에서는 1000°C에서 열처리한 시료에서 침출 후에도 백금이 잔존하는 현상이 뚜렷하게 관찰되었다.
이는 고온 열처리 과정에서 백금이 일가 산화물(PtO)이 아닌, 더 안정한 이산화백금(PtO2) 형태로 주로 존재하게 됨을 시사한다. PtO2의 경우, 염산과의 침출 반응은 아래 식 (7)과 같으며 ΔG°는 +32 kJ/mol로 양수이다.
이처럼 ΔG°가 양수인 비자발적 반응에서는, 실제로 침출이 거의 일어나지 않는다. 따라서, 1000°C 이상 고온 열처리된 시료에서 백금이 침출 후에도 구조 내에 잔존하는 현상은, 백금이 PtO2 형태로 존재하기 때문임을 열역학적으로도 뒷받침할 수 있다. 즉, PtO라면 자발적으로 침출되어 잔류하지 않아야 하므로, 실제로 남는 백금의 화학적 형태는 PtO2임을 TEM 관찰과 열역학 계산 모두에서 일관되게 확인하였다.
결론적으로, 고온(1000°C)에서 열처리된 MEA 시료에서 침출 후에도 백금이 남아 있는 이유는, 열분해 과정에서 백금이 PtO2(이산화백금)로 전환되어, 이 화합물이 염산 침출 반응에서 열역학적으로 비자발적(ΔG° > 0)이기 때문임을 알 수 있다13). 따라서 백금 회수 공정의 효율 향상을 위해서는 지나친 고온 열처리를 피하고, 백금이 침출 가능한 금속 상태 또는 PtO 형태로 존재하도록 공정조건을 최적화하는 것이 매우 중요하다.
Fig. 5는 600°C에서 열처리한 MEA 시료를 대상으로, 다양한 침출 변수에 따른 백금 침출율(LE, %)과 용해량(mg/kg)의 변화를 정량적으로 비교한 결과이다. Fig. 5(a) 교반속도(150, 250, 300 rpm) 변화에 따른 실험에서, 250 rpm에서 가장 높은 침출율(약 71%)과 4800 mg/kg 수준의 백금 용해량이 관찰되었다. 이는 교반이 너무 약할 경우 용액 내 확산 저해, 너무 강할 경우 입자 재침전이나 교반에 의한 실질적 유효반응면적 감소가 발생할 수 있음을 시사한다. Fig. 5(b) 광액농도(2.5, 5.0, 7.5, 10.0, 15.0 g/L)별 시간에 따른 침출율 변화를 보면, 대부분의 농도에서 침출 초기(특히 100~200분 사이)에 가장 높은 침출율을 보인 뒤, 시간이 지날수록 점진적으로 감소하는 경향이 나타났다. 이는 침출 초기에 표면 노출 Pt가 빠르게 용출되고, 시간이 지남에 따라 용액 내 Pt 농도 포화, 표면 피막 형성, 미세구조 변화 등으로 침출 속도가 저하되기 때문이다. 특이하게 5 g/L 조건에서는 시간 경과에 따라 침출율이 점차 증가하는 경향이 확인되었다. 이는 5 g/L가 침출제와 고형분의 균형이 가장 적절하여, 확산 또는 표면 반응 지연 없이 꾸준히 Pt 용출이 지속적으로 진행될 수 있음을 의미한다.
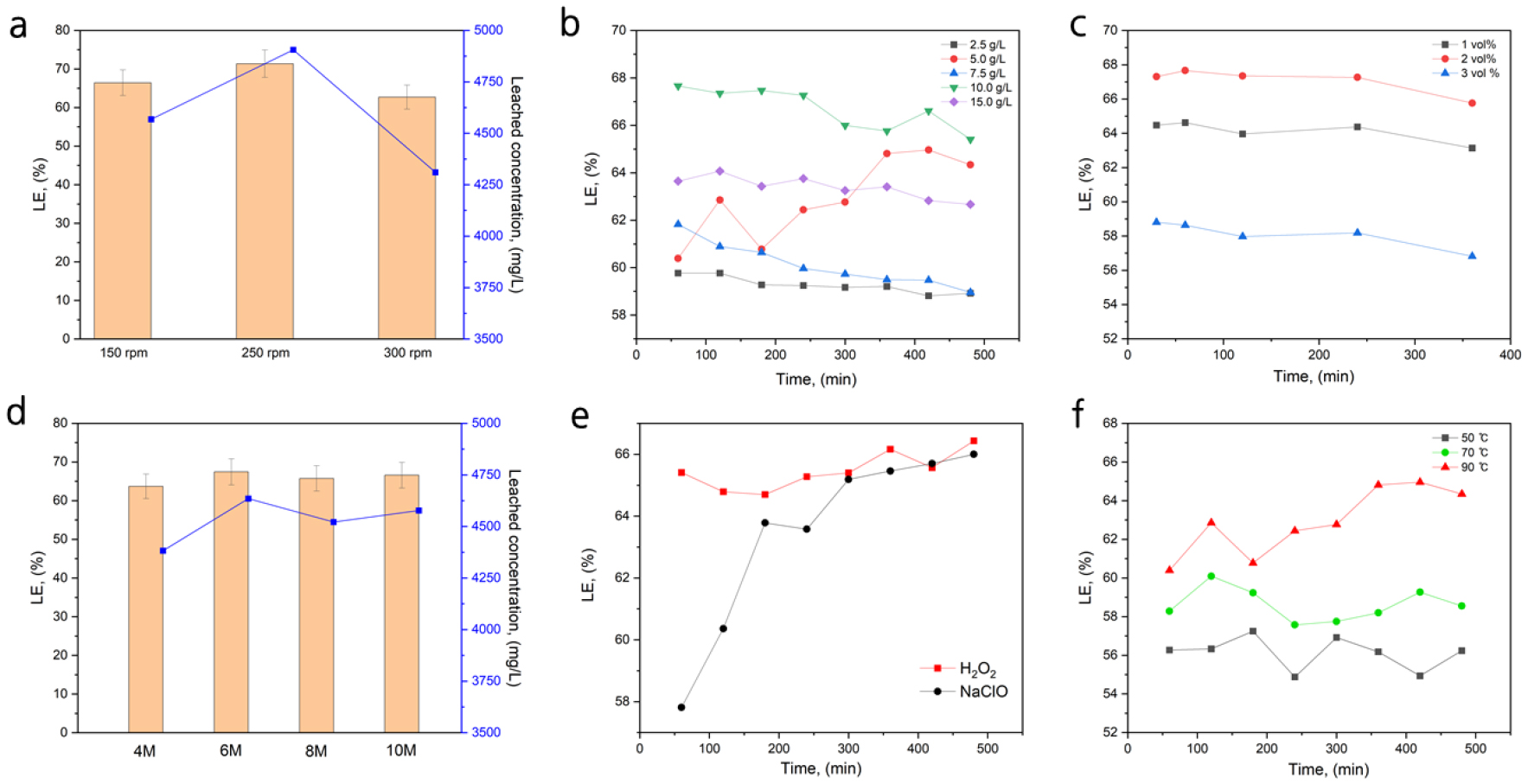
Fig. 5.
Platinum leaching efficiency and dissolution behavior of MEA heat-treated at 600°C under different leaching variables: (a) effect of stirring speed, (b) effect of pulp density, (c) effect of H2O2 concentration, (d) effect of HCl concentration, (e) effect of oxidant type, and (f) effect of temperature.
반면, 2.5 g/L 이하의 저농도에서는 초기 반응성이 빠르나 금속 총량이 적고, 10 g/L 이상 고농도에서는 확산 장벽 및 포화 효과로 인해 오히려 침출율이 감소하는 특성이 관찰된다. Fig. 5(c) 산화제(H2O2) 농도(1, 2, 3 vol%) 실험에서는, 2 vol%에서 약 67%의 침출율로 가장 우수한 결과를 보였다. 1 vol%에서는 64%, 3 vol%에서는 오히려 58%로, 산화제 농도가 과도할 경우 불필요한 산화종 생성이나 용액 내 Pt 이온의 재침전 등 부반응으로 침출 효율이 저해될 수 있음을 시사한다. 시간 경과에 따른 침출율 변화는 크지 않았다.
Fig. 5(d) 염산 농도(4, 6, 8, 10 M)별 실험 결과, 전반적으로 65% 이상의 높은 침출율을 보였으며, 6 M 조건에서 약 4752 mg/kg의 백금이 용해되어 가장 효율적인 결과를 나타냈다. Fig. 5(e) 산화제 종류에 따른 실험에서는, 과산화수소(H2O2)는 반응 초기부터 64% 이상의 침출율을 보이며 시간이 지날수록 꾸준히 상승, 8시간 시점에서 약 68%의 침출율에 도달하였다.
반면, 차아염소산나트륨(NaClO)은 초기 침출율이 58%로 낮았으나, 시간이 경과하면서 점차 증가하여 최종적으로 H2O2와 비슷한 수준의 침출율을 나타내었다. 이는 산성(HCl) 조건에서 H2O2는 표준환원전위(E° = +1.77 V) 자체가 매우 높고, 동시에 H2O2 + 2HCl → Cl2 반응으로 Cl2(E° = +1.36 V)를 빠르게 생성하므로 초기 산화 용해 속도가 크다. 반면, NaClO는 염기성 용액으로 도입되어 초기 중화 및 HOCl/Cl2 전환 평형에 시간이 소요되고, 유기물에 의한 산화제 소모가 비교적 느리게 진행되어 산화력이 장기적으로 지속되는 경향을 보인다. 그 결과, 초기 침출율은 H2O2 > NaClO이나, 시간이 경과함에 따라 NaClO 조건에서도 Cl2/HOCl 생성과 Cl- 과잉에 의한 [PtCl6]2- 안정화가 충분히 확보되어 최종 침출율이 H2O2 조건과 유사한 수준으로 수렴한다.
Fig. 5(f) 온도(50, 70, 90°C) 변수 실험에서는, 반응 온도가 높아질수록 침출율이 뚜렷하게 증가하였다. 90°C 조건에서 약 7시간 반응 시 65% 이상의 침출율이 확인되었으며, 이는 온도 상승에 따른 반응 속도 향상과 Pt 표면 활성화 증가에 기인한다.
이상의 결과를 종합하면, 600°C 열처리 MEA의 백금 침출에서는 교반속도 250 rpm, 광액농도 5 g/L, 산화제 농도 2 vol%, 염산 6 M, H2O2 사용, 반응 온도 90°C 등이 침출 효율 향상에 가장 효과적임을 알 수 있다. 또한, 광액농도 및 산화제 농도 등 세부 변수에 따라 침출 초기와 후기의 거동이 다르게 나타나므로, 공정 설계 시 이를 반드시 고려해야 함을 시사한다.
3.3. 사이클론 전해채취에 의한 백금 회수 및 특성 분석
최적 조건에서 MEA를 침출하여 얻은 백금 침출액으로부터 귀금속을 효과적으로 회수하기 위해 사이클론 전해채취 공정을 적용하였다14). 사이클론 전해조는 일반적인 정전기적 전해채취나 화학적 침전법 대비, 특히 수십~수백 ppm 수준의 저농도 금속 용액에서 뛰어난 회수 효율을 보인다15,16). 이는 저농도 조건에서는 금속 이온의 농도분극(concentration polarization)이 전극 표면에서 빠르게 발생하여, 일반 전해공정만으로는 금속 회수가 제한적이지만, 사이클론 전해채취는 내부에서 형성되는 강한 난류 및 지속적 유동을 통해 용액과 전극 사이의 농도분극을 효과적으로 완화함으로써, 보다 낮은 농도까지도 금속 이온의 전기화학적 환원을 촉진할 수 있기 때문이다17).
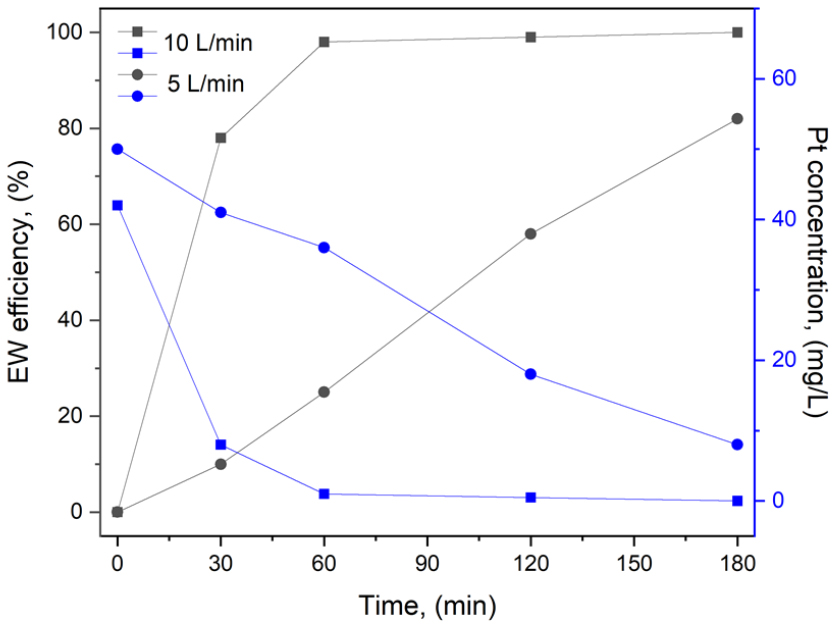
실험은 정전류 3.9 A 조건에서 수행되었으며, 유량을 5 L/min과 10 L/min으로 변화시키며 회수 효율의 변화를 비교하였다. 5 L/min 조건에서는 전해 시작 30분에 약 10%의 백금 회수율을 보이며 점차 증가하여, 180분 반응 후 약 81%까지 회수 효율이 상승하는 경향을 나타내었다. 반면, 10 L/min 조건에서는 30분 시점에서 이미 약 79%의 높은 회수 효율을 기록하였고, 이후 시간이 증가할수록 백금이 급격히 회수되어 120분 이내에 대부분의 백금이 전해채취되는 결과를 확인하였다(Fig. 6).
동시에 용액 내 백금 농도는 반응 시간이 경과함에 따라 급격히 감소하였으며, 특히 유량이 높은 조건에서 더욱 빠른 농도 감소가 이루어졌다. 이러한 결과는 사이클론 전해채취 공정의 난류 생성 및 빠른 유체 순환이 전극 표면의 농도분극을 실질적으로 낮추고, 저농도 용액에서도 백금을 효과적으로 회수할 수 있음을 뒷받침한다. 따라서 본 공정은 귀금속의 극저농도 회수가 요구되는 친환경 자원순환 및 배출수 처리 분야 등에서 매우 효과적인 회수 기술로 활용될 수 있음을 보여준다.
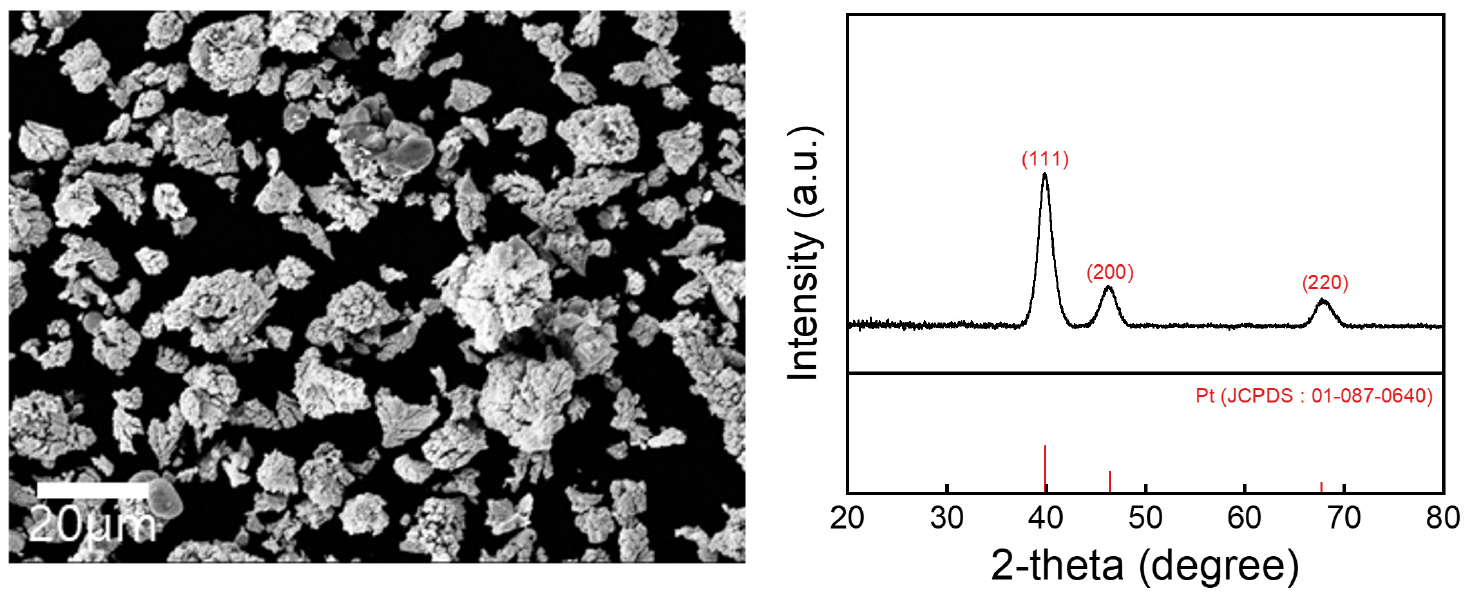
사이클론 전해채취를 통해 회수한 백금의 특성은 SEM 및 XRD 분석을 통해 평가하였다. Fig. 7 좌측의 SEM 이미지는 전해 후 전극 표면에 전착된 백금의 미세구조를 보여주며, 전형적인 입상 형태의 백금 입자들이 균일하게 분포하고 있음을 확인할 수 있다. Fig. 7 우측의 XRD 결과에서는 회수된 시료에서 백금(Pt)의 결정 피크가 뚜렷하게 나타나며, 이는 JCPDS(01-087-0640)와의 비교를 통해 표준 백금 금속의 결정 구조와 잘 일치함을 알 수 있다. 이로써 사이클론 전해채취 공정을 통해 고순도의 결정성 금속 백금이 효과적으로 회수되었음을 확인하였다.
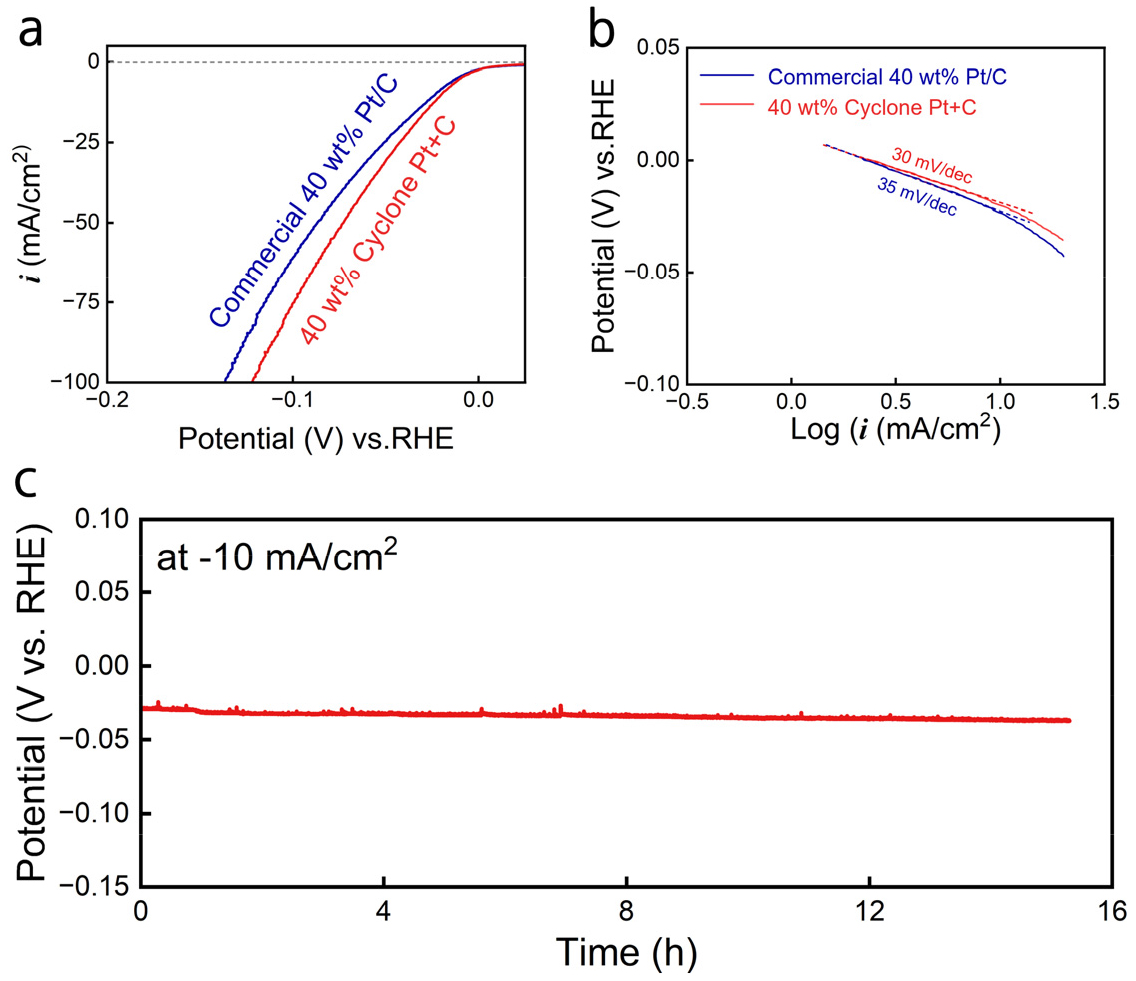
사이클론 전해채취를 통해 회수된 백금을 사용하여 수전해용 전극을 제작한 후, 상용 Pt/C(40 wt%:60 wt%) 촉매와의 수소 발생 반응(HER) 성능 및 내구성 평가를 수행하였다. 두 시료 모두 동일한 조건에서 3전극 셀을 구성하여 측정하였으며, 작동 전극은 glassy carbon RDE(active area: 0.2 cm2), 상대전극은 graphite rod, 기준전극은 Hg/HgO(1 M KOH)로 설정하였다. 전해질로는 N2로 퍼징된 1 M KOH를 사용하였고, RDE는 1600 rpm으로 회전시키며 실험을 진행하였다. Fig. 8(a)와 (b)의 전기화학적 성능 평가는 Cyclic voltammetry(scan rate: 5 mV/s)로 측정하였고, Fig. 8(c)의 내구성 평가는 -10 mA/cm2의 일정한 전류를 인가하며 시간에 따른 전압 변화를 분석하였다.
실험 결과, 사이클론 전해채취로 제조된 Pt 전극은 10 mA/cm2에서 30 mV의 과전압(overpotential)을 나타내어, 상용 Pt/C(35 mV) 전극보다 더 우수한 수소 발생 반응(HER) 촉매 활성을 보였다. 이는 동일 조건(1 M KOH, RDE 1600 rpm, 3전극 셀)에서 측정된 값으로, 사이클론 전해 후 제조된 Pt 전극이 실질적으로 상용 촉매를 대체할 수 있는 충분한 성능을 갖추었음을 의미한다18). 또한 Tafel slope 분석 결과, Cyclone Pt 전극의 Tafel slope가 상용 제품 대비 낮게 나타나, 수소 발생 반응에서의 전기화학적 반응 속도(kinetic)가 더욱 빠르고 효율적으로 진행됨을 확인할 수 있었다. 이는 전극 표면의 촉매 활성점 노출이 충분하고, 회수·재활용된 백금이 고유의 촉매 활성을 효과적으로 유지하고 있음을 시사한다19).
내구성 평가에서도 사이클론 전해 제조 Pt 전극의 성능이 입증되었다. Fig. 8(c)에서 나타냈듯이 -10 mA/cm²의 일정 전류 조건에서 15시간 연속 동작 시, 전극의 전압 변화가 매우 미미하게 유지되어 전기화학적 안정성이 뛰어난 것으로 확인되었으며, 초기 성능 저하나 전기화학적 분해 현상 등도 관찰되지 않았다.
이러한 결과는, 본 연구에서 제안한 사이클론 전해채취 기반의 백금 회수 및 재자원화 공정이 수전해용 고성능·고내구성 촉매 전극 제조에 실질적으로 적용될 수 있음을 강하게 시사한다. 더불어, 폐 MEA 등 백금 함유 폐촉매의 재활용을 통한 자원순환 및 경제적·환경적 효과까지 함께 달성할 수 있는 친환경 기술로서의 활용 가능성도 높음을 보여준다.
4. 결 론
본 연구에서는 연료전지 폐촉매(MEA)로부터 백금의 효율적 회수 및 재활용을 위한 통합 공정 개발과 그 효과를 실험적으로 규명하였다. 무산소 열분해를 통해 600°C 전처리 시 MEA 내 유기물이 효과적으로 제거되었으며, 침출 실험에서 백금이 높은 효율로 용출됨을 확인하였다. 과도한 고온(1000°C) 열처리에서는 백금이 PtO2로 안정화되어, 침출 반응의 열역학적 자발성이 크게 저하되고 실제 침출 효율이 급감하는 한계도 함께 규명하였다.
침출액 내 저농도 백금 회수를 위해 적용한 사이클론 전해채취 공정은, 단일 공정에서 난류와 빠른 용액 흐름을 바탕으로, 농도분극 완화 및 극저농도까지의 효율적 백금 회수를 실현할 수 있음을 입증하였다. 회수된 백금은 고순도의 결정성 금속 상태로 확인되었으며, 이를 이용해 제작된 수전해 촉매 전극은 상용 Pt/C 대비 더 낮은 과전압, 더 작은 Tafel slope, 우수한 장시간 내구성을 나타내어 실용적 재자원화 가능성을 높였다.
종합적으로, 본 연구에서 제안한 무산소 열분해-침출-전해회수-전극 제조로 이어지는 통합 공정은, 폐 연료전지 MEA의 고부가가치 백금 회수와 그 실질적 활용의 전 과정을 아우르는 실용적 자원순환 기술임을 실험적으로 입증하였다. 향후 귀금속 및 다양한 폐촉매 재자원화 분야에서 본 공정이 널리 활용될 것으로 기대된다.