1. 서 론
2. 실리콘의 생산량과 용도
3. 금속 실리콘의 제련
4. 금속 실리콘의 정제
4.1. 화학적인 방법
4.2. 야금학적 방법
5. 실리콘의 용융과 반도체용 실리콘의 제조
6. 종 합
1. 서 론
실리콘(규소, Si)의 지각 중 원소 존재도는 28.2 %로 산소의 46.1 %에 두 번째로 풍부한 자원이며1), 1787년 라부아지에(Antoine-Laurent de Lavoisier)가 처음으로 원소로 나타내었으나, 당시에는 수석(부싯돌, flint) 자체를 원소로 생각하였다. 결정질 Si은 1854년에 Henri Sainte-Claire Deville에 의해 만들어졌다2). 현재는 고온의 전기로에서 소모형 탄소 전극을 사용하여 금속 Si을 만들고 있으며, 실리콘(silicon)이라는 명칭은 1817년 톰슨(Thomas Thomson)이 부싯돌의 라틴어 silex에 이 새로운 원소가 금속과는 다르고 붕소(boron), 탄소(carbon)와 성질이 비슷하여 어미로 ‘on’을 붙여 명명하였다3).
Si은 천이금속으로 액체의 밀도가 2.55 g/cm3으로 고체(2.33 g/cm3) 보다 큰 특징이 있다. 또 반도체로서 Ge과 유사한 성질을 갖고 있으나, 순수한 Si의 전기 저항은 2.3×103 Ω·m으로 Ge(1 Ω·m) 보다 현저히 높은 값을 갖고 있다. 금속 Si은 물론 페로실리콘(Fe-Si)은 취성이 높아 구조용 재료로는 거의 용도가 없으나, 금속 Si(페로실리콘 포함)은 주로 제강공정의 탈산제로 사용되고 있으며, 비철금속의 주요한 합금원소로서 널리 사용되고 있다. 그리고 Si은 반도체로서의 성질이 발견되고, 고순도 Si의 제조법이 발달되어 현대 산업의 중요한 재료가 되었다. 특히 태양 전지의 대부분은 다결정이나 단결정 금속 Si을 사용하고 있다. 최근에는 리튬이온 이차전지의 차세대 음극재로서도 각광을 받고 있다. 따라서 본 논문에서는 이러한 Si의 생산량과 용도, 그리고 실리콘의 제련법과 태양전지용이나 반도체용으로 정련하는 기술에 대하여 고찰하였다.
2. 실리콘의 생산량과 용도
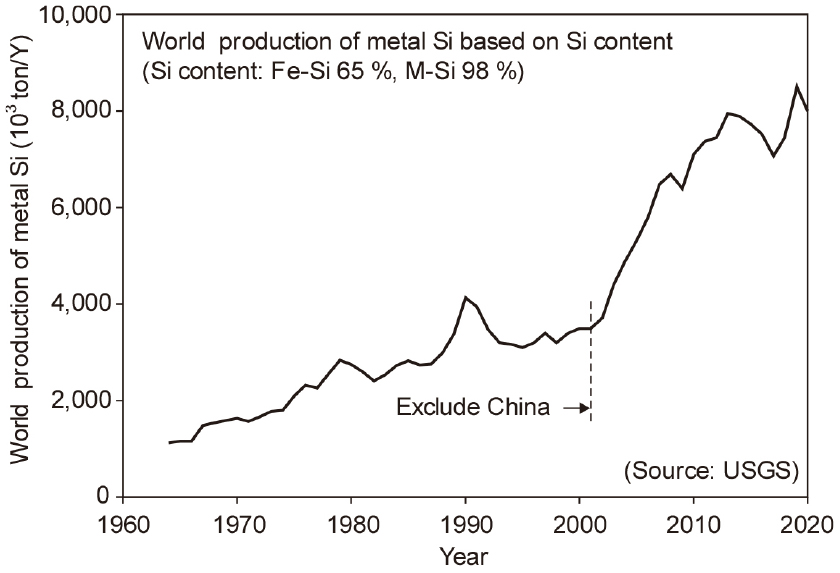
Fig. 1에는 Si 함유량 기준의(금속 Si: 98 %Si, 페로실리콘: 65 %Si 기준) 전 세계의 금속 Si 생산량 변화를 나타내었으며4), 현재 연간 약 800만 톤의 금속 Si이 생산되고 있다. 2000년대부터 중국의 생산량이 포함되면서 전 세계의 금속 Si 생산량이 급격하게 늘어나는 것을 알 수 있으며, 이러한 변화는 중국의 철강 생산량 급증에 따른 페로실리콘 생산량 증대 및 Al 생산량 증대5)에 따른 합금용 금속 Si 사용량 증대에 따른 것으로 생각된다.
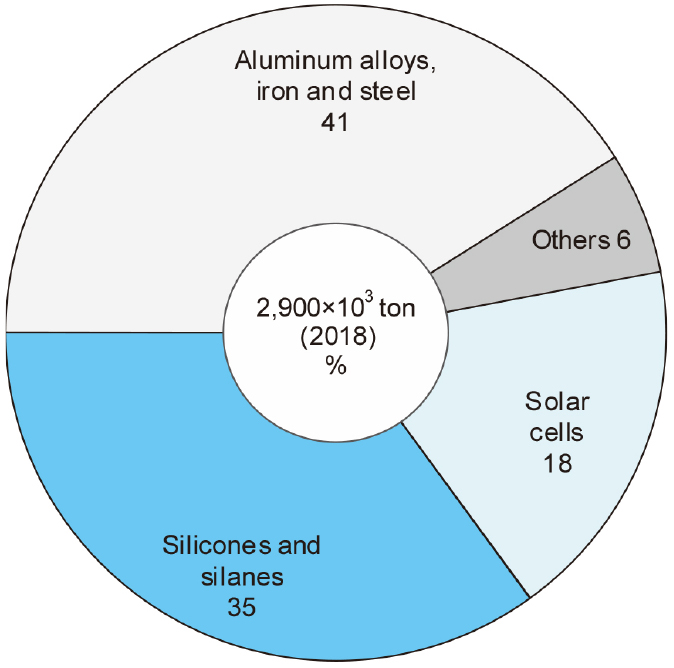
Fig. 2에는 페로실리콘을 제외한 2018년도 금속 Si의 주요한 용도를 나타내었다6). 약 250만 톤의 금속 Si이 생산되었고, 알루미늄 합금용(41 %)으로 가장 많이 사용되었으며, 그 외 화학 제품용(35 %) 및 태양 전지용(18 %) 등으로 사용되었다. 이러한 금속 Si의 용도는 태양 전지용을 제외하면 향후에도 큰 변화는 없을 것으로 생각되지만, Al 합금이나 화학 제품용 등의 증가에 의해 년간 4~5 % 정도 성장할 것으로 추산하고 있다6). 따라서 Si의 리사이클링 관점에서는 태양전지용과 반도체용으로 사용된 것을 고려할 수 있으나, 실질적으로는 Si의 제조공정이나 웨이퍼를 절삭하는 과정에서 발생하는 분말(슬러지 포함)의 리사이클링이 중요할 것이다.
3. 금속 실리콘의 제련
Si은 주로 산화물이나 규산염의 형태로 존재하고 있다. 일반적으로 금속 규소나 공업용 실리콘으로 불리는 것은 산화물을 탄소로 환원하여 얻어진 것이며, 이것을 정제, 용융하여 태양전지용 및 반도체용 Si을 비롯하여 다양한 제품으로 만든다. 금속 Si은 최종 용도와 관계없이 규석을 탄소 열환원하여 만들고 있으며, 총괄 반응식은 다음과 같다.
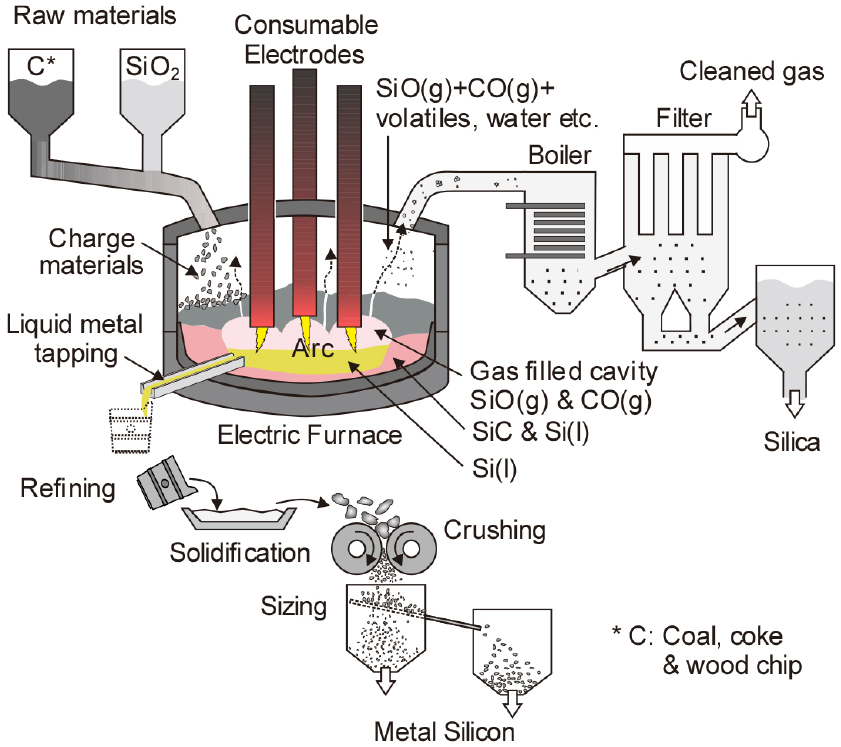
이 총괄 반응은 흡열반응이지만, 전기로 내의 위치에 따라 온도가 다르므로 여러 가지 반응들이 일어난다. Fig. 3에는 전기로를 이용한 금속 실리콘 제조 공정도를 나타내었다7).
규석(SiO2 99 % 이상)과 환원제인 고순도 코크스를 혼합하여 3개의 소모형 탄소 전극을 갖는 전기로 중에서 고온으로 가열한다. 특히 환원제는 B, P 등의 불순물이 적어야 한다. 환원된 금속 Si의 순도는 97~99 %이며, Al, Cu, Ni 등의 합금용으로는 이 상태로 사용된다. 환원 반응 중에 발생한 SiO(g) 흄은 실리카로 회수되며, 내화물 재료 등으로 판매되고 있다.
금속 Si은 약 2,000 K 이상에서 C으로 환원하지만, 온도가 낮은 부분에서 SiC가 생성된다8).
전극 선단부는 약 2,400 K의 고온이므로 C에 의해 SiO2가 환원되지 못하고 SiO(g)를 생성한다.
그리고 전극 주변부는 상기한 반응의 생성물인 SiO(g), CO(g) 등에 의해 공극(cavity)을 형성하고 있으며, 고온에서 아래 식과 같이 SiC가 SiO2, SiO(g)와 반응하여 금속 Si이 만들어진다.
총괄적으로는 식 (1)과 같은 환원반응에 의해 금속 Si이 만들어진다.
한편 Fe가 존재하면 페로실리콘이 만들어지며,
SiC가 있으면 Fe와 다음과 같이 반응하여 페로실리콘이 만들어진다.
Si/SiO2 평형보다 산소 친화력이 낮은 B, P, Fe 등은 노 내에서 환원되어 Si 중으로 들어가며, 산소 친화력이 높은 Al, Mg, Ca 등은 부분적으로 환원되어 Si 중으로 용해되거나 슬래그로 제거된다. 그리고 공극 내의 온도보다 끓는점이 높은 W, Mo, B, V, Fe의 대부분은 생성물인 Si 중으로 분배된다. 끓는점이 낮은 Mg, Cd, Se, As, S 등은 일부를 제외하면 실리카 흄으로 분배되지만, P의 대부분은 Si으로 분배된다. 특히 야금학적 방법에 의한 SOG급 Si을 제조할 때, B, P 등의 제거가 어려우므로9) 원료 중의 이러한 불순물은 엄격하게 관리하여야 한다.
한편 전극 선단부의 공극내에서 생성된 SiO(g)가 노 외로 배출되면 다음식과 같이 공기 중의 산소와 반응하여 SiO2(s)가 생성된다.
실리카 흄(silica fume)은 비정질의 매우 미세한 구형 분말이며, 백색의 것과 C이 많이 함유된 회색의 것이 있다. 불순물로 C, S, Al, Fe, Ca, Mg, Na, K 등이 함유되어 있다. 특히 페로실리콘 제조공정에서 발생한 실리카 흄에는 Fe와 Mg 산화물의 함유량이 높은 편이다. 일반적으로 실리카 흄은 약 95 % SiO2이며 비표면적은 약 28 m2/g이다.
4. 금속 실리콘의 정제
전기로에서 환원된 금속 Si의 순도는 약 98 % 수준이지만, 합금용으로 사용할 때는 별도의 정제가 필요없다. 그러나 태양 전지용(>7N)이나 반도체용 Si(>11N)은 정제가 필요하다. 반도체용 Si은 전체 Si 생산량의 약 3 %에 불과하지만 태양 전지용은 약 18 %이므로 금속급 Si을 정제하여 사용하기 위한 많은 연구들이 이루어져 있다. 금속 Si의 정제는 크게 화학적인 방법과 야금학적인 방법으로 구분하고 있다.
4.1. 화학적인 방법
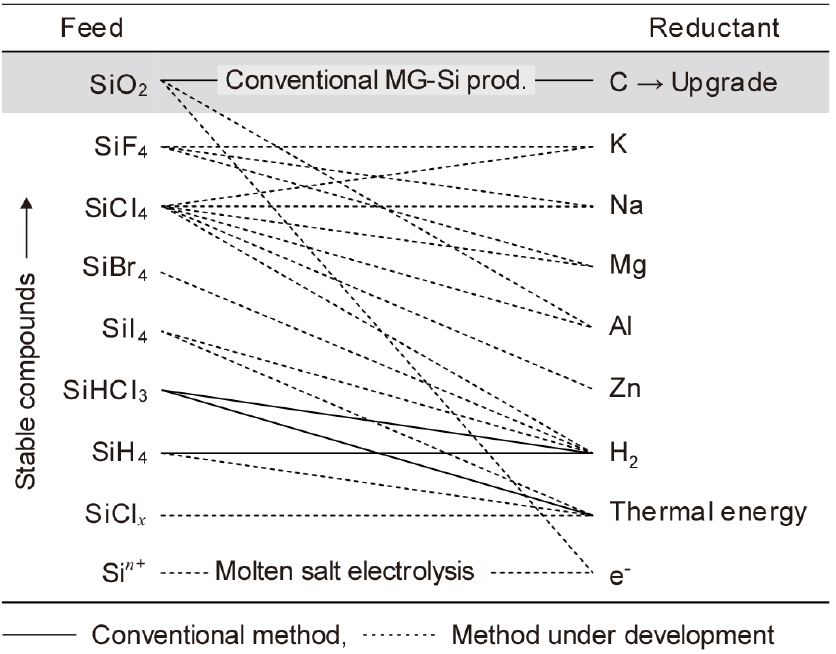
Fig. 4에는 지금까지 검토되어왔던 Si 화합물과 환원제의 관계를 정리하여 나타내었다10). 그림에서 SiO2를 제외하면 위쪽의 화합물일수록 열역학적으로 안정하여 환원이 어려운 화합물이다. 그리고 C을 제외하면 위쪽의 것일수록 환원력이 큰 환원제를 나타내었다. Si의 정제는 할로겐화물, 수소화물, 수소화 할로겐화물 등 정제하기 쉬운 화합물을 이용하고 있다. 특히 Si 화합물은 다른 활성 금속과 비교하여 비교적 환원이 쉬운 화합물이어서 여러 가지 환원제를 이용할 수 있는 장점이 있다. 그리고 환원제는 고체, 액체, 기체 상태에서도 공급할 수 있고, Si 할로겐화물 등은 증기압이 높아서 Si 원료를 가스 상태로 공급할 수 있는 장점이 있다.
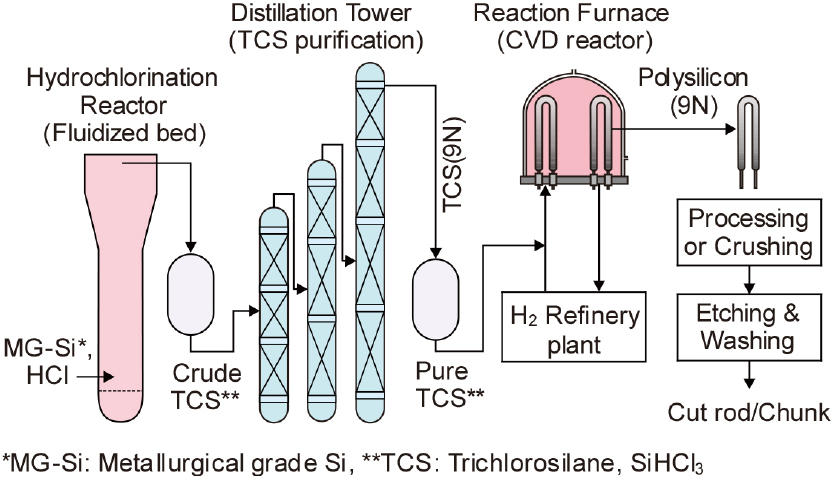
상업적으로는 삼염화실란(SiHCl3)을 출발 원료로 사용하는 것이 가장 일반적이며, Fig. 5에 이러한 Siemens법에 의한 폴리 실리콘 제조 공정도11)를 재구성하여 나타내었다. 충분히 건조한 MG-Si와 건조한 무수 HCl 가스를 250~300 ℃의 유동층 반응기에서 반응시켜 SiHCl3 (trichlorosilane, TCS)를 얻는다.
이 반응은 현저한 발열 반응으로, 반응 온도를 적절히 제어하지 못하면 사염화 규소(SiCl4, STC) 등이 생성되어 TCS의 실수율이 저하하거나 노의 수명이 짧아진다. 노에서 나오는 반응 가스는 약 300 °C이며, TCS 외에 STC, H2는 물론 미반응한 HCl 등을 함유하고 있으므로 –70 °C까지 냉각하여 TCS와 STC를 액화시켜 분리 회수한다. TCS는 STC 보다 휘발하기 쉬우며, 고온에서 다음식과 같이 열분해되어 Si이 생성되기도 한다.
TCS는 끓는점이 31.8 °C로 상온에서는 액체 화합물이다. 원료인 MG-Si 중에 함유된 불순물은 염화반응에 의해 대부분은 고체 상태의 화합물이 되므로 증류 전에 제거된다. 그러나 반도체로 사용하기 위해서는 P, B 등은 10-11 수준까지 제거하여야 하므로 다단계의 증류탑을 거쳐서 고순도화하고 있다.
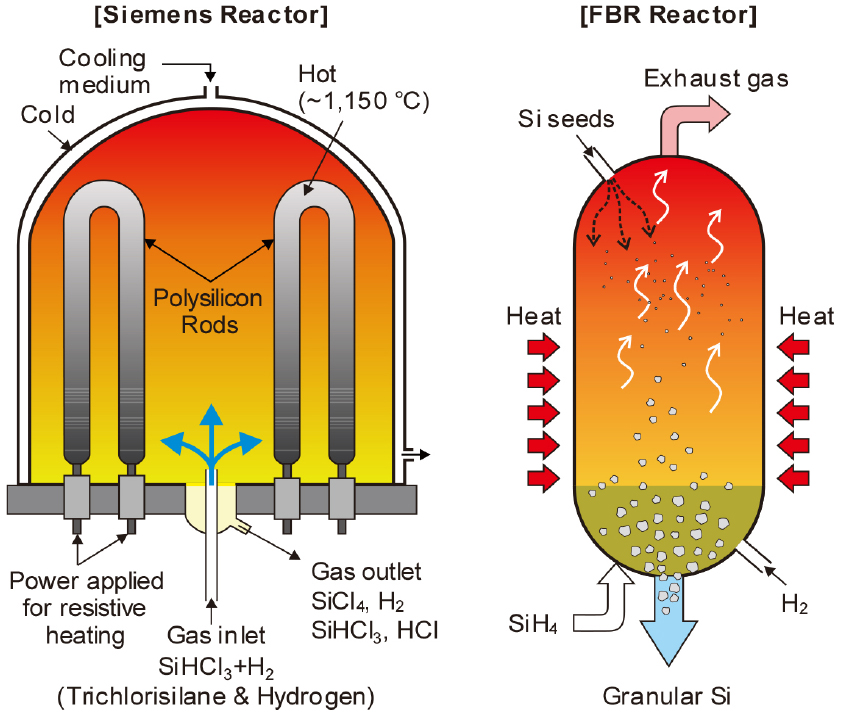
Simens법에서는 Fig. 6에 나타낸 것처럼 정제한 TCS를 수소와 혼합하여 표면 온도를 1,000 °C 이상으로 통전 가열한 Si 표면에서 반응시켜 Si을 석출시킨다.
H2/SiHCl3의 혼합 몰비는 5~15가 적당하지만 클수록 Si의 실수율은 증가한다. 생성 Si은 석영 반응관의 내벽이나 가열한 Si봉에 석출된다.
한편 Fig. 6에 나타낸 바와 같이 유동층 반응기(FBR, fludized bed reactor)에서 실란가스(SiH4)를 열분해하여 고순도의 Si을 얻는 방법도 있다. 이 방법은 FBR의 하부에서 가열한 SiH4와 H2를 분사하고 상부에서 공급한 Si seed 분말을 유동시키고 SiH4를 분해시켜 Si seed에 증착, 성장시켜 EG Si를 제조하는 것으로 반응식은 다음과 같다12).
증착에 의해 성장한 입자가 원하는 크기가 되면 FBR의 하부로 배출시키고, 상부에서는 seed 입자를 계속 공급한다.
4.2. 야금학적 방법
금속급 Si의 야금학적인 정제방법으로는 산침출, 슬래그 처리, 응고시의 편석 이용, 진공 증발제거, 수증기나 가스에 의한 용탕처리, 플라즈마에 의한 고온 가열 등의 방법이 있다.
① 산침출(acid leaching)
산침출은 불순물을 함유하는 상(phase)을 산으로 용해시켜 제거하는 방법이다. 일반적으로는 MG-Si에 Ca을 첨가하여 용융시키고 불순물을 CaSi2 상 중에 함유시켜 산으로 용해시켜 제거한다. Ca은 CaO나 CaCO3 상태로 첨가하며, 용융된 Si-Ca합금을 서냉시키면 고순도의 Si이 우선적으로 응고되면서 입계(grain boundary)에 일방향 응고의 경우와 마찬가지로 액상의 합금상이 모이면서 최종적으로는 CaSi2가 석출한다. 이때 CaSi2와 함께 FeSi2, AlSiCa, FeAlSiCa, FeSi(Ti,V) 등이 함께 석출된다. Fig. 7에는 결정립계에 생성된 CaSi2 중에 FeSi2가 포집되어 있는 것을 나타내었다13). 응고가 완료된 후, 적절한 크기로 파쇄하여 FeCl3, HCl 등으로 용해시키면 고순도의 Si만 남게 된다.
② 용융 Si의 슬래그 처리
MG-Si 중 불순물의 용융 Si과 슬래그 사이의 분배비를 이용하여 불순물을 슬래그상으로 분배시켜 정제하는 방법이다. 특히 B 등은 산 침출이나 진공정련, 일방향 응고 등으로는 제거가 곤란하지만, B을 잘 흡수하는 슬래그를 이용하면 일정 수준까지는 제거가 가능하다. CaO-SiO2계 슬래그계에서 B은 다음식과 같이 SiO2에 의해 산화되어 슬래그로 흡수된다14).
B의 슬래그와 Si 사이의 분배비()는 1823 K, 염기도(CaO/SiO2) 1.21에서 가장 높은 5.5로 측정되어 B의 제거는 분위기 중의 산소분압과 염기도에 의존하는 것으로 보고하였다.
③ 산화에 의한 정제
MG-Si 중 B이나 C은 수증기를 이용하여 산화시켜 제거할 수 있다. Si, B, C의 수증기에 의한 산화반응은 각각 다음과 같다.
이러한 반응식으로부터 온도와 에 따른 BO와 CO의 분압을 검토하면, 고온일수록 산소 퍼텐셜이 낮아도 B의 산화는 진행한다. 그리고 동일한 산소 퍼텐셜에서 고온일수록 Si의 산화반응은 억제된다. 따라서 가스 조성을 적절히 제어하면 고온일수록 Si의 산화를 억제하면서 B과 C을 제거할 수 있다15).
한편 CaCO3의 분해에 의해 발생된 CO2가스에 의해 B을 산화시켜 제거한 결과도 보고되어 있다16).
그러나 B, C 등을 제외하면 열역학적으로 Si 보다 산소 친화력이 낮은 Cu, Fe, Mn 등은 산화에 의한 슬래그로의 제거는 거의 불가능하다.
④ 일방향 응고에 의한 불순물 제거
Si 중의 많은 불순물들은 고체 상태의 Si 중 용해도가 매우 낮다는 것을 이용하여 일방향 응고에 의해 불순물을 액상에 남겨 제거하는 방법으로, 시료가 용융될 때 고상/액상 사이에서의 용질 성분의 편석을 활용하는 방법이다. 따라서 용질성분의 편석계수를 지표로 사용하고 있으며, 용질 성분 의 평형 편석계수 는 다음과 같다9).
여기서 와 는 각각 고액 계면에서 고체와 액체 중의 용질 농도(ppm)를 나타내며, 2원계 상태도에서 고상선과 액상선에서의 농도이다. 실제 상태도에서는 고상선과 액상선이 완만한 곡선이지만 여기서는 직선이고 그 비율이 일정한 것으로 가정하고 있다. Table 1에는 Si 중 주요 불순물들의 평형 편석계수값을 SoG-Si에서의 요구 수준과 함께 나타내었다17,18).
Table 1.
Impurity demand of SoG-Si and segregation coefficient of impurities in silicon
한편, 초기 불순물의 농도가 이고 응고 후의 불순물 농도를 하면 와의 관계는 다음과 같다.
여기서 와 은 각각 고체와 액체에서 불순물 의 평형 농도이다.
액상의 농도가 균일하고 고상에서 확산이 없는 경우에는 Scheil식을 적용하여 고상에서 용질의 농도는 고상 비율 에 따라 다음과 같이 나타낸다19).
한편 실질적으로 응고가 일어날 때, 고액 계면 앞쪽의 액상층에 경계층이 존재하여 농도 구배가 있는 경우에는 유효 편석계수 를 사용하여야 한다20).
여기서 는 결정 성장 속도(m/s), 는 용질의 경계층 두께(m), 는 액상에서 불순물의 확산 계수(m2/s)를 나타낸다. 따라서 →0이면 가 되며, →∞이면 =1이 된다.
⑤ 증발제거
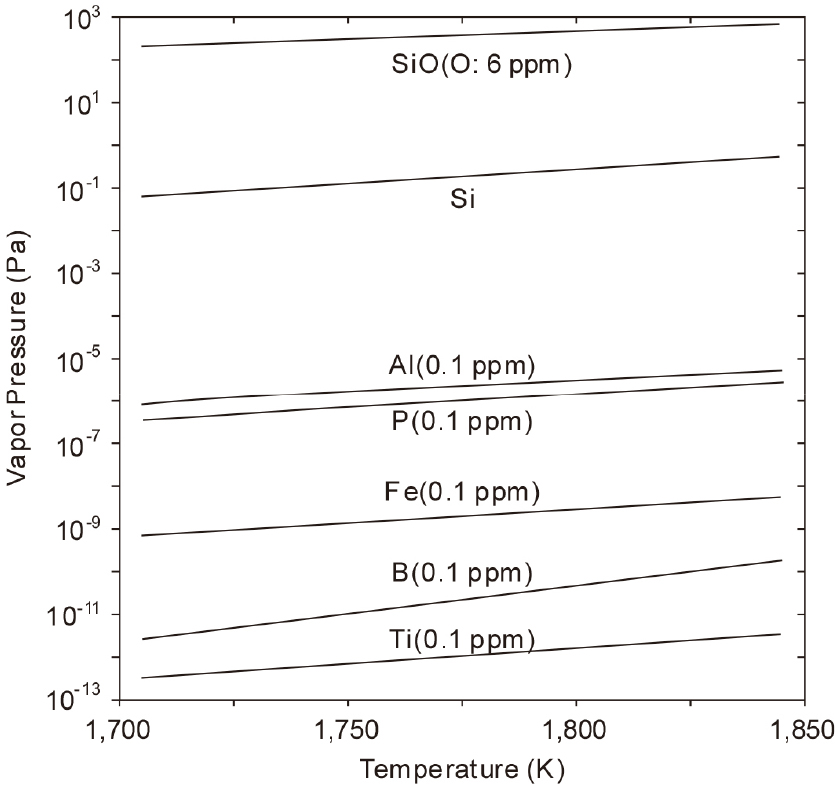
Fig. 8에는 SOG-Si 중 각 불순물의 정제 목표 농도의 최대값에서 증기압(Pa)과 온도의 관계를 나타내었다15). 그림으로부터 SiO, Al, P의 증기압이 Fe, B, Ti에 비하여 매우 큰 것을 알 수 있다. 또 1,800 K에서 0.1 ppm P와 순 Si의 증기압 비가 (1.43×10-6)/(2.58×10-1)=(5×10-6)이지만, 중량 농도비는 (0.1×10-6)/(1)=(1.43×10-7)이 되므로 0.1 ppm P인 경우에도 기체측으로의 우선 탈린이 진행하여 인이나 산소에 대해서는 증발 제거가 유효한 것을 알 수 있다. 따라서 플라즈마나 전자빔 등으로 MG-Si를 용해시켜 불순물을 진공제거하고 있다.
5. 실리콘의 용융과 반도체용 실리콘의 제조
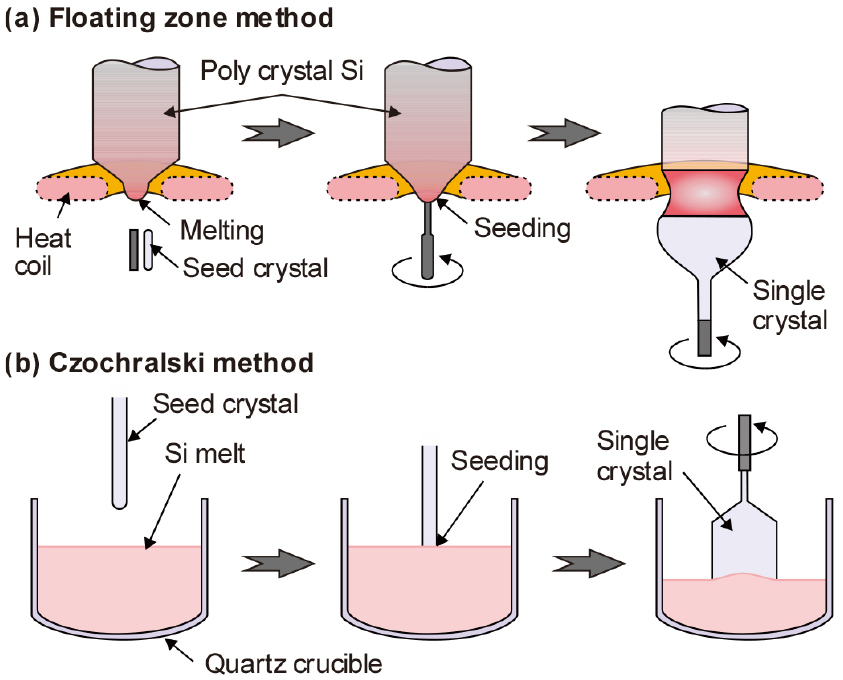
분말상의 정제 Si은 투명 석영 도가니를 이용하여 10-2 Pa의 진공이나 Ar, He 중에서 용융한다. 반도체용으로는 고순도의 단결정 Si이 필요하므로, 봉상의 Si 다결정체를 부유 대용융법(FZ, floating zone method)이나, 용융 실리콘에 Si의 시드(seed) 결정을 붙여 회전하면서 끌어 올려 단결정을 얻는 회전인상법(CZ, Czochralski법) 등이 상용화 되어 있다. 그러나 현재는 약 95 %가 CZ법에 의해 제조되고 있다. Fig. 9에는 FZ법과 CZ법의 원리를 비교하여 나타내었다21).
FZ법은 2원계 합금의 정제에 사용하는 zone melting법을 응용한 것이다. 다결정 Si의 한쪽 끝이 단결정 seed와 함께 melting zone을 통과하면서 단결정으로 바뀌게 된다. 특히 FZ법에서는 용융 Si이 도가니와 접촉하지 않고 반도체용 단결정을 성장시키므로 CZ법 보다 고순도의 단결정을 만들 수 있다. CZ법 Si의 경우 약 1018 atoms/cm3 정도의 산소를 함유하지만, FZ법에서는 1016 atoms/cm3 정도이다. 그러나 산소 농도가 낮아 기계적 강도는 CZ법 보다 떨어지며, 가공 과정에서 열응력을 영향을 더 많이 받는다. 따라서 FZ법에서는 Si 결정을 성장시킬 때 산소나 질소를 각각 1~1.5×1017 atoms/cm3 또는 1.5×1015 atoms/cm3 정도를 doping 시켜서 기계적 강도를 현저하게 상승시킨다.
CZ법은 Fig. 9에 나타낸 바와 같이 3단계를 거쳐서 단결정을 제조하고 있다. 우선 다결정 Si을 불활성 분위기의 융점(1,420 °C) 이상에서 용융시킨다. 용융 Si을 고온에서 일정시간 동안 유지시켜 미세한 기포 등을 방출시킨다. 그 후 원하는 방향을 단결정 seed가 용융될때까지 용융 Si에 담궈서 seeding 시킨다. 그리고 seed를 위쪽으로 끌어 올리면 서서히 직경이 감소하여 neck가 형성되며, 뒤이어 점점 직경이 증가하여 cone이 생성되게 된다. 상승 속도를 줄이거나 온도를 낮추어 원하는 직경까지 성장한다. 그리고 상승 속도나 온도를 조절하여 일정한 직경의 원통형 단결정을 제조한다. 단결정을 성장시키는 동안 상부에서 Ar 등의 불활성 가스를 흘려서 반응 생성물인 SiO와 CO를 하부로 제거한다. CZ법에서의 불순물 거동은 일방향 응고의 경우와 동일하다. 한편 용융 Si에 전자기장을 인가하는 MCZ(magnetic field applied CZ)법22)이나 연속 CZ법(CCZ, continuous Czochralski method)23)도 개발되어있다.
6. 종 합
실리콘은 매우 풍부한 자원으로 전 세계 연간 생산량은 약 800만 톤이지만, 금속 Si의 생산량은 약 290만 톤 수준으로 나머지는 대부분 Fe-Si 형태로 생산되어 제강공정의 탈산제로 사용되고 있다. 금속 실리콘의 약 41 %는 Al 등의 합금원소로 사용되고 있으며, 약 18 %가 태양전지용으로 사용되고 있다. 최근에는 리튬이온 이차전지의 유력한 음극재로 각광받고 있다. 이러한 금속 Si은 규석을 전기 아크로 중에서 탄소 열환원하여 만들고 있으며, 고순도 실리콘은 SiHCl3나 SiH4를 거쳐서 태양전지나 반도체용으로 제조하고 있다. 야금학적인 방법에 의한 금속급 Si의 고순도화에 관하여 많은 연구들이 이루어져 있으나 실용화된 예는 극히 드문 것으로 알려져 있다. 반도체용 실리콘의 대부분은 회전인상법(Czochralski법)에 의해 만들어지고 있다. 이러한 실리콘의 제조와 정제법을 잘 응용하면 스크랩으로부터 금속 실리콘을 회수할 수 있는 새로운 리사이클링 공정 개발에 큰 기여를 할 수 있을 것으로 기대된다.