1. 서 론
전기자동차용 리튬이온 배터리(lithium-ion batteries, LIBs)에는 NCM(LiNixCoyMn1–x–yO2)계의 삼원계 리튬이온 배터리가 많이 사용되고 있다. 최근 전기자동차의 캐즘 현상으로 인하여 사용량이 정체되고 있으나 장기적으로는 LIBs의 사용량이 늘어나 폐LIBs 발생량도 증가할 것으로 예상된다. 이러한 삼원계 LIBs에는 핵심금속인 Ni. Co, Mn 및 Li 등의 다양한 화합물이 사용되어 이러한 금속의 회수가 필요하다.
LIBs 양극재의 주성분인 Li은 전기자동차가 보급되면서 그 수요가 급증하여 2024년에는 약 24만 톤1)이 생산되었지만, 칠레, 호주, 아르헨티나, 중국 등 일부 국가에만 매장되어 있거나 생산되고 있다2). 그리고 Ni과 Co는 2024년에 각각 약 370만 톤3)과 약 29만 톤4)이 생산되었으나, 인도네시아의 Ni 광산 생산량이 약 220만 톤으로 전체 생산량의 약 60 %를 차지할 만큼 지역적 편재가 심하다. 광석에서 이러한 핵심금속을 추출하기 위해서는 채굴, 선광, 제련, 정제 등의 다양한 공정을 거쳐야 하므로 지구온난화 방지의 걸림돌이 되고 있다. 그러나 2차자원에서 이러한 금속을 리사이클링하면 이산화탄소 발생량과 에너지 원단위를 대폭 절감할 수 있다5).
전기자동차에 사용된 폐LIBs는 광석에서 금속을 추출하는 제련기술과 마찬가지로 건식제련법, 습식제련법은 물론 건식제련과 습식제련을 융합한 하이브리드 제련법 등을 적용하여 처리하고 있다. 특히 최근에는 건식법과 습식법을 결합한 친환경적인 하이브리드법에 많은 관심이 주어져 있다. 폐양극재 등을 고온의 CO2 분위기에서 탄산화시켜 Li만 수침출로 추출하고 잔사를 별도의 건식법이나 습식법으로 처리하는 등의 하이브리드법을 적용하기도 하였다6,7,8). 그리고 폐LIBs에서 회수한 black mass(B/M)를 환원 및 수침출하여 Li을 우선적으로 회수하기도 하였다9,10).
한편 CH4(g)는 C-H가 결합된 안정한 환원제이지만, 고온이 되면 다음 식과 같이 다단계로 열분해가 일어나 CHx(1≤x<4) 중간체와 함께 H2(g)가 발생하는 것으로 알려져 있다11,12,13).
따라서 CH4(g)의 열분해로 발생한 H2(g)는 폐LIBs 양극재의 환원제로 작용할 수 있다. 전 연구에서는 사용전 NCM계 양극재 분말의 CH4(g)에 의한 환원 거동을 검토하여 910 ℃ 이상에서 Ni, Co 산화물의 대부분이 환원된 것으로 보고하였다14). 본연구에서 NCM계 폐LIBs에서 회수한 B/M에서 유가금속을 회수하기 위한 기초 연구로 CH4(g)에 의한 B/M의 환원 거동과 Li 회수율에 미치는 반응 온도의 영향에 관하여 조사하였다.
2. 실험방법
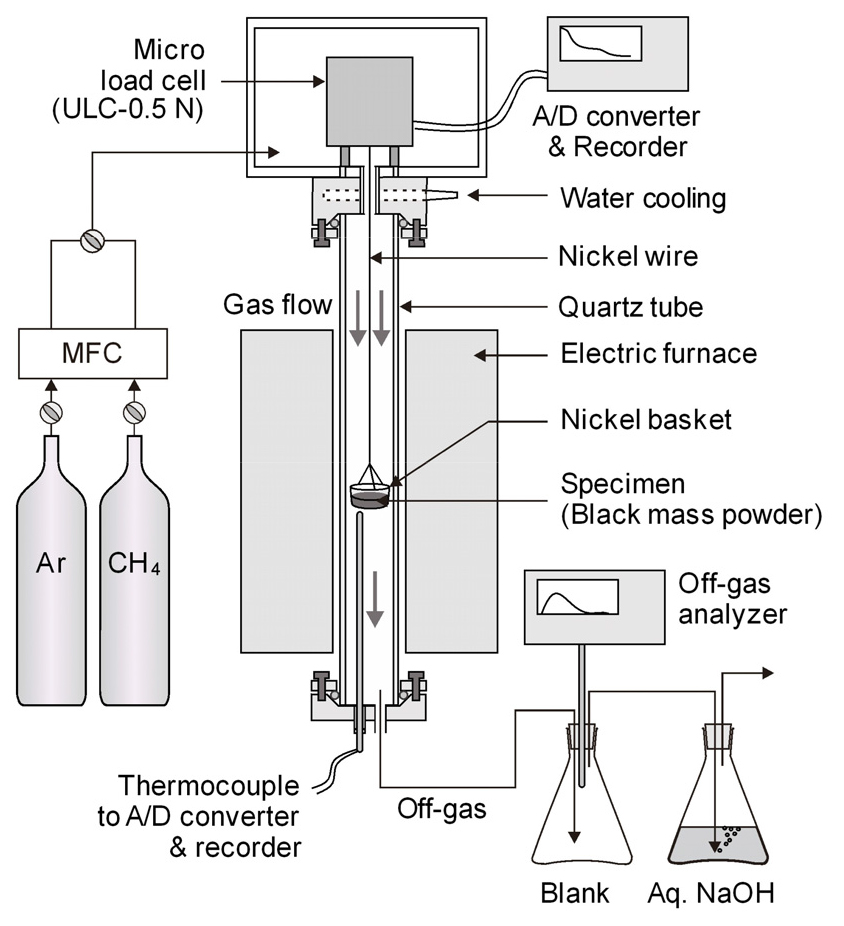
본 실험에서 사용한 시료는 폐리튬이온 배터리에서 회수한 것으로, 22.31 wt%Ni, 5.69 wt%Co, 6.33 wt%Mn, 0.54 wt%Al, 0.23 wt%Zr, 4.13 wt%Li과 함께 C이 약 32 wt% 함유되어 있는 NCM(LiNixCoyMn1–x–yO2)계 양극재의 B/M 분말이다. Fig. 1에는 열중량 분석을 위한 마이크로 로드셀(ULC-0.5N, Interface)과 수직 관상 전기로, 배가스 분석을 위한 연소가스 분석기(NOVA-9K, MRU)의 구성을 모식적으로 나타내었다.
실험은 B/M 분말 약 10 g을 장입한 Ni제 도가니를 전기로의 등온부에 위치시키고, Ar(99.995%) 가스 분위기 중에서 실험 온도까지 승온하였다. 실험 온도에 도달하면 1,500 cm3/m의 Ar+50 vol.%CH4(g)를 송입하여 등온 배소를 진행하였다. 등온 배소 중 시료의 무게와 배가스 성분의 농도를 연속 측정하였다. 또 상온에서 1,100 ℃까지 10 ℃/min로 승온하면서 시료의 무게 변화 및 배가스 성분의 농도를 연속적으로 측정하였다. 실험을 완료한 시료는 Ar 분위기 중에서 상온까지 냉각한 후 회수하였다.
회수한 시료는 상온의 증류수 중 고액비 250 g/L, 300 rpm으로 교반하면서 3시간 동안 수침출 한 후 침출 잔사와 여액을 분리하였다. 침출 여액 중 Li 농도를 원자흡광 분광광도계(Atomic Absorption Spectrometry, AAS)로 분석하여 원시료의 Li 함유량으로부터 Li 회수율을 구하였다. 또 환원배소 생성물과 침출 잔사 및 침출 여액의 수분을 증발·제거하여 회수한 리튬 화합물을 X-선 회절분석(X-Ray Diffractometer, XRD: D/Max-2500V, Rigaku)하여 생성상을 조사하였다.
3. 실험결과 및 고찰
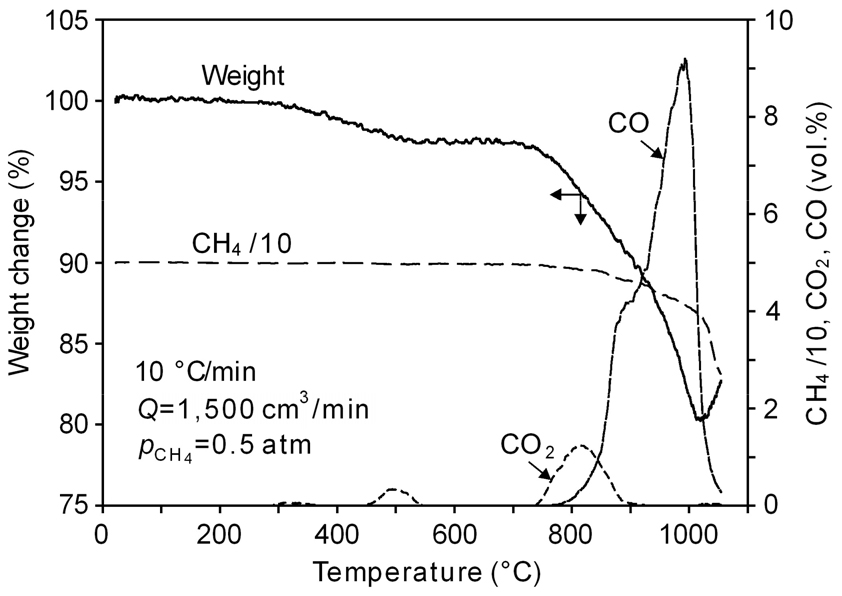
Fig. 2에는 B/M 시료를 1,500 cm3/min의 Ar+50 vol.% CH4(g) 분위기에서 1,100 ℃까지 열중량 분석한 결과를 배가스 분석 결과와 함께 나타내었다. 초기부터 약 300 ℃까지는 무게 변화가 관찰되지 않았으며, 이후 약 520 ℃까지 시료의 무게가 약간 감소한 후 약 700 ℃까지는 무게 변화가 없었다. 이후 서서히 무게가 감소하기 시작하여 약 760 ℃부터 무게가 급격하게 감소하였으나, 약 1,020 ℃부터는 다시 급격하게 증가하였다. 1차 무게 감소가 일어나는 구간(300 ℃~520 ℃)에서 2단계에 걸쳐서 소량의 CO2(g)가 발생하였으나 무게 변화가 정체한 구간(520 ℃~ 700 ℃)에서는 CO2(g)의 발생이 관찰되지 않았으며, 이러한 현상은 B/M 중 NCM계 양극재가 분해되어 발생한 O2(g)가 C과 반응하여 CO2(g)가 생성되었으나 곧바로 양극재 중 Li2O의 탄산화에 소비되었기 때문으로 생각된다. 그리고 3단계의 CO2(g)가 최곳값을 보인 후 감소하면서 약 800 ℃ 부근에서 CO(g)가 급격하게 발생하여 2단계의 무게 감소가 일어나는 700 ℃ 이후부터 CH4(g)의 농도도 감소하였다. 그리고 시료의 무게가 다시 증가하는 약 1,020 ℃부터는 CH4(g)의 농도가 급격하게 감소하여 CH4(g)의 열분해가 일어난 것으로 생각된다.
약 800 ℃ 부근에서 시료 무게의 급격한 감소와 CO(g) 농도의 급격한 증가는 다음 식에 나타낸 부도아 반응(Boudouard reaction, 708 ℃ 이상에서 )에 의해 C의 solution loss가 발생하였기 때문으로 생각된다.
또 시료 무게가 급격하게 감소할 때 CH4(g) 농도가 감소하는 것은 일부 CH4(g)의 분해와 함께 식 (2)의 부도아 반응에 따른 CO(g) 발생에 의한 상대적인 감소에 의한 것으로 생각된다.
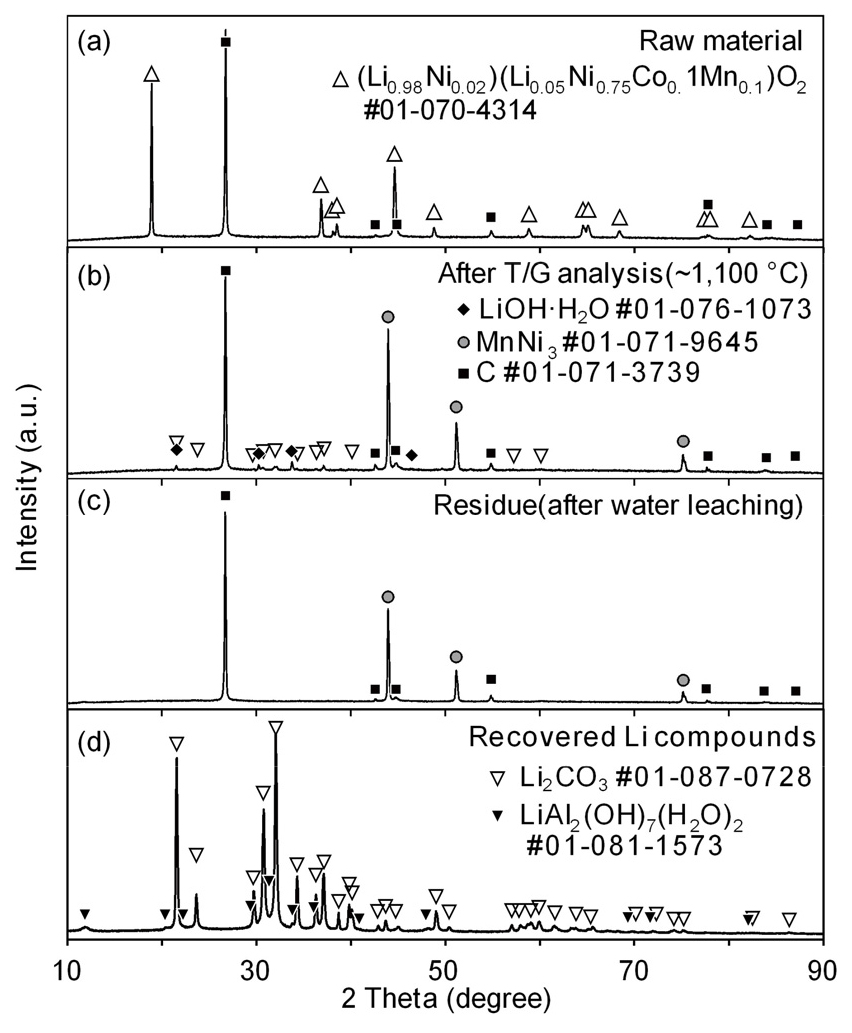
Fig. 3에는 B/M 시료(a)와 Ar+50 vol.%CH4(g) 분위기에서 약 1,100 ℃까지 열중량 분석한 시료(b), 수침출한 후 회수한 잔사(c) 및 여액에서 회수한 Li 화합물(d)의 X-선 회절 분석 결과를 비교하여 나타내었다. 열중량 분석 후의 시료에서는 C과 MnNi3 및 Li2CO3, LiOH·H2O가 관찰되었으며, 잔사에는 Li화합물이 제거되어 C과 MnNi3만 검출되었다. 따라서 NCM의 분해에 의해 생성된 NiO와 CoO는 CH4(g)의 분해에 의해 생성된 H2(g)나 B/M 중 C에 의해 다음 식과 같이 환원된 것으로 생각된다(M은 Ni, Co).
그러나 Ni, Co에 비하여 산소 친화력이 상대적으로 큰 Mn의 산화/환원에 관해서는 별도의 고찰이 필요하다. 우선 Mn의 금속/산화물 평형 관계는 다음과 같다15).
평형상태()에서 는 다음 식과 같다.9)
따라서 온도()에 따른 평형 산소분압()은 다음과 같다.
여기서 MnO와 Mn의 활동도 이면 약 1,400 ℃ 이상이 되어야 MnO가 C에 의해 환원될 수 있다. Lee 등은 B/M의 CO(g)에 의한 환원에서 MnNi3 생성 거동에 관하여 이고 =1~0.0001인 조건에서 –의 관계를 검토하였다.15) NCM계 양극재가 분해되어 Li2O가 탄산화되고 NiO와 CoO가 전부 환원되었다면 MnO의 활동도는 1로 가정할 수 있다. 또 환원된 Mn이 Ni 중으로 확산되어 고용체를 생성하면 Mn의 활동도는 매우 낮은 값이 되어 본 실험 조건에서도 MnO의 환원이 일어날 수 있는 것으로 보고하였다. 따라서 본 실험에서도 이러한 조건을 만족하여 MnNi3가 생성된 것으로 생각한다.
한편 C이나 CO(g)에 의한 산화물의 환원으로 발생한 CO2는 식 (2)의 부도아 반응에 의해 소비되어 CO(g)를 생성하지만, 일부는 다음 식과 같이 Li2O의 탄산화 반응에도 기여하는 것으로 생각된다.
식 (9)에서 Li2O와 Li2CO3가 순수 물질이라 가정하여 활동도를 1로 두면 평형상수의 역수()가 평형 이며, 이 보다 높을 때 열역학적으로 탄산화 반응이 일어난다. 720 ℃에서의 평형 는 2.5×10-4 atm이며 온도가 상승함에 따라 평형하는 도 상승하지만 1,000 ℃에서의 평형 도 0.015 atm에 불과하여 Li2O의 탄산화 반응이 쉽게 일어난 것으로 생각된다.
또 식 (3)에 의해 생성된 H2O(g)는 다음 식과 같이 수산화리튬의 생성 반응에 소비된 것으로 생각된다.
침출 여액을 증발시켜 회수한 Li 화합물에는 Li2CO3와 LiAl2(OH)7·(H2O)2(lithium dialuminate hydroxide, LDH)가 검출되었다. LDH는 환원 반응 중 원시료 중 Al이 Li2O와 결합하고, 또 수침출된 LiOH와 Al(OH)3가 여액에서 Li 화합물을 회수할 때 결합되어 생성된 것으로 생각된다16). 이러한 LDH는 B/M를 수소 분위기에서 환원하였을 때도 생성되었으며, Li 화합물의 순도와 회수율 저하의 원인이 되는 것으로 보고되어 있다.10)
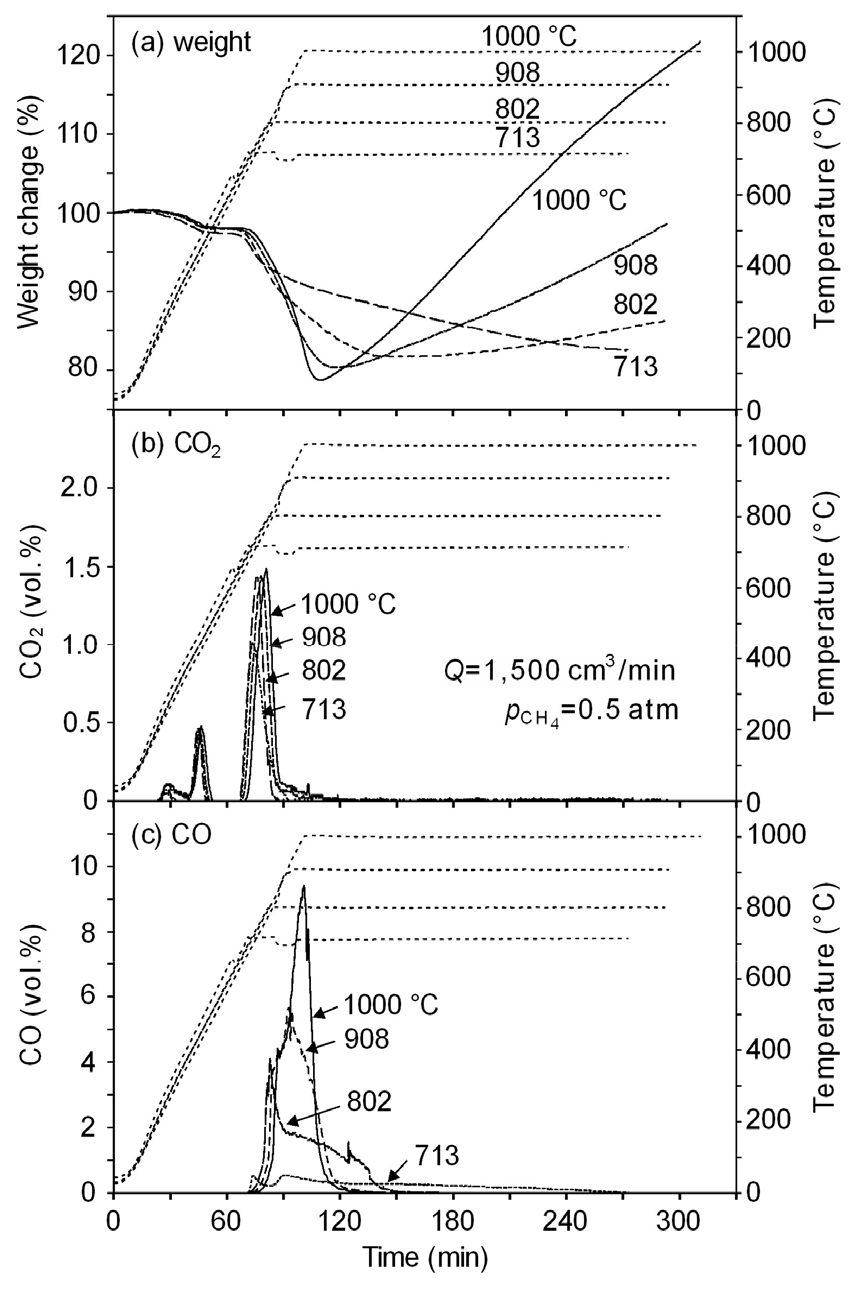
Fig. 4(a)~(c)에는 B/M 시료를 등온의 Ar+50 vol.% CH4(g) 분위기에서 환원배소할 때 시간에 따른 시료의 무게 변화 거동(a)과 함께 배가스 중 CO2(b)와 CO(c) 농도 변화를 나타내었다. 순 Ar 분위기 중에서 실험 온도까지 가열할 때는 Fig. 2의 약 700 ℃까지와 동일한 무게 변화 거동을 나타내었다. 713 ℃에서는 CH4(g) 공급과 함께 시료의 무게가 서서히 감소하였으나, 그 이상의 온도에서는 시료의 무게가 현저하게 감소한 후 다시 증가하였다. 특히 온도가 높을수록 시료 무게의 증가 속도와 증가량이 높게 나타나 온도 상승과 함께 흡열반응인 CH4(g)의 분해가 활발하게 일어난 것으로 생각된다.
CO2(g)는 CH4(g) 공급 전에 3단계에 걸쳐서 발생하였으며, CH4(g)가 공급되면서 더 이상 CO2(g)는 발생하지 않았다. 그리고 CO2(g)가 최곳값을 보인 후 감소할 때 CO(g)가 급격하게 발생하였으며, 반응온도가 높을수록 최곳값도 높게 나타났으나 CH4(g)가 공급되면서 현저하게 감소하였다. 따라서 B/M의 환원은 Ar 분위기 중 B/M에 다량으로 함유되어 있는 C의 영향이 큰 것으로 생각된다. 또 시료 무게의 현저한 감소는 산화물의 C 환원으로 생성된 CO2에 의한 식 (2)의 부도아 반응에 따른 기여가 큰 것으로 생각된다.
한편 식 (1)에 나타낸 CH4(g)의 열분해 반응은 약 700 ℃에서 시작하는 것으로 알려져 있으나,12) 802 ℃ 이상에서 시료의 무게가 증가하여 이 온도 이상에서 CH4(g)가 일정 수준 분해되어 생성된 C이 시료에 축적되는 것으로 생각된다.
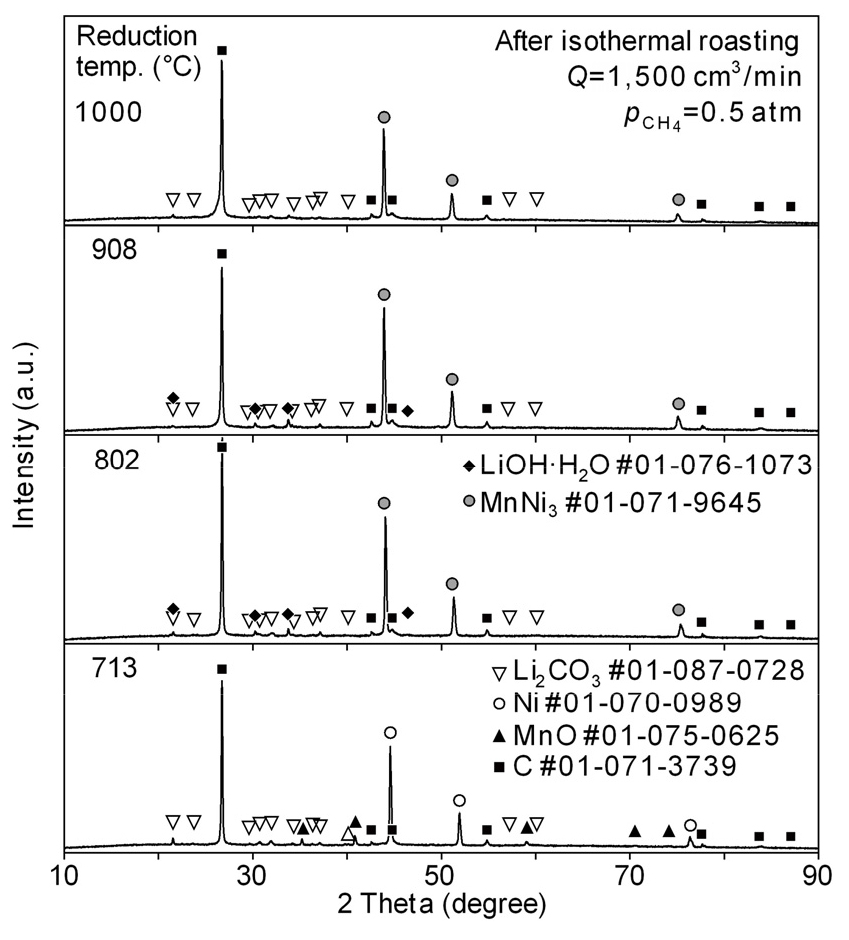
Fig. 5와 Fig. 6에는 각각의 온도에서 환원배소한 시료와 환원한 시료를 수침출한 후 분리하여 회수한 잔사의 X-선 회절 분석 결과를 나타내었다. 713 ℃에서는 C, Ni 및 Li2CO3와 함께 MnO가 관찰되었으나, 802 ℃ 이상에서는 Fig. 3에서 설명한 바와같이 MnO가 환원되어 Ni(Co) 상에 고용된 MnNi3상으로 관찰되었다. 그리고 시료의 무게가 증가한 802 ℃ 이상에서는 LiOH·H2O가 관찰되어 CH4(g)의 분해에 의해 생성된 H2에 의한 산화물의 환원이 일어나 식 (10)과 같이 수산화물을 생성한 것으로 생각된다. 한편 1,000 ℃에서는 수산화물이 검출되어 않아 식 (10)의 역반응인 수산화물의 중합반응이 일어났기 때문으로 생각된다17).
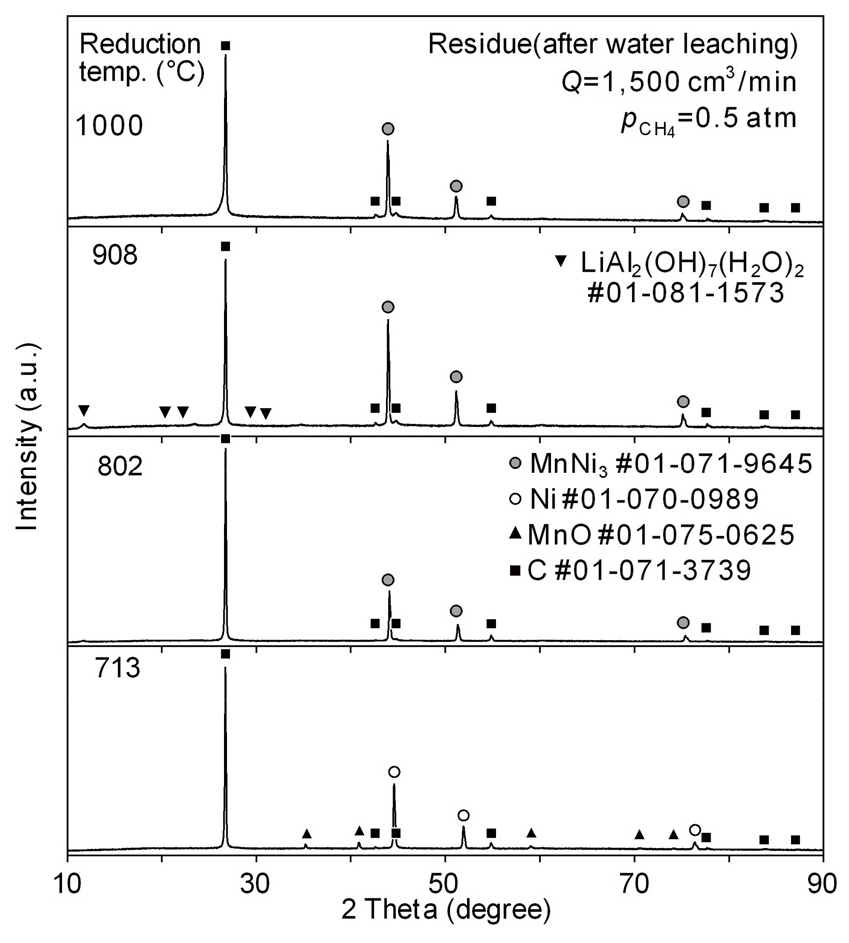
Fig. 6에는 나타낸 바와 같이 환원한 시료에서 검출되었던 Li 화합물은 수침출에 의해 제거되어 C, MnNi3, MnO, Ni 등이 검출되었으나, 908 ℃에서는 수침출에서 제거되지 못한 LiAl2(OH)7·(H2O)2의 일부가 잔류하는 것이 관찰되었다. 따라서 802 ℃ 이상에서는 Li을 제외한 금속 산화물은 전부 환원된 것으로 생각된다.
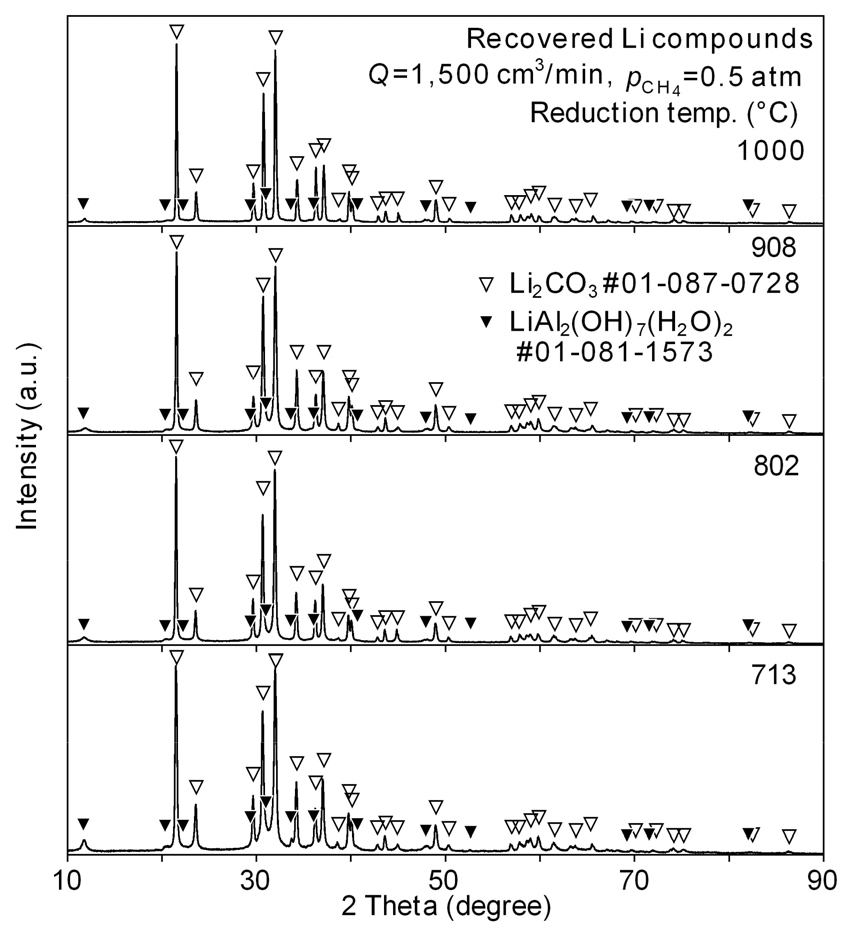
Fig. 7에는 각각의 온도에서 환원한 시료를 수침출하여 여과·분리한 여액의 수분을 증류시켜 회수한 Li 화합물의 X-선 회절분석 결과를 나타내었다. Li 화합물의 대부분은 Li2CO3이며, Fig. 3에서 설명한 바와 같이 LiAl2 (OH)7·(H2O)2(lithium dialuminate hydroxide, LDH)가 관찰되었다. Lee 등이 본 실험과 동일한 B/M 시료를 CO(g)로 환원한 후 수침출과 증류로 회수한 Li 화합물에서도 LDH가 관찰되었다.15)
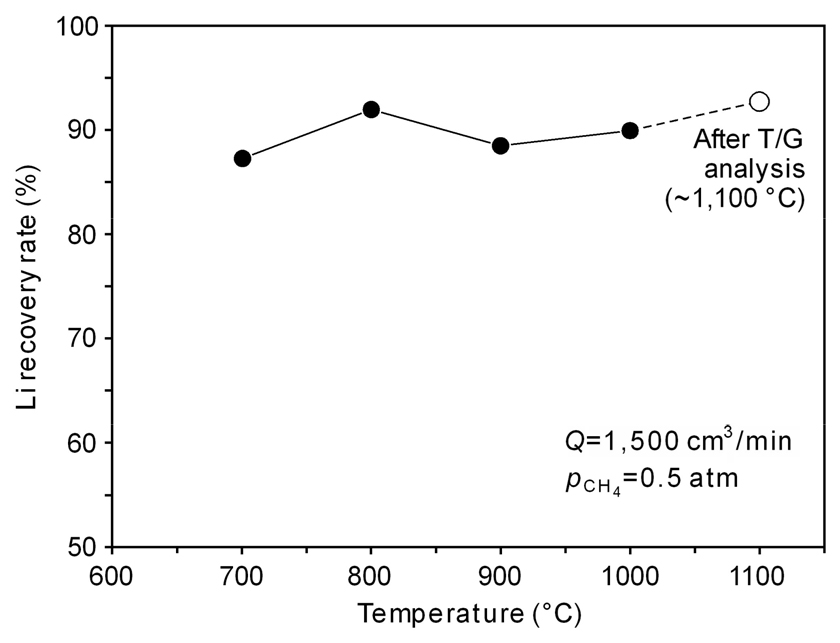
Fig. 8에는 각 온도에서 환원배소한 생성물을 수침출한 여액 중 Li 농도와 원시료의 Li 함유량으로부터 구한 Li 회수율을 나타내었다. 환원 반응 온도와 무관하게 87 % 이상의 회수율을 나타내어 B/M을 CH4(g)로 환원배소한 후 수침출에 의해 금속상의 잔사와 Li 성분을 분리하여 회수할 수 있을 것으로 생각된다. 그리고 Figs. 6과 7에서 설명한 바와 같이 일부 LDH의 생성을 제어할 수 있으면 Li 회수율도 높일 수 있을 것으로 기대된다.
4. 결 론
본 연구는 폐LIBs 중 유가금속 회수를 위한 기초 연구로 CH4(g)에 의한 NCM계 폐LIBs의 B/M 분말의 환원에 미치는 온도의 영향을 조사하였으며, 그 결과를 종합하면 다음과 같다.
1) 50 vol.%CH4(g)+Ar 분위기 중 1,100 ℃까지 열중량 분석 했을 때 5단계에 걸쳐서 무게 변화가 일어났다. 특히 약 760 ℃~1,020 ℃에서 시료의 무게가 급격히 감소한 후 다시 증가하였으며, 시료 무게가 급격히 감소할 때 CO2(g)가 최곳값을 보인 후 감소하면서 CO(g)가 현저하게 발생하여 최곳값을 보인 후 급격하게 감소하였다. 이러한 시료 무게의 급격한 감소는 부도아 반응에 의한 C solution loss의 기여가 큰 것으로 생각된다.
2) 동일 분위기 중의 등온 배소에서 CO2(g)와 CO(g)는 CH4(g) 공급 전에 발생하면서 시료 무게도 감소하기 시작하였다. 713 ℃를 제외하면 배소 온도 상승과 함께 시료의 무게 감소 속도 및 무게 감소율이 증가하였으며, CH4(g)를 공급하면 시료 무게가 더욱더 감소하여 최솟값을 보인 후 시료 무게가 현저하게 증가하였다. 특히 1,000 ℃에서는 CH4(g)의 분해에 의한 C으로 인해 원시료 무게의 100 %를 초과하였다. 그리고 배소 온도와 무관하게 Li2CO3가 관찰되었으며, 802 ℃와 908 ℃에서는 LiOH도 검출되었다. 또 713 ℃에서는 Ni이, 그 이상의 온도에서는 MnNi3 상이 관찰되어 B/M 중 산화물의 대부분이 환원되었다.
3) Li 회수율은 등온 배소 온도와 무관하게 약 87 % 이상을 나타내어 B/M을 CH4(g)로 환원배소한 후 수침출에 의해 금속상의 잔사와 Li 성분을 분리·회수할 수 있지만, Li 회수율과 Li 화합물의 순도를 높이기 위해서는 LDH의 생성 제어가 필요할 것으로 생각된다.