1. 개 요
2. 습식 공정 분류
2.1. 침출(Leaching)공정
2.2. 정제(purification) 및 회수(Recovery) 공정
3. 분리·회수 공정 분석
3.1. 단일 성분 추출 공정
3.2. 다성분 공추출(Co-extraction) 공정
3.3. Pre-loading 용매추출 공정
3.4. 불순물 제거 후 공침(Co-precipitation)에 의한 회수 공정
4. 결론 및 전망
1. 개 요
지난 20년 동안 다양한 휴대용 전자기기 사용으로 인하여 이에 따라 많은 이차전지가 생산되어 적용되고 있다. 2차전지 중에서 리튬이온전지(LIB)는 높은 작동 전압, 높은 에너지 밀도, 낮은 메모리 효과, 경량, 소형화, 낮은 자체 방전율, 긴 주기 수명 및 넓은 작동 온도 범위 등 우수한 성능으로 인하여 널리 사용되고 있다1). 전통적인 전자기기의 수요를 제외하고 에너지 저장장치 및 전기자동차와 같은 분야에 대한 수요는 급증하는 추세이다. 따라서 전기차 보급이 급성장함에 따라 폐배터리 처리 문제가 큰 관심이 되고 있으며2), 이에 따라 배터리 제조 원자재 수급 리스크와 폐배터리 처리 문제를 동시에 해결할 수 있는 배터리 재활용 기술이 주목받고 있고 재활용 시장도 급성장이 예상되고 있다. 기존 전기차 배터리 기술은 대한민국이 세계시장을 선도하고 있었으나, 막대한 물적, 인적 자원을 앞세운 중국 업체들로 인해 점유율이 감소하고 있으며 특히 리튬, 니켈, 코발트 등의 핵심 원재료 수급에서 어려움을 겪고 있다. 또한 국내·외적으로 폐배터리 활용에 대한 협약이 진행되면서 EU에서는 EU 배터리 법안을 발의하여 원료 재사용을 의무화 하였고, 미국은 인플레이션 감축법(IRA)을 통해 자국 원자재 수출을 제한하고 있어 폐배터리 재활용을 통한 핵심소재의 확보가 매우 중요한 상황이다.
리튬 이온 배터리는 양극, 음극, 전해질, 분리막 및 외부 쉘로 구성된다. 음극은 동박으로 코팅된 탄소 분말과 폴리머 바인더로 구성되어 있고 양극은 알루미늄 호일로 코팅된 탄소 분말, 폴리머 바인더 및 LiCoO2, LiMn2O4, LiNiO2 및 LiNixCoyMnzO2(LNCM)와 같은 리튬 전이 금속 산화물로 구성되었다. 분리막은 고분자 재료로 만들어지며 외부 쉘은 일반적으로 스테인리스 스틸 또는 플라스틱으로 구성된다. 폐LIB의 유기 전해질과 중금속은 독성이 있기 때문에 폐LIB를 단순 처리하거나 부적합한 처리 방법(예: 매립)으로 처리할 경우 누출된 유해 물질로 인해 토양 및 지하수 오염 등 심각한 환경오염이 발생할 수 있다. 한편 폐LIB에는 유가금속(Li, Co, Ni, Mn, Cu, Al, Fe)이 다량 함유되어 있다. 일반적으로 폐LIB에는 코발트 5~20wt.%, 리튬 5~7wt.%, 니켈 5~7wt.%, 유기물 15wt.% 및 플라스틱 7wt.%가 함유되어 있으며 조성은 제품에 따라 조금씩 다르다. 금속 함량이 일반적으로 천연 광석보다 훨씬 높으며 또한 코발트와 니켈 및 리튬은 희소금속으로 중요한 전략적 금속으로 취급하고 있다. 따라서 폐LIB의 재활용은 환경보호와 자원절약의 관점에서 필요하고 시급하다고 할 수 있다3).
폐배터리의 재활용 공정4)은 크게 습식과 건식 그리고 직접재생 공정으로 구분할 수 있다. 건식 공정은 사용 후 폐배터리를 건식용융 공정을 통해 발생된 합금상(Co-Ni-Cu)을 다시 습식 처리하여 금속화합물로 회수는 공정으로 복잡한 폐배터리를 팩 해체 공정단계가 필요 없이 대용량 처리를 할 수 있는 유리한 점은 있으나, 투자비 및 공정비용이 고가이고 리튬 등의 유가금속을 회수하는데 제한이 있다. 직접재생 공정은 사용 후 배터리에서 양극 및 음극 활물질을 분리해내고, 열처리 등의 공정을 거쳐 양극을 재생하는 공정으로, 일부 LFP 양극재에 적용이 가능하나 NCM계 양극재의 경우는 혼합물질의 경우 문제점이 많아 아직까지는 기초 연구 단계에 머무르고 있는 실정이다. 습식공정은 폐배터리(폐LIB)를 방전시킨 후 파·분쇄하여 전처리를 거쳐 얻은 블랙파우더(Black powder 또는 Black mass)를 산 용액에 침출시켜 양극활물질 내 유가금속들을 침출시킨 후, Mn, Co, Ni, Li 성분을 단계적으로 회수하는 공정으로 고순도로 유가금속들을 효과적으로 회수할 수 있으며 건식공정에 비해 투자비가 적고 배기가스 처리 문제는 없으나, 공정이 복잡하고 폐수처리에 문제가 있다.
현재의 재활용 기술은 중국을 필두로 습식 공정이 주를 이루고 있으며 국내에서도 성일하이텍(주)을 위시로 다수의 기업에서 습식공정을 기반으로 한 리사이클링 사업을 확장하거나 계획하고 있다5). 이러한 습식공정의 핵심 요소 기술은 블랙파우더에서 유가금속의 침출공정과 침출용액에서 알루미늄, 철, 구리 등의 불순물을 제거시키는 기술 그리고 용매추출(solvent extraction)에 의해 망간, 코발트, 니켈, 리튬을 선택적으로 분리·회수하는 기술로 분류할 수 있고6) 주요 회수 생성물은 NiSO4, CoSO4 및 Li2CO3와 같은 염 또는 NMC 및 NCA에 기초한 전구체 생산을 위한 혼합물 형태의 생성물이다.
따라서 본고에서는 NCM계 폐LIB에서 재활용을 위한 요소 기술인 침출 기술, 침출액으로부터의 금속 분리·회수 기술 등 폐LIB의 습식제련 재활용 기술에 대해 기존 기술 및 개발 중인 기술 등의 현황을 공정도를 통하여 소개하고 현 기술의 문제점을 분석하여 향후 보다 효율적이며 환경영향을 최소화할 수 있는 개발 방향을 제시하고자 한다. 특히 분리공정의 핵심이라 할 수 있는 용매추출의 적용사례 분석을 통해 효율적인 유가금속(Mn, Co, Ni, Li) 회수 방안에 대하여 주안점을 두고 설명하고자 한다.
2. 습식 공정 분류
전통적으로 폐LIB 재활용 기술의 공정의 개략도는 Fig. 1과 같다. 먼저 폐LIB를 적절한 전처리(pretreatment)후에 얻은 양극물질로 구성된 블랙파우더를 환원산침출(reductive acid leaching)을 거쳐 고액분리(S/L separation) 후 분리·정제(purification)을 거쳐 개별 금속염이나 또는 복합염 형태로 회수하여 다시 양극재로 재생하는 공정으로 구분할 수 있다7).
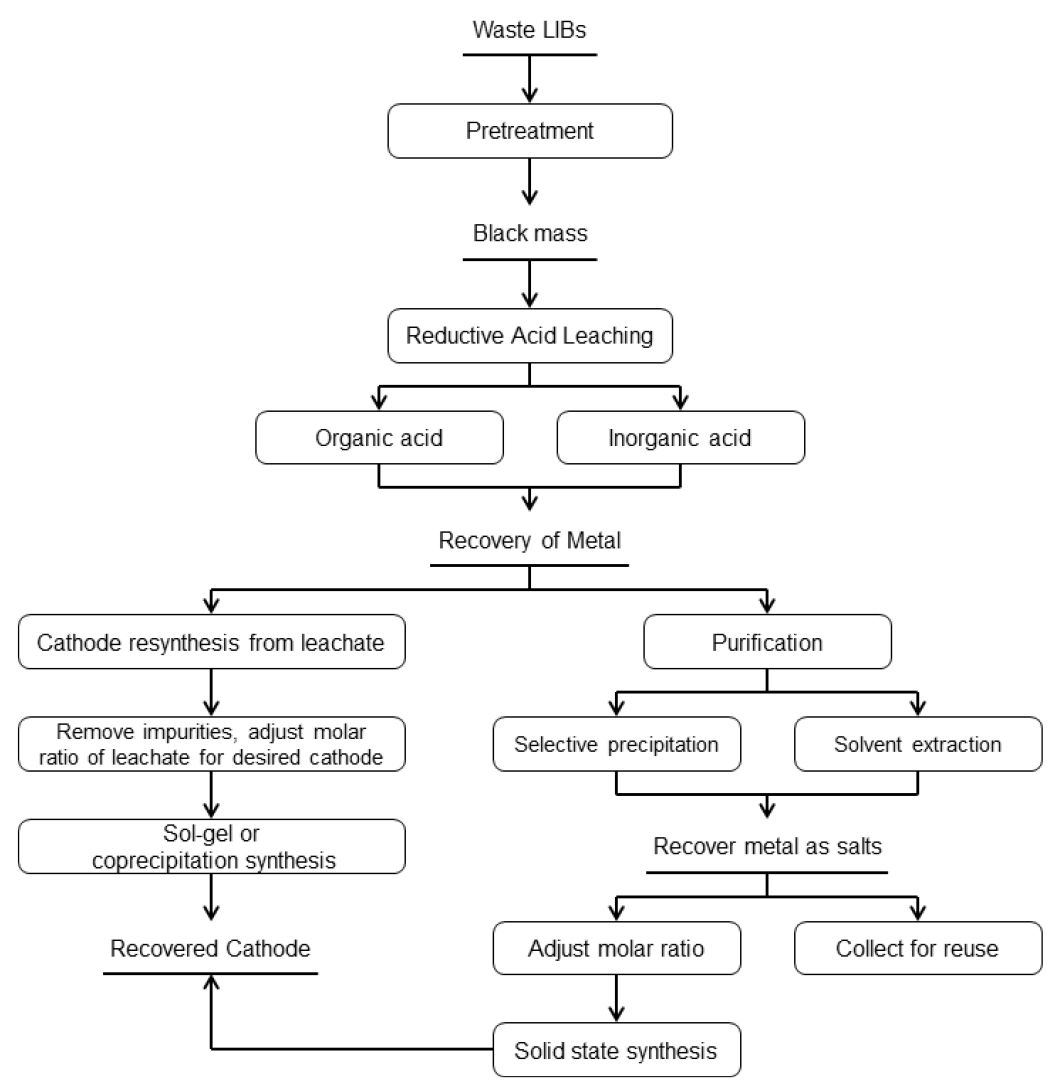
Fig. 1.
Overview of hydrometallurgical LIB recycling approaches for diverse cathode chemistries(Source: Adapted from ref.7).
2.1. 침출(Leaching)공정
전처리 공정을 거쳐 얻는 양극활물질(블랙파우더)로부터 코발트 및 니켈 등의 유가금속을 회수하기 위해서는 적절한 화학적 처리 공정이 필요하다. 먼저 침출공정은 전처리를 거쳐 얻어진 양극활물질 분말을 무기산이나 알칼리 또는 유기산 등이 다양하게 사용될 수 있다. 무기산은 황산(H2SO4), 염산(HCl), 질산(HNO3) 등이 사용되고, 산의 농도와 환원제 주입량, 반응시간, 온도, 고액농도 등이 침출 효율에 영향을 미친다. 현재는 주로 무기산 중 황산을 사용하고 환원제로 일정량의 과산화수소를 첨가하여 99% 이상의 금속을 침출 하고 있다8,9,10). 무기산을 사용하면 대부분의 금속이 침출되지만, 유해가스와 폐산 발생과 같은 2차 오염의 우려가 있고, 전극물질에 존재하는 모든 금속을 침출할 수 있어 목표 금속의 선택적 회수 가능성이 낮다는 단점이 있다. 무기산 사용에 따른 환경영향을 최소화하기 위해 유기산(구연산, 말릭산, 숙신산 등)을 사용할 경우, 선택적 침출 및 침전제로도 사용이 가능하다는 장점이 있다11,12,13,14,15). 예로 1.5M 젖산(lactic acid)을 사용할 경우 고액농도 20g/L, 70℃, 0.5vol% H2O2 조건하에서 20분 만에 98% Li, 99% Co, 98% Ni 및 98% Mn의 높은 침출율을 보였다16,17). 그러나 유기산은 매우 고가이므로 실제 현장에서는 제한적으로 사용되고 있다. 이러한 문제 해결을 위해서는 미생물 발효 기술을 활용하여 저렴하게 유기산을 생산하여 이용하는 것이 바람직하다. 알칼리 침출은 암모니아(NH3), 탄산암모늄((NH4)2CO3), 황산암모늄((NH4)2SO4), 염화암모늄(NH4Cl)를 주로 사용하는데 특히 Ni, Co, Li이 암모니아와 안정한 착화합물을 형성하여 선택적 침출 특성으로 인하여 금속의 추출과 정제에 널리 적용되고 있다18,19,20). 암모늄-탄산암모늄을 침출액으로 사용하고 아황산암모늄((NH4)2SO3)를 환원제로 사용하여 폐LIB를 침출실험 결과, Co와 Cu는 완전히 침출된 반면, Mn과 Al은 침출되지 않아 Li, Co, Ni을 선택적으로 침출할 수 있다. 금속의 침출을 촉진하기 위해 일반적으로 과산화수소(H2O2)를 많이 사용하고 있으나 과산화수소가 불안정하고 빛이나 열에 노출 시 분해된다는 점이 있어 NaHSO3, SO2, Na2SO3, Na2S2O5, glucose 등이 대체 환원제로 제안되고 일부 사용되고 있다21,22,23). 또한 초음파 사용 시 금속의 침출 촉진 효과가 있는데, 유기산 침출에 초음파 기술을 적용할 경우 리튬을 100% 침출시킬 수 있다24). 산/알칼리를 이용한 침출법은 다양한 중금속과 유기물을 포함한 폐수가 발생하며, 이의 처리에 많은 노력과 비용이 필요하다. 따라서 특정 금속만을 침출할 수 있고, 동시에 침출 효율 향상과 환경오염을 저감할 수 있는 방법에 대한 연구가 필요하다. 최근 친환경 기술로 주목 받고 있는 미생물 침출법은 미생물의 직·간접적인 작용에 의해 금속성분을 이온상태로 침출 시키는 방법으로 저품위 광석이나 금속함유 전자폐기물로부터 환경친화적으로 구리 등의 유가금속을 회수 할 수 있는 기술로 많은 주목을 받고 있다25,26). 폐 LIB의 침출에 사용될 수 있는 미생물 그룹은 일반적으로 박테리아(bacteria) 및 곰팡이(Fungi) 등이 알려져 있다27). Acidithiobacillus ferrooxidans 박테리아를 사용하여 미생물 침출할 경우 고액농도 100g/L에서 72시간 반응 시 폐LIB에서 90% Ni, 92% Mn, 82% Co 및 89% Li 침출율을 보였다28). 곰팡이의 일종인 Aspergillus niger를 사용할 경우에는 구연산 등의 유기산이 생성되어 침출반응에 이용되기 때문에 더욱 환경친화형 공정이라 할 수 있다29,30,31). 그러나 이 방법은 미생물의 활성과 조건(온도, pH, 기질의 종류와 농도)에 따라 효율이 크게 변하고 반응속도가 느리다는 단점이 있고 또한 유기전해질 및 불화물 결합제와 같은 물질은 미생물에 대해 독성이 있기 때문에 산업현장에 적용하기 위해서는 앞으로도 많은 연구가 필요하다고 할 수 있다.
최근에 주목을 받고 있는 기술로 공융용매(DESs; Deep Eutectic Solvents)를 사용하는 연구가 활발히 진행 중에 있다. DESs는 기존 침출제 보다 환원제 사용 없이도 선택적 추출 특성 및 추출효율이 우수하고 회수 비용이 낮아 더 친환경적인 공정으로 평가되고 있다32,33). Luo et al. 등의 연구에 의하면 Betaine hydrochloride/ethylene glycol DES를 사용하여 환원제를 추가하지 않고 폐LIB 양극물질에서 99% 이상의 Li, Ni, Co 및 Mn 침출이 가능하다고 발표하는 등 차세대 배터리 재활용 기술로 기대를 모으고 있다34).
2.2. 정제(purification) 및 회수(Recovery) 공정
침출 단계 후에 금속 이온의 효과적인 분리가 필요하다. 가장 일반적인 분리 방법은 화학적 침전(precipitation), 용매추출(solvent extraction), 이온교환(ion exchange), 치환(cementation)기술 등이 있으며 침출액 중의 금속 성분의 종류 및 농도 등에 따라 적절한 방법을 선택할 필요가 있다. 침출액중의 불순물을 제거하고 순수한 용액을 얻은 다음 금속이나 금속염으로 회수하는 공정은 전해 회수(Electrowinning) 및 화학 환원법(chemical reduction), 공융동결결정화(eutectic freeze crystallization: EFC)기술 등이 적용되고 있다. 침출액 중의 각 성분의 분리·회수는 일반적으로 여러 단위 기술의 조합으로 구성되어 있다. 본고에서는 분리정제 공정의 핵심이라 할 수 있는 용매추출법에 대하여 원리 및 반응 변수 등에 대하여 구체적으로 설명하고자 한다.
2.2.1. 화학적 침전(Chemical precipitation)에 의한 불순물 제거
화학적 침전은 침출된 금속을 침전시켜 분리하는 방법으로 주로 NaOH, H2C2O4, H3PO4, Na2CO3, Na2S 등이 침전제로 많이 사용되고 있다. 폐LIB 양극활물질을 황산을 이용하여 금속성분을 침출시키면 침출용액 중에는 Co, Ni, Mn 및 Li 외에 Al, Fe, Cu 등의 불순물이 존재하게 되며, 이러한 불순물들은 pH를 조절하여 수산화물 형태로 침전·제거시킨다35). Al과 Fe의 경우는 pH 5에서 99%이상, Cu의 경우 90% 이상 제거할 수 있다. 그러나 pH 5.0이상에서는 Co와 Ni의 공침에 의한 손실이 크기 때문에 pH 3.5~4.0이 바람직하다. 또한 고가의 Cu는 Na2S를 사용하여 선택적으로 분리하거나36) Fe shots에 의한 치환(cementation)으로 회수37) 또는 LIX984N에 의한 용매추출 방법으로 회수38)하고 있다. Mn의 경우는 KMnO4를 첨가하여 MnO2로 침전시켜 제가가 가능하지만, Co와 Ni의 공침전으로 인한 손실율이 크다는 단점이 있다. 이후 얻어진 Mn, Co, Ni용액에서 용매추출법에 의해 각 성분으로 분리하거나 또는 직접 3성분 공침전법에 의해 NMC계 전구체를 제조하는 경우도 있다.
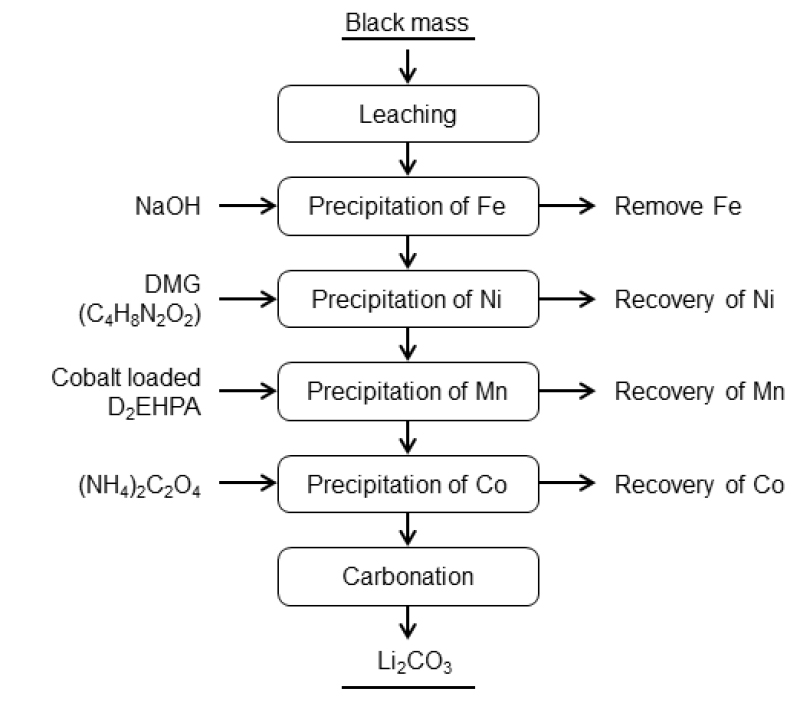
리튬과 코발트가 함께 존재하는 추출 용액에서는 옥살산(H2C2O4)으로 코발트를 먼저 옥살레이트 침전물로 침전시켜 회수하고, H3PO4와 NaOH를 주입하여 pH가 13이 되도록 조절 후 Li3PO4 형태로 리튬을 회수할 수 있다. 침출액에서 니켈을 선택적으로 침전시키기 위해서 Dimethylglyoxime(DMG : C4H8N2O2)이 사용 된다39). 이 경우 Ni-DMG 침전물의 형성으로 99% 니켈을 선택적으로 침전시켜 분리가 가능하며 사용된 DMG는 염산을 이용하여 재생이 가능하다. 화학적 침전법은 침출액에 존재하는 다양한 금속을 여러 공정을 거쳐 개별적으로 회수할 수 있지만 이 과정에서 많은 약품이 소요된다. 따라서 약품비 절감을 위해서는 금속을 회수한 후에 현장에서 바로 약품을 재생할 수 있는 시스템 개발이 필요하다.
2.2.2. 용매추출(Solvent extraction)에 의한 분리·회수 공정
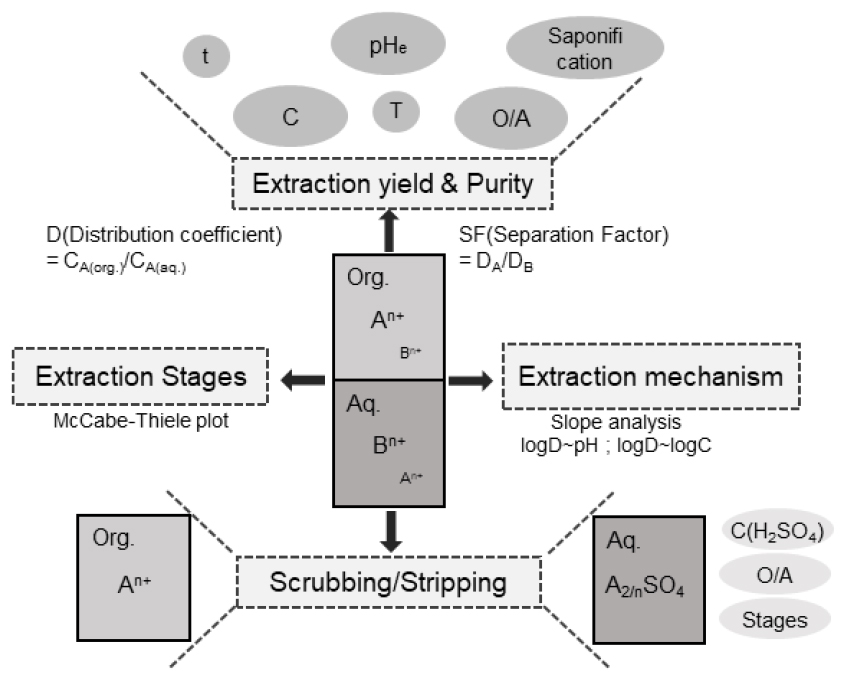
Black mass를 황산으로 침출한 용액에서 Al, Fe, Cu 등을 제거하고 난 후에 용액 중에 함유된 Mn, Co, Ni 및 Li 분리를 위해 용매추출법이 사용되고 있다40,41,42,43). 용매추출법은 일반적으로 유기상과 수용액상인 2상 시스템을 사용하여 서로 다른 금속 이온을 두 상으로 분배시켜 분리하는 공정이다. 용매추출의 효율성은 추출률과 상 분리 성능에 의해 결정될 수 있으며 이 두 가지 성능 지표를 특성화하는 데에는 Fig. 2와 같이 몇 가지 요소가 사용 된다40). 첫 번째는 분배계수(Distribution coefficient : D)로, 평형 상태에서 수용액상과 유기상중의 금속이온 농도의 비로 계산된다. D 값이 클수록 금속 이온의 추출률이 높다는 것을 의미한다. 분리계수(Separation factor : SF)는 서로 다른 금속 이온의 분리 성능을 결정하는 데 사용되는데, A금속과 B금속 사이의 SF 값은 SF = DA/DB에 따라 계산한다. 일반적으로 분리계수인 SF값은 상호분리의 가능성을 나타내는 수치이며 SF ≥ 10인 경우는 2성분의 상호 분리가 가능하나 다단 추출이 필요하며 SF ≥ 100인 경우는 분리가 양호함을 나타내며 SF ≥ 1000인 경우는 분리성이 매우 우수하여 1단이나 2단으로도 추출이 가능하다고 할 수 있다.
추출 공정 중에는 추출 시스템, 평형 pH, 추출제 농도, 상비(O/A), 비누화율, 반응온도 및 반응시간을 포함한 여러 매개변수가 추출 성능에 영향을 미칠 수 있는데 이 중에서 특히 중요한 요인은 평형 pH라 할 수 있다. 침출용액에서 Mn, Co, Ni 등을 분리하기 위해 주로 사용되는 추출제(extractant)는 Cyanex272(bis-2,4,4-trimethylpentyl phosphinic acid), D2EHPA(di-2-ethylhexyl phosphoric acid), PC88A(2-ethylhexyl phosphoric acid mono-2-ethylhexyl ester), Versatic acid 10(carboxylic acid) 등이 있다. 일반적인 추출 및 탈거 반응은 다음 식 (1), (2)와 같으며 pH에 매우 민감하다는 것을 알 수 있다.
추출반응 :
탈거반응 :
다양한 추출용매에서 Cu, Co, Ni 추출에 대한 적절한 pH 범위를 Fig. 3에 나타내었다41). 그림에서 알 수 있듯이 D2EHPA의 경우는 Cu의 추출에는 유리하나 pH 2.2~3.0 범위에서 Co에 대한 추출 선택성은 좋지 않고 침출액의 pH가 증가함에 따라 Co의 추출률은 증가한다. PC88A는 pH 4.5에서 Co 및 Ni을 다른 금속 이온으로부터 효과적으로 분리할 수 있는 반면에 pH 3.0 미만에서는 추출률이 낮다. Co 및 Ni의 분리계수의 경우는 Cyanex272가 PC88A(P507)보다 커서 고농도 Ni 및 저농도 Co 용액에서 추출·분리 시에 유리하나 가격이 고가라는 단점이 있다. Co와 Ni의 분리에 적합한 pH 범위는 3.0에서 5.0 사이로 제안되어 있으나 이 범위는 산성영역이므로 내식성이 좋은 장치재료의 선정이 필요하다. 이러한 이유로 보다 높은 pH 범위에서 추출 할 수 있는 추출제가 바람직한데 이 경우에는 혼합추출제나 특정 용매를 혼합하여 사용함으로써 개선할 수 있다. 예를 들어, 그림에서 PC88A를 사용하여 Co를 선택적으로 추출할 경우 TOA(Tri-octal amine)를 상 조절제(modifier)로 용매에 혼합하여 사용할 경우 적정 pH 범위가 3.5와 5.0 사이로 이동하여 추출·분리 효과를 개선할 수 있다. 또한 Cyanex 272에 상 조절제로 5vol% TBP(Tributyl phosphate)를 사용할 경우 pH 5.0에서 85.42% Co 추출이 가능하고44), isodecanol을 사용할 경우에는 pH 5.0에서 Co의 추출률이 99.9%까지 가능하다45). 한편, Mn 및 Co가 제거된 Ni/Li 혼합용액에서 Ni을 회수하기 위해서는 일반적으로 D2EHPA, PC88A(P507) 그리고 Versatic acid 10과 같은 산성추출제를 사용할 경우 Ni을 선택적으로 분리할 수 있다. D2EHPA를 사용할 경우에는 비교적 낮은 평형 pH 5.0-6.0 에서 Ni을 Li과 분리할 수 있으나 분리효율이 다소 낮다. 반면에 PC88A 나 Versatic acid 10를 사용할 경우에는 추출 pH가 7.0 이상이 되어야하기 때문에 용액의 중화에 따른 가성소다가 많이 소요된다. 또한 Versatic acid 10을 사용할 경우에는 pH 7.5~8.0에서 Ni의 분리가 가능하나 Versatic acid 10이 물에 대한 용해도가 높아 손실율이 크다는 단점이 있고, LIX-84I(β-hydroxl oxime)의 경우는 Ni과 Li의 선택적 분리추출이 용이하나 유기상에 추출된 니켈을 탈거하는데 어려움이 있다. 따라서 Versatic acid 10과 LIX-84I를 혼합한 추출제를 사용한 연구 결과도 있다46). 한편 추출반응에 의한 수용액상의 급격한 pH 감소를 방지하고 일정한 pH조절을 위해 비누화(Saponification)시킨 추출제를 사용하고 있으며 최근에는 비누화된 추출제에 특정 금속(Ni 등)을 사전에 loading시킨 Ni-loaded Mextral 272P 등의 추출제를 사용하여 반응 중 pH의 급격한 변화를 방지하고 또한 추출여액상의 금속농도를 증가시키기 위한 목적으로 일부 공정에 적용되고 있다.
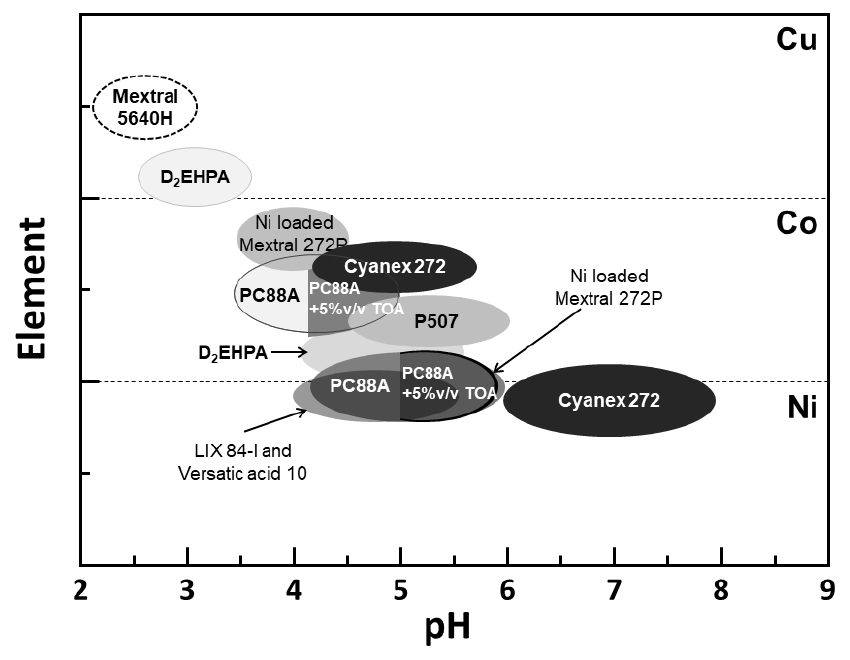
Fig. 3.
Effect of suitable pH on the solvent extraction of different extraction reagents(Source: Adapted from ref.41).
용매추출에서 계면화학반응은 주요한 추출 메커니즘이며 양성자(H+)가 방출되기 때문에 앞서 언급한 바와 같이 수용액상의 pH에 영향을 미친다40,41). O/A 계면에서 산성추출제가 해리되는 반응에 대하여 일반적으로 logD와 pH의 관계식이나 또는 logD와 log[H2R2](org)(H2R2는 추출제가 이합체(dimer) 형태인 경우) 관계식의 기울기(slope)를 분석하여 반응에 참여한 추출제 분자의 몰수를 결정하는 데 사용 된다47). 예를 들어, Cyanex 272를 사용하여 Co를 추출하는 경우 logD 대 pHe의 기울기가 대략 2.0이 나왔다면 유기상에서 Co2+ 당 2개의 수소이온(H+)이 반응하여 교환된다는 의미이다. 또한 반응식에서 logD 대 log[H2R2](org)의 기울기가 2인 경우는 4몰의 Cyanex272 가 1몰의 Co2+와 이합체 형태로 반응하여 유기상 중 Co(R2H)2 형태로 결합한다는 것을 의미한다. 연속공정을 위한 필요한 추출 단수 또는 탈거 단수를 결정하기 위해서는 상비(O/A) 변화에 따른 추출등온곡선(extraction isotherm), 즉 McCabe-Thiele 다이어그램을 작성하여 분석함으로써 다단추출에 필요한 단수를 이론적으로 결정할 수 있다48). 용매추출에서 추출 공정 후에는 후속 공정으로 세정(scrubbing)과 탈거(stripping)가 있다. 세정 공정은 추출 시 공추출 된 불순물을 제거하기 위한 단계로 세정제의 산 농도, 상비 등이 변수로 작용한다. 탈거는 유기상으로 추출된 금속 이온을 수용액으로 이동시키는 과정이며 적절한 탈거제를 사용하여 순수한 용액으로 회수가 가능하고 또한 상비 조절을 통해 고농도의 농축액으로 회수할 수 있으며, 일반적으로 사용되는 탈거제로는 황산(H2SO4)이 널리 사용된다. 용매추출 기술은 현재 현장에서 널리 사용되고 있으며 개별 금속 성분을 효율적으로 분리가 가능하여 고순도의 제품으로 생산이 가능하다. 그러나 다단추출 조작이 복잡하고 추출용매의 비용이 고가라는 단점이 있다. 따라서 향후 연구개발의 방향은 값싼 용매의 사용과 용매의 재활용에 초점을 맞춰야 할 것으로 생각한다.
3. 분리·회수 공정 분석
3.1. 단일 성분 추출 공정
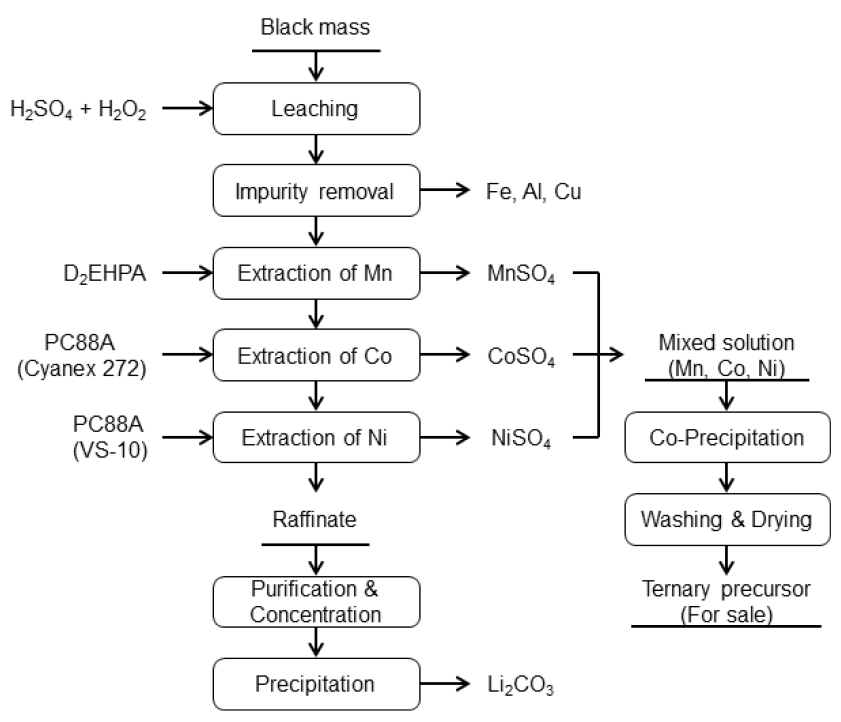
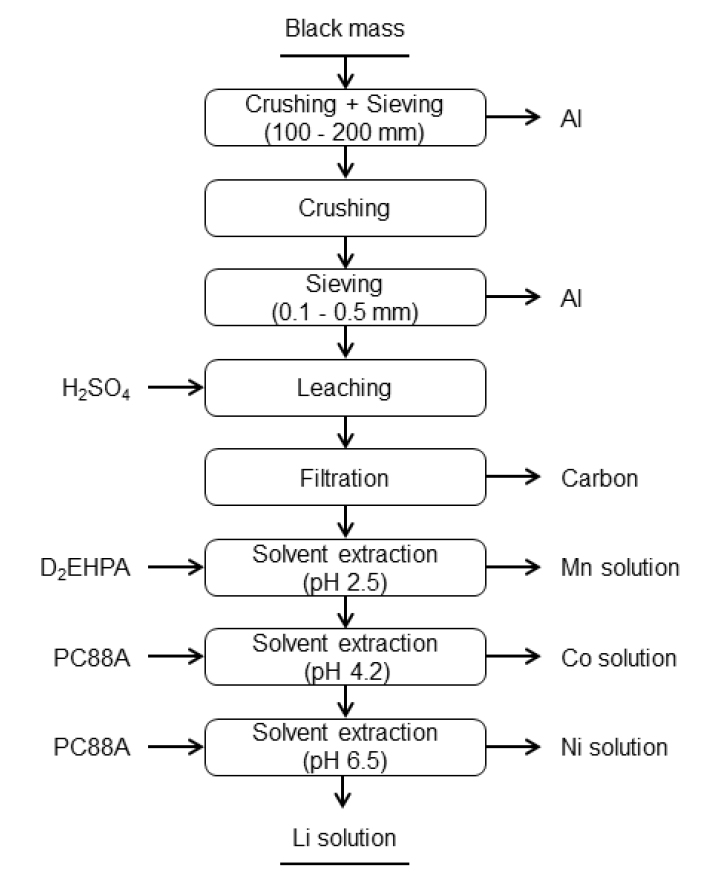
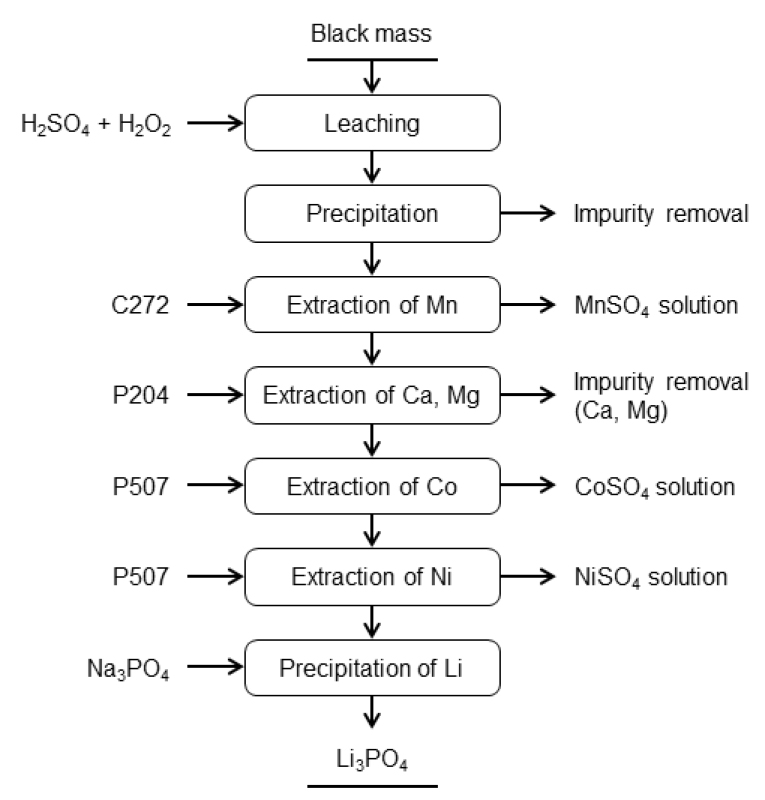
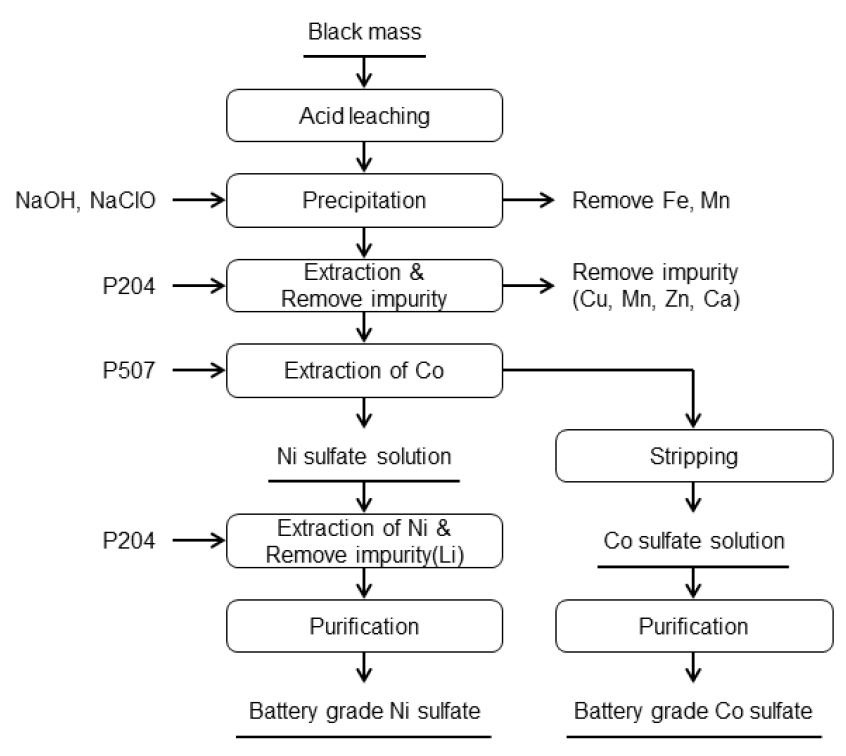
일반적으로 양극활물질 침출액에서 유가금속을 회수하는 공정은 Fig. 4와 같이 Black mass를 황산과 환원제로 과산화수소(H2O2)를 사용하여 침출한 후 불순물인 Fe, Al, Cu 등을 침전시켜 제거한 후 용매추출 공정에 의해 각 금속을 회수하고 있다. Cu의 경우는 용매추출이나 치환법으로 회수하여 재활용하는 경우도 있으며, Li의 경우는 Black mass에서 직접 회수하는 방법 또는 침출액에서 우선 회수하는 방법 등이 있고 그림과 같이 마지막 단계에서 회수하는 방법이 있다. 일반적으로 금속 성분을 회수하는 공정은 그림과 같이 Mn의 경우 D2EHPA를 사용하고 Co는 PC88A나 Cyanex272 등을 사용하여 분리한 후 마지막 단계에서 PC88A나 Versatic acid 10을 사용하여 Ni을 회수하고 있고, 추출잔액에서 Li을 회수하는 공정으로 구성되어 있다. 이때 Mn, Co, Ni은 황산염으로 회수하여 리튬배터리 3원계(NCM) 양극재 원료인 전구체 제조용으로 사용하고 있다. 이러한 공정을 채택하고 있는 곳은 국내의 성일하이텍(주)이 있고 유사한 공정으로 여러 기업에서 재활용을 하고 있다. Fig. 5는 일본의 JX Nippon사의 공정으로 전처리를 통해 불순물을 제거한 침출액에서 D2EHPA를 사용하여 pH 2.5에서 Mn을 추출하고, 추출잔액에서 PC88A를 사용하여 pH 4.2에서 Co를 추출·분리하고 이어서 PC88A를 사용하여 pH 6.5에서 Ni과 Li을 분리하여 각각 염으로 회수하고 있다49,50). Fig. 6은 중국의 화유코발트의 공정으로 Cyanex272를 사용하여 Mn을 사전에 추출하여 분리한 후 P204(D2EHPA)를 사용하여 불순물인 Ca, Mg을 제거한 후에 P507(PC88A)을 사용하여 Co와 Ni을 단계적으로 분리하여 순수한 황산코발트 및 황산니켈로 회수하고 최종 추출잔액에서 Li을 인산염으로 침전하여 회수하고 있다. 이 공정은 3가지 추출제를 사용하여 각 성분을 분리하기 때문에 공정비용이 다소 증가하는 단점이 있으나 Co 및 Ni 황산염의 순도가 높다는 장점이 있다51). Fig. 7은 Ganpower 공정으로 1차 불순물(Fe, Mn)을 침전법으로 제거하고 잔류하는 불순물(Cu, Mn, Zn, Ca)을 P204를 사용하여 제거한 후에 P507을 사용하여 Co를 추출·분리하여 황산코발트로 회수하고, 남은 추출여액에서 P204를 사용하여 불순물을 제거한 후에 Ni을 역시 배터리급 황산니켈로 회수하고 있다. 이 공정도 다소 복잡하고 다량의 폐수가 발생된다는 문제가 있다51). 이외에 Li-cycle사의 Hub 공정에서도 전형적인 추출분리 방식을 사용하고 있으며 Mn, Co, Ni을 단계적으로 추출하여 회수하고 최종 잔액에서 Li을 회수하는 공정으로 구성되어 있다. 주 생산품으로 배터리급 황산코발트, 황산니켈 및 탄산리튬을 95% 이상 회수하는 것을 목표로 공업용 MnCO3, Copper sulfide, Sodium sulfate 등과 함께 생산하는 공정으로 알려져 있다51).
3.2. 다성분 공추출(Co-extraction) 공정
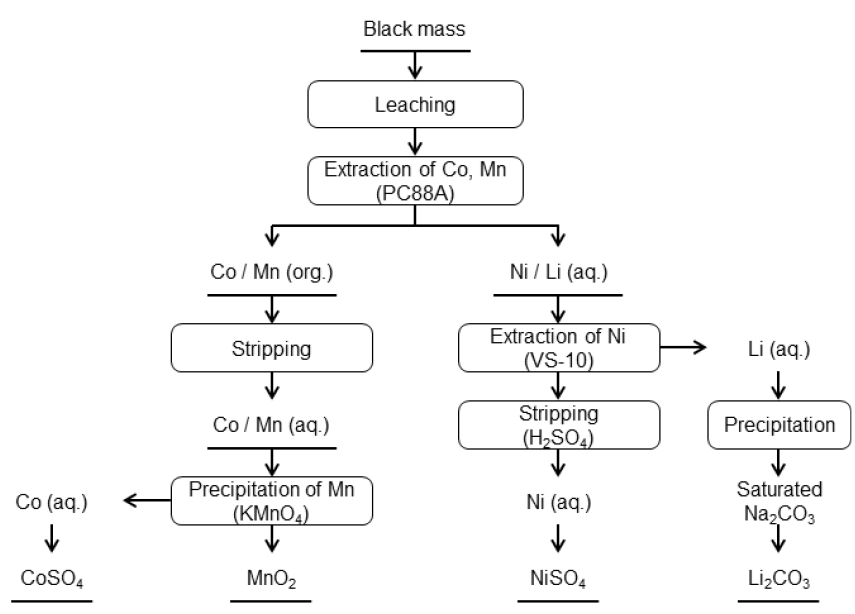
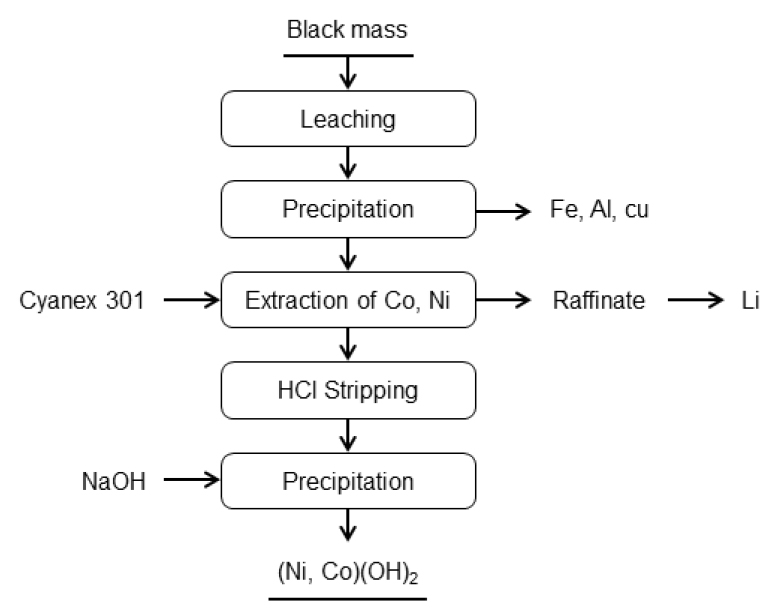
3원계 폐LIB 양극활물질 침출액에서 금속 이온을 개별 성분으로 단계적으로 분리할 경우에는 고순도의 유가금속 화합물을 회수할 수 있다는 장점이 있는 반면에 몇 가지 단점이 있다. 첫째는 침출액 중 Co, Ni, Mn의 물리적, 화학적 성질이 유사하기 때문에 개별 이온으로 분리할 경우 금속 손실이 발생하고 회수 효율이 떨어진다는 점이다. 둘째는 전체 분리 공정이 다단추출 공정으로 매우 복잡하고 긴 공정이라는 점이다. 셋째는 단일 금속으로 분리한 후에 다시 혼합하여 3원계 전구체로 합성할 경우 공정비용이 많이 소요된다는 점이다. 따라서 금속이온의 회수효율을 향상시키기 위하여 유사 분리 특성을 갖는 금속원소들을 공추출하여 전구체로 직접 합성하는 방안에 대한 관심이 증가하고 있다. 특히 High-Ni 양극재의 경우 Ni함량에 비하여 Mn 및 Co 함량이 낮다. 따라서 Mn 및 Co의 우선적 추출은 추출 공정 중 Ni 및 Li의 손실을 방지할 수 있기 때문에 High-Ni 양극재의 침출액에서 금속 이온의 분리 및 회수에 유리하다고 할 수 있다. 이에 대한 기초 연구로 Y. Yang 등은 Fig. 8과 같이 LiNi0.5Co0.2Mn0.3O2 침출액에서 Mn과 Co를 하나의 원소로 생각하여 2성분(Mn, Co)을 공추출하여 Ni와 Li로부터의 분리하는 연구를 하였다52). Mn 및 Co의 공추출은 pH = 5, O/A = 2 및 30vol% PC88A에서 98% 및 90% 이상 가능하고, 이후 Mn과 Co혼합용액에서 Mn은 KMnO4를 사용하여 MnO2로 Co의 경우는 CoSO4 용액을 회수하고, Ni와 Li혼합용액의 경우는 Versatic 10으로 분리하여 각각 염으로 회수하는 공정을 제시하였다. W.S. Chen 등은 0.1M Cyanex272를 사용하여 pH 6.0, 상비 1.5에서 Co 와 Mn 그리고 Ni 과 Li의 두 그룹으로 분리하고, Co와 Mn은 다시 0.2M D2EHPA를 사용하여 pH 2.95, 상비 1.0에서 분리하였다. 또한 Ni 와 Li 혼합용액에서 Ni성분을 DMG(dimethylglyoxime)를 사용하여 침전법으로 회수하는 공정을 제안 하였는데 이때 회수된 Co, Ni, Li 화합물의 순도는 99.5% 이상이고 Mn화합물의 경우는 90% 이상이라고 발표하였다53). 또한 Zhao 등은 Mn, Co 및 Li이 함유된 침출액에서 Al과 Fe를 제거한 후에 Mn과 Co를 공추출할 경우, pH = 4.95에서 혼합추출제(0.05M Cyanex272+0.05M PC88A)를 사용할 경우 추출률이 상승한다고 발표하였다54). Y. Yang 등은 침출액에서 D2EHPA를 추출제로 사용하여 Co, Mn, Ni 3성분을 공추출하여 Li 성분과 분리하는 연구를 실시하였다. NCM111 침출용액에서 40% D2EHPA를 사용하여 O/A = 1, pH = 3.5에서 99% Co, 100% Mn 및 85% Ni을 공추출하고 0.5M H2SO4로 탈거한 후 용액의 성분 조절을 거쳐 수산화물로 3성분을 공침시켜 Ni1/3Co1/3Mn1/3(OH)2 형태의 양극재 전구체로 제조가 가능하다고 제시하였다55). 이와 비슷한 개념으로 L. Shuya 등은 Ni-rich 양극재 침출용액에서 Versatic acid 10을 사용하여 Co, Ni 및 Mn을 공추출하는 연구 결과를 발표하였다. 침출액의 pH 6.0에서 Ni, Mn, Co 성분을 공추출시 추출률은 각각 97.05%, 99.18%, 98.47%이었고, 이때 회수되는 Li2CO3의 순도는 약 99.61%이었고 Li의 손실율은 8% 정도 이었다. 연구결과 Ni, Co, Mn의 공추출을 통하여 고농도의 Ni, Co, Mn 혼합용액을 얻을 수 있으며, 이를 직접 양극재 재생하는데 직접 사용할 수 있다고 제안하였다56). E.Y. Kim 등도 불순물(Fe, Al 등)을 제거한 폐양극활물질 침출액에서 카르복실산계 유기용매인 네오데칸산(Neodecanoic acid) 혹은 Versatic acid 10을 사용하여 Co, Ni, Mn 성분을 동시 추출하여 3성분 혼합염으로 회수하여 전구체 원료로 사용 가능성이 있다고 발표하였다. 이 경우 추출제로 D2EHPA를 사용하는 것보다 3성분(Co, Ni, Mn)과 Li 성분의 분리가 쉬우며, 특히 중화제 사용에 의한 Ca, Mg 등의 불순물 함량이 높은 경우에도 별도의 불순물 제거 공정 없이 고순도의 전구체 제조용 3성분 혼합용액을 제조할 수 있다고 보고하였다57). C. Liu 등은 LIB 양극물질(NCM622, NCM811)을 염산으로 침출한 용액에서 0.6M P227(Di-2-ethylhexyl phosphinic acid)을 사용하여 pH 2.5에서 3성분(Ni, Co, Mn)을 공추출한 후에 탈거하여 옥살산을 사용하여 공침전시켜 3성분 복합전구체를 제조하는 연구결과를 발표하였다58). 한편, Y.C. Cho 등은 Fig. 9와 같이 Cyanex 301을 추출제로 사용하여 일부 불순물을 침전 제거시킨 후 Co와 Ni만을 선택적으로 공추출하고 탈거후 [Co,Ni]복합염이나 단일염으로 회수할 수 있는 공정을 제시하였다. 이 방법은 특히 강산성(pH 1.5 이하)용액에서 Co와 Ni을 공추출함으로서 중화에 따른 NaOH 사용량을 대폭 절감할 수 있고 또한 Mn, Ca, Mg이 불순물로 존재할 경우 Co와 Ni을 선택적으로 추출·분리하는데 효과적이다59).
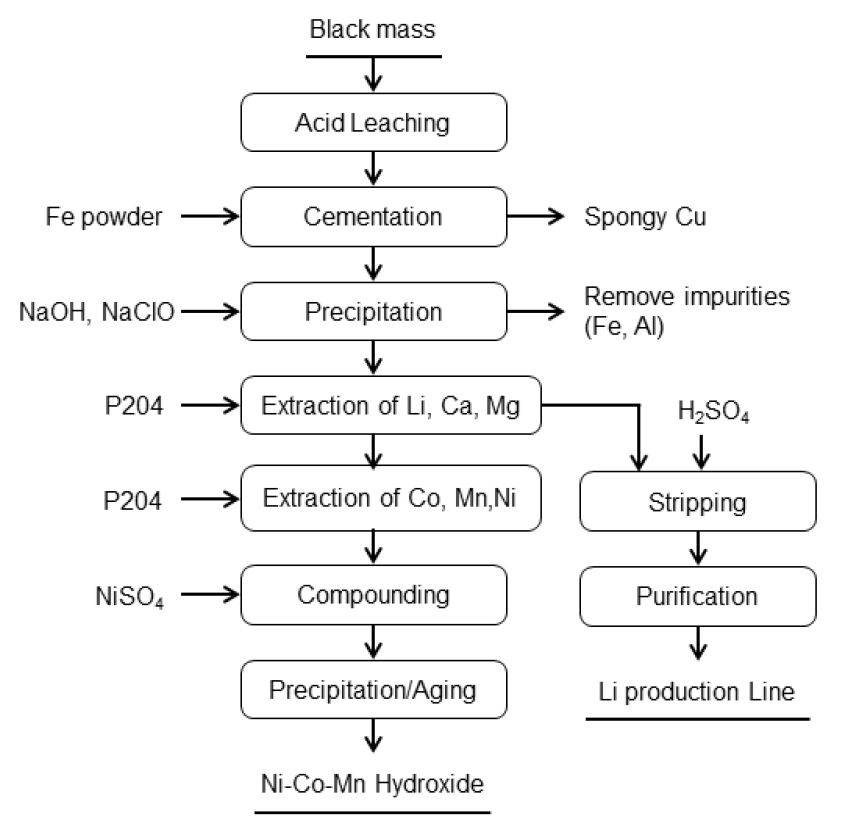
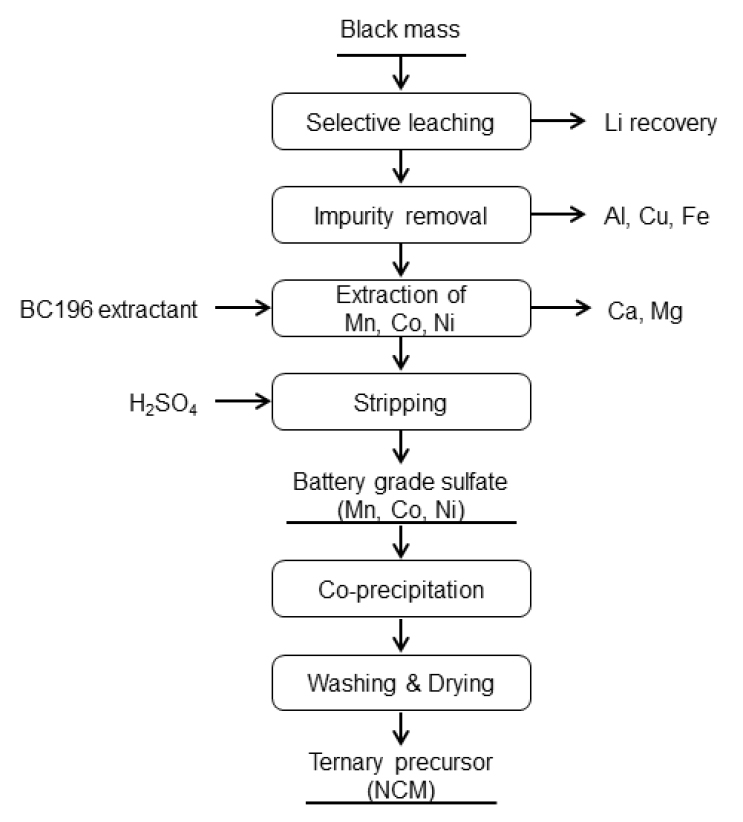
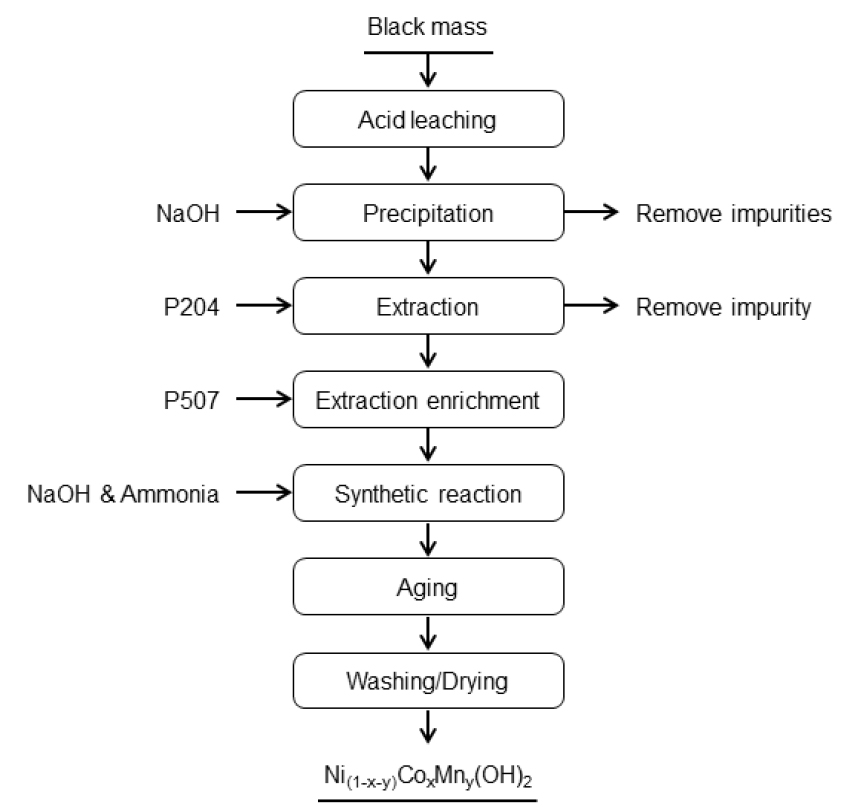
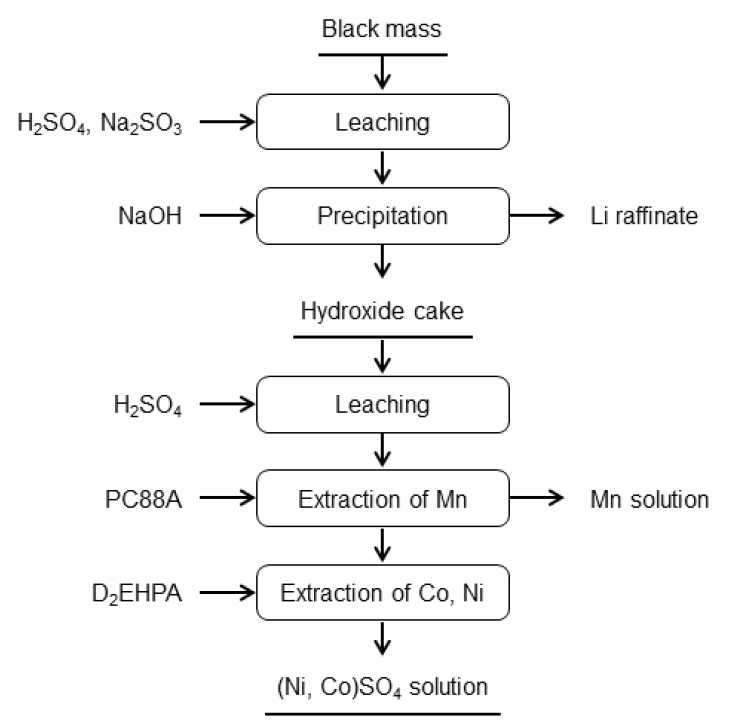
이와 같이 3성분(Ni, Co, Mn) 공추출 방식은 재활용 공정을 단순화하고 분리 효율을 개선할 수 있고 회수된 복합염을 전구체로 바로 사용함으로써 제조비용을 절감할 수 있는 공정이라 할 수 있으며 현재 일부 상용화된 공정을 소개하면 다음과 같다. 중국의 Brunp사의 경우 Fig. 10과 같이 Black mass 황산침출액에서 먼저 Cu 성분을 Fe powder를 사용하여 치환시켜 spongy 형태로 회수하고 이어서 Fe와 Al을 pH 2.0~2.4에서 침전 제거시킨다. 이후에 이 용액에서 1차로 P204를 사용하여 Li, Ca, Mg을 추출하여 Li 성분을 회수하고 다시 2차로 P204를 사용하여 3성분(Co, Mn, Ni)을 공추출하여 황산염으로 회수한 후 공침전 시켜 3성분(Ni, Co, Mn) 복합수산화물로 회수하고 있다. 이 공정의 특징은 P204만을 사용하여 반복된 추출방식을 통해 3성분 복합염으로 회수하는 공정으로 전처리 공정은 비교적 간단하나 분리 공정이 다소 복잡하고 공정이 길다는 단점은 있으나 회수된 화합물의 순도가 높고 3성분(Ni, Co, Mn)의 회수율은 99.3% 이상이라고 알려져 있다51). 중국의 Botree사의 공정은 Fig. 11와 같이 Black mass에서 선택적 침출을 통해 먼저 Li을 분리하여 회수하고 남은 용액에서 Al, Cu, Fe를 침전 제거한다. 이후에 BC196이라는 추출제를 사용하여 3성분(Mn, Co, Ni)을 공추출 하여 불순물인 Ca, Mg을 제거한다. 이후 공추출 된 유기상에서 3성분을 황산으로 동시 탈거한 후에 공침전을 통해 3성분 NCM계 전구체를 제조하는 공정을 실시하고 있다51). 또한 GEM사의 경우 Fig. 12과 같이 Black mass 침출용액에서 1차로 NaOH에 의한 침전법으로 불순물을 제거한 후 2차로 P204를 추출제로 사용하여 불순물을 제거한 후 다시 P507을 사용하여 3성분(Mn, Co, Ni)을 공추출 및 농축을 한 후에 3성분 NCM계 전구체용 수산화물을 제조하는 것으로 알려져 있다51). 한편, 국내 S사의 경우 Fig. 13와 같이 H2SO4 및 Na2SO3를 사용하여 Black powder에서 금속성분을 침출시킨 후 먼저 NaOH를 사용하여 Mn, Co, Ni 등 주요 금속성분을 수산화물로 침전시켜 Li 성분과 분리하고, 이 침전물을 H2SO4를 사용하여 다시 침출시킨 후 침출액중의 Mn을 PC88A를 사용하여 먼저 선택적 추출·분리하고 남은 용액에서 D2EHPA를 사용하여 Ni 및 Co의 2성분을 공추출하여 혼합용액으로 회수하여 전구체 원료로 사용하는 공정이다60).
3.3. Pre-loading 용매추출 공정
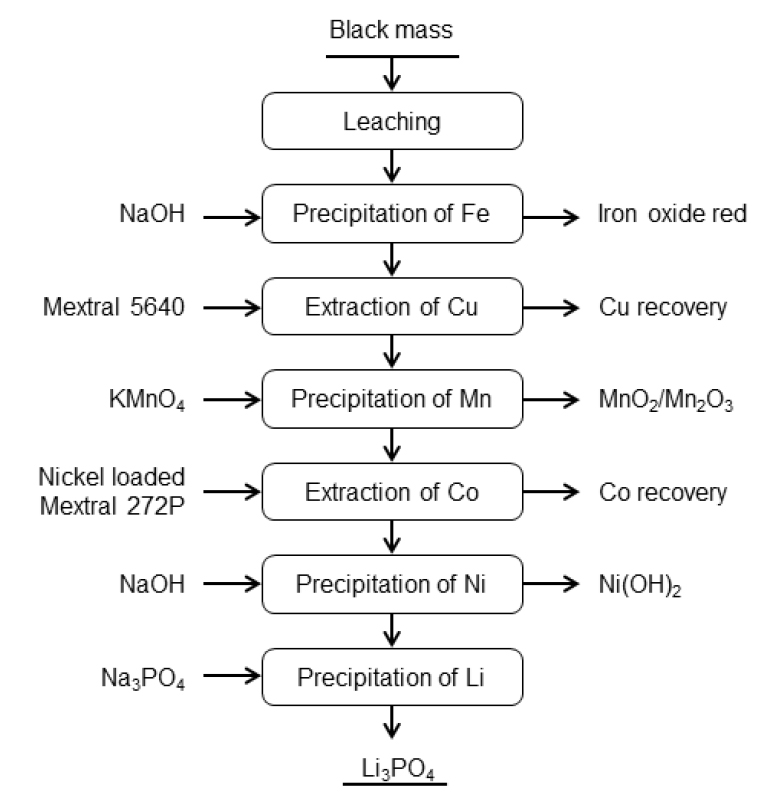
현재 용매추출 공정은 산성추출제를 사용하여 다단추출방식으로 진행되기 때문에 각 추출 공정에서 비누화된 추출제를 사용한다. 비누화된 추출제를 사용할 경우 추출여액으로 Na의 혼입 등 여러 가지 문제가 발생되는데 이를 해결하기 위해 Ni-Cyanex 272나 Co-D2EHPA와 같이 금속 성분을 Pre-loading 시킨 추출제를 사용하는 방법이 있다. 이러한 추출제를 사용할 경우에는 추출 단계에서 금속염 발생으로 인한 추출 효율성 감소 현상을 개선할 수 있고, 추출여액 중 Na혼입이 감소되어 고순도 금속용액을 얻을 수 있으며 또한 추출제에 loading된 금속성분이 추출 반응 후에 수용액상으로 이동되어 고농도의 금속농축액으로 회수가 가능하여 후속 공정을 단축시킬 수 있다는 장점이 있다61). 이에 대한 연구로 M.C. Olivier62) 등은 황산니켈 정제 공정에 적용하고자 하였다. Co(1g/L) 및 Fe(3g/L)이 함유된 황산니켈용액(80g/L)용액에서 Ni-Cyanex 272를 사용하여 Co 및 Fe 분리에 관한 연구를 하였다. 이 경우 추출에 가장 큰 영향을 미치는 요인은 상비(O/A)와 Pre-loading된 Ni 농도이고, 추출실험 결과 대부분의 Fe 성분과 95~96%의 Co를 분리·추출이 가능하였고 추출여액에서 고순도의 황산니켈 용액의 제조가 가능하다고 제안하였다. X. Chen63) 등은 Fig. 14와 같이 폐리튬배터리 침출용액에서 Fe, Cu, Mn을 제거 후에 Ni을 Preloading 한 Ni-Mextral®272P 용매를 사용하여 Co를 먼저 추출하고 남은 추출여액에서 Ni의 경우는 NaOH를 사용하여 Ni(OH)2로 회수하고, Li의 경우는 Li3PO4 형태로 회수하는 공정을 제안하였다. 또한 Fig. 15와 같이 침출용액에서 Fe을 먼저 침전시켜 제거하고 이어서 Ni을 DMG(dimethylglyoxime)를 사용하여 선택적으로 침전시켜 회수한 후에 남은 3성분(Co, Mn, Li) 혼합용액에서 Co를 preloading한 D2EHPA를 사용하여 Mn, Co 및 Li을 회수하는 연구를 하였다. 이 경우 15vol.% Co-D2EHPA를 사용하여 pH 3.5, O/A = 1, 2단으로 97.1~99%의 Mn이 회수가 가능하며 추출여액에서 Co는 옥살산염으로 회수한 후에 남은 용액에서 Li을 Li2CO3로 회수하는 공정을 제시하였다64). D.H. Kim65) 등은 침출액 중의 Fe을 과산화수소 및 수산화니켈(Ni(OH)2)을 첨가하여 침전·제거하고 이어서 Ni-D2EHPA를 사용하여 침출액으로부터 1차로 Mn을 추출하여 MnSO4 용액으로 회수하고, 2차로 Ni-PC88A를 사용하여 Co를 추출·분리하여 CoSO4용액으로 회수한 후에 추출여액에서 직접 NiSO4용액을 회수하는 연구를 실시하였다.
3.4. 불순물 제거 후 공침(Co-precipitation)에 의한 회수 공정
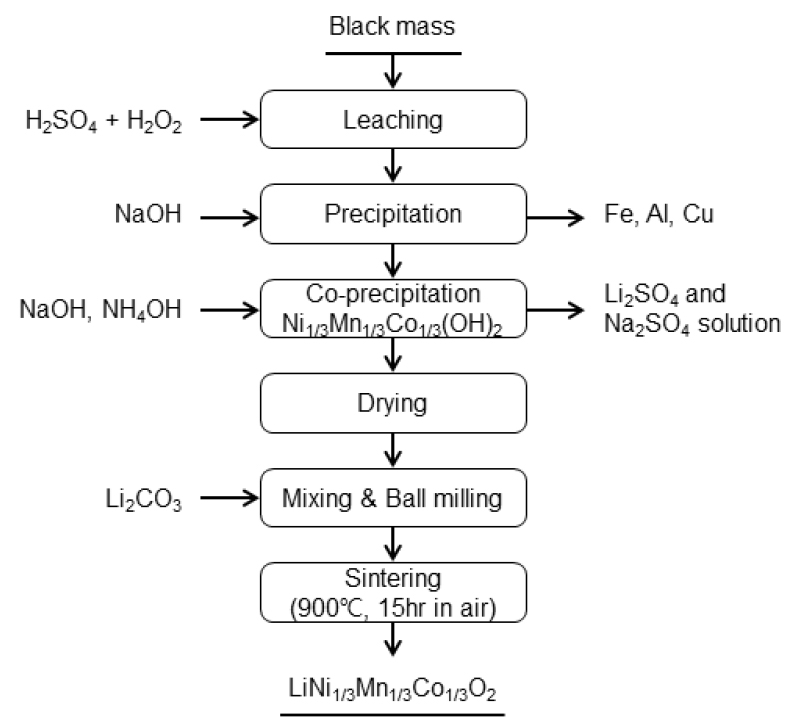
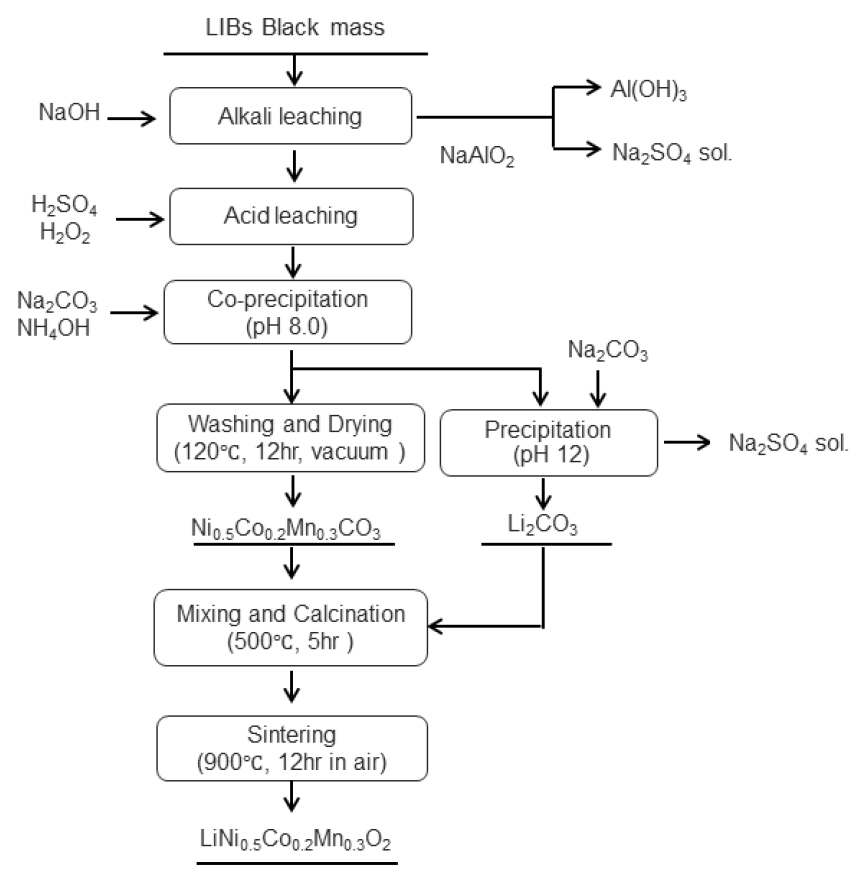
Black mass 침출액에서 전구체용 금속화합물을 제조하는 방법 중 하나는 침출액에서 불순물을 먼저 제거 시킨 후에 용매추출 공정을 거치지 않고 3성분(Ni, Co, Mn)을 공침전 시켜 NCM 복합황산염 용액으로 회수하는 방법으로 Fig. 16에 공정 개략도를 나타내었다. 그림에서와 같이 Black mass를 황산과 과산화수소를 사용하여 침출시킨 용액을 먼저 NaOH를 사용하여 Fe, Al, Cu 성분을 수산화물로 공침시켜 제거하고, 남은 3성분(Mn, Co, Ni)황산염 용액의 몰비를 조절한 후에 NaOH와 NH4OH를 사용하여 pH 11 부근에서 수산화물(Ni1/3Mn1/3Co1/3(OH)2) 형태로 공침시킨다. 이후에 건조 공정을 거쳐 Li2CO3와 혼합하여 소결과정을 거친 후에 양극재용 산화물(LiNi1/3Mn1/3Co1/3O2)로 제조하는 방법이다66,67,68,69,70,71). 이 방법은 복잡한 용매추출 공정을 사용하지 않고 침전법만으로 전구체를 제조할 수 있는 비교적 공정도 간단하고 금속의 회수율도 높은 편이나 균일한 성분 조절이 어려워 전구체의 균질도를 감소시킬 수 있다는 단점이 있다. 이 방법은 Ascend Elements, American Manganese Inc 그리고 Li-Cycle 등에서 유사한 공정을 실시하고 있다. 한편, 침출액 중에서 3성분을 침전시키기 위해서 탄산염을 사용하는 방법도 있다. J. Fang 등은 불순물이 제거된 Black mass 황산침출액중에 Ni:Co:Mn의 몰비를 5:2:3으로 조절한 후에 Na2CO3용액(2mol/L)과 NH3∙H2O(0.4mol/L)를 첨가하여 pH 8.0으로 조절하여 55℃에서 12 h 침전반응에 의해 탄산염으로 3성분을 공침시켰다. 이후 세척과 건조과정을 거쳐 탄산염(Ni0.5Co0.2Mn0.3CO3)전구체로 제조한 후에 Li2CO3와 반응시켜 양극재용 산화물(LiNi0.5Co0.2Mn0.3O2)로 제조가 가능하다고 보고하였다. 이에 대한 공정 개략도를 Fig. 17에 나타내었다72). L. He 등은 침출액중의 Ni:Co:Mn의 몰비를 순수한 NiSO4·6H2O, CoSO4·7H2O 및 MnSO4·H2O를 사용하여 1:1:1로 조절한 후에 Na2CO3용액(1.8mol/L)과 일정량의 NH3·H2O를 첨가하여 pH를 7.5로 조절하고 60℃에서 12 h 침전반응에 의해 탄산염(Ni1/3Co1/3Mn1/3CO3) 전구체로 합성한 뒤 최종적으로 양극재용 산화물(LiNi1/3Co1/3Mn1/3O2) 제조가 가능하다고 하였다. 이와 같이 침전제로 Na2CO3를 사용할 경우, NaOH를 사용하는 것보다 안정하고 균일한 탄산염으로 공침이 가능하고 가격 면에서도 절감할 수 있다고 보고하였다73).
4. 결론 및 전망
본고에서는 폐LIB를 회수하는 공정 중 분리·회수 공정을 분석하여 각 공정에 대한 설명과 문제점에 대해 검토하였다. 이를 통해 폐LIB를 효과적이고 친환경적으로 회수하기 위해 필요한 연구개발 방향을 다음과 같이 제시하고자 한다. 폐LIB에서 가치 있는 금속을 회수하기 위해서는 Black mass에서 금속원소를 침출시켜 분리하는 것이 필수적인 과정이며, 강산과 환원제가 사용된다. 강산을 사용함에 따라 유해가스와 폐산이 발생한다. 앞으로는 작업자들의 안전과 환경보호를 위해 강산의 사용을 줄이거나 아예 사용하지 않는 방법의 개발이 필요하다. 강산 대신 유기산을 사용하는 것이 대안이 될 수 있으나 유기산의 사용은 처리비용의 상승을 가져온다. 따라서 침출 후 유기산을 재사용할 수 있는 기술이나 또는 저가의 유기산을 생성하여 침출에 사용할 수 있는 미생물 배양 기술 등을 융합한 기술을 개발하여 경제성이 있는 공정 개발이 필요하다고 할 수 있다. 또한 특정 금속에 대한 선택적 침출이 가능하고 침출효율이 좋으며 가격이 저렴하고 친환경적인 용매로 알려져 있는 Deep Eutectic solvents(DESs) 를 사용한 기술개발도 필요하다.
침출액 중에서 유가금속의 추출과 회수 과정에서도 사용되는 용매나 화학약품 양을 최소화하고, 저렴하고 친환경적으로 금속을 회수할 수 있는 기술의 개발이 필요하며 공정을 최대한 간단하게 구성하고, 가급적 용매추출 공정을 줄일 수 있는 공정 구성이 필요하다. 이를 위해 침출액중의 불순물을 제거한 후 바로 3성분(Mn, Co, Ni)을 침전법으로 회수하거나 또는 침출용액중의 3성분(Mn, Co, Ni) 또는 2성분(Co, Ni 또는 Co, Mn)을 동시 추출하여 NCM계 복합체로 회수하여 전구체용 원료로 제공할 경우 복잡한 공정을 단축하고 보다 저렴하게 전구체를 제조할 수 있는 방안이 될 수 있다. 또한 처리공정 중 발생하는 폐수용액(Na2SO4)의 저감 방안이나 재활용할 수 있는 기술 개발이 필요하며 Electro-membrane74) 등의 공정 개발을 통해 폐수무방류 시스템(Zero Discharge System)을 구축하는 것도 필요하다고 할 수 있다.
습식 공정의 주요 이점은 고순도로 폐배터리로부터 새로운 배터리 전구체를 생산할 수 있다는 것이다. 비록 많은 양의 화학약품을 사용하지만 습식 제련은 수년 동안 많은 용매와 부산물을 재활용함으로써 전체 2차 폐기물 생성을 최소화 할 수 있었다. 미래의 배터리 법안과 더 높은 소재 회수율에 대한 요구에 친환경 습식 공정 기술은 아직 해결해야할 문제는 있지만 향후 배터리 재활용 시장에서 순환 경제로 가는 가장 유망한 접근 방식이라고 할 수 있다.