1. 서 론
2. 실험방법
3. 결과 및 고찰
3.1. 2차분진(2nd-Dust)의 용해 및 고상/액상 분리
3.2. Cementation에 의한 여과액의 정제 및 Zn-탄산염제조
3.3. 고/액 분리한 고형물(Pb-Cake)의 수용액 정제와 Pb-탄산염제조
4. 결 론
1. 서 론
세계 각국에서 발생되고 있는 전기로제강 부산물 중에서도, 특히 분진부산물들은 1970년 전까지는 특별한 처리방법이 개발되지 않아서 주로 매립되고 있었다. 그러나 자원이 고갈되기 시작한 근년에 와서는 시멘트공장의 철원(Fe-Source)으로 주로 사용되기 시작하였으며, 최근에는 선진공업국에서 아연성분을 조산화아연 및 정제산화아연의 형태로 재활용할 수 있는 기술을 개발하여 상업화에 성공하였다1,2,3). 국내에서도 다수의 전기로제강분진의 자원화플랜트가 가동되고 있으며, 현재 국내의 전기로제강 분진발생량은 년간 약40만톤에 달하며, 분진의 조성은 사용하는 고철의 종류 및 제강사의 조업조건에 따라 다소의 차이는 있다4).
특히, 고온의 전기로제강 조업과정에서 용융점이 낮으며 높은 증기압을 나타내는 Zn, Pb, Cd 등은 다른 성분보다 먼저 휘발되어 전기로 외부로 배출되는 과정에서 산화되어 산화물의 형태로 백필터(Bag Filter)에 포집되게 된다5,6,7). 이러한 제강분진 내에는 유해한 중금속원소들도 다량 함유되어 있기 때문에 대부분의 국가에서는 지정폐기물로 분류하고 매립을 금지하고 환경법으로 재활용을 의무화하고 있다. 특히, 자원이 부족한 우리나라의 현실을 고려하면, 전기로제강분진에서 유가금속을 회수하는 것은 대단히 중요한 과제라고 생각된다.
국내에서도 현재 Rotary Kiln Process와 Rotary Hearth Furnace(RHF) Process를 이용한 상업화플랜트가 가동되고 있다. 기본적인 반응측면에서 이들 프로세스는8) 탄소환원재(코크스, 무연탄)로 분진 중의 유용금속산화물들을 환원/휘발시켜 슬래그성분과 분리(Clinker)한 후에, 휘발된 금속원소(Zn, Pb, Cd 등)들을 반응기 내의 산소와 반응시켜 조산화아연(76% ZnO)의 형태로 회수한다는 점에서는, 매우 유사한 프로세스라고도 할 수 있다.
회수된 조산화아연 중에는, Zn, Pb, Cd, Cu, Cr 등과 같은 대표적인 유용금속성분 뿐만 아니라 K, Na, Cl, F, Si 등과 같은 비금속성분들도 산화물과 염화물의 형태로 다량 함유되어 있는데, 이러한 비금속성분들 중에서도, 특히 Cl 및 F는 아연전해시의 생산성에 악영향을 미치므로, 조산화아연의 경제적 가치를 크게 낮추기 때문에 이들 성분원소들을 효과적으로 제거할 수 있는 건식휘발 또는 습식세척에 의한 정제공정이 적용되고 있다9,10). 습식세척공정(Washing Process)은 조산화아연 중에 함유된 아연성분을 제외한 기타의 성분원소들의 염화물을 수용액 또는 저농도의 산용액에 용해하여 제거하는 정제방법이며, 건식정제공정은 특히 조산화아연 중에 다량으로 함유되어 있는 염소(Cl)성분이 Zn에 비하여 Pb와 더욱 용이하게 염화물을 생성하여 쉽게 휘발한다는 물리화학적 특성을 응용한 방법으로, 종합적으로 볼 때에 건식정제법이 습식세척법 비하여 훨씬 더 경제성이 우수하며 효율적으로 고순도의 산화아연(약99% ZnO)를 생산할 수 있는 방법이라고 사료된다11). 그러나 이와 관련한 연구결과는 거의 찾아보기 어렵다. 따라서 본 연구에서는 조산화아연의 건식정제과정에서 백필터에 포집된 Zn과 Pb를 함유하는 2차분진(2nd-Dust)으로부터 Zn 및 Pb를 효율적으로 분리하고, 더욱 부가가치를 높이기 위하여 이들 성분원소들을 금속(Zn, Pb 등)탄산염의 형태로 회수할 수 있는 가능성에 대한 기초적인 연구를 수행하였다.
2. 실험방법
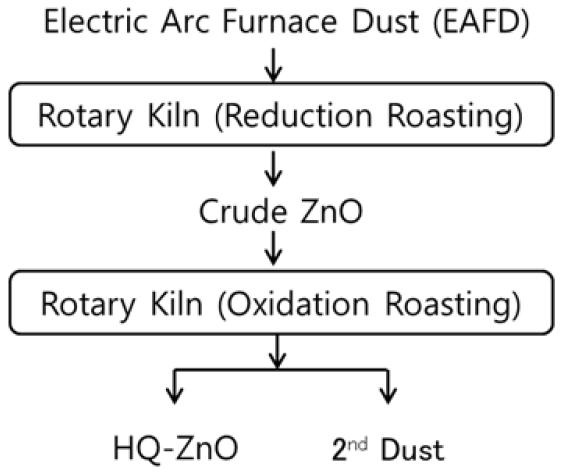
본 실험에서는 Table 1에 나타낸 조성의 전기로 제강분진에 코크스와 석회석을 첨가하여 직경 1~5mm의 pellet으로 성형/건조 후에, Fig. 1에 나타낸 1단계의 Rotary Kiln(환원반응)에 장입(1150°C)하여 Table 2에 나타낸 조성의 조산화아연(Crude-ZnO)을 회수하였다. 회수된 조산화아연은 2단계의 Rotary Kiln(산화반응)에 장입(1200°C)하여 Table 3에 나타낸 것과 같은 조성의 고순도산화아연(High Quality-ZnO : HQ-ZnO)과 정제과정에서 발생한 배가스에 포함된 휘발물질들을 백필터로 포집한 Table 3의 조성의 2차분진(2nd- Dust)을 회수하여 실험에 사용하였다.
Table 1.
Chemical composition of Electric Arc Furnace Dust(EAFD)
| Elements | Zn | Fe | Ca | Si | Pb | S | Na | K | Cl |
| Amount(wt%) | 23.0 | 32.8 | 4.8 | 1.3 | 0.8 | 0.3 | 1.25 | 2.2 | 2.8 |
Table 2.
Chemical compositon of Crude Zinc Oxide
| Elements | Zn | Fe | Ca | Si | Pb | S | Na | K | Cl |
| Amount(wt%) | 60.1 | 1.7 | 0.7 | 0.4 | 3.47 | 0.1 | 2.7 | 5.6 | 8.7 |
Table 3.
Analysis result of HQ-ZnO and 2nd-Dust
| Elements | Zn | Pb | Cu | Fe | Na | K | Sn | Cd | Cl | S | F |
| HQ-ZnO(wt%) | 77.0 | 0.03 | - | 1.2 | 0.18 | 0.04 | 0.024 | 0.004 | - | 0.23 | 0.1 |
| 2nd-Dust(wt%) | 4.88 | 15.9 | 0.03 | 0.08 | 10.0 | 14.6 | 0.05 | 0.35 | 46.1 | - | - |
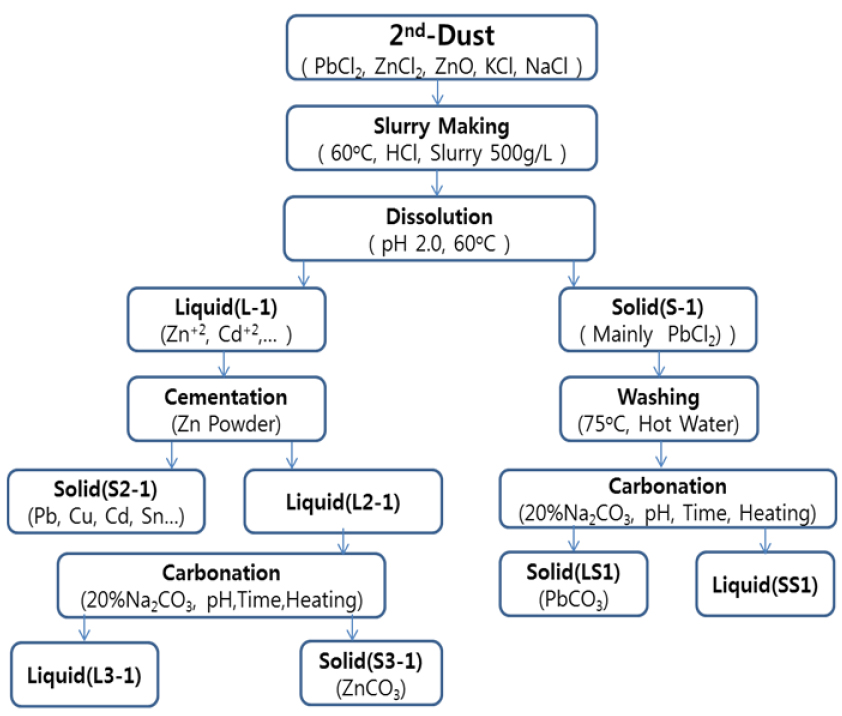
포집된 2차분진(2nd-Dust) 중의 Pb와 Zn의 분리방법으로는 건식법인 환원휘발법과 수용액에 대한 Pb염화물과 Zn염화물의 용해도의 차이를 이용한 습식법이 있다. 환원휘발법에 의한 Pb와 Zn의 분리방법은 분리된 Pb염화물 내에 소량의 Zn 또는 기타 원소들이 함유되어 있어도 환원반응에 의한 Metal-Pb을 제조하고자 할 때에, Pb의 회수율 및 순도를 크게 낮추므로 실용화에 문제점이 있다. 그러나 2차분진(2nd-Dust)은 주로 수용액에 대한 용해도가 큰 염화물들로 이루어져 있으므로, 본 실험에서는 습식법을 선택하였으며 2차분진 중의 ZnO 또는 Zn화합물들로부터 Zn을 가능하면 수용액 중으로 용출시키기 위하여 HCl(aq)를 사용하여 pH=2로 장시간 유지하였다. Fig. 2에 Pb와 Zn의 효율적인 분리공정도를 나타내었다.
한편, Fig. 2에 나타낸 여과용액 중에는 Pb, Cd, Sn, Cr, Fe, K, Cl 등과 같은 많은 성분들이 다량으로 함유되어 있어서, 용액중의 Zn의 순도를 더욱 높이기 위하여 Zn과의 이온화 경향의 차이를 이용한 Zn-Cementation처리를 실시하여 Zn을 제외한 성분들을 가능하면 고형물로 석출시키고자 하였다12). 따라서 수용액 중에 존재하는 석출시키고자 하는 성분원소들의 함유량에 대하여 1.5~3.0배당량의 Zn분말(99.9% Zn)을 첨가하고 상온에서 10분 동안 시간에 따른 pH변화와 Cementation거동을 조사하였다. 그리고 Cementation 후에 여과/분리한 Zn-여과액을 60℃로 가열하면서, 반응속도와 반응과정을 관찰하기 위하여 20% Na2CO3(aq)을 소량씩 첨가하면서, Zn계 탄산염의 생성거동을 관찰하였다. 한편 2차분진을 용해하여 얻은 고형물(Pb-Cake이라고 함)은 수차례 순수(Pure Water)로 세척하여 Pb염화물(Pb Cake)의 순도를 높인 후에, 다시 슬러리화한 용액에 동일한 방법으로 20% Na2CO3(aq)을 소량씩 첨가하면서 Pb계 탄산염의 생성거동을 조사하였으며, 여과액중의 성분의 농도 및 석출물의 물질종류와 형상 등을 ICP(In ductively Coupled Plasma Spectrometer; Optima 7000DV, PerkinElmer), XRD(X-ray Diffractometer; NL/X Pert PROMPD, PANalytical) 등으로 조사하였다.
3. 결과 및 고찰
3.1. 2차분진(2nd-Dust)의 용해 및 고상/액상 분리
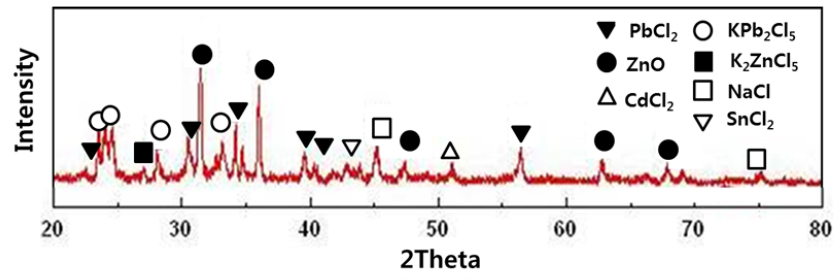
조산화아연을 재차 2차 Rotary Kiln(산화성 분위기)에 장입하여 정제하는 과정에서 발생하여 Bag Filter에 포집된 2차분진(2nd-Dust)에 대한 XRD분석결과를 Fig. 3에 나타내었다. Fig. 3으로 부터 2차분진은 PbCl2, KPb2Cl5, K2ZnCl5, NaCl, SnCl2, CdCl2와 같은 염화물과 ZnO와 같은 산화물들이 혼재되어 있음을 알 수 있다. 이들 염화물 중에서도 PbCl2는 수용액에 대한 용해도가 매우 작으나 NaCl, KCl, SnCl2, CdCl2는 수용액에 대한 용해도가 대단히 크다. 따라서 주요 성분인 Pb와 Zn을 간단하게 분리할 수 있는 방법으로는 이들 화합물들의 수용액에 대한 용해도의 차이를 이용하여 용해도가 작은 PbCl2는 고체상에 남기고, NaCl, KCl, SnCl2, CdCl2는 수용액에 용해시켜 분리하는 것이 가장 편리한 방법이라고 사료된다.
한편 난용성의 ZnO(또는 Zn계 복합화합물)의 경우는 가열상태에서 HCl을 첨가하면 식 (1)과 같은 반응이 가능하므로, 더욱 Zn과 Pb를 용이하게 분리할 수 있다고 사료된다.
Fig. 4에, 2차분진에 함유된 Pb와 Zn을 수용액에 대한 용해도의 차이를 이용하여 분리하기 위한 슬러리화 장치(Fig. 4(a),(b)), 고/액 분리장치 그리고 분리된 고형물(Pb-Cake)과 수용액(Fig. 4(c))을 나타내었다. 2차분진(2nd-Dust) 200g을 400mL의 순수(Pure Water)에 용해하고(pH=4.0), 분진중의 난용성화합물들을 용해시키기 위하여 60℃로 가열하면서 염산(500g/L)을 첨가하여 pH=2.0(±0.2)으로 유지하였다. 이때 2차분진에 함유된 난용성화합물들로부터 성분이 용해되는데 시간이 소요되므로 pH를 2.0으로 안정화시키는데 약3시간이 소요되었으며, pH값이 안정된 후에도 추가로 2시간을 더 정치한 결과 하부에는 갈색의 고체상(Solid Phase), 상부에는 녹색의 액체상(Liquid Phase)으로 분리되었다(Fig. 4(C)). 이와 같이 액체상이 녹색을 띄는 것은 액체 중에 미량으로 존재하는 Cu와 Cr의 영향이라고 사료된다. 그리고 분리시간의 단축을 위하여 Suction Filtering을 하였으며, 분리된 고체상은 먼저 여과액으로 2회 세정한 후에 다시 50ml의 순수로 2회 세정하였으며, 이때 여과액에 곧 바로 수산화물로 판단되는 백색고형물이 생성되기 시작하였다. 그리고 용해하기 전의 2차분진(2nd-Dust)의 무게와 용해/분리/건조후의 Cake의 무게비로부터 구한 침출율은 약76%였다. 여과액(L-1)과 건조한 고형물(S-1:Pb-Cake)에 대한 분석결과를 Table 4와 Table 5에 각각 나타내었다.
Table 4.
ICP Analysis results of 1'st Filtering Solution(L-1)
| Elements | Zn | Pb | Cr | Fe | Cu | Cd | Sn |
| Amount(mg/ℓ) | 25,290 | 2,784 | 0.00 | 4.4 | 1,783 | 1,767 | 49 |
Table 5.
ICP Analysis results of Pb-Cake(S-1)
| Elements | Zn | Pb | Cr | Fe | Cu | Cd | Sn |
| Amount(wt%) | 0.192 | 59.19 | 0..11 | 0.068 | 0.012 | 0.015 | 0.197 |
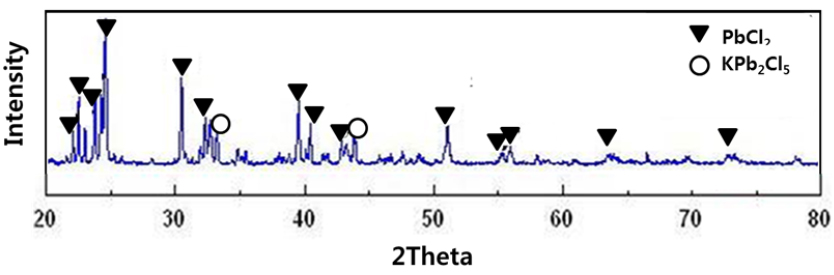
Table 4와 Table 5의 분석결과로부터 2차분진의 구성원소 중에서 수용액에 대한 용해도가 큰 염화물로 존재하는 Zn, Cu, Cd, Sn는 예상대로 주로 여과액에 존재하고, Pb성분도 소량이지만 여과액에 공존하고 있었다. 그리고 분리한 고형물(Pb-Cake)을 건조한 후에 XRD분석한 결과를 Fig. 5에 나타내었다. XRD분석결과로부터 고형물(Pb-Cake)은 대부분이 수용액에 대한 용해도가 작은 난용성의 PbCl2, KPb2Cl5로 이루어져 있으며, 용해도가 큰 KCl, K2ZnCl4, NaCl 등과 같은 염화물들은 대부분이 수용액에 용해되어 고형물과 분리할 수 있었다.
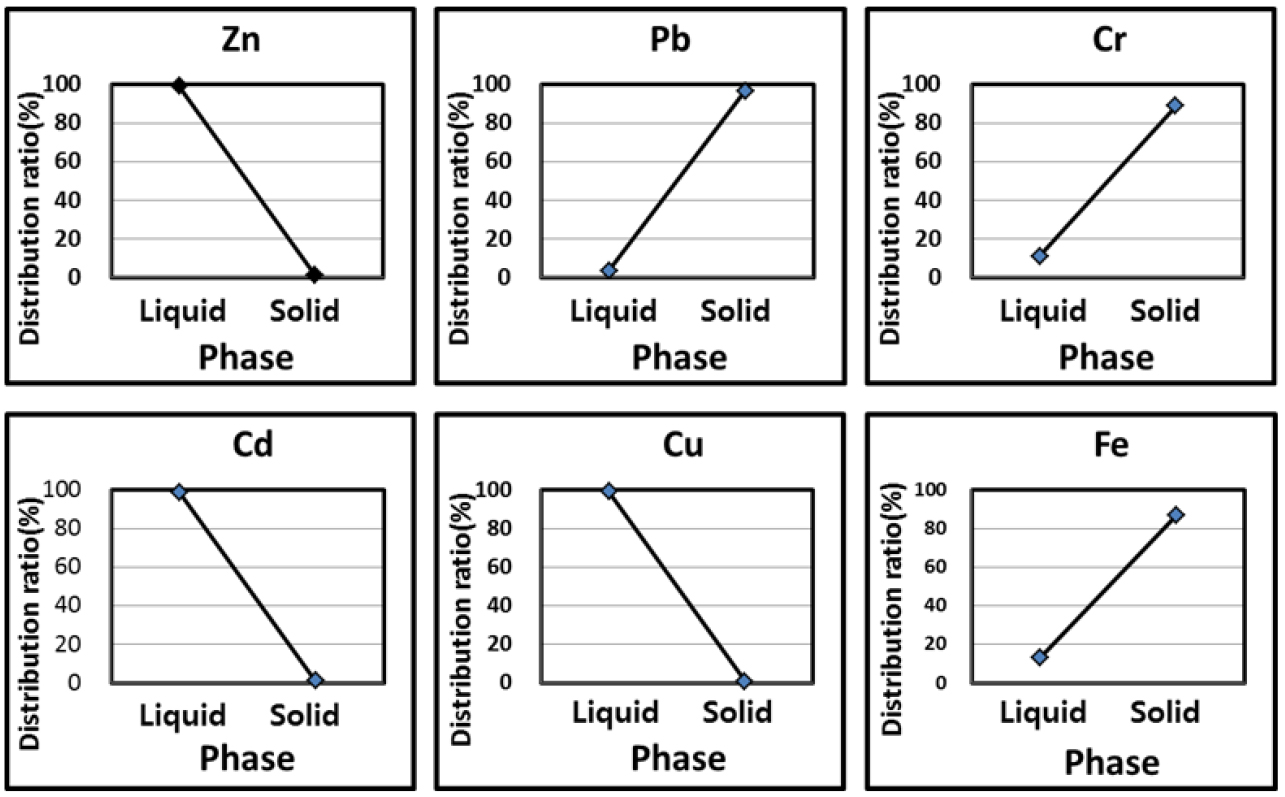
한편, 고액분리한 후의, 수용액상(Liquid Phase)과 고형물상(Solid Phase)으로의 성분원소들의 분배거동(Distribution Behavior)을 2차분진중의 성분원소들의 함량과 여과액 및 고형물상에서의 각각의 원소들의 함량을 ICP로 분석하여 구한 분배율을 Fig. 6에 도시하였다. Zn과 Cd, Cu는 각각 99%, 98%, 99% 수용액상에 Pb와 Cr, Fe는 각각 고체상에 96.6%, 88.9%, 86.8% 분배됨을 알 수 있었다.
침전물(Pb-Cake) 내에 잔존하는 소량의 Zn과 기타의 알칼리금속 화합물들은 이후의 공정(Pb-Metal 회수 등)에 크게 영향을 미치는 정도는 아니지만 반복적인 추가세척을 통하여 충분히 제거할 수 있었으며, 2차분진(2nd- Dust)내에 혼재하는 대표적인 Zn성분과 Pb성분을 수용액에 대한 용해도차와 슬러리화 조건 등의 조절을 조절함으로 더욱 효율적으로 분리할 수 있다는 가능성을 확인할 수 있었다.
3.2. Cementation에 의한 여과액의 정제 및 Zn-탄산염제조
3.2.1. Zn-Cementation에 의한 여과액의 정제
Metal-Cementation법은 수용액에 존재하는 금속들의 이온화 경향의 차이를 이용하여 외부로부터 별도의 전원공급이 없이 수용액중의 비한금속(less noble metal)을 수용액에 첨가하여 비한금속을 용해시키고 귀한금속(noble metal)을 석출시키는 공정으로, 소요되는 비용이 전체적으로 다른 공정에 비하여 저렴하기 때문에 공업적으로 널리 사용되고 있는 방법이다. 따라서 본 연구에서도 Table 4와 Table 5에 나타낸 것과 같이, 여과액(L-1) 중에는 Zn에 비하여 상대적으로 귀한 Pb, Cr, Cd, Cu, Fe 등과 같은 금속이온들이 다량으로 존재함으로, 이들 귀한 금속이온들을 비한 Zn금속분말(99.9% Zn)을 첨가하여 환원석출시킴으로서 Zn용액의 순도를 높이고자 하였다. 이러한 Cementation반응의 가능성을 이론적으로 검토하기 위하여 Table 6에 관련된 금속원소들에 대한 표준전극전위값을 나타내었으며, Table 7에는 25°C에서의 표준자유에너지변화(⊿G°)값을 나타내었다. 이상의 결과들로부터 관련한 금속원소들이 Zn에 비하여 귀(noble)하며, 환원석출반응시의 표준자유에너지변화(⊿G°)값이 음(-)의 값이므로 목적하는 Cementation반응이 일어날 것으로 사료된다.
Table 6.
Standard reduction potentials of various metals
Table 7.
Standard free energy values(⊿G°) at 25°C
그러나 Cr의 경우는 Zn과의 표준전극전위값이 다른 금속에 비해서 차이가 크지 않으며 표준자유에너지(⊿G°)값도 작은 음(-)의 값이므로 과량의 Zn분말이 소요될 것으로 예상된다. 그리고 Cu, Pb, Cd의 경우는 Zn과의 표준전극전위차값이 어느 정도 크고 표준자유에너지값도 어느 정도 큰 음(-)의 값을 나타내므로 용이하게 Cementation반응이 진행되리라고 사료된다. 한편, Fe족(Fe, Ni, Co) 금속원소인 Fe의 경우는 Fe이온이 수용액 중에서 Cementation반응(산화환원반응)에 의해 석출될 때에 수소이온과 수소가스발생에 기인하는 석출과전압현상 때문에 치환반응이 방해를 받을 가능성이 있다고 사료된다. 따라서 본 실험에서는 Cementation반응에 영향을 미치는 용액의 pH, 온도, 시간, 아연분말의 투입량 등과 같은 인자들의 영향을 조사하였다. 한편, Cementation반응 후 여과액의 하부에는 소량의 백색침전물이 빠르게 생성되는 것을 관찰할 수 있었는데, 이것은 분석결과 Cu+2와 Cr+3이온의 수화반응(Hydrate reaction)에 의해서 생성된 수화물임을 알 수 있었다.
Cementation처리를 위하여, 우선 여과액 50cc를 채취하고 500ml로 희석하여 농도를 조절한 후 석출시키고자 하는 금속량의 1.5배당량, 2.0배당량, 2.5배당량, 3.0배당량의 아연분말을 첨가하여 상온에서 10분간 Cementation반응을 실시하였다. Fig. 5에 대표적으로 나타낸 것과 같이, 3.0배당량의 Zn분말을 첨가한 경우 교반초기부터 치환반응이 빠르게 진행되면서(소량의 기체도 관찰됨) 흑색의 반응생성물이 표면에 부유하는 것을 관찰할 수 있었으며(Fig. 7(b)), 녹색의 여과액의 색갈이 백색으로 변화하였다(Fig. 7(c)).
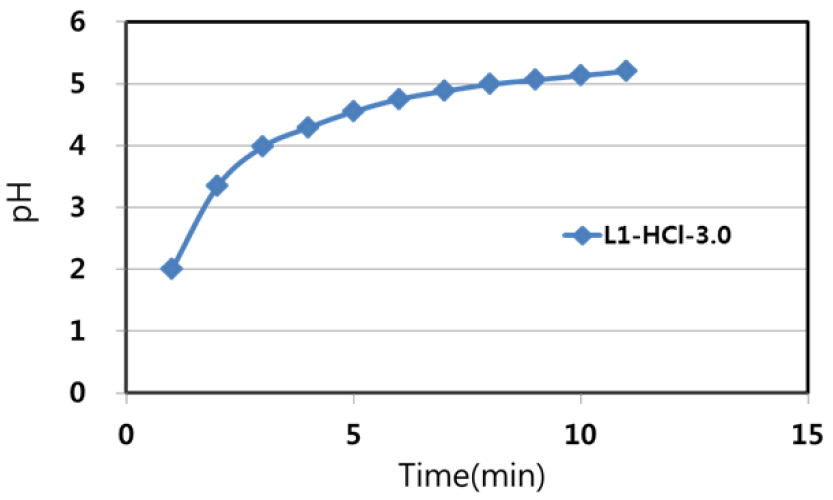
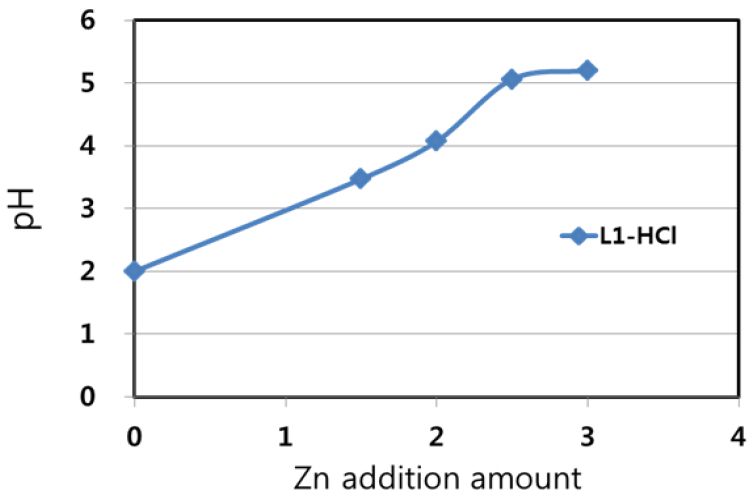
그리고 Cementation반응시간의 증가에 따라서 pH값도 2.0에서 서서히 증가하여 10분 후에는 pH=5.0까지 상승하였다(Fig. 8). 한편 Fig. 9에 나타낸 것과 같이 Zn분말을 1.5~2.0배당량 첨가할 때까지는 Zn첨가량에 비례하여 pH값이 2에서 4까지 증가하다가 첨가량 2.5당량에서는 급격히 pH=5까지로 증가하고 첨가량이 2.5배당량부터는 pH값이 다시 거의 일정한 값을 나타내었다. 또한 전반적으로 Zn첨가량의 증가에 따라 수화물로 판단되는 백색의 침전물의 생성량도 비례하여 증가하였다.
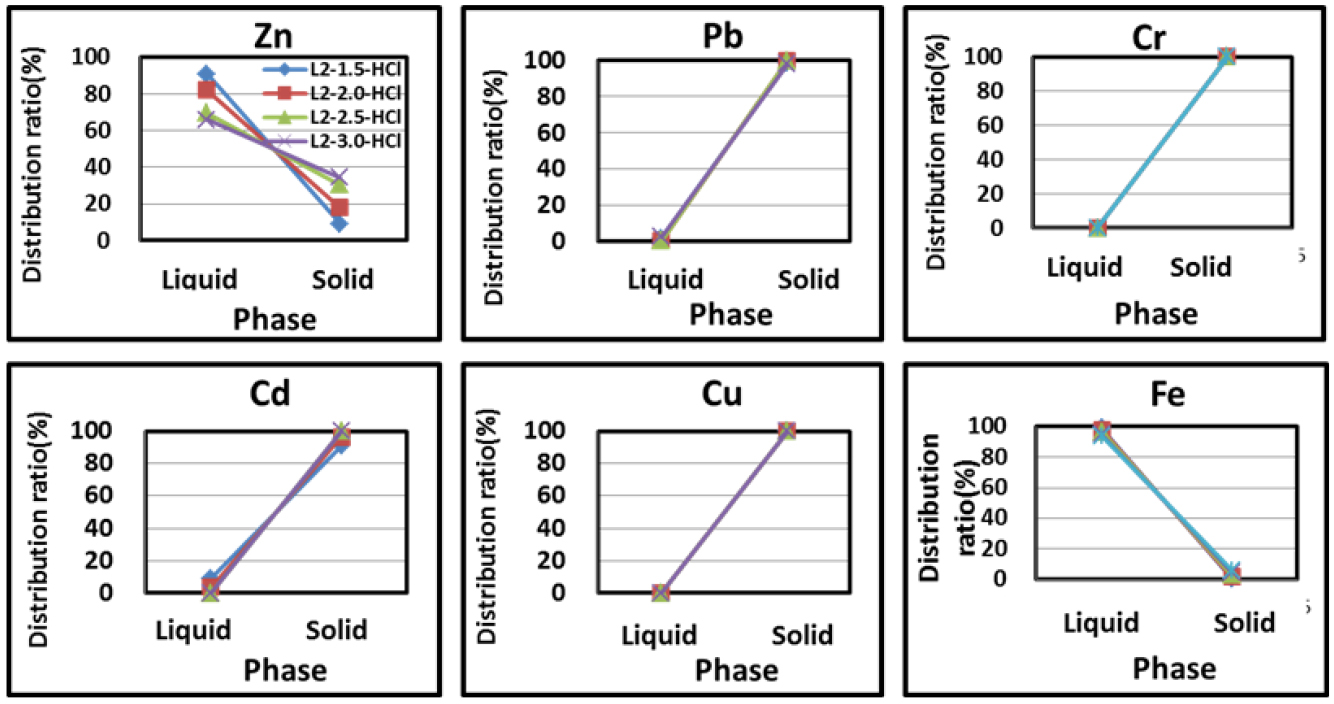
Fig. 10은 Zn-Cementation시의, Zn첨가량에 따라서 석출물상(고체상)과 수용액상의 Pb, Cr, Cd, Cu, Sn의 성분함량을 분석하여 각각의 원소이온들의 분배비율을 나타낸 것이다. 그림으로부터 Pb, Cr, Cd, Cu는, 1.5~3.0배당량의 Zn분말을 첨가하였을 때에 모든 Zn첨가량의 범위에서 고체상으로의 분배비율(%)이 Pb는 98~99%, Cr은 100%, Cd는 91~100%, Cu는 100% 고체상으로 분배되는 거동을 나타내었다. 이것은 앞서서 설명한 것과 같이, 표준전극전위차와 Zn-Cementation시의 표준자유에너지 값으로부터 예상한 것과 동일하게 Zn이 이들 원소들을 원활하게 환원하여 석출시켰기 때문이라고 사료된다. 그러나 Fe의 경우는, Zn첨가량이 증가하여도 고체상으로의 분배율이 1~6%에 지나지 않고 대부분이 액체상에 존재(93~99%)하였는데 Zn첨가 시에 많은 기체가 발생하는 것으로 보아서, 앞서서 설명하였듯이 수소이온과 수소가스발생에 기인하는 Fe족 금속(Fe,Ni,Co)의 석출과전압현상 때문이라고 사료된다. 그리고 Cementation에 의한 여과액(L-1)의 정제를 위해서는 Zn의 Zn수화물로의 환원능력의 손실과 경제성 등을 고려하여 과량인 2.0배당량의 Zn분말을 첨가하는 것이 적절하다고 판단된다. 그리고 본 공정을 실제로 생산에 적용하기 위해서는 석출물에 대한 재활용에 대해서도 향후에 추가적인 연구가 필요하다고 사료된다.
3.2.2. 정제한 여과액으로부터 Zn-탄산염의 제조
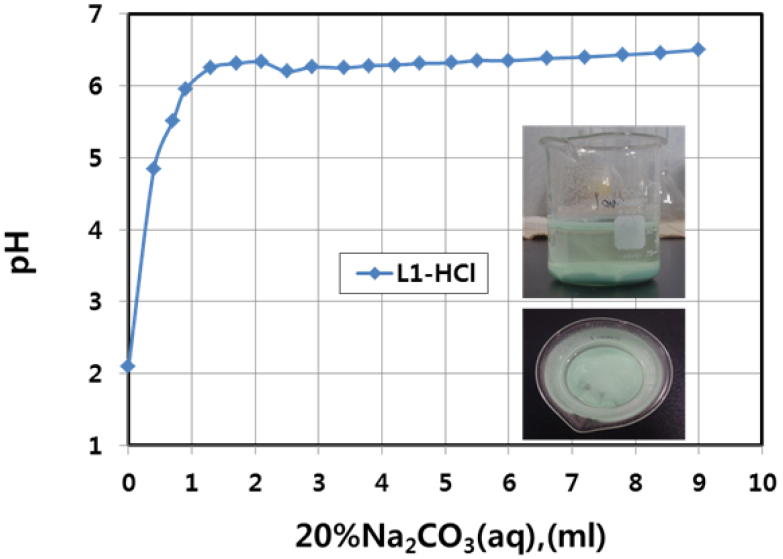
Fig. 11은 Cementation처리하지 않은 여과액(L-2)에 100ml의 순수(Pure Water)를 첨가한 용액으로부터 50ml을 나누어, 이 수용액에 뷰렛을 사용하여 상온에서 1시간동안 20% Na2CO3(aq)을 소량씩 첨가하면서 pH변화를 관찰한 적정곡선으로, 2ml의 20% Na2CO3(aq)을 첨가하여도 빠르게 반응이 진행하여, 백색의 반응생성물이 생성되면서 pH는 2에서 6.4까지 급증하였다. 그러나 2.5~9.0ml의 20% Na2CO3(aq)을 첨가하였을 때는 pH=6.2에서 서서히 증가하여 pH=6.5을 나타내었다.
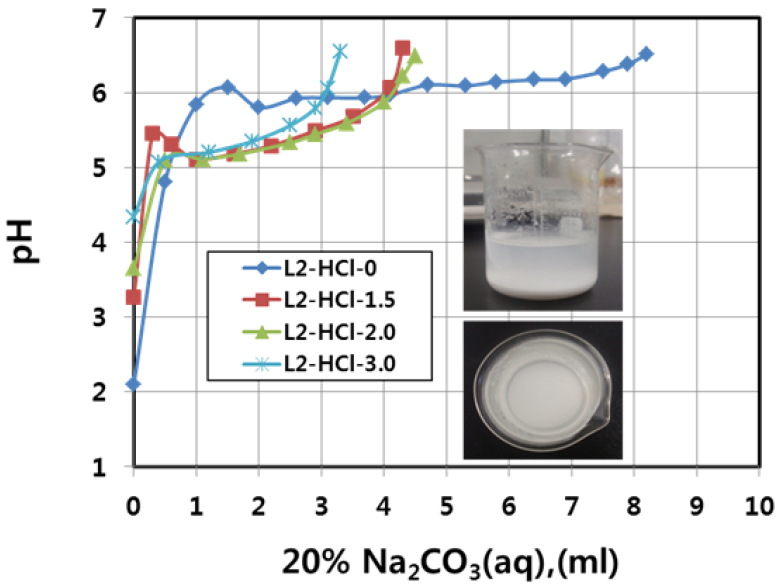
Fig. 12는 Zn-Cementation처리하지 않은 여과액(L-1)과 Zn-Cementation(1.5~3.0배당량 Zn분말첨가)처리한 여과액들(L-2)에 대하여, Fig. 9와 동일하게 100ml의 순수(Pure Water)를 첨가한 수용액으로부터 50ml을 채취하여, 이 수용액을 70°C로 가열하면서 1시간동안 20% Na2CO3(aq)을 첨가하였을 때의 탄산염 생성거동과 pH변화를 조사한 적정곡선이다. 70°C에서 Zn-Cementation처리하지 않은 여과액(L-1)에 대한 20% Na2CO3(aq)의 첨가량에 따른 pH변화는 상온에서의 결과와 매우 유사한 거동을 나타내었다. 한편 Zn-Cementation처리한 용액들의 경우는, 20% Na2CO3수용액을 첨가하면 초기에는 pH가 급격히 pH=5.0~5.5까지 급증하였다가 pH값이 일정한 정체구역이 존재하였으며, 다시 서서히 pH가 증가하는 경향을 나타내었다. 그리고 과량의 Zn첨가량으로 Cementation처리한 경우는 이러한 pH값이 일정한 정체구간이 점점 짧아지는 것을 볼 수 있다. 이것은 과량의 Zn을 첨가한 Cementation의 경우일수록 Zn을 제외한 기타의 원소들의 함량이 대단히 소량이며 또한 용액중의 Zn과의 탄산화반응이 비교적 빠르게 진행되었기 때문이라고 사료된다.
반응종료 후에 백색의 침전물과 여과액을 분리하고 백색침전물은 조성성분분석 XRD에 의한 석출물질의 종류 SEM에 의한 석출물질의 형상을 조사하였다. Table 8에 나타낸 것과 같이 Zn-cementation처리하지 않고 20% Na2CO3(aq)첨가하여 얻어진 탄산염고형물(S3-0)의 경우는 상온과 70℃로 가열한 상태에서, 모두 여과액(L-1)중에 기타의 원소들이 Zn과 공존하므로, Zn-cementation처리하여 얻어진 백색의 고형물(S3-1.5~3.0)에 비하여 Zn함량이 낮으며 Pb, Fe, Cu, Cd, Sn 등도 어느 정도 함유되어 있다. 그러나 Zn-cementation처리 후에 Na2CO3(aq)첨가하여 얻어진 모든 백색고형물(S3-1.5~3.0)의 경우는 Zn함량이 58~59%로 높고, 미소량의 Pb, Fe, Cu, Cd, Sn이 존재하였으며 XRD회절분석결과를 Fig. 13에 나타내었다.
Table 8.
Chemical composition of solids obtained by filtration after adding 20%Na2CO3(aq) at room temperature and 70°C
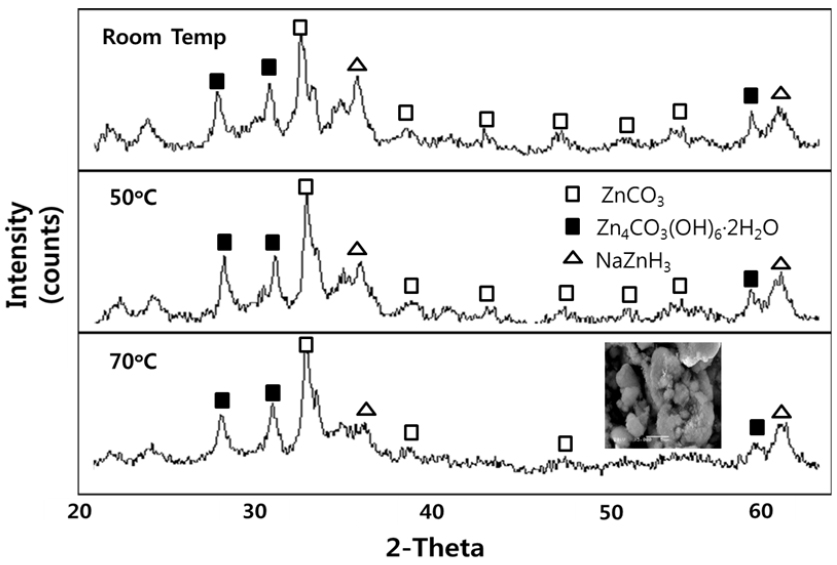
Fig. 13은 대표적으로 2.5배당량의 Zn-cementation후에 상온 50°C, 70°C에서 각각 20% Na2CO3(aq)첨가하여 석출시킨 침전물을 건조하여 XRD분석한 결과로 ZnCO3(s), Zn5(OH)8Cl·2H2O(s), NaZnH3(s)가 석출됨을 확인할 수 있었다. 이상과 같은 XRD결과로부터 다음과 같은 반응식 (2), (3), (4)에 의해서 화합물의 석출반응이 일어났을 것으로 사료된다. 그리고 생성물들에 대해서 SEM관찰결과 미세한 입자상의 석출물들이 응집된 형상을 나타내고 있었다.
3.3. 고/액 분리한 고형물(Pb-Cake)의 수용액 정제와 Pb-탄산염제조
조산화아연의 건식정제과정에서 포집된 2차분진(2nd Dust)을 재용해한 후, Suction Filtering으로 분리한 여과액(L-1)은 Zn-Cementation에 의해 정제하여 탄산아연염 제조실험에 사용하였고 남은 고형물(Pb-Cake)은 100ml의 순수(Pure water)로 3회 세척한 후 건조하여 분석한 결과 Table 9에 나타낸 것과 같이 Zn, Sn, Ni, Cr 등의 함유량은 매우 낮고 Pb염화물의 순도는 매우 높은 고형물(Pb-Cake)을 얻을 수 있었다. 다음은 세척에 의해 정제된 일정량(43.23g)의 고형물(Pb-Cake)에 75ml의 20% Na2CO3(aq), 40ml의 온수(Hot water)를 첨가하여 얻은 pH=9.74의 수용액에, 20%HCl을 첨가하여 pH=9.0로 유지하며 70°C에서 1.2시간 교반하면서 식 (5)과 같은 탄산화반응을 진행하였다.
Table 9.
Analysis result of solid and liquid after carbonation reaction of Pb-Cake at 70°C
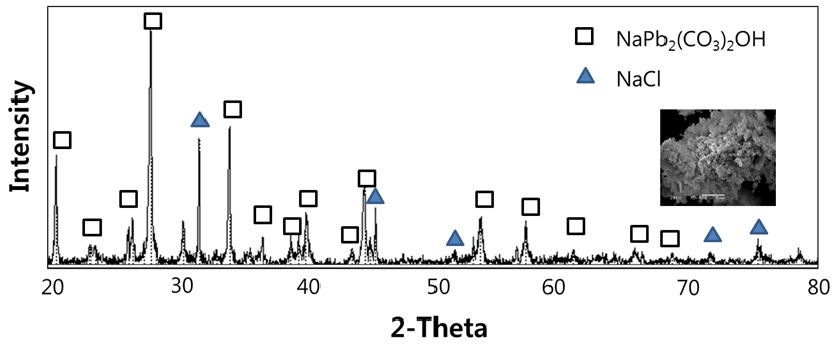
그 결과 탄산화반응은 매우 빠르게 진행되었으며 일정시간 정치시킨 후에 Suction filtering하여 고액/분리하여 어두운 갈색(Dark brown)의 여과액과 회색(Gray)의 고체침전물을 얻었으며, 그 분석결과를 Table 9에 함께 나타내었다. 그리고 Fig. 14에 나타낸 건조한 고형물에 대한 XRD분석결과로부터 반응생성물은 NaPb2(CO3)2OH이 대부분이며 생성된 NaCl중에서 수용액에 용해되고 남은 NaCl은 NaCl(s)로 석출되어 NaPb2(CO3)2OH과 혼재한다고 사료된다. 그리고 SEM에 의해 건조한 고형물의 형상을 관찰한 결과, 앞서의 Zn-탄산염의 경우와 유사하게 미세한 입자상의 반응생성물들이 응집된 형상을 하고 있었다.
4. 결 론
조산화아연의 정제과정에서 발생된 2차분진(2nd Dust)으로부터 Zn, Pb를 최종적으로는 Zn계 탄산염과 Pb계 탄산염으로 분리회수하기 위한 기초연구를 수행하여 다음과 같은 연구결과를 얻었다.
1. 조산화아연의 정제과정에서 발생한 2차분진을 60℃의 염산수용액에서 용해한 후에, Suction Filtering으로 고상과 액상을 분리하여 PbCl2, KPb2Cl6 등으로 이루어진 고형침전물(갈색)과 ZnCl2 NaCl, KCl 등으로 이루어진 여과액(녹색)을 얻었다.
2. 여과액 중의 Cr, Cd, Cu, Fe, Sn 등과 같은 불순원소들을 Zn-Cementation법으로 제거하기 위하여 1.0~3.0몰의 Zn(99%분말)분말을 첨가한 결과, 흑색의 반응생성물이 생성되며 환원석출반응이 빠르게 진행함과 동시에 pH가 2.0에서 5.0까지 상승하였다. 이때에 Zn분말의 첨가량에 비례하여 pH와 불순원소들로 구성된 고형침전물량이 증가하였으며 녹색의 여과액이 백색으로 변화하였다.
3. Zn-Cementation처리한 후의 여과액에 20% Na2CO3(aq)첨가하여 70℃에서 1시간 동안 반응시킨 결과 ZnCO3(s), Zn5(OH)8Cl·2H2O(s), NaZnH3(s)와 같은 반응석출물이 생성되었다.
4. 조산화아연의 정제과정에서 얻어진 2차분진을 60℃의 염산수용액에서 반응시킨 후 Suction Filtering하여 얻은 침전물을 건조한 고형물(Pb-Cake)에 20% Na2CO3(aq)을 첨가하고 20% HCl용액으로 pH를 9.0으로 유지하면서 70°C에서 1.2시간 반응시켰을 때, 어두운 갈색(Dark brown)의 여과액과 회색의 고체침전물을 얻었다. 여과액은 주로 NaCl, KCl로 이루어져 있었으며 고형물을 건조하여 XRD로 분석한 결과 미세한 침상의 NaPb2(CO3)2OH(s), NaCl(s) 입자들이 응집된 형상을 하고 있었다.
5. 이상의 결과로부터 조산화아연(Crude Zinc Oxide)의 건식정제과정에서 포집된 2차분진(2nd Dust)에서, Zn과 Pb를 Zn계-탄산염과 Pb계-탄산염으로 분리하여 자원화 할 수 있다는 가능성을 확인할 수 있었다.