1. 서 론
2. 실험 재료 및 방법
2.1. 실험재료
2.2. 실험방법
3. 결과 및 고찰
3.1 황산침출액에서 구리(II)의 분리
3.2. 황산침출액에서 코발트(II)의 분리
4. 결 론
1. 서 론
최근 전기자동차 시장의 급격한 성장과 함께 2025년까지 리튬이온배터리의 수요는 10배 이상 증가할 것으로 예상되며, 폐리튬이온배터리의 발생량 역시 2030년 1,100만톤을 넘어설 것으로 전망되고 있다1,2). 수명이 다한 폐리튬이온배터리에는 5~20% 코발트, 5~10% 니켈, 5~7% 리튬 및 미량의 구리, 알루미늄, 철 등이 함유되어 있다3). 폐리튬이온배터리와 같은 2차자원에는 천연광석보다 높은 농도의 유가금속들이 함유되어 있으며, 천연자원과 비교해 간단한 공정 및 적은 에너지를 사용해 회수가 가능하다4). 따라서 초합금(super alloy), 촉매, 배터리 등 다양한 분야에서 수요가 증가함에 따라 가격이 상승중인 리튬, 코발트 및 니켈 등의 안정한 공급을 위해 폐리튬이온배터리에서 유가금속을 회수하는 것은 매우 중요하다5). 폐리튬이온배터리의 재활용시 리튬의 경우 건식공정에서 알루미늄과 함께 슬래그를 형성시켜 분리할 수 있으며, 코발트, 니켈 및 구리는 금속합금의 형태로 회수된다6,7). 이러한 금속합금은 건식 또는 습식제련법을 통해 분리할 수 있는데, 건식법의 경우 높은 에너지 소비 및 초기 설비 투자비용에 대한 부담이 있는 반면, 습식법의 경우 높은 추출 효율, 낮은 에너지 소비, 적은 유해 가스 배출 및 비교적 적은 시설 비용으로 운영이 가능하다는 장점이 있다8). 또한 폐리튬이온배터리에는 6종 이상의 금속이 함유되어 있으므로 각 금속을 효과적으로 분리해 고순도의 금속 및 금속화합물로 회수하기 위해서는 습식공정이 보다 유리하다9,10,11,12).
이전의 연구에서 코발트, 니켈, 및 구리의 금속혼합물을 2 M 황산용액에 침출시키면 코발트와 니켈이 각각 99.9%와 47.9% 침출되었으며, 이 때 구리는 전혀 침출되지 않았다13). 문헌에 따르면, 황산용액에 산화제로 과산화수소를 첨가하면, 코발트와 니켈의 침출률을 향상시킬 수 있다고 보고되었다14). 따라서 3%의 과산화수소를 첨가해 황산용액에서 코발트와 니켈을 완전히 침출시켰으며, 이 때 9.6%의 구리가 함께 침출되었다. 본 연구에서는 금속혼합물의 황산침출액 조성을 모사한 합성용액을 제조해 용매추출로 코발트(II), 니켈(II) 및 구리(II)의 분리를 위한 최적의 추출조건과 탈거조건을 조사했다.
2. 실험 재료 및 방법
2.1. 실험재료
금속혼합물은 코발트(Co, size < 44 μm, Alfa Aesar, 99.5%), 니켈(Ni, size: 3-7μm, Alfa Aesar, 99.9%) 및 구리(Cu, granular, Junsei Chemical Co., 99.5%) 금속분말을 동일한 질량 비율로 혼합해 준비했다. 침출용액은 60°C에서 2 M 황산(H2SO4, Daejung Co., >95%, Korea)용액에 50 g/L의 금속혼합물과 3%의 과산화수소(H2O2, Daejung Chemical. Co., Korea., 30%)를 첨가해 1시간동안 침출해 준비했다. 침출 후 용액과 잔사를 여과지를 사용해 분리했으며, 이 때 침출용액에서 각 금속의 침출률과 농도를 Table 1에 나타냈다.
Table 1.
The composition of the sulfuric acid leaching solution of the metallic mixture of Cu, Co and Ni in presence of H2O2 (Leaching Conditions ; 2 M H2SO4, 60°C, 300 rpm, 60 min, pulp density : 50 g/L, H2O2 : 3%)
| Metal ions | Co(II) | Ni(II) | Cu(II) |
| Concentration, mg/L | 16667 | 16667 | 1618 |
| Leaching percentage, % | 99.9 | 99.9 | 9.6 |
용매추출 실험은 침출용액의 조성을 모사한 합성용액으로 수행했으며, 합성용액은 황산코발트수화물(CoSO4·7H2O, Daejung Co., >98%, Korea), 황산니켈수화물(NiSO4·6H2O, Daejung Co., >98.5%, Korea), 황산구리수화물(CuSO4·5H2O, Duksan chemical Co., >99%, Korea)을 2 M 황산용액에 용해시켜 제조했다. 추출제로는 Cyanex 301(Cytec Inc., Canada., 70%)과 ALi-SCN을 사용했고, ALi-SCN은 Aliquat 336(BASF Co. Ltd., 93%)을 기반으로 NH4SCN(Daejung chemicals & metals Co. Ltd., Korea., 99%)과 반응시켜 Aliquat 336의 음이온인 Cl-를 SCN-으로 치환하여 합성했다15). 또한 Aliquat 336으로 추출시 제 3상이 형성되는 것을 방지하기 위해 개질제로 15%의 1-decanol(Daejung Chemical & Metals Co., Ltd., 98%)을 첨가했고, 희석제로는 등유(Daejung chemicals & metals Co. Ltd., Korea., 100%)를 사용했다. 탈거제는 염산(Daejung chemicals & metals Co. Ltd., Korea., 35%)과 질산(HNO3, Daejung Co., Korea, 60%)으로 제조한 왕수 및 암모니아수(NH4OH, Junsei Chemical Co. Ltd, Japen, 28%)를 사용했으며, 본 연구에 사용된 모든 시약은 분석등급으로 별도의 정제과정없이 사용했다.
2.2. 실험방법
용매추출실험을 위해 금속혼합물의 황산침출액을 모사한 합성용액을 제조했으며, 합성용액에서 코발트(II), 니켈(II) 및 구리(II)의 농도는 각각 16667, 16667 및 1618 mg/L로 고정했다. 용매추출 실험을 위해 50 mL 광구병에 수상과 유기상을 일정 부피비로 넣고, Burrell wrist action shaker(model 75, USA)를 사용해 30분간 교반후 분액여두에서 수상과 유기상으로 분리했다. 이때 분리한 유기상은 탈거실험에 사용했다. 용매추출 후 수상의 금속농도는 ICP-OES(Arcos, Spectro, Germany)로 측정했고, 금속의 추출률 및 탈거율은 다음 식으로 구했다.
여기서 mini과 me는 각각 추출 전후 수상에서 금속의 질량을 의미하고, m*ini과 m*e는 탈거 전후 유기상에서 금속의 질량을 나타낸다.
3. 결과 및 고찰
3.1 황산침출액에서 구리(II)의 분리
3.1.1. Cyanex 301에 의한 구리(II)의 선택적 추출
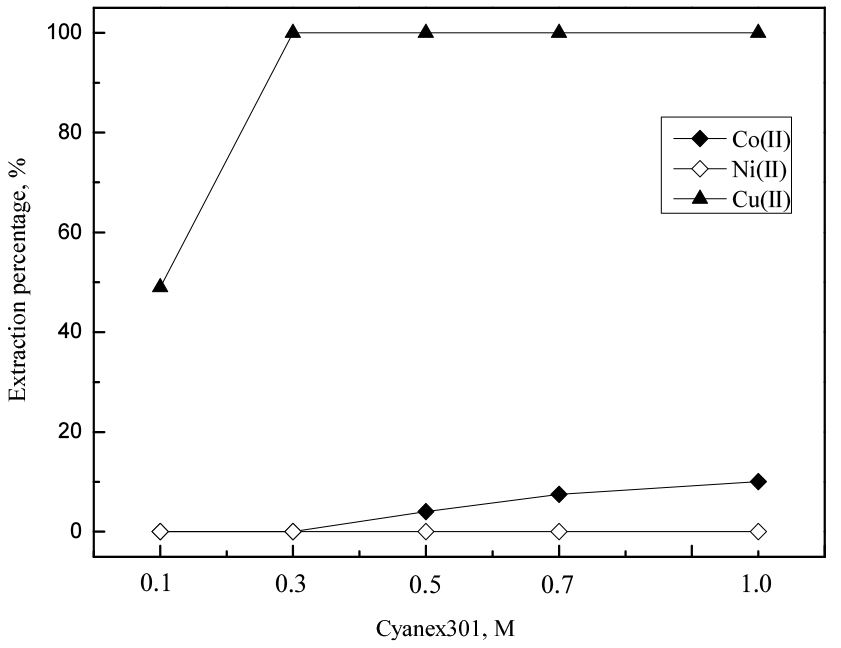
Cyanex301은 구리(II)를 선택적으로 추출하는 것으로 알려져 있다16). 따라서 코발트(II), 니켈(II) 및 구리(II)가 혼합된 합성용액에서 구리(II)를 분리하기 위한 추출제로 Cyanex 301을 사용했다. 추출제 농도에 따른 금속의 분리거동을 조사하기 위해 Cyanex 301의 농도를 0.1에서 1 M까지 변화시켰으며 실험결과를 Fig. 1에 나타냈다. 실험결과 추출제 농도가 0.3 M 이하일 때 코발트(II)는 전혀 추출되지 않다가 0.5 M에서 1 M로 추출제 농도가 증가함에 따라 추출률이 4.0%에서 10.1%로 증가했다. 본 실험조건에서 니켈(II)은 전혀 추출되지 않았으며, 구리(II)는 추출제 농도가 0.1 M에서 0.3 M로 증가함에 따라 48.9%에서 99.9%가 추출되었다. 코발트(II), 니켈(II) 및 구리(II)가 함유된 2 M 황산용액에서 구리(II)는 Cyanex 301에 선택적으로 추출되었으며, Cyanex 301에 의한 구리(II)의 추출반응을 아래 식에 나타냈다17).
Cyanex 301의 작용기에 존재하는 황원자와 구리(II) 사이에서는 산화환원 반응이 일어나 구리(II)는 구리(I)로 환원되고, Cyanex 301의 산화된 R2PS2- 리간드와 서로 [R2P(S)SCu]n 형태의 올리고머 복합체를 형성한다18). 구리(I)와 구리(II)의 전자배치는 각각 [Ar] 3d10 4s1과 [Ar] 3d9 4s2로 4s보다 에너지준위가 낮은 3d 오비탈에 전자가 채워진 구리(I)는 구리(II)보다 에너지적으로 안정하다. 따라서 Cyanex 301에 의해 환원된 구리(I)의 탈거는 어려울 것으로 생각된다.
3.1.2. 왕수에 의한 구리(II)의 탈거
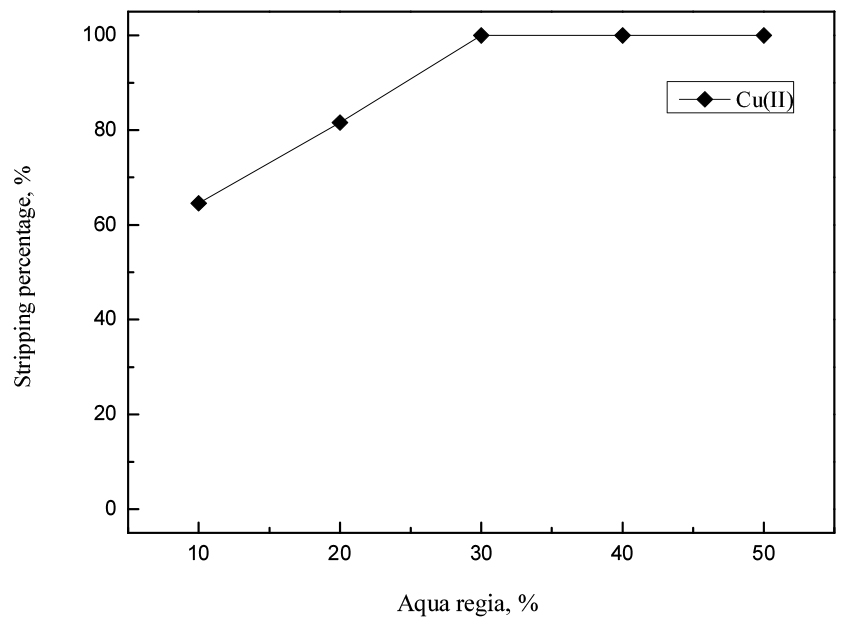
코발트(II), 니켈(II) 및 구리(II)가 함유된 황산용액에서 0.3 M Cyanex 301에 의해 1618 mg/L의 구리(I)가 선택적으로 추출되었다. Cyanex 301에서 구리(I)는 산화환원반응을 통해 강력한 착물을 형성하면서 추출되므로 황산 및 염산과 같은 진한 무기산으로는 탈거가 어려운 반면, 상온에서 산화력이 있는 질산으로는 탈거가 가능하다고 알려져 있다16). 따라서 보다 산화력이 강한 왕수를 사용해 구리이온이 추출된 Cyanex 301로부터 탈거를 시도했다. 이때 왕수의 농도는 10에서 50%까지 변화시켰으며, 실험결과를 Fig. 2에 나타냈다. 왕수의 농도가 10에서 30%로 증가함에 따라 구리(I)의 탈거율은 64.6%에서 99.9%로 증가했으며, 왕수의 의한 구리이온의 탈거반응을 아래와 같이 나타냈다.
왕수는 강력한 산화제인 염화니트로실(NOCl)을 형성하며 위 식과 같이 산화제가 Cyanex 301에 추출된 구리(I)를 구리(II)로 재산화시킴으로써 탈거가 가능한 것으로 생각된다.
3.2. 황산침출액에서 코발트(II)의 분리
3.2.1. ALi-SCN에 의한 코발트(II)의 선택적 추출
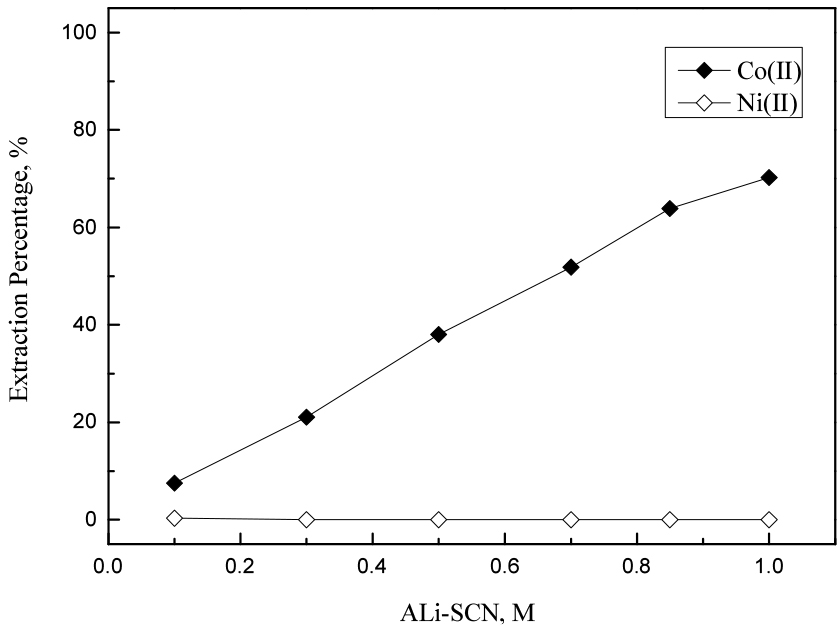
황산용액에서 Cyanex 301로 구리(II)를 선택적으로 추출해 분리하면 여액에는 코발트(II)와 니켈(II)만 남는다. 일반적으로 코발트(II)와 니켈(II)은 비슷한 물리화학적 성질로 인해 분리가 어렵다. 그러나 코발트(II)는 니켈(II)보다 Cl-이나 SCN-과 같은 음이온과 착물을 형성하려는 경향이 강하다. 또한 이러한 코발트(II) 착물은 아민계 추출제에 의해 추출될 수 있으며, 이전 연구를 통해 ALi-SCN과 같은 이온성액체에도 선택적으로 추출될 수 있다고 밝혀졌다19). 따라서 코발트(II)와 니켈(II)의 분리를 위해 ALi-SCN을 추출제로 사용했고, 추출제 농도를 0.1에서 1 M까지 변화시켜 추출 및 분리에 미치는 영향을 조사했다. 실험결과를 Fig. 3에 나타냈으며, ALi-SCN에 의한 코발트(II)의 추출 반응을 다음 식에 나타냈다.
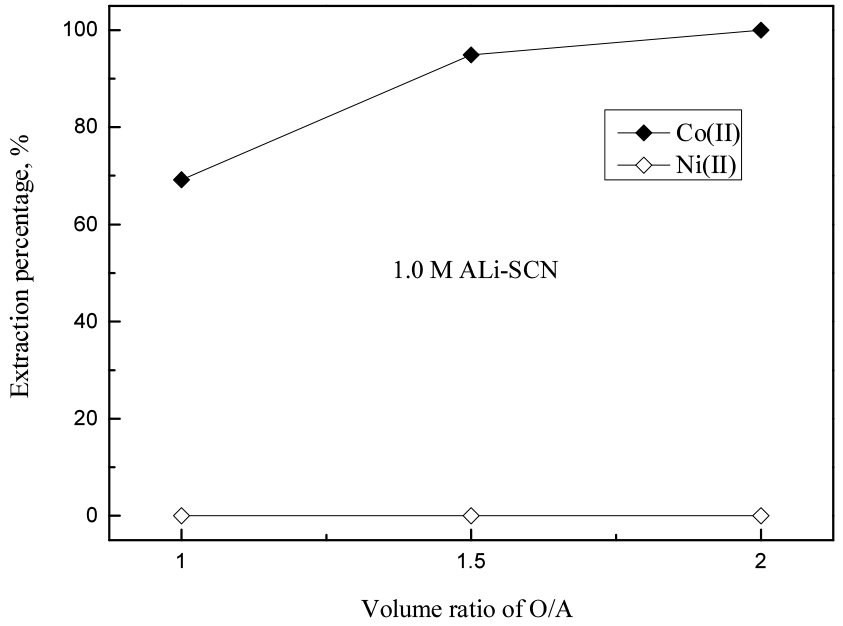
ALi-SCN의 농도가 0.1 M에서 1 M로 증가함에 따라 코발트(II)의 추출률은 7.5에서 70.2%로 증가했고, 이때 니켈(II)은 전혀 추출되지 않았다. ALi-SCN에 의해 황산용액에서 코발트(II)가 선택적으로 추출되었으나 1 M의 높은 추출제 농도에서도 코발트(II)가 완전히 추출되지 않았다. 따라서 코발트(II)를 완전히 추출해 두 금속을 분리할 목적으로 1 M 농도의 ALi-SCN에 대해 유기상과 수상의 부피비를 1에서 2까지 변화시켜 추출실험을 수행했고, 결과를 Fig. 4에 나타냈다. 실험결과 유기상 대 수상의 비가 2일 때 1 M ALi-SCN에 코발트(II)가 99.9% 이상 추출되었고, 여액에는 니켈(II)만 남아 두 금속을 완전히 분리할 수 있었다.
3.2.2. 암모니아 용액에 의한 코발트(II)의 탈거
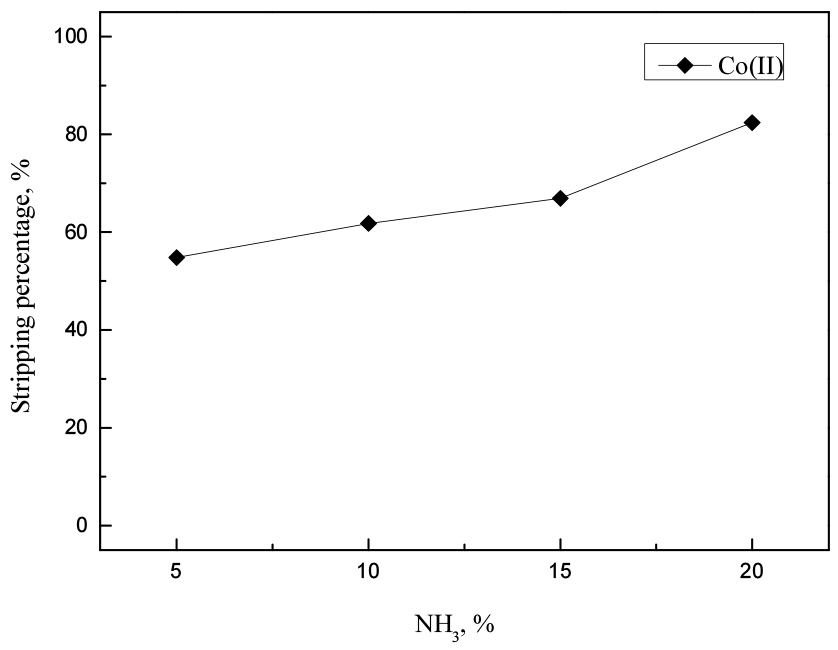
유기상 대 수상의 비가 2일 때 8333 mg/L의 코발트(II)가 선택적으로 추출된 1 M ALi-SCN에서 암모니아 용액을 사용해 탈거실험을 수행했다. 암모니아용액의 농도는 5~20%까지 변화시켰고, 실험결과를 Fig. 5에 나타냈다. 실험결과 암모니아 농도가 5에서 20%까지 증가함에 따라 코발트(II)의 탈거율은 54.8에서 82.4%까지 증가했으며, 암모니아에 의한 코발트(II)의 탈거반응을 아래 식에 나타냈다.
위 식은 암모니아 농도가 증가함에 따라 탈거율이 증가하는 실험결과와 잘 일치한다. 그러나 암모니아 용액의 농도가 15%를 초과하면 암모니아 농도를 증가시키는 것은 탈거에 효과적이지 않았으며, 20% 농도에서도 코발트(II)는 완전히 탈거되지 않았다. 따라서 코발트(II)를 완전히 탈거하기 위한 추가 실험을 수행했다.
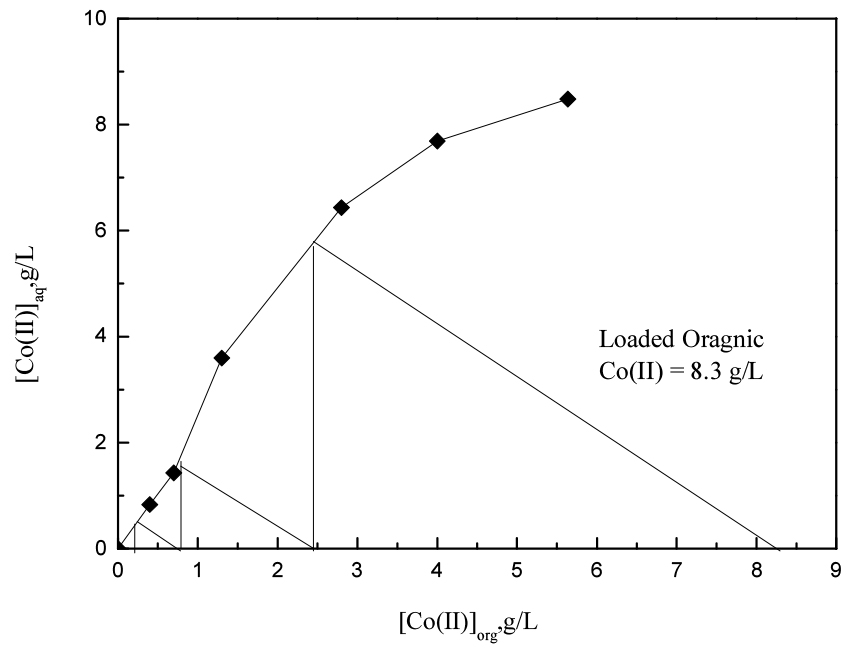
3.2.3. 코발트(II) 탈거에 대한 McCabe-Thiele도 및 3단 교차식 다단탈거
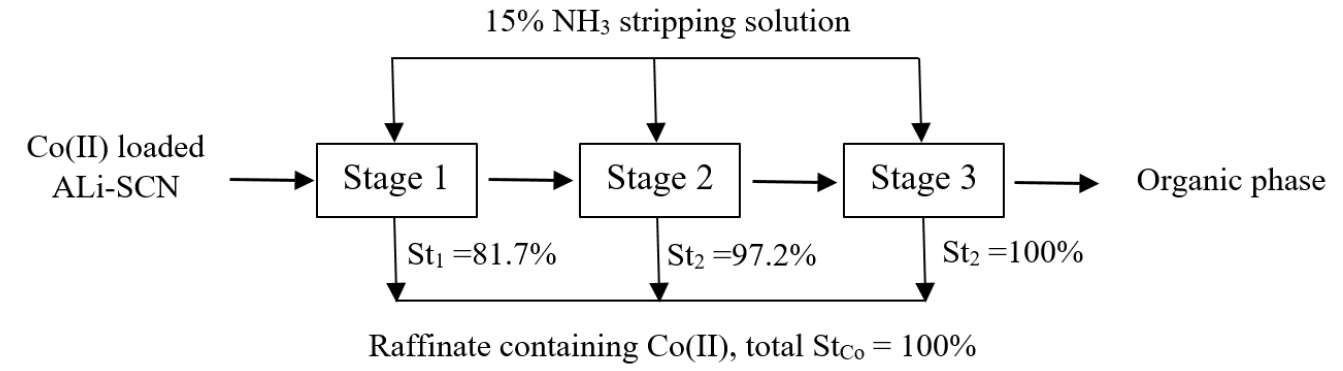
15% 암모니아용액을 사용해 유기상 대 수상의 비를 5에서 0.2까지 변화시켜 탈거실험을 수행했고, 코발트(II)를 모두 탈거할 수 있는 단수를 구하기 위해 McCabe-Thiele도를 구해 Fig. 6에 나타냈다. 실험결과 McCabe-Thiele도를 통해 3단의 교차식 다단탈거로 1 M ALi-SCN으로부터 코발트(II)를 완전히 탈거할 수 있을 것으로 예측된다. 따라서 15% 암모니아용액을 사용해 3단의 교차식 다단탈거 실험을 수행했으며, 실험결과를 Fig. 7에 나타냈다. 실험결과, 15% 암모니아 용액을 사용해 3단으로 코발트(II)를 완전히 탈거할 수 있었다. 황산용액에서 용매추출로 구리(II)와 코발트(II)를 분리한 여액에는 니켈(II)만 남았다.
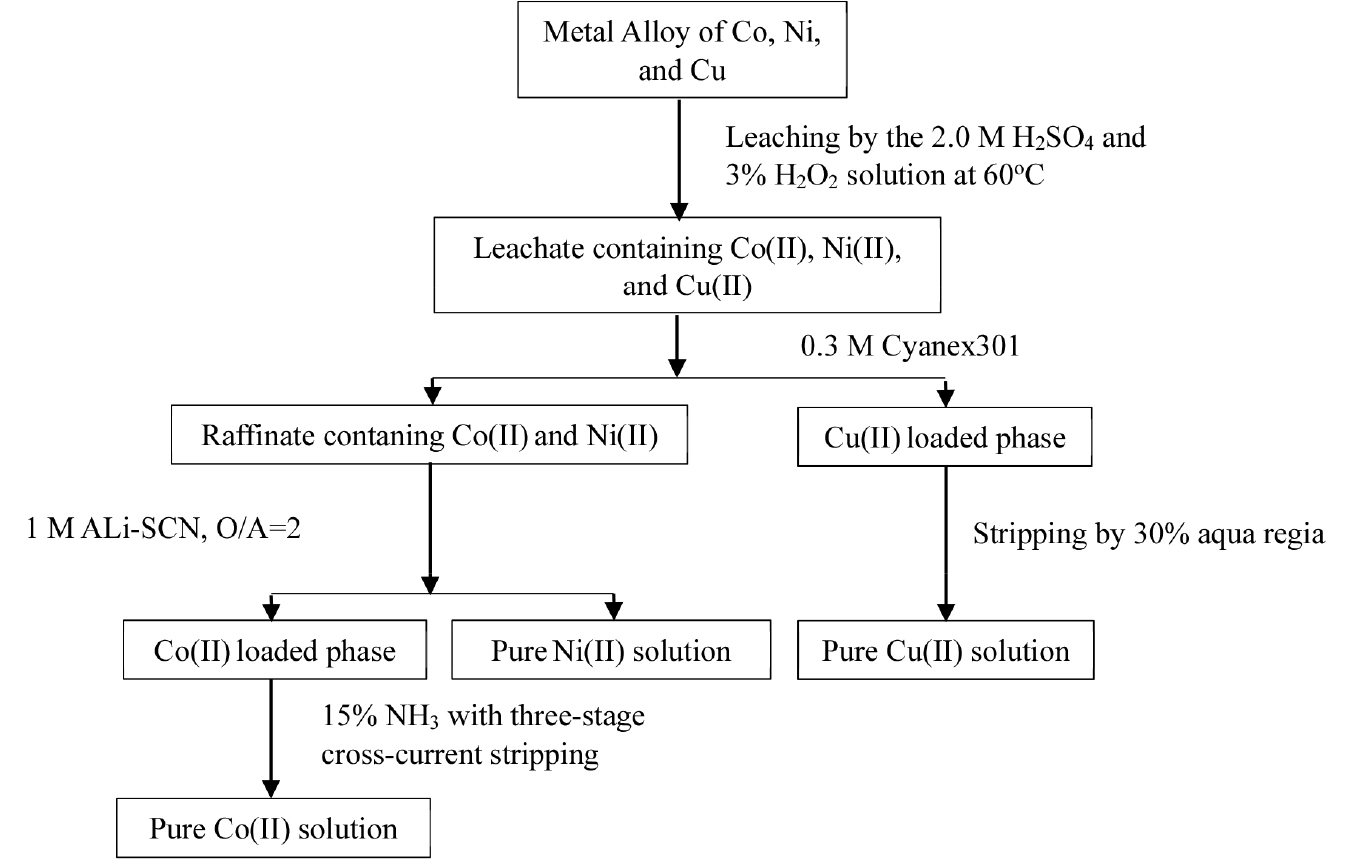
본 연구를 통해 폐리튬이온배터리에서 용융환원된 금속합금상의 황산 침출액에서 각 금속을 분리하기 위한 습식공정도를 Fig. 8에 나타냈다. 동일중량비로 혼합한 코발트, 니켈 및 구리의 금속혼합물을 2 M 황산용액과 3% H2O2로 침출하면, 9.6% 구리가 침출되고 코발트와 니켈은 완전히 침출된다. 침출액에서 0.3M Cyanex 301로 구리(II)를 선택적으로 추출한 다음 유기상에서 30% 왕수를 사용해 탈거하면 순수한 구리(II) 용액을 회수할 수 있다. 그리고 코발트(II)와 니켈(II)만 남은 여액에서 O/A 비를 2로 조절해 1 M ALi-SCN으로 코발트(II)를 선택적으로 추출하면, 여액에는 순수한 니켈(II)만 남는다. 유기상으로 추출된 코발트(II)는 탈거액으로 15% 암모니아용액을 사용하여 3단 교차식 다단탈거를 수행하면 순수한 코발트(II)용액을 회수할 수 있다. 각 단계에서 얻어진 금속용액의 순도는 99.9%이며, 본 연구에서 제안된 습식공정을 통해 폐리튬이온배터리에서 회수된 금속합금상으로부터 고순도 금속용액의 회수가 가능할 것으로 기대된다.
4. 결 론
폐리튬이온배터리를 고온에서 용융환원처리하면 금속합금상을 회수할 수 있다. 본 연구에서는 코발트, 니켈 및 구리가 동일한 중량비로 존재하는 금속혼합물에 대하여 2 M 황산용액에 3% H2O2를 첨가해 침출액을 얻었다. 침출액을 모사한 황산합성용액을 0.3 M의 Cyanex 301로 추출하면 구리(II)가 선택적으로 추출되었다. 또한 Cyanex 301에 추출된 구리는 30% 왕수를 사용해 탈거하는 것이 가능했다. 코발트(II)와 니켈(II)이 존재하는 여액을 이온성액체인 ALi-SCN을 사용해 유기상과 수상의 부피비가 2인 조건에서 코발트(II)를 선택적으로 추출했다. ALi-SCN에 추출된 코발트(II)는 15%의 암모니아 용액을 사용해 3단의 교차식 다단탈거로 완전히 탈거할 수 있었다. 이러한 결과를 바탕으로 구리(II), 코발트(II), 및 니켈(II)이 용해된 황산용액에서 세 금속을 용매추출로 분리하는 공정을 제안했다.