1. 서 론
2. 실험 방법
2.1. 시료
2.2. 방법
3. 실험 결과 및 고찰
3.1. 실험계획법에 의한 염배소 실험 결과
3.2. 실험계획법에 의한 염배소 결과 분석
3.3. 실험계획법에 의한 알루미늄의 침출 모델
4. 결 론
1. 서 론
바나듐은 자동차용 철강의 첨가제로 사용되기 시작한 이래로 세계 생산량의 80% 이상이 고강도 철강 제조 시 첨가제로 사용되어 온 희유금속이다1). 최근에는 전력 저장 시스템(ESS) 시장의 급성장에 따라 리튬이온전지와 함께 폭발, 화재 등의 위험이 없는 바나듐 레독스 전지도 큰 관심을 받고 있다. 세계적인 규모의 철강 산업을 갖고 있는 우리나라는 주요 바나듐 소비국으로 주로 브라질, 중국 등으로부터 정광, 금속, 합금, 화합물, 스크랩 등 다양한 형태로 수입하며, 2002년 10,212 천달러에서 2022년 158,662 천달러로 15배 이상 증가하였다2). 주요 수입 형태로는 오산화바나듐과 페로바나듐으로 각각 2023년 5,279 톤, 2,450 톤에 달한다3). 신재생에너지/ESS 분야 역시 국가적인 정책 추진 및 투자에 따라 많은 발전이 기대됨에 따라 국내 바나듐 수요량은 더욱 증가할 것으로 예상된다.
전 세계 바나듐 매장량 및 생산량의 90 % 이상을 중국, 러시아, 그리고 남아공이 차지하고 있으며4), 가격은 시장 상황에 따라 공급 과잉과 부족 사이를 오가며 지난 20년간 매우 큰 변동 폭2,5)을 나타내었다. 국내 바나듐 공급은 일부 석유화학 폐촉매의 재활용을 통해 생산되는 것 외에는 거의 대부분 수입에 의존하고 있으며, 국내 광산 자원으로부터 바나듐 원료 확보는 없는 실정이다4). 한편 국내 포천 관인광산에 매장된 함바나듐 티탄 자철석에서 비교적 높은 품위의 바나듐(V2O5∼0.54 wt%)이 함유된 것을 확인하였으며5), 현재는 제철소 노벽 보호제로만 활용되고 있다.
바나듐은 구리, 니켈, 아연 등의 다른 금속들과는 달리 농축된 광산이 존재하지 않고 다양한 광석에서 주로 Fe3+를 치환한 V3+로 분포하고 있다5). 포천 관인광산의 광석은 자철석 매트릭스내에 티탄 철석이 두께 나노미터 수준의 용리 구조로 나타나고 바나듐은 자철석 부분에 주로 분포하고 있다6). 따라서 함티탄 자철석의 파분쇄 후 자력선별을 통해 바나듐 정광을 효과적으로 얻을 수 있다. 일반적으로 바나듐 정광의 제련은 ⅰ) 파분쇄, ⅱ) 자력선별 ⅲ) 나트륨염을 이용한 염배소, ⅳ) 염배소 산물의 수침출, ⅴ) 암모니아를 이용한 암모늄-바나듐염 석출, ⅵ) 하소를 통한 오산화바나듐 제조 등으로 이루어져 있다7). 일반적으로 염배소 단계에서 탄산나트륨이나 염화나트륨을 바나듐 정광과 혼합한 뒤 800∼1200 °C에서 식 (1)과 같은 반응을 통해 수용성의 메타바나듐산 나트륨을 제조한다7,8). 그러나 이 과정에서 식 (2), (3)에 따른 Si, Al 등의 수용성 나트륨염의 생성은 침출 이후 바나듐 습식 정제 단계를 복잡하게 하는 요인이 되기도 한다7). 한편, 염배소에 황산나트륨을 사용하면 탄산나트륨보다 염배소 온도가 높아지고 부식성 가스가 발생하지만 바나듐 침출율도 향상되고 바나듐에 대한 선택성이 높아지는 것으로 보고된 바 있다8). Kim 등1)은 황산나트륨을 사용한 함바나듐 티탄 자철석의 배소 시 탄산나트륨에 비해 배소온도는 200 °C 높지만 VS4 또는 VOSO4 상의 형성 가능성과 이의 선택적 침출로 바나듐의 침출율이 높고 알루미늄, 실리콘 등의 불순물은 낮은 침출율을 보임을 보고하였다.
탄산/황산 혼합염을 이용한 배소는 남아프리카의 Mokopane vanadium project에서 제안되었지만 자세한 것은 알려지지 않았다8).
따라서 본 연구에서는 바나듐 정광의 염배소 온도가 상대적으로 낮고 부식성 가스가 발생하지 않는 탄산나트륨과 바나듐의 침출율과 선택성이 높은 황산나트륨의 장점을 취하기 위해 이 둘을 혼합한 나트륨염을 배소에 사용하고 배소산물의 수침출 특성을 조사하고자 하였다. 바나듐 정광은 철과 티타늄을 주성분으로 하여 바나듐, 알루미늄, 실리콘, 망간 등이 함유되어 있는데, 염배소 바나듐 정광의 수침출 후 바나듐을 바나듐산나트륨으로 침전 회수하기 위한 전 단계로 알루미늄을 먼저 침전 회수하여야 한다. 이때 침출된 알루미늄의 농도가 높으면 침전 제거 시 바나듐과 공침이 발생하여 바나듐의 회수율이 낮아지게 된다9). 따라서 본 연구에서는 염배소 산물의 수침출 시 바나듐, 알루미늄의 침출 선택성에 대한 배소 요인들의 영향과 이들의 상호작용을 조사하고자 실험계획법을 적용하여 탄산나트륨과 황산나트륨의 혼합비, 배소온도 및 이 둘의 상호작용 등의 요인 영향력을 통계적 방법으로 분석하였다.
2. 실험 방법
2.1. 시료
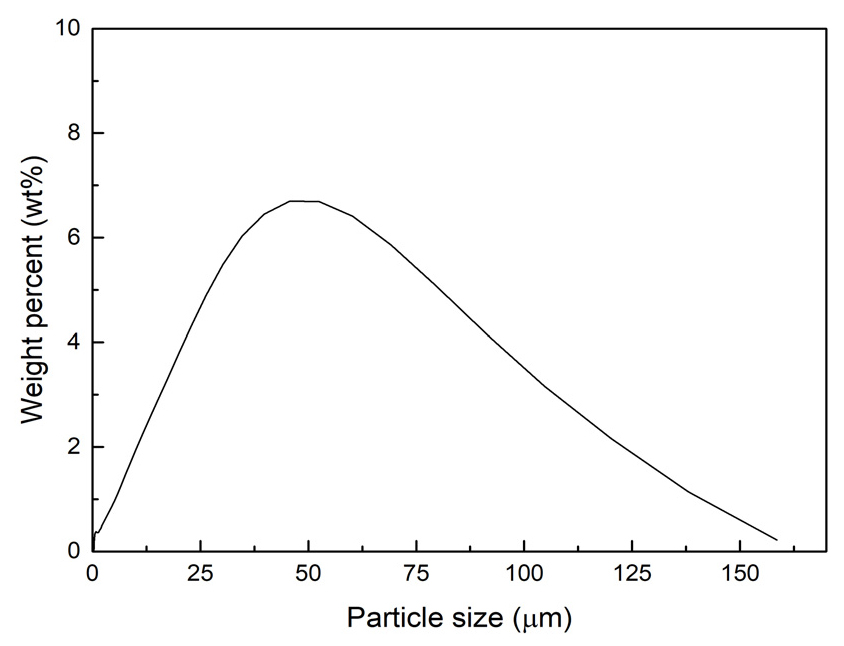
본 연구에서는 국내 포천 관인광산에서 생산되는 함티탄 자철석을 사용하여 파분쇄 및 자력선별을 통해 제조한 160 μm 이하 입도의 바나듐 정광을 염배소 실험에 사용하였다(Fig. 1). Table 1은 바나듐 정광의 XRF(X-ray Fluorescence) 분석 결과를 나타낸 것이다. 제조된 바나듐 정광은 오산화바나듐 기준으로 1 wt%의 함량을 나타낸다. 염배소에 사용된 탄산나트륨과 황산나트륨은 각각 Junsei Chemical의 GP급을 사용하였다. 수침출은 18 MΩ・cm의 초순수를 사용하였다.
Table 1.
Chemical composition of vandium concentrate
| Material | Concentration (wt%) | ||||||||
| TiO2 | Total-Fe | SiO2 | Al2O3 | CaO | MgO | MnO | P2O5 | V2O5 | |
| V-conc. | 9.8 | 61.1 | 1.7 | 2.4 | 0.13 | 1.2 | 0.21 | 0.03 | 1.0 |
2.2. 방법
2.2.1. 염배소
바나듐 정광과 염배소에 사용된 탄산나트륨, 황산나트륨을 실험계획법에서 설계된 비율로 혼합하고 20 g의 시료를 백금 도가니(가로×세로×높이=50 mm×70 mm×15 mm)에 담아 관상로 중앙부 열전대 직하에 장입하고 염배소를 실시하였다. 실험에 사용된 관상로는 수퍼칸탈 발열체를 사용하고 분위기가 조절되는 형태이다. 설정된 실험 온도에 도달하면 공기를 2 L/min의 유량으로 주입하면서 10 분 뒤 시료가 담긴 백금도가니를 장입하였다. 정해진 시간동안 배소 반응 뒤 백금 도가니를 꺼내어 상온에서 자연 냉각시켰다.
2.2.2. 수침출
수침출을 위한 시료는 염배소산물을 막자사발로 일차 분쇄 후 shatter box로 20초간 재분쇄하였다. 수침출을 위해 250 mL 용량의 이중자켓 경질유리 반응조를 사용하였고 교반을 위해 오버헤드 모터에 연결된 교반봉을 사용하였다. 분쇄된 염배소 시료 15 g을 초순수 150 mL에 투입하고 25 °C, 300 rpm 조건에서 30분간 실시하였다. 침출액은 일회용 주사기로 채취하고 0.2 μm 실린지 필터를 사용하여 혼입된 침출 잔사를 제거하였다. 또한, 침출액과 침출잔사의 고액분리 후 건조된 침출잔사 0.5 g을 왕수에 용해시키고 이를 200 또는 250 mL로 희석하여 분석용 용액을 준비하였다. 바나듐과 알루미늄의 침출율은 유도결합플라즈마 분광분석기(Inductively Coupled Plasma Optical Emission spectroscopy, OPTIMA 8300, Perkin Elmer, USA)를 이용하여 침출액과 잔사처리 용액내 바나듐 및 알루미늄을 정량분석하고 이를 이용하여 해당금속의 침출율을 계산하였다.
2.2.3. 실험계획법 설계
실험계획법 적용을 위해 바나듐 정광(20 g): 혼합 나트륨염(5 g) = 4:1 의 무게비로 고정하고 혼합나트륨염 제조 시 탄산나트륨과 황산나트륨의 무게비율, 배소온도를 요인으로 사용하였고 중심점을 포함한 2 요소 2 수준, 3 회 반복 요인배치법을 실시하였다. 실험계획은 Table 2에 나타내었다. 실험 결과 분석은 Minitab 프로그램과 Design Expert 프로그램을 사용하였다.
Table 2.
Two factors 2-level factorial design with a central point for water leaching of vanadium concentrate
| Factor | Level | Numerical transformation | ||
| 1 | 2 | 1 | 2 | |
| Na2SO4 ratio1) (wt.%) | 30 | 70 | -1.0 | 1.0 |
| Temperature (°C) | 1000 | 1200 | -1.0 | 1.0 |
3. 실험 결과 및 고찰
3.1. 실험계획법에 의한 염배소 실험 결과
Fig. 2는 실험계획법에 따라 수침출 시료를 제조하는 염배소 과정과 산물의 사진을 나타낸 것이다. Fig. 2(a)는 시료의 정확한 온도조절을 위해 관상로의 알루미나 튜브 중앙지점 열전대 직하에 시료를 담은 백금도가니가 위치하는 것을 나타내고 있으며, 배소 후 시료의 상태는 배소 조건에 따라 약간의 차이는 있으나 대체로 Fig. 2(b)와 같다.
Table 3은 실험계획법에 따라 실시한 실험 결과를 나타낸 것이다. 바나듐 침출율은 요인 수준의 변동에 크게 영향을 받지 않고 평균 86 % 의 침출율을 나타내었으나 알루미늄의 침출율은 조건별로 0∼9 % 사이에서 매우 큰 차이를 나타내었다.
Table 3.
Factorial design and experimental results of vanadium concentrate
3.2. 실험계획법에 의한 염배소 결과 분석
Table 4는 위로부터 얻어진 실험 결과를 이용하여 요인들의 효과에 대한 영향력 및 T 검증 결과를 나타낸 것이다. 바나듐 침출의 경우 배소 온도, Na2SO4 비율, 그리고 이 둘의 교호작용의 영향력이 각각 64.23, 0.016, 35.75 %로 나타났지만, T 검증으로부터 얻어진 P 값은 각각 0.177, 0.982, 0.302로 유의수준(α) 0.05 보다 상당히 커서 이 요인들의 변화가 통계적 유의한 차이를 만들지 않는다는 귀무가설이 기각되지 않는다. 즉 바나듐 수침출은 요인들의 변동에 통계적으로 유효한 영향을 받지 않았다는 의미이다. 한편 알루미늄의 경우 바나듐과는 상이하게 T 검증 결과 P 값이 모두 0으로 유의수준보다 현저히 낮았으며 이는 요인들의 변동이 뚜렷한 영향을 준다는 뜻이다. 각 요인들의 영향력은 대체로 30∼40 % 사이로 비슷한 정도이나 효과의 부호는 배소온도, Na2SO4 비율이 마이너스, 이 둘의 교호작용이 플러스로 서로 반대 방향으로 영향을 준다는 의미이다. 마이너스 부호는 요인의 수준이 높아질 때 침출율이 낮아지고 플러스 부호는 이와 반대이다.
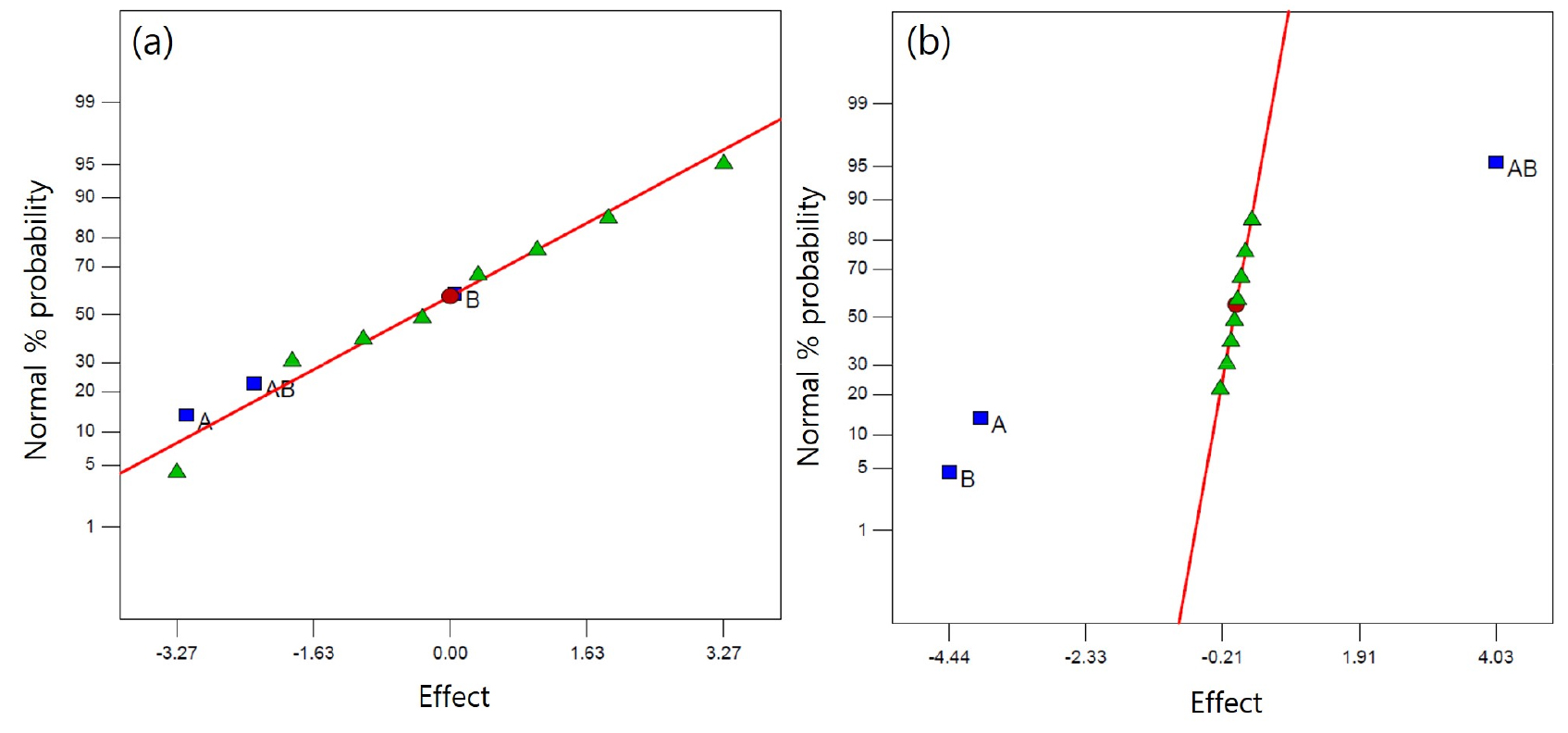
Fig. 3는 Table 4의 바나듐과 알루미늄 수침출에 대한 DOE 결과를 정규확률(Normal Probability) 분석으로 나타낸 그림이다. 요인 조작이 효과가 없는 경우 침출 실험 결과가 확률적으로 일어날 수 있는 정규분포를 따른다고 가정하였을 때, 이로부터 벗어나는 정도가 클수록 요인 조작 효과가 크고 침출에 미치는 요인의 영향력이 보다 유의미함을 의미한다. Fig. 3(a)의 바나듐은 확률적으로부터 일어날 수 있는 정규분포로부터 요인들이 크게 떨어져 있지 않아 요인 변동이 침출율에 통계적으로 유의미한 영향을 주지 않는 것으로 나타났다. 배소 온도나 나트륨염 혼합비의 변동에 따른 바나듐 침출율의 유의미한 차이가 없는 것으로부터 혼합염을 사용한 본 실험의 요인 변동 범위에서는 배소후 수용액과 접촉, 용해될 수 있는 형태의 NaVO3나 VOSO4 같은 가용성 상의 형성량이 요인 변동에 따라 유의미한 차이를 보이지 않는 것으로 통계적 해석이 가능하다.
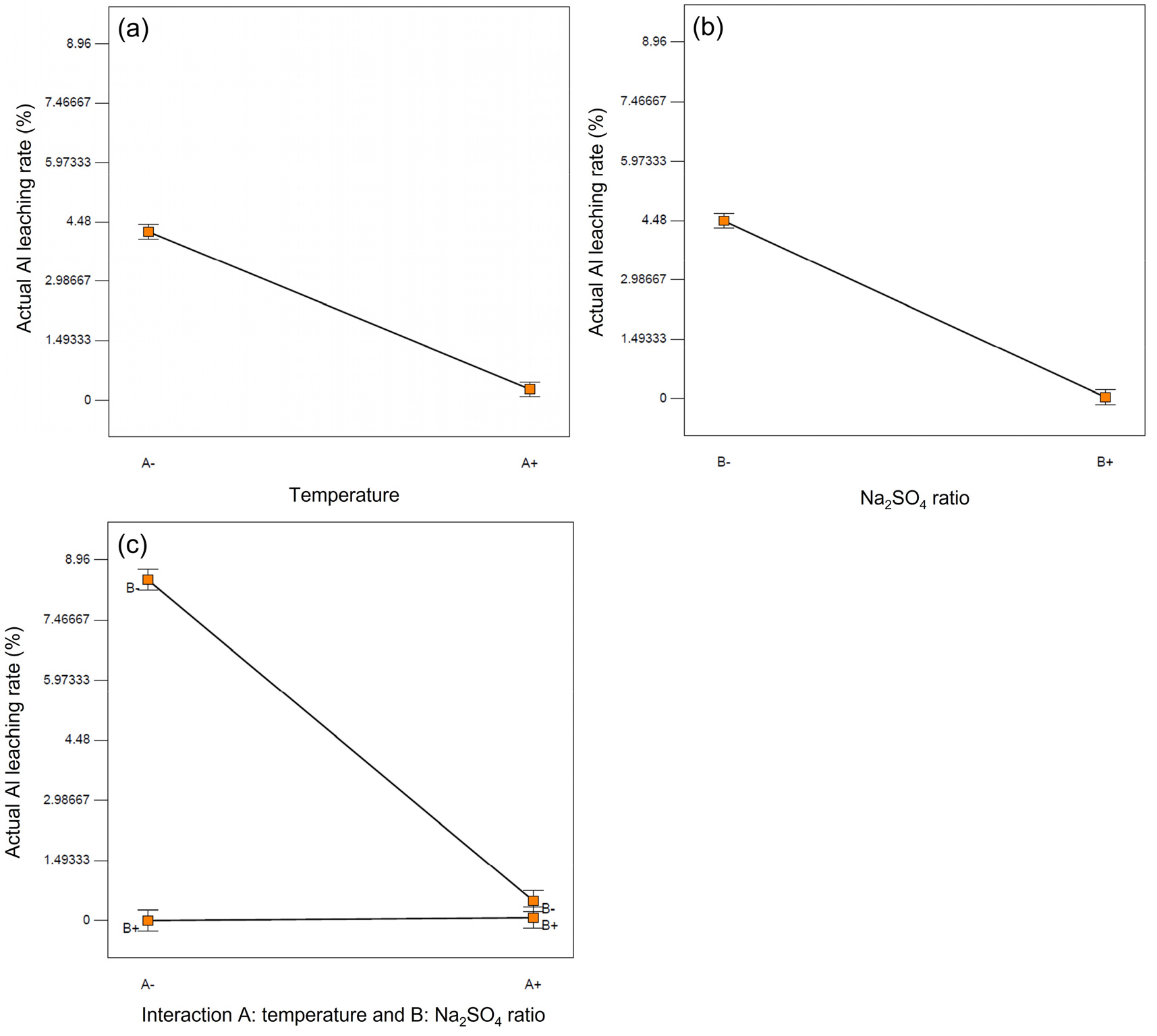
한편 알루미늄의 침출율의 경우는 Table 4의 effect contribution에서 보듯이 배소온도, Na2SO4 비율, 그리고 이 둘의 교호작용이 비슷한 수준의 값을 나타내고 있다. 이는 알루미늄의 침출을 억제하기 위해 배소온도와 Na2SO4 비율을 조절할 때 어느 하나가 주도적인 조절 효과를 가지지 못함을 의미하며, 이 둘과 반대로 작용하는 교호작용에 의한 효과 또한 배소 단계 설계 시 고려해야 할 요소임을 알 수 있다. Fig. 3(b) 정규분포로부터 배소 온도 (A)와 Na2SO4 비율 (B)이 뚜렷하게 좌측의 음부호쪽으로 위치하고 이 둘의 교호작용 (AB)은 양부호쪽으로 위치하고 있다. 이는 요인 변동이 알루미늄의 침출율에 뚜렷한 영향을 미쳤음을 의미한다. Fig. 4는 Table 4의 알루미늄에 대한 주요인과 교호작용의 침출율에 대한 영향을 도식화한 것이다. 배소온도와 Na2SO4 비율은 모두 요인 수준이 높아질수록 알루미늄의 침출율이 현저히 낮아짐을 보여준다. 황산나트륨은 배소 시 알루미늄과 반응하여 가용성 염을 만들지 않는 것으로 생각되며, 배소 온도 또는 Na2SO4 비율이 높을수록 황산나트륨의 영향력이 뚜렷해져 알루미늄의 침출율을 낮추는 것으로 생각된다. 이 둘의 교호작용의 경우는 온도가 낮을 때(A-)는 Na2SO4 비율이 낮은 경우(B-) 침출율이 현저히 높았으며 온도가 높을 때(A+)는 Na2SO4 비율에 상관없이 전체적으로 침출율이 낮았다. 식 (3)에 따라 형성된 알루민산 나트륨(NaAlO2)은 물에 잘 녹는 수용성 물질로 탄산나트륨만을 배소에 사용하면 알루미늄의 침출율도 높을 것으로 예측된다. 그러나 황산나트륨은 배소 시 알루미늄과 반응하여 가용성 염을 만들지 않는 것으로 생각된다. 탄산나트륨 대비 황산나트륨의 배소온도가 높다는 점으로부터 배소온도가 높아지면 황산나트륨의 첨가 효과가 뚜렷해지고 이로부터 첨가비가 30 % 일때도 Fig. 4(c)에서 보듯이 알루미늄의 침출율은 70 % 첨가에 근접하게 낮아지는 것으로 생각된다. 또한 황산나트륨의 첨가비가 높아지면 비록 배소온도가 낮을 경우라도 높은 첨가량이 낮은 온도의 단점을 극복하고 알루미늄의 침출율을 낮추는 것으로 생각된다.
Table 4.
T-test of DOE result for vanadium and aluminum
Table 5는 알루미늄 실험 결과에 대한 분산분석(ANOVA) 결과를 나타낸 것이다. T 검증에서 나타난 바와 같이 F 검증에서도 주요인인 온도(A), Na2SO4 비율(B) 뿐만 아니라 이들의 교호작용(AB)도 F 값이 F(0.05) 보다 모두 유의미하게 커서 유효한 것으로 판명되었다. 그러나 곡률효과(curvature)에 해당하는 F 값은 F(0.05)보다 작고 이로부터 계산된 P 값이 0.102로 유의수준(α) 0.05 보다 커서 곡률효과는 없다고 판단할 수 있다.
Table 5.
ANOVA analysis of DOE experiment for Al leaching
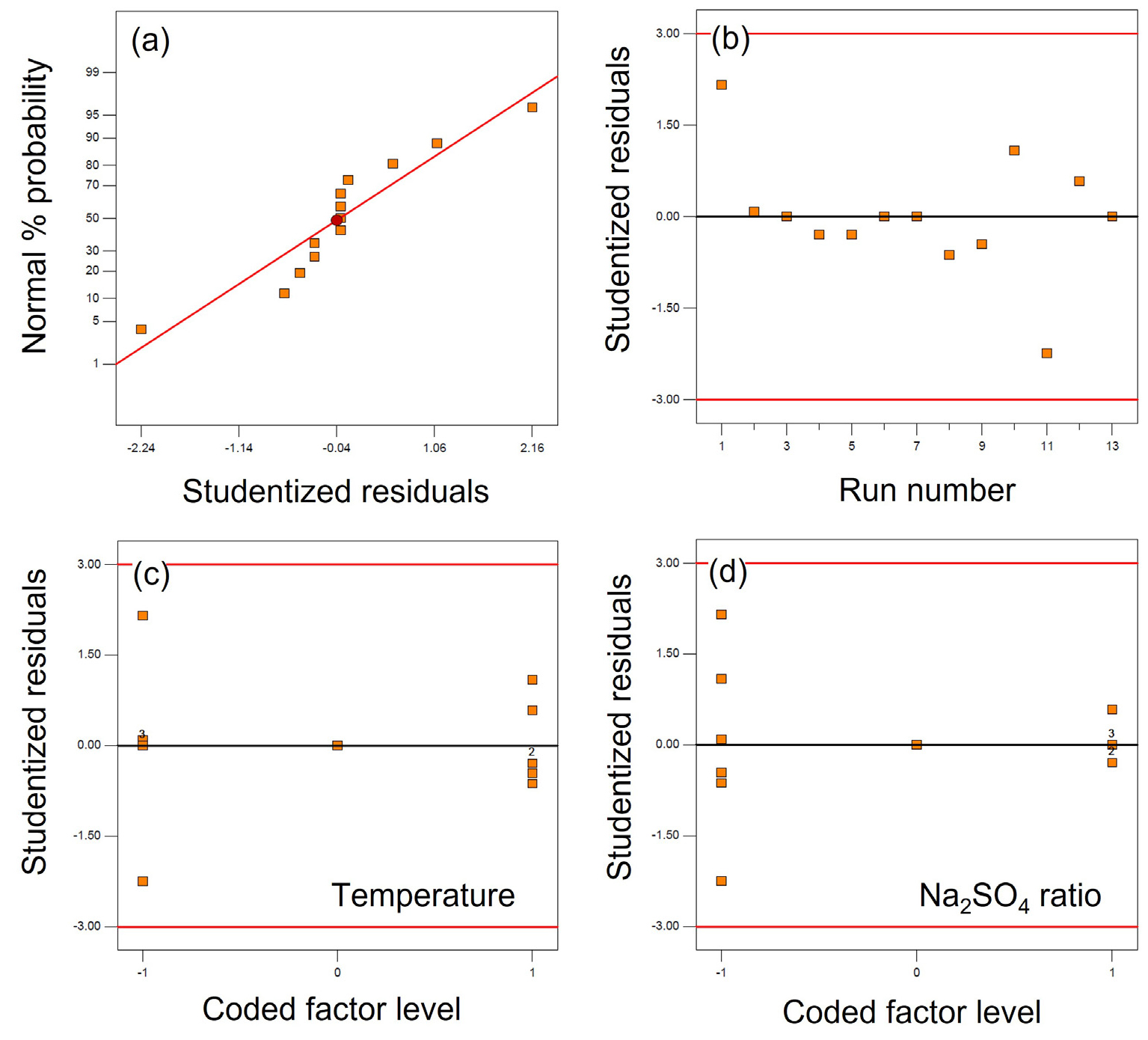
Fig. 5는 본 실험의 잔차분석을 행한 결과이다. 잔차분석을 통해 실험이 유효한지 요인 외 의도치 않은 다른 것들의 영향이 있었는지를 알 수 있다. Fig. 5(a)는 잔차의 정규확률 분석을 나타낸 것으로 모든 실험이 확률적으로 일어날 수 있는 정규분포로부터 유의미하게 벗어나지 않았다. Fig. 5(b)∼(d)는 실험 순서, 요인의 레벨에 따라 잔차를 잔차의 표준오차로 나눈 스튜던트화 잔차가 허용범위(±3) 밖으로 벗어나는지를 나타낸 것으로 모든 경우 이상치는 보이지 않는다. 다만 요인의 레벨이 낮은 경우 허용범위 내에서 좀 더 분산된 값들을 보이고 있다. 이에 대한 원인 분석은 향후 좀 더 연구가 필요한 부분이다.
3.3. 실험계획법에 의한 알루미늄의 침출 모델
이상의 실험 결과 분석으로부터 바나듐은 요인의 변동에 따른 침출율의 차이가 유효한 결과를 나타내지 않았으나 알루미늄은 유의미한 결과를 얻었다. 이를 바탕으로 알루미늄의 침출 모델식을 도출하고자 하였다. 본 실험 결과의 T 검증과 분산분석으로부터 모델식 도출 시 고려해야 할 요소는 배소온도와 Na2SO4 비율 등 두 가지 주요인과 이 둘의 교호작용임을 확인하였다. 이로부터 침출 모델식은 식 (4)와 같이 나타낼 수 있다10).
식 (4)에서 Y는 알루미늄의 침출율, β는 인자계수, A, B, AB는 각각 온도, Na2SO4 비율, A와 B의 교호작용, 그리고 ε는 Y를 측정할 때 발생하는 오차이다.
실험결과의 회귀분석을 통해 얻은 침출 모델식은 식 (5)와 같고 Table 6은 침출 모델식에 대한 분산분석을 실시한 결과이다. 모델식의 F 값은 667.03으로 F(0.05) 보다 유의미하게 크서 해당 모델식이 유효한 것으로 나타났다. 또한 곡률효과의 F 값은 3.41로 F(0.05) 5.32보다 작아 곡률효과는 없는 것으로 생각할 수 있다. 식 (5)의 결정계수(R-squrared) 0.9960은 침출모델식이 알루미늄의 침출율에 대해 99 %를 설명력을 가지고 있음을 의미한다.
Table 6.
ANOVA of multiple linear regression model for Al leaching
| Source | SS | DF | MS | F | F (0.05) | P |
| Model | 154.92 | 3 | 51.64 | 667.03 | 4.07 | 0.000 |
| Curvature | 0.26 | 1 | 0.26 | 3.41 | 5.32 | 0.102 |
| Residual | 0.62 | 8 | 0.077 | |||
| Pure error | 0.62 | 8 | 0.077 | |||
| Total | 155.80 | 12 | ||||
| R-squared | 0.9960 |
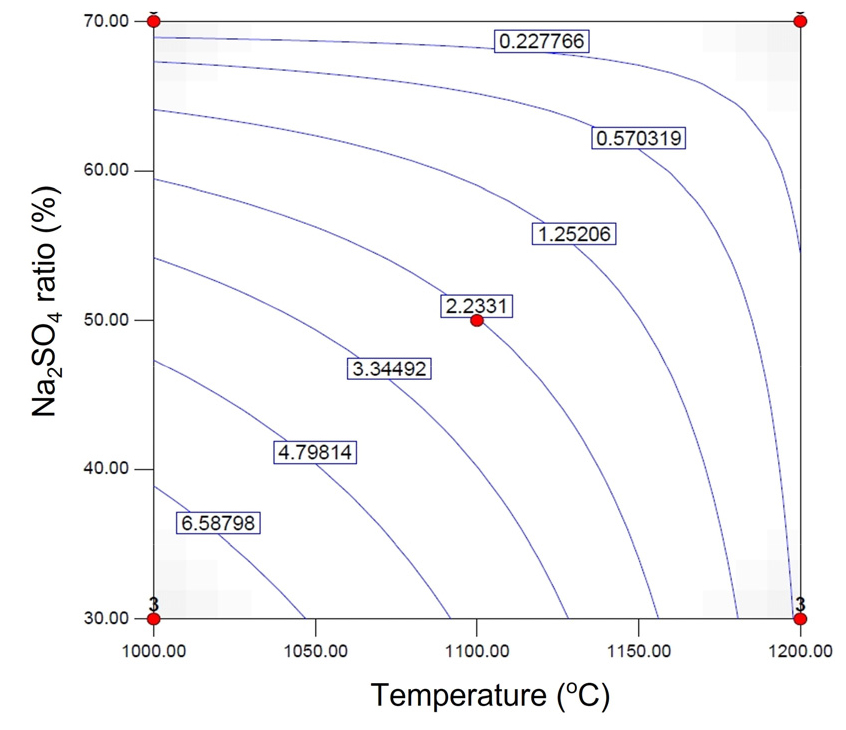
Fig. 6은 식 (5)의 침출 모델식을 이용해 요인의 수준 변화에 따른 알루미늄의 등침출율선을 나타낸 것이다. 알루미늄의 침출율은 다른 요인이 고정될 때 온도가 높아질수록, Na2SO4 비율이 높아질수록 낮아져 침출이 억제되는 것을 알 수 있다. 또한 침출온도가 매우 높거나 Na2SO4 비율이 매우 높은 경우에는 등침출율선이 활처럼 휘면서 나머지 요인의 수준 변화에 알루미늄의 침출율이 둔감하게 움직이는 것을 알 수 있다. 예를 들면 Na2SO4 비율이 69 % 정도에 이르면 배소온도 1000∼1100 °C 사이에선 알루미늄 침출율이 0.2 % 수준에서 온도 증가에 따라 매우 천천히 감소한다. 이는 Na2SO4 비율이 높을 경우에는 알루미늄 침출을 억제하기 위해 높은 온도에서 배소를 진행할 필요가 없음을 의미한다. 반대로 배소온도가 매우 높을 경우에 해당하는 그림의 오른쪽 수직에 가까운 등침출선 형태로부터 Na2SO4 비율을 크게 높이지 않아도 높은 알루미늄 침출 억제를 달성할 수 있음을 알 수 있다.
4. 결 론
본 연구에서는 국내 포천 관인광산에서 생산된 함티탄 자철석을 사용하여 제조한 바나듐 정광(V2O5 기준 1 % 함량)의 염배소 요인의 수침출에 대한 영향을 실험계획법을 이용한 통계학적 방법으로 조사하였다. 바나듐 정광의 염배소 온도가 상대적으로 낮고 부식성 가스가 발생하지 않는 탄산나트륨과 바나듐의 침출율과 선택성이 높은 황산나트륨의 장점을 취하기 위해 이 둘을 혼합한 나트륨염을 배소에 사용하였고 이때 나트륨염의 혼합비를 배소온도와 함께 요인으로 선택하고 중심점을 포함한 2수준 3회 반복 실험을 설계하고 실시하였다. 실험 결과에 대한 T 검증을 통해 바나듐의 침출율에는 요인들의 변동이 통계학적으로 유의미한 영향을 주지 않았지만, 알루미늄의 침출율에는 큰 영향을 주는 것을 확인하였다. 알루미늄의 침출에 미치는 요인들의 분산분석(ANOVA)을 통해 T 검증에서와 같이 배소온도, 황산나트륨의 비율, 그리고 이 둘의 교호작용의 모두 중요한 요인으로 나타났으며, F값이 F(0.05)보다 작은 곡률효과는 배제할 수 있었다. 또한, 실험 결과의 잔차분석에서 이상치는 발견되지 않아 실험 결과가 유효함을 확인하였다. 회귀분석을 통해 유의수준 α=0.05에서 결정계수(R-squared) 0.9960으로 알루미늄의 침출 결과에 대해 99 %의 설명력을 가진 아래의 침출 모델식을 얻었다.