1. 서 론
2015년 12월, 제21차 유엔기후변화협약 당사국 총회(COP21)에서 파리기후변화 협약이 합의된 이후 전 세계적으로 온실가스 감축을 위한 노력이 이루어지고 있다. 이에 각국에서는 신재생 에너지, 특히 태양광 발전 중심의 에너지믹스 재편을 통해 지속 가능한 신재생에너지 보급 확대에 박차를 가하고 있다. 국내의 경우, 태양광 모듈의 사용기한이 도래함에 따라 2030년 약 8만 톤의 폐 모듈 발생이 예상되며, 2045년에는 155만 톤 이상의 폐 모듈 발생이 예상되고 있다1). 국내 태양광 발전시장에서는 결정질계 실리콘 모듈이 90% 이상을 차지하고 있으며, 일반적으로 태양광 모듈은 알루미늄 프레임, 강화유리 EVA(ethyl vinyl acetate) 필름, 태양전지, 백시트 등으로 구성되어 있다. 실리콘은 모듈 구성 소재의 3.65~4.1%를 차지하므로2,3), 2045년 실리콘 배출량은 약 6만 5천 톤에 이를 것으로 추정된다. 현재 폐 모듈은 재활용 기술이 존재하지 않아 대부분 매립 처분해야 하는 상황이다. 국내는 2022년까지 태양광 모듈 회수〮보관 체계 구축 및 재활용 기술개발 등 재활용 기반을 마련 한 후, 2023년부터 폐 모듈 생산자책임재활용제도(EPR)를 도입할 예정으로 업체는 회수한 폐패널을 80% 이상 재활용 하여야한다4). 따라서 태양광 폐패널에서 고순도 실리콘을 회수하고 재활용 하는 것은 태양광 폐모듈 재활용 경제성제고 및 재활용율 증진을 위해 매우 중요하다.
탄화규소는 강한 공유결합을 하고 있어서 결합력이 아주 강하기 때문에 고온안정성, 열 충격 저항성이 높고, 내마모성, 자기윤활성이 좋을 뿐 아니라 내산화성, 내식성 등의 특성이 우수하여 베어링, 메커니컬실 및 반도체용 부품 소재로써 주목받는 재료이다. 가장 대표적인 탄화규소 제조 방법은 실리카를 고온에서 탄소환원 시키는 에치슨(Acheson)법을 사용하여 제조되는데, 이는 α상의 탄화규소(α-SiC)를 제조하는데 적합한 대표적 산업적 양산 방법이다. 그 외에도 β상의 탄화규소 제조방법에는 탄소환원법(carbothermal reduction method), 직접탄화법(direct carbonization), 기상반응을 이용한 합성법, 액상고분자 반응법 등이 잘 알려져 있다5,6,7,8). 본 연구에서는 태양광 폐실리콘 웨이퍼에서 고순도 실리콘 분말을 회수하였으며, 탄화규소 분말 합성특성을 살펴보기 위하여, 직접탄화법을 이용해서 실리콘 분말과 탄소분말을 혼합한 후, Ar 분위기에서 열처리온도 변화에 따른 탄화규소 분말 합성특성을 연구하였다.
2. 실험방법
2.1. 실리콘 정제 및 회수율 계산
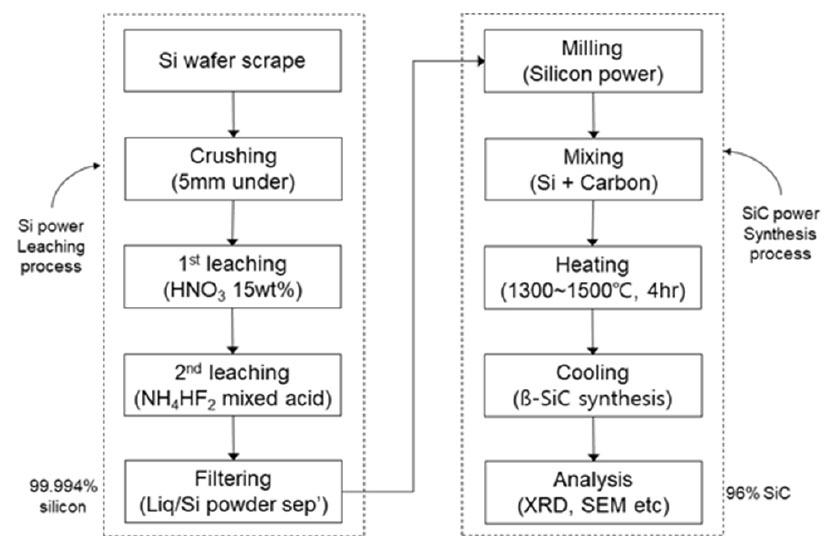
폐실리콘 웨이퍼에서 침출 정제공정을 거쳐 고순도 실리콘을 회수하고, 회수한 실리콘을 활용하여 탄화규소 분말을 합성하는 공정은 Fig. 1과 같다. 실리콘 정제를 위해서 태양광패널 생산 공정에서 발생하는 폐실리콘 웨이퍼를 5mm 이하 크기로 파쇄한 후, 180ℓ 반응기에 폐실리콘 14kg과 침출액 42ℓ를 투입하였다. 폐실리콘에 함유된 불순물을 정제하기 위해서 상온(20℃)에서 각 단계별 60분간 반응시켰으며, 정제효율을 높이기위해서 교반기를 이용하여 200rpm으로 교반하였다. 실리콘 정제를 위하여 당초에는 산 종류를 변경하면서 3단계에 걸쳐 실험하였으나, 공정단계 변화에 따른 시간절약 및 공정효율을 향상시키기 위해서 2단계에 걸쳐서 정제를 진행하였다. 1단계에는 15wt% 질산(HNO3) 용액을 사용하였으며, 2단계에서는 5~10% 불화암모늄(NH4HF2), 과산화수소(H2O2) 및 15~20% 황산(H2SO4) 혼합산을 사용하여 실리콘 불순물을 제거하였다. Fig. 2는 정제실험 전 폐실리콘 웨이퍼와 정제과정을 거친 후의 실리콘 및 침출액 사진이다. 실험에 사용한 실리콘에 대한 순도분석은 유도결합 플라즈마 방출분광기 ICP-OES(Perkin Elmer OPTIMA 8300) 및 원소분석기(LECO CS 744, Leco ONH836)를 이용하였다. 폐실리콘 웨이퍼 고순도화 과정에서 얻은 실리콘 회수율은 정제과정을 거친 실리콘분말에서의 실리콘함량을 실리콘웨이퍼에서의 실리콘 함량으로 나누어 계산(Eq. (1)) 하였다.
2.2. 탄화규소 분말 합성
탄화규소 분말 합성을 위하여 정제된 실리콘을 볼밀로 12시간 분쇄하였으며, 분쇄된 실리콘 분말과 카본블랙을 1 : 1.2 몰비로 혼합하였다. 실리콘 분말과 카본블랙의 입자형상 및 크기는 JEOL사 전계방출형 주사전자현미경(FE-SEM, JSM-7610F)을 이용하여 분석하였다. 실리콘과 카본블랙 혼합물을 1300℃, 1400℃ 및 1500℃ Ar 분위기에서 4시간 열처리하였다. 열처리 생성물 특성평가를 위하여 HORIBA 레이저 회절 입도 분석기(LA-950)를 이용하여 입도분포를 측정하였으며, 광물특성 변화는 X-회절분석기(BRUKER사 D8 Advance)를 이용하여 분석하였다. 화학성분은 유도결합 플라즈마 방출분광기 ICP-OES(Perkin Elmer OPTIMA 8300) 및 원소분석기(LECO CS 744, Leco ONH836)를 이용하였고, 입자형상 및 크기는 JEOL사 전계방출형 주사전자현미경(FE-SEM, JSM-7610F)을 이용하여 분석하였다. 열처리 생성물의 표면 구조 및 특성변화를 살펴보기 위하여 Bruker사 퓨리에 변환 적외선분광기(FT-IR, Vertex 80v)를 사용하였다.
3. 실험결과 및 고찰
3.1. 실리콘 정제
폐실리콘 웨이퍼 및 2단계에 걸쳐 불순물을 제거한 실리콘 성분은 유도결합 플라즈마 방출분광기 및 원소 분석기를 이용하여 분석하였으며, 원 시료 기준 30ppm 이상인 성분의 분석결과를 Table 1에 나타내었다. 분석결과에서와 같이 실리콘 순도 95.743%의 폐실리콘을 1차 질산용액 침출과정을 거쳐 99.932% 순도의 실리콘 분말을 얻을 수 있었으며, 혼합산을 사용한 2차 침출과정을 통해 99.994%의 고순도 실리콘 분말을 확보하였다. 1차 침출과정에서 질산을 사용한 것은 금속성분을 제거&회수하기 위한 것이고, 2차 침출과정에서 혼합산을 사용한 것은 비금속 성분을 효율적으로 제거하기 위한 것이다. 폐실리콘 웨이퍼의 회수율 계산결과를 Table 2에 나타내었다. 계산결과에서와 같이 실리콘 순도 95.74% 폐실리콘 웨이퍼 14kg을 사용하여 99.994% 실리콘 12.187kg을 회수하여 90.91%의 회수율을 확보할 수 있었다.
Table 1.
Analysis results of silicon components
Table 2.
Recovery rate of waste silicon wafer
|
Weight (kg) |
Silicon purity (%) | Recovery rate = | |
| Silicon wafer | 14.000 | 95.743 | |
| High purity silicon | 12.187 | 99.994 |
3.2. 탄화규소 분말 합성
탄화규소 분말 합성원료로 사용한 실리콘 분말과 카본블랙의 SEM 측정결과를 Fig. 3에 나타내었다. SEM 측정결과, 카본블랙의 경우에 30~50nm크기의 구형 일차 입자가 불규칙하게 뭉쳐져 있으며, 실리콘 분말은 각형의 조대한 3~10μm 입자표면에 1μm이하의 미세입자가 응집되어 있음을 관찰할 수 있다. 입도 분석기를 사용하여 측정한 실리콘분말의 평균입자 크기는 2.82μm로 측정되었다.
열처리 생성물에 대한 화학성분을 유도결합 플라즈마 방출분광기 및 원소 분석기를 이용하여 분석하였으며, 100ppm 이상인 성분의 분석결과를 Table 3에 나타내었다. 분석결과에서와 같이 열처리 온도가 1300℃에서 1400℃, 1500℃로 증가함에 따라 탄화규소 함량이 89.8%에서 95.9% 및 95.6% 로 증가함을 알 수 있다. 열처리온도 1300℃에서 1400℃로 증가할 때, 탄화규소 함량이 89.8%에서 95.9%로 크게 증가하였지만, 1400℃와 1500℃로 증가할 때, 탄화규소 함량 변화가 거의 없음을 알 수 있다. 이것은 Si와 탄소의 직접반응이 1150℃ 부근에서 시작해서9) 1400℃ 전에 대부분 완료되는 것을 의미한다. 열처리온도가 증가함에 따라 잔류 실리콘과 아울러 Na, K, 및 Fe 등의 불순물의 양을 감소시켜 탄화규소 순도 96% 까지 향상시켰으며, 열처리 온도증가에 따른 탄화규소 분말의 순도향상을 확인할 수 있었다.
Table 3.
Chemical components according to heat treatment temperature (1300℃, 1400℃ and 1500℃)
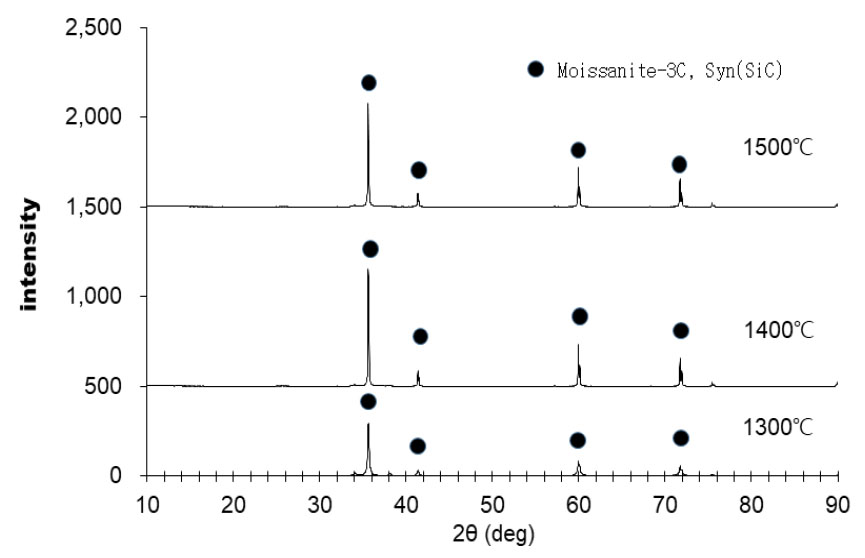
Fig. 4에 1300℃, 1400℃ 및 1500℃, Ar 분위기에서 4시간 열처리한 생성물에 대한 X-선 회절분석기 측정결과를 나타내었다. X-선 회절분석결과, β-SiC상의 주 피크인 35°, 60°, 73°에서 피크가 관찰되어, 열처리 생성물이 β-SiC임을 확인할 수 있었다. 피크강도를 보면 1300℃와 비교하여 1400℃ 및 1500℃ 피크강도가 증가하고 명확해져, β-SiC상의 결정도가 증가함을 확인할 수 있다.
열처리한 생성물에 대한 SEM 측정결과를 Fig. 5에 나타내었다. SEM 측정결과, 1300℃에서 열처리한 경우에는 입자형상이 원료물질인 실리콘 형상과 유사하게 각형의 모난 형상을 보여주고 있으나, 1400℃, 1500℃에서 열처리한 경우에는 표면이 용융된 것 같은 둥근 형상을 보여주고 있음을 확인하였다. 이것은 원료물질인 실리콘과 탄소반응이 시작되는 1150℃ 부근에서는 고상반응이 진행되어10) 원료물질인 실리콘 형상을 유지하지만 실리콘이 melting되기 시작하는 1400℃ 부근에서는 액상반응에 의해 실리콘 입자표면이 둥근 형상을 보여주게 된다. 1차 입자는 200nm~3μm 크기로 온도가 증가할수록 입자간 응집현상이 증가함을 알 수 있다. 이 결과는 0.35μm 크기의 실리콘 입자를 사용하고 1300℃에서 열처리 하였을 때, 100nm 크기의 미세한 1차 탄화규소 입자가 생성된 기존 연구 결과와5) 차이가 있었다. 0.35μm 실리콘 입자를 사용하였을 때 100nm크기의 미세한 탄화규소 입자가 생성된 기존 연구결과와, 2.82μm의 조대한 실리콘 입자를 사용하였을 때 1차 입자가 200nm~3μm로 증가한 본 실험결과를 비교할 때, 탄화규소 입자크기는 탄소분말의 입자크기뿐 아니라 실리콘 입자크기에 영향을 받는 것으로 판단되었다.
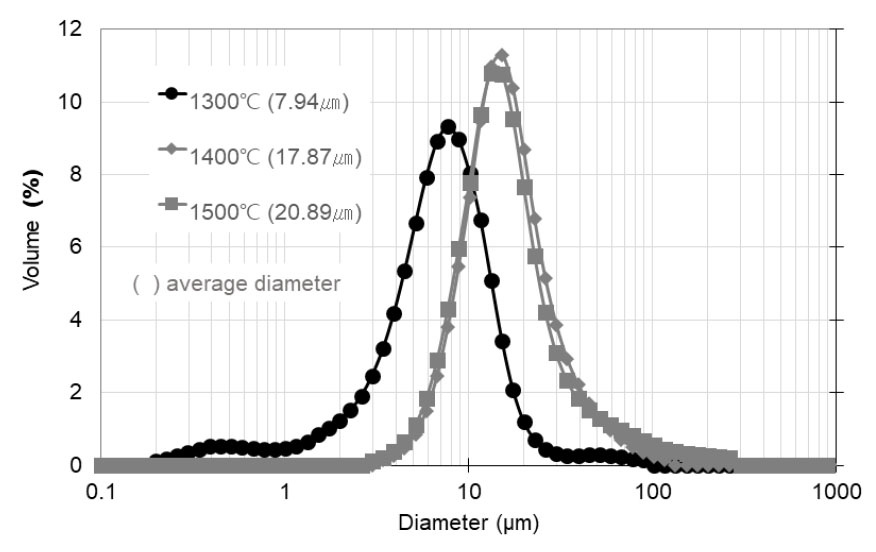
Fig. 6에 열처리 생성물의 입도분석 측정결과를 나타내었다. 입도분석결과, 1400°C와 1500°C에서 합성된 탄화규소 분말의 평균입경은 18~21μm로 유사한 경향을 보이나, 1300°C에서 합성된 탄화규소 분말의 입자크기는 8μm로 차이가 나는 것을 알 수 있다. 이러한 현상은 두 반응 메커니즘의 차이로 설명될 수 있다. 1400°C 부근인 실리콘의 융점보다 높은 값으로 온도를 증가시키면, 용융된 실리콘 Si(액체)와 C(s)의 반응은 기본적으로 Si(l) + C(s) → β-SiC(s) 반응 매카니즘을 따른다. 이 상태에서, 액체 Si는 침투하거나 Si 원자가 C(s)로 확산될 것이고, 여기서 반응이 일어나 β-SiC를 형성하거나 용융된 실리콘에서 탄소의 용출이 일어나 탄화규소가 용액 또는 증착 장소에서 (차가운) 증착 위치로 운반된다. 이러한 고체-액체 반응은 큰 입자를 만드는데 유리한 것으로 보인다10). 그러나 Si의 융점 이하의 온도에서는 Si(고체) + C(고체)형 반응이 일어나는 것을 알 수 있다. 상압 하에서 Si와 탄소의 분말 혼합물의 직접 반응은 1150°C 부근에서 천천히 시작된다9). 이러한 고체-고체 반응은 고체-액체 반응에 비해 작은 입자를 형성한다.
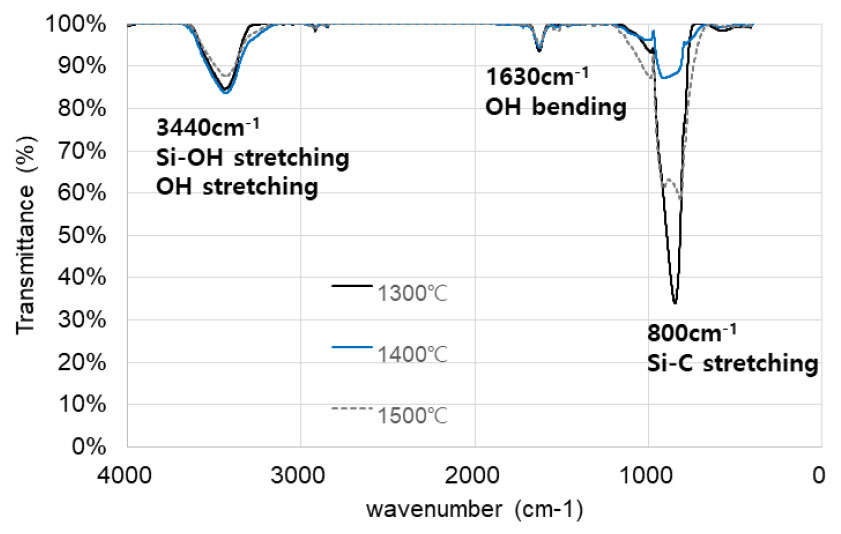
제조된 탄화규소 시료 표면의 화학결합과 작용기를 Fig. 7와 같이 FT-IR 스펙트럼을 이용하여 확인하였다. 그림에서 알 수 있는 바와 같이, Si-C 진동에 기인하는 피크가 800cm-1에 나타나는데, 이것은 탄화규소가 형성되었음을11) 나타낸다. 또한 Si-OH 및 OH 진동에 기인하는 3440cm-1 및 1630cm-1의 두 개의 강한 피크가 발견되었는데 이것은 탄화규소 표면에서 Si-OH의 존재와 시료 표면에 수분이 존재함을 보여준다.
4. 결 론
태양광 폐패널에서 고순도 실리콘을 회수할 뿐 아니라, 이를 활용하여 탄화규소 분말 제조가능성을 확인하고자 하였다. 본 연구에서는 질산용액과 혼합산을 사용한 2차에 걸친 정제과정으로 95.74% 폐실리콘 웨이퍼로부터 99.99% 실리콘 분말을 회수하였으며, 90.91%의 실리콘 회수율을 확보하였다. 아울러 정제된 99.99% 실리콘 분말과 탄소분말을 원료로 사용하여 열처리과정을 거쳐 β-SiC 분말을 합성하였다. 또한 반응온도 변화에 따른 탄화규소 분말 합성특성을 살펴보았다. 반응온도의 상승은 잔류 실리콘과 아울러 Na, K, 및 Fe 등의 불순물의 양을 감소시켜 탄화규소 순도 96% 까지 향상시켰으며, 고온열처리에 의한 탄화규소 분말열처리온도가 증가함에 따라 탄화규소 분말의 순도향상을 확인할 수 있었다. XRD 및 FT-IR 분석결과로부터 1300℃의 낮은 온도에서 β-SiC 분말이 합성되었음을 알 수 있었다. SEM 측정결과, 1차 입자는 200nm~3μm 크기로 온도가 증가할수록 각형의 모난 형상에서 표면이 용융된 것 같은 구형입자로 변화되면서 입자간 응집현상이 증가하는 것을 확인할 수 있었다. 아울러 미세한 실리콘 입자를 사용한 기존 연구결과5)와 2.82μm의 조대한 실리콘 입자를 사용하여 탄화규소 입자를 합성한 실험결과를 비교할 때, 탄화규소 입자크기는 실리콘 입자크기에 영향을 받는 것으로 판단되었다.