1. 서 론
2. 실 험
2.1. 실험재료
2.2. 실험방법
3. 결과 및 고찰
3.1. 사용 후 LAS 첨가양의 변화에 대한 영향
3.2. 교반 시간에 대한 영향
3.3. 초기 중금속 농도의 영향
3.4. pH 변화에 대한 영향
4. 결 론
1. 서 론
다양한 잠재적 가치를 가진 산업 광물인 제올라이트는 견고한 삼차원 구조로 된 결정성수산화 알루미노규산염(crystalline hydratedaluminosilicate)으로 정의된다. 순수한 의미의 제올라이트는 2.0~2.3 정도의 비중과 1.44~1.52 정도의 굴절률을 가지며 3~20Å 정도 크기의 균일한 세공을 지니고 있다. 50여종의 천연 제올라이트 및 산업용 촉매, 합성세제, 필터 등 다양한 목적의 150여종의 합성 제올라이트까지 합쳐 현재 약 200여종의 다양한 세공구조를 지닌 제올라이트가 알려져 있다1,2,3,4).
모든 제올라이트의 기본적인 구조는 각각의 산소를 두개의 사면체(tetrahedra)가 공유하고, 상대적으로 큰 양이온과 물분자들로 점유되며 서로 연결된 공동(cavity; surface pore)으로 둘러싸인 (Si, Al)O4 골격구조를 가진다. AlO4 단위의 음이온 충진은 교환성을 가진 양이온 들의 존재에 의해 균형을 이룬다. 이러한 이온 들은 쉽게 다른 물질들, 예를 들어 중금속이나 암모늄 이온들로 치환될 수 있다. 이 현상을 양이온치환(cation exchange)이라고 하며, 주로 나트륨, 칼륨, 칼슘 등의 양이온 및 마그네슘, 바륨, 스트론튬, 철 등의 일부 부수적인 양이온과 물이 구조 내에서 자유로운 활동 상태를 보임으로써 제올라이트에 양이온 치환성과 가역 탈수성(reversible-dehydration property)등의 특성을 가질 수 있도록 해준다. 즉, 제올라이트의 다공성 골격구조는 분자화합물의 크기와 형상에 따른 분자 혼합물 분리를 위한 분자체(molecular sieve) 반응을 가능하게 해준다. 상대적으로 매우 높은 양이온 치환능력을 가지는 제올라이트의 일종인 클리놉틸로라이트(clinoptilolite)는 이러한 특성을 활용한 황화수소(H2S)나 이산화황(SO2)과 같은 유독성가스의 강력한 흡착제로도 잘 알려져 있다5,6,7,8,9,10).
제올라이트의 독특한 선택적 이온교환 및 흡착 특성을 응용하여 실용화할 수 있는 주요 응용분야로는 현재 축산 및 농업 폐수 처리, 생활하수의 처리, 공업 폐수의 처리, 음용수의 수질 개선, 방사성 폐기물 처리 및 방사성 물질의 오염 방지, 폐기물 매립 및 소각처리 과정에서의 토양오염 성분의 제거 등을 들 수 있다. Loizidou와 Townsend는 수용액으로부터 중금속의 제거를 위한 천연 제올라이트의 선택적 이온교환 성질만이 중요한 것이 아니며 제올라이트가 재생되어 사용될 수 있는가의 여부도 중요하다고 언급하였고, 천연 페리어라이트(ferrierite)와 모데나이트(mordenite)가 클리놉틸로라이트보다 납에 대하여는 더 낮은 교환 성능을 보여주지만 폐수에서 납의 제거에 유용함을 제시하였다11). Semmens와 Seyfarth,의 연구에서는 천연 클리놉틸로라이트(특히 농축된 NaCl로 사전에 처리되었을 경우)는 폐수 내 중금속 제거에 아주 높은 선택성을 가지고 있음을 보여 준다. 특히, 다종의 금속으로 오염된 폐수의 처리 연구에 의하면 2N의 NaCl로 처리한 클리놉틸로라이트를 이용하여 15분의 접촉 시간 안에 90%의 중금속이 제거됨을 보고하였다. 이들의 연구에 의하면 클리놉틸로라이트의 선택성은 Pb2+>Cu2+>Cd2+>Zn2+>Cr3+>Co2+>Ni2+의 순을 보인다12). Blachard et al.은 클리놉틸로라이트로 이루어진 층(bed)을 만들어 암모늄 이온과 중금속을 제거하여 음용수를 순수하게 하는 처리공정에 대하여 연구하였다. 그들은 Na-클리놉틸로라이트층은 Pb2+>NH4+>Cd2+, Cu2+, Sr2+>Zn2+>Co2+의 순서로 중금속을 포함한 오염물질에 선택성을 보인다고 하였다5). 일반적으로 정화 작용의 최대 효과는 화학적 침전, 활성화된 탄소 컬럼, 음이온 교환물질등과 클리놉틸로라이트를 혼합하여 적용하면 쉽게 얻을 수 있다13). 이런 방법을 통한 오염물질의 제거 효율은 암모늄 90%, 인 90~99%, suspended solid 99%, 유기물질 94% 등이다. Kayablai와 Kezer는 매립지에서 전형적인 점토 대신 천연 제올라이트를 사용함으로써 요구되어지는 라이너의 두께를 줄이고 지하수에 있어 침출수에 의한 피해를 줄인다고 보고하였다14).
현재 LAS 소재는 조리기구, LCD 패널, 망원경 유리, 치과 기구, 자기 디스크 메모리, 방열 유리, 내화용 유리 등 전자소재 산업부터 주변 취사도구까지 다양한 산업 분야에 사용하고 있다. 하지만 LAS 소재의 재활용은 Li 소재를 중점적으로 회수하여 활용되는 연구가 주로 진행되고 있으며, 사용 후 LAS 자체를 활용하는 연구는 미흡한 수준이다. 최근에는 안전 문제 등의 이유로 인덕션의 보급이 증가하고 있고 향후 많은 양의 인덕션 탑플레이트들이 발생될 것이다.
본 연구에서는 인덕션 탑플레이트(induction top plate) 소재로 많이 사용 되고 있는 LAS(Lithium-Aluminum-Silicate, Li2O-Al2O3-SiO2) 소재를 중금속 흡착제 활용 연구를 진행하였다. LAS는 Li2O-Al2O3-SiO2로 제올라이트(Mx/n((Al2O3)x(SiO2)y)·zH2O)와 유사한 화학식과 성분을 지니고 있다. 사용 후 LAS계 결정화 유리를 중금속 용액 내 흡착제로써 첨가하여 중금속 원소 제거 실험을 수행하였다. Pb, Cd, Cr6+, Hg의 4종 중금속 용액들의 사용 후 LAS를 흡착제로 투입하였으며, 중금속 원소를 제거하기 위하여 첨가한 사용 후 LAS 양, 흡착 시간, 중금속 원소의 농도, pH 등 흡착 반응 조건에 따른 중금속 원소의 함량 변화를 조사하였다.
2. 실 험
2.1. 실험재료
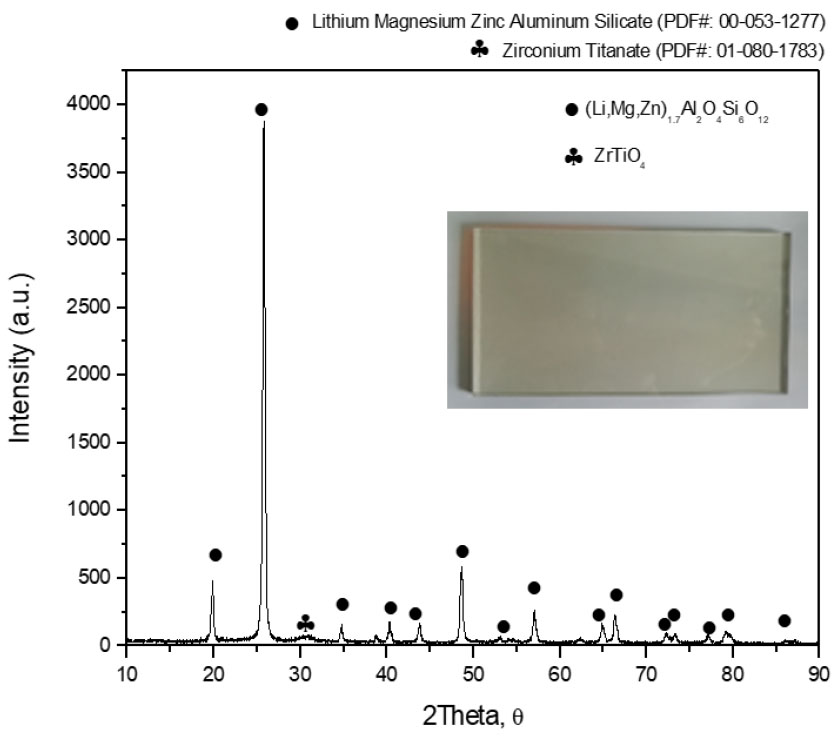
본 연구에서 사용한 LAS(Lithium Aluminum Silicate) 시료는 인덕션 탑플레이트를 파분쇄하여 회수한 분말이다. XRD분석을 통해 LAS는 (Li, Mg, Zn)1.7Al2O4SiO6O12와 ZrTiO4 혼합물로 구성되어 있음을 알 수 있다(Fig. 1). ICP 측정결과를 Table 1에 나타내었으며, LAS 내 유가 금속의 함량만 나타내었다.
Table 1.
ICP Result of LAS Raw Material15)
| Element | Si | Al | Li | Ti | Zr | Zn | Mg | Fe |
| Wt.% | 28.9 | 9.37 | 1.56 | 1.36 | 1.33 | 1.20 | 0.26 | 0.24 |
| Oxide | SiO2 | Al2O3 | Li2O | TiO2 | ZrO2 | ZnO | MgO | Fe2O3 |
| Wt.% | 62 | 17.7 | 3.35 | 2.27 | 1.8 | 1.5 | 0.44 | 0.34 |
또한 사용 후 LAS의 중금속 원소 흡착 특성을 조사하기 위하여 중금속 용액 제조에는 순수제조장치로 제조한 증류수와 중금속 표준 용액을 혼합하여 제조하였다. 사용한 표준 용액은 KANTO사제 검정곡선 작성용 표준 용액으로 계량표준시약 1,000ppm Pb, Cd, Cr6+, Hg 표준 용액을 사용하였다. pH 조절을 위한 시약은 아세트산(순도 99.0%)과 암모니아수(순도 25%)를 사용하였다.
2.2. 실험방법
사용 후 LAS를 이용한 중금속(Pb, Cd, Cr6+, Hg)용액 내 중금속 제거 실험을 진행하였다. 중금속 제거 실험 조건에 따른 사용 후 LAS의 중금속 제거 효율을 비교하기 위하여 사용 후 LAS 첨가양, 반응시간, 초기 중금속 용액 농도, 초기 중금속 용액 pH를 변수로 두어 실험을 진행하였다.
모든 실험에 사용한 중금속 용액은 1,000ppm 농도의 검정곡선 작성용 표준용액을 사용하여 증류수와 혼합하여 제조하였다. 중금속 제거 실험 전 후 중금속 용액의 농도를 유도 결합 플라즈마 발광 분석기(ICP-OES)로 측정하였으며, 이 측정값을 바탕으로 중금속 제거 효율을 계산하였다.
본 실험에서는 동일한 온도의 조건에서 사용 후 LAS의 중금속 흡착능만을 비교하는 목적으로 다음 식에 따라 실험 전 후 용액 내 중금속 농도를 측정하여 중금속 제거 효율을 계산하였다.
Ci는 초기농도(ppm), Cf는 흡착 실험 후 용액 농도(ppm)이다. 이 식을 통하여 중금속 제거 효율을 계산하였다.
3. 결과 및 고찰
3.1. 사용 후 LAS 첨가양의 변화에 대한 영향
사용 후 LAS 첨가양에 따른 변화를 확인하기 위하여 1, 2, 3, 4, 5g 조건으로 중금속 용액에 첨가하였다. 중금속 용액은 농도 1,000ppm Pb, Cd, Cr6+, Hg 표준 용액과 증류수를 혼합하여 농도 100ppm 용액을 제조하였다. 사용 후 LAS와 제조한 농도 100ppm 중금속 용액 50ml를 비커에 넣은 후 300rpm 속도로 30분간 교반하였다. 실험 전 후 중금속 용액의 농도를 ICP-OES로 측정하였으며, 식 (1)을 사용하여 중금속 제거 효율을 계산하였다. 실험 후 중금속 용액 농도와 계산된 중금속 제거 효율은 Table 2에 나타내었다.
Table 2.
The heavy metal content and removal efficiency in the solution after the experiment according to the amount of zeolite added
실험 결과 흡착제로 첨가한 사용 후 LAS의 양이 증가할수록 실험 후 측정된 중금속 농도가 감소하였다. Pb의 경우 2g 조건과 5g 조건이 0.08%만 차이가 있었다. Cd의 경우 2g 첨가 조건부터 41% 이상의 제거 효율을 나타냈다. Cr6+은 2g 첨가 조건부터 제거 효율이 확연히 올랐으며 제거 실험에는 최소 2g이 필요한 것으로 보였다. Hg의 경우 첨가량에 따른 변화를 확인하기 어려웠다. 이 결과들을 통해 최소한의 흡착제를 사용하여 중금속 제거 성능이 발휘된 2g 조건을 실험조건으로 선택하여 다른 흡착 조건에 따른 중금속 제거 실험을 진행하였다.
3.2. 교반 시간에 대한 영향
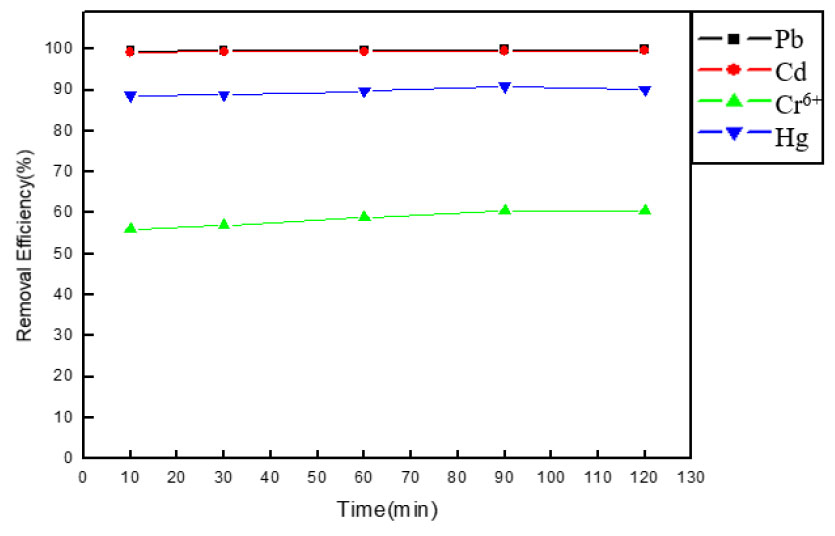
사용 후 LAS의 중금속 제거에 미치는 교반시간의 영향을 조사하기 위한 실험을 진행하였다. 시간은 10, 30, 60, 90, 120분으로 설정하여 진행하였으며, 이전과 동일하게 제조한 농도 100ppm 중금속 용액을 사용하였다. 사용 후 LAS 2g과 제조한 농도 100ppm 중금속 용액 50ml를 비커에 넣은 후 300rpm 속도로 교반하였다. 실험 전 후 중금속 용액의 농도를 ICP-OES로 측정하였으며, 식 (1)을 사용하여 중금속 제거 효율을 계산하였다. 실험 후 중금속 용액 농도와 계산된 중금속 제거 효율은 Table 3과 Fig. 2에 나타내었다.
Pb의 경우 Fig. 2에 나타낸 것처럼 제거 효율이 99.3%로 매우 높았다. Pb를 제외한 나머지 중금속 원소들의 제거 효율은 교반 시간에 따라 증가하였으나, 충분히 제거되지는 못하였다. 또한 흡착제거 효율은 동일조건에서 Pb> Cd> Cr6+≥ Hg 순으로 나타났다.
Table 3.
The heavy metal content and removal efficiency in the solution after the experiment according to Stirring time
제올라이트, 활성탄과 같은 흡착제의 흡착은 3단계로 진행된다. 첫 번째 단계는 이동과 확산에 의해 유기물질이 물을 통해 고액 경계면까지 이동하며, 두 번째 단계는 유기물질이 흡착제의 공극을 통해 분산되는 단계이며, 마지막으로는 확산된 유기물질이 입자의 미세 공극의 표면 위에 흡착되는 단계이다. 흡착이 가능한 표면적은 입자의 외부 표면과 더불어 공극 표면도 포함되어 실제로 공극 표면적이 입자의 표면적보다 훨씬 크고, 대부분의 흡착은 공극 표면에서 발생한다. 또한 내부 공동(Cavity)의 크기, 결정구조, 성분, 표면 특성 등 다양한 조건에 따라서 흡착 특성이 달라진다. 흡착제의 이온 흡착은 흡착제 표면에 이온이 부착 가능한 활성점에 이온들이 급격한 속도로 부착이 된다. 그 후 내부의 공동으로 천천히 확산해가다 평형에 도달하여 더 이상 흡착 성능을 나타내지 못하게 된다.
실험에 사용한 사용 후 LAS의 경우 Pb는 초기 표면 흡착 특성에서 대부분 흡착이 되어 99%이상의 제거 효율을 보인 것으로 사료된다. Cr6+과 Hg은 사용한 LAS와 흡착 특성이 좋지 않다는 연구 결과가 있고 그와 유사하게 나타났다12,13). Cd의 제거 실험 결과 반응시간 증가에 따라 중금속 제거 효율이 선형적으로 상승함이 확인되었다. Cd의 흡착은 표면 흡착 과정만으로 바로 제거가 어렵고 LAS 내부까지 충분히 확산될 시간이 필요한 것으로 생각된다.
3.3. 초기 중금속 농도의 영향
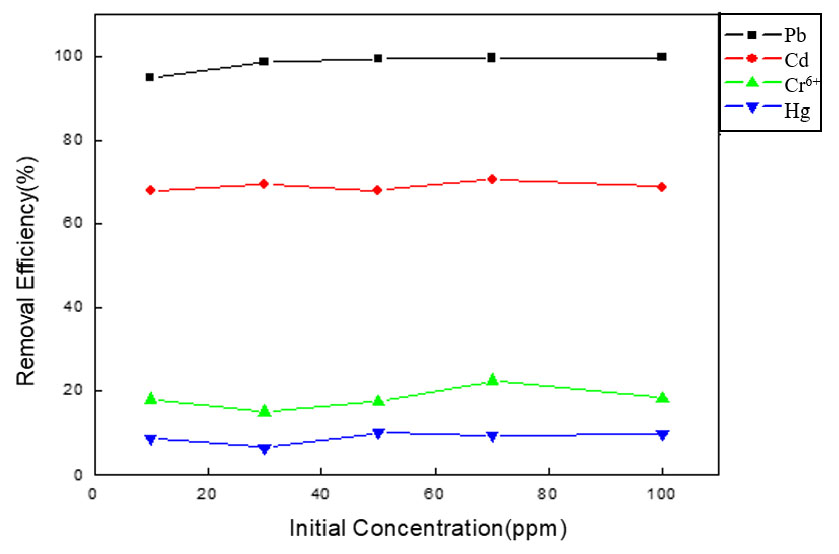
사용 후 LAS의 중금속 제거에 미치는 초기 중금속 용액 농도의 영향을 조사하기 위한 실험을 진행하였다. 농도 조건은 10, 30, 50, 70, 100ppm으로 진행하였으며, 농도 1,000ppm 중금속 표준용액과 증류수를 혼합하여 제조하였다. 제조한 중금속 용액 50ml와 사용 후 LAS 2g을 혼합하여 300rpm 속도로 30분간 교반하였다. 실험 전 후 중금속 용액의 농도를 ICP-OES로 측정하였으며, 식 (1)을 사용하여 중금속 제거 효율을 계산하였다. 실험 후 중금속 용액 농도와 계산된 중금속 제거 효율은 Table 4와 Fig. 3에 나타내었다.
실험 결과 Pb를 제외한 중금속 원소의 제거 효율에는 초기 용액 농도가 크게 영향을 미치지 않았다. Cd의 경우도 반응시간 실험 결과와 달리 중금속 제거 효율이 감소되었다. Pb는 초기 중금속 농도가 증가할수록 점차 중금속 제거 효율이 향상되었는데, 반응시간 실험 결과에서 보다시피 사용 후 LAS의 Pb 제거 매커니즘은 대다수가 표면 흡착으로 작용하는 결과로 사료된다.
Table 4.
The heavy metal content and removal efficiency in the solution after the experiment according to initial heavy metal concentration
3.4. pH 변화에 대한 영향
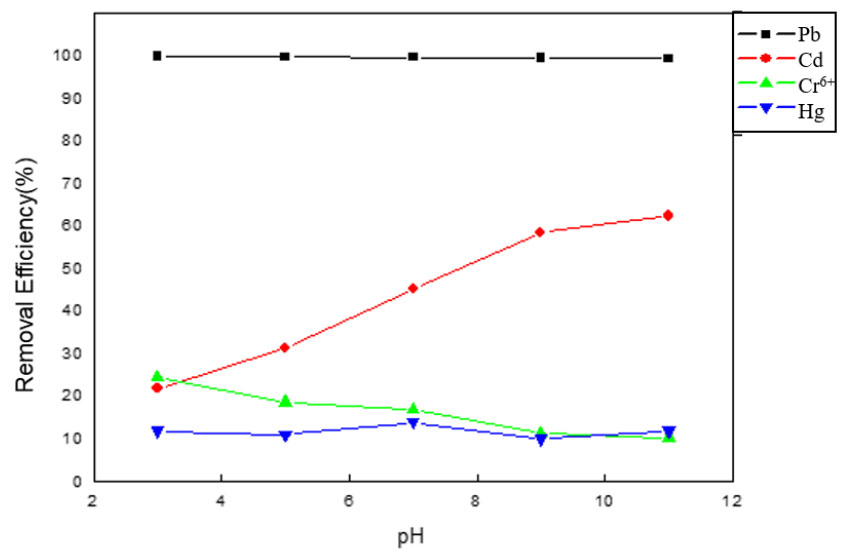
사용 후 LAS의 중금속 제거에 미치는 초기 중금속 용액의 pH의 영향을 조사하기 위한 실험을 진행하였다. 이전과 동일하게 제조한 농도 100ppm의 중금속 용액 50ml와 사용 후 LAS 2g을 혼합하여 300rpm 속도로 30분간 교반하였다. 실험 전 후 용액의 농도를 ICP-OES로 측정하였으며, 식 (1)을 사용해 중금속 제거 효율을 계산하였다. 실험 후 중금속 용액 농도와 계산된 중금속 제거 효율은 Table 5과 Fig. 4에 나타내었다.
중금속 용액의 pH 조절은 사용 후 LAS와 상변화를 일으키지 않는 아세트산과 암모니아수를 사용하였다. 증류수와 혼합하여 1M 용액을 pH조절에 사용하였으며, pH는 3, 5, 7, 9 11 5가지 조건에서 중금속 제거 실험을 진행하였다. 또한 사용 후 LAS를 증류수와 혼합하였을 때 pH 변화 유무를 확인하였으며, 확인 결과 pH는 7~7.2로 중성을 유지하였다.
Table 5와 Fig. 4에 나타낸 것처럼 pH 증가에 따라 Pb, Cr6+의 제거 효율이 감소하였으며, Cd의 경우에는 중금속 제거 효율이 증가하였다. Hg의 경우 pH 변화가 중금속 제거 효율에 큰 영향을 주지 못하였다.
Table 5.
The heavy metal content and removal efficiency in the solution after the experiment according to initial heavy metal concentration
일반적인 제올라이트, 활성탄, 흡착제 등은 낮은 pH에서는 금속 원소의 흡착량이 감소한다는 경향을 보인다는 보고가 있다16). 이는 금속의 흡착 대신 흡착제와 수소이온이 결합하려 하는 경향을 보이고 이러한 경쟁으로 인해 흡착률이 감소하게 된다. 또한 용액의 pH가 증가하면 제올라이트와 같은 광물성 물질의 표면은 음전하를 증가시키게 한다. 이러한 탈수소화반응은 표면의 음전하를 증가시켜 원소가 흡착될 수 있는 활성점들로 작용하고 중금속 화학종의 흡착 반응을 증진시킨다.
하지만 실험결과 Pb, Cr6+의 경우 pH 증가에 따라서 중금속 제거 효율이 감소함이 확인되었다. 용액의 pH 제어에 사용한 암모니아수가 중금속 이온 대신 LAS에 흡착되어 중금속 제거 효율이 감소한 것으로 보인다.
Cd의 경우 pH가 증가할수록 중금속 제거 효율이 선형적으로 상승함이 확인되었다. Cd의 중금속 흡착 실험 후 회수한 LAS 물질의 양이 기존의 2g보다 증가함이 확인되었는데, pH 증가에 의해 수산화물이나 고상 침전물 등이 형성되어 중금속 제거 효율이 향상된 것으로 보인다.
4. 결 론
본 연구에서는 인덕션 탑플레이트 소재로 사용되는 LAS계 결정화 유리를 활용하여 중금속 용액 내 중금속 제거 실험을 진행하였다. 중금속 제거 실험 조건에 따른 중금속 제거 효율을 비교하였다.
1) 사용 후 LAS 첨가량에 따른 중금속 제거 실험 결과 첨가량 증가에 따라서 중금속 제거 효율이 상승함을 확인하였다.
2) 교반시간 증가에 따라 중금속 제거 효율이 향상됨을 확인하였다. 특히 Cd의 경우 10분 교반시 22.04%의 제거 효율에서 120분 교반시 72.01%로 49.97% 향상되었다.
3) 초기 중금속 농도는 LAS의 중금속 제거 성능에 큰 영향을 미치지 못하였다.
4) pH 변화에 따라 LAS의 중금속 제거 실험 결과 Cd의 경우 pH 증가에 따라 제거 효율이 증가하였다. Pb, Cr6+의 경우 제거 효율이 감소하였으며, Hg의 제거에는 pH가 큰 영향을 미치지 않았다.
5) 사용 후 LAS의 중금속 제거 성능 확인 결과 대부분의 조건에서 90% 이상의 Pb 제거 효율이 확인되었으며 효과적인 Pb 제거제로 사용이 가능하다.