1. 서 론
2. 타이타늄의 생산량과 제조법 개요
3. 스펀지 타이타늄의 제조
3.1. 일메나이트의 고품위화
3.2. TiCl4의 제조와 고순도화
3.3. 환원과 분리 공정
3.4. MgCl2의 전해환원
4. 스펀지 Ti의 파쇄와 잉곳 제조
5. 종 합
1. 서 론
타이타늄(Ti, titanium)의 지각 중 존재도(Abundance of elements in Earth’s crust)는 9위(0.57 %)이며, 구조용 금속으로는 알루미늄(8.23 %), 철(5.63 %), 마그네슘(2.33 %)에 이어서 네 번째로 풍부한 원소이다1). Ti은 비중이 4.5 g/cm3으로 철의 60 % 정도이지만 비강도가 높아 항공, 국방 등 고강도와 경량성을 요구하는 첨단산업의 핵심소재로 사용되고 있다. 또 해수 중에서는 스테인리스강보다 우수한 내식성을 가지고 있어서 해수 담수화 설비나 화학 장치 등에 사용되고 있다. 그리고 인체에 대한 금속 알러지 등이 없는 등 생체 적합성이 매우 우수하여 인공관절, 임플란트 등에 이용되고 있다. 그러나 금속소재로의 제련이 어려워 희소금속(rare metals)으로 분류되고 있다. Table 1에는 이러한 Ti의 물리ㆍ화학적 성질을 나타내었다.
Table 1.
Physico-chemical properties of titanium
Ti을 함유하는 광석에는 루타일(rutile, 95~100 % TiO2), 일메나이트(ilmenite, FeTiO3, 52.7 % TiO2), 류코신(Leucoxene, 67.3 % TiO2)이 있으나2), 경제적인 가치가 있는 것은 루타일과 일메나이트이다. 특히 일메나이트는 매장량이 가장 풍부한 원료이며, 영국의 광물학자인 그리거(William Gregor)가 1791년에 발견하여 Manaccanite로 명명하면서부터 알려지게 되었다. 그 후 1795년에 독일의 화학자인 M. H. Klaproth가 루타일을 발견하여 그중에 함유된 금속원소를 타이타늄으로 명명하였다3). 금속 Ti은 고온에서 매우 활성인 금속으로, Ti과 반응하지 않는 것은 Na, Mg, Ca 등 알칼리 금속, 알칼리토류 금속의 일부이며, Ti 중으로 용해되지 않는 것은 F, Cl 등의 할로겐 원소뿐이다. 특히 C, O, N에 대해서는 매우 강한 화학적 친화성이 있어서 큰 용해도를 가지고 있다4). 이러한 Ti은 1909년 Hunter 박사가 TiCl4를 Na으로 환원하여 사용되기 시작하였다5). 그리고 1937년에 Kroll 박사가 TiCl4를 Mg으로 환원하여 금속 Ti을 제조하였으며6,7), 1947년에 DuPont사에서 상업생산을 시작하면서 Ti의 시대가 열리게 되었다8).
Ti의 공업적 제조방법은 Hunter법과 Kroll법이 병존하였으나, 1992년에 영국 RMI(Reactive Metals Inc.)의 Hunter법 Ti 공장이 폐쇄되면서 현재 시판되는 Ti은 Kroll법에 의해서만 제조되고 있다. Kroll법은 TiCl4의 환원과 MgCl2의 분리를 위한 비용이 많이 들고 시간이 많이 걸리는 회분식 조업이라는 문제점을 가지고 있다. 특히 Kroll법으로 10 ton batch의 스펀지 Ti을 생산할 때, 환원, 증류, 냉각에 각각 4일 정도가 소요되고, 환원공정에서 부득이하게 Fe 등의 불순물 함유량이 높은 부분이 스크랩으로 처리되어 Ti이 다른 금속에 비하여 코스트 경쟁력이 낮은 이유 중의 하나이다. 따라서 이러한 문제점을 해결할 수 있는 새로운 Ti의 제련기술에 관하여 많은 연구들이 수행되고 있다2,9).
한편 타이타늄의 새로운 제련법이나 리사이클링 기술을 개발하기 위해서는 기존의 타이타늄 제조기술에 대한 검토와 이해가 필요하다. 따라서 본 논문에서는 Kroll법에 의한 Ti 제조기술에 대해 고찰하였다.
2. 타이타늄의 생산량과 제조법 개요
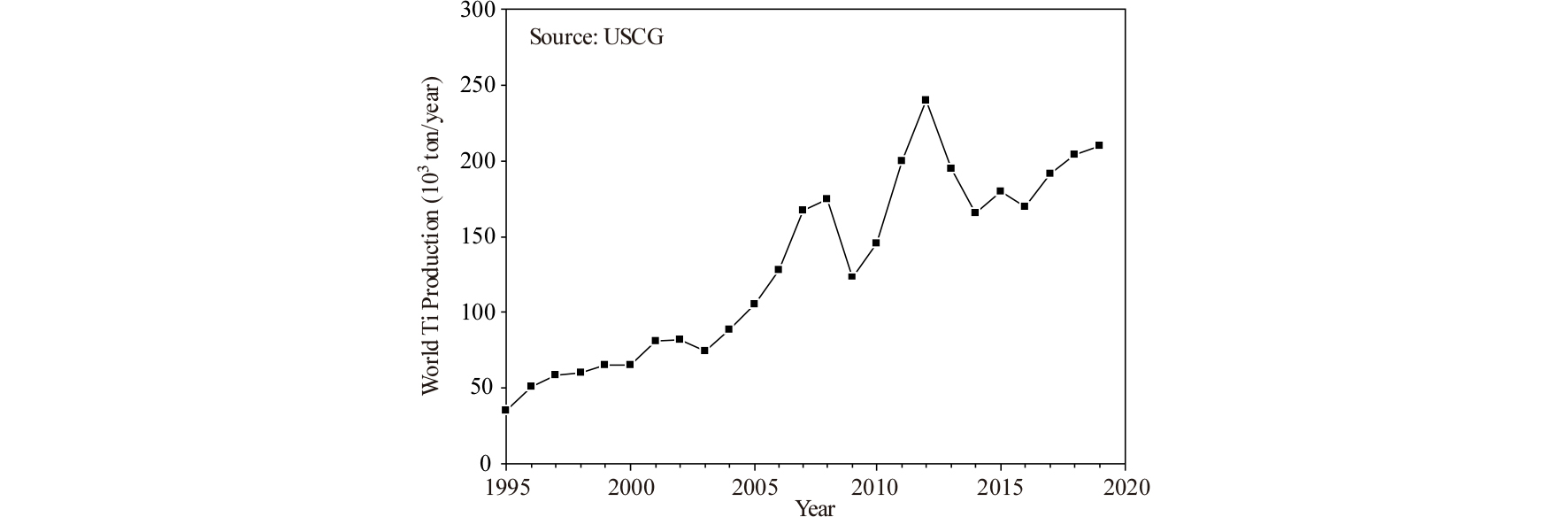
Fig. 1에는 1995년부터 스펀지 Ti의 생산량 변화를 나타내었다. 1947년에 미국에서 최초로 1톤의 스펀지 Ti을 공업적으로 제조한 후에 1990년대 초반까지의 생산량은 5만 톤을 넘지 못하였다. 중국이 2000년대에 들어 본격적으로 Ti을 생산하기 시작하면서 스펀지 Ti의 생산량은 비약적으로 증가하기 시작하였으며, 2019년에는 약 21만 톤의 스펀지 Ti이 생산되었다. 전세계 스펀지 Ti의 약 37 %는 중국에서 생산되고 있으며, 이어서 일본이 약 25 %를 생산하고 있다. 나머지는 러시아, 카자흐스탄, 미국, 우크라이나에서 생산되고 있다. 우리나라는 스펀지 Ti을 생산하지 않지만, 세계 7위의 Ti 소비국이다.
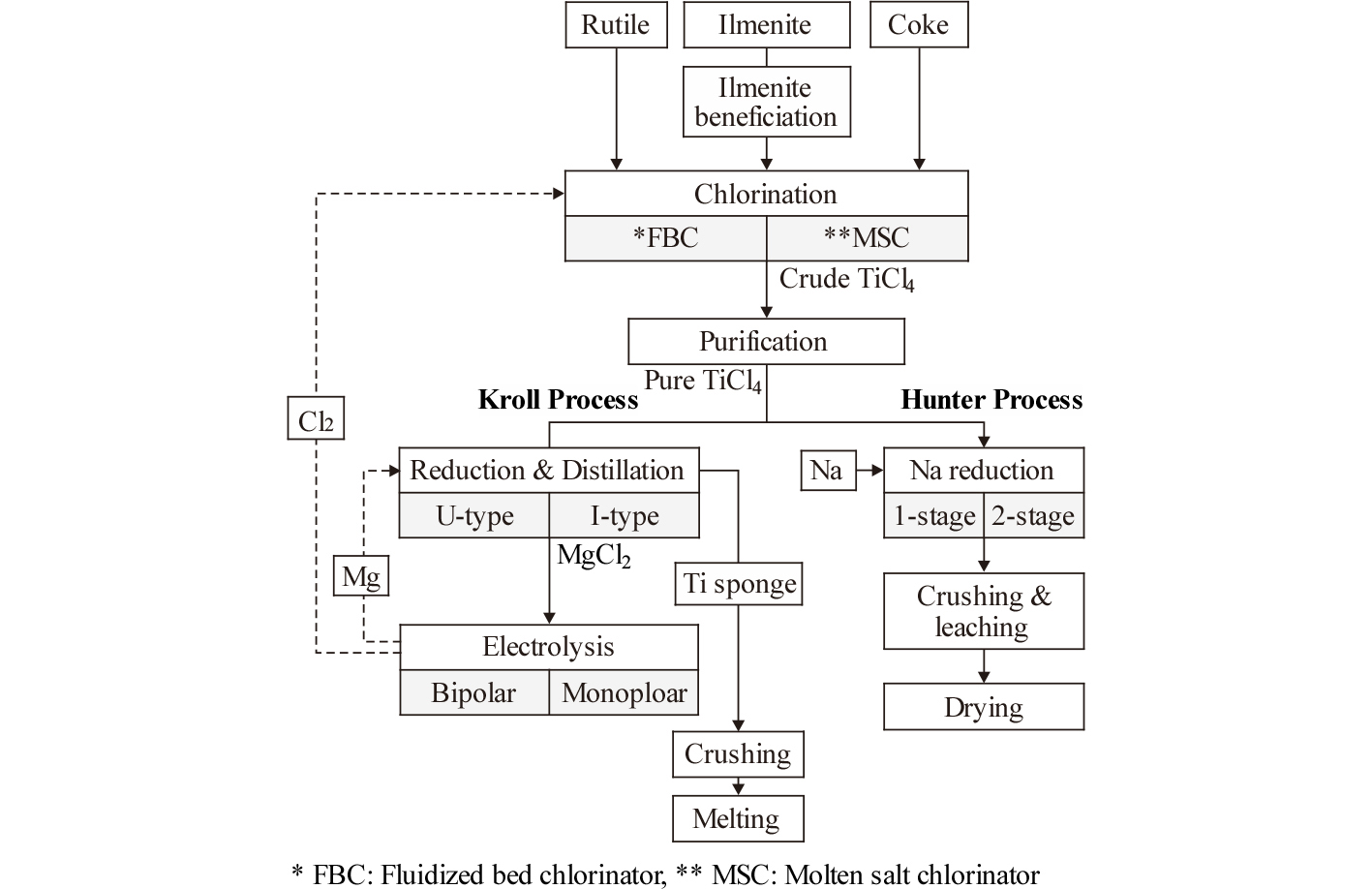
Fig. 2에는 Kroll법과 Hunter법에 의한 Ti 생산공정의 대략을 비교하여 나타내었다. 원료에는 루타일과 일메나이트가 있으며, 일메나이트는 염화공정에 앞서 불순물인 Fe를 제거하여 합성루타일(synthetic rutile, up graded ilmenite, TiO2 90~96 %)로 만든다. 이후에 유동층법(fluidized bed chlorinator)이나 용융염법(molten salt chlorinator)에서 TiCl4를 제조한 후에 정제를 거쳐서 환원공정으로 보낸다. 환원공정은 Na을 환원제로 사용하는 Hunter법과 Mg을 환원제로 사용하는 Kroll법이 있으나, 현재는 대부분 Kroll법으로 대체되었다. 그리고 환원 후에 미반응한 Mg과 반응 생성물인 MgCl2를 증류ㆍ제거하는 방법에 따라 역U-type과 I-type이 있다. 반응 생성물인 MgCl2는 용융염 전해공정에서 Mg과 Cl2를 재생하여 각각 환원공정과 염화공정으로 보낸다. MgCl2의 용융염 전해 공정에는 복극형(bipolar)과 단극형(monopolar)이 있다. 환원ㆍ분리한 스펀지 Ti은 불순물 농도가 높은 외각부를 제거한 후에 일정한 크기로 파쇄한다. 그리고 2차에 걸친 진공용해에 의해 잉곳으로 만들고 있다.
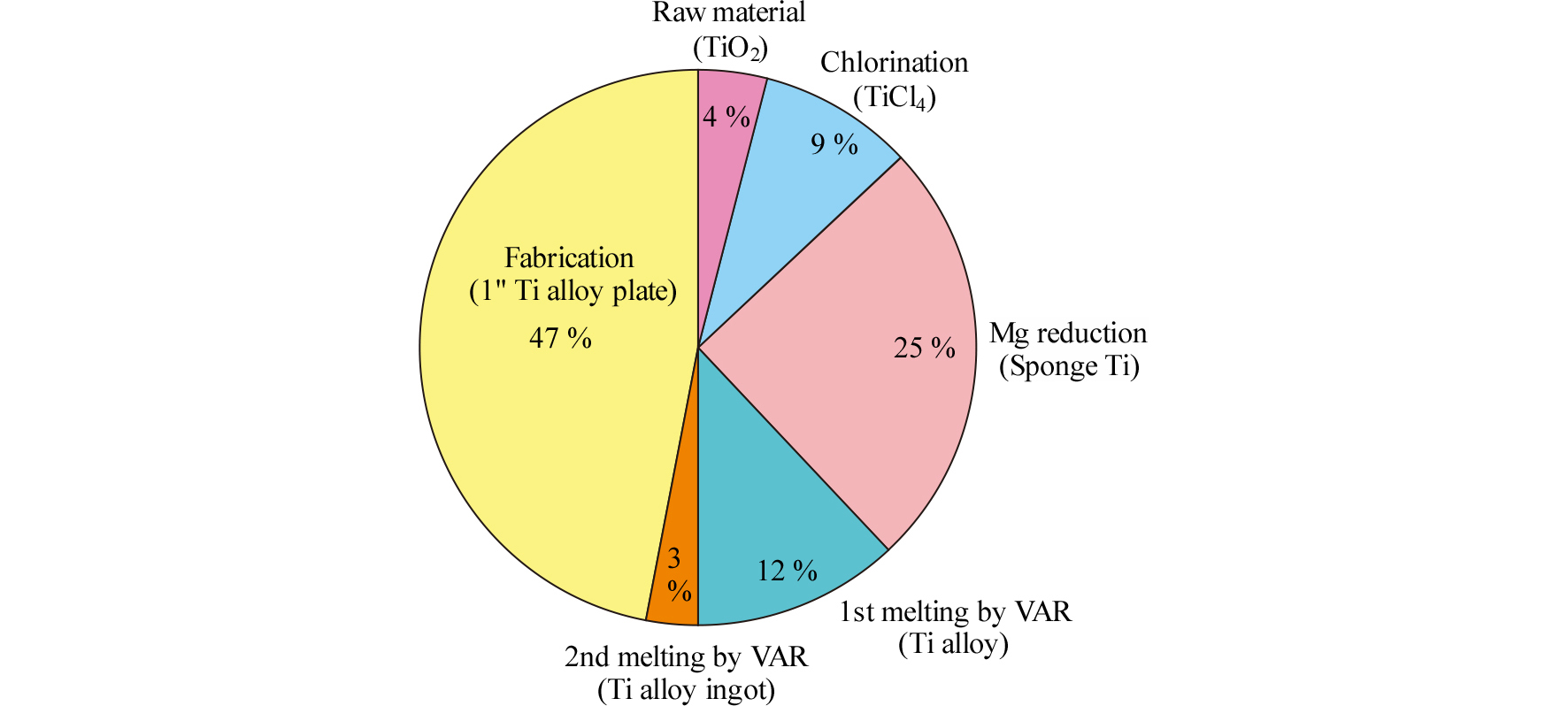
Fig. 3에는 1 inch 두께의 Ti 판재 제조비용의 비율을 나타내었다9). 그림에서와 같이 Kroll법에서는 원료비와 TiCl4 제조비용에 비해 TiCl4에서 스펀지 Ti을 얻는 비용의 비율이 높은 편이다. 또 스펀지 Ti의 용해와 잉곳으로부터 판재로 가공하는 비용의 비율도 높은 편이므로, Ti의 보급을 활성화하기 위해서는 이러한 제조 비용의 절감이 중요하다. 따라서 이하에 Kroll법을 중심으로 Hunter법을 포함하여 원료부터 잉곳 제조까지 각각의 공정에 대해 고찰하였다.
3. 스펀지 타이타늄의 제조
3.1. 일메나이트의 고품위화
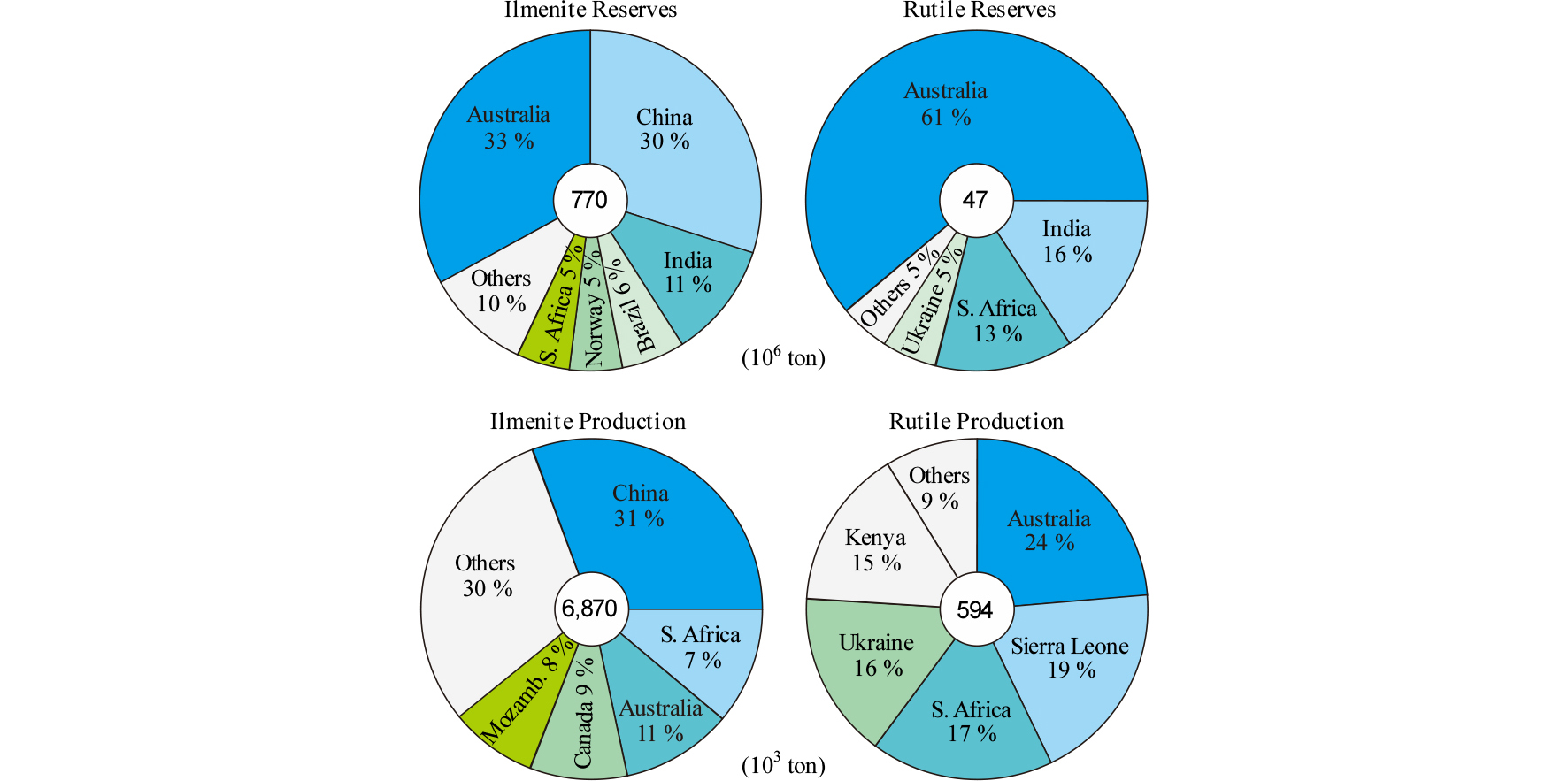
Ti을 함유하는 광석 중 경제적인 가치가 있는 것은 루타일과 일메나이트이며, Fig. 4에 2018년도의 일메나이트와 루타일의 TiO2 함량 기준의 국가별 매장량과 생산량 비율을 나타내었다10). Ti 광석의 약 92 %가 일메나이트로부터 공급되므로 일메나이트 중 Fe를 제거하여 천연 루타일에 버금가는 고품위의 합성 루타일을 제조하는 방법이 중요하게 되었다.
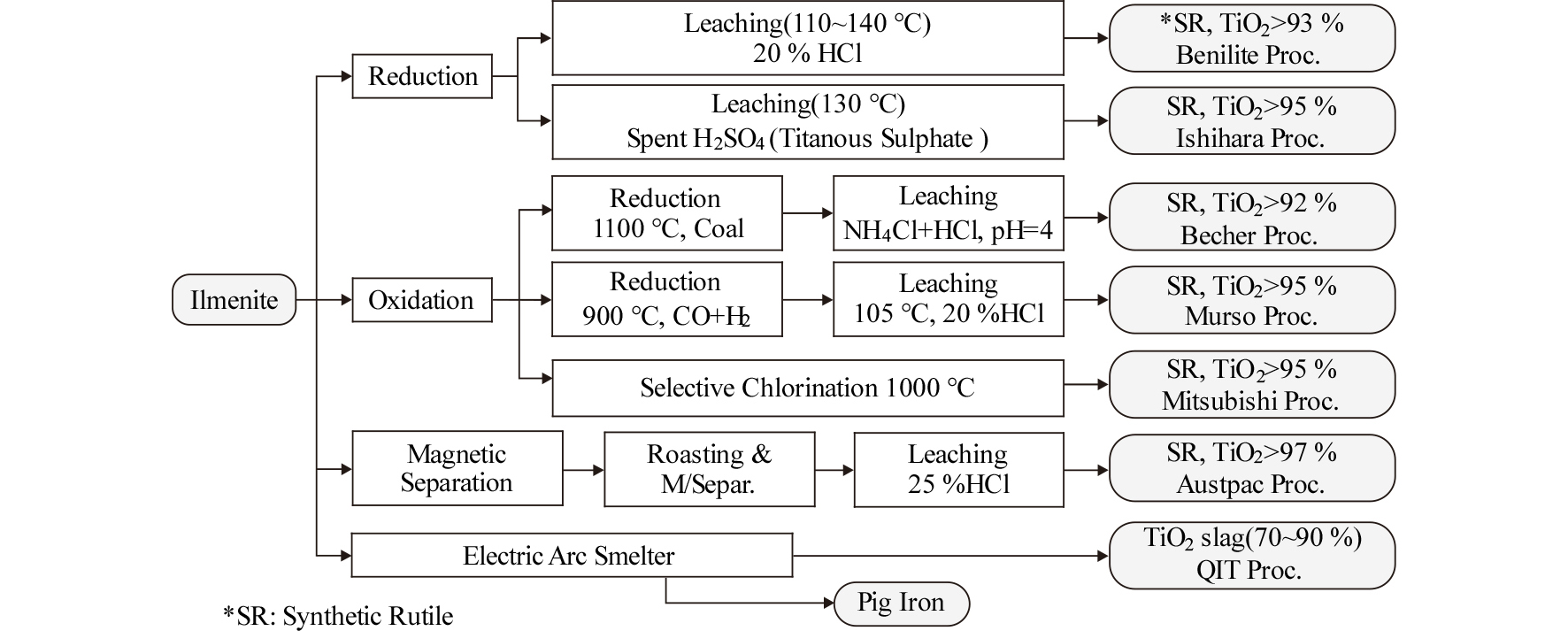
Fig. 5에는 금속 Ti이나 TiO2를 제조하기 위한 원료가 되는 일메나이트의 고품위화 방법을 정리하여 나타내었다11). 합성 루타일을 제조하는 방법은 원료인 일메나이트의 조성이나 지역적 특성, 최종목적 등에 따라 여러 가지 방법이 있다. 이러한 일메나이트의 고품위화법에는 일메나이트를 전기로 등에서 정련하여 선철을 생산하면서 TiO2 농도가 높은 슬래그를 만드는 방법, 일메나이트 중의 Fe나 기타 불순물을 제거하기 위한 산 침출법, 일메나이트 중의 산화철을 부분 환원하거나 완전히 환원한 후에 물리적 선별이나 화학적 처리를 하는 방법, 그리고 선택적 염화에 의해 Fe만 제거하는 방법 등이 있다12).
3.2. TiCl4의 제조와 고순도화
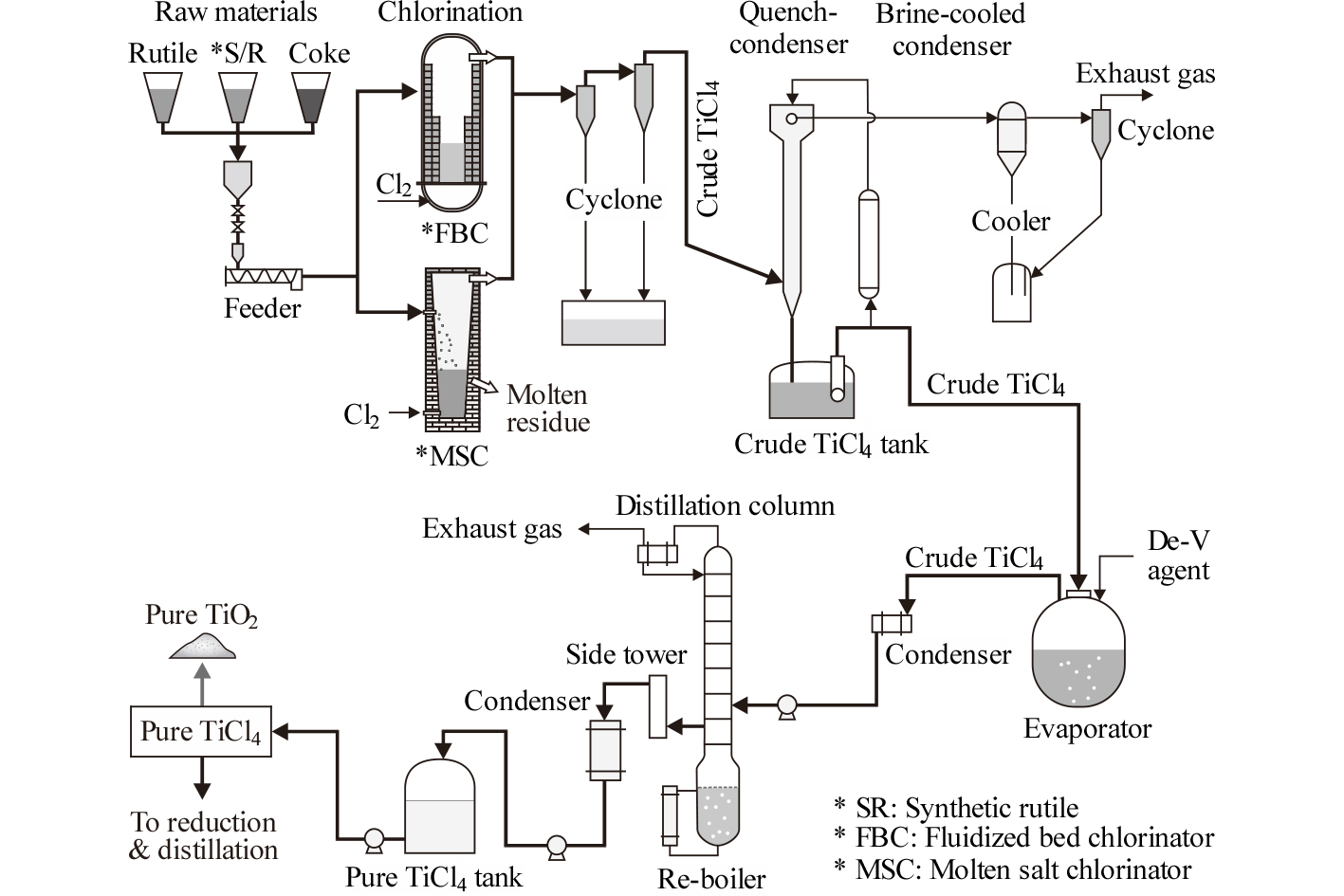
Ti원(천연 루타일, 합성 루타일, 고Ti 슬래그 등)과 코크스, 염소가스를 이용하여 TiCl4를 만드는 공정에는 유동층 염화법과 용융염 염화법이 있으며, Table 2에는 각국에서 사용하는 염화법을 종합하여 나타내었다13). Fig. 6에는 OTC(Osaka Titanium Technologies Co.)의 유동층 염화공정을14) 기반으로 두 공정을 재구성하여 나타내었다. 두 공정은 염소가스를 취입하는 방법만 다를 뿐 기본적인 반응식은 동일하며, TiO2 자체의 염화반응은 다음식과 같다.
Table 2.
Chlorination technology in different country13)
| $$\begin{array}{l}{\mathrm{TiO}}_2+2{\mathrm{Cl}}_2={\mathrm{TiCl}}_4+{\mathrm O}_2,\\\mathit\triangle G^0=174,450-53.73T\;(\mathrm J/\mathrm{mol})\end{array}$$ | (1) |
이 반응은 2,973 °C 이상이 되어야 가 음의 값이 되므로 공업적인 온도에서는 염화되지 않는다. 그러나 식 (2)와 같이 TiO2 중의 산소를 제거하기 위해 탄소와 함께 반응시키면 가 항상 음의 값이므로 TiCl4가 만들어 진다15).
| $$\begin{array}{l}\frac12{\mathrm{TiO}}_2+\mathrm C+{\mathrm{Cl}}_2=\frac12{\mathrm{TiCl}}_4+\mathrm{CO},\\\mathit\triangle G^0=-23,695-115.87T\;(\mathrm J/\mathrm{mol})\end{array}$$ | (2) |
TiCl4의 끓는점은 136 °C이며, 비중은 1.726 g/cm3으로 무색투명한 액체이지만, 염화공정에서 생성된 TiCl4의 순도는 약 98 % 정도이며 흑갈색을 띤다. 노 내가 약 1,000 °C이므로 생성된 TiCl4는 기체로 되어 있다. 염화로 후단에는 건식제진, 순환액에 의한 냉각ㆍ액화, 광물유에 의한 탈V, 증발, 다단 증류탑에 의한 정제를 거쳐서 99.98 % 이상의 순도를 갖는 TiCl4가 얻어지며, 5N까지 만들고 있는 것으로 알려져 있다16).
용융염 염화법은 1960년대에 구소련에서 개발된 것으로 Table 2에 나타낸 바와 같이 러시아나 중국에서 많이 사용하고 있다. 특히 Ti 슬래그 중에 CaO, MgO 등의 불순물이 많은 경우에 사용하고 있으며, 일부 Ti 원광에 CaO와 MgO가 6~9 % 정도 함유되어 있으면 Ti 슬래그 제조 공정에서 완전히 제거하는 것이 곤란하여 용융염 염화법을 사용하고 있다17). 용융염 염화법은 분쇄한 Ti 슬래그와 코크스를 용융염(KCl 72~76 %, NaCl 16 %, MgCl2 4~6%, CaCl2) 상부에 공급하고 염소가스를 용융염 중에 취입하여 TiCl4로 염화시킨다. Ti의 실수율은 약 96 % 정도이며, 120~150 t/d-TiCl4가 생산되고 있다. 다만 약 250 kg/t-crude-TiCl4 정도의 폐 용융염이 발생하는 문제점을 가지고 있으나13), 불순물 농도가 높은 Ti 원료의 염화법으로는 적합한 것으로 생각된다.
유동층 염화법은 미국에서 개발되어 현재 미국, 일본, 중국 등에서 사용하고 있는 방법이다. 유동층 염화법이 개발되기 전에는 Ti 원료와 코크스를 점결제인 피치(pitch)를 사용하여 단광(briquette)으로 만들어 염화반응에 공급하였으나, 생산성이 낮고 실수율도 낮아 유동층 염화법으로 대체되었다. 유동층 염화법에서는 Ti 원료를 환원제와 함께 분체 상태로 유동로에 장입하고, 하부로부터 Cl2를 취입하여 약 900 °C에서 반응시키면 TiCl4가 증발하여 나오므로 냉각하여 응축시킨다. 뒤이어 증류탑을 이용하여 고순도 TiCl4를 만들어 환원공정에 공급하고 있다. 유동층 염화법은 TiCl4를 만드는 가장 성숙된 기술이지만, 원료의 크기분포와 CaO+MgO 함유량에 제한이 있다13). 특히 CaO+MgO가 높은 Ti 원료를 사용할 수 없는 문제점을 가지고 있다. 일반적으로 유동층 염화법의 Ti 원료는 TiO2>95 %, CaO+MgO<0.5 %인 것을 사용하는 것이 바람직하다.
한편 TiCl4 중의 불순물은 환원반응에서 전부 금속 Ti 중으로 흡수되므로, 금속 Ti을 제조하기 위해서는 99.98 % 이상의 고순도 TiCl4가 필요하다. Table 3에는 염화공정에서 발생하는 금속 염화물의 상변태점을 끓는점(승화점) 순서로 나타내었다. FeCl2, MnCl2, CrCl3, CrCl2, MgCl2, CaCl2, 등의 끓는점(승화점)은 TiCl4보다 월등히 높으므로 염화 반응로의 온도가 약 1,000 °C 이하가 되면 액상으로 남아 용융염 반응로 등의 슬래그가 된다. VOCl3, SiCl4, AlCl3, FeCl3의 경우 끓는점이 낮으므로 TiCl4의 주요한 불순물이 되며, 증류탑이나 약품처리에 의해 제거한다.
Table 3.
Phase transition temperature of metal chlorides
3.3. 환원과 분리 공정
Ti의 제조방법에는 Hunter법과 Kroll법이 공존하였으나, 현재는 대부분 Kroll법만 적용하고 있다. 미국의 HEM(Honeywell Electronic Materials)에서 자체 소비를 위해 소량의 전자재료용 Ti만 Hunter법의 1단법으로 생산하고 있는 것으로 알려져 있다18). 그리고 아직 상용화 단계에 이르지는 못하였으나, Hunter법을 개량한 Amstrong법이 개발되어 있다20).
3.3.1. Hunter법
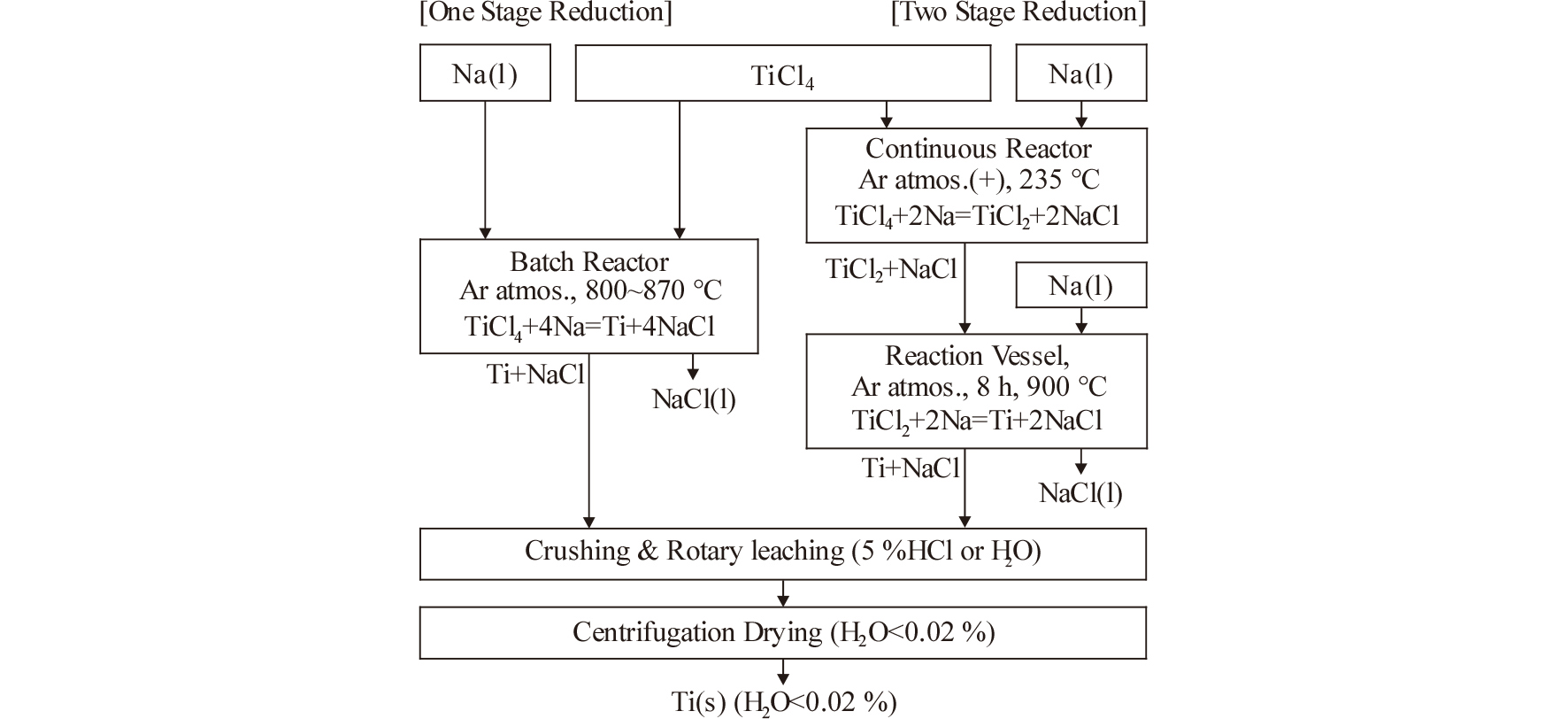
Hunter법에는 식 (3)과 같이 TiCl4와 당량비의 Na을 반응시켜 Ti을 제조하는 1단법과, TiCl4를 당량보다 적은 Na과 반응시켜 저급 염화물(TiCl2)을 만든 후에 다시 Na과 반응시켜 환원시키는 2단법이 있다.
| $${\mathrm{TiCl}}_4(\mathrm l)+4\mathrm{Na}(\mathrm l)=\mathrm{Ti}(\mathrm s)+4\mathrm{NaCl}(\mathrm l)$$ | (3) |
Fig. 7에는 문헌으로부터 정리한 두 방법을 비교하여 나타내었다19). 초기의 Hunter법에서는 1단법으로 환원하였으나, 반응열 때문에 반응조가 고압이 되는 문제점이 있어서 이후에 2단법으로 개선되었다. 특히 1단법에서는 NaCl의 융점인 800 °C와 Na의 끓는점인 877 °C 사이의 좁은 온도범위에서 조업하여야 하는 문제점도 있었다. 그리고 1 mol의 Ti을 얻기 위해서는 4 mol의 NaCl이 생성되므로 반응조가 매우 커야 하는 단점도 있다.
2단법은 우선 다음 식과 같이 TiCl4를 TiCl2로 환원한다.
| $${\mathrm{TiCl}}_4(\mathrm l)+2\mathrm{Na}(\mathrm l)={\mathrm{TiCl}}_2(\mathrm l)+2\mathrm{NaCl}(\mathrm s)$$ | (4) |
이 반응은 120~130 °C의 액상 Na을 압송한 후에, Ar으로 가압한 반응조에서 235 °C의 비교적 저온에서 교반하면서 연속적으로 반응시킨다. 연속적으로 배출되는 TiCl2와 NaCl 혼합물을 2단계의 반응조로 보내어 액상 Na과 반응시키면 다음 식과 같이 금속 Ti과 NaCl이 생성된다.
| $${\mathrm{TiCl}}_2(\mathrm l)+2\mathrm{Na}(\mathrm l)=\mathrm{Ti}(\mathrm s)+2\mathrm{NaCl}(\mathrm l)$$ | (5) |
반응 생성물인 액상의 NaCl은 주기적으로 배출하고, 잔류하는 NaCl과 Ti 혼합물은 분쇄한 후에 순수나 0.5 %HCl로 침출하며, 이어서 원심분리와 진공건조를 거쳐 수분이 0.02 % 이하인 금속 Ti을 얻는다.
Hunter법은 비교적 낮은 온도에서 반응이 일어나므로 반응용기에 의한 오염이 적어 Fe 농도가 매우 낮은 Ti을 얻을 수 있으며, NaCl과의 분리도 용이하고 과잉의 Na이 필요 없는 장점이 있었다. 2000년대에 들어와서 Hunter법을 개선하여 미국의 ITP(International Titanium Powder)에서 기체상의 Na과 TiCl4를 반응시켜 Ti 분말을 얻는 Armstrong법을 제안하였다20).
3.3.2. Kroll법
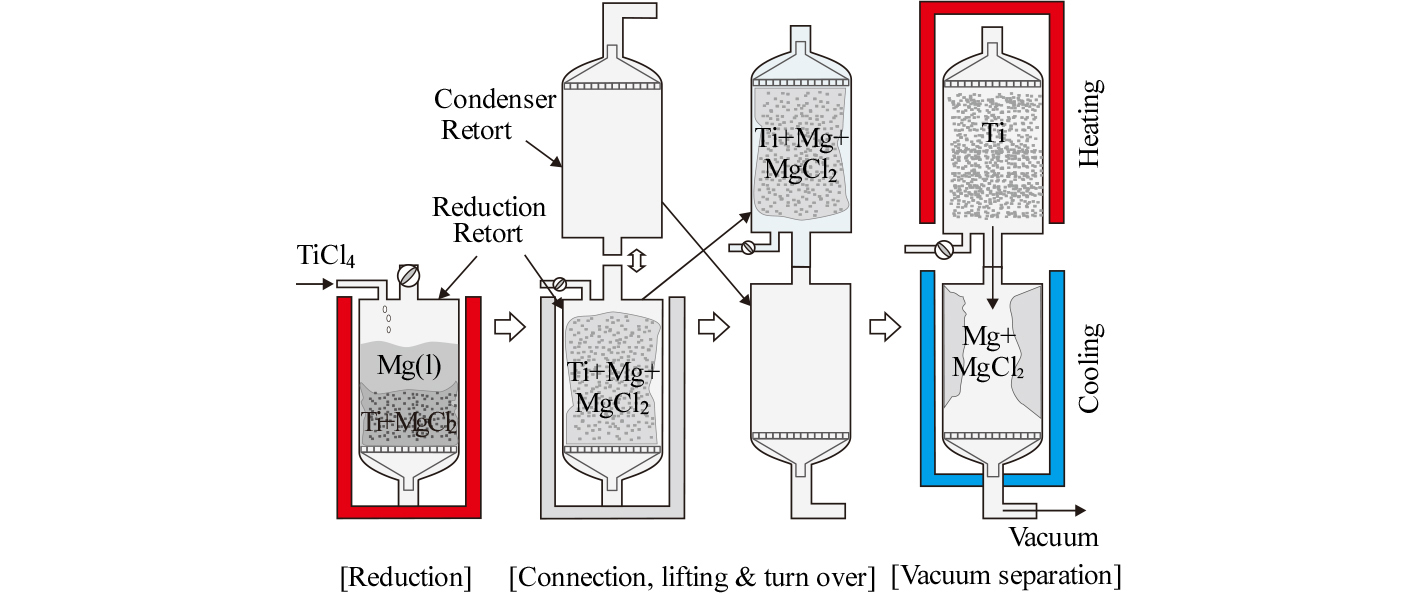
Kroll법에서는 TiCl4와 Mg을 반응시켜 스펀지 Ti을 생성하고, 부산물인 염화마그네슘(MgCl2)과 미반응한 Mg을 증류에 의해 분리한다. 환원반응은 아래와 같이 동일하지만, 환원조와 응축조의 조립형태에 따라 역U자형과 I자형의 두 가지 방식이 사용되고 있다.
| $${\mathrm{TiCl}}_4(\mathrm g)+2\mathrm{Mg}(\mathrm l)=\mathrm{Ti}(\mathrm s)+2{\mathrm{MgCl}}_2(\mathrm l)$$ | (6) |
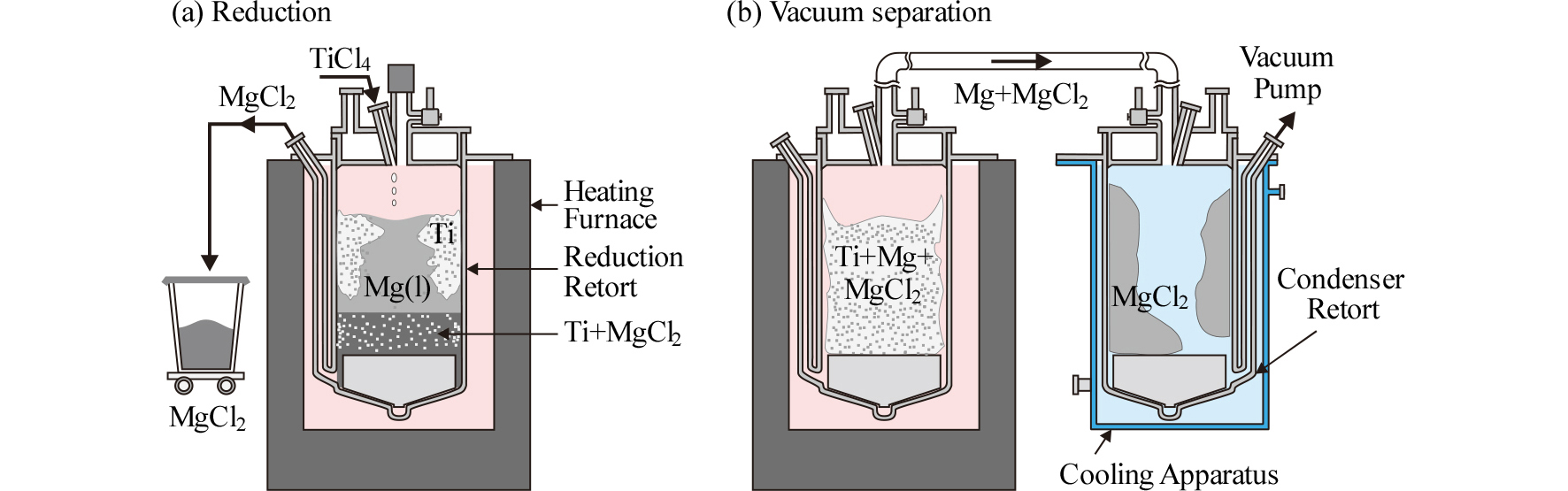
Fig. 8에는 일본 등에서 사용 중인 역U자형 환원ㆍ분리 공정을 모식적으로 나타내었다. 우선 환원조에 용융 Mg을 장입하고 반응기 내부를 Ar 분위기로 만든 후, 액상의 TiCl4를 상부에서 공급하면 식 (6)과 같이 고체 Ti이 생성된다. 반응 부산물인 MgCl2가 밀도 차이에 의해 환원조 바닥으로 침강되면 Ar 가스로 환원조내를 가압하여 배출시킨다. 식 (6)의 반응은 발열반응이므로 반응 중에는 TiCl4의 공급량을 조절하여 약 900 °C로 제어하고 있으며, Ti의 생성속도는 약 60~80 kg/(m2ㆍh)인 것으로 알려져 있다. 실제로 10 ton의 스펀지를 제조할 때 반응개시부터 종료까지 약 90시간이 소요된다14). 그리고 환원조 내에서의 Mg, MgCl2, Ti의 거동에 대해서 많은 연구들이 이루어지고 있으며21,22), 상온에서는 Mg과 MgCl2의 밀도는 각각 1.74 g/cm3와 2.32 g/cm3로 약간의 차이가 있으나, 780 °C에서 Mg과 MgCl2의 밀도는 각각 1.545 g/cm3와 1.667 g/cm3로22) 큰 차이가 없어서 복잡한 거동을 하는 것으로 알려져 있다.
역U자형 환원ㆍ분리 공정에서는 반응 생성물인 MgCl2를 반응 도중에 액체상태에서 흡인하여 전해조로 보내고 있으나, 일부는 미반응한 Mg과 함께 스펀지 Ti 중에 남아 있다. 분리공정에서는 환원 반응이 끝난 후 곧바로 환원조를 약 1,000 °C로 가열하고, 응측조를 냉각하면서 진공배기하면 스펀지 Ti 사이사이에 잔류하는 Mg과 MgCl2가 증발되어 연결관을 통해 응축조로 들어가 내벽에 응측된다. 이러한 분리시간도 10 ton 스펀지의 경우 약 90시간이 소요되는 것으로 알려져 있다14). 가열온도를 올리면 분리시간이 단축되지만, 과도하게 높으면 반응조와 스펀지 Ti이 반응하며, 또 스펀지 Ti의 소결에 의해 밀도가 올라가서 압축성이 떨어지므로 바람직하지 못하다. 스펀지 Ti의 압축성은 Ti 용해에 사용되는 소모 전극식 진공아크 용해(VAR, vacuum arc remelting)에서 스펀지 Ti을 압축성형하여 만드는 소모 전극의 강도에 큰 영향을 미치는 중요한 성질이다. 또 분리공정 시간을 단축하면 스펀지 Ti 중의 Cl 농도가 상승한다. 특히 MgCl2의 증발은 온도와 진공도에 의존하므로 스펀지 Ti 내의 열전달 속도를 일정하게 하기 위해 일정한 시간이 필요하여, 생산성 향상에는 한계가 있어서 환원ㆍ분리로의 개수를 늘려서 대처하고 있다22). 환원ㆍ분리로의 일체화 등으로 사이클 타임이 단축되고, batch도 대형화되어 생산성이 향상되었지만, 10 ton batch를 생산하는데 10일 이상이 소요되어14) Ti이 다른 금속에 비하여 가격 경쟁력이 낮은 문제점을 가지고 있다.
한편 러시아, 우크라이나 그리고 중국의 일부 공장에서는 I자형 환원ㆍ분리로를 사용하고 있다. 문헌13,14)으로부터 I자형 환원ㆍ분리로에서의 조업방법을 모식적으로 나타내면 Fig. 9와 같다. 환원반응이 종료한 후에 용기를 냉각하고 뚜껑을 제거한다. 그리고 노 내부의 반응기 상부와 응축조 하부를 결합한 후 거꾸로 세워 스펀지 Ti이 들어 있는 위쪽의 환원조를 재가열 한다. 이때 아래쪽의 응축조를 냉각시키면서 진공배기하여 Mg과 MgCl2를 제거한다. 이 방법은 고온상태의 환원용기를 냉각한 후에 재가열하므로 여분의 에너지 비용이 발생하며, 생산성을 올릴 수 없는 단점이 있다. 그리고 결합된 환원조와 응축조를 대형 크레인으로 들어 올려서 옮겨야 하는 등 작업이 번거로운 단점이 있다. 현재 한 batch의 크기는 3.5~7.5톤 정도인 것으로 알려져 있다.
3.4. MgCl2의 전해환원
Kroll법에서는 Ti 1톤을 제조할 때 환원제인 Mg도 약 1톤이 필요하며, Mg은 식 (6)과 같이 반응 생성물인 MgCl2가 된다. 이 MgCl2를 전해환원하여 Mg과 염소를 생성시켜, 각각 환원 및 염화공정에 사용한다. Kroll법에서는 Mg 전해공정의 전력 소비량이 전체 전력소비량의 70 % 이상을 차지하고 있다.
MgCl2의 용융염 전해조에는 전극의 연결 및 배치 방식에 따라 단극형(mono-polar형)과 복극형(bipolar형)이 있으며, Fig. 10에 각각의 전해조를 모식적으로 나타내었다. Table 4에는 각각의 조업조건들을 나타내었다24). 단극형 전해조는 각각의 전극에 모두 전기를 공급해주는 것으로 양극과 음극으로 이루어진 한 쌍의 전극을 직렬 또는 병렬로 배치한다. 복극형 전해조는 양쪽 끝에 위치한 양극과 음극에만 전기를 공급하고, 그 사이에 음극과 양극 역할을 동시에 수행하는 3~5개 정도의 bipolar전극이 설치되어 있다. 각 전극에서의 반응은 다음과 같다.
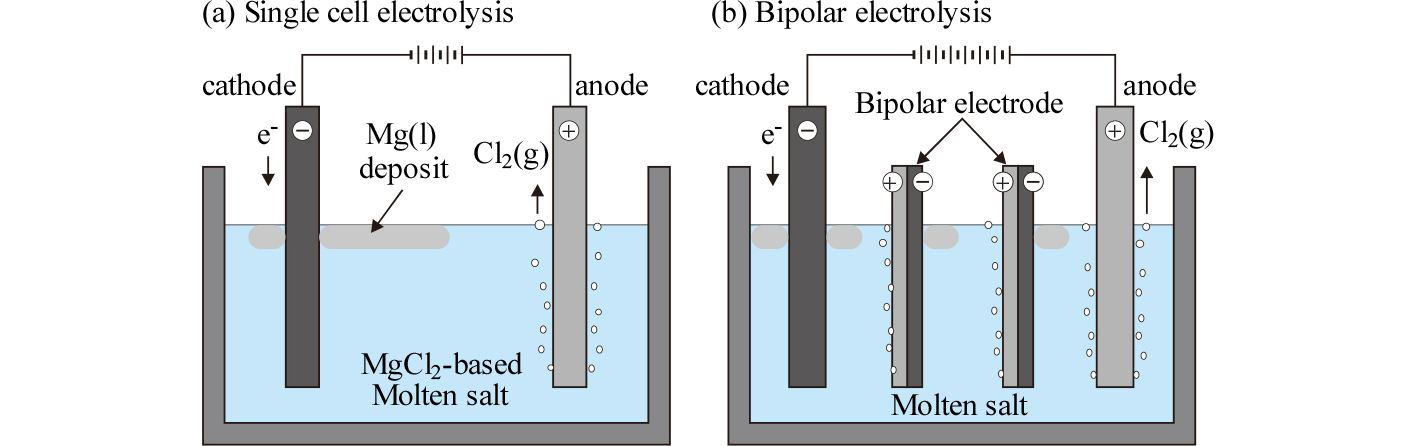
Fig. 10.
Principle of magnesium electrolysis for regenerating magnesium for titanium smelting. (a) conventional magnesium electrolysis, (b) using a bipolar electrochemical cell24).
Table 4.
Operation Results of monopolar and bipolar electrolysis cell of anhydrous MgCl2 for use in regeneration electrolysis of titanium smelting24)
| $$\mathrm{Cathode}:\;\mathrm{Mg}^{2+}(\mathrm{salt})+2\mathrm e^-=\mathrm{Mg}(\mathrm l)$$ | (7) |
| $$\mathrm{Anode}:\;2\mathrm{Cl}^-(\mathrm{salt})={\mathrm{Cl}}_2(\mathrm g)+2\mathrm e^-$$ | (8) |
| $$\mathrm{Overall}:\;{\mathrm{MgCl}}_2(\mathrm l)=\mathrm{Mg}(\mathrm l)+{\mathrm{Cl}}_2(\mathrm g)$$ | (9) |
이 반응의 이론 분해전압은 750 °C에서 2.51 V이지만, 전해조에서의 저항 등에 의해 실제 전해조(cell) 전압은 약 7~9 V가 필요하다.
MgCl2를 약 20 % 함유하는 NaCl-CaCl2계 용융염을 약 670 °C에서 전해하면, 음극(cathode)에서는 액체 Mg이, 양극(anode)에서는 염소가스가 생성된다. Li 등을 함유하는 저밀도 용융염이 아니라면 액체 Mg의 밀도(1.584 g/cm3, at m.p.)가 용융염보다 작으므로, 전극에서 생성된 Mg은 전해욕 표면으로 떠 오른다. 또 용융염 중에 소량의 불화물 이온을 첨가하면 Mg의 응집이 촉진되기도 한다. Fig. 10(a)의 단전극 전해조를 이용하여 Mg의 생산성을 향상하기 위해서는 여러 개의 동일한 전해조를 직렬로 연결하거나, 전해 전류를 증대시켜야 하지만 전해에 따른 발열이 커지므로 에너지 절약에는 큰 도움이 되지 않는 것으로 알려져 있다.
Fig. 10(b)의 bipolar 전해법에서는 양극과 음극 사이에 bipolar 전극(복극)을 삽입하여 용융염 전해조를 여러 개의 전해조로 분할하는 것이다. 이 경우 일정한 전류 조건하에서도 전해속도를 증대시킬 수 있다. 실제로 Fig. 10(a)의 단전극 전해조와 비교하면 동일한 전류조건 하에서 생산성이 약 3배 정도 증가한다. 현재 공업적으로는 70~120 kA, 조전압 10~11 V의 3극식 bipolar 전해조가 가동 중에 있으며, OTC에서는 5극식 bipolar 전해조가 가동되고 있다16). 단전극 전해조의 전력 원단위는 14~18 kWh/kg-Mg 정도이지만, bipolar 전해조에서는 9~11 kWh/kg-Mg 정도로 원가절감에 큰 기여를 하고 있다. 이와 같이 마그네슘 생산량 당 소비전력 면에서 bipolar형이 다소 유리하나, 일반 Mg의 전해제련에서는 Alcan 전해조를 제외하면 대부분 단전극 전해조를 사용하고 있다25).
4. 스펀지 Ti의 파쇄와 잉곳 제조
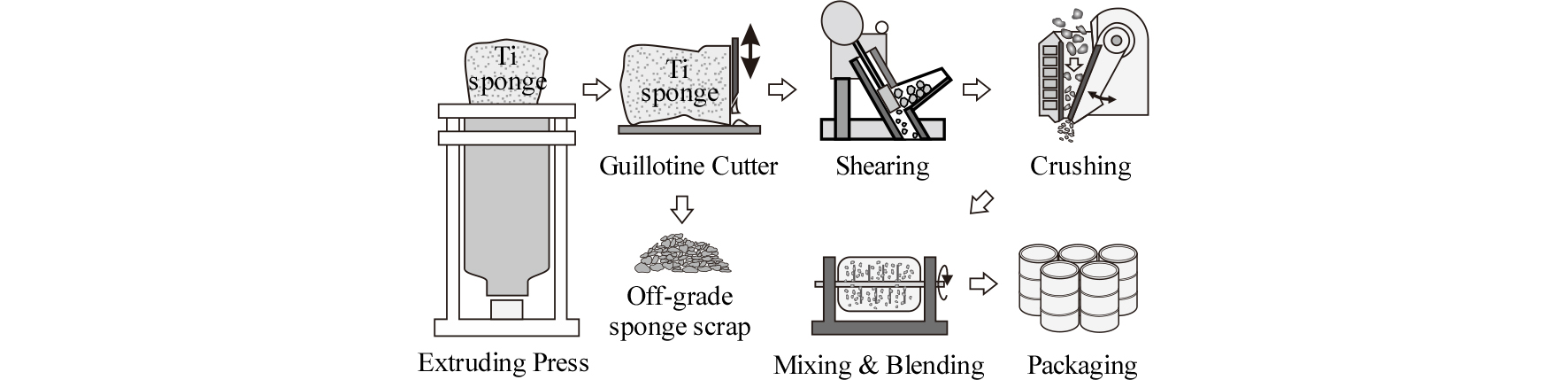
Fig. 11에는 환원ㆍ분리 공정을 거쳐 제조된 스펀지 Ti괴를 일정한 크기로 파쇄하여 포장하는 공정을 모식적으로 나타내었다. 우선 환원조 중의 스펀지 Ti을 압출 프레스를 이용하여 꺼집어 내어 기요틴(guillotine) 프레스로 적당한 크기까지 파쇄한다. 특히 기요틴 공정에서 Fe 등의 불순물이 많은 스펀지 Ti괴의 바닥부분과 측면 부분은 미리 제거하여 페로타이타늄(Fe-Ti) 제조공정으로 보내기도 한다. 그 후 전단 파쇄기와 크러셔 등을 이용하여 필요한 입도까지 분쇄한 후 필요에 따라 혼합하여 포장한다. 일반적인 스펀지 Ti의 입도는 20 mesh(0.84 mm)~1/2'(12.7 mm) 정도이다. 그리고 Fe가 10 ppm 이하인 고순도의 스펀지 Ti은 스펀지 Ti괴의 중심부에만 있으므로 특별히 관리하고 있다23).
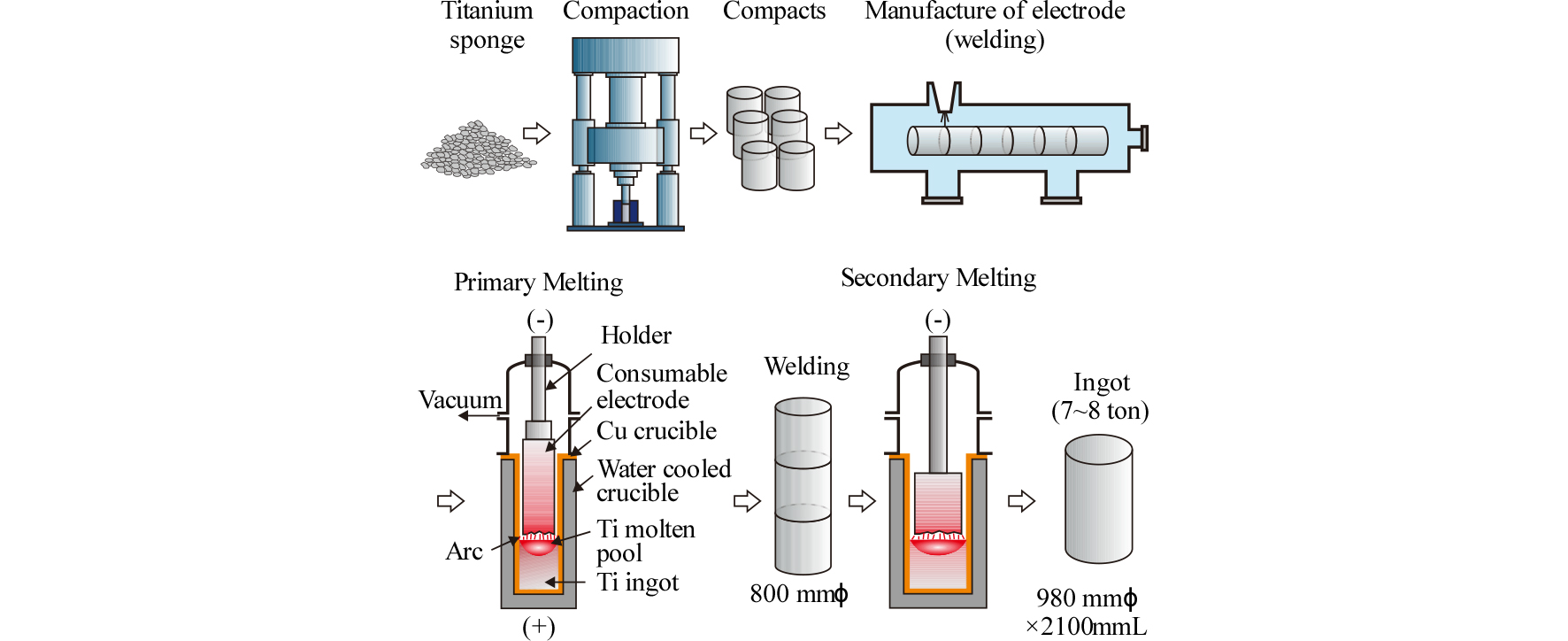
Table 5에는 Ti이나 합금을 용해하는 방법을 종합하여 나타내었다26). 스펀지 Ti이나 Ti 스크랩으로부터 잉곳을 제조하는 방법에는 VAR(vacuum arc remelting)법과 Electron Beam Melting(EBM), Plasma Arc Melting(PAM), Cold Crucible Induction Melting(CCIM) 등이 있다. Fig. 12에는 VAR법을 재구성하여 모식적으로 나타내었다27). 스펀지 Ti을 프레스로 압축성형하고, 이것을 Ar 분위기 중에서 용접하여 1차 전극(직경 약 788 mm)을 만든다. 1차 전극은 진공 아크로(VAR)에서 용해하고, 수냉 구리 도가니 중에서 응고시켜 2차 전극으로 만든다. 1차 용해에서는 가스방출이나 불연속 용해에 의해 잉곳 표면에 요철이 생기기 쉬우며, 응고시에 발생하는 blowhole 등의 내부결함도 존재한다. 따라서 건전한 잉곳을 얻기 위해 1차 용해 후의 전극 여러 개를 접합하여 2차 용해하는 것이 일반적이다. 특히 Ti 합금을 만들 때는 배합성분의 균일화나 국부적 편석을 방지하기 위해서도 2차 용해가 중요하며, 보다 균일화가 요구되는 경우에는 3차 용해를 하기도 한다.
Table 5.
Characteristics of titanium melting processes26)
VAR법은 1~0.1 Pa 정도의 진공도를 유지하면서 용해하므로 스펀지 Ti 중의 MgCl2, Mg, H2O 등은 완전히 제거되어 고순도의 Ti을 얻을 수 있다. 또 전극이나 도가니로부터의 오염이 없으며, 대용량의 용해가 가능한 특징을 가지고 있다. 다만 1차 용해용 소모전극의 제조비용이 높으며, 소모전극을 만들 때 스크랩 등의 형상이나 배합율에 제한이 있다. 스크랩 배합비를 높이기 위해 스크랩을 잘게 파쇄하여 노의 상부에서 소모전극과 구리 도가니 벽 사이를 통해 직접 아크가 발생하는 부분에 투입하는 기술도 개발되어 있다.
전자빔 용해법은 탄탈륨(Ta) 등 고융점 금속의 용해에 사용한 것이지만, Ti 스크랩을 쉽게 용해할 수 있는 수냉 구리 hearth를 이용하는 대형로(EBCHM, Electron Beam Cold Hearth Melting)가 실용화되어 미국의 Timet(EB 출력 5 MW, 6 EB gun) 등에서는 20톤의 잉곳도 만들고 있다26).
5. 종 합
최근에 새로운 Ti 제련기술들이 보고되고 있으나 상용화된 기술은 없는 실정이다. 향후의 Ti 제련기술 도입이나 신제련 기술과 Ti 스크랩의 재활용 기술을 개발하기 위해서는 기존의 Kroll법에 대한 이해가 필요하다. 따라서 본 논문에서는 Kroll법에 의한 타이타늄 제련기술에 대해 고찰하였다. Ti 제련은 우선 루타일이나 저품위의 일메나이트 광석을 고품위화시킨 UGI(up graded ilmenite)를 유동층 염화로나 용융염 염화로에서 TiCl4로 염화시킨다. 정제공정을 거친 TiCl4는 Mg을 이용하여 환원시키고 있으나, 환원 부산물인 MgCl2와 미반응의 Mg을 제거하는 증류공정에 따라 역U자형과 I자형이 있다. 작업성이나 에너지 측면에서는 역U자형이 유리한 것으로 알려져 있다. 그리고 부산물인 MgCl2는 용융염 전해에 의해 Mg과 Cl2(g)로 재생시켜 각각 환원공정과 염화공정에서 사용하고 있다. 이러한 MgCl2의 전해공정은 전극배치에 따라 monopolar형 단극 전해조와 bipolar 전극을 사용하는 복극 전해조가 있으며, 에너지 절약 측면에서는 bipolar형 복극식 전해조가 유리하다. 환원공정에서 만들어진 스펀지 Ti괴의 바닥과 측벽부근에는 Fe 등의 불순물 농도가 높아 기요틴 공정에서 제거하여 규격외 스크랩이 되며, 페로타이타늄 등의 제조에 사용되고 있다. 그 외의 스펀지 Ti은 파쇄하여 압축성형한 후에 용접을 거쳐서 2단계의 VAR을 이용한 진공용해로 잉곳을 만들고 있으며, 경우에 따라서는 EB를 사용하여 용해하기도 한다. 이러한 Kroll법에 의한 Ti 제련공정은 부산물인 MgCl2를 용융염 전해를 통해 환원제인 Mg과 염화제인 Cl2를 재생하여 계속 사용할 수 있는 장점이 있으나, 환원조와의 접촉에 의해 규격외의 공정 스크랩이 발생하고 있다. 향후에 이러한 제련공정에서 발생하는 스크랩을 리사이클링할 수 있는 기술의 개발이 기대된다.