1. 서 론
2. 실험 방법
2.1. 출발원료 및 물리화학적 분석
2.2. 다공성 지지체 및 촉매 비드의 제조
2.3. 물성 평가
2.4. HCHO 제거 특성 평가
3. 결과 및 고찰
3.1. 출발원료 화학분석 및 특성
3.2. 다공성 지지체 및 촉매 비드의 물성특성
3.3. HCHO 제거 특성
4. 결 론
1. 서 론
규석(i.e., 실리카)은 지구 지각의 60% 이상을 차지하고 있는 화합물로서 건축 재료부터 전자공업용 소재 및 광학용 유리 등으로 다양한 산업에 이용된다. 국내에도 물론 다량의 규석이 매장되어 있는데 문제는, 이러한 국내 부존 실리카의 경우 상당부분 화학적 품위가 낮고 산출 상태가 불균일한 특성을 가지고 있다1,2). 반면, 고품위 실리카는 이미 고갈되어 현재는 중국, 인도 등에서 수입한 후 처리 및 소비하고 있는 실정이다1). 실리카의 연간 수입양은 매년 8% 정도 증가하여 최근에는 300억 원대 이르고 있고 실리카 관련 수입 제품은 연간 약 수천억 원대에 이르고 있다3). 이에, 국내산 저품위 실리카의 용도 개발을 위한 품위 향상 또는 저품위 실리카 자체를 활용하기 위한 용도 개발이 필요하다.
한편, 다공성 소재(porous materials)는 촉매, 센서, 반사체, 슈퍼캐패시터 등등 다앙한 산업 현장에 적용되고 활용되고 있다. 일반적으로 다공성 소재는 기공구조(e.g., 기공형태, 기공율, 기공크기, 열린 기공 및 닫힌 기공)에 따라 여러 가지 특성을 가지며, 특성에 따라 사업 현장에 적용되는 분야가 달라진다4,5,6). 이러한 다공성 소재를 제작함에 있어 원료로는 금속, 비금속(i.e., 세라믹) 그리고 플라스틱 등 여러 가지들이 사용되고 있다. 특히, 세라믹 원료의 경우 가격이 저렴하고 상대적으로 다른 원료와 달리 비표면적을 크게 조절할 수 있으며, 내열성도 우수하여 다양한 소재의 원료로 많이 사용된다. 또한 세라믹 원료로 제작된 다공성 소재의 단열재, 촉매지지체, 분리여과 필터 등등으로 적용이 용이하다5,6,7).
마지막으로 본 연구에서 제거 물질로 선정된 포름알데히드(formaldehyde, HCHO)는 접착제, 방부제, 수지 및 화장품과 같은 다양한 재료를 제조하기 위해 업계에서 널리 사용되고 있다8). 문제는 HCHO가 잠재적으로 발암성 등 건강에 악영향을 미치기 때문에 최근 몇 년 동안 많은 대중의 우려를 불러 일으키고 있다는 점이다. 이를 해결하기 위해 HCHO의 저감이 시급한 실정이다. 최근에는 코로나 방전, 표면 방전 및 충전층 플라즈마와 같은 으로 HCHO 등 휘발성 유기화합물 (VOC) 제거 연구에 대한 조사가 많이 수행되었다8,9,10). 그러나 이와 같은 방식은 제거 방식이 초기 설치 및 운전비용이 매우 크며, 게다가 운전방식이 까다롭기 때문에 소규모 사업장의 설치 및 운영에 매우 제한적이다. 반면, 흡착법 또는 촉매에 의한 방식은 상대적으로 설치 및 운영이 용이하기 때문에 HCHO 제거 관련 많은 연구가 이루어지고 있다11,12).
본 연구에서는 소규모 사업장의 활용을 향상시키기 위한 가격 경쟁력을 가질 수 있도록 국내산 저품위 실리카를 원료로 다공성 촉매 지지체를 제작하였다. 그리고 잘 알려진 촉매(구리-제올라이트(Cu-ZSM5), 코발트-제올라이트(Co-ZSM5)) 두 종류 중 테스트를 통해HCHO 제거에 보다 적합한 촉매를 선정하고자 하였다. 구체적으로 최적의 분해열을 확인하고자 150 ℃에서 300 ℃에서 HCHO 제거 특성을 평가하였다.
2. 실험 방법
2.1. 출발원료 및 물리화학적 분석
본 연구에서 사용된 출발원료는 경상북도 문경의 규석광산의 실리카를 사용하였다. 사용된 실리카의 화학적 성분은 XRF (X-ray fluorescence, MXF-2400, Shimadzu) 분석을 통하여 확인하였으며, 입자크기 분포는 레이저 산란 입도분석기(Mastersizer 2000, Malvern)을 사용하였다. 사용된 시료의 결정상 및 결정구조는 XRD (X-ray diffraction, D8 ADVANCE, Bruker)을 통하여 확인하였다.
2.2. 다공성 지지체 및 촉매 비드의 제조
저품위 실리카를 출발원료로서 다공성 지지체 제조는 직접 발포 및 drop-in-oil 성형법을 이용하였다13,14). 간략히 설명하자면, 먼저 저품위 실리카 시료를 어트리션 밀을 통하여 2시간 동안 습식 분쇄하였다. 이때, 슬러리 농도는 50 wt%으로 제조하였으며, 실리카 입자의 분산을 유도하기 위해 SHP (sodium hexametaphosphate)를 1 wt% 첨가하였다. 발포 슬러리에 파라핀 오일 용액내에 떨어뜨려 구형 성형체를 제작하였다. 파라핀 오일과 성형체하고 분리한 후, 80 ℃에서 3일 동안 건조하였다. 그리고나서, 1200 ℃에서 1시간 동안 공기 분위기에서 소성하여 다공성 지지체(the porous support)를 제조하였다.
제작된 다공성 지지체에 구리(copper, Cu)와 코발트(cobalt, Co) 촉매를 담지하여 제조하였다. 두 촉매는 비표면적이 우수한 제올라이트(zeolite, ZSM5) 입자에 담지하여 제조된 다공성 실리카 지지체에 dip-coating 법을 이용하였다. 본 연구에서 사용된 제올라이트는 ZSM5로서 1.0 M의 ammonium nitrate (NH4NO3, Aldrich) 수용액 1.5 L에 15 g의 제올라이트를 넣고 6시간 동안 이온 교환을 실시하였다. 이온 교환된 샘플을 증류수로 충분히 세척하고 90 ℃에서 12시간 이상 건조하여 NH4+형 제올라이트를 제조하였다. 이렇게 이온 교환된 NH4+형 제올라이트를 Co-ZSM5 촉매 그리고 Cu-ZSM5 촉매를 제조하였다. 코발트 촉매는 cobalt nitrate hexahydrate (Co(NO3)2․6H2O, Aldrich, USA)이며, 구리 촉매는 copper nitrate (Cu(NO3)2, Aldrich, USA)를 출발 시약으로 사용하였다. 두 출발원료를 각각 0.1 M 용액을 250 ml를 제조하였다.
제작된 Co-ZSM5 그리고 Cu-ZSM5 촉매 비드와 일정량의 증류수를 혼합한 수용액 상에 다공성 지지체를 혼합하였으며, 회전감압농축기에 촉매 수용액 250 ml와 지지체 250 ml를 혼합하여 사용하였다. 담지조건은 0.1 mbar 그리고 500 rpm으로 진행하였으며, 온도는 상온에서 실시하였다. 담지유지 시간은 1시간으로 진행하였다. 분리된 촉매는 항온항습기에서 온도 50 ℃ 그리고 습도 50 %에서 건조하였다. 이렇게 건조된 샘플을 꺼내어 하소온도 450 ℃에서 2시간 진행하여 촉매 비드를 제조하였다.
2.3. 물성 평가
미세구조 및 표면분석은 SEM-EDS (Scanning electron microscopy, JSM-6300, JEOL)을 이용하였다. 제작된 샘플의 기공율은 벌크밀도 그리고 겉보기 밀도를 통하여 계산하였으며, 진밀도는 헬륨 피코노메터(Accupyc 1330, Micromeritics)을 이용하여 측정하였다14,15). 국내산 저품위 실리카로부터 제작된 다공성 지지체 그리고 제작된 촉매 비드는 가스 물리흡착분석기(gas physisorption analyzer, ASAP 2020, Micromeritics)를 통하여 비표면적을 측정하였다. 제조된 Co-ZSM5 그리고 Cu-ZSM5 코팅 표면의 특성을 확인하기 위해 FT-IR (FT/IR-4100, JASCO) 분석을 수행하였다.
2.4. HCHO 제거 특성 평가
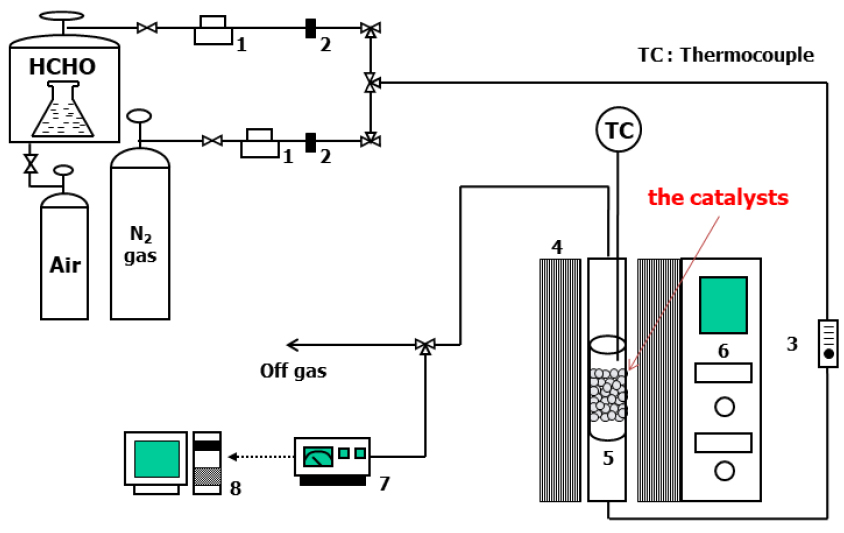
본 연구에서 제조된 Co-ZSM5 실리카 촉매 그리고 Cu-ZSM5 실리카 촉매의 HCHO 제거 성능 평가를 하고자 하였다. HCHO은 가스상으로 제조하기 어렵기 때문에 5% HCHO 용액으로 제조하여 사용하였다. Fig. 1은 촉매를 이용한 HCHO 제거 실험장치 모식도를 나타내었다. 이 실험장치는 크게 가스주입 부분, 반응기 부분 그리고 반응가스 분석 부분으로 구성되어 있다. 반응기에 공급되는 HCHO 가스의 경우, 5% 용액으로 제조하여 사용하였으며, carrier 가스로는 질소를 사용하여 농도를 조절하였다. 반응기에 공급되는 가스는 상향류 시스템인 석영 반응기로 유입되어 반응온도에 따른 제거 성능을 측정하게 된다. 이 때 촉매필터 후단에 온도 측정기을 연결하여 반응온도를 측정하였다. 반응기의 온도를 일정하게 유지하기 위해서 자켓 히터를 석영관 반응기에 장착하였다. HCHO 농도 측정기(Z-300XP, Environmental Sensors Co.)을 이용하여 실시간으로 측정하여 결과를 얻었다.
3. 결과 및 고찰
3.1. 출발원료 화학분석 및 특성
본 연구에서 사용된 실리카의 평균 입자크기는 20 μm으로 확인되었으며, 겉보기 밀도는 2.56 g/cm3으로 확인되었다. 화학성분 결과는 Table 1에 나타내었으며, SiO2 품위가 90.8 %으로 확인되었으며, 일반적으로 첨단산업(예, 반도체 산업 등)으로의 적용하기 위해서는 상대적으로 매우 낮은 품위를 가지는 것으로 확인되었다. 이에, 고순도 원료로 사용하기에는 상대적으로 품위가 낮은 저품위 실리카로 판단된다.
Table 1.
Chemical composition of the silica used in this study
| Starting material | Chemical composition (wt.%) | |||||
| Silica | SiO2 | Al2O3 | CaO | K2O | Fe2O3 | L.O.I. |
| 90.8 | 4.4 | 2.7 | 0.8 | 0.7 | 0.6 | |
출발원료의 결정구조 분석은 XRD을 통하여 수행하였으며, 대부분이 석영(quartz) 그리고 백운모(muscovite)로 관찰되었다. 이에, 화학분석 결과 및 XRD 분석을 통하여 본 연구에서 사용된 시료는 국내산 저품위 실리카로서 확인되었다.
3.2. 다공성 지지체 및 촉매 비드의 물성특성
출발원료인 저품위 실리카를 이용하여 다공성 지지체를 제조하기 위해서는 습식 분쇄를 먼저 수행해야 한다. 이때, 발생된 기포의 표면에 안정적으로 형성하기 위해서 평균 입자크기 3 μm 이하로 분쇄해야 한다. 분쇄시간 2시간에 본 연구에서 사용된 실리카의 평균 입자크기가 3 μm가 되는 것으로 관찰되었다. 제작된 다공성 실리카 지지체의 기공율은 72%으로 확인되었다. 촉매 비드의 크기는 0.5에서 5 mm를 가지며, 평균 2.5 mm으로 확인되었으며, 2 종류의 촉매 사진은 Fig. 2에 나타내었다.
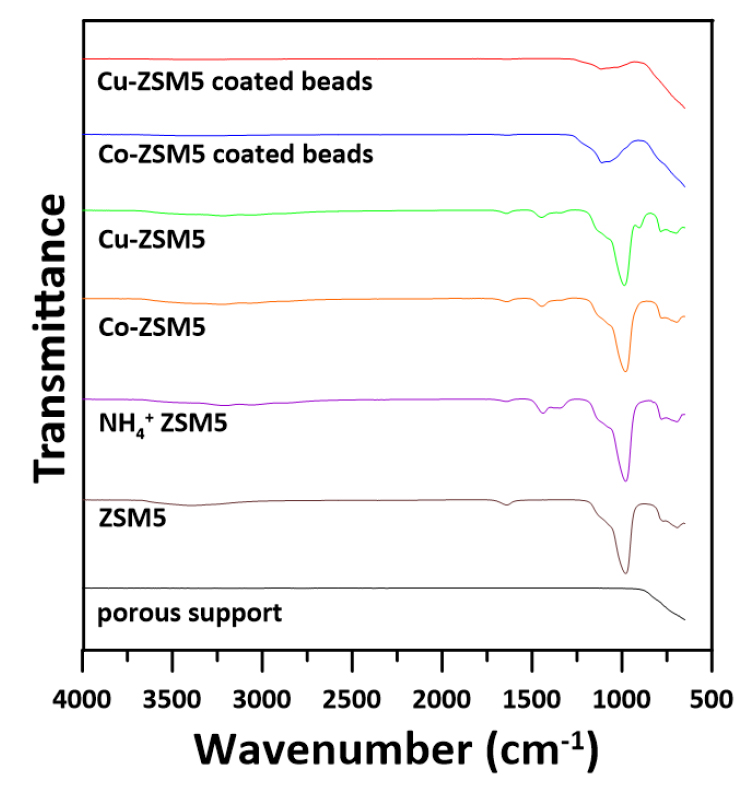
Co-ZSM5 코팅된 촉매의 경우에는 보라색 빛을 띄며, Cu-ZSM5 코팅된 촉매은 초록색 빛을 나타내고 있다. Co-ZSM5 그리고 Cu-ZSM5 코팅된 촉매 비드의 표면을 확인하기 위해 FT-IR 분석을 수행하였으며 그 결과는 Fig. 3에 나타내었다.
Fig. 3은 지지체, ZSM5 그리고 촉매 코팅된 비드의 FT-IR 결과를 나타내었다. 실리카의 경우, 800 cm-1 이하에서 피크가 나타남에 따라 실리카의 결정이 됨을 확인 할 수 있었다16). 또한, 이온교환된 제올라이트 경우, 제올라이트에 존재하지 않는 1200 cm-1에서 1500 cm-1 부근에서 넓게 피크가 나타남에 따라 이 부근이 이온교환된 피크를 나타나는 것으로 판단된다. 그러나, 구리 및 코발트가 담지된 제올라이트 경우, 이온교환된 제올라이트 비해 특별히 나타나는 피크가 보이지 않았다. 하지만, 촉매 비드의 경우, 제올라이트의 주 피크인 1200 cm-1 ~ 800 cm-1가 나타났다. 따라서, 본 연구에서 적용된 다공성 실리카 지지체에 Co-ZSM5 촉매 및 Cu-ZSM5 촉매가 담지된 것을 확인되었다.
제작된 다공성 실리카 지지체와 Co-ZSM5 촉매 비드 그리고 Cu-ZSM5 촉매 비드의 비표면적 및 기공부피 결과는 Table 2에 나타내었다. 국내산 저품위 실리카로부터 제작된 다공성 지지체의 비표면적은 0.82 m2/g으로 관찰되었으며, 기공부피는 0.0011 cm3/g로 나타났다. 전반적으로 촉매 코팅으로 인하여 제작된 비드의 비표면적이 증가하였으며, ZSM5 제올라이트가 대략 700 m2/g으로 높은 비표면적을 가지기 때문에 다공성 비드 지지체 표면에 코팅됨으로서 지지체 비드에 비해 상대적으로 촉매 비드의 비표면적이 증가하였다. 또한, Co-ZSM5 촉매 코팅된 비드가 Cu-ZSM5 촉매 코팅된 비드가 비표면적 그리고 기공부피가 높은 것으로 확인되었다.
Table 2.
BET specific surface area and pore volume of the porous supports, the Co-ZSM5 coated beads and the Cu-ZSM5 coated beads, respectively
| Sample |
BET specific surface area (m2/g) |
Pore volume (cm3/g) |
| Porous supports | 0.82 | 0.0011 |
| Co-ZSM5 coated beads | 54.8 | 0.0844 |
| Cu-ZSM5 coated beads | 31.6 | 0.0446 |
3.3. HCHO 제거 특성
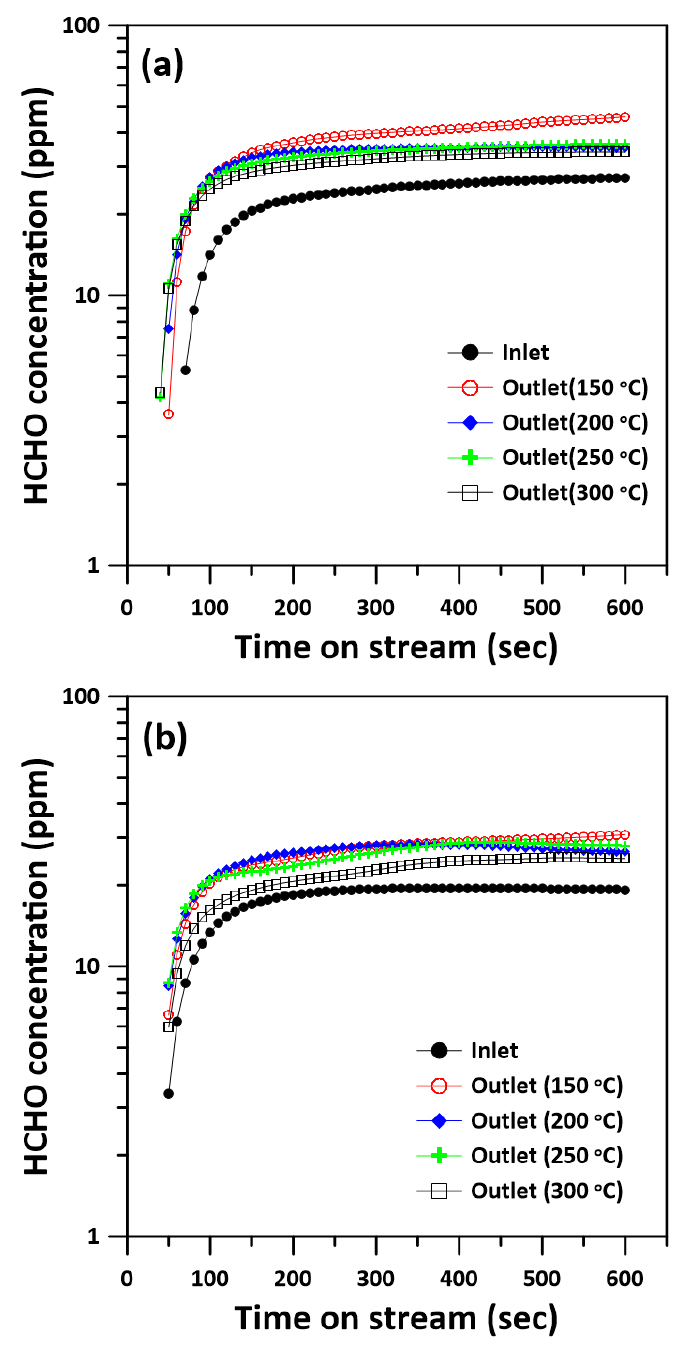
본 연구에서 제작된 Co-ZSM5 코팅된 비드 그리고 Cu-ZSM5 코팅된 비드를 HCHO 제거 특성을 평가하고자 하였다. 일단, 제조된 촉매 비드들의 HCHO 제거 실험 이전에 셋팅된 실험 장비에서의 반응온도에서의 HCHO의 평행한 가스 농도 유지에 대한 평가를 먼저 실시하였다. Fig. 4(a)는 반응온도에 따른 촉매 비드가 설치되지 않는 상태의 설치된 실험장비에서 입구 및 출구에서의 HCHO 농도 결과를 나타내었다.
HCHO의 가스 흐름 농도는 대략 200 초부터 일정해지는 것으로 확인되었다. 그러나, 반응온도가 존재하는 조건에서 배출되는 HCHO 농도는 상대적으로 높은 것으로 관찰되었다. 이는 아마도 높은 온도 조건에서 HCHO의 분자부피 증가로 인하여 상대적으로 높게 측정되는 것으로 판단된다. 그러나, 흥미롭게도 반응온도에서도 대략 200 초에서부터 HCHO 농도 또한 평행하게 유지되는 것으로 관찰되었다. 따라서, 모든 HCHO 제거 평가 실험은 200 초부터의 가스 흐름을 유지하도록 하였다. Fig. 4(b)는 반응온도 조건에 따른 다공성 지지체의 HCHO 배출 농도 결과를 나타내었다. 전체적으로 HCHO 배출 농도가 유입농도보다 약간 높아지는 것으로 확인되었으며, 이에 따라 다공성 지지체에 의한 HCHO 제거 되지 않는 것으로 나타났다.
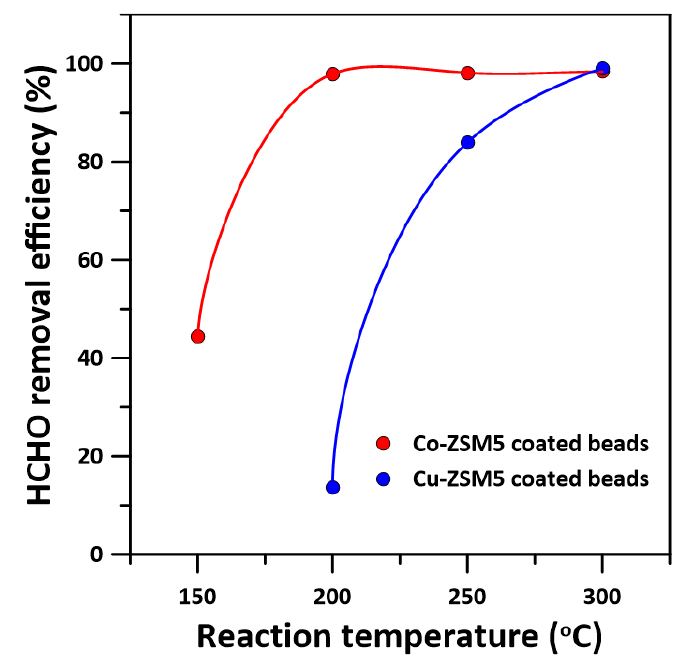
Fig. 5는 제조된 Co-ZSM5 코팅된 비드 그리고 Cu-ZSM5 코팅된 비드에 의한 반응온도 조건에서의 HCHO 제거율 결과를 나타내었다. 초기 HCHO 농도는 20 ppm이었으며, 공간속도는 2200 h-1으로 설정하였다. HCHO 주입시간은 200초 이상으로 수행하여 주입 농도가 20 ppm이 안정적으로 유지됨을 확인하였다. 본 연구에서 제조된 Co-ZSM5 코팅된 비드에 의한 150 ℃에서 HCHO 제거율은 대략 44%이었으며, 200 ℃에서 대략 97%으로 관찰되었다. 그리고 250 ℃ 이상에서 98% 이상의 HCHO 제거율이 유지되었다. 그러나, 제조된 Cu-ZSM5 코팅된 비드는 150 ℃에서 HCHO 제거가 일어나지 않았으며, 200 ℃에서 대략 13% 제거율이 관찰되었다. 그리고 반응온도가 증가됨에 따라 HCHO 증가되어 300 ℃에서 99% HCHO 제거율이 확인되었다.
전체적으로 반응온도가 증가됨에 따라 두 촉매 비드 모두 HCHO 제거율 모두 증가되었다. 그러나, 제조된 Co-ZSM5 코팅된 비드가 Cu-ZSM5 코팅된 비드에 비해 동일 반응온도에서도 HCHO 제거율이 높게 관찰되었다. 이것은 아마도 다공성 실리카 지지체 위에 코팅된 촉매의 활성화된 표면적 증가로 인하여 HCHO의 흡착 및 효과적인 분해가 일어나는 것으로 판단된다. 따라서, 본 연구에서 사용된 국내산 저품위 실리카로부터 다공성 지지체를 HCHO 제거를 위한 촉매 제조하기 위해서는 Co-ZSM5가 더 적합한 것으로 확인되었다. 그러므로, 국내산 저품위 실리카를 HCHO 제거를 위한 촉매 제조에 사용할 수 있는 출발원료로서 충분히 활용할 수 있을 것으로 판단된다.
4. 결 론
본 연구에서는 국내산 저품위 실리카를 활용하여 다공성 지지체 제조 및 촉매 코팅을 통하여 HCHO 제거를 위한 촉매 비드에 대한 연구를 조사하였다. 먼저, 얻어진 시료는 실리카 함량이 90%이었으며 결정상은 석영으로 관찰되어 저품위 실리카임을 확인하였다. EDS 그리고 FT-IR 분석을 통하여 제조된 다공성 실리카 지지체 표면에 Co-ZSM5 그리고 Cu-ZSM5 촉매의 담지가 되어 있음을 확인하였다. 제작된 촉매 비드들을 사용하여 HCHO 제거 실험을 수행하였으며, 전체적으로 반응온도 조건에서 Co-ZSM5 촉매 비드가 Cu-ZSM5 촉매 비드보다 높은 제거율을 나타내었으며, 이는 아마도 상대적으로 우수한 표면활성특성(비표면적, 기공부피)로 인하여 HCHO의 표면 분해를 유도하여 결과적으로 높은 HCHO 제거율을 가지는 것으로 판단된다. 따라서, 본 연구에서 사용된 국내사 저품위 실리카를 활용하여 제작된 다공성 지지체를 HCHO 제거용 촉매로서 사용하기 위해서는 Co-ZSM5 촉매가 적합하며, 200 ℃에서 97% 이상의 제거율을 가지는 것으로 나타났다.