1. 서 론
2. 전기투석(Electrodialysis : ED)의 원리 및 구성(configuration)
2.1. 전기투석(Electrodialysis : ED)의 원리 및 특징
2.2. 셀(Cell) 구성에 따른 특성
2.3.전기투석 스택의 구성 및 공정설계 시 고려사항24)
3. 바이폴라 전기투석(Bipolar Membrane Electrodialysis : BMED)의 원리 및 구성
3.1. 바이폴라 전기투석(BMED)의 원리 및 특징
3.2. 셀(Cell) 구성에 따른 특징
3.3. 폐수무방류 시스템에 적용사례
4. 바이폴라막의 제조 기술 현황 및 전망
5. 결 론
1. 서 론
습식공정에 의해 금속을 회수하기 위해서는 먼저 금속함유 광석이나 스크랩 등을 적절한 용매을 사용하여 금속성분을 침출시키는데 이때 가장 많이 사용되는 용매는 황산이다. 이러한 황산에 의해 용해되어 있는 각 금속을 회수하기 위해서 침전 및 중화처리, 또는 침출액의 pH 조절용으로 다량의 알칼리(NaOH)를 사용한다. 따라서 이러한 알칼리의 사용으로 인하여 다량의 Na2SO4 폐액이 발생하게 된다1,2). 이러한 Na2SO4 폐액은 기존 습식제련공장 외에 폐리튬전지 재활용 공정에서 Mn, Co, Ni, Li 등의 금속 회수 공정3,4), Rayon 제조공정5), 아황산가스를 정화하기 위해 NaOH를 사용하는 공정6) 등 화학공정에서도 다량 발생되고 있다. 비록 이러한 Na2SO4 폐수의 경우는 독성이 크지는 않지만 방류 시에는 엄격한 규제 대상이 되어있다. 이러한 폐염용액을 처리하기 위한 방안으로는 기존에 증발(evaporation)-증류(distillation)방법을 통해 처리하거나7), 증발–결정화(crystallization)과정을 통해 96% 순도의 Na2SO4로 회수가 가능하다8). 그러나 이러한 방법으로 처리할 경우 증발 농축 과정에서 많은 에너지 비용이 부담이 되고 있고 회수된 결정성의 Na2SO4를 재활용하는데 어려움이 많다. Na2SO4가 세제(detergent)나 염색제 등으로 재활용하여 사용하기 위해서는 엄격한 품질기준에 적합해야 하나 상기 재활용 제품은 불순물 등의 영향으로 그 기준에 맞추기가 까다로워 사용이 어렵다. 이로 인하여 공정 중에 발생되는 Na2SO4로 인하여 또 다른 환경오염을 유발할 수 있기 때문에 적절한 처리방안이 필요하다. 따라서 이러한 Na2SO4 폐액을 적절히 처리하여 재활용할 수 있는 방안으로 전기투석(electrodialysis: ED), 바이폴라전기투석(bipolar membrane electrodialysis: BMED) 등과 같은 전기분리막(Electro-membrane) 기술이 주목을 받고 있다9,10,11). 전기분리막 기술은 전기투석이나 바이폴라 전기투석 등과 같이 셀 내에 양이온 및 음이온교환막을 설치하고 전기에너지를 이용하여 이온들을 선택적으로 분리 이동 시키는 기술로 그동안 해수담수화 처리, 유기산 회수, 식품 공업, 도금산업 등에 다양하게 응용이 되어 왔다. 이 기술의 특징은 산 및 염기를 회수하여 재활용함으로써 화학약품의 구매 비용을 절감할 뿐만 아니라 처리수 또한 공정수로 재사용하여 폐수처리 비용을 절감할 수 있는 폐수무방류(Zero liquid discharge)가 가능한 기술로 평가되고 있다. 특히 BMED는 바이폴라막을 사용하여 염(Na2SO4)용액 에서 산(H2SO4)및 염기(NaOH)를 효과적으로 분리·회수가 가능하기 때문에 환경친화형 기술로 평가되고 있으며12,13,14), 최근에는 Li2SO4용액에서 배터리 소재인 LiOH와 H2SO4로 회수하는 기술이 많은 주목을 받고 있다15).
본 연구에서는 친환경 기술로 급부상하고 있는 전기분리막 기술인 ED와 BMED 기술의 원리 및 셀(Cell) 구성에 따른 여러 가지 특성에 대한 조사하고 특히 금속회수 공정 중 다량 발생되고 있는 Na2SO4 처리 분야에 적용된 연구사례 분석 등 기술 개발 동향을 조사하여 향후 최적의 시스템 개발을 하는데 기여하고자 한다.
2. 전기투석(Electrodialysis : ED)의 원리 및 구성(configuration)
2.1. 전기투석(Electrodialysis : ED)의 원리 및 특징
전기투석 공정은 직류전류를 구동력으로 하여 전리되어 있는 이온을 양이온 및 음이온교환막에 투과시켜 분리하는 공정으로 이온 수용액이 전기투석장치 격실 내로 들어오면 전기장에 의해 음이온은 양극실로, 양이온은 음극실로 이동하여 이 과정에서 양이온은 양이온교환막을 쉽게 통과하고 음이온도 음이온교환막을 선택적으로 통과한다. 두 전극사이에 교차적으로 양이온막과 음이온막을 설치하고 직류를 흐르게 하면 교차된 막 사이에서는 이온농도가 증가하지만 다른 막 사이에서는 이온 농도가 감소하는 농도가 나타나 결과적으로 농축 용액으로 분리된다. 전기투석 공정은 양극과 음극사이에 양이온교환막과 음이온교환막을 교대로 연속적으로 배치하고 있고 한 쌍의 양이온교환막과 음이온교환막이 하나의 셀(Cell)을 구성하며 전기적으로 하전 된 막과 전위차의 조합에 의해 다양하게 배열하여 사용할 수 있다. 이러한 전기투석 공정은 운전 도중에 부산물이 거의 발생하지 않고 추가적으로 재사용을 위한 화학적 처리를 하지 않아도 되는 환경 친화형 공정이며 전기에너지 외의 추가적인 에너지 변환이 요구되지 않기 때문에 에너지 효율 측면에서도 장점을 가지고 있다. 최근에는 우수한 이온선택성 및 내열성 그리고 내화학성이 있는 이온교환막의 개발로 인하여 다양한 조건의 환경에서 조업이 가능하게 되었다. 전기투석 기술은 해수담수화 처리 분야는 물론 폐수처리 분야에 응용되면서 공업용수의 재순환 및 구리도금 공정 등 도금폐수 처리 분야에 적용이 되고 있으며 이외에 질산나트륨 농축, 황산나트륨, 염화칼슘의 농축 및 회수, 황산리튬의 농축에도 응용되고 있다16,17).
2.2. 셀(Cell) 구성에 따른 특성
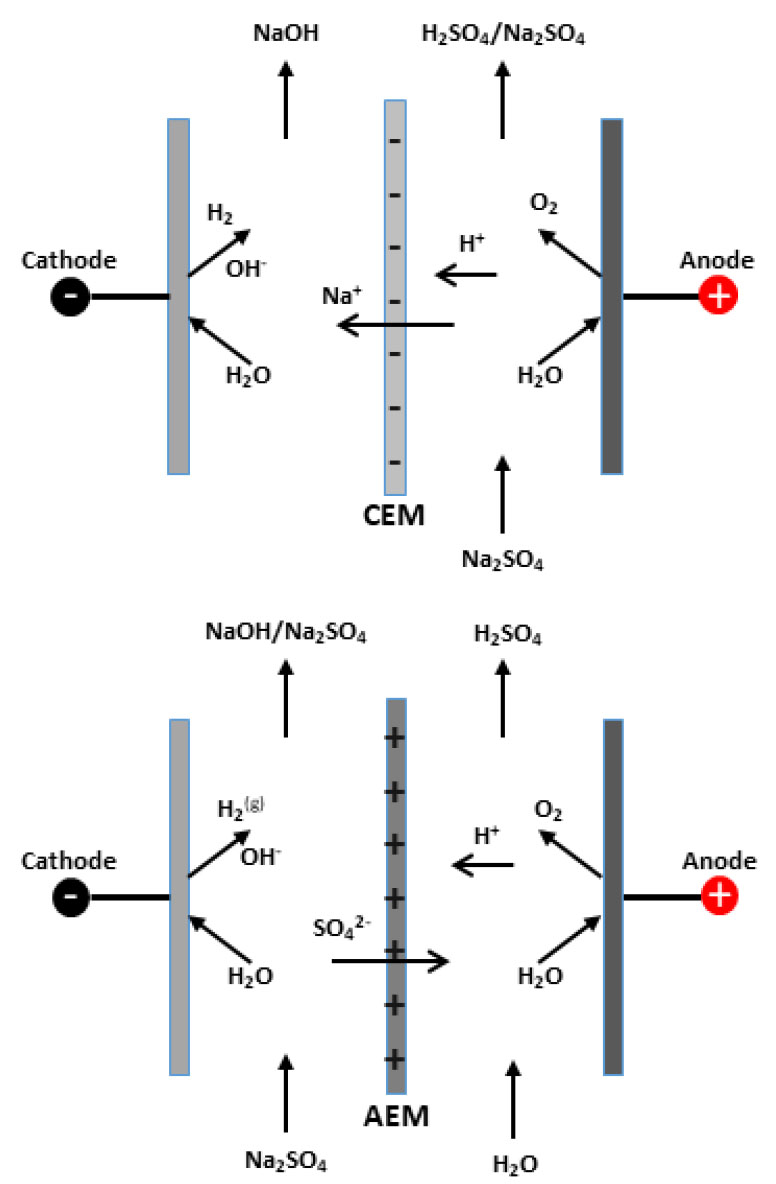
전기투석 공정은 셀 구성에 따라 2실(two compartment)-ED 및 3실(three compartment)-ED로 구분할 수 있다. 2실-ED의 경우는 Fig. 1과 같이 양극(anode)에서는 물이 산화되어 산소와 수소이온(H+)이 발생되고 음극(cathode)에서는 물이 환원되어 수소와 수산화이온(OH-)으로 된다. 이 경우 중간에 양이온교환막(CEM)을 설치할 경우 이 막을 통과한 Na+와 물 분해에 의해 생성된 OH-가 반응하여 음극실에서는 순수한 NaOH가 생성되고, 양극실에서는 황산(H2SO4)과 Na2SO4가 혼합된 용액으로 생성된다. 만일 중간에 음이온교환막(AEM)을 설치할 경우에는 SO4- 이온이 음이온교환막을 통과하여 양극실에서 순수한 황산이 생성된다. 그러나 특별한 경우를 제외하고는 음이온교환막을 설치하는 것보다 양이온교환막을 설치하는 것이 여러 가지 면에서 바람직하다. 이때 반응식은 다음과 같으며, Na2SO4염의 NaOH로의 전환율은 50~60% 정도로 다소 낮은 편이다.
Cathode : 2H2O + 2e- → 2OH- + H2 (Eo = -0.83 V)
Anode : H2O → 2H+ + 1/2O2 + 2e- (Eo = 1.23 V)
Total : 3H2O → 2OH- + H2 + 2H+ + 1/2O2
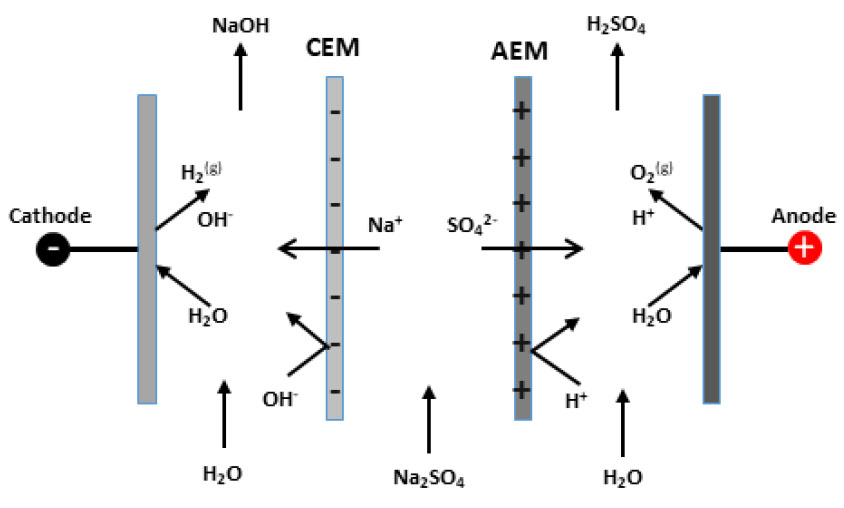
3실-ED는 Fig. 2와 같이 전기분해셀 내에 음이온교환막(AEM) 과 양이온교환막(CEM)을 동시에 설치한 구조이다. 이 경우에는 Na2SO4염이 셀내에 투입되면 양극실에서는 순수한 H2SO4, 음극실에서는 순수한 NaOH가 생성되고 전환율은 거의 100%에 근접할 정도로 전류효율이 높다는 장점이 있다. 단점으로는 셀 구조가 다소 복잡하고 투자비가 다소 많이 들고, 전극들 사이의 거리와 저항에 따라 전기에너지 소비량이 증가한다는 점이다. 그러나 높은 전류효율로 인하여 에너지 소모량은 어느 정도 보상받을 수 있다.
이와 같이 셀 구조에 따라 특성이 조금씩 다르기 때문에 폐액의 성상이나 농도, 회수하고자 하는 물질 및 순도, 그리고 경제성 등을 고려하여 적절한 셀 구조를 고려하여야 하며 이에 대한 연구 결과들을 소개하면 다음과 같다. J. Jörissen 등18)은 전기투석 실험을 통해 전류효율이 양극실(황산, 황산나트륨)의 농도 또는 음극실(가성 소다, 황산나트륨)의 농도에 의존하며 이러한 현상을 설명하기 위해 양이온교환막과 음이온교환막 모두에 적용할 수 있는 막의 “산” 및 “알칼리성” 상태 모델을 개발하여 황산나트륨, 황산 및 가성소다의 농도를 최적화 하는데 기여를 하였다. M. Rakib et al. 등19)은 2실-ED 실험에서 Na2SO4염이 황산 및 가성소다로 분리하는데 free H+이 Na+와 함께 막을 통해 이동함으로써 전류효율을 감소시킨다고 설명하고, 막을 통한 Na+ 및 H2O의 이동현상을 측정하고 모델링을 통해 연속 공정에 의한 Na2SO4염 분해에 관한 연구를 하였다. N. Tzanetakis 등20)은 Na2SO4용액에서 3실-ED를 사용하여 산과 염기의 재생에 관한 연구를 실시하였다. Pall RIO10 및 Pall RI030을 각각 양/음이온교환막으로 사용하여 유속, 전류밀도 및 초기 염농도 등 전기투석 장치 효율에 미치는 영향에 대해 고찰하여 2실-ED와 비교하였다. 연구결과 3실-ED가 2실-ED보다 전류효율, 전력 소비 및 제품농도 측면에서 우수하고 고순도 산과 염기를 생산할 수 있는 장점이 있지만 운영비가 더 많이 소요된다는 연구 보고를 하였다. F. ohman등21)은 pulp mill에서 발생되는 Na2SO4를 처리하기 위해 2실-ED 및 3실-ED를 사용하여 산(H2SO4) 및 염기(NaOH)로 분리·회수하는 연구를 실시하였는데, 3실의 경우가 회수되는 산 및 염기의 전환율이 높고 순도가 좋지만 경제성 면에서는 2실이 효과적이라 제안하고 이에 대한 분석 결과를 Table 1과 같이 제시하였다.
Table 1.
Comparison of two and three compartment electrolyzer systems for sodium sulphate splitting21)
| Two compartment electrolyzer system (Fig. 1) | Three compartment electrolyzer system (Fig. 2) | |
|
Electrolyzers available on the market |
Many different suppliers of electrolyzers, the chlor-alkali market is very large industry |
Few suppliers have three compartment electrolyzers available. |
| Membranes | Cation exchange membranes | Cation and Anion exchange membranes |
| Anode reaction | H2O → 2H+ + 1/2O2 + 2e− | |
| Cathode reaction | 2H2O + 2e− → 2OH− + H2 | |
|
Possible conversion of sodium sulphate to acid | 50-60% | Almost complete |
| Current efficiency | 50-70% | |
| Cell voltage | 3-6 V/cell | |
| Operating temperature | 60-80℃ | |
| Current density | 2-5 kA/m2 | |
| Energy consumption | 4000 kWh/ton NaOH | |
| Caustic purity | Comparably to commercial NaOH from membrane plants. | |
| Caustic strength | Up 10-15 wt% NaOH | |
| Acid purity |
Contains approximately 50/50 /H2SO4 | Pure H2SO4, may be very high purity. |
| Acid strength |
Upto 20 wt% H2SO4 + 30 wt% Na2SO4. (50 wt% NaHSO4) | Upto 20 wt% H2SO4, No Na2SO4. |
| Hydrogen purity | Pure, concentrated | |
| Oxygen purity | Concentrated, scrubbing from Cl2 necessary if feed Na2SO4 contains chloride | |
| Investment cost |
Comparable to chlor-alkali plant cell rooms of the same installed electrode area. |
Significantly higher due to arrangement for extra compartment |
| Maintenance cost | Comparable to chlor-alkali plant cell rooms |
Higher cost, due to mid-compartment and extra membrane. |
| Overall economics |
Depends on integration to mill. In general it might be considered that despite the higher capital cost for the three compartment system these offers better integration to the mill and hence a better economical option. | |
Yang, C. 등은6) Fig. 3과 같이 Flue Gas Desulfurization(FGD) 처리 과정에서 나오는 Na2SO4 용액을 3실 전기투석 방법을 통하여 산 및 염기 그리고 gas(H2, O2)를 회수하는 연구를 실시하였다. 연구 결과 NaOH 회수 시 전류효율은 84%, H2SO4 회수 시 87%이며 회수된 NaOH는 Scrubbing agent로 공정에 재투입하여 사용이 가능하고, 부생으로 산소 및 수소 가스를 얻을 수 있는 환경친화형 공정이라고 소개하였다. B. Pisarska 등은22,23) 사이클로헥사논 제조공정에서 발생되는 황산나트륨 폐액을 황산, 가성소다 및 투석액으로 재생하기 위한 기초 연구를 실시하였다. 폐액 내 유기화합물의 존재는 전류효율에 영향을 미치지 않았으나, 용액의 COD가 증가하면 에너지 소비가 증가하고 고온(55~58°C)에서 전류효율 개선 효과가 좋다고 하였다. 또한 회수된 NaOH와 H2SO4는 온도 및 유기물의 농도 및 조성에 따라 일부 유기물이 혼입 될 수는 있으나 생성물을 공정 원료로 재사용 하는 데는 문제가 없다고 하였다. 이어서 공정개발을 위해 온도, 셀전 압, 농도 및 에너지소비 등의 영향에 대한 연구를 실시하여 초기농도 80.90 g/dm3인 Na2SO4 용액에서 13.96% NaOH과 10.15% H2SO4 및 투석액(3.23 g/dm3 SO42-)으로 회수가 가능하다고 보고하고, 다단 실험을 통해 연속공정 설계를 위한 기초를 마련하였다.
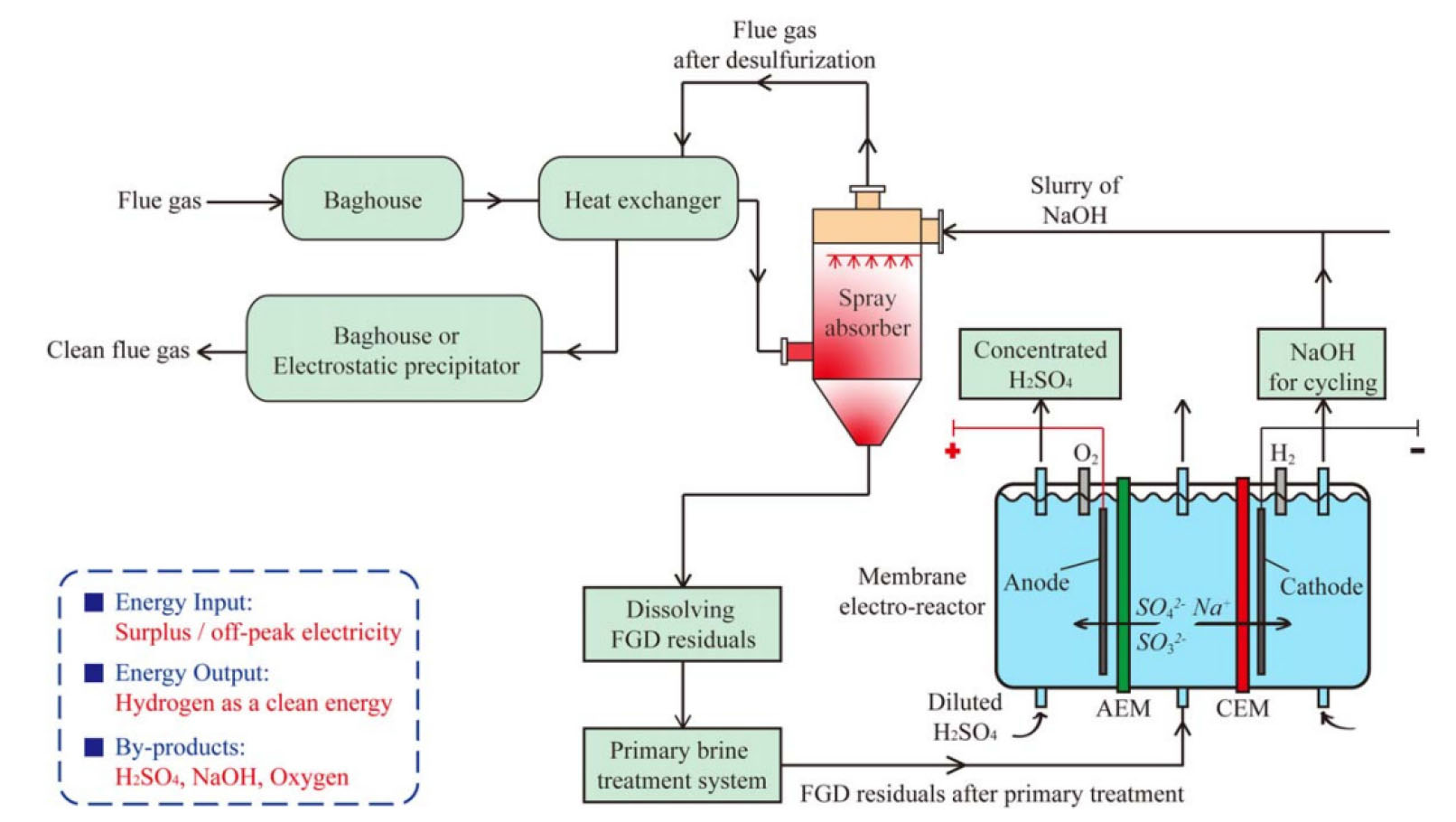
Fig. 3.
Schematic diagram of the designed electrochemical process for recycling and resource recovery of FGD residuals3).
2.3.전기투석 스택의 구성 및 공정설계 시 고려사항24)
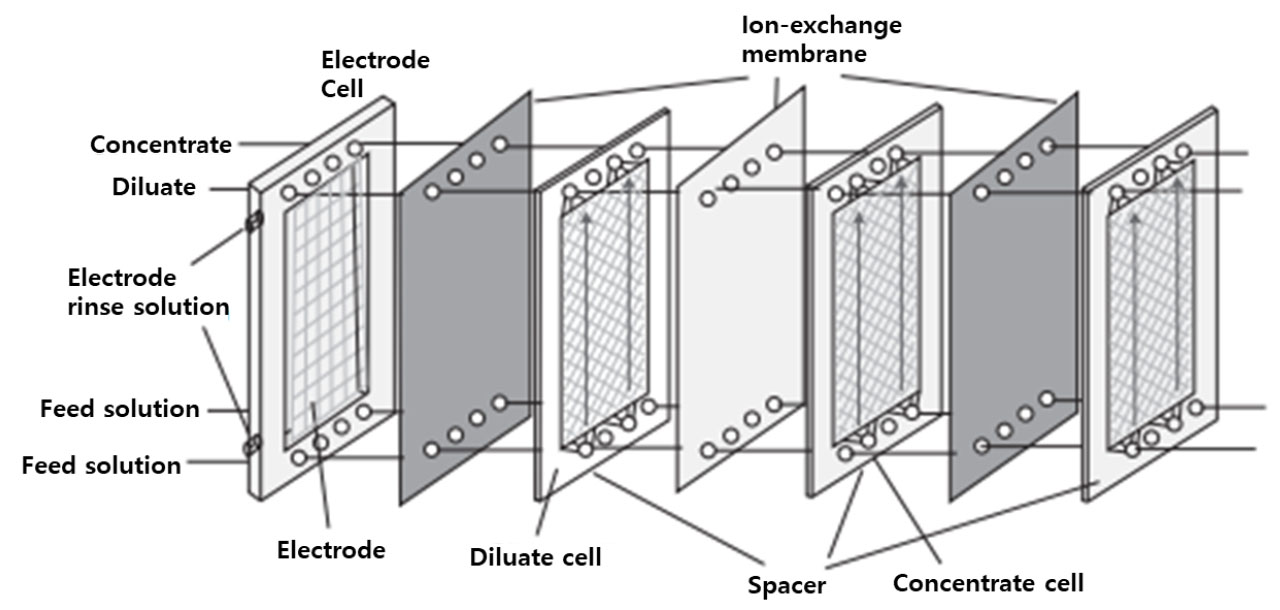
전기투석 장치의 핵심은 스택이라 할 수 있는데 그 구조는 Fig. 4와 같다. 양단의 지지판 안쪽에 전극이 있고, 이어서 전극액을 순환시키는 전극실이 있으며 전극액은 전극에서 일어나는 산화환원 반응에 필요한 이온을 포함하고 있다. 전극실 안쪽으로 양/음이온교환막이 교대로 배열되면서 농축실과 희석실이 연속적으로 구성된다. 양/음이온교환막 사이에는 적절한 유로를 형성시키기 위해 스페이서가 있는 개스킷을 배열하게 되고 이렇게 형성된 공간에 전해질 용액이 통과하게 된다. 일반적으로 수십에서 수백장의 양/음이온교환막 셀이 한 스택 내에 구성된다. 셀의 두께가 증가함에 따라 용액의 저항이 증가하기 때문에 가능하면 막간거리는 얇게 설계해야 하며 상용화 설비에서는 0.5~2.0 mm의 두께로 제작된다. 전극과 끝에 위치한 막사이의 간격은 10 mm 정도이고, 스페이서는 각 이온교환막 사이에서 막을 지지하고 흐름의 고른 분산을 위해 사용되며 두께는 0.42–10 mm이며, 막 과 스페이서 사이에는 개스켓이 설치되어 있으며 두께는 약 1 mm이다. 전기투석 공정 설계에서 용액의 혼합과 최소압력 조건에서 고른 유로 분포가 이루어지기 위해 스페이서는 중요하다. 대부분의 전기투석 스택은 난류(tortuous flow)와 평판유로(sheet flow)로 구분할 수 있다9,25). 난류의 속도는 15~50 cm/s, 평판유로는 5~10 cm/s 정도이다. 한 스택 내에서 막의 수가 많아지면 막의 기계적인 지지가 어려워지고 용액의 누출 가능성이 높아지므로 30~50쌍의 막을 소단위로 구성하여 분리판을 중간에 설치하게 된다. 전기투석 장치는 스택 부피당 최대 유효막 면적이 설치되어야 하며 각 실의 용액 흐름이 고르게 이루어 질 수 있도록 해야 한다. 스택은 대부분 평판형으로 제작되지만 나선형 전기투석 장치도 제안되었다26). 전극의 재질은 314 스테인레스강, 티타늄, 백금 코팅된 티타늄, 산화루테늄 코팅된 티타늄, 이리듐 코팅된 티타늄, 백금 코팅된 이리듐, 티타늄과 루테늄 산화물(70RuO2/30TiO2)이 코팅된 티타늄 또는 graphite 등이 사용된다.
전기투석공정을 설계 시에는 이온교환막의 특성, 에너지소비, 처리용량, 유입수의 조건, 이온의 제거효율, 농축액의 처리 등을 고려하여야 한다24). 초기 투자비용은 전기투석 스택, 펌프, 전기설비, 막 등 감가상각 설비와 토지, 임금 등 비감가상각비 등으로 구분될 수 있다. 이에 비해 운전비용은 에너지소비 비용과 액체이송(pumping) 비용 등이 있다. 액체이송 비용의 경우는 용액의 농도와 무관하지만 에너지 소비는 회수율 및 온도 등에 따라 달라진다. 일반적으로 전류밀도가 증가함에 따라 에너지 비용은 증가하지만 막 면적은 감소한다. 따라서 초기 투자비용, 에너지 비용, 운전비용을 합한 총비용이 최소가 될 수 있는 전류밀도를 설정해야 한다. 일반적인 전기투석 공정의 전류밀도는 용액의 전기전도도에 따라 10~100 mA/cm2 범위에서 결정한다. 또한 전기투석 공정의 유입수의 염농도가 증가할 수 록 제거할 이온의 양이 많아지고 전력소모가 증가하기 때문에 운전비용이 높아진다. 전기투석에 적용되는 가장 경제적인 염농도는 약 500 mg/L이다. 염농도가 증가함에 따라 비용이 현저히 증가하기 때문에 5,000 mg/L 이상의 농도 조건에서는 전기투석 보다는 역삼투(Reverse Osmosis)가 경제적인 공정이며, 100,000 mg/L 이상의 고농도 조건에서는 증발법(evaporation)이 효과적인 공정으로 알려져 있다. 그러나 탈염공정의 선정은 에너지 소비 외에도 농축액의 활용, 설치의 용이성, 장치의 유지관리 등을 동시에 고려되어야 한다. 한편, 이온교환막 공정의 문제는 막의 Fouling 현상으로 인하여 전기저항이 증가하고 나아가 막이 손상되는 현상이 나타날 수 있다는 점이다. 이러한 요인으로는 부유물질이나 용해된 고형물질이 원인이 되거나 유기물이나 무기화합물, 침전물 등도 원인이 될 수 있다27). 이러한 현상을 저감시키기 위해서는 전처리를 하거나 스택 청소를 하면 일부 가능하다. 주기적으로 역전기를 걸어주는 EDR(electrodialysis reversal)법25)이나 펄스를 걸어주는 PET(pulsed electric field)법28,29)이 이러한 fouling 현상을 해결하기 위해 고안되었다.
3. 바이폴라 전기투석(Bipolar Membrane Electrodialysis : BMED)의 원리 및 구성
3.1. 바이폴라 전기투석(BMED)의 원리 및 특징
바이폴라 전기투석(BMED)은 양/음이온교환막으로 구성된 탈염용 전기투석 공정에 물을 분해하여 수소이온(H+)과 수산화이온(OH−)을 생성할 수 있는 바이폴라막(BM)을 도입한 공정으로 바이폴라막의 구조 및 원리는 Fig. 5와 같다9). 바이폴라막은 양/음이온교환막을 결합한 새로운 형태의 막으로 전기장 하에서 촉매반응에 의해 물 분해 반응을 촉진시켜 H+ 와 OH-를 생성하는 기능을 가지고 있다. 바이폴라막은 고분자 양/음이온막을 접합시켜 제조하고 물분해가 일어나는 양/음이온교환막 사이(transition layer)의 간격은 약 4-5 nm이다. 이론적으로 바이폴라막을 통해 1 mol/L의 산과 알칼리 수용액이 접하는 경우 ΔpH는 14이며, 25℃에서의 이론적인 물분해 전압(ΔE) 및 Gibbs자유에너지 변화(ΔG)는 각각 ΔE=0.83 V, ΔG =0.022 kWh/mol이다. 이 경우 물 분해에 필요한 전압 0.83 V는 전기분해시 물의 이론분해전압인 1.23 V에 비해서 작으므로 이론적으로는 저에너지로 산∙알칼리를 제조할 수 있어 고효율로 물을 분해하여 H+ 와 OH−를 생성할 수 있다는 것이 바이폴라막의 최대 특징이라 할 수 있다.
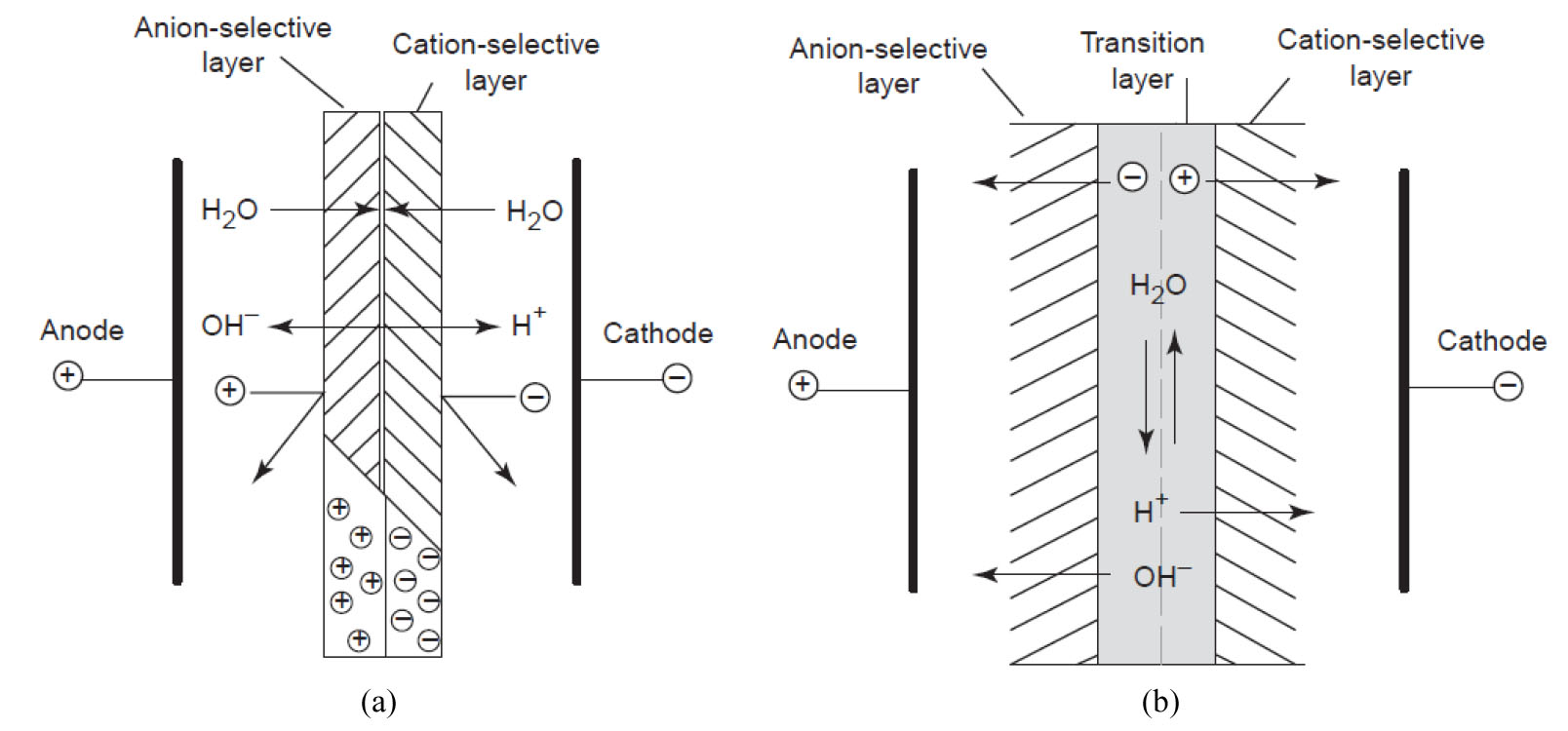
Fig. 5.
Schematic diagram illustrating the function of a bipolar membrane showing (a) a bipolar membrane and (b) the 4–5 nm thick transition region at the interphase of the two cation and anion exchange layers9).
BMED공정의 디자인은 기존의 전기투석의 탈염공정과 비슷하나 큰 차이점은 스택 구성과 물 분해를 위한 부가적인 에너지가 필요하다는 점이다. Fig. 6에 BMED 시스템을 나타내었다. 바이폴라막은 물 분해에 의해 생성되는 H+ 및 OH-에 의해 산과 염기가 생성되기 때문에 염용액을 산/염기로 변환하여 회수하는 시스템으로 사용이 가능하다. 이러한 BMED 기술의 특징은 다음과 같다. (1) 저전압에 의한 물분해 (2) 부산물 미발생 (3) 무기산염 및 유기산염으로부터 산과 알칼리를 한 공정으로 생산이 가능 (4) 산 및 알칼리의 농도 조절 가능 (5) 전해처리와 달리 모든 단일 셀에 전극이 필요하지 않으므로 가스 발생이 적음 (6) 폐수 발생량이 현저히 감소하여 폐수 무방류 공정 가능 (7) 이온교환수지공정에서와 같은 재생공정이 필요 없어 장시간 연속운전이 가능 등이다. 그러나 상기 장점이 있는 반면에 주요 단점으로는 (1) 전해질 농도와 전류 밀도의 한정 (2) 생성되는 산 및 염기에 염 혼입 현상 (3) 운전온도의 제한(40℃) (4) 물 또는 CO2에 의한 balloning 현상 등을 들 수 있다. 현재까지 BMED 기술은 많은 장점이 있어 꾸준한 연구가 진행되었지만 상용화 사례는 많지 않고 Lab scale 규모의 연구가 많이 진행되었다. 향후 상용화를 위한 Scale-up 시 G. Pourcelly는 다음과 같은 사항을 고려해야 한다고 하였다30). 첫째는 폐수(액)의 순도이다. 폐수 중 방향족 화합물이 있는 경우에는 이온교환막 및 바이폴라막이 팽창할 수 있고, 2가 양이온이 존재할 경우에는 막에 금속 수산화물이 침전되어 효율을 감소시키는 요인이 된다. 이 경우에는 용액의 전처리가 필요하다. 둘째는 회수되는 산/염기의 농도이다. 음이온교환막을 통한 양성자 누출로 인하여 생성되는 무기산의 최대 농도는 2~3 N이고, 유기산의 경우는 5 N이다. 또한, 양이온교환막을 통해 수산화물 이온의 누출로 인하여 생성되는 염기의 최대 농도는 4.5 N 정도이다. 셋째는 기본 셀 당 전압 강하는 1,000 A/m2에 대해 1.5~3.0 V 범위에서 유지되어야 하며, 인가 전류밀도 범위는 500~1,000 A/m2이어야 한다. 넷째, 염용액의 농도가 감소함에 따라 전기전도도가 감소하여 효율을 떨어뜨리는 요인이 되기 때문에 염농도 감소에 따른 최소 전기전도도는 40℃에서 20 mS/cm 정도 되어야 한다. 마지막으로 유기염(organic salts)의 전환율은 95~98%이어야 한다. 상기 요건들을 고려할 경우 BMED의 scale-up은 어렵지 않으며 대부분의 경우 실험실 규모 BMED의 작동 조건을 상업적 규모로 재현할 수 있다.
3.2. 셀(Cell) 구성에 따른 특징
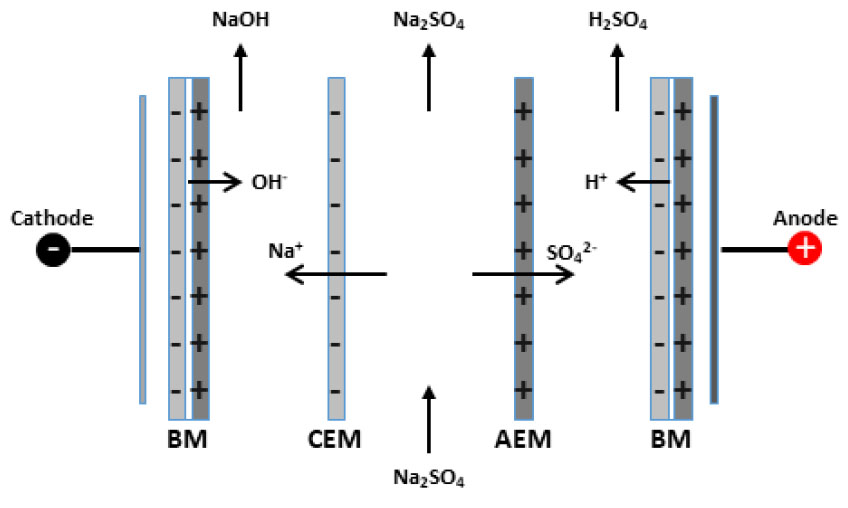
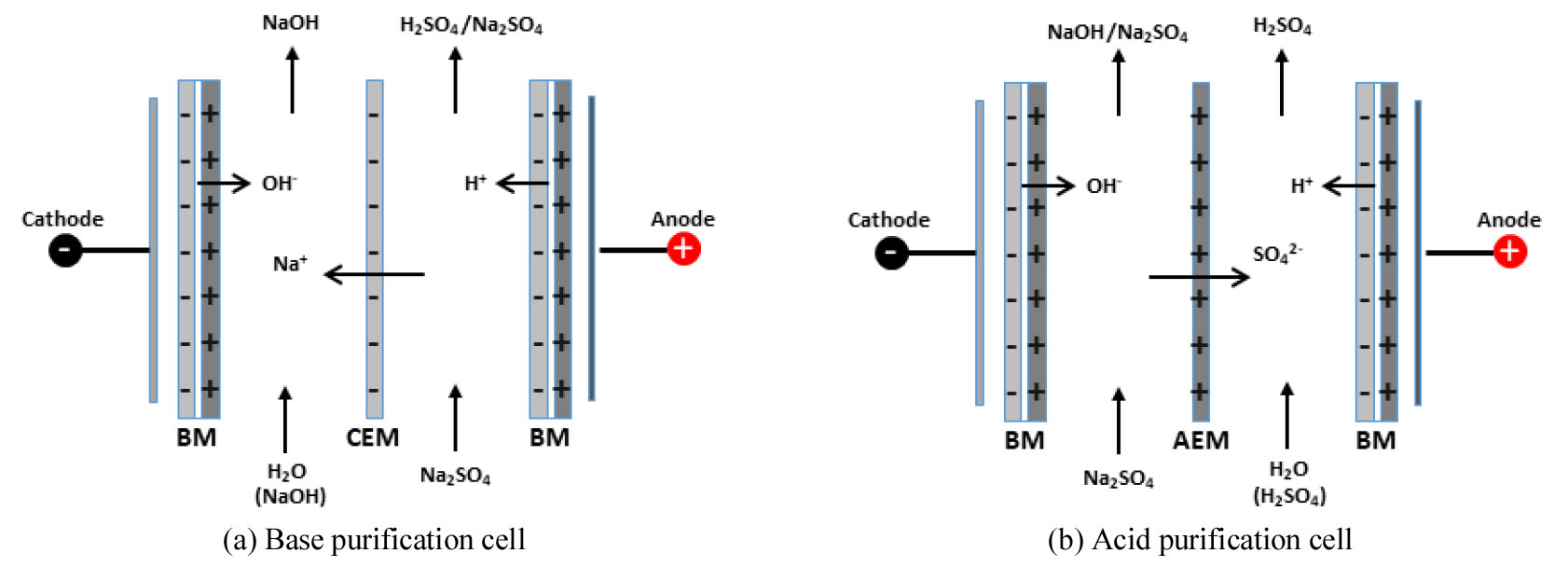
염(salt)으로부터 산과 염기를 제조할 수 있는 BMED공정은 산, 염기 그리고 염용액 흐름이 독립적으로 반복되는 3실(3-compartment) 구조를 갖는 것이 일반적이다. 3실-BMED에 의해 Na2SO4로부터 H2SO4와 NaOH가 생성되는 원리는 Fig. 6과 같으며 주로 고순도의 산과 염기를 동시에 생산하기 위한 공정에 적용된다13,31,32). 그러나 BMED공정의 cell 구조는 염의 종류와 응용목적에 따라 바이폴라막과 음이온교환막을 조합한 BM/AEM과 바이폴라막과 양이온교환막을 조합한 BM/CEM으로 구성된 2실 구조가 가능하고, 나아가 4실 구조도 가능하다고 할 수 있다. 2실 구조는 Fig. 7과 같이 2실-BM/CEM 형과 2실-BM/AEM 형으로 구성된 cell을 사용한다. 2실-BM 구조는 재생되는 산이나 염기 중 하나는 순수한 물질로 회수가 가능하나 다른 하나는 초기 투입염(feed salt)이 혼합된 상태로 회수되기 때문에 순수한 상태로 얻을 수 없다. 예를 들어 2실-BM/CEM 형의 경우는 Fig. 7(a)와 같이 강염기를 포함한 염에서 순수한 염기가 회수 가능하고, 2실-BM/AEM 형의 경우는 Fig. 7(b)와 같이 강산을 포함한 염에서 순수한 산을 회수할 수 있다. 2실-BM법의 경우 구조면에서 덜 복잡하고, 투자비와 공정비용면에서 경제적이기 때문에 효과적인 경우도 있는데, 주로 약산과 약알칼리의 염으로부터 유기산과 유기염을 회수하는데 주로 이용되고 있다.
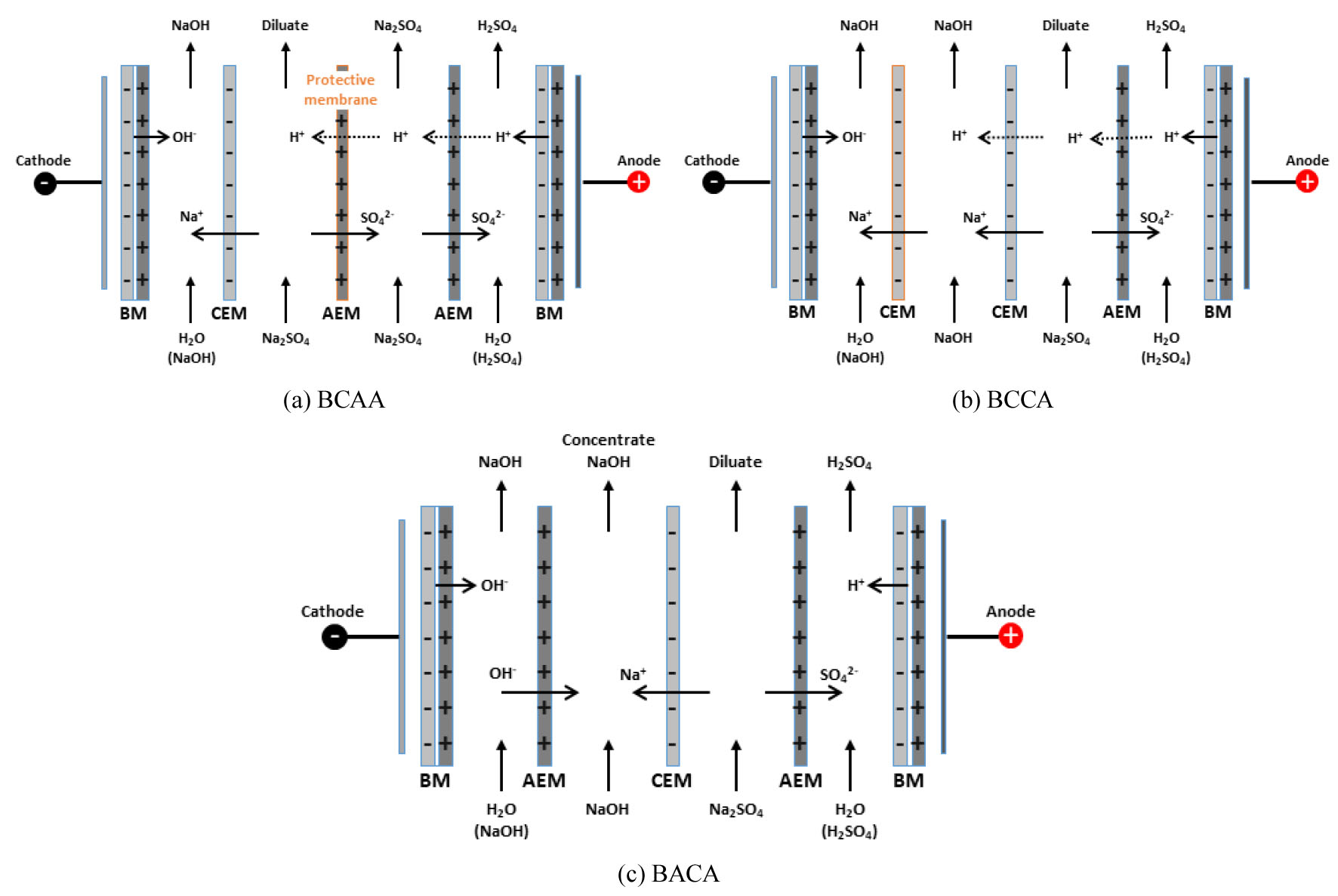
4실-BMED 구조의 경우는 Fig. 8과 같이 기본 3실-BMED 형태에 양이온교환막이나 음이온교환막을 추가 도입한 형태로 Kroupa, J. 등이 제안하였다33,34). Fig. 8(a)는 3실-BMED 구조에 음이온교환막을 추가로 설치된 BCAA구조이다. 이 경우에는 H+ 이온의 이온 반경이 작아 음이온교환막을 통과하여 생성된 NaOH용액 중 OH- 와 반응하여 물을 생성하여 NaOH 농도를 감소시키는 요인이 되기 때문에 음이온교환막의 추가 설치하여 H+ 이동을 방해함으로써 기본 3실-BMED에 비하여 NaOH 농도 증가가 가능한 구조이다. Fig. 8(b)는 기본 3C-BMED 구조에 양이온교환막이 하나 더 설치된 BCCA 구조로 NaOH를 생성하는 실이 하나 더 추가되면서 생성된 NaOH가 H+ 이동을 방해함으로써 NaOH의 농도를 증가시키는 역할을 한다. Fig. 8(c)는 기본 3실-BMED 구조에 음이온교환막이 더 설치된 BACA구조로 추가로 설치한 음이온교환막이 이온 이동의 방해 역할을 하지는 않지만 NaOH농도를 증가시키는 보조 역할을 할 수 있다. 그러나 상기 4실법의 경우는 생성되는 NaOH 농도를 증가시킬 수는 있으나 장치비 및 공정운영비가 증가한다는 단점이 있다.
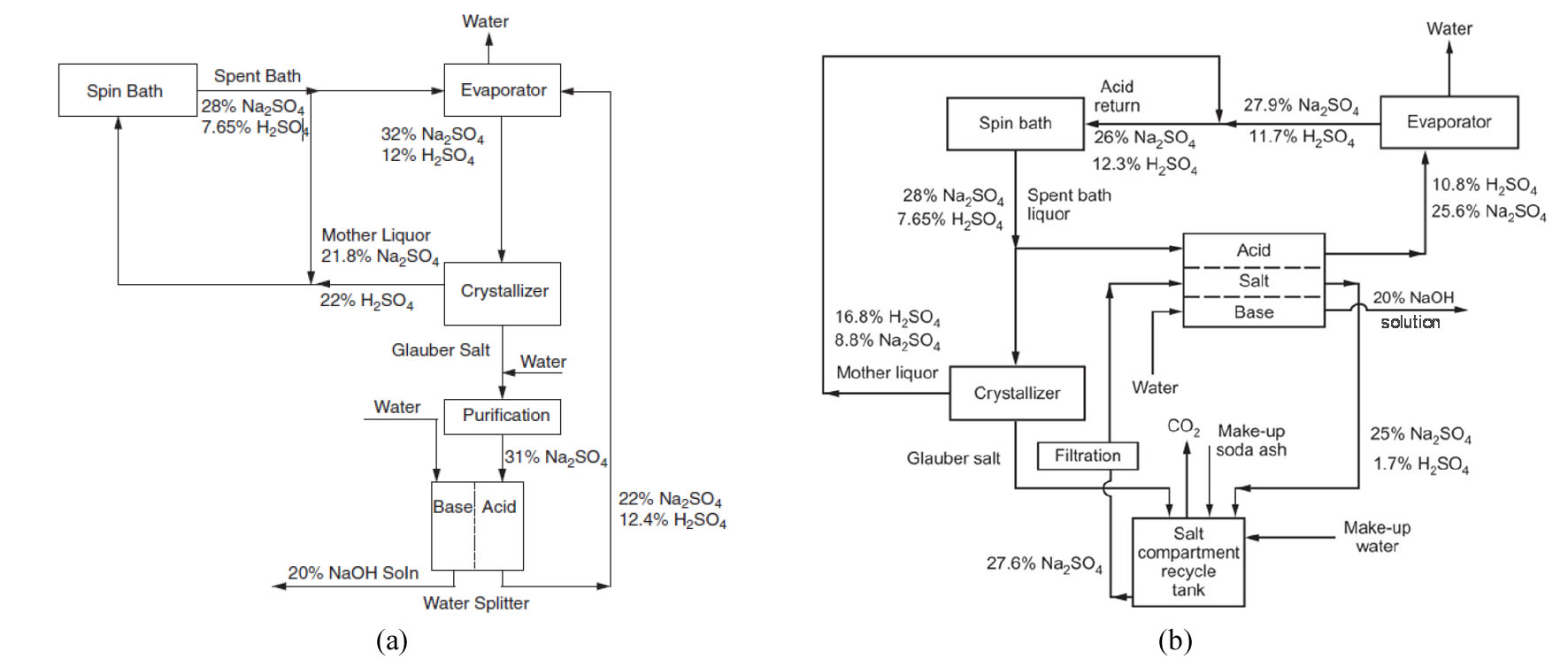
이러한 cell 구조는 염의 종류, 회수되는 산 및 염기의 순도, 에너지 효율, 경제성 등을 고려하여 적적한 형태로 구성하여 사용할 필요가 있고, 그동안 여러 연구자 들에 의해 다양한 응용 분야에 대한 연구가 소개되어 있는데 특히 Na2SO4 처리에 적용하기 위한 연구 사례를 소개하면 다음과 같다. Mani, K.N. 등은 Fig. 9와 같이 Rayon 제조공정에서 발생되는 황산폐액을 1차 처리하여 발생한 약 31% Na2SO4용액에서 Aquatech사 2실-BM/CEM를 사용하여 20% NaOH용액과 H2SO4/Na2SO4 혼합 용액으로 회수하는 연구와 3실-BMED 를 사용하여 순수한 H2SO4용액과 NaOH 용액으로 회수하는 연구를 실시한 후에 두 공정의 경제성 분석을 하였다. 이 경우 Cell stack의 수명은 약 2년 정도이고 공정비용으로 가장 중요한 요소는 전력비와 Cell 유지비라고 설명하였다35,36).
D. Raucq et al. 등도 Na2SO4 용액에서 H2SO4와 NaOH를 재생하기 위해 3실- ED 와 2실-BMED 공정을 비교하였다37). 이 두 공정에서 양이온교환막을 통한 나트륨 이온의 이동과 관련된 전기삼투현상이 생성된 염기(NaOH)의 농도를 좌우한다고 설명하고, 두 공정 모두 Co-ion의 누출현상이 전류효율을 감소시키는 요인으로 작용한다고 설명하였다. BMED 연구 결과를 통해 1 mol/L Na2SO4 (2 L)에서 4 mol/L NaOH(0.25 L) 와 3.5 mol/L H2SO4 (0.25 L)를 각각 95% 순도로 생성이 가능하다고 보고하였다. 한편, BMED와 ED 공정을 비교한 결과, BMED 공정이 전류효율면에서는 우수하나, 투자비면에서는 고가인 바이폴라막의 사용으로 인하여 불리하다고 하였다. M. Paleologou 등은 Na2SO4 용액에서 NaOH 와 H2SO4로 회수하기 위해서 2실-BMED를 사용할 경우는 전류효율이 40% 정도로 전류효율 60%인 3실-BMED보다 낮아 이에 대한 개선 방안을 제시하였다38). 2실-BMED의 경우는 염/산 혼합실에서 유리산(free acid) 농도가 증가하여 양이온교환막을 통과하려는 Na+ 및 H+ 이온의 경쟁으로 인하여 NaOH를 생성하는 전류효율에 부정적인 영향을 미친다고 하였다. 따라서 전류효율을 증가시키기 위한 방안으로 Feed용액의 sodium salt 농도를 증가시켜 염/산 혼합실에서 [free H+]/[Na+] 비율을 감소시켜 Na+농도를 증가시키거나 또는 염/산 용액실에 약한 염기를 첨가하여 산과 반응하게 함으로써 [free H+]/[Na+] 비율을 감소시켜도 비슷한 효과를 기대할 수 있다고 제안하였다. Harato T 등은 고실리카 보오크사이트 잔사로부터 황산침출을 통해 발생되는 Na2SO4용액에서 NaOH와 H2SO4를 회수하여 침출공정으로 재사용하기 위해 2실- BMED와 3실-BMED에 대한 비교 연구를 실시하였다39). 연구 결과, 초기 Na2SO4농도가 250 g/L인 경우 2실-BMED를 사용하여 160 g/L NaOH 농도로 회수가 가능한데 이때 전류효율은 50% 이상이었고 전기소모량은 NaOH 1톤 생산시 약 1500 kwh정도라고 하였다. 그리고 3실-BMED 보다는 2실-BMED을 사용할 경우 투자비 및 운영비면에서 경제성이 있다고 분석하였다. Y. Wei et al. 등은40) 염기성 폐수(spent caustic) 처리를 위해서 2실- BM/AEM형 cell을 사용할 경우에는 순도가 높은 NaOH를 얻기가 힘들기 때문에 2실-BM/CEM형으로 변경하여 연구를 실시하였다. 이 경우 전류밀도 30~60 mA/cm2에서 NaOH 회수가 가능하고, 약 2시간 정도 반응 후에 폐수로 부터 0.11 mol/L NaOH를 얻을 수 있었으며 1 kg NaOH를 회수하는데 약 0.97 US$의 공정비가 소요되어 비교적 경제성 있는 공정이라고 분석하였다. 또한 2실-전기투석(ED)과 2실-BMED 공정을 비교하였는데, 2실-BMED/CEM을 사용할 경우 2실-ED/CEM 보다 염기 회수율 및 전류효율 면에서는 우수하나, 공정운영비는 1.0 kg NaOH를 생산시 BMED의 경우는 0.97$이고, ED의 경우는 0.86$로 ED법이 다소 유리하다고 하였다. 그러나 향후 BM 가격이 하락하고 친환경적인 공정이 강조될 경우에는 BMED법이 더 유망할 것으로 분석하였다41). Kroupa et al. 등은 Na2SO4 폐액에서 3실-BMED를 사용하여 NaOH와 H2SO4으로 회수하는 연구를 통하여 바이폴라막의 투과성 및 선택성이 제품의 순도를 결정하는데 중요하고, 단일막의 선택성은 회수되는 제품의 농도와 관련이 깊다고 설명하였다. 또한 고농도 NaOH(30 g/L) 및 저농도(15 g/L 이하) 황산으로 동시 회수할 경우에 에너지 효율이 높았고, 회수 황산의 농도를 증가시킬 경우에는 에너지 소모가 급격히 증가한다고 하였다. 또한 온도 및 유량을 증가시킬 경우에는 에너지 소모가 감소한다고 발표하였다33). 또한 후속 연구에서는 4실법을 제안하고 3실법과 비교 연구를 실시하였다. 조성이 35 g/L Na2SO4 인 Feed용액을 3실-BMED(BCA구조) 사용할 경우에는 약 8시간 실험 후 H2SO4 60 g/L 및 NaOH 46 g/L을 회수할 수 있었다. 그러나 4실-BMED를 사용할 경우에는 회수되는 H2SO4 의 농도는 비슷하지만 NaOH 농도를 58 g/L까지 증가할 수 있다고 보고하여 4실을 사용할 경우 염기의 농도가 증가한다는 연구 보고를 하였다42). Kuldeep 등은 BMED의 효율은 사용한 막 및 폐액의 특성 그리고 온도와 깊은 관계가 있으며 특히 확산계수, 점도 및 유속 등에 영향을 미칠 수 있는 온도 증가가 효율을 개선시킬 수는 중요한 요인이라고 제시하였다. 그러나 고온에서 조업시 투자비나 운전비용 증가 그리고 막의 이온선택성 감소 및 막 성능 감소 현상 등이 있어 신중히 결정해야 할 사항이라고 하였다. 또한 Na2SO4 용액에서 산과 염기 회수를 위하여 3실-BMED에 대한 연구 결과, 양이온교환막을 통한 OH-의 누출보다 음이온교환막을 통한 H+의 누출이 크기 때문에 산 회수실에 비해 염기 회수실에서 전류효율이 더 높은 현상을 보였고, 2.6 V/cell, 500 A/m2, 41℃에서 회수된 NaOH 및 H2SO4의 순도가 95% 이상이라고 발표하였다43).
3.3. 폐수무방류 시스템에 적용사례
최근에는 BMED공정과 조합하여 Na2SO4가 함유된 폐수로부터 NaOH산/H2SO4 재활용은 물론 투석액을 공정수로 재사용하는 폐수무방류(Zero Liquid Discharge : Z.L.D.) 시스템에 대한 관심이 높다. Kincl 등은 Na2SO4가 함유된 우라늄 광산 폐수(Mine water)를 무방류 처리하고자 연구를 실시하였다11). 전처리 공정으로 기존의 증발농축(EV) 대신에 ED공정을 거쳐 폐수를 농축시킨 후 농축된 Na2SO4용액에서 BMED공정으로 NaOH와 H2SO4로 회수하여 공정 중에 재사용하고, 투석액은 RO공정을 거쳐 방류수를 최소화하는 연구를 실시하였다. Pilot 규모의 3실-BMED를 사용한 연구 결과, 전처리하여 농축된 4 wt% Na2SO4 용액에서 1.5% H2SO4 및 4% NaOH를 얻을 수 있었고 순도는 약 80% 정도이었다. 이때 얻어진 NaOH는 바로 공정에 재사용하고, 황산의 경우는 ED 공정을 거쳐 10% 황산으로 회수가 가능하였다. 이 경우 전류밀도는 350 A/m2, 전류효율은 62%, 이때 에너지 소모는 1 kg Na2SO4 처리 시 약 2.0 kWh이며, 운전비의 88%는 전력비라고 분석하였다. Gao, W. 등은 Fig. 10과 같이 Li2CO3 제조 공정 시 발생되는 Na2SO4 폐수로 부터 무방류 처리를 위해 3실-BMED를 사용하였다44). 공정변수로 초기 염농도, 전류밀도, 상비(volume ratio), 유량에 대한 영향에 대해 고찰 하였다. 자체 제작한 BMED stack을 사용하였는데 stack은 6개의 BM과 각각 5개의 양/음이온교환막 으로 구성되었고 유효 막면적은 189 cm2이었다. 그리고 극간거리는 0.7 5mm이고 막은 일본의 Tokuyama 회사 제품을 사용하였으며 전극은 루테늄을 코팅한 티타늄을 사용하였다. 연구결과 최적 조건으로 초기 공급 염농도는 0.2–0.3 mol/L, 전류밀도 30 mA/cm2, flow rate 500 ml/min., 상비(volume ratio)는 1:2로 제시하였다. 이때 회수된 황산 및 가성소다의 순도는 각각 98.32% 와 98.23%이었다. 경제성 분석 결과 1 kg Na2SO4를 처리할 경우 0.705 $가 소요되어 경제적 및 환경적 측면에서 효과적인 공정이라 제안하였다.
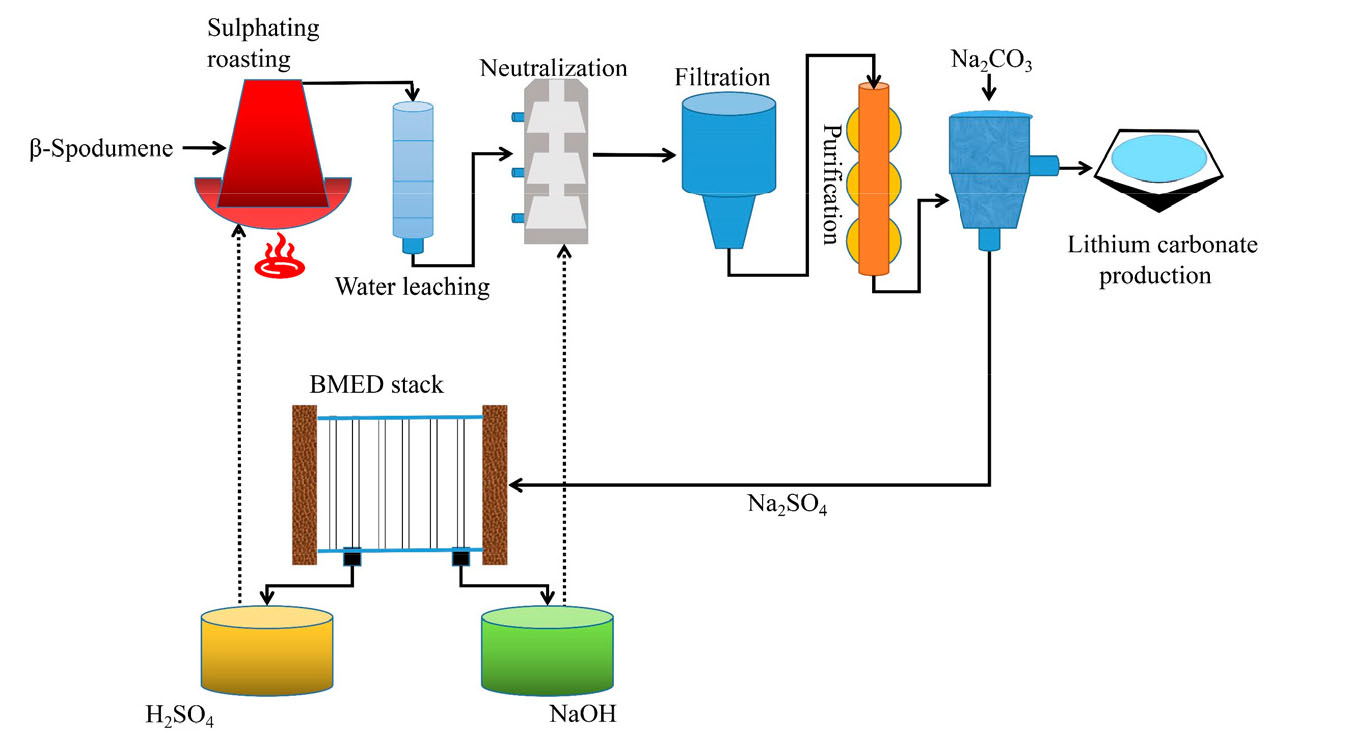
Fig. 10.
A flow chart of the preparation of lithium carbonate by acid roasting and bipolar membrane electrodialysis (BMED) technology44).
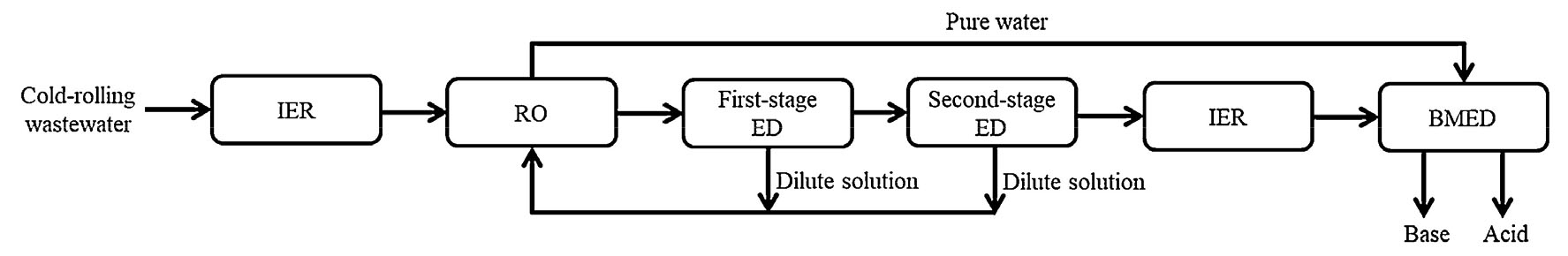
Bruinsma 등은 비철제련공장에서 발생하는 0.7 M Na2SO4 용액으로부터 NaOH 와 H2SO4을 회수하고 투석액을 공정수를 재활용하기 위하여 연구를 실시하였다1). Bench scale 규모의 3실-BMED 모듈을 사용하여 전기삼투, 전류밀도, 전류효율, 염분해 속도, 에너지 소비 및 생성물의 순도 등 모듈의 효율에 영향을 미치는 요인들에 대하여 연구하였다. 연구결과, 1 kg Na2SO4를 처리 시 전기삼투 현상에 의해 3.17 kg H2O이 염용액에서 산/염기/공정수 로 투과되는 현상이 나타나나기 때문에 공정에 큰 영향을 미치지는 않는다고 하였다. 온도를 25℃에서 35℃로 올릴 경우에는 전류밀도와 염분해속도가 약 25% 정도 증가하는 효과가 있으나, 양이온교환막을 통한 proton leakage의 증가로 인해 전류효율은 100%에서 83% 까지 급격히 감소한다고 보고하였다. 이 경우 생성된 NaOH의 순도는 약 99%, H2SO4의 경우는 약 90% 정도로 공정에 재사용이 가능하고, 염(Na2SO4) 농도가 전기전도도를 좌우하기 때문에 고전류밀도를 유지하기 위하여 염 농도는 100~150 g/L가 적절하다고 하였다. 또한, 역삼투(DRO: Disk Reverse Osmosis))기술을 조합한 BMED-DRO공정을 통해 Zero brine solution 공정이 가능하다고 제시하였다. Jiang, G. 등은 cold-rolling 공정에서 배출되는 Na2SO4 폐수를 무방류 처리하기 위해 Fig. 11과 같이 RO-ED-BMED를 조합한 연구를 실시하였다45). 그림에서와 같이 발생폐수를 먼저 IXR(이온교환수지)를 거쳐 Mg2+, Ca2+ 등을 제거한 후에 RO 공정을 거쳐 1차로 염농도를 증가시키고 ED 공정을 거쳐 염농도를 2차 농축시킨 후에 최종 단계에서 BMED를 적용하여 산/염기/공정수로 회수하여 재활용하는 폐수무방류 시스템에 대하여 연구를 하여 그 가능성에 대하여 발표하였다.
Ming Zhu 등은 염분이 다량 함유된 Na2SO4 용액에서 폐수무방류 처리를 하고 생성된 염을 고부가화 하기 위하여 위해 5실-BMED를 제안하였다46). 공급액으로 폐수인 Na2SO4와 추가로 NH4Cl을 사용하여 BMED 공정을 거쳐 (NH4)2SO4, HCl 그리고 NaOH를 동시에 회수할 수 있는 연구를 실시하였다. 5-BMED을 적용하여 에너지 효율과 염/산/염기 전환율이 최적화 조건에 대해 조사하였다. 연구 결과 3-BMED에 의해 산/염기를 회수하는 것보다 약간의 에너지가 더 소모되며, 초기 0.8 mol/L Na2SO4에서 (NH4)2SO4(0.44 mol/L), HCl(1.03 mol/L) 그리고 NaOH(1.35 mol/L)을 얻을 수 있었는데 이때 전류밀도는 40 mA/cm2, 전환율은 96% 이상 그리고 에너지 소모는 Na2SO4 1 kg 당 약 2.961 kWh 이였다. Reig, M. 등은47) NaCl이 함유된 Na2SO4 폐수로부터 폐수무방류 공정개발을 하기 위해 SED(Selective Electrodialysis)와 BMED 기술을 조합한 공정을 제시하였다. 먼저 Na2SO4와 NaCl이 혼합된 염용액으로부터 선택적으로 음이온 1가와 2가를 분리할 수 있는 음이온교환막을 사용하여 1차적으로 SO42-와 Cl-를 분리하여 Na2SO4 와 NaCl로 분리하는 SED공정을 거친 후에, Na2SO4와 NaCl 염을 BMED공정을 통해 NaOH와 H2SO4 및 NaOH와 HCl로 회수하는 연구를 수행하고 효과적으로 폐수무방류 공정이 가능하다는 제안을 하였다. Anh T.K. Tran 등은48) 금속 회수 공정에서 발생되는 고농도의 칼슘 및 니켈 이온을 함유한 폐수로부터 유동화 펠릿 반응기와 BMED로 구성된 통합 시스템을 이용하여 산/염기의 재생을 위한 연구를 진행하였다. Fig. 12와 같이 유동화 펠릿 반응기를 통해 칼슘과 니켈 성분을 각각 74% 및 94.4% 정도 제거한 후, BMED을 사용하여 산/염기를 재생하고자 하였다. BMED공정의 전류효율은 산의 경우 69%, 염기의 경우 80%이었고, 에너지 소비의 경우는 초기농도 0.2 N, 60 mA/cm2의 전류밀도에서 산의 경우는 5.5 kWh/kg이었고 염기의 경우는 4.8 kWh/kg이었다. 장기간 실험을 통해 펠릿 반응기를 사용하여 전처리한 용액을 사용할 경우 양이온교환막 성능을 증가시켰고 산농도는 1.76 N 및 염기 농도 2.41 N 정도의 비교적 높은 농도로 재생이 가능하여 금속 회수공정에 재사용이 가능하여 산/염기를 재생뿐만 아니라 수질 오염을 줄일 수 있는 친환경 기술 이라고 소개하였다.
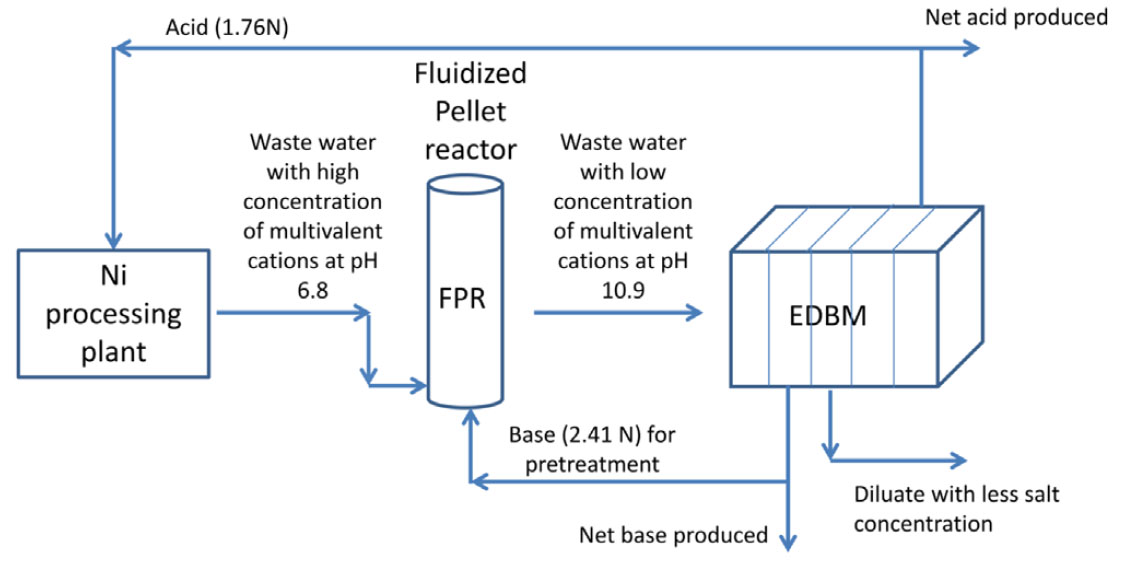
Fig. 12.
Scheme of an acid/base regenerating process by fluidized pellet reactor and bipolar membrane electrodialysis48).
4. 바이폴라막의 제조 기술 현황 및 전망
이온교환막을 막의 특성에 따라 크게 양이온교환막(CEM), 음이온교환막(AEM), 바이폴라막(BM, Bipolar Membrane)으로 구분할 수 있다. 양이온교환막은 음이온이 고정전하로서 양이온만을 통과시킬 수 있으며, 음이온교환막은 양이온이 고정전하로서 음이온만을 통과시킬 수 있는 막이다. 바이폴라막은 양/음이온교환막을 양쪽 측면에 결합한 형태로서 양/음이온을 모두 선택적으로 투과시킬 수 있다. 이온교환막은 막내에 연결된 전하를 띤 관능기의 종류/분포에 따라 균질(homogeneous), 불균질(heterogeneous) 교환막 등으로 구분하기도 하며 막의 소재에 따라 탄화수소 필름막 혹은 불소폴리머 필름막 등으로 구분하기도 한다. 양이온/음이온교환막의 제조 기술 및 제조 업체에 대해서는 이미 많이 알려져 있다32). 따라서 본 연구에서는 바이폴라막에 제조시 고려 사항 및 제조업체에 대해서 간단히 소개하고자 한다. 바이폴라막은 양/음이온교환막이 접합되어 있는 형태이기 때문에 단일 막의 제조에 비하여 고려해야할 사항이 많고 제조과정이 복잡하다49). 초기 전기투석용 바이폴라막은 단순히 양이온교환막과 음이온교환막을 겹쳐서 배열하는 스택 구조에 불과하였다. 그러나 이 경우에는 계면 사이 접촉면이 완벽하게 형성되지 않을 뿐만이 아니라 막간 거리가 멀어 물이 분해될 때 큰 전기 저항이 발생된다. 이러한 현상을 개선하기 위해 고분자 접착제를 사용하였지만 접착제 자체가 갖는 높은 저항성 때문에 현재는 잘 사용하지 않고 접촉면 형성과 물 분해시 발생하는 저항을 감소시키고자 중간층에 철, 크롬 이온과 같은 무기금속 촉매를 도입하는 방법이 연구되었다. 현재 대표적인 상업용 바이폴라막인 BP-1(NEOSEPTA 社)의 경우 양이온교환막을 제조 후에 저농도의 철 이온용액에 표면을 함침 시킨 후 한쪽 면의 세척, 건조를 진행하고 세척하지 않는 면에 음이온교환막의 고분자 용액을 캐스팅하여 막을 제조하는데 이 경우에 양/음이온교환막 사이에 미량 존재 하는 철 이온에 의하여 물 분해 성능이 크게 개선되는 것으로 알려져 있다. 이외에도 금속 촉매로 크롬, 티타늄, 루비듐, 팔라듐 이온 등이 물 분해시 발생하는 저항을 낮추는데 효과가 있는 것으로 보고되었다50). 또한 촉매층으로 고분자 물질인 폴리에틸렌글리콜51)이나 폴리비닐알코올(polyvinyl alcohol)을 사용한 바이폴라막도 개발되었다52). 이외에도 막의 형상 등을 변형시키는 기술도 제안되었는데 J. Balster 등은 바이폴라막의 두께를 비대칭적으로 제조할 경우 이온의 선택성이 증가하고 이온의 누출이 적어 고순도의 산과 염기의 생산이 가능하다고 하였다53).
앞에서 설명한 많은 응용 분야에도 불구하고 BMED 기술은 여전히 실험실 규모 또는 개발 초기 단계라 할 수 있다. 따라서 BMED의 효율 향상 및 새로운 응용 분야를 개척하기 위해서 많은 연구가 필요하며 R. Parnamae 등에 의하면 다음과 같은 특성을 갖는 BMED 기술이 필요하다고 하였다12). 첫째는 고 전류밀도에서 안정성이다. 고 전류밀도에 견디기 위해서는 기계적 안정성을 높이는 것은 중요하다. 일반적인 바이폴라막의 권장 전류밀도는 500–1000 A/m2(역방향 바이어스의 경우 >1000 A/m2) 이다. 고전류밀도를 견디기 위해서는 접합부의 접착력과 바이폴라막을 통한 물(H2O) 이동이 향상되어야 한다. 이 경우에는 막 두께 감소54)나 표면에 평행한 내부 통로를 가압/레이저 처리 또는 표면 주름 형성 등 막의 형상을 변형시켜 개선이 가능하다55,56,57). 또한 3D 접합이 있는 전기방사막은 역 바이어스 조건에서 최대 11,000 A/m2의 전류밀도를 견딜 수 있다58). 둘째는 열적 안정성 이다. 대부분의 상업용 바이폴라막은 최대 40℃에서 작동할 수 있다. 작동 온도가 높아지면 용액의 점도를 낮추고 에너지 소비를 줄이는데 도움이 되고 또한 물 해리도도 향상되기 때문에 60℃ 이상에서도 사용할 수 있으면 좋다. 이와 관련하여 무기재료를 유기 매트릭스에 같이 사용하면 열 안정성이 향상될 수 있다59). 셋째는 화학적 안정성 이다. 모든 바이폴라막은 넓은 pH 범위에서 화학적으로 안정하도록 설계되었지만, 고 알칼리성 조건(pH>11)에서는 음이온교환막이 문제가 될 수 있기 때문에 이에 대한 개선이 필요하다60). 또한, 유기용매(예: 메탄올, 에탄올)에서 화학적 안정성을 개선하면 응용이 확대될 수 있다. 넷째는 이온선택성 이다. 이온선택성을 증가시키면 모든 막 공정에서 유리하다. 산/염기 생산에 있어서 선택성은 특히 고농도 산 및 염기용액에서 이온 누출에 의한 제품의 오염을 초래할 수 있다. 이러한 이유로 대부분의 상업용 바이폴라막의 경우는 재생된 산/염기 농도가 1 M을 초과하지 않는다. 이에 대한 개선 방안으로 고도로 가교 결합된 막을 사용함으로써 막의 밀도가 향상되어 Donnan 배제에 대한 co-ion 이동을 감소시킴으로써 이온선택성이 개선될 수 있다. 오늘날 전 세계에는 많은 양이온교환막 및 음이온교환막을 생산하는 업체가 있으며, 이중에서 특히 바이폴라막을 제조하고 있는 업체들은 Table 2와 같다12). 또한 여러 업체에서 다양한 응용 분야를 위하여 상업용 BMED 장치를 제조 하고 있다. 대표적으로 Neosepta BP-1 바이폴라막은 일본 Astom사의 “Acilyzer BMED”에 사용되고 있으며, 무기산 및 염기 용액의 생산 및 회수, 유기산(글루콘산) 또는 아미노산 생산을 위해 BMED 장치가 상용화 되었다. 또한 Suez WTS사의 AR103BM은 pH 조절 및 약산 생산을 위한 2실-BMED와 염수 회수 및 강산 생산을 위한 3실-BMED를 상용화 하였다. Tosoh사의 바이폴라막인 B-17은 가성소다 생산을 위하여 BiTAC라는 BMED에 사용되고 있으며, 일본의 가성소다 생산 공장을 포함하여 전 세계 일부 공장에 사용되고 있다. 현재까지는 BMED 기술이 일부 산업에 적용되고 있으나 향후 다양한 분야로의 응용 확대가 기대됨에 따라 바이폴라막의 제조업체들이 늘어날 것으로 예상된다.
Table 2.
Overview of commercial bipolar membranes12)
5. 결 론
전기막(Electro-membrane) 기술은 전기투석(ED) 및 바이폴라 전기투석(BMED)과 같이 이온에 대해 선택적 투과성을 갖는 막을 이용하여 전기장 내에서 수용액 내의 물질을 분리·정제하는 공정이다. 전기막(Electro-membrane) 기술은 공정중에 부산물이 발생하지 않는 환경친화적 공정이며 화학물질의 추가 없이 조업이 가능한 장점을 갖고 있어 미래지향적인 공정으로 각광받고 있고, 최근에 세계적으로 관심사가 되고 있는 ESG(Environmental, Social and Governace) 정책과도 잘 부합된다고 할 수 있다. 또한 우수한 특성을 갖는 이온교환막의 개발로 인하여 기존의 역삼투(R.O.) 기술이나 나노필터(N.F.) 기술들과 조합한 폐수무방류(Z.L.D.) 분야에도 적용될 것으로 기대된다. 이에 따라 기존 전기막(Electro-membrane) 공정의 주된 응용 분야인 해수의 담수화나 탈염 공정 외에 토양 중의 중금속 제거, 각종 산업 폐수(폐기물)의 처리 등의 환경 분야에 응용이 확대되리라 기대된다.