1. 서 론
2. Coupled reaction 모델 기반의 종합 모델
2.1. Coupled reaction 모델(Robertson 등)
2.2. Multi-component kinetic 모델(Graham 등)
2.3. LF 모델(Harada 등)
2.4. Inclusion Evolution 모델(Kim 등)
3. 시뮬레이션의 예시
4. 결 론
1. 서 론
산업이 발달함에 있어 고품질의 철강 수요 증가로 인해 제강 공정에서 2차 정련의 중요성이 증가하고 있다. 제강 공정 중 2차 정련 공정은 수요자가 원하는 합금 조성을 충족시키기 위해, 합금 원소 첨가를 통해 조성을 제어하는 공정이다. 또한, 탈황 및 탈산 반응을 통해 강의 불순물 원소들을 슬래그로 흡수시키며, 강의 불순물들을 슬래그로 원활히 흡수하기 위해 로 하부에서의 가스 교반을 통해 용강의 온도 균일화 및 개재물 제거를 실시하는 공정이다1). 특히, 강의 탈산 제어를 위해 공정 중 탈산제를 첨가하며, 이때 탈산 생성물인 비금속 개재물이 생성된다. 생산된 철강의 품질은 비금속 개재물의 제어를 통한 청정도를 척도로 평가하며, 개재물 제어는 슬래그의 조성에도 영향을 크게 받는다고 알려져 있다. 또한, 2차 정련 중 비금속 개재물들은 황화물계 개재물과 산화물계 개재물의 형태로 발견된다2). 이러한 비금속 개재물들은 최종 철강 제품의 물리화학적 성질을 낮추어 제품 품질을 저하시키며, 고융점 개재물의 경우 노즐 막힘 현상을 야기하여 공정 문제를 초래하기도 한다3).
많은 종류의 비금속 개재물 중, 특히 MgO-Al2O3계 스피넬 개재물은 제강공정 중 매우 유해한 비금속 개재물로 알려져 있다3). 이전 연구자들에 의해 스피넬 개재물은 Al 탈산 생성물인 Al2O3 개재물과, 슬래그 및 내화물에서 용강으로 공급된 Mg의 농도가 증가함에 따라 생성되는 것으로 밝혀졌다4,5,6). 용강 중 Al2O3 개재물은 탈산을 위해 투입되는 Al의 탈산 반응에 의해 형성되지만7), 일부 비교적 부피가 큰 클러스터 형태로 슬래그로 흡수된다. 슬래그 중 흡수된 Al2O3 성분은 슬래그의 융점과 염기도에 영향을 준다고 알려져 있다8,9). 크기가 수십 μm 이하의 비교적 작은 Al2O3 산화물들은 슬래그로 흡수되지 못하고 용강 중 비금속 개재물로 존재할 수 있으며, 수에서 수 백 ppm의 단위를 갖는 소량의 비금속 개재물이 강의 물리화학적 성질을 저하시킨다. 한편, 황화물의 개재물의 경우, 개재물 주위에서 형성되어 스테인리스 강의 부식을 촉진한다는 보고가 있다10). MnS계 개재물의 경우, 스테인리스 강과 MnS 개재물 사이의 미세한 틈에서 황산염과 염화물의 임계농도 이상 조건에서 재부동태가 일어나지 않아 공식 부식의 원인으로 보고된 바 있으며11), 탈황을 위해 투입되는 Ca에 의해 형성된 CaS계 개재물은 부식에 영향을 미칠 뿐만 아니라 융점이 높아 주조성을 저해한다는 보고가 있었다12). 하지만 2차 정련 공정 중 시간이 흐름에 따라 용강, 슬래그 및 비금속 개재물의 조성은 변화하며, 이는 곧 공정이 평형 상태가 아님을 의미하기 때문에 공정 제어가 쉽지 않음을 시사한다.
비금속 개재물들을 슬래그로 부유하여 흡수, 제거하며 동시에 로 내의 온도 및 농도를 균일화하기 위해, 로 하부에서 Ar 가스를 취입한다. 2차 정련 공정은 연속 주조 전 마지막 공정이기 때문에, 연속 주조 공정에 적합한 용강의 온도를 유지하는 것이 중요하다13). 수 십 톤 이상의 실제 공정에서 이를 예측할 수 있는 모델은 공정 제어를 더욱 효율적으로 개선시킬 수 있다.
2차 정련 공정은 용강, 슬래그, 비금속 개재물, 내화물 및 합금 원소 간의 복잡한 반응을 비평형 상태에서 동시에 수반하기 때문에 일반적인 열역학적 평형 계산으로 시간변화에 따른 예측이 어렵다. 하지만 공정을 정밀히 제어하기 위하여 많은 이전 연구자들이 실험적 접근을 통해 공정에 대한 세부적인 메커니즘을 밝혀냈다2,3,4,5,6,7,8,9,10,11,12,13). 수 십 톤 이상의 실제 공정을 실험을 통해 제어하기에는 시간과 재화 등의 물리적 제한 사항이 따를 수 있기에, 많은 연구자들이 실험실 규모의 실험 결과를 통해서 도출된 각종 수식, 및 실제 공정의 결과를 바탕으로 공정 예측이 가능한 반응 속도(Kinetic) 기반의 시뮬레이션 모델을 발표하였다.
상기 시뮬레이션 모델들은 용강, 슬래그 혹은 비금속 개재물 등에 포함되어 있는 각 성분들의 물질 이동 속도를 고려하여 각 성분의 조성 계산이 가능하다. 공정 중 동시에 수반되는 각 반응들의 율속 단계를 고려하여 반응의 정도를 수치화할 수 있다. 하지만, 실험적 검증을 통해 도출된 각종 수식이 적용됐음에도, 현재까지 반응 해석 모델에는 각 공정에서 발생할 수 있는 반응들 중, 용강/슬래그의 반응, 비금속 개재물의 반응 등 지배적인 반응들만 수반되어 있기 때문에 조건의 스케일이 커짐에 따라 조업 규모 등에서는 정확한 수치 예측 방법에 대한 모색이 필요하다. 정확한 반응 예측을 위해 현재까지 발표된 2차 정련의 반응 해석 모델들을 검토하고 분석하여 추후 반응 모델들의 연구개발 방향을 정립할 필요가 있다.
본 연구에서는 더욱 정밀한 시뮬레이션 개발을 위해 지난 수십 년간 발표된 국내외의 2차 정련 시뮬레이션 모델의 중요 이론과 실험식을 검토하고 여러 모델의 특징을 분석하였다. 본 논문(part. 1)에서는 Coupled reaction 모델 기반의 종합 모델들의 이론을 소개하고, 반응 속도에 영향을 주는 물질 이동 계수에 대하여 여러 모델들의 접근 방법에 대하여 검토하였다. 후속 논문(part. 2)에서는 Coupled reaction 모델 이외의 2차 정련 종합 모델들에 대한 이론과 특징을 분석하였고, 공정 내 한 가지 반응에 초점을 맞춘 단일 반응 모델들을 소개하였다.
2. Coupled reaction 모델 기반의 종합 모델
본 연구에서 종합 모델은 용강-슬래그 간의 반응을 기초로, 합금 원소 첨가 반응에 대한 고려, 비금속 개재물의 형성 및 거동에 대한 고려, 내화물의 용손 반응에 대한 고려 등 여러 가지 반응을 동시에 수반하고 있는 모델을 의미한다. 본 절에서는 보고된 종합 모델들 중 현재에도 많은 분야에서 응용되어 사용되는 Coupled reaction 모델에 대하여 검토하였다.
2.1. Coupled reaction 모델(Robertson 등)
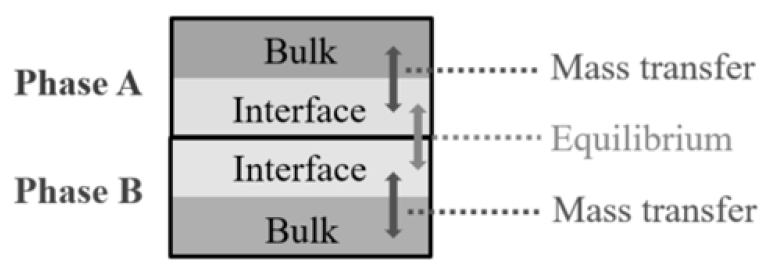
1984년 Robertson 등은 Coupled reaction 모델을 발표하였다14,15). 모델의 반응은 식 (1)에서부터 식 (6)까지로 표현되는 이중 경막 이론(Double film theory)의 수학적 모델을 통해 설명된다. 이 수학적 모델은 현재에도 인접한 상과의 반응을 고려하기 위해, 혹은 반응 계면에서의 산소의 활동도를 결정하기 위해 활용하고 있다16,17,18,19,20,21). Fig. 1은 이중 경막 이론의 모식도를 나타내고 있으며, 그림과 같이 하나의 상은 일정한 비율의 벌크 영역(Bulk zone)과 계면 영역(Interface zone)으로 나뉠 수 있다22). 만약 두 상이 인접하였을 경우 각 상의 계면은 접촉된 계면 영역으로 나타낼 수 있다. 반응이 일어나는 접촉된 계면 영역에서의 화학 반응 속도는 고온에서 매우 빠르기 때문에 평형이라고 가정할 수 있으며, 단일 상내 벌크 영역과 계면 영역의 물질 이동은 물질 이동 속도 계수 (Mass transfer coefficient) 에 의해 결정된다고 정의한다.
이중 경막 이론을 바탕으로 산화물인 슬래그와 금속과의 반응을 표현하면 다음과 같다. 식 (1)은 금속 성분 “M”에 대한 산화 반응식을 나타낸다. 식 (2)와 식 (3)은 각각 금속 상과 산화물 상 내 벌크 영역과 계면 영역에서의 농도를 나타낸다. 각 단일 상 내 벌크 영역과 계면 영역의 농도 변화는 식 (4)에 의해 물질 이동 계수를 사용한 몰 유속 밀도에 의존한다고 나타낸다. 식 (5)는 금속과 슬래그가 접촉한 계면 영역에서의 평형 반응을 고려하기 위한 평형 분배비를 나타낸다. 식 (6)은 시스템 내 모든 원소의 반응과 이동에 대한 질량 보존을 나타낸다.
식 (1)에서 식 (6)을 연립하여 계산하면, 단일 시점에서 각 상 내의 벌크 영역과 계면 영역 내 “M” 및 “MO”의 농도를 계산할 수 있다. 그리고 식 (7)과 (8)을 통해 벌크 영역과 계면 영역의 농도의 계산 값을 사용하여 시간 변화에 따른 농도 변화를 계산한다. Coupled reaction 모델은 시간에 따라 용강 및 슬래그의 각 성분의 농도 변화를 계산할 수 있는 반응 속도 모델이며, 물질 이동 계수 값은 시간에 따라 변화하는 벌크 영역과 계면 영역의 농도 변화를 계산하는 데 매우 중요한 의미를 지니고 있다.
Robertson 등이 발표한 초기 모델에서의 용강 중 물질 이동 계수의 값은 실험을 통해 얻은 값을 사용하였고, 용강과 슬래그 상의 물질 이동 계수 값의 비율은 kM/kS = 2로 결정하여 사용하였다14,15). 3 kg의 용강에 대한 실험 측정값과 계산 값을 비교하여 일치성이 높은 결과를 도출하였다.
2.2. Multi-component kinetic 모델(Graham 등)
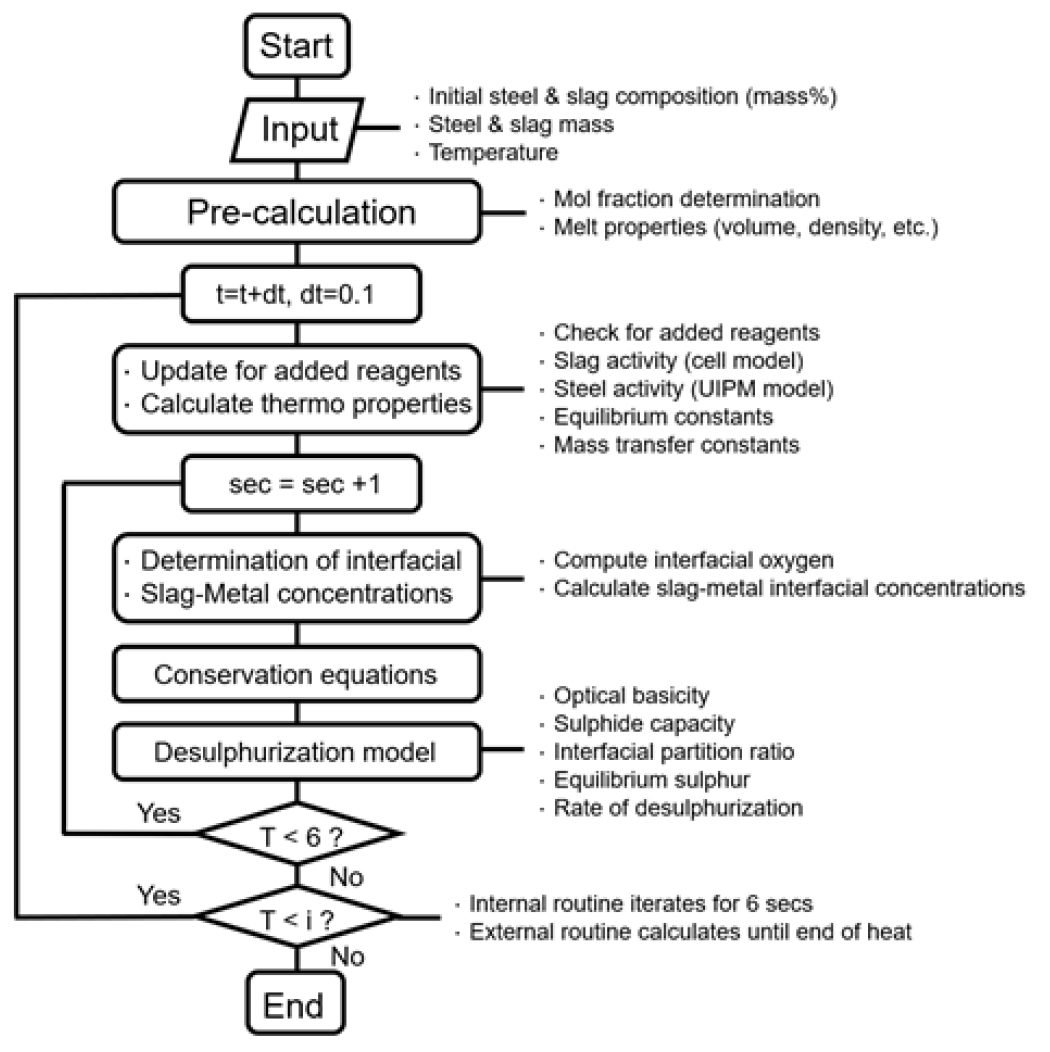
2008년 Graham 등은 Coupled reaction 모델을 응용한 Multi-component kinetic 모델을 발표하였으며, 용강과 슬래그간의 반응과 함께 용강 성분의 활동도를 고려한 상 안정도를 통해 개재물의 형태를 결정할 수 있다23,24,25). 또한 합금 원소 첨가를 고려하여 용강 및 슬래그 내 농도 변화도 고려되었다. Fig. 2는 모델 계산에 대한 알고리즘을 보여준다23). 계산에 사용된 열역학 데이터는 ArcelorMittal의 Chemical Equilibrium Calculation for the Steel Industry (CEQCSI) 소프트웨어를 사용하였다26). 용강 상의 활동도는 UPIM 모델을 사용하여 계산하였으며, 슬래그 상의 활동도는 Cell 모델을 사용하여 계산하였다. 용강의 물질 이동 계수 값은 Ladle 하부로 취입되는 Ar 가스의 유량으로 계산되는 교반 에너지를 통해 계산된다. 식 (9)는 Ar 가스 유량에 대한 교반 에너지를 의미한다. 계산된 교반 에너지를 식 (10)에 대입하여 물질 이동 계수를 계산하였고, 용강과 슬래그의 물질 이동 계수 비는 실험값과 비교하여 결정하였다. 모델의 계산 결과는 165 톤의 실제 조업 데이터와 비교하였으며, 계산값과 조업 데이터의 값이 잘 일치하였다. 또한, 용강-슬래그 반응 및 탈황 반응, 용강 내 각 성분의 활동도에 따른 개재물의 형태가 비교되었다.
2.3. LF 모델(Harada 등)
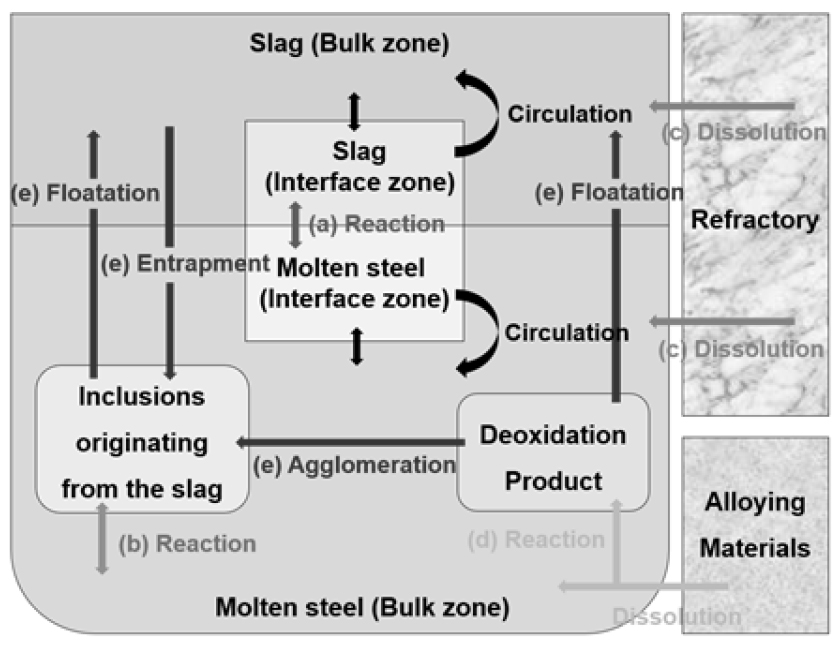
2013년 Harada 등은 Coupled reaction 모델 기반의 2차 정련 예측 모델인 LF 모델을 발표하였다27,28,29). 이전 발표된 Multi-component kinetic 모델과 비교하여, 추가적으로 내화물의 용강 및 슬래그로의 용손 반응이 고려되었으며, 비금속 개재물에 대한 부유, 응집 및 혼입 등의 세 종류의 거동이 고려되었다. Al, Fe-Mn 및 Fe-Si 등의 합금 원소 첨가에 의한 탈산 생성물과, Ar 가스 취입에 의한 용강 내 혼입되는 슬래그로부터 형성된 개재물의 형성 역시 고려되었다. 보고된 값으로 정해진 각 개재물의 거동 속도를 사용하여 Mg-Al 계, Ca-Al 계 및 Mn-Si 계 개재물의 양을 계산할 수 있다. Fig. 3은 모델에서 고려하고 있는 전체 반응을 모식도로 나타냈었다22). Fig. 3과 같이 LF 모델은 용강-슬래그의 반응(a), 용강-비금속 개재물의 반응(b), 내화물의 용강 및 슬래그로의 용손 반응(c), 합금 원소의 첨가반응(d) 및 슬래그로의 부유, 슬래그로부터의 혼입, 개재물간응집 등 비금속 개재물의 세 종류의 거동(e)에 대하여 고려하였다.
Fig. 3에서 반응 (a)와 (b)는 2.1절에서 언급한 이중 경막 이론을 사용하여 계산한다. 용강의 성분들은 금속의 상으로 정의되는 “M”으로 고려하며, 슬래그와 비금속 개재물의 상은 산화물의 상으로 정의되는 “MO”로 고려한다. 특히 용강 내 수 ppm의 Mg은 MgO∙Al2O3 스피넬 개재물의 형성에 영향을 미치기 때문에, 더욱 정밀한 용강 중 Mg의 농도를 계산하기 위해 MgO-C 기반의 내화물의 용강 및 슬래그로의 용손 반응 (c)를 식 (11)과 같이 고려하였다29). 식 (11)에서 Mg의 물질 이동 계수는 식 (12)로 계산된다. 식 (12)의 레이놀즈 수와 슈미트 수는 로 하부의 제원과 하부로부터 취입되는 Ar 가스의 유량에 따른 용강의 상승 속도 등의 계산을 통해 사용한다. 식 (11)을 통해 계산되는 용강 중 용손되는 Mg의 양과, 슬래그로부터 용강으로 환원되는 Mg의 농도를 토대로 MgO∙Al2O3 스피넬 개재물의 양을 계산하였다. 반응 (d)의 경우 용강으로 투입되는 합금 원소의 밀도를 고려하여, 용강의 하부에 투입되는 비교적 높은 밀도를 갖는 Fe 기반의 첨가 원소는 용강의 벌크 영역에, Al과 같이 비교적 낮은 밀도, 혹은 용강과 슬래그의 밀도의 사이 값을 갖는 첨가 원소에 대해서는 용강의 계면 등에 투입된다. 또한 세 종류의 비금속 개재물의 거동 속도 (e)에 대한 영향을 평가하였다29).
이중 경막 이론 계산에 사용된 열역학 데이터에 대하여, 용강 내 성분의 활동도 계수는 JSPS 데이터30)를 사용하였으며, 슬래그와 개재물로 표현되는 산화물 상 내의 활동도 계수는 열역학 데이터베이스 소프트웨어인 FactSage의 데이터31)를 통해 계산하였다. 용강 내 물질 이동 계수의 경우, 하부에서 취입되는 Ar 가스의 유량 및 Ladle의 조건을 사용하여 계산되는 교반 에너지로 정의된다. 식 (13)을 통해 교반 에너지를 계산하며, 식 (14)는 계산된 교반 에너지를 사용하여 계산되는 용강 내 물질 이동 계수를 나타낸다. 용강과 슬래그의 물질 이동 계수 값의 비율은 이전에 보고된 값인 kM/kS = 10으로 결정하여 사용하였다. 165 톤의 실제 조업 결과를 토대로 용강 및 슬래그의 농도 변화를 잘 예측하였으며, 생성되는 비금속 개재물 중 MgO∙Al2O3스피넬 개재물을 억제하기 위해 모델을 응용하였다.
2.4. Inclusion Evolution 모델(Kim 등)
2018년 Kim 등은 LF 모델을 기반으로 개재물의 진화에 초점을 둔 Inclusion Evolution 모델을 발표하였다32,33,34,35,36). 2차 정련간 용강, 슬래그, 비금속 개재물, 내화물 및 합금 원소 간의 동시 다발적 반응을 고려하고 있으며, 특히 Mg- Al 계 개재물의 진화를 고려하여 용강과 슬래그 및 전체 개재물의 조성 예측과 더불어 시간에 따른 Mg-Al 계 개재물의 조성 변화 및 양적 변화를 예측할 수 있다. 또한, Ca- Al 계, Mn-Si 계 개재물의 양적 변화도 계산할 수 있다. 슬래그의 점도와 융점에 영향을 미치는 불화물계 슬래그 성분인 CaF2가 추가적으로 고려되었다.
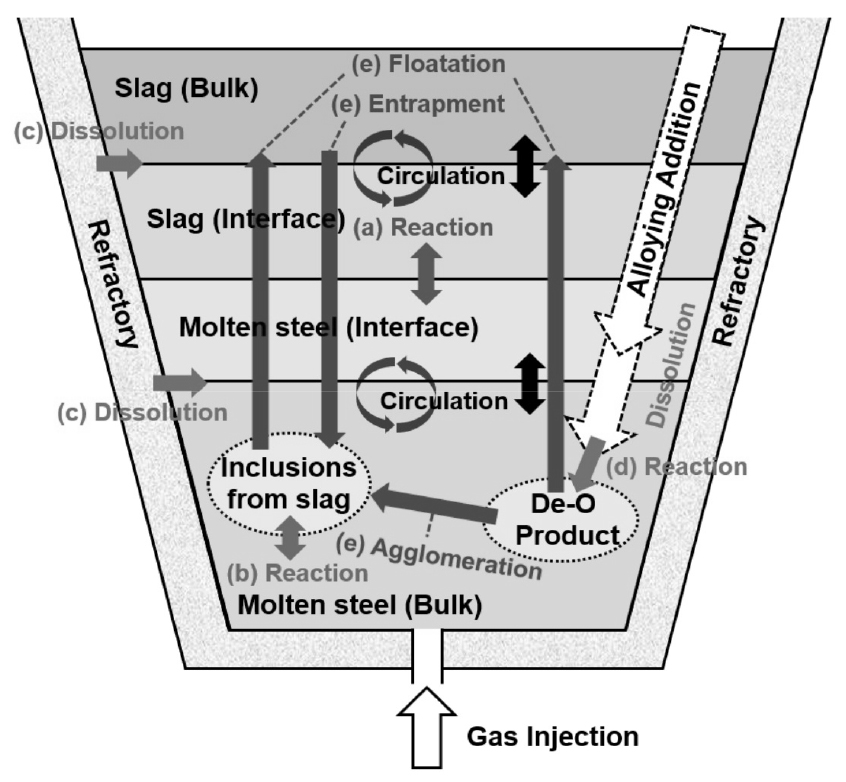
Fig. 4는 Inclusion Evolution 모델에서 고려하고 있는 반응들의 모식도를 나타내며36), 기본적인 반응들은 2.3절에서 소개한 모델의 반응들을 바탕으로 한다. 특히, 철강 품질에 악영향을 미치는 Mg-Al 계 개재물의 거동을 예측하기 위해 Mg-Al-O의 상 안정도를 바탕으로 Al2O3 개재물로부터 MgO 포화 개재물까지, 용강 중 Mg과 Al의 농도에 따라 안정한 상의 개재물 생성을 고려하였다. 식 (15)은 시간의 흐름에 따라 Al2O3 개재물과 반응하는 용강 내 Mg의 양을 나타낸다. 용강에서 Al2O3 개재물로 이동하는 Mg의 물질 이동 계수는 MgO∙Al2O3 산화물 층을 통해서 확산되는 MgO의 확산 계수37)를 사용한 식 (16)으로 정의된다. 식 (16)에서 셔우드 수는 하부 Ar 취입으로 발생하는 용강의 이동 속도를 사용하여 계산하였다. 식 (15)을 사용하여 Al2O3 개재물로부터 MgO 포화 개재물까지의 농도 변화를 계산하고, 그 농도에 따른 활동도의 변화를 적용하였다. 210 톤의 공정 결과와 모델의 계산 결과가 잘 일치하였으며, MgO∙Al2O3 스피넬 개재물의 생성 거동을 파악하기 위해 용강 및 슬래그의 초기 조성에 대한 영향을 열역학적으로 평가하였다.
3. 시뮬레이션의 예시
보고된 모델들은 2차 정련 공정에서 용강, 슬래그 및 개재물의 조성 변화와 양적 변화를, 실제 공정 조건을 대입한 시뮬레이션을 통해 예측할 수 있어야 한다. 2.4 절에서 서술한 Inclusion Evolution 모델의 계산 결과를 예시로 보여준다32,33,34,35,36). 계산 조건은 이전에 보고된 210 톤의 실제 공정 조건을 사용하였으며 Table 1에 나타냈다38). 이 모델에서 비금속 개재물의 거동은 크게 세 종류로 고려한다. 개재물의 슬래그로의 부유, 슬래그로부터의 혼입, 탈산 반응으로 생성된 개재물과 슬래그로부터 혼입된 개재물 간의 응집 반응이다. 세 종류 개재물의 거동 속도는 이전 연구에서 일정한 속도 상수로 최적화 되었으며 Table 2에 나타냈다32). Table 1과 Table 2의 조건을 사용하여 시뮬레이션 한 결과는 다음과 같다.
Table 1.
Industrial conditions for simulation input (process scale for 210 tons)35)
Table 2.
The optimized parameters of various inclusion behaviors32)
용강과 슬래그 성분의 농도 변화는 2.1 절에서 서술한 이중 경막 이론에 의해 계산된다. Fig. 5는 시간의 흐름에 따른 용강 중 Al과 O의 농도 변화를 보여준다34). 공정 초기 탈산제로 투입되는 Al에 의해 용강 중 Al의 농도가 증가하고, 이후 Al의 탈산 반응으로 인해 용강 중 O의 농도가 감소한다. 1200 초에서의 공정 결과 값과 시뮬레이션 결과가 잘 일치함을 보이며 3600 초 이후 반응 평형의 상태에 도달함을 보인다. Fig. 6은 슬래그 중 CaO, Al2O3, SiO2및 MgO의 농도 변화에 대한 결과를 보여준다34). 용강 중 Al의 탈산 반응으로 생성된 Al2O3 산화물은 슬래그로 부유하여 흡수되기 때문에 시간의 흐름에 따라 슬래그 중 Al2O3의 농도가 점진적으로 증가하는 것을 보인다. 슬래그 역시 3600 초 이후 반응 평형 상태에 도달하는 것을 보이며, 1200 초에서 공정 결과 값과 시뮬레이션 결과가 잘 일치함을 보인다. 용강과 슬래그의 농도 변화에 대하여 실제 공정 결과 값과 시뮬레이션 결과가 잘 일치하기 때문에 위 모델은 공정 예측에 대한 신뢰성을 갖는다.
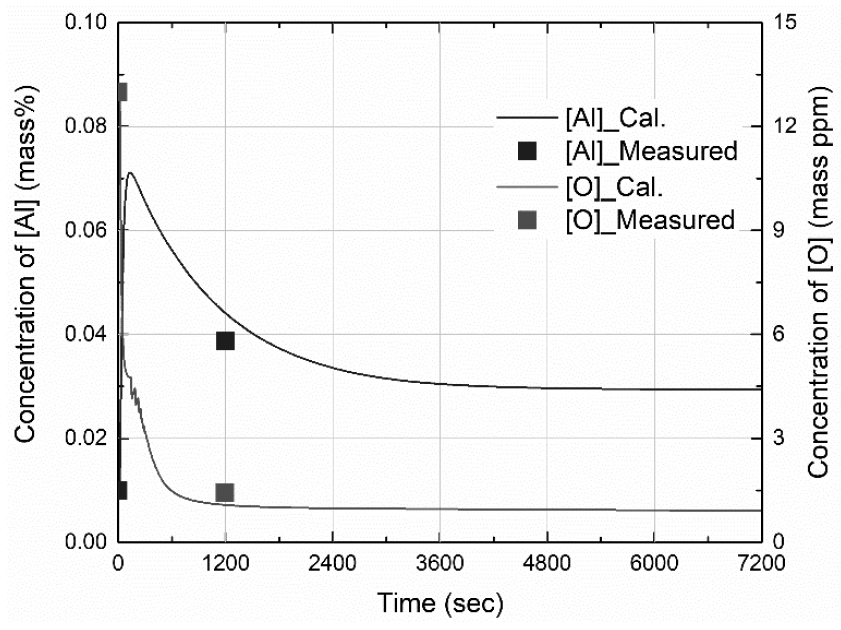
Fig. 5
Concentration changes of Al and O in the molten steel with compared between calculation results and measured data34).
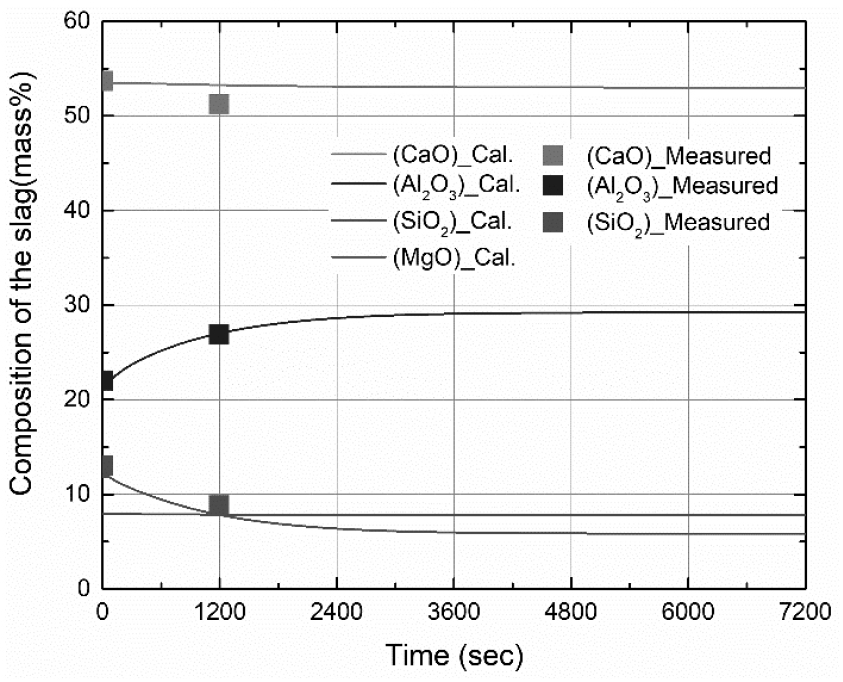
Fig. 6
Compositional changes of CaO, Al2O3, SiO2 and MgO in the slag with compared between calculation results and measured data34).
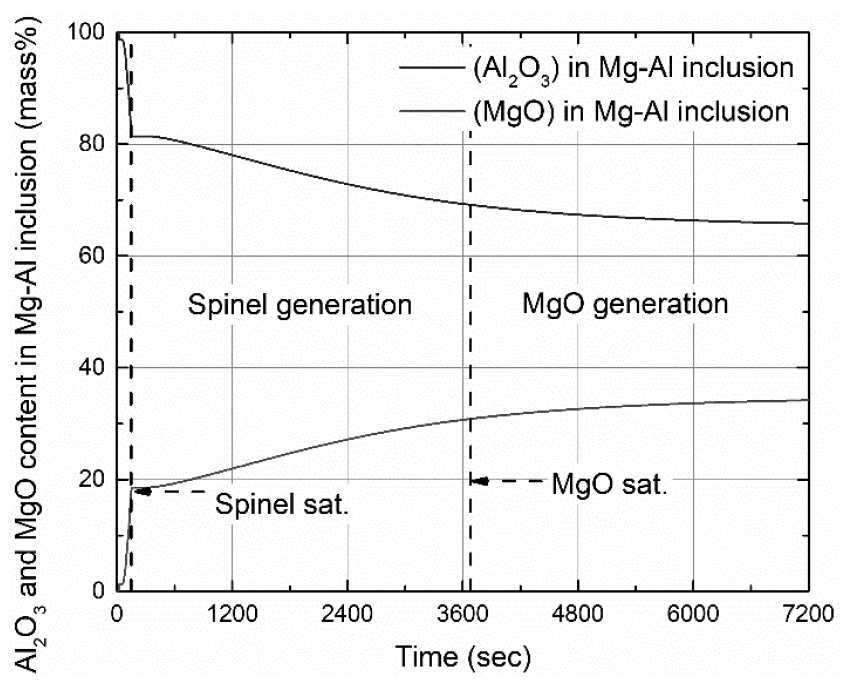
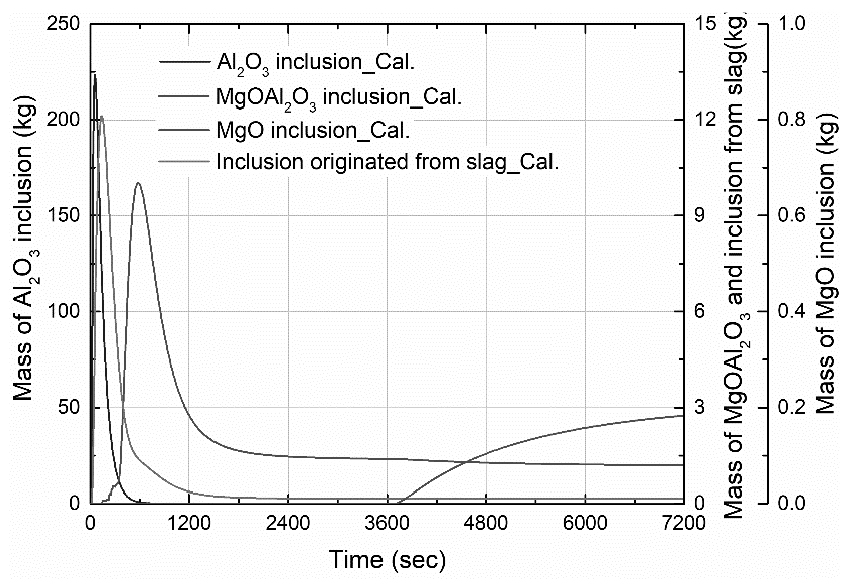
Fig. 7은 식 (15)에 의해 계산되는 시간의 흐름에 따른 Mg-Al 계 개재물의 농도 변화를 나타낸다. 슬래그 중 MgO 성분의 용강으로의 환원 반응과, MgO-C 기반의 내화물의 용강 및 슬래그로의 용손 반응이 고려되었기 때문에, 용강 중으로 Mg이 공급된다. 용강으로 공급된 Mg과, Al 탈산 반응에 의해 형성되고 부유하여 슬래그에 흡수 되지 못 한 Al2O3 개재물이 반응하여, 식 (15)에 의해 Mg-Al 계 개재물 중 MgO의 농도가 계산된다. 용강 중 Mg의 첨가 없이도 지속적으로 Mg이 공급되기 때문에, Mg-Al 계 개재물 중 MgO의 농도는 시간의 흐름에 따라 점진적으로 증가한다. 150 초에 Al2O3/MgO∙Al2O3 포화 농도에 근접하며, 이후 점진적으로 증가한 MgO의 농도는 3680 초 이후 MgO∙Al2O3/MgO 포화 농도에 근접한다. Fig. 8은 Mg-Al 계 개재물 및 슬래그로부터 혼입된 개재물의 양을 나타낸다. 공정 초기 첨가된 Al의 탈산 반응으로 Al2O3 개재물이 생성된다. 150 초 이후 Mg-Al 계 개재물의 농도가 Al2O3/MgO∙Al2O3 포화 농도에 근접하였기 때문에, Al2O3 개재물이 MgO∙Al2O3 개재물로 변화하며, 150 초 이후 MgO∙Al2O3 개재물이 생성되었다. 3680 초 이후 Mg-Al 계 개재물의 농도가 MgO∙Al2O3/MgO 포화 농도에 근접하였고, MgO∙Al2O3 개재물은 MgO 포화 개재물로 변화한다. 따라서 3680 초 이후 MgO∙Al2O3 개재물의 양은 MgO 포화 개재물이 생성되는 양만큼 감소한다. 각 개재물이 생성된 후 시간에 따라 그 양이 감소하는 이유는, 개재물의 슬래그로의 부유 현상을 고려하였기 때문이다. Fig. 9는 총 개재물에 대한 CaO-MgO-Al2O3의 3원계 조성 그래프를 나타낸다. MgO∙Al2O3 개재물의 형성으로 인해 총 개재물 중 MgO의 농도가 시간의 흐름에 따라 증가한다. 총 개재물 중 CaO의 농도가 증가하는 이유는 하부 취입 Ar 가스에 의한 용강의 교반으로 슬래그로부터 혼입된 개재물이 고려되었으며, 이러한 개재물의 농도는 CaO 농도가 높은 슬래그 조성의 영향을 받았기 때문이다.
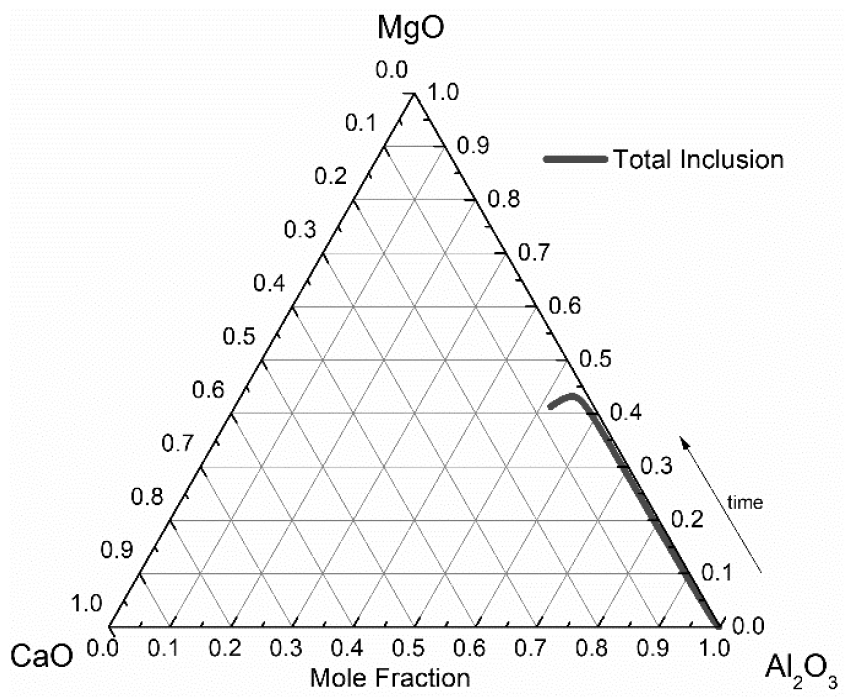
Fig. 9
Ternary diagram for the compositional changes of MgO, CaO and Al2O3 in the total inclusion34).
위와 같이 2차 정련의 종합 모델 중 하나인, Inclusion Evolution 모델은 시간의 흐름에 따른 용강, 슬래그 및 비금속 개재물의 조성 변화와 양적 변화를 예측할 수 있으며, 210 톤의 실제 조업 결과로부터 신뢰도를 갖는다.
4. 결 론
본 연구에서는 고급강 제조를 위해, 현재까지 보고된 Coupled reaction 모델 기반의 2차 정련 반응 모델들을 검토하고 분석하였다. Coupled reaction 모델의 반응은 이중 경막 이론으로 표현되며, 인접한 상의 접촉한 계면 영역의 반응은 평형이라고 가정되며, 각 상 내의 벌크 영역과 계면 영역의 반응은 물질 이동을 고려한다. 발표된 모델들은 수 kg의 실험실 규모부터 210 톤의 실제 조업 규모까지, 용강, 슬래그 및 개재물의 조성 변화 및 양적 변화를 시뮬레이션을 통해 예측 가능하였다. 초기에 발표된 모델은 용강-슬래그 반응만 고려하였지만, 연구자들의 지속적인 모델 개발로 인해 합금 원소 첨가, 비금속 개재물의 형성 및 거동, 내화물의 용손 반응들을 추가적으로 고려하였다.
부 록
본문에서 사용된 수식의 기호는 다음과 같이 정의된다.
| [i] | 금속 상 내 성분 i의 질량 분율[mass%] |
| (i) | 산화물 상 내 성분 i의 질량 분율[mass%] |
| Ji | 성분 i에 대한 몰 유속 밀도[mol/m2/s] |
| ki | 성분 i에 대한 물질 이동 계수[m/s] |
| ρi | 성분 i의 밀도[kg/m3] |
| Mi | 성분 i의 원자량 및 분자량[kg/mol] |
| EM | 금속 성분 M의 산화 반응식에 대한 평형 분배 비[-] |
| aO | 산소의 활동도[-] |
| fM | 금속 상 내 성분 M에 대한 활동도 계수[-] |
| γMOn | 산화물 성분 MOn에 대한 활동도 계수[-] |
| KM | 금속 성분 M의 산화 반응식에 대한 평형 상수 |
| C | 산화물 내 총 몰 농도[mol/m3] |
| Vi | 상 i의 부피[m3] |
| t | 시간[s] |
| A | 반응 면적[m2] |
| Wi | 성분 i에 대한 질량[kg] |
| pin | 금속 내 산화물 상의 공급 속도14) |
| ε | 교반 에너지[W/s] |
| mol | 반응 몰 수[mol] |
| R | 이상 기체 상수[8.314 J/mol/K] |
| T | 절대 온도[K] |
| P | 분압[atm] |
| Q | 유량[Nl/min] |
| h0 | 취입되는 가스의 깊이[m] |
| hv | 로의 높이[m] |
| η | 액상으로 취입되는 기체의 운동 에너지 계수[0.06] |
| dv | 로의 직경[m] |
| Re | 레이놀즈 수[-] |
| Sc | 슈미트 수[-] |
| Sh | 셔우드 수[-] |
| DMgOSpinel | MgO·Al2O3 스피넬 층으로의 MgO의 확산도[m2/s] |
| dinclusion | 비금속 개재물의 직경[m] |
본문에서 사용된 첨자의 기호는 다음과 같이 정의된다.