1. 서 론
폐플라스틱으로 인한 환경오염과 화석연료의 무분별한 사용으로 인한 지구 온난화 문제가 전지구적인 환경 문제로 떠오르고 있으며 최근 국내에서도 미세먼지를 넘어서는 가장 큰 환경 이슈로 자리 잡으며 해결책에 대한 활발한 정책적, 과학적 접근이 시도되고 있다. 플라스틱의 무분별한 생산, 사용으로 인한 방대한 양의 폐플라스틱의 발생은 가장 잘 알려진 해양의 미세플라스틱 문제뿐만 아니라 화석연료의 사용으로 인한 화학공정 산업의 탄소배출 비율의 증가를 가져오고 있다. 플라스틱 문제 해결에 가장 큰 어려움은 급격히 증가하는 사용량에 반해 플라스틱을 대체할만한 효과적인 대체품이 생산되지 못하는 데 있어 향후에도 플라스틱의 사용과 폐플라스틱의 배출량은 크게 줄어들지 않을 것으로 예상되고 있다1).
Geyer et al.(2017) 에 따르면 전세계 플라스틱 생산량은 1950년 2백만 톤에서 2015년 4억7백만톤으로 매년 급격히 증가하였으며 누적 생산량 약 83억톤 중 현재 빌딩 내장재 등으로 폐기되지 않고 사용되는 플라스틱 25억톤과 10%이하의 재활용 및 일부 소각 비율 이외에 대부분의 플라스틱이 적절한 방법 없이 배출된 것으로 예상되고 있으며 배출 경로는 매립, 유출 등 그 비율을 특정하기가 어려운 실정이다1,2). 이 추세대로라면 향후 누적 생산량 및 폐기량은 지속적으로 급격히 증가할 것이며 Borrelle et al.(2020)에 따르면 플라스틱 생산, 사용, 재활용량 등 현재 상태를 기반으로 향후 20년 안에 13억 톤의 플라스틱 쓰레기가 발생할 것으로 예측되었다2,3). 해양으로 배출되어 미세플라스틱 문제를 일으키는 육상 플라스틱의 유출을 최소화하고 플라스틱 생산에 사용되는 화석연료의 사용을 줄이기 위해서는 폐플라스틱을 효율적으로 재활용하는 기술이 필요하다4).
가스화란 석탄, Biomass, 폐기물 등과 같이 탄소를 기본 성분으로 하고 있는 연료를 산소를 이용한 부분산화 및 수증기, 이산화탄소와 같은 기체와 반응시켜 CO와 H2가 주성분인 합성가스로 전환하는 기술이다5). 최근 이 기술을 통하여 고품질의 수소 및 합성석유, 메탄올 그리고 DME (Dimethy ether) 등의 고품질 연료를 생산하는 기술 개발이 활발히 진행되고 있다6). 폐플라스틱의 가스화 공정은 플라스틱을 이용하여 석유 대체 연료로 활용이 증가하는 있는 수소를 생산하고 미세플라스틱과 탄소 배출, 2가지 문제를 한꺼번에 해결할 수 있다는 점에서 주목할 만하다5,6). 폐플라스틱의 경우 함유된 플라스틱의 종류에 따라 Cl2 및 HCl 등이 발생되어 공정 내 부식 등 고려하여야 할 요소가 많아 Cl 함유 폐플라스틱의 경우 사전에 탈염처리가 필요할 수 있다6).
가스화 공정의 생산 가스를 수소 수율을 극대화하거나 적절한 H2/CO 비율의 조절을 통하여 화학원료로 전환하기 위해서는 반응 (1)과 같은 수성가스 전환(Water-gas shift reaction, WGS) 공정이 가스화 후속 공정으로 이용되고 있으며 이는 합성가스 중의 CO 성분을 H2O와 반응시켜 H2 수율을 극대화하는 기술로 적용 시스템에 따라 CO와 H2의 비율을 적절히 조절하는 것을 목표로 하게 된다7).
수성가스 전환 반응은 가역적인 발열 반응으로서 온도가 올라갈수록 RWGS(Reverse water-gas shift reaction)인 역반응이 우세하게 되므로 1000°C 부근의 고온에서 운전되는 가스화 공정과 달리 촉매를 이용하여 400°C이하의 저온에서 수행된다. 수성가스 전환 공정은 크게, 250-400°C의 온도범위에서 운전되는 고온 전환반응과 (High Temperature Shift, HTS), 180-250°C 사이에서 진행되는 저온 전환반응(Low Temperature Shift, LTS)으로 나뉘게 되며 현재도 촉매 개발 및 폐기물 합성가스 적용 등에 대하여 활발히 연구가 진행되고 있다. 일반적으로 고온 전환 반응에서는 공정 온도가 높아 반응 속도가 빠르지만 발열 반응인 수성가스 전환반응의 특성상 역반응으로 인한 낮은 CO 전환율을 나타내게 되며 LTS의 경우 반응 속도는 HTS에 비해서 느리지만 CO 전환율이 높아 고온과 저온 촉매를 동시에 이용하는 2단 반응기 형태를 이용하게 된다. 수성가스 전환반응에는 다양한 형태의 촉매가 사용되며 Pt등의 귀금속부터 Co, Cu, Ce 등의 촉매가 혼합된 형태로 사용되게 되며 LTS 촉매로 Cu계열의 촉매가 잘 알려져 있으며 대표적으로 Cu/ZnO/Al2O3를 들 수 있다8).
본 연구에서는 한국기계연구원에서 보유하고 있는 0.5 ton/day RPF(Refuse Plastic Fuel) 가스화로 후단부에 WGS 공정을 적용하고자 가스화로 생성 합성가스와 동일한 모사 가스를 이용하여 LTS 및 HTS 촉매를 이용하여 수성가스 전환 반응 특성을 살펴보았다. HTS 및 LTS 촉매를 lab scale의 기초 반응기에서 각각의 합성가스의 전환 특성을 살펴보고자 관형의 촉매 반응기에서 유량별, 온도별, S/C ratio별로 운전 조건을 변화시키면서 실험을 진행하고 각 조업 변수가 H2, CO2, CO의 농도에 미치는 영향 및 CO 전환율에 대한 영향을 살펴보았다.
2. 실험장치 및 방법
수성가스 전환 반응에 이용된 합성가스의 조성은 0.5t/d RPF 순산소 가스화 기체의 농도를 기준으로 하였으며 농도 조건은 Table 1과 같다. 전체 유량은 200-400ml/min으로 변화되었으며 WGS 반응을 위한 steam 공급량은 steam/ carbon mole ratio(S/C ratio)가 1.5-3.5가 되도록 공급하였다.
Table 1.
Inlet gas condition
| H2 | CO | CO2 | N2 | |
| From KIMM gasifier (%) | 25 | 40 | 25 | 10 |
| Flow rate (ml/min) | 50-100 | 80-160 | 50-100 | 20-40 |
| Steam/Carbon ratio | 1.5-3.5 | |||
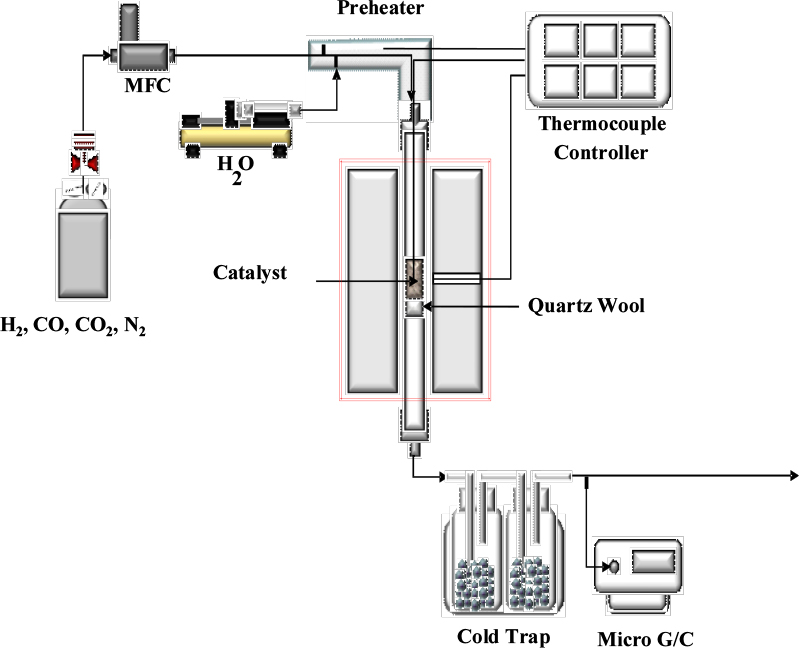
Fig. 1은 수성가스 전환 반응에 이용된 고정층 촉매 반응기의 구성을 나타내고 있다. 전체 시스템은 반응 기체 및 H2O 주입부와 main reactor, 후단 분석 시스템으로 이루어져 있다. 반응가스인 H2, N2, CO, CO2 는 MFC(Mass Flow Controller, MKS Co)를 통하여 H2O는 syringe (Hamilton co, 50㎖)와 syringe pump(KDS100)를 통하여 정량 공급되고 H2O를 스팀으로 변환하기 위하여 반응기 전단에 line heater를 설치하고 관내 온도를 약 150-200°C유지하여 주입하였다. Main 반응기는 석영관(9.0mm I.D., 48.5cm L)으로 제작되었고 같은 재질로 반응기 중심부에 촉매 지지층이 부착되어 있으며 반응기내 온도는 촉매층 중심부에 설치된 열전대(Thermocouple ,K-type)를 기준으로 외부 Furnace의 반응온도 설정은 PID 시스템(YOKOGAWA, UP351E)을 이용하여 조절된다.
본 실험에서는 WGS 촉매로 SUD-CHEMIE사의 촉매를 3g씩 1mm이하로 분쇄하여 사용하였으며 구성성분은 Table 2와 같다. 생성가스의 H2, CO2, CO, N2는 cold trap을 거친 후 micro GC(Agilent Technology, Micro GC3000A, Molsieve:12μm/32.0μm/10m & PLOTQ:10μm/320.0μm/ 8m)에 의하여 실시간으로 분석되게 된다. CO의 전환율은 다음과 같이 계산되었다.
Table 2.
HTS and LTS catalyst
3. 결과 및 고찰
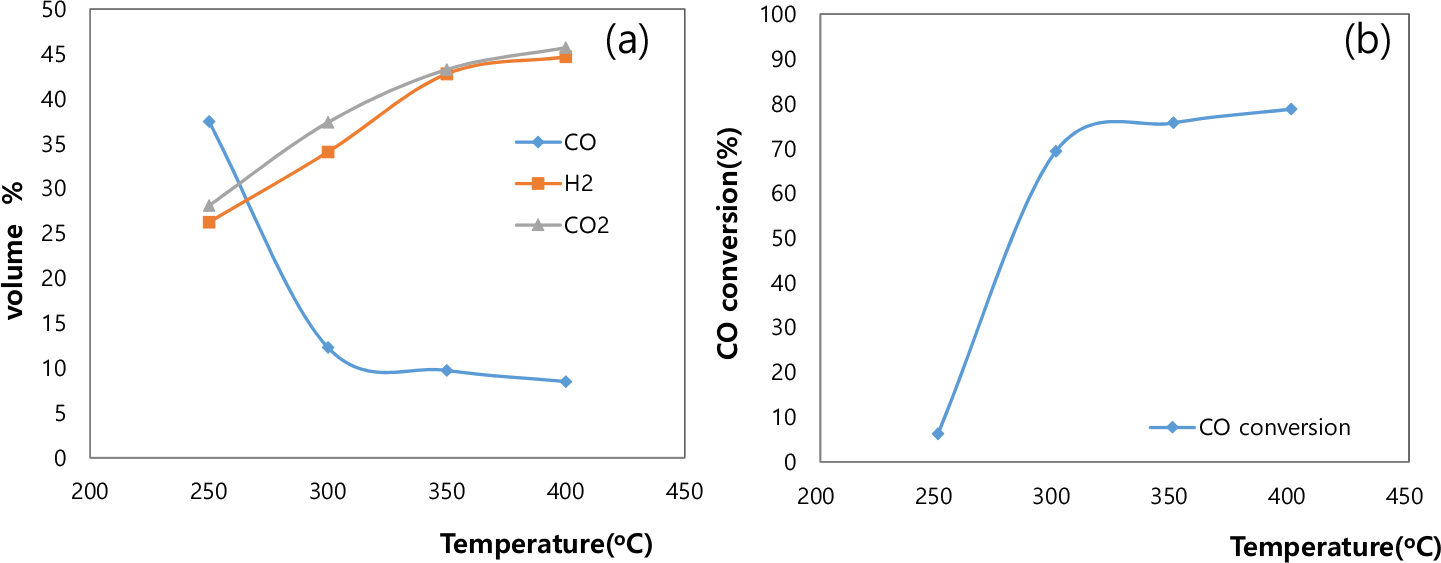
고온 전환반응(HTS) 실험에서 유량 200ml/min, S/C ratio가 2.5일 때 온도에 따른 합성가스 농도 변화를 Fig. 2에 나타내었다. 실험은 50°C간격으로 온도를 상승시키며 수행되었고 반응 온도가 증가할수록WGS 반응이 활발해지며 H2, CO2 농도가 증가하는 경향을 나타내고 있다. CO의 농도도 반응 온도에 따라서 감소하여 CO 전환율은 반응 온도가 증가할수록 증가하는 경향을 나타내고 있다. H2 농도가 250°C, 26%에서 400°C, 45%까지 CO2 농도가 28%에서 46%까지 증가하고 CO 농도는 250°C, 37%에서 400°C, 8%로 감소하고 이에 따라 CO의 전환율이 6%에서 79%로 크게 증가하게 된다. 350°C와 400°C 조건을 살펴보면 H2 및 CO2의 농도는 일부 증가하고 CO의 농도는 감소하여 CO 전환율이 높아지는 경향을 나타내나 그 차이가 2% 이내로 크지 않아 HTS 촉매의 최적 반응 온도는 350°C임을 알 수 있었고 향후 S/C ratio나 유량 변화 실험에서는 이 반응 온도 조건에서 실험을 수행하였다.
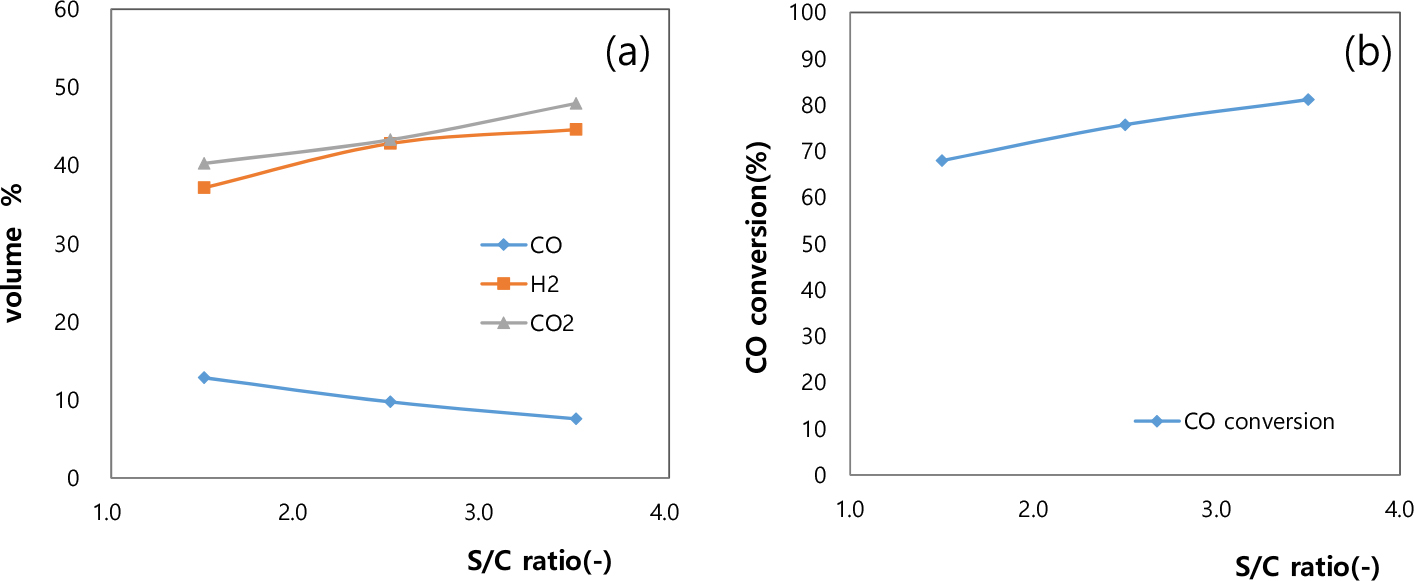
S/C ratio가 수성가스 전환반응에 미치는 영향을 알아보기 반응 온도 350°C, 유량 200ml/min 조건에서 S/C ratio를 1.5, 2.5, 3.5로 변화시키면서 실험을 수행하였다. Fig. 3과 같이 S/C ratio가 증가함에 따라 H2 및 CO2의 농도와 CO 전환율은 증가하는 경향을 나타내었다. 이는 반응물인 steam의 주입이 많아질수록 WGS 반응이 활성화되어 수소 농도가 높아지게 되며 CO 농도가 감소하게 되는 것으로 S/C ratio가 1.5일 때 H2, CO2 농도 37%, 40%에서 S/C ratio가 3.5에서 44%, 47%로 증가하는 것을 볼 수 있다9). CO농도는 12%에서 8%로 감소되어 CO 전환율은 S/C ratio가 1.5인 조건에서 68%, 3.5인 조건에서 81%로 증가함을 알 수 있다.
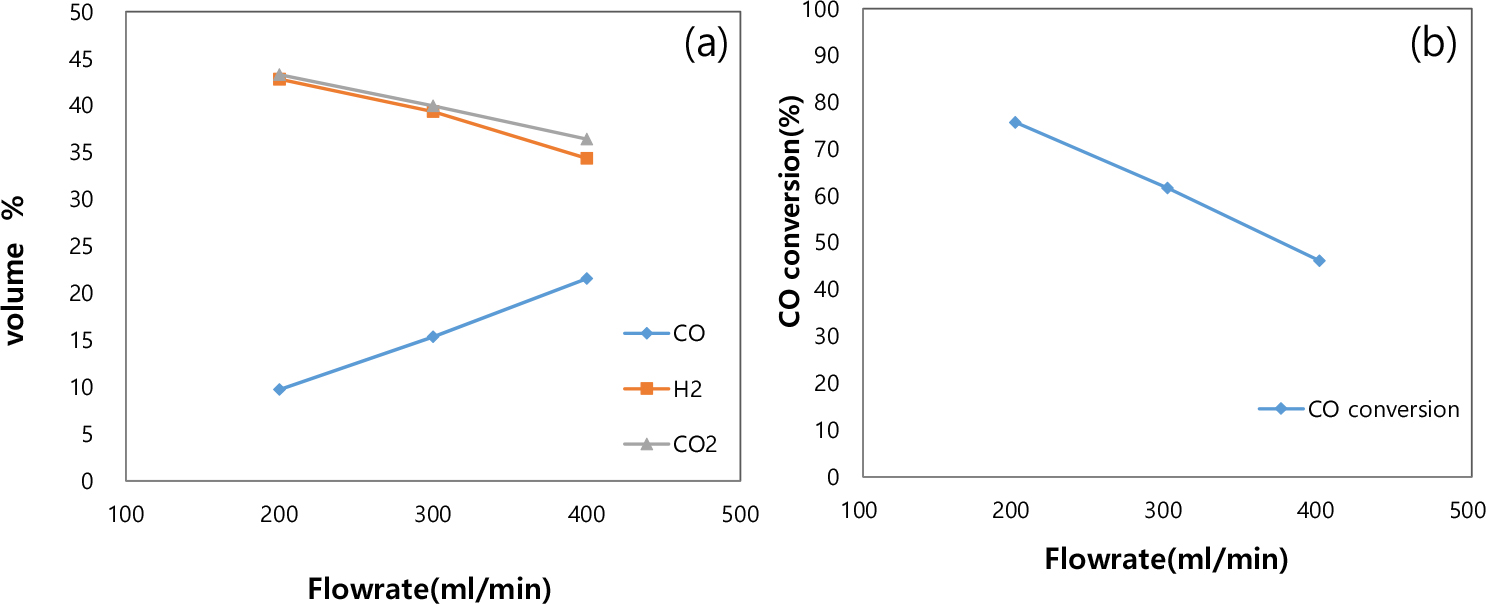
주입된 전체 합성가스 유량의 수성가스 전환 반응에 대한 영향을 살펴보기 위하여 전체 합성가스 유량을 200- 400ml/min으로 변화시키며 S/C ratio, 2.5, 반응 온도 350°C일 때 유량 영향을 살펴보았다. 반응기에 주입되는 가스 유량이 증가할수록 촉매층내 체류시간이 감소하게 되어 Fig. 4에서 알 수 있듯이 H2, CO2 농도는 각각 43%에서 34%로, 43%에서 36%로 감소하는 경향을 나타내며 CO 전환율도 마찬가지로 76%에서 46%로 감소하는 경향을 나타내었다. 모든 실험에서 같은 양의 CO2 및 H2 가스를 주입하였음에도 CO2 농도가 약간 높은 경향을 나타내었는데 이는 일부 CO가 반응 중 다음과 같은 Boudouard Reaction을 일으켜 산화되어 CO2 로 전환되는 것으로 예상되며 반응기에도 일부 탄소 침적을 육안으로 확인할 수 있었다10).
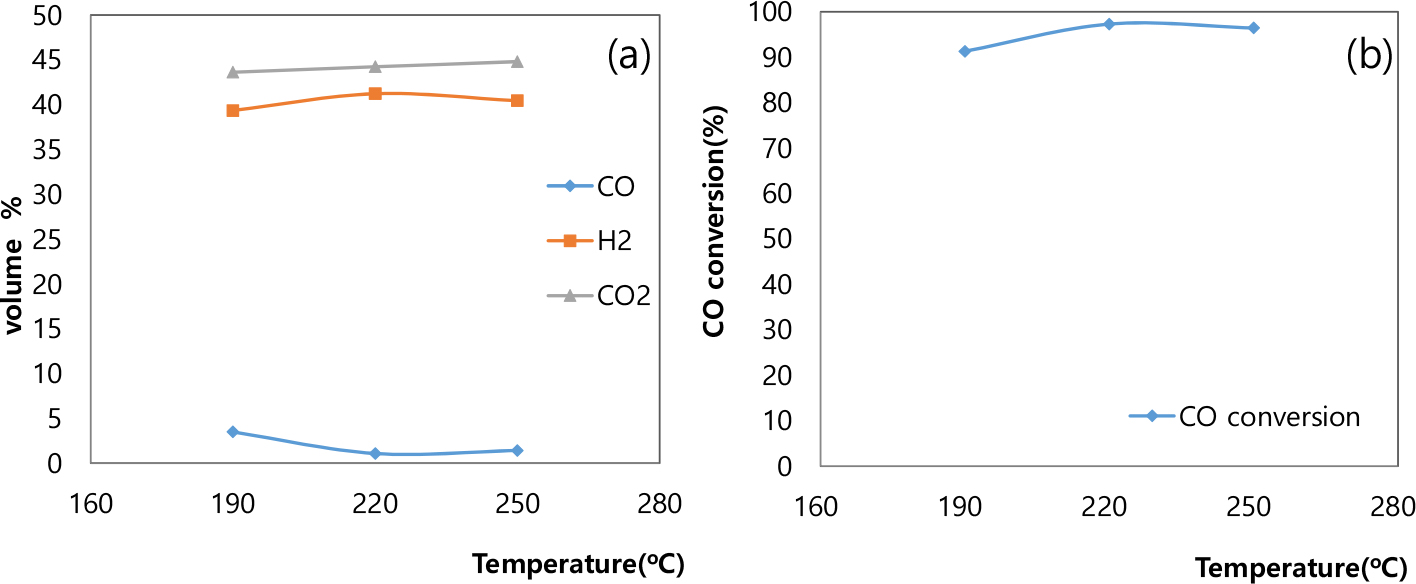
저온촉매인 LTS 촉매를 이용하여 HTS 촉매와 같이 반응 온도, S/C ratio, 전체 유량의 영향에 대한 수성가스 전환 반응 실험을 수행하였다. LTS 촉매의 경우 유량 200ml/min에서 S/C ratio가 2.5일 때 190°C-250°C로 반응 온도를 변화시키면서 그 영향을 살펴보았다. Fig. 5와 같이 온도가 올라감에 따라 H2, CO2의 농도는 190°C의 39%, 43%에서 250°C에서는 40%, 45%로 미량 증가 하고 CO의 농도는 3.5%에서 1%내외로 감소하여 CO 전환율도 91%에서 97%로 증가하게 된다. HTS 시스템과 달리 LTS 시스템에서는 190-250°C의 전체 온도에서 90% 이상의 높은 전환율과 H2 농도 40% 내외를 나타내었고, 그래프에서 알 수 있듯이 220°C 및 250°C에서 전환율 및 H2 농도 및 CO 전환율이 220°C가 250°C에 비하여 미량 높아 최적의 조업 온도임을 알 수 있다.
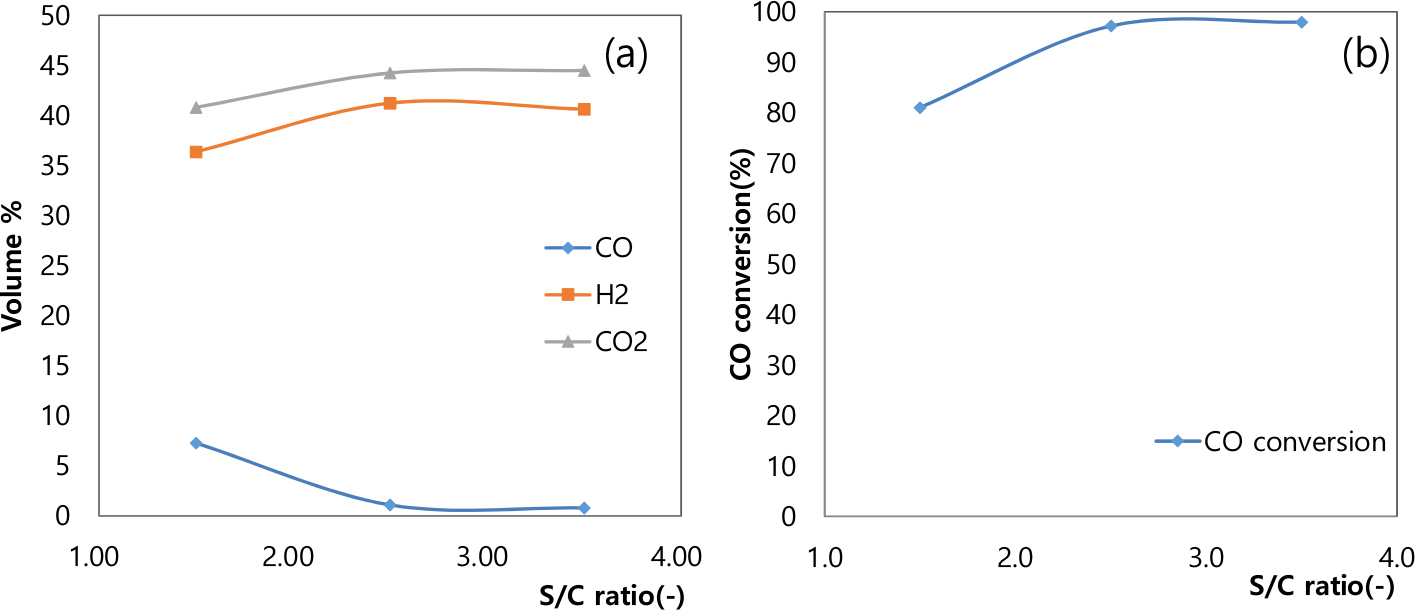
S/C ratio에 따른 LTS 반응 영향을 살펴보기 위하여 유량 200ml/min, 반응 온도 220°C에서 S/C ratio를 1.5-3.5로 변화시키며 그 영향을 살펴보았다. Fig. 6과 같이 S/C ratio가 증가함에 따라 HTS 결과와 마찬가지로 CO 전환율은 증가하는 경향을 나타내며 S/C ratio가 1.5일 때 H2, CO2 농도 36%, 40%에서 S/C ratio가 3.5에서 40%, 44%로 증가하는 것을 볼수 있으며 H2 농도는 2.5에서 좀 더 높은 값을 나타내었다. CO 전환율은 S/C ratio가 1.5인 조건에서 81%, 3.5인 조건에서 98%의 매우 높은 전환율을 나타내어 최대 전환율이 81% 수준인 HTS 촉매에 비하여 전체적으로 높은 값은 나타냄을 알 수 있다.
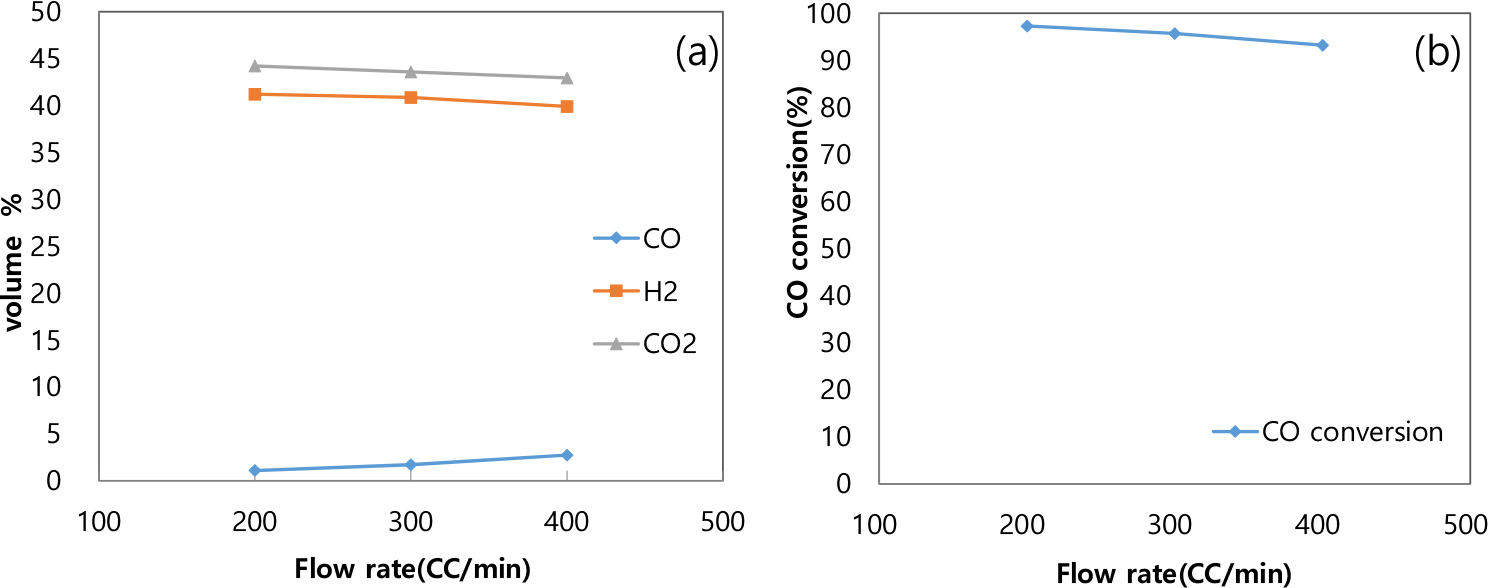
LTS 반응에서도 주입된 전체 합성가스 유량의 수성가스 전환 반응에 대한 영향을 살펴보기 위하여 전체 합성가스 유량을 200-400ml/min으로 변화시키며 S/C ratio가 2.5, 반응 온도가 220°C일 때 유량 영향을 살펴보았다. Fig. 7과 같이 반응기에 주입되는 가스 유량이 증가할수록 HTS 촉매 실험과 마찬가지로 층내 체류시간의 감소에 따라 H2, CO2 농도는 유량이 200ml/min일 때 H2와 CO2의 농도는 41%, 44%에서 400ml/min일 때 40%, 43%로 소량 감소하게 되었고 미반응 CO의 농도가 증가하여 CO 전환율이 유량 200ml/min, 97%에서 400ml/min, 93%로 감소하는 경향을 나타내었다. HTS 촉매에 비하여 가스 유량에 따라 감소되는 CO전환율 및 CO2, H2 농도가 적어 전체적으로 안정적이고 상대적으로 높은 CO 전환율을 보이고 있으며 CO2와 H2 농도의 차가 HTS 시스템에 비하여 더 크고 HTS 시스템의 최고 수소 농도 45%에 비하여 최고 H2 농도가 41%로 낮아 WGS 반응 뿐 아니라 Boudouard Reaction이 활발히 일어난 것으로 예상할 수 있다.
4. 결 론
본 연구에서는 RPF(Refuse Plastic Fuel)을 이용한 폐기물 가스화를 통해서 생성되는 합성가스를 토대로 수성가스 전환반응(WGS, Water Gas Shift reaction)에서 HTS (High Temperature Shift)와 LTS(Low Temperature Shift) 상용촉매를 사용하여 Lap Scale의 고정층 촉매 반응기에서 온도 변화, S/C ratio, 가스 유량에 따른 반응 특성을 실험하였다. HTS와 LTS 시스템 모두에서 온도가 증가함에 따라 CO 전환율이 증가는 경향을 나타내었으며 S/C ratio 증가에 따라 H2 및 /CO2의 생성율이 증가하였고 비례적으로 CO 농도가 감소하며 CO 전환율이 증가하는 경향을 보였다. HTS와 LTS 공정 모두 유량이 증가함에 따라 촉매층내 체류시간이 짧아져서 전환율 및 수소 수율이 감소하는 것으로 나타났다. HTS시스템에서는 최고 CO전환율 81%, LTS 시스템에서 최고 전환율 98%로 CO 전환율은 LTS 시스템이 더 높았으며 최종 수소 농도는 HTS 시스템에서 최고 농도 45%, LTS 시스템에서 최고 농도 41%를 나타내어 HTS 시스템에서 더 높은 농도의 수소를 얻을 수 있었다.