1. 서 론
구리는 전기특성이 우수하고 가공하기 용이하여 구리 사용량의 60%가 전선으로 사용되고 있으며1), 리튬이온전지의 음극재를 고정하는 동박으로 최근 수요량이 증가하고 있다. 구리는 주로 황동석(Chalcopyrite, CuFeS2)을 비롯한 구리 황화광의 정광을 건식제련공정으로 처리하여 전기동을 생산하며, 황동석은 세계 구리 매장량의 약 70%를 차지한다2,3,4). 건식제련공정은 SO2의 배출과 고가의 건설 경비가 단점으로 지적되어 왔으며, 비소 등 불순물 함유량 상승으로 황동석의 저품위화가 심화되고 있다5). 따라서 황동석을 함유하는 저품위 황화동광에 대한 습식제련공정개발이 요구되어 왔다6).
황화동광의 습식제련공정은 직접적인 침출공정(direct leaching processes)과 간접적인 침출공정(indirect leaching processes)로 대별되며, 다시 직접적인 침출공정은 침출액의 종류에 따라 황산염(sulfate)과 염화물(chloride)을 기반으로 분류 가능하다5,7). 황산을 사용하는 공정은 침출 후 용매추출과 전해채취에 의해 구리가 회수되며, 산화구리광을 대상으로 하는 기존 시설을 활용할 수 있는 장점이 있다8). 그러나 상압 조건에서 황산용액으로 황동석을 침출하는 경우 광석 표면에 부동태층(passivating layer)을 형성시켜 침출속도를 늦추는 단점이 보고되었다8). 따라서 침출 중 황동석 표면의 부동태층 형성을 방지하거나 제거하기 위한 다양한 연구가 수행되었다.
부동태층을 제거하여 황동광의 침출효율을 상승시키기 위한 방법으로 금속분말첨가, 산화환원전위(oxidation-reduction potential) 조절, SO2 첨가, 미립분쇄, 가압침출법 등 다양한 습식제련공정이 보고되었다5). 이 중 고온고압 조건에서 산소를 산화제로 활용하며 부동태 형성을 억제하는 산소가압(POX, Pressure Oxidation) 공정은 개발된 후 미국 애리조나의 Bagdad 및 Morenci 광산, 브라질 카라하스의 Sossego 광산의 황동석 광석 침출에 적용되었다9). 산소가압 침출공정은 온도에 따라 저온, 중온 및 고온공정으로 분류할 수 있다. 산소가압침출공정은 침출이 이루어지는 동안 황동석 표면의 부동태층 형성을 억제하지만 가압침출공정에서 황동석의 황 성분은 산화되며 단체황(elemental sulfur, S0)으로 전환되어 구리 침출율 저하의 원인이 되기도 한다10). 저온공정(90~110℃)에서는 80~90% 황화물(sulfide)의 단체황(elemental sulfur) 전환이 관찰되었으며10), 중온공정(일반적으로 140~150℃)에서는 70~80%의 단체황 전환율이 관찰되었다11). 고온공정(200~230℃)에서는 모든 황화물이 황산염(SO42-)으로 전환되며 단체황에 의한 침출효율 저하는 관찰되지 않으나 과량 생산된 황산의 중화처리가 별도로 요구된다10,11).
본 연구는 국내에 수입되는 황동석 정광을 대상으로 한국광해광업공단이 자체 제작한 가압침출기를 이용하여 중온범위의 가압침출실험을 수행하고 황동광으로부터 구리 침출에 대한 염소이온과 계면활성제 첨가의 영향을 조사하였다. 입도크기, 황산농도, 염소이온 및 계면활성제의 영향을 조사하였고, 침출잔사를 XRD(X-ray diffractometer)로 분석하여 실험결과를 고찰하였다.
2. 실험방법
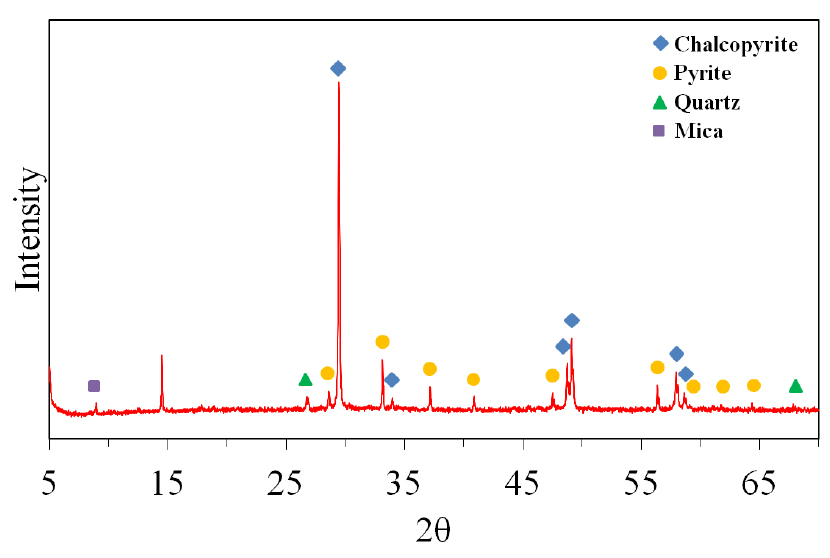
본 연구에서 사용한 황동석은 국내에 수입되고 있는 황동석 정광을 확보하여 사용하였고, 시료의 입도 분석 결과(Malvern사의 MS 2000 이용), 전체 입도분포에서 90%의 크기(D90)는 60μm이었다. 정광시료를 산용해 후, 성분분석을 실시하고 분석결과를 Table 1에 나타내었고(Si는 SiO2로 환산하여 표시), XRD(SmartLab X-ray diffractometer, Rigaku Co.) 분석결과를 Fig. 1에 나타내었다. 시료를 구성하고 있는 주요 광종은 황동석이며, 그 외에 황철석, 석영 등이 수반되고 있음을 확인하였다. 정광시료는 추가로 분쇄하여 D90 입도를 각각 10μm과 45μm로 조절하여 실험에 사용하였다.
Table 1.
Elemental composition of the samples
| Composition | Cu | Fe | S | SiO2 | Al | Zn | Ca | Pb |
| Content (wt. %) | 25.68 | 27.33 | 30.53 | 7.28 | 0.98 | 0.48 | 0.34 | 0.12 |
모든 침출실험은 한국광해광업공단이 자체 설계 및 제작한 반응기 용량 2L 규모의 회분식(batch) 가압침출기(autoclave)를 이용하여 수행하였다. 반응기 재질은 내식성, 내마모성 및 내열성 등을 고려하여 티타늄(Grade 2)으로 설계되었고, 최대 압력 및 온도는 각각 130atm, 350℃이다. 교반기는 마그네틱 드라이브를 사용하며, 최대 교반속도는 1,750rpm으로 설계되었다. 온도 상승은 반응기 외부에 전기 히터(세라믹)를 사용하며, 침출반응 시 발열에 의한 온도 조절을 위해 냉각기를 이용하여 반응기 내부에 코일을 설치하고 냉각수를 공급하였다. 모든 침출실험은 다음과 같은 순서로 진행하였고, 침출조건은 Table 2에 나타내었다. 첨가제와 황산농도가 조절된 침출액과 시료 100g을 가압침출기에 투입한 후, 반응기에 약 7atm 산소의 주입과 배출을 3회 반복하여 반응기 잔존 내부 가스를 외부로 배출하였다. 외부히터의 온도를 450℃로 설정해 내부온도가 150℃까지 상승하고 유지하였다. 용액을 교반기로 800rpm으로 교반하며 냉각수를 순환시킨다. 용액의 온도가 목표온도에 도달하면 7atm의 압력에 이르도록 산소를 주입하고 실험 중 정해진 시간에 시료채취를 진행한다. 용액은 0.45μm 필터로 여과한 후, ICP-OES(inductively coupled plasma optical emission spectrometer, OPTIMA 8300, PerkinElmer, Inc.)를 이용하여 분석하였다.
Table 2.
Leaching conditions performed in this study
3. 실험결과 및 고찰
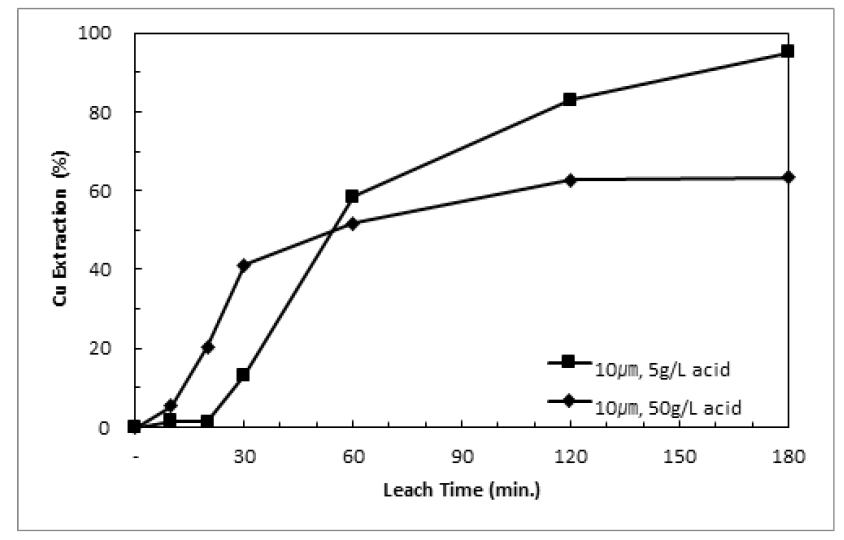
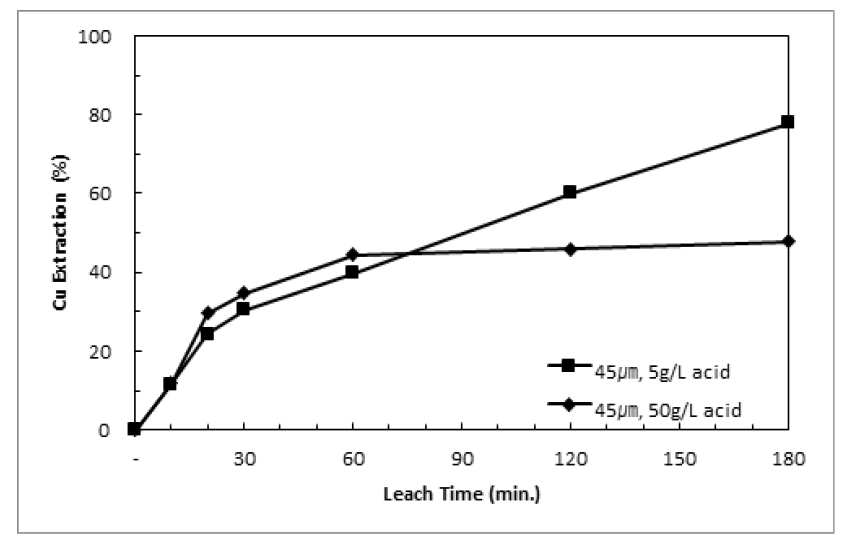
가압침출기에서 P90 10μm와 45μm의 황동석 정광시료를 5g/L와 50g/L 황산용액을 이용해 700kPa와 150℃에서 3시간 침출한 결과를 Fig. 2와 Fig. 3에 나타내었다. 침출 후 60분까지 모든 조건에서 구리의 침출율이 증가하지만 황산농도가 5g/L인 경우 구리 침출율이 지속적으로 증가하는 것에 비해, 황산농도가 50g/L인 경우 침출율의 증가가 멈추거나 상승속도가 매우 느려진다. 황산농도가 5g/L이고 P90 10μm 정광시료를 침출한 경우 침출율은 180분에 95%까지 증가하는 것을 관찰하였으나 50g/L이고 P90 45μm 정광을 침출하는 경우 180분에 침출율은 48%에 불과하다. 침출실험 중 단체황이 생성되며 입자의 응집되는 현상이 관찰되었으며, 실험 후 침출잔사에 대해 32μm 체를 사용하여 분리하고 결과를 Table 3에 나타내었다. 5g/L로 침출하는 경우보다 50g/L로 침출할 때 응집효과가 뚜렷이 관찰되었으며, Fig. 4에 나타낸 바와 같이 침출 후 입자가 응집된 것이 관찰되었다. 즉, 황산 농도가 높을수록 단체황이 발생하며 응집효과에 의해 60분 이후 침출이 저하된 것으로 판단할 수 있다.
Table 3.
Size Distribution of leach residue particles
| Conditions | Fraction | |
| -32μm | +32μm | |
| P90 10μm, 5g/L acid | 0.54 | 0.46 |
| P90 10μm, 50g/L acid | 0.42 | 0.58 |
| P90 45μm, 5g/L acid | 0.47 | 0.53 |
| P90 45μm, 50g/L acid | 0.29 | 0.71 |
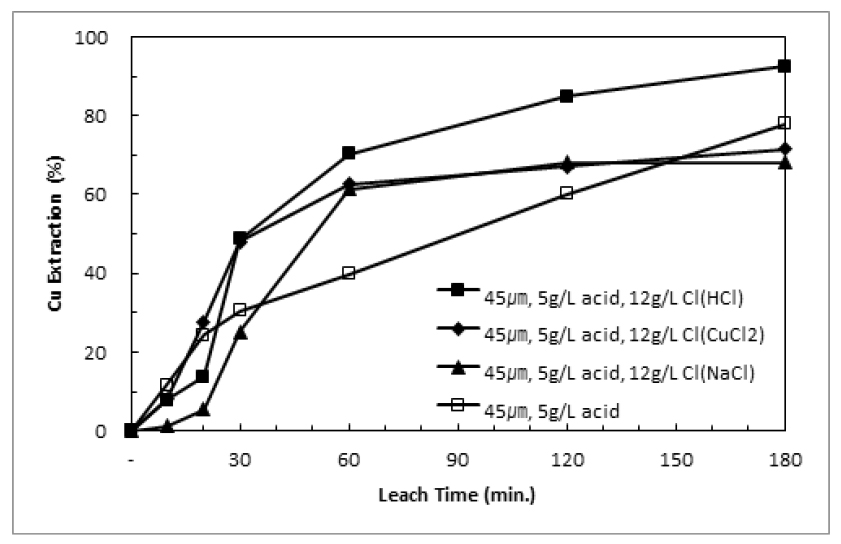
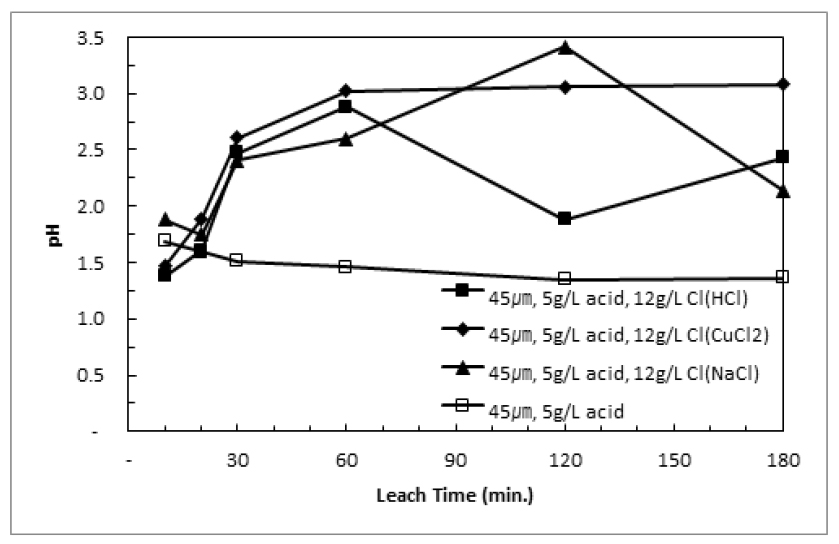
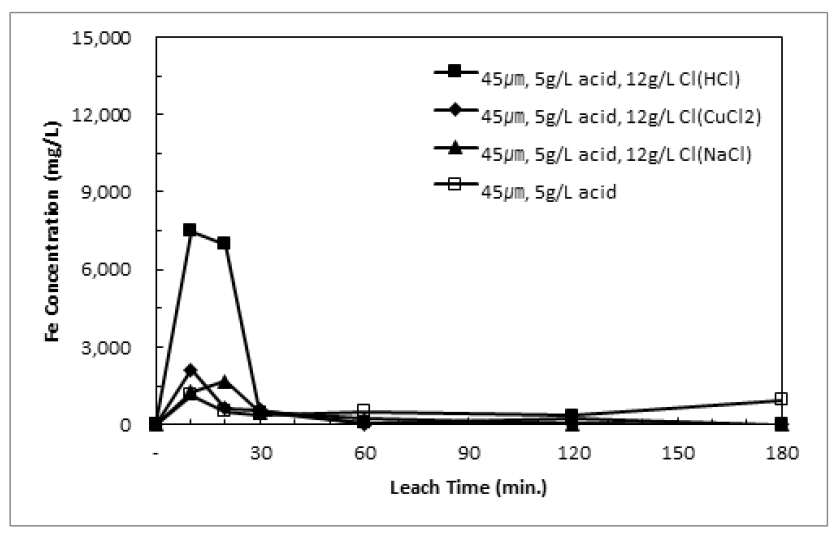
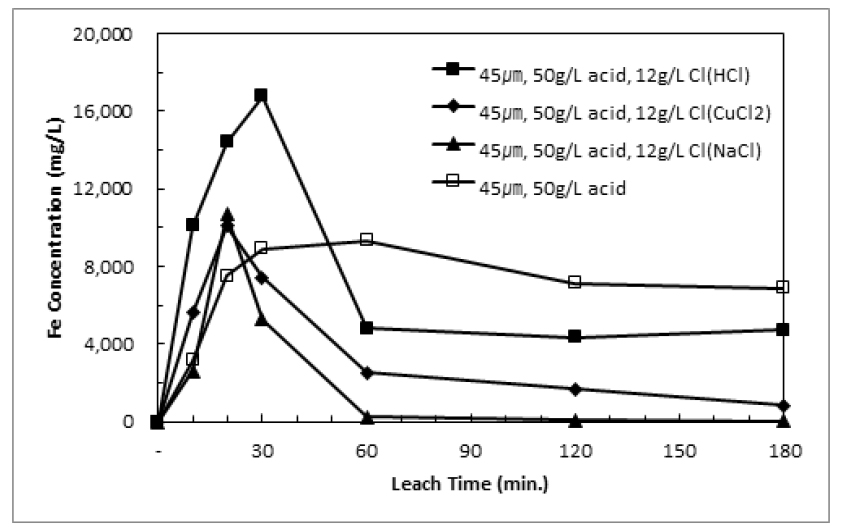
황동광의 가압침출 중 염소이온이 첨가될 경우 황동석의 침출률을 상승시킴과 동시에 침출액의 철의 농도 제어가 가능한 것으로 알려져 있다8). 이 연구에서는 염산, 염화구리, 염화나트륨을 첨가하여 구리 침출에 대한 효과를 조사하고자 하였다. Fig. 5에 각 화합물 첨가에 따른 구리침출거동을 나타내었다. 염소이온을 첨가한 경우 초기 침출속도가 약간 상승하나 염산을 첨가할 경우 침출율이 상승하는 것에 비하여 염화구리와 염화나트륨을 첨가하는 경우는 큰 차이가 나타나지 않았다. Fig. 6과 Fig. 7에 Fig. 5에 수행한 침출실험 중 pH와 철농도변화를 각각 나타내었다. 염소이온을 첨가한 경우 pH는 다소 상승한 것을 알 수 있으며, 이는 침출이 진행되며 수소이온이 소모된 것이 원인으로 생각된다.
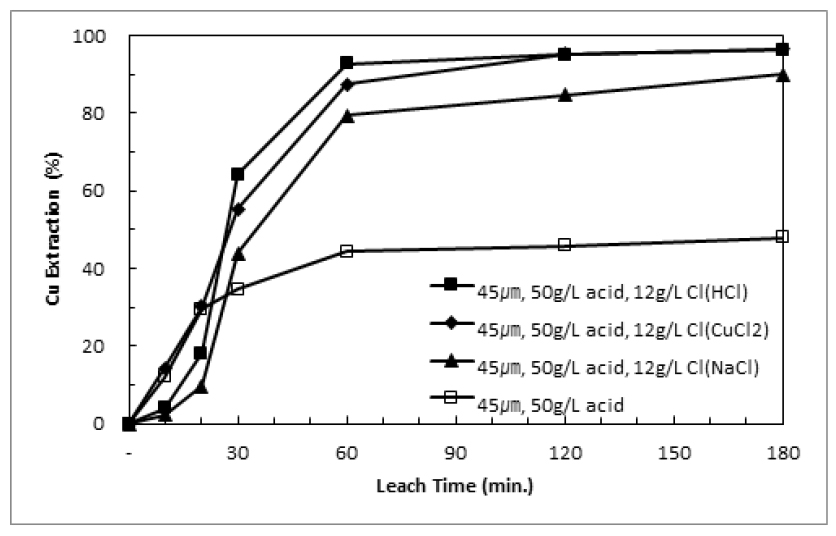
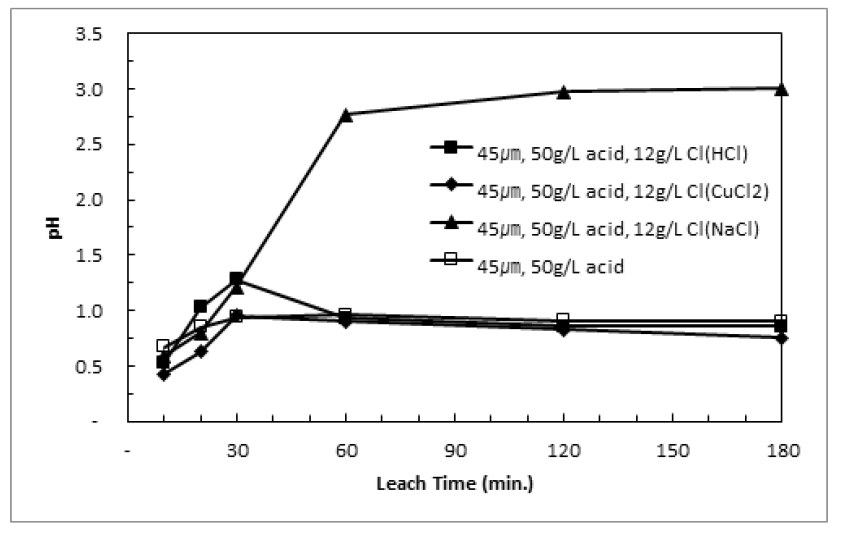
염소이온 첨가에 따른 침출개선효과를 검증하기 위해 50g/L 황산용액에서 가압침출실험을 진행하였다. Fig. 8에서 알 수 있듯이 염소이온을 첨가할 경우 침출효율개선효과가 뚜렷이 나타났으며, 염산과 염화구리를 첨가했을 때 180분에 침출율은 각각 96%와 97%로 나타났다. Fig. 9와 Fig. 10에 Fig. 8에서 수행한 실험 중 pH와 철농도 변화를 나타냈으며, 염화나트륨을 첨가한 경우 외에 pH의 거동은 유사하게 나타났다.
황동석의 가압침출반응은 식 (1)과 같이 나타낼 수 있으며, 산이 소모되기 때문에 pH가 상승하게 된다12). 그러나 침출반응이 진행됨에 따라 철이 수산화철이나 자로사이트로 침전되어 수산화이온이 소모되므로 pH가 감소하는 반응이 함께 발생한다. Fig. 10에서 알 수 있듯이 철 농도는 침출 반응 중 감소경향을 나타내며, 결국 침출에 의한 산의 소모와 철 침전에 의한 수산화이온의 소모의 균형이 pH변화를 나타내는 것으로 생각된다. 회수된 미립잔사를 대상으로 Table 4에 QXRD(Quantitative XRD)분석을 통한 광물학적 분석결과를 나타내었다. 5g/L 황산용액을 이용해 침출한 경우 적철석(Hematite)가 주로 관찰되었으나 50g/L 황산용액으로 침출한 경우 자로사이트와 침철석(goethite)가 주요한 철 침전물인 것으로 나타났다.
Table 4.
QXRD analyses of leach residues obtained from leaching tests with chloride ions
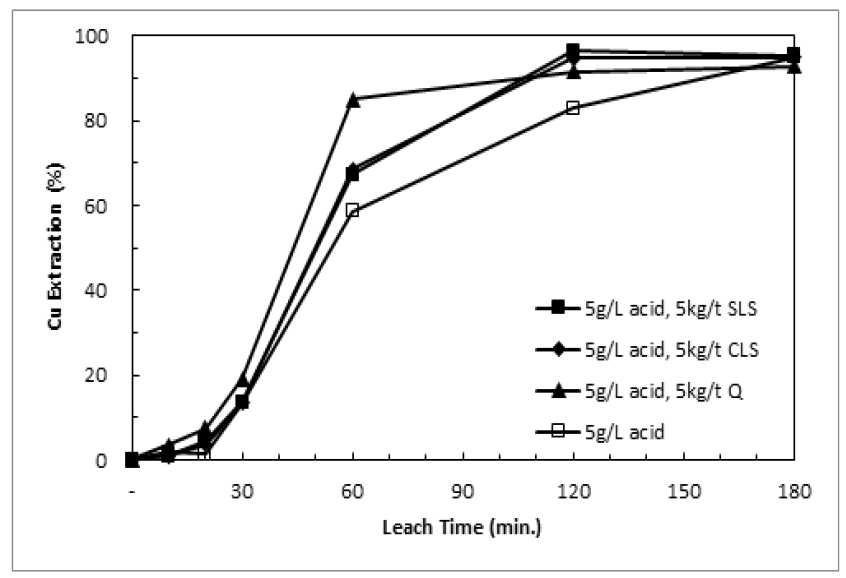
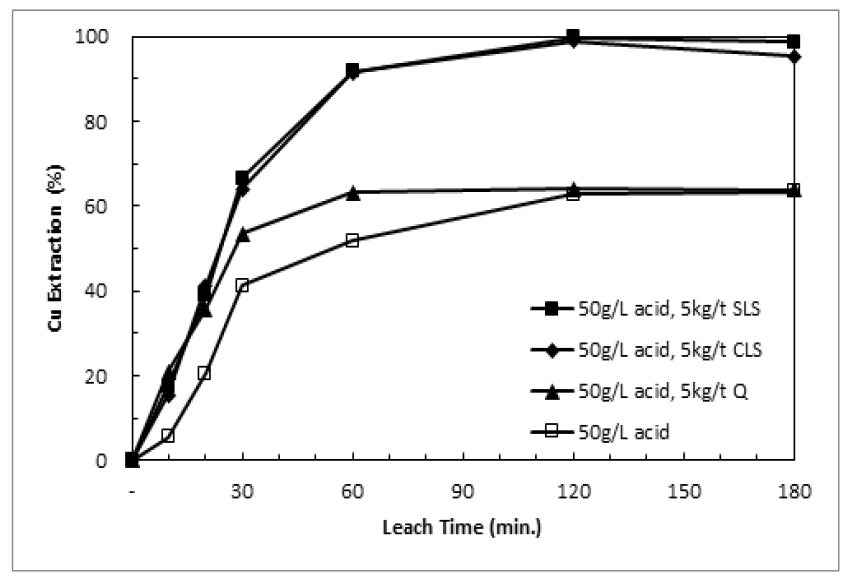
염소이온이 황동석 침출의 촉매역할을 하기 위해 첨가된다면 계면활성제는 단체황을 분산시켜 침출억제효과를 해소하기 위해 투입된다8). 본 연구에서는 Quebracho, SLS(Sodium lignosulfonate), CLS(calcium lignosulfonate)를 첨가하여 가압침출실험을 진행하였다. Fig. 11과 Fig. 12에 5g/L과 50g/L의 황산용액에서 구리침출에 대한 각각의 계면활성제 첨가효과에 대해 나타내었다. 5g/L의 황산용액을 사용했을 때 초기 구리 침출율 상승속도가 첨가하지 않은 경우에 비해 다소 빠르게 나타나지만 180분 침출을 진행한 경우 큰 차이가 관찰되지 않았다. 그러나 Fig. 12에서 알 수 있듯이 SLS나 CLS를 첨가한 경우 구리침출율은 크게 상승하여 99% 이상의 침출율을 나타냈으며, 이는 계면활성제에 의해 단체황이 분산되어 침출이 원만히 진행된 결과로 판단된다. 계면활성제를 첨가한 경우 침출 후 침전물을 회수하여 QXRD 분석을 진행하였고 Table 5에 결과를 나타내었다. Table 4의 결과와 마찬가지로 5g/L 황산용액을 사용한 경우 침전물 중 주요한 광물은 적철석이나, 50g/L 황산용액으로 침출을 진행했을 때 자로사이트의 양이 증가하며, 특히 침출율이 높았던 SLS와 CLS 첨가결과에서는 단체황이 29.5%와 19.5% 관찰되었다. 즉 분산된 단체황이 침전물 중에 온존되어 회수된 것으로 판단된다. 따라서 염소이온과 계면활성제 첨가에 의한 가압침출공정 중 구리침출율 개선효과가 존재하는 것으로 판단되었다.
Table 5.
QXRD analyses of leach residues obtained from leaching tests with surfactants
4. 결 론
황동석의 150℃의 중온 가압침출공정 중 구리침출율에 대한 염소이온과 계면활성제 첨가의 영향을 5g/L과 50g/L 황산용액에서 조사하였다. 염소이온으로 염산, 염화구리, 염화나트륨을 사용하였고, 계면활성제로 Quebracho, SLS(Sodium lignosulfonate), CLS(calcium lignosulfonate)를 첨가하였다.
황동석 정광의 D90 입도를 10μm와 45μm로 조절하여 가압침출실험을 진행했을 때 첨가제가 존재하지 않는 경우 황산농도를 5g/L에서 50g/L로 증가시켰을 때 응집잔사의 형성이 뚜렷이 관찰되어 침출율이 저하되었다. 염화이온의 경우 염산과 염화구리 첨가에 의한 구리침출율 상승효과가 뚜렷이 나타났으며, 180분 침출을 진행했을 때 염산과 염화구리 첨가시 침출율이 각각 96%와 97%로 분석되었다. 계면활성제 첨가의 경우 SLS와 CLS 첨가에 의한 구리침출율 상승효과가 뚜렷이 나타났으며, 180분 침출을 진행했을 때 99% 이상의 침출율을 나타내었다. 즉, 황동석의 가압침출에서 황산농도를 증가시킨 경우 응집잔사의 형성과 함께 구리의 침출율이 저하되나, 염소이온을 첨가하여 황동석의 침출을 촉진시키거나 계면활성제를 첨가하여 단체황 분산을 통해 구리침출율을 상승시키는 것으로 판단되었다.