1. 서 론
2. 실험방법
2.1. 실험재료
2.2. 실험방법
3. 결과 및 고찰
3.1. 회수·가공한 산화마그네슘의 반응성 평가
3.2. 회수·가공한 산화마그네슘 기반 시험체의 이산화탄소 포집 특성
4. 결 론
1. 서 론
산업화가 야기한 온실가스 증가는 기후위기를 촉발하였고, 이러한 기후위기에 대응하고자 유엔기후변화협약의 협정국들은 1997년 교토의정서에 이어 2016년 파리협정이 채택하여 온실가스 감축하고자 하였다. 2018년 10월 대한민국 인천 송도에서 개최된 제 48차 IPCC(기후변화에 관한 정부 간 협의체, Intergovernmental Panel on Climate Change) 총회에서 전 지구적으로 2030년까지 이산화탄소 배출량을 2010년 대비 최소 45 % 이상 감축하여야 하고, 2050년경에는 탄소중립을 달성하여야 한다는 결론에 도달하였다1). 이에 따라, 세계 이산화탄소 발생량의 7 %를 담당하는 시멘트 업계는 사회의 요구에 따라 지속가능한 산업으로의 전환을 진행 중에 있다2). 시멘트 산업의 친환경으로의 전환을 주도하는 다양한 연구 중 유력하게 연구되고 있는 분야는 대체 연료 혹은 대체 원자재 사용과 소성 공정의 에너지 효율 개선, 새로운 유형의 결합재를 통한 경화기술 개선과 시멘트 제품의 탄소 포집 능력 향상으로 나누어진다3). 이 중 시멘트 제품의 탄소 포집 능력 향상의 경우, CCUS(Carbon Capture, Utilization and Storage)기술 중 알칼리 토금속을 활용한 광물탄산화 방법으로 알려져 있으며 크게 직접 탄산화, 간접 탄산화, 기타 공정으로 분류된다4,5). 특히, 알칼리 토금속 중 마그네슘을 활용한 방법은 칼슘 기반의 탄산염보다 이산화탄소 고정량이 높은 것으로 알려져 있다6,7). 그러나, Miller and Myers8) 에 따르면 전주기적 관점에서 보았을 때에, 탄산마그네슘을 소성·가공하는 산화마그네슘 시멘트는 생산과정에서 이산화탄소의 총방출량이 흡착량에 비해 오히려 과다할 수 있으며, 현재 상용 중인 일반 포틀랜드 시멘트보다 큰 환경적 부하를 야기할 수 있음을 확인하였다8). 따라서, 알칼리 토금속 중 마그네슘을 기반으로 하는 이산화탄소 포집 메커니즘의 경우, Mg-Si계 광물에서 회수하는 방법과 산업부산물에서 합성하는 방법이 요구되고 있다.
간수는 천일염 생산 과정에서 발생하는 부산물로, 간수의 범위는 소금을 보관하는 과정 중에 조해작용에 의해 용출되거나 소금을 제조하는 과정에서 발생하는 부산물 액체를 통칭하기도 하며 천일염을 생산하고 부산되는 모액과 소금 가공공장에서 원심분리를 통해 분리된 액체도 간수로 분류된다. 이러한 간수는 고농도의 무기물을 포함하기 때문에 폐기물의 자원화 관점에서 다양한 연구를 통하여 유의미한 결과를 거두었으나 대부분 폐기되고 있는 실정이다9). 또한, 간수와 유사한 폐수인 해수담수화 과정에서 발생하는 농축수 역시 이와 비슷하게 폐기되고 있는 실정이다9,10,11). 그러나 농축수는 근래 물에 대한 필요성이 증가함에 따라, 해수 담수화 플랜트의 보급과 함께 농축수의 방출량이 증가하고 있으며, 그에 따른 부작용인 환경적 부하에 관하여 국내외적으로 관심이 높아지고 있는 실정이다. 그 예로 Park et al.10)에 따르면 농축수의 농도에 의한 해산물 독성평가가 각국에서 연구되고 있으며, 염분의 증가에 따른 치사율이 선형적으로 증가하는 형태를 띄어 적절한 처리와 관리가 요구되고 있음을 보여주고 있다10). 그에 따라 이러한 농축수의 친환경적 처리와 리싸이클링을 위한 연구도 수행되고 있으며, 그 예로 Bang et al.11)에 따르면 해수담수화 농축수에서 마그네슘과 칼슘을 회수하여 이산화탄소 포집체로서의 실험적 시도와 하이드로마그네사이트와 같은 마그네슘 기반 탄산화물을 형성한 연구도 존재하고 있다11).
기존 연구의 경우, 간수에서의 유가금속의 회수법과 회수된 마그네슘의 물리·화학적 분석에 그쳤으며 회수한 유가금속의 직접적 활용과 그에 대한 양상에 관한 연구가 부족한 실정이었다. 이에 따라 본 연구에서는 Miller and Myers8)에서 제기된 바와 같이 환경적 부하가 예상되는 마그네사이트의 소성이 아닌 폐기되는 간수에서 마그네슘을 회수하고 이를 가공하여 만든 산화마그네슘을 기반으로 이산화탄소 포집형 시험체로써의 적용 가능성을 검토하고 회수된 마그네슘의 물리·화학적 특성 분석과 간접 탄산화 과정에서의 이산화탄소 포집 가능성을 평가하였다.
2. 실험방법
2.1. 실험재료
2.1.1. 실험 원재료
대조군으로서 사용된 브루사이트(Mg(OH)2) 광석의 경우, 러시아산 광석을 수입하여 분쇄 및 판매하는 S업체를 통하여 구매하였다. 원시료의 물리·화학적 분석을 위하여 Rigaku사의 ‘ZSX Primus Ⅱ’ 장비를 활용한 X선 형광분석(X-ray Fluorescence Spectrometer, XRF)을 수행하였다. 측정된 시료의 화학적 구성을 Table 1에 나타내었다. 시료의 결합구조와 결정성을 분석하기 위하여 Bruker사의 ‘D8 ADVANCE’ 장비를 활용한 X선 회절 분석(X-ray Diffraction analysis, XRD)을 수행하였다. 간수의 경우 G사에서 연구목적으로 제공받아 사용하였다. 간수는 액상의 시료로 양이온의 경우, Thermo Fisher Scientific사의 ‘iCAP 7400 Duo’ 장비를 활용한 ICP-OES(Inductively Coupled Plasma-Optical Emission Spectrometry)분석을 수행하여 Mg2+, Ca2+, K+, Na+ 이온의 농도를 측정하였으며, 음이온의 경우 Dionex 사의 ‘ICS-1100’ 장비를 활용한 IC(Ion Chromatography) 분석을 통해 Cl-, SO42- 이온의 농도를 측정하여 Table 2에 함께 나타내었다.
Table 1.
Chemical composition of brucite ore (Unit : mass%)
| MgO | CaO | SiO2 | Fe2O3 | Al2O3 | |
| Brucite ore | 86.119 | 6.964 | 6.471 | 0.257 | 0.189 |
Table 2.
Chemical concentration of brine (Unit : g/L)
| ICP | IC | |||||
| Mg2+ | Ca2+ | K+ | Na+ | Cl- | SO42- | |
| Brine | 41.069 | 19.826 | 39.437 | 31.280 | 191.00 | 0.500 |
2.1.2. 간수에서의 마그네슘 회수와 산화마그네슘 가공
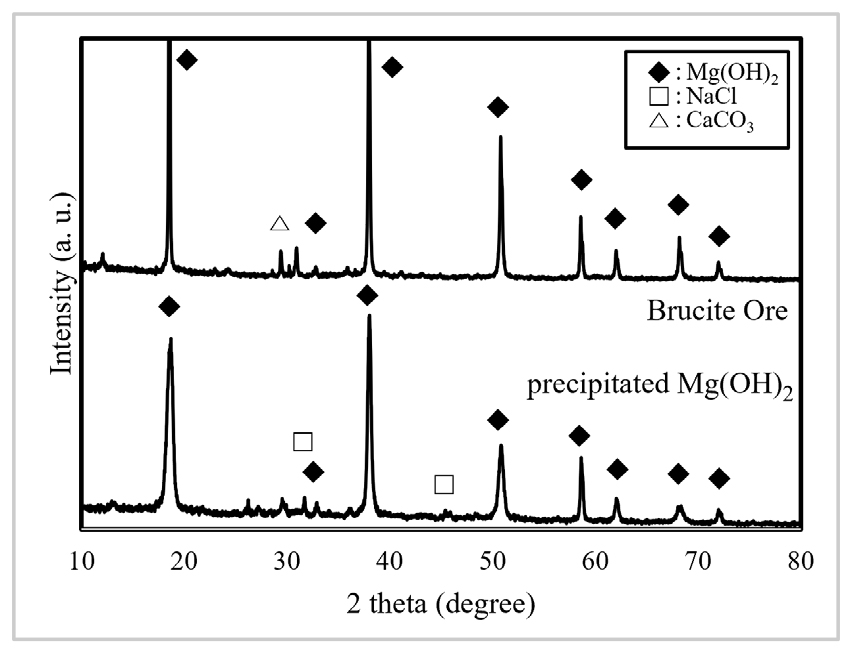
간수에서의 마그네슘 회수에 관한 연구는 다양한 염기성 용액을 통한 추출과 활용에 관하여 국내외적으로 연구 중이다. 본 연구에서는 앞서 연구된 자료들을 토대로 가장 효율적이라고 평가받는 방법인 2 M의 수산화나트륨을 활용한 pH swing 법을 적용하였다12). 간수에 수산화나트륨 수용액을 첨가하여 수산화마그네슘을 결정화시킨 후 고액 분리를 통해 고상의 시료를 회수하였다. 회수과정에서 공침된 불순물을 분리하기 위하여 40 ℃ 초순수에서 300 rpm으로 12시간 교반하여 고액 분리를 통해 고상의 시료를 회수하여 105 ℃ 오븐에서 건조 후 분석 및 실험을 수행하였다. 회수된 수산화마그네슘을 XRF, XRD 분석을 수행하여 Table 3과 Fig. 1에 작성하였다.
Table 3.
Chemical composition of precipitated Mg(OH)2 from brine (Unit : mass%)
| MgO | CaO | Cl | Na2O | K2O | SiO2 | SO3 | |
| Brucite from brine | 87.03 | 7.84 | 3.45 | 0.79 | 0.61 | 0.14 | 0.14 |
수산화마그네슘의 시료에서 이산화탄소를 흡착하는 산화마그네슘으로의 탈수반응을 유도하는 소성과정을 거쳐 산화마그네슘으로 가공하고자 하였으며, 유도되는 식은 아래 식 (1)과 같다. 일반적으로 수산화마그네슘의 탈수가 일어나는 온도는 400-700 ℃로 알려져 있으나 시료의 합성과 분쇄 과정에서의 차이 및 결정화 정도에 따라 탈수되는 온도가 다르기 때문에, 최적의 소성 온도를 구하기 위하여 시료를 WATERS 사의 ‘Discovery SDT 650’ 장비를 활용하여 동시열분석(Simultaneous Differential Scanning Calorimetry Thermogravimetric Analyzer, SDT) 을 수행하였으며 질소 환경에서 상온에서 800 ℃까지 분석을 수행하였다. 그 결과 500 ℃에서 두 시료가 모두 탈수가 완료된 것을 확인하여, 시료를 500 ℃ 전기로에서 한 시간 소성함으로써 산화마그네슘을 가공하였다.
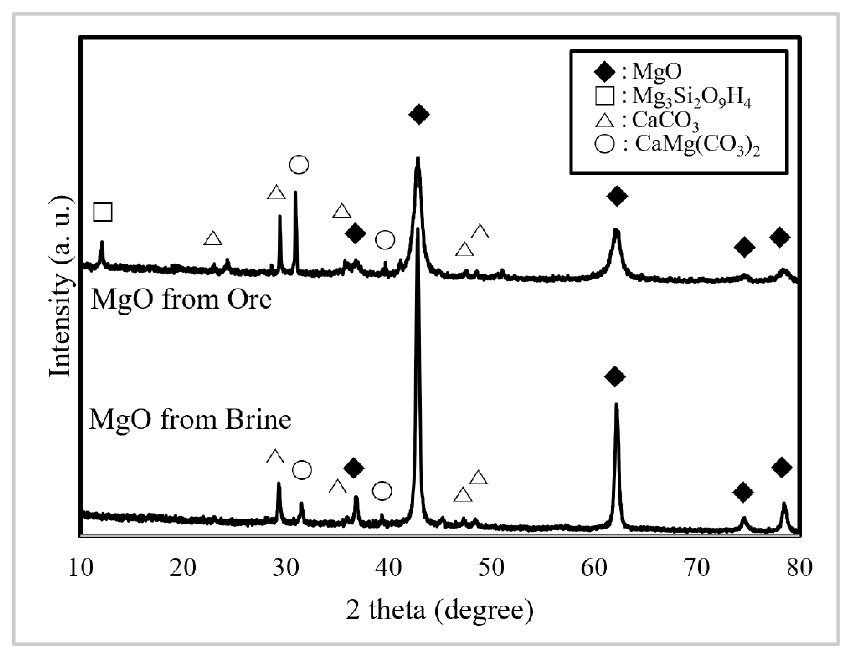
소성이 완료된 산화마그네슘의 XRD 분석을 수행하였으며 Fig. 2에 나타내었다.
2.2. 실험방법
2.2.1. 반응성 실험
소성 완료된 시료의 물리적 특성을 평가하기 위한 분체에 대한 평가 방법 중 하나로 분체의 반응성 평가가 제시되고 있다. 분체의 반응성에 대한 평가는 시험체의 수화 및 탄산화 반응에 대한 직접적 영향을 미치는 평가 지표로 해석할 수 있다. 해외의 경우 ASTM C 1897을 통하여 혼화재료에 관한 반응성 시험 방법으로 제시하고 있으며, 그와 더불어 많은 연구에서 분체의 반응성 평가에 대한 실험 방법으로 시트르산과 아세트산을 활용한 산 환경에서 혼화재료의 중성화 반응 속도를 판별하여 분체의 반응성을 비교하는 방법을 채택하고 있다. 특히, 시멘트 혼화재료로서 소성한 산화마그네슘의 반응성 지표로 60초보다 빨리 도달할 때 높은 반응성, 180초에서 300초 사이에 도달할 때 중간 반응성, 600초 이상 소요될 때 낮은 반응성으로 평가한다. 본 연구에서는 앞선 연구의 실험방법을 차용하여 본 연구에서 제조된 산화마그네슘 두 시료에 대한 반응성을 평가하고자 하였다13,14,15). 시료의 입도는 입자의 크기로, 입도가 작게 나타날수록 시료의 비표면적이 증가하여 반응성이 증가하는 경향을 갖는 것으로 알려져 있다. 이러한 시료의 반응성 평가에 대한 보조지표로 활용하기 위하여 시료의 입도를 분석하였다. 분석장비로는 Particulate Systems 사의 NanoPlus HD 장비를 활용하였다.
2.2.1.1. 시트르산을 활용한 반응성 실험
2.0 g의 산화마그네슘을 분취하여 마그네틱 교반기에서 300 rpm으로 회전하는 0.4 N 시트르산 용액 100 ml에 첨가하여 pH 8.6까지 도달하는 시간을 측정한다.
2.2.1.2. 아세트산을 활용한 반응성 실험
5.0 g의 산화마그네슘을 분취하여 마그네틱 교반기에서 300 rpm으로 교반하는 1.0 M의 아세트산 용액 100 ml에 첨가하여 pH 7에 도달하는 시간을 측정한다.
2.2.2. 시험체의 배합과 양생
간수와 광석에서 회수한 산화마그네슘과 이를 기반으로 탄산화를 개선하는 중탄산나트륨을 배합하여 이산화탄소 포집형 시험체를 Table 4와 같이 계획하였다. 일반적인 산화마그네슘의 수화 및 탄산화 메커니즘은 앞서 연구되었던 MgO-H2O-CO2 system 에 따라서 진행되며 양생되는 이산화탄소의 분압에 의해서 순차적으로 탄산화되는 것으로 알려져 있다16,17). 중탄산나트륨의 경우, 물에서 용해시 이온화를 통하여 배합수 상의 중탄산염을 가함으로 이온화된 마그네슘의 탄산화를 돕는 혼화재로 알려져 있으며 또한, 산화마그네슘과 수산화마그네슘에 대한 촉매작용을 함으로써 수용액상의 용해를 촉진하는 것으로 알려져 있다. 수용액상의 중탄산염은 수산화마그네슘과 산화마그네슘 표면에 결합하여 다배위 단핵 표면 착물을 형성하고 이로 인해 산화마그네슘의 구조가 약해져 용해과정이 촉진되며 이후, 반응 물질로도 참여하여 탄산염 생성을 촉진시킨다18,19). 따라서, 본 연구에서는 회수하여 얻은 산화마그네슘과 탄산 촉진제를 5, 10 % 중량비로 치환하여 Table 4와 같이 혼화재를 반영한 마그네슘 기반 이산화탄소 포집형 시험체를 배합하였다. 양생 조건은 상압에서의 촉진 탄산화 조건으로 CO2 20 %, 상대습도 95 %, 온도 25 ℃으로 설정하였으며, 이를 유지할 수 있는 CO2 항온·항습기에서 28일간 양생하였다. Soares and Castro-Gomes20)에 따르면 제시된 촉진 탄산화 조건은 산화마그네슘의 탄산화 유도를 용이하게 하여 시험체의 이산화탄소 포집을 역량을 단기간에 평가할 수 있는 조건으로 채택하고 있다20). 제시된 촉진 탄산화 양생이 종료된 이후, 시험체를 105 ℃ 오븐에서 24시간 건조한 뒤에 XRD 분석과 질소 환경에서 25-800 ℃까지 SDT 분석을 수행하였다.
3. 결과 및 고찰
3.1. 회수·가공한 산화마그네슘의 반응성 평가
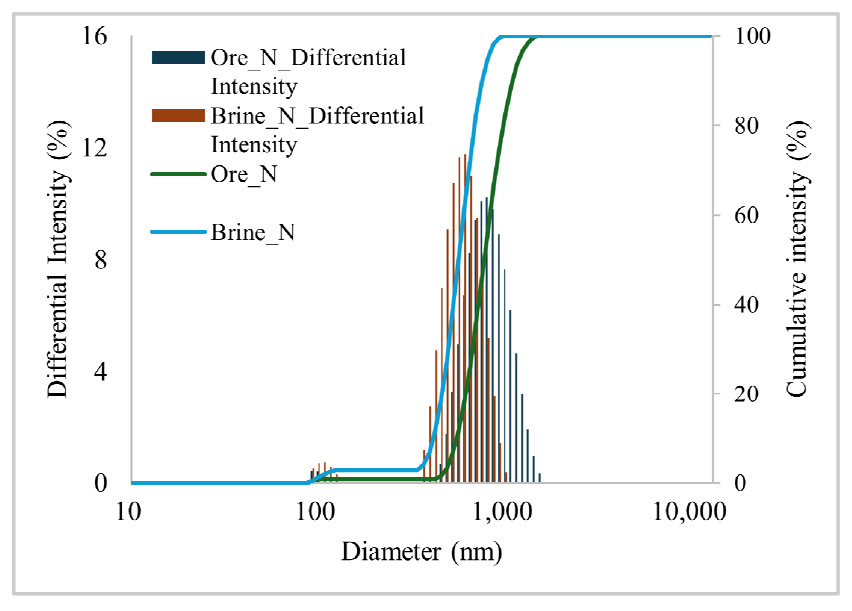
시트르산을 활용한 반응성 시험 결과, 광석에서 회수한 산화마그네슘의 경우 183초 소요되었으며, 간수에서 회수한 산화마그네슘의 경우 75초 소요되었다. 아세트산을 활용한 반응성 시험 결과, 광석에서 회수한 산화마그네슘의 경우, 24초 소요되었으며, 간수에서 회수한 산화마그네슘의 경우, 12초 소요되었다. 두 시험법의 결과에 따르면 간수에서 회수한 산화마그네슘이 광석에서 회수한 산화마그네슘에 비해 상대적으로 높은 반응성을 갖는 것으로 나타났으며, 광석에서 회수한 산화마그네슘의 경우 시트르산 법에서는 중간 반응성, 아세트산 법에서는 높은 반응성을 갖는 것으로 나타났다. 이는 입도 분석 결과를 나타낸 Fig. 3에 따르면 간수에서 회수된 산화마그네슘이 광석에서 회수한 산화마그네슘에 비해 입자의 크기가 상대적으로 작기 때문인 것으로 판단되었다. 이러한 차이는 시료의 합성과 자연적으로 형성된 광물의 분쇄의 차이에서 비롯된 것으로 판단할 수 있었다. 마그네슘 이온이 수용액 상태로 존재할 때에 첨가되는 염기성 반응 물질의 농도와 투입 속도, 온도에 따라 그 입자의 크기가 다르게 형성되고 반응 시간이 증대됨에 따라 입자가 성장하여 그 크기가 변화할 수 있는 것으로 알려져 있다21,22,23). 따라서, 본 연구에서 사용된 합성 산화마그네슘의 입자가 자연적으로 형성된 광물을 분쇄하여 얻은 시료에 비해 상대적으로 입자의 크기가 작고 조밀하게 분포되어 산과 맞닿는 비표면적이 넓어 상대적으로 높은 반응성을 갖는 것으로 판단되었다.
3.2. 회수·가공한 산화마그네슘 기반 시험체의 이산화탄소 포집 특성
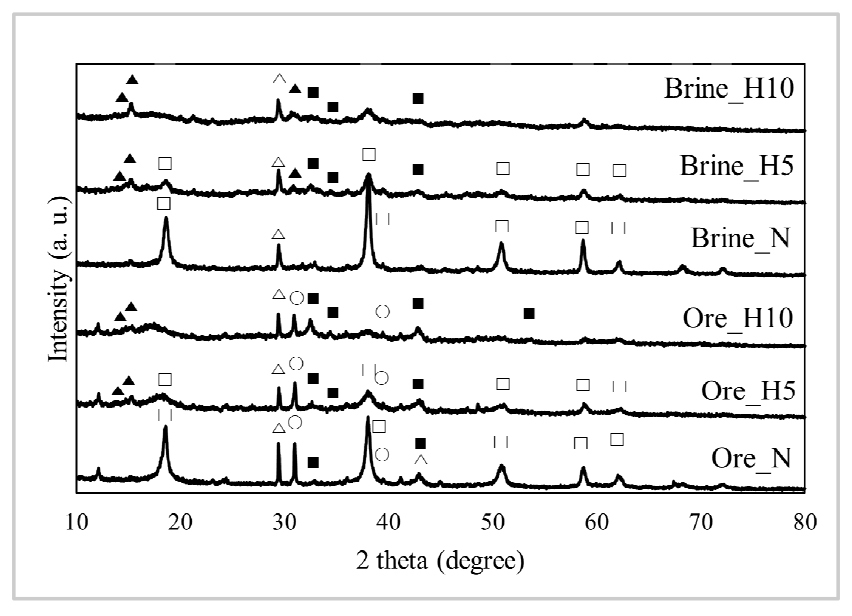
간수와 광물에서 회수한 산화마그네슘을 기반으로 탄산화를 돕는 중탄산나트륨을 첨가하여 Table 4와 같이 배합하여 28일간 CO2 항온·항습기에서 양생하였다. 양생이 완료된 시험체를 분쇄하여 XRD 분석을 수행하였으며 그 결과를 Fig. 4에 나타내었다. 모든 시험체에서 산화마그네슘의 피크를 확인할 수 없었다. 이는 두 시료의 높은 반응성으로 인하여 시료의 표면에 수화되지 못한 산화마그네슘 결정을 확인하기 어려웠다.
28일간 CO2 항온·항습기에서 양생하였음에도 불구하고 탄산화를 개선하는 혼화재를 넣지 않은 시험체인 Ore_N과 Brine_N에서 마그네슘 기반의 탄산화 결정체를 확인하기 어려웠다. 이는 앞서 연구되었던 Königsberger et al.16)와 Hänchen et al.17)에 따르면 MgO-H2O-CO2 system에 따라 본 연구에서 조성된 양생의 환경은 열역학적으로 안정적인 마그네사이트의 형성이 유도되어야하지만, 높은 반응성으로 인하여 수화 반응으로 전환된 경우, 브루사이트가 산화마그네슘 표면에서 수화 결정체를 형성하게 된다. 이렇게 산화마그네슘 표면에 형성된 브루사이트는 피막과 같은 역할을 하여 산화마그네슘의 이산화탄소와의 접촉을 제한하고 탄산화로의 전환을 억제하였음을 확인하였다24,25).
반면, 탄산화 과정을 돕기 위한 혼화재가 첨가된 시료에서는 하이드로마그네사이트(Mg5(CO3)4(OH)2·4H2O)와 마그네사이트(MgCO3)와 같은 탄산염 광물이 형성된 것을 확인할 수 있었다. 특히, 중탄산나트륨의 혼입량이 10 %의 시험체가 5 %의 시험체에 비해 탄산염광물의 결정화도가 증대되었으며, 브루사이트(Mg(OH)2)의 결정화도는 감소하였음을 확인할 수 있었다. 이는 수화과정 중 배합수에 용해되어있는 중탄산염이 이온화된 마그네슘과 반응하여 하이드로마그네사이트(Mg5(CO3)4(OH)2·4H2O)를 형성하는데 직접적인 영향을 미쳤음을 확인할 수 있었다. 또한, Dung and Unluer26)에 따르면 산화마그네슘 사이의 중탄산나트륨은 시험체 매트릭스 내에서 씨앗의 역할을 하면서 시험체 내의 반응할 수 있는 비표면적을 증대시키고, 배합수 내의 HCO3- 이온을 직접적으로 증대시킴으로써 시험체 내의 산화마그네슘의 탄산화를 가속시킬 수 있음을 확인하였다. 따라서, 중탄산나트륨을 포함한 시험체에서 하이드로마그네사이트(Mg5(CO3)4(OH)2·4H2O)와 마그네사이트(MgCO3)의 상대적으로 더 높은 결정성을 갖게 된 것으로 판단되었다26).
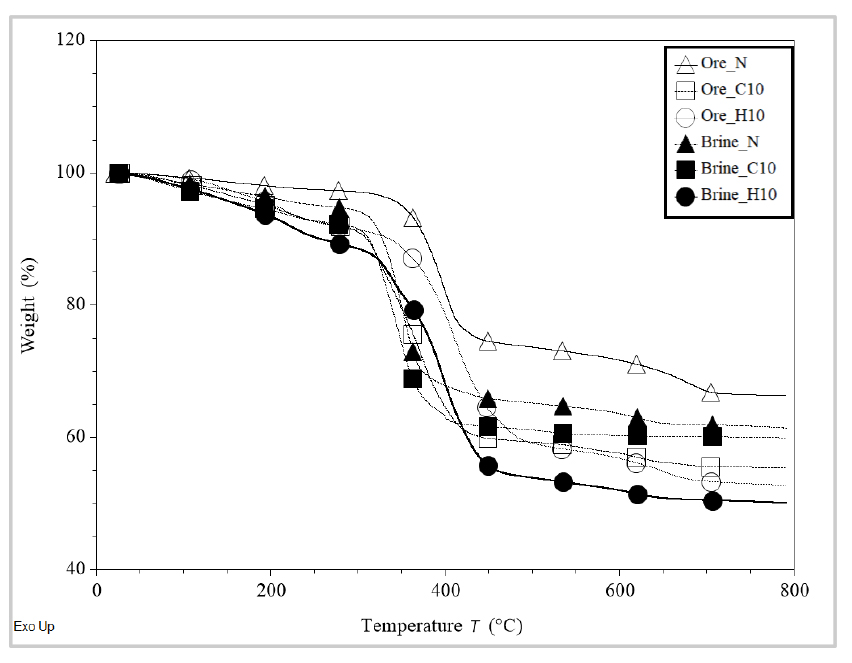
모든 시험체를 질소 환경에서 상온에서 800 ℃까지 동시열분석 결과를 Fig. 5에 나타내었으며, 그에 대한 중량 감소율을 수치화하여 Table 5에 함께 나타내었다. 시험체의 탄산화를 개선하기 위하여 첨가하였던 중탄산나트륨의 배합량 증가시 시험체의 전반적인 중량 감소율이 증대되는 것을 확인할 수 있었다. 특히, 300-500 ℃구간에서의 중량 감소율이 증대되었는데, 이는 브루사이트의 탈수반응이 일어나는 구간과 하이드로마그네사이트, 마그네사이트의 탈탄산화가 일어나는 구간으로, XRD 분석 결과와 함께 비교시 중탄산나트륨이 첨가되면서 탄산화가 개선되었음을 확인할 수 있었다27). 50-300 ℃구간에서도 중량 감소율이 증대되었는데, 이는 하이드로마그네사이트, 마그네사이트에 함께 형성되었던 수화물이 탈수되는 과정에서 발생하는 중량 감소로 보통 240-280 ℃부근에서 피크를 형성하는 것으로 알려져 있다28). 500-800 ℃ 부근에서 광석시료에서 상대적으로 두드러지는 중량 감소율은 브루사이트 광석에서 함께 검출되었던 칼사이트(Calcite)의 이산화탄소 해리과정에서 나타나는 중량 감소로 판단되었다.
Table 5.
Mass loss of all samples obtained by SDT after 28 days of carbonation
4. 결 론
본 연구에서는 환경적 부하가 예상되는 마그네사이트의 소성이 아닌 폐기되는 간수에서 마그네슘을 회수하고 이를 가공하여 만든 산화마그네슘을 기반으로 이산화탄소 포집형 시험체로서의 적용 가능성을 검토하고 회수된 마그네슘의 물리·화학적 특성 분석과 간접 탄산화 과정에서의 이산화탄소 포집 가능성을 평가하였으며 중탄산나트륨에 의한 탄산화 개선도 함께 평가하여 다음과 같은 결론을 얻었다.
간수에서 회수 및 소성한 산화마그네슘은 브루사이트 광물에서 소성한 산화마그네슘과 소성온도를 같이할 시, 브루사이트 광석 기반 산화마그네슘에 비해 높은 반응성을 띄며, 입도 분석 결과 더 작은 입자의 산화마그네슘을 합성할 수 있었다. 하지만, 높은 반응성은 수화 반응시 브루사이트 결정을 만들어 피막을 형성하여 추가적인 수화를 제한하고 그에 따른 탄산화도 함께 제한됨을 확인하였다.
탄산화 반응의 개선을 위해 배합된 중탄산나트륨은 시험체를 25 ℃, 95 %의 상대습도, 20 %의 이산화탄소 농도를 유지하는 CO2 항온·항습기에서 28일 양생시, XRD 분석결과 시험체의 탄산화 반응이 개선되었음을 확인할 수 있었으며, 혼입량이 증가할수록 브루사이트 피크의 결정도가 감소하고 하이드로마그네사이트와 마그네사이트 피크가 증가함을 확인할 수 있었다. SDT 분석 결과 중탄산나트륨 배합시 50-300 ℃ 구간과 300-500 ℃ 구간에서 중량감소율이 증가하였으며, 이는 중탄산나트륨이 첨가되면서 탄산화 반응이 개선되었음을 확인할 수 있었다.
이러한 결과는 간수에서의 마그네슘 회수와 이를 활용한 이산화탄소 포집형 시험체를 개발함에 있어, 회수된 산화마그네슘의 높은 반응성은 시험체의 이산화탄소 포집 능력을 제한할 수 있음을 확인하였다. 또한, 중탄산나트륨을 혼입함으로써 제한된 이산화탄소 포집 능력을 개선할 수 있음도 확인하게 되었다. 본 연구 결과는 향후 각국에서 폐기되고 있는 간수와 해수담수화 농축수의 재활용에 기초 자료로 기여할 수 있을 것으로 판단된다.