1. 서 론
리튬계 이차전지는 휴대전화, 컴퓨터, 전기 자동차 등의 산업 확대와 더불어 그 수요가 상승하고 있다1,2). 그중 리튬인산철(LiFePO4, LFP) 전지는 우수한 안정성 및 상대적으로 저렴한 비용으로 인하여 미국의 테슬라를 비롯한 전기차 업계에서 상용화하는 등 LFP의 사용이 증가하고 있다3,4). 이러한 전지의 수요 증가는 폐리튬이온전지의 증가로 이어지며 2025년까지 약 100만 톤의 폐전지가 발생할 것으로 예측된다5). 또한, 리튬계 전지 관련 시장이 확대됨에 따라 핵심 소재인 리튬의 수요 또한 증가하고 있으나 매장량이 제한된 천연 리튬 자원은 그 수요를 맞추기에 어려운 실정이다6,7,8). 더욱이 리튬 자원은 가격 변동성이 크고 지역적 편재성이 큰 자원으로 수입 의존성이 크기 때문에 리튬 자원을 회수하여 재사용하는 연구가 필요하다. 동시에 폐리튬이온전지에 포함된 전해질, 중금속 및 유기화합물의 누출은 환경오염 및 인간의 건강에 큰 위협이 될 것으로 보인다9,10). 따라서 위와 같은 문제들을 해결하기 위해서 폐전지로부터 리튬 자원을 회수하여 재활용하는 연구와 활발히 진행되고 있다11,12,13,14,15).
일반적으로 폐LFP 전지의 재활용 연구는 크게 직접 재생법 및 습식 공정법이 있다. 직접 재생법의 경우 사용 중 구조의 변화 없이 손실된 리튬을 보충하여 재사용하며 공정이 단순하지만, 불순물 제어가 어려워 재활용 후 전기화학적 성능이 떨어지게 된다16,17,18). 전통적인 습식 공정에 있어 고농도의 산을 이용한 침출과정은 리튬뿐만이 아닌 타 성분이 함께 침출되어 이를 분리하는 공정이 추가로 필요하다19). 따라서 전 성분을 침출하는 것이 아닌 리튬을 선택적으로 선침출 하는 연구가 수행되었으며, 옥살산, 구연산, 아세트산과 같은 약산을 활용하여 리튬을 회수하는 연구도 수행되었다20,21,22). 또한, 과황산나트륨, 과황산칼륨, 그리고 과황산암모늄과 같은 산화제를 침출제로 이용한 연구들도 수행되었다23,24,25,26,27). 그러나 위와 같은 방법은 리튬을 선택적으로 회수할 수 있지만, 불순물에 대한 선택성, 경제성, 그리고 산의 사용에 따른 추가적인 환경오염 등을 내포하고 있다.
최근에는 폐LFP를 재활용하기 위하여 동형치환 반응이 제시되었다. Liu et al.은 LFP와 NaCl을 기계화학적 방법을 통하여 Na+와 Li+ 사이의 동형치환 반응을 이용해 NaFePO4와 Li2CO3를 얻을 수 있었다고 하였다28). Dai et al.은 LFP의 리튬 침출에 Fe2(SO4)3 및 H2O2 이용하였으며, 이는 Fe3+가 LFP의 Fe2+를 동형치환하여 Li+을 방출하였고 이에 리튬을 약 96% 이상 추출할 수 있다고 하였다29). Niu et al.은 시약급 FeCl3·6H2O 및 H2O2 이용하여 Fe3+가 LFP와 동형치환 반응을 발생시켜 리튬을 침출하였으며, 이후 용매추출법을 이용하여 철 제거 및 리튬을 회수하는 연구를 수행하였다30). 산의 소모를 줄이고 빠른 반응을 통한 리튬의 침출이 수행되었다. 그러나 위와 같은 Fe3+에 의한 리튬 침출 및 회수에 관한 연구에서는 철 제거에 있어 비교적 공정비용이 비싼 용매추출을 이용하였으며, 시약급 FeCl3·6H2O를 침출제로 사용하여 부족한 산화력을 보충하기 위하여 H2O2를 첨가하였다.
본 연구에서는 염화철 에칭액을 활용하여 동형치환 반응을 적용하였으며, 리튬의 침출 효과 및 회수 방법 연구하였다. 기존의 Fe3+가 포함된 침출제에서는 동형치환 과정에서 부족한 산화력을 보완하기 위하여 H2O2와 같은 추가적인 첨가제를 투입하였다. 그러나 본 연구에서는 염화철 에칭액을 사용하였으며, 이에 추가적인 첨가제를 투입하지 않았다. 또한, 염화철 에칭액의 농도에 따른 리튬의 침출율을 비교하였으며, 단순한 공정을 통하여 철을 제거하였다. 이후 철이 제거된 리튬 용액에서 탄산리튬을 합성하였으며, 이의 분말 특성을 분석하였다. 최종적으로 리튬의 침출율 및 분리 효율을 비교하였으며, 리튬의 선택적 침출 및 회수에 관하여 동형치환 반응의 가능성을 확인하였다.
2. 실험 방법
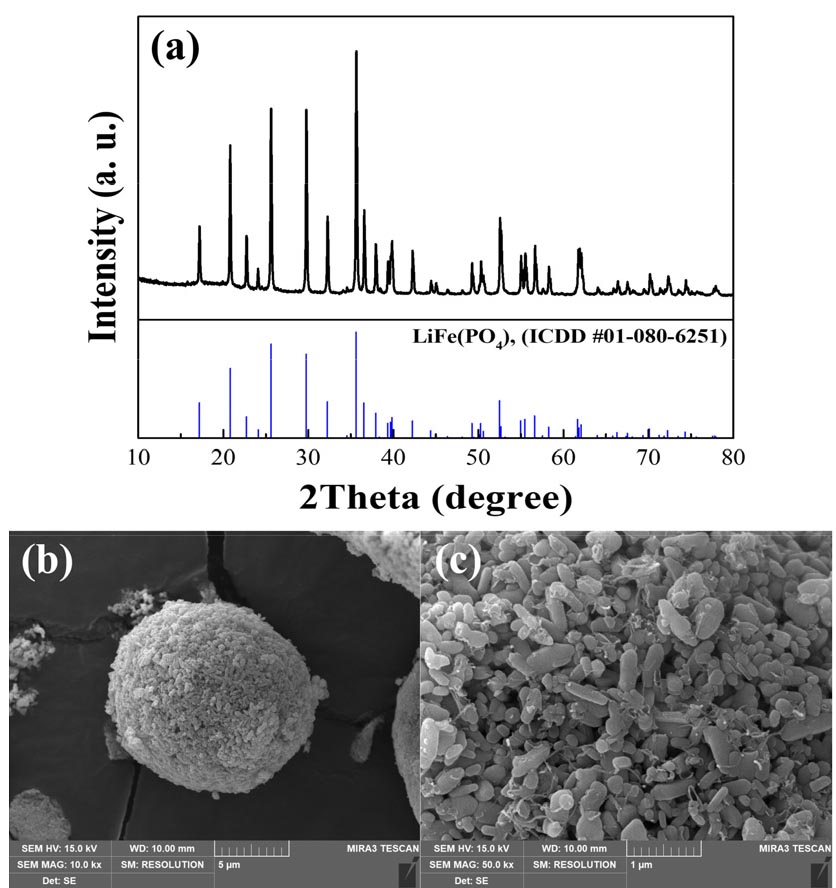
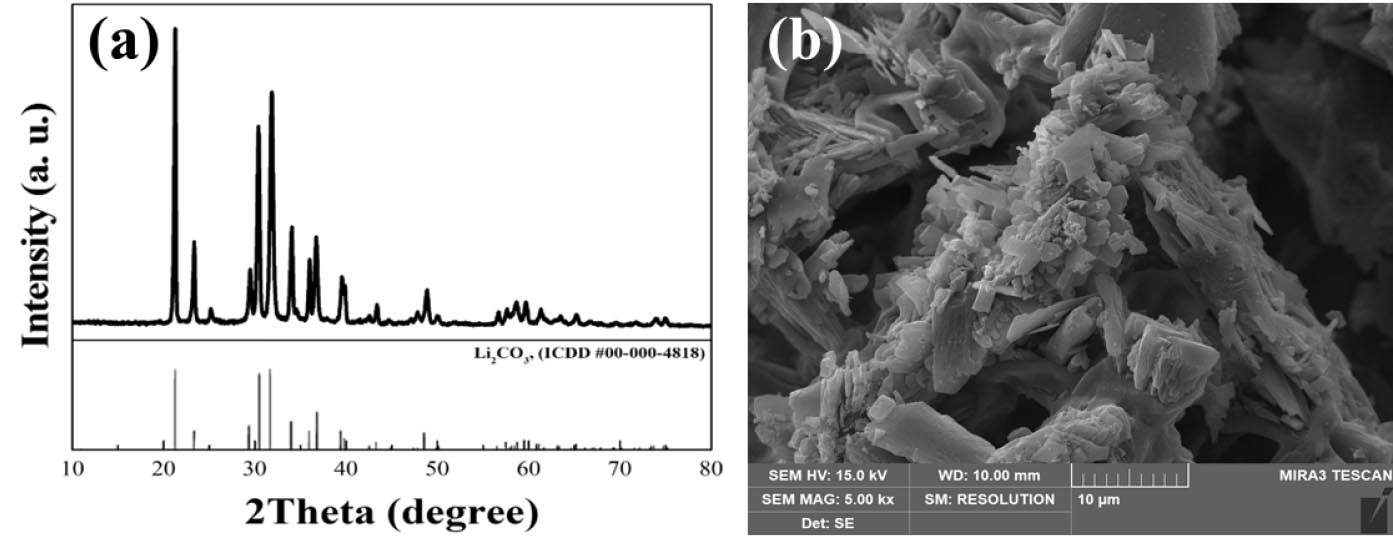
본 연구에서 사용된 폐LFP 양극재 분말은 K사에서 공급된 양극재 스크랩으로 분쇄공정을 통해 150 μm로 분급되어진 분말을 사용하였다. 사용된 양극재 분말의 주요 성분은 유도결합 플라즈마 분광기(Inductively Coupled Plasma-Optical Emission Spectroscopy, ICP-OES, iCAP Pro XP, ThermoFisher)를 이용하여 분석하였고, Table 1에 그 결과를 나타내었다. 폐LFP 양극재 분말에는 리튬이 약 4.27% 함유되어 있으며, 주사전자현미경(Scanning Electron Microscope, SEM, Mira3, TESCAN) 및 X-선 회절분석법(X-ray diffraction spectroscopy, XRD, XRD-6100, Shimadzu)을 통하여 표면 형상 및 결정상을 분석하였으며, 그 결과를 Fig. 1에 나타내었다. Fig. 1(a)의 XRD 분석 결과 폐LFP 양극재 분말은 올리빈 구조의 LiFePO4(ICDD #01-080-6251) 결정상으로 분석되었다.
Niu et al.에 의하면 염화철의 Fe3+가 LFP 구조의 Fe2+와 동형치환되어 동시에 Li+의 선택적 침출이 이루어진다고 하였으며30), 이에 본 연구에서는 리튬을 선택적으로 침출하기 위하여 염화철 에칭액(38%, FeCl3)을 사용하였다. Dai et al.29) 및 Niu et al.30)은 부족한 산화력을 위하여 H2O2를 첨가하였으나 본 연구에서는 추가적인 첨가제를 투입하지 않았다. 염화철 에칭액과 LFP 분말 대비 반응 몰비를 계산하여 증류수에 희석하여 사용하였다. 먼저, 염화철 에칭액이 LiFePO4의 이론적 몰 비 대비 0.7, 1.0, 1.3, 그리고 1.6배(이하 0.7M, 1.0M, 1.3M, 1.6M이라고 함)로 증류수에 희석하였으며, 광액농도는 50 g/L로 고정하여 폐LFP 분말을 투입하였다. 이때, 교반속도는 250 rpm 및 침출시간은 3시간으로 고정하였다. 염화철 에칭액의 농도에 따른 침출실험 수행 후 필터페이터(Qualitative Filter Paper 150 mm, ADVANTEC)를 이용하여 고액을 분리하였으며, 침출잔사는 80℃ 오븐에서 건조하였다. 이후 고상은 분말특성을 확인하였고, 액상은 ICP 분석을 통하여 침출율을 계산하였으며 계산식은 식 (1)에 나타내었다27).
여기서 ni는 성분 i의 침출율(%), ci는 침출용액 내의 성분 i 농도(g/L), 는 침출용액의 부피, m0는 투입한 폐LFP 분말의 질량(g), wi는 투입한 폐LFP 분말 내 성분 i의 함량(%)이다.
이후 동형치환 후 액상으로 존재하는 Fe2+의 제거를 위하여 5M NaOH를 투입하였으며, pH미터기로 각각 pH 3, 4, 5로 조절하여 철의 제거율을 비교하였다. 이때, Fe2+가 Fe3+로 쉽게 산화되어 pH의 안정성을 위하여 1차 제거 후 충분한 시간을 두고 반응시켜 2차로 철을 제거하였다. 철이 제거된 리튬 용액에서 탄산리튬의 합성을 위하여 증발농축 및 불순물을 제어하였다. 증발농축은 리튬 용액의 약 80%가 농축되었으며, 농축 후 5M Na2CO3를 LFP 이론적 몰 비 대비 1:1 비율로 투입하여 탄산리튬을 결정화하였다. 이후 합성된 탄산리튬의 분말 특성 및 순도를 확인하였다. 본 연구에서 사용된 시약은 모두 시약급을 사용하였다.
Table 1.
Chemical composition of waste LiFePO4 cathode powders (%)
| Element | Li | Fe | P | etc |
| Content (%) | 4.27 | 33.38 | 6.93 | - |
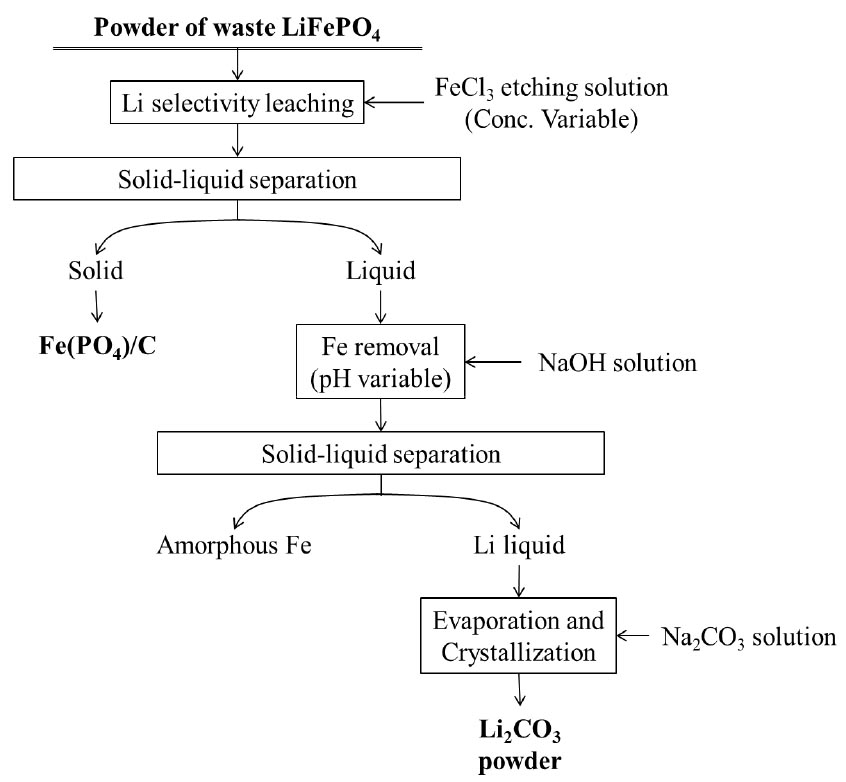
또한, 본 연구의 리튬 침출 및 회수에 관한 공정 흐름도는 Fig. 2에 나타내었다.
3. 결과 및 고찰
3.1. 폐LFP 분말의 침출
폐LFP 양극재 분말에서 리튬을 선택적으로 분리하기 위하여 사용된 염화철 에칭액과의 화학적 반응식은 식 (2)와 같다.
폐LFP 양극재 분말에서의 리튬의 선택적 침출에 사용된 염화철 에칭액은 상기 반응식에 따라 계산하였으며, LiFePO4의 이론적 몰 비 대비 0.7, 1.0, 1.3, 그리고 1.6배로 증류수에 희석하여 투입하였다. 이론적으로 FeCl3와 LFP의 몰비가 1:1일 때, LFP의 Li+이 완전히 침출될 수 있다고 보았으며, 이에 몰 비의 영향에 따른 침출율을 비교하였다. 침출 실험의 고정 변수는 광액농도를 50 g/L 및 폐LFP 분말이 염화철 에칭액과 충분히 반응할 수 있도록 반응 온도, 시간 그리고 교반속도는 각각 상온에서 3시간 동안 250 rpm으로 진행되었다. 이는 본 연구진의 이전 연구 결과에서 리튬 침출율은 반응 시간 및 온도에 대한 영향이 낮으며, 광액농도가 50 g/L일 때 가장 높은 침출율을 확인하여 본 연구의 실험 조건을 결정하였다30).
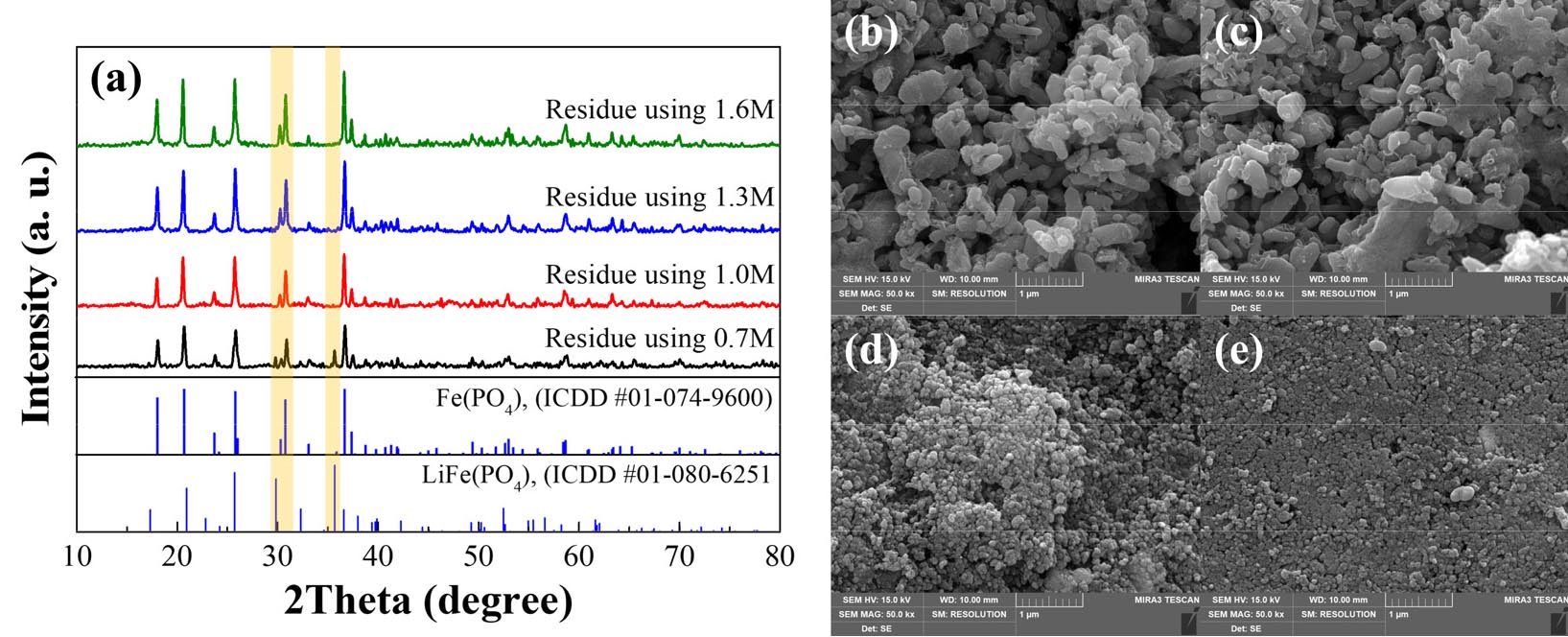
광액농도 50 g/L의 조건에서 염화철 에칭액의 몰 비에 따른 리튬의 선택적 침출 영향을 보고자 하였다. 각 조건의 염화철 에칭액 농도에서 침출 후 얻은 침출잔사는 결정상 및 표면 형상의 변화를 확인하기 위하여 SEM 및 XRD 분석하였으며, 그 결과는 Fig. 3에 나타내었다. 침출 후 얻은 침출액의 각 성분 농도는 ICP 분석을 통해 확인하였으며, 식 (1)을 통하여 침출율을 계산하여 Table 2 및 Fig. 4에 나타내었다.
Fig. 3(a)의 염화철 에칭액을 이용한 침출 후 침출잔사의 XRD 결과를 보면 이론적 몰 비 대비 0.7배인 0.7M 농도의 경우 기존 원료인 LiFePO4 피크가 남아있는 모습을 보였으나 1.0M 농도 이상에서부터 잔존 LiFePO4 결정상 피크가 사라졌다. 1.0M 농도 이상에서는 모두 리튬이 제거되어 FePO4(ICDD #01-074-9600) 결정상으로 분석되었다. 이를 보아 FeCl3와 LFP의 이론적 반응 몰 비가 1:1일 때, LFP의 Li+이 완전히 침출될 수 있다는 반응식 상의 이론과 일치하는 것을 확인하였다. 또한, 염화철 에칭액의 농도가 증가함에 따라 산화력의 증가로 인하여 침출잔사의 결정성이 높아졌다. 또한, Fig. 3(b)-(e)의 SEM 분석 결과를 보면, 염화철 에칭액 농도가 0.7M 및 1.0M 농도까지는 침출 전의 LFP 분말과 표면 형상에서 큰 차이를 보이지 않았다. 하지만 1.3M 농도 이상부터 결정립의 크기가 매우 감소하였다. 이러한 결과는 폐LFP 분말과 염화철 에칭액의 이론적 반응 몰 비보다 큰 농도에서 충분한 산화력을 가진 침출제와의 반응으로 인해 응집되어있던 2차 입자가 분리되어 1차 입자 형태로 된 것으로 보인다. Yan et al.의 연구 결과에서도 산 침출 후 LiFePO4의 2차 입자가 분리되었으며, 이는 리튬이 추출되고 결정구조가 FePO4로 변화함에 따른 구조적 응력에 기인한 것으로 확인되었다31).
Table 2.
Chemical composition of leachate using ferric chloride etching solution from LiFePO4 cathode powder
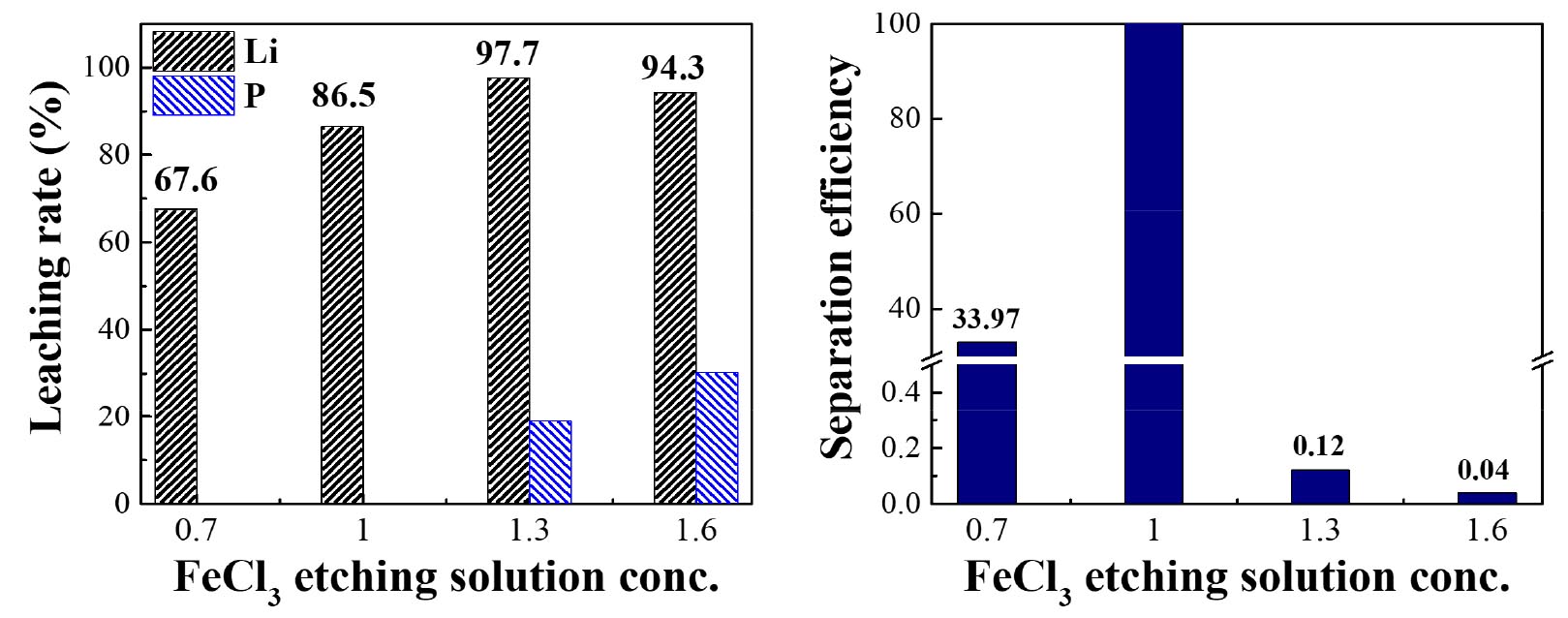
반응 전 염화철 에칭액의 pH는 0.7M 농도에서 1.6M로 증가함에 따라 pH 1.5에서 pH 1.0으로 감소하였으며, 모든 농도에서 반응 후 pH가 증가하였다. ICP 분석 결과를 토대로 염화철 에칭액 농도에 따른 리튬의 침출율을 비교한 결과, 0.7M 농도에서 1.3M 농도까지는 약 67.9%에서 약 97.7%로 크게 증가하였다. 0.7M 농도에서는 리튬의 침출율이 현저히 낮았으며, 이는 침출잔사에 LFP 피크가 잔존해있던 XRD 결과와 일치하는 경향을 보였다. 반응식 상 이론적 반응 몰 비가 1:1일 경우에 리튬이 모두 침출된다고 하였으나, 본 연구에서는 1:1.3의 이론적 반응 몰 비에서 가장 높은 침출율을 보였다. 또한, Fig. 4를 보면 1.0M 농도까지는 인이 거의 침출되지 않았으나, 충분한 산화력을 가진 1.3M 농도부터 인이 침출되었다. 이는 충분한 염화철 에칭액 농도에서 Fe3+가 가수분해되어 H+가 생성되며 인산이 용해될 수 있다는 기존의 문헌과 일치한다29). 그 결과 반응 후 염화철 에칭액의 pH 또한 에칭액의 농도가 증가함에 따라 감소하는 경향을 보였다. 또한, Dai et al. 및 Niu et al.의 연구에서는 Fe3+의 산화 및 반응을 위하여 H2O2를 첨가하였으나 본 연구에서는 첨가제를 넣지 않고 염화철 에칭액만을 이용하여 약 98%의 리튬 침출율을 달성하였다.
Table 2의 ICP 분석 결과를 바탕으로 염화철 에칭액 농도에 따른 리튬과 인의 분리 효율을 확인하고자 하였다. 이에 본 연구진의 이전 연구에서 사용한 분배계수 식을 바탕으로 리튬과 인의 분리 효율을 확인하였다27). 리튬과 인에 대한 분배계수 및 분리 효율은 식 (3) 및 식 (4)에 나타내었다.
여기서 는 성분 i의 분배계수, 은 침출 반응 후 침출잔사 내 성분 i의 농도(g/L)이며 은 침출수 내 성분 i의 농도(g /L)이다. 침출잔사의 성분 i 농도는 투입한 원료의 성분 i 농도에서 침출수의 성분 i 농도를 빼서 계산하였다. 그다음 리튬과 인의 분리 효율을 확인하기 위해 식 (4)와 같이 계산하였다.
식 (3)에서 계산된 를 이용하여 β를 계산하였으며, 리튬과 인의 분리 효율을 Table 3와 Fig. 4(b)에 표시하였다. Table 3의 결과를 토대로 백분율화하여 Fig. 4(b)에 나타내었으며, 그 결과 염화철 에칭액의 농도가 1.0M일 경우 가장 높은 분리 효율을 보였다. 1.0M 농도까지는 인이 거의 침출되지 않아 그 분리 효율이 매우 높았으며 이후 인의 침출로 분리 효율이 감소하였다. 이는 기존에 언급한 가수분해 후 생성된 인산수소의 영향으로 인이 검출되었기 때문으로 판단된다. 이후 본 연구에서는 리튬을 자원으로써 회수하기 위하여 가장 높은 침출율을 보인 1.3M 농도로 고정하여 실험을 진행하였다.
Table 3.
Separation efficiency of reaction leachate using ferric chloride etching solution from LiFePO4 cathode powder
|
FeCl3 etching solution (Conc.) | D (Li) | D (P) | β (Li-P) |
| 0.7 | 2.09 | 0.00 | 28,510 |
| 1.0 | 6.41 | 0.00 | 86,473 |
| 1.3 | 25.12 | 0.24 | 105 |
| 1.6 | 16.53 | 0.43 | 38 |
3.2. 침출액으로부터 철의 제거
염화철 에칭액의 Fe3+와 동형치환 반응으로 폐LFP 분말에서 Li+ 및 Fe2+가 액상으로 침출되었고, 최종적으로 리튬만을 회수하여 탄산리튬으로 합성하기 위하여 Fe2+를 제거하였으며, 침출액과 NaOH와의 화학적 반응식은 식 (5)와 같다.
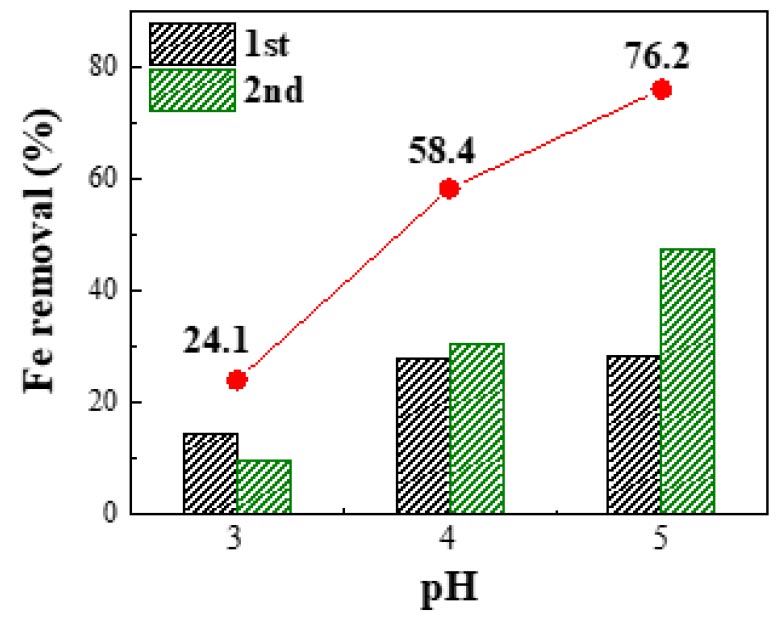
철이 제거된 리튬 용액을 얻기 위하여 5M NaOH 용액을 사용하였으며, pH를 조절하여 각각의 제거율을 비교하였다. pH는 3, 4 그리고 5로 조절하였으며, 철 의 산화성으로 인해 pH가 안정되지 않아 1차 및 2차로 나누어 제거하였다. 1차 제거 후 여액에는 미반응 철이 다량 포함되어 있어 일정 시간 후 다시 철이 침전되었다. 이후 2차 제거 시 충분한 반응을 통하여 pH를 안정화하여 철을 제거하였으며, 시간의 경과 후에도 철의 침전은 발생하지 않았다. 철 제거율은 Table 4 및 Fig. 5에 나타내었다.
pH 3에서 철을 제거한 경우, 빠른 안정화로 인하여 1차 및 2차에서 철의 제거율이 낮았다. 그러나 1차 철 제거실험의 pH 4 및 pH 5의 경우, 대기 중에서 Fe2+와 Fe3+의 산화반응으로 인하여 pH가 안정화되지 않아 제거율이 매우 낮았다. 특히, 2차 철 제거에서 pH 4 및 pH 5의 경우 NaOH와 충분한 반응시간을 주어 철을 제거하자 1차 제거 시보다 철 제거율이 높아졌으며, pH 5의 경우 가장 높은 제거율을 보였다. 이때, 제거한 철 생성물은 결정성이 없는 철 화합물로 확인되었고, 약 pH 3.0 이상에서 생성물이 형성되었다. 또한, 모든 실험 조건에서 리튬의 손실은 발생하지 않았다. 본 실험을 통하여 pH 5 이상에서 충분한 철의 제거가 이루어진 것으로 확인되었고, 이에 철이 제거된 리튬 용액에서 탄산리튬을 합성하였다.
Table 4.
Chemical composition after removing Fe2+ ion from leachate and Fe removal rate
| pH |
Li (ppm) |
Fe (ppm) |
P (ppm) |
Fe removal rate (%) |
| 3 | 2,000 | 12,051 | 70 | 24.1 |
| 4 | 2,078 | 6,612 | 0.4 | 58.4 |
| 5 | 2,083 | 3,786 | 0.3 | 76.2 |
3.3. 회수된 용액으로부터 탄산리튬 합성
pH 5에서 철이 제거된 리튬 용액으로부터 탄산리튬을 합성하기 위하여 회수된 용액의 약 80%를 증발농축하였다. 이 과정에서 생성된 불순물은 필터페이퍼를 이용하여 제거되었으며, 이후 5M Na2CO3를 LFP의 이론적 몰 비 대비 1:1 비율로 투입하였다. 투입 후 탄산리튬 결정화를 위하여 150℃에서 농축하였다. 생성된 탄산리튬은 XRD 및 SEM을 통하여 결정상 및 분말 형상을 확인하였고, ICP 분석을 통하여 순도를 확인하였다. Fig. 6(a)의 결과 합성된 분말은 Li2CO3(ICDD #00-000-4818)임을 확인하였고, 표면 형상 또한 기존의 문헌과 유사한 것으로 분석되었다32,33). 이때, 주요 불순물로는 소듐이 약 3%, 철은 약 0.5% 그리고 황이 0.8%로 함유되어 있으며, 나머지 인, 알루미늄, 칼슘, 니켈 등과 같은 성분들이 존재하였다. 그 결과 탄산리튬의 순도는 약 95%로 계산되었다. 고순도의 탄산리튬을 합성하기 위해서는 침출 시 고농도 및 고순도의 리튬 용액을 얻는 것이 유리하며, 본 연구에서는 철의 동형치환으로 철의 혼입이 있었다. 또한, 탄산소듐을 이용한 합성으로 인하여 소듐의 혼입이 있었으며, 이는 증류수를 이용한 수세를 통하여 더 높은 순도의 탄산리튬 합성이 가능할 것으로 보인다.
4. 결 론
폐LFP 양극재 분말로부터 리튬을 회수하기 위하여 기존의 산 침출이 아닌 염화철 에칭액을 이용하여 침출을 수행하였다. 염화철의 Fe3+와 동형치환 반응에 의한 리튬의 침출율을 비교하기 위하여 본 실험을 진행하였으며, 추가적인 첨가제 없이 염화철 에칭액의 농도에 따른 침출율을 비교하였다. 이후 침출액에서 철을 제거하였으며, 철이 제거된 용액으로부터 증발농축을 통해 탄산리튬을 합성하였다.
최종적으로 산 및 추가적인 첨가제 없이 충분한 산화력을 가진 염화철 에칭액만을 이용하여 리튬을 침출하였으며, 동형치환 반응에 의한 침출을 수행하였고, 이를 이용한 리튬의 선택적 침출 가능성을 확인하였다.
1) 폐LFP 분말은 XRD 분석 결과 LiFePO4 결정상으로 분석되었으며, 리튬이 약 4.3% 함유되어 있는 분말로 확인되었다.
2) 염화철 에칭액의 농도에 따른 리튬의 침출 후 침출잔사의 결정상은 Fe(PO4)결정구조로 변하였으며, 0.7M 농도에서는 LFP 피크가 남아있었으나 1.0M 농도 이상에서는 모두 제거되었다.
3) 침출잔사의 표면 형상을 보면 0.7M 및 1.0M 농도에서는 원료인 폐LFP와 큰 차이를 보이지 않았으나, 1.3M 및 1.6M 농도로 증가할수록 입자의 크기가 감소하였다.
4) 침출액의 ICP 분석 결과, 염화철 에칭액의 농도가 1.3M일 경우 리튬의 침출율이 약 98%로 가장 높았으며 XRD 분석 결과와 같이 0.7M 농도에서는 약 68%로 매우 낮은 리튬 침출율을 보였다. 또한, 리튬과 인의 분리 효율은 1.0M에서 가장 높았다.
5) pH를 조절하여 Fe2+를 제거하였으며, pH 5에서 충분한 반응시간을 두었을 때 가장 높은 철 제거율이 확인되었고, 이때 리튬의 손실은 없었다.
6) 이후 증발농축 및 탄산나트륨을 투입하여 분말을 결정화하였고, XRD 분석 결과 탄산리튬으로 확인되었다.