1. 서 론
2. 마그네슘의 생산량과 용도
3. 마그네슘의 제련 기술
3.1. 마그네슘 원료
3.2. 열환원법
3.3. 용융염 전해법
4. 마그네슘의 리사이클링 기술
4.1. Mg 합금 중 불순물의 영향
4.2. Mg합금 스크랩의 전처리
4.3. Mg 합금의 용탕 처리
4.4. 진공증류에 의한 정제
4.5. Mg 절삭 칩의 고체 상태 리사이클링
5. 종 합
1. 서 론
마그네슘(Mg)은 지각 구성 원소 존재도에서 7번째로 풍부한 원소(2.33 %)이며, 특히 구조용 금속인 Mg은 알루미늄(8.1 %), 철(5.1 %)에 이어서 세 번째로 풍부한 원소이다1). 1808년에 영국의 험프리 데이비(Humphry Davy)가 산화 마그네슘과 산화 수은의 혼합물을 전기분해하여 얻은 아말감에서 수은을 증발시켜 최초로 마그네슘을 분리하였다2). 1828년에는 프랑스의 앙투안 뷔시(Antoine Alexandre Brutus Bussy)가 염화 마그네슘(MgCl2)을 칼륨으로 환원시켜 분리하였다. 1833년에는 영국의 마이클 패러데이(Michael Faraday)가 용융 무수 염화 마그네슘을 전기분해하여 액체 마그네슘을 생산하는 방법을 개발하였다. 제1차 세계대전과 제2차 세계대전 때는 군용기와 소이탄 등에 마그네슘 합금이 사용되었다.
Table 1에는 Mg의 물리∙화학적 성질을 Al, Ti, Fe과 비교하여 나타내었다. Mg의 밀도는 1.738 g/cm3로 Al의 2/3, Ti의 1/3, Fe의 1/4에 해당하여, 실용 금속 중 가장 가볍고 비강도∙비강성(중량당 강도와 강성), 열전도율이 높은 구조용 금속이다. 또 진동이나 충격 흡수가 쉽고, 전자파 차폐능이 높은 특징을 가지고 있다. Mg의 이러한 특성을 살려 경량 소재로서 자동차 부품, 휴대폰이나 노트북의 케이스 등에 사용되고 있다. 2019년도 전 세계 마그네슘 생산량은 약 110만 톤에 달하고 있다3). 한때 우리나라에서도 Mg을 생산하였으나, 현재 1차 지금은 생산하지 않고 있다. 2018년 기준 우리나라의 Mg 1차 지금 수요는 약 24,400 톤이며, 12,800 톤의 1차 지금을 수입하였고, 리사이클링한 2차 지금 생산량은 11,800 톤 정도이다4). 본 논문에서는 이러한 Mg의 제련 기술과 리사이클링 기술 현황에 대하여 고찰하였다.
Table 1.
Physico-chemical properties of Mg, Al, Ti and Fe
2. 마그네슘의 생산량과 용도
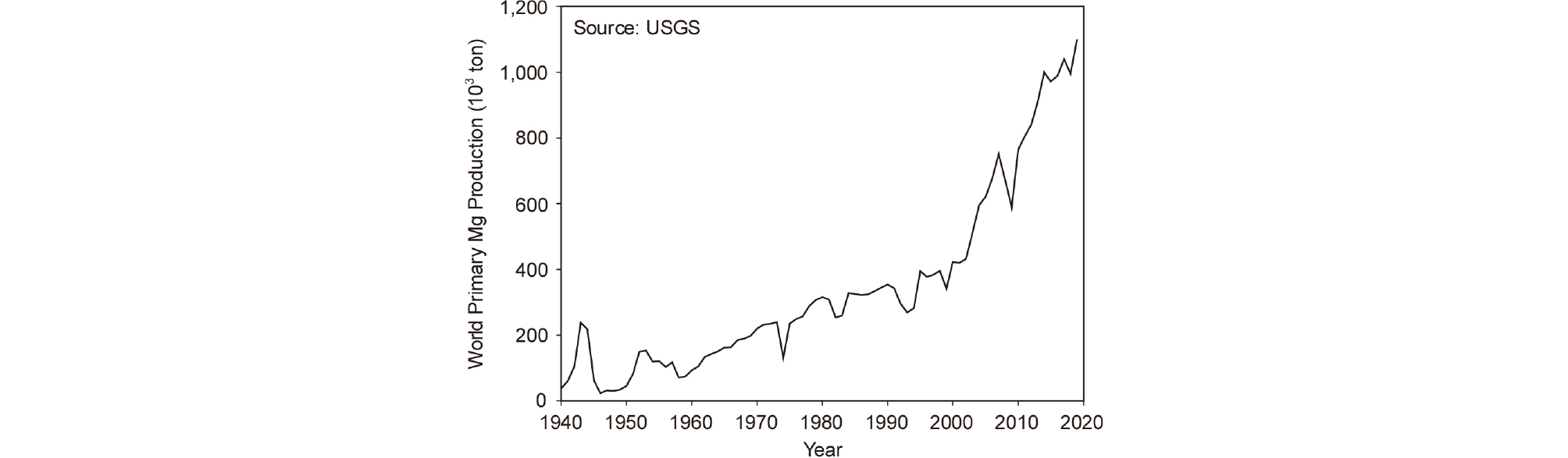
Fig. 1에는 1940년부터 2019년까지 전 세계 Mg 생산량의 추이를 나타내었다5). Mg 생산량은 제2차 세계대전 시기에 군사 목적으로 연간 20만 톤 이상을 생산하기도 하였다. 그 이후 1960년대부터 서서히 증가하기 시작하였으나, 2000년대부터 중국의 급격한 증산으로 생산량이 급증하여, 현재 미국을 제외한 연간 전 세계 생산량은 110만 톤에 달한다. 미국을 제외하면 2019년 기준 전 세계 생산량의 약 82 %인 90만 톤이 중국에서 생산되고 있다. 그 외 러시아(8만 톤), 카자흐스탄(2.5만 톤), 이스라엘(2만 톤), 브라질(1.5만 톤) 등에서 생산되고 있다.
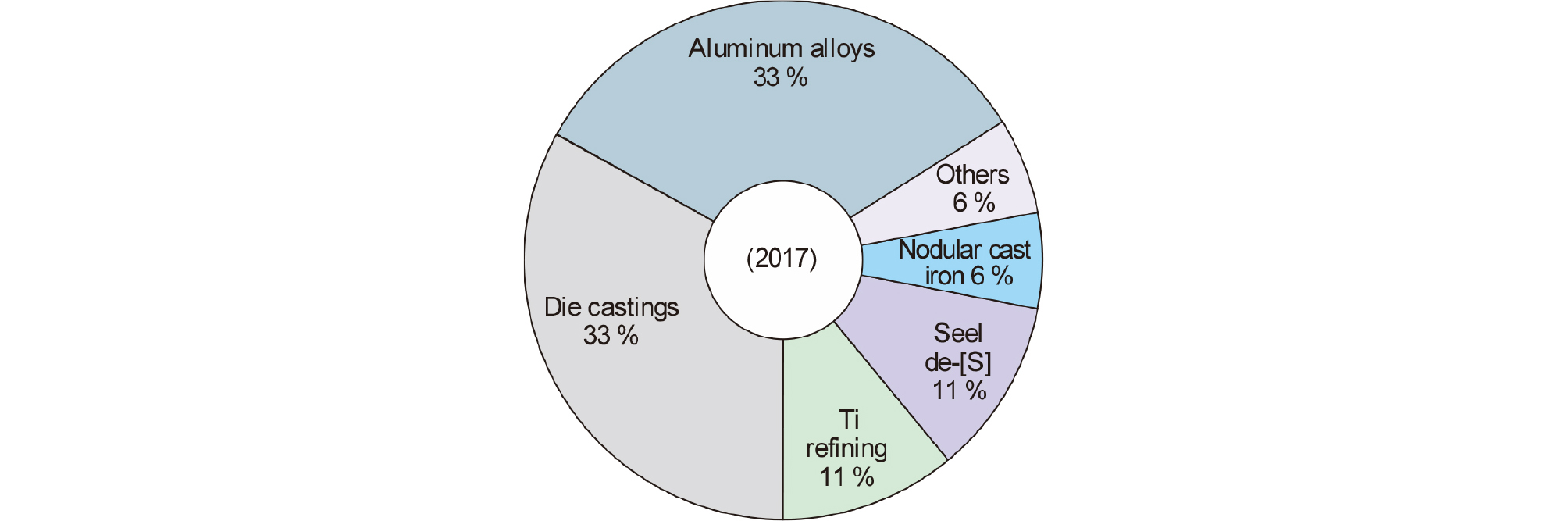
Fig. 2에는 2017년도 기준의 Mg 용도를 나타내었다6). Mg은 알루미늄 합금과 Mg 다이캐스팅용으로 가장 많이 사용되고 있다. 그 외에 Ti 제련에서 TiCl4의 환원제, 철강의 탈황제, 주철 구상화제 등으로 사용되고 있다. 철강 탈황제로 사용된 Mg은 리사이클링이 곤란하고, Ti 제련에 사용된 Mg은 자체에서 리사이클링되고 있으므로, 리사이클링 대상이 되는 것은 다이캐스팅용이나 알루미늄 합금에 사용된 것이다.
한편 순 Mg은 매우 물러서 구조재료에 적합하지 않으나, 다른 금속을 첨가하면 Mg의 독특한 성질을 가진 합금이 되어 우수한 구조재료가 된다. Table 2에는 Mg 합금의 주요 첨가 원소와 첨가 목적을 나타내었으며7), Table 3에는 Mg 합금의 대표적인 조성 예를 나타내었다. Mg 합금에는 Al을 합금 성분으로 하는 AZ, AM, AE계 등 다양한 종류의 합금이 개발되어 사용되고 있다. Mg 합금을 리사이클링할 때 이러한 합금들이 혼합되어있는 경우 합금 원소가 불순물로 작용할 수 있으므로 사전에 파악해 두는 것이 필요하다.
Table 2.
An ASTM code and the effect of various alloying elements in magnesium7)
Table 3.
Chemical composition of various magnesium alloys
3. 마그네슘의 제련 기술
3.1. 마그네슘 원료
마그네슘의 원료에는 광석과 해수 및 염수의 두 가지가 있다. 광석에는 마그네사이트(magnesite, MgCO3), 돌로마이트(dolomite, MgCO3∙CaCO3), 카날라이트(carnallite, MgCl2∙KCl∙6H2O) 등이 있으나 마그네사이트가 대표적이다. 또 가용성 염류로서 바닷물, 염수 및 광천수 등에도 함유되어 있다. Table 4에 중요한 마그네슘 원료를 나타내었다.
Table 4.
Raw materials and their molecular formula of magnesium sources
Mg 제조법에는 크게 열환원법과 용융염 전해법의 두 가지가 있다. 열환원법은 MgO를 C, CaC2, Al, Si 등의 환원제를 이용하여 열화학 반응으로 환원하는 방법이지만8), 최근에는 중국을 중심으로 페로실리콘(Fe-Si)을 환원제로 이용하는 규소 열환원법이 주류를 이루고 있다. 용융염 전해법은 무수 MgCl2를 사용하는 IG Farben법과 Alcan법, 그리고 MgCl2∙1.25H2O를 사용하는 Dow법으로 구분할 수 있다. Table 5에는 이러한 Mg 제조법을 종합하여 나타내었다9).
Table 5.
Selected magnesium production processes9)
3.2. 열환원법
환원제 X를 사용하여 마그네시아(MgO)를 Mg으로 환원하는 반응은 다음과 같다.
| $$\mathrm{MgO}+\mathrm X=\mathrm{Mg}(\mathrm g)+\mathrm{XO}$$ | (1) |
XO는 산화물이며 환원제인 X에 따라 기체나 고체가 된다. X로 탄소를 이용하면 탄소 열환원법이며, 금속(Si, Al 등)을 사용하면 금속 열환원법이 된다. 탄소 열환원법은 MgO의 환원제로 C을 이용하는 것으로, 아래 반응식과 같이 생성 산화물은 CO(g)가 된다.
| $$\mathrm{MgO}(\mathrm s)\;+\;\mathrm C(\mathrm s)\;=\mathrm{Mg}(\mathrm g)+\mathrm{CO}\;(\mathrm g)$$ | (2) |
Al을 환원제로 사용하여 MgO를 환원하는 반응은 다음과 같다.
| $$3\mathrm{MgO}(\mathrm s)+2\mathrm{Al}(\mathrm s)={\mathrm{Al}}_2{\mathrm O}_3(\mathrm s)+3\mathrm{Mg}(\mathrm g)$$ | (3) |
Si을 환원제로 사용하여 MgO를 환원하는 기본 반응식은 다음과 같다.
| $$2\mathrm{MgO}(\mathrm s)+\mathrm{Si}(\mathrm s)=2\mathrm{Mg}(\mathrm g)+{\mathrm{SiO}}_2(\mathrm s),\;K_{1373}=1.8\times10^{-9}$$ | (4) |
열역학적으로 평형상수인 값이 작아 환원 반응이 일어나기 힘들지만, 진공으로 처리하면 Mg 증기만 생성되어 연속적으로 계외로 배출되므로 이러한 반응이 가능하다10). 환원로는 가열방식, 반응조, 진공계 등의 설계에 따라 I.G.사의 수평 내열로, Bagley의 입형 내열로, Pidgeon의 수평 레토르트(retort)로, 이탈리아의 Ravelli로 등이 있으나, 현재는 대부분 Pidgeon법을 사용하고 있다. 그리고 반응 온도 올려서 반응 시간을 단축함과 동시에 연속 조업을 할 수 있는 Magnetherm법과 Mintek법 등이 있다.
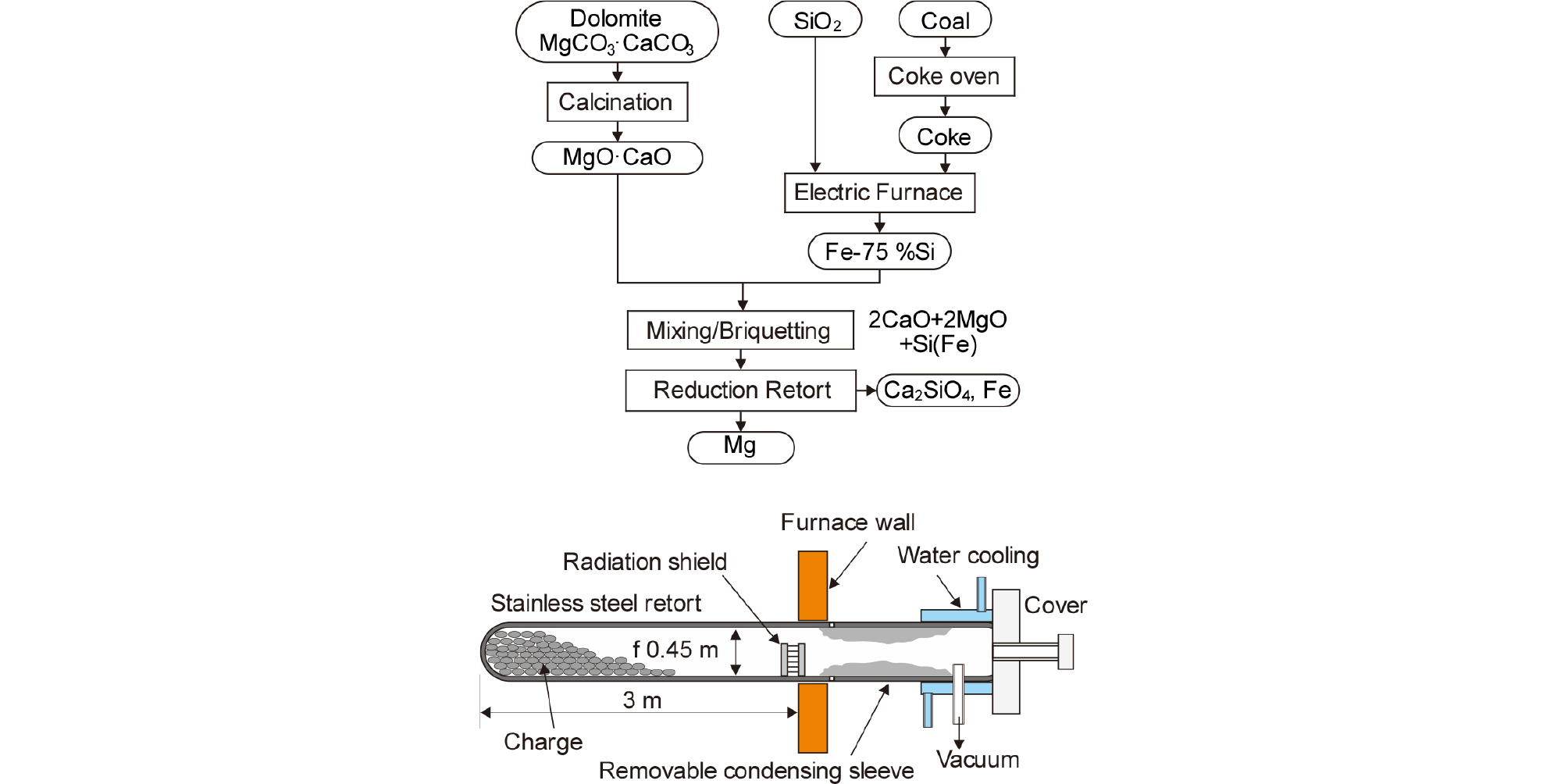
Fig. 3에는 Pidgeon법의 공정도와 함께 수평 레토르트의 단면 모식도를 나타내었다. 특수강제의 반응기를 이용하여 돌로마이트(dolomite, MgCO3‧CaCO3)를 하소한 후 아래 식과 같이 페로실리콘으로 환원하고 있다.
| $$2\mathrm{MgO}(\mathrm s)+2\mathrm{CaO}(\mathrm s)+\mathrm{Si}(\mathrm s)=2\mathrm{CaO}\cdot{\mathrm{SiO}}_2(\mathrm s)+2\mathrm{Mg}(\mathrm g)$$ | (5) |
3.3. 용융염 전해법
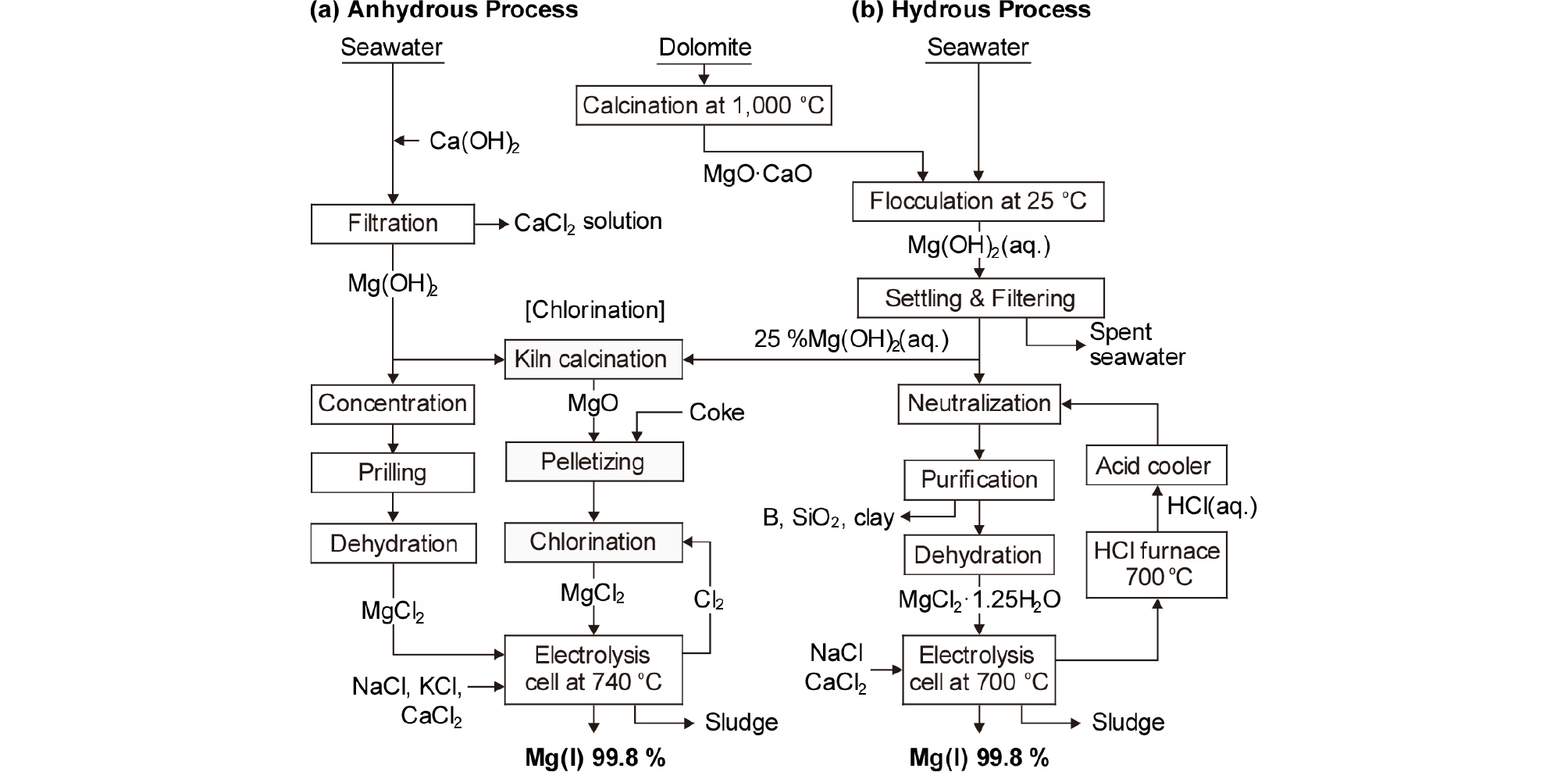
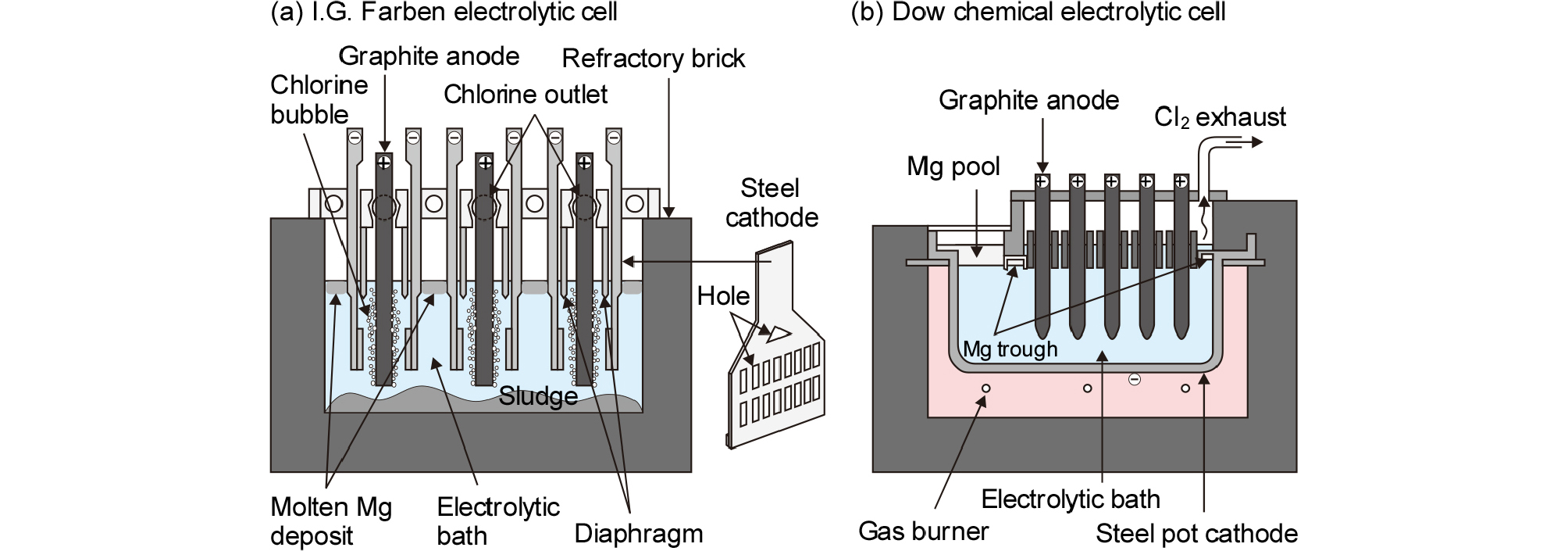
용융염 전해법에는 무수 MgCl2를 사용하는 IG Farben법, Norsk Hydro법, VAMI법 등이 있으며, 함수 염인 MgCl2∙1.25H2O를 사용하여 전해하는 Dow Chemical법이 있다. Fig. 4에는 무수 염과 함수 염 전해법의 공정도를 비교하여 나타내었다.
3.3.1. IG Farben process
IG Farben process(이하 IG법)은 Fig. 4(a)와 같이 무수 염화마그네슘을 원료로 사용한다. 무수 MgCl2를 만드는 방법은 2 단계로 구분할 수 있다. 1 단계에서는 MgCO3를 하소하여 MgO로 만들며, 돌로마이트(dolomite, MgCO3∙ CaCO3)는 하소한 후 물을 첨가하여 석회유(milk of lime)로 만들고, MgCl2가 함유되어있는 해수와 반응시켜 Mg (OH)2를 침전시킨다. 이것을 다시 하소시켜 MgO를 얻는다.
2 단계에서는 MgO분말과 석탄, 이탄(泥炭, peat)을 혼합하고 MgCl2를 점결제로 사용하여 단광(briquette)이나 펠릿으로 만들어 가열∙건조하여 코크스화시킨 후 염화로에 투입한다. 염화로에서는 약 1,000 ℃로 가열하면서 노의 아래쪽에서 Cl2가스를 취입하여 아래 식과 같이 염화시켜 만들어진 MgCl2를 전해조에 공급한다11).
| $$\mathrm{MgO}(\mathrm s)+\mathrm C(\mathrm s)+{\mathrm{Cl}}_2(\mathrm g)={\mathrm{MgCl}}_2(\mathrm l)+\mathrm{CO}(\mathrm g)$$ | (6) |
| $$2\mathrm{MgO}(\mathrm s)+\mathrm C(\mathrm s)+2{\mathrm{Cl}}_2(\mathrm g)=2{\mathrm{MgCl}}_2(\mathrm l)+{\mathrm{CO}}_2(\mathrm g)$$ | (7) |
전해조는 내화벽돌로 장방형으로 만들어져 있으며, Fig. 5(a)에 전해조의 단면을 나타내었다. 용융염 전해조의 용융염 중에는 한 쌍의 판상 탄소제 양극(anode)과 철강제의 음극(cathode)이 침지되어 있으며, 각 전극의 상부는 격벽으로 분리되어 있다. 전해조에서의 반응은 다음과 같다.
| $$\mathrm{Cathode}:\;\mathrm{Mg}^{2+}(\mathrm l,\;\mathrm{in}\;\mathrm{molten}\;\mathrm{salt})+2\mathrm e^-=\mathrm{Mg}(\mathrm l)$$ | (8) |
| $$\mathrm{Anode}:\;2\mathrm{Cl}^-(\mathrm l,\;\mathrm{in}\;\mathrm{molten}\;\mathrm{salt})={\mathrm{Cl}}_2(\mathrm g)+2\mathrm e^-$$ | (9) |
| $$\mathrm{Overall}:\;{\mathrm{MgCl}}_2(\mathrm l)=\mathrm{Mg}(\mathrm l)+{\mathrm{Cl}}_2(\mathrm g)$$ | (10) |
양극에서 발생하는 Cl2 가스는 염화로에 보내어 MgO의 염화반응에 사용한다. 음극에 석출한 Mg은 음극의 구멍을 통과하여 음극실의 전해욕 상부로 떠오르며, 이것을 모아 출탕하여 잉곳을 만든다. 전해욕은 MgCl2-KCl이나 MgCl2-KCl-CaCl2계의 적당한 조성의 것을 사용한다.
3.3.2. Dow법
Dow법은 함수 염인 MgCl2·1.25H2O를 전해 원료로 사용하는 방법이며, Fig. 4(b)에 공정도를 나타내었다. 해수와 돌로마이트로부터 수산화 마그네슘을 추출하고, 염산으로 중화한 염화 마그네슘(MgCl2) 수용액을 건조하여, 2수화 염의 플레이크를 만들어 전해 원료로 사용한다. 해수로부터 원료를 조제하는 경우, 해수에 석회유를 첨가하여 Mg(OH)2를 침전시켜 여과∙분리한다. 여기에 HCl(일부는 전해 시의 회수물을 사용)을 첨가하여 MgCl2 용액으로 만들고, 가열하여 MgCl2·4H2O로 농축한 후, 유동층 탈수로에서 MgCl2·1.25H2O를 얻는다. 이때 MgCl2가 가수분해하여 MgO가 생성되지 않도록 주의하여 가열∙탈수하여야 한다.
원료인 MgCl2는 가수분해되기 쉽고, 도전성이 작은 결점이 있으므로, NaCl과 CaCl2를 첨가한 전해욕을 사용한다. 그림에서와 같이 한 열이 여러 개의 흑연 전극으로 구성된 anode열을 2열로 배치하고, 그 사이를 분할하는 구조로 되어 있다.
3.3.3. Ti 제련 부산물의 재생 전해법
Kroll법에서는 Ti 1톤을 제조할 때 환원제인 Mg도 약 1톤이 필요하며, Mg은 식 (11)과 같이 반응 생성물인 MgCl2가 된다.
| $${\mathrm{TiCl}}_4(\mathrm g)+2\mathrm{Mg}(\mathrm l)=\mathrm{Ti}(\mathrm s)+2{\mathrm{MgCl}}_2(\mathrm l)$$ | (11) |
이 MgCl2를 전해환원하여 Mg과 염소를 생성시켜, 각각 환원 및 염화공정에 사용한다. MgCl2의 용융염 전해조에는 전극의 연결 및 배치 방식에 따라 단극형(mono- polar형)과 복극형(multi-polar형)이 있다. 단극형 전해조는 각각의 전극에 모두 전기를 공급해주는 것으로 양극과 음극으로 이루어진 한 쌍의 전극을 직렬 또는 병렬로 배치한다. 복극형 전해조는 양쪽 끝에 위치한 양극과 음극에만 전기를 공급하고, 그 사이에 음극과 양극 역할을 동시에 수행하는 3~5개 정도의 bipolar 전극이 설치되어 있다12,13).
4. 마그네슘의 리사이클링 기술
Mg 스크랩에는 크게 공정 내에서 발생하는 스크랩과 Mg 제품의 수명이 다하여 발생하는 시중 스크랩이 있다. Mg 합금 성형품의 가공 공정에서 약 50 %의 마그네슘 합금 스크랩이 발생하는 것으로 알려져 있으며, 제조 공정에서 발생하는 스크랩은 적극적으로 리사이클링되고 있다. 그러나 시중에서 제품의 사용 불능상태에서 발생하는 스크랩은 아직 효율적인 리사이클링 방법이 확립되어 있지 못한 상태이다. Table 6에는 이러한 Mg(합금) 2차 자원과 리사이클링 기술을 요약하여 나타내었다14).
Table 6.
Secondary magnesium material and recycling scenarios14)
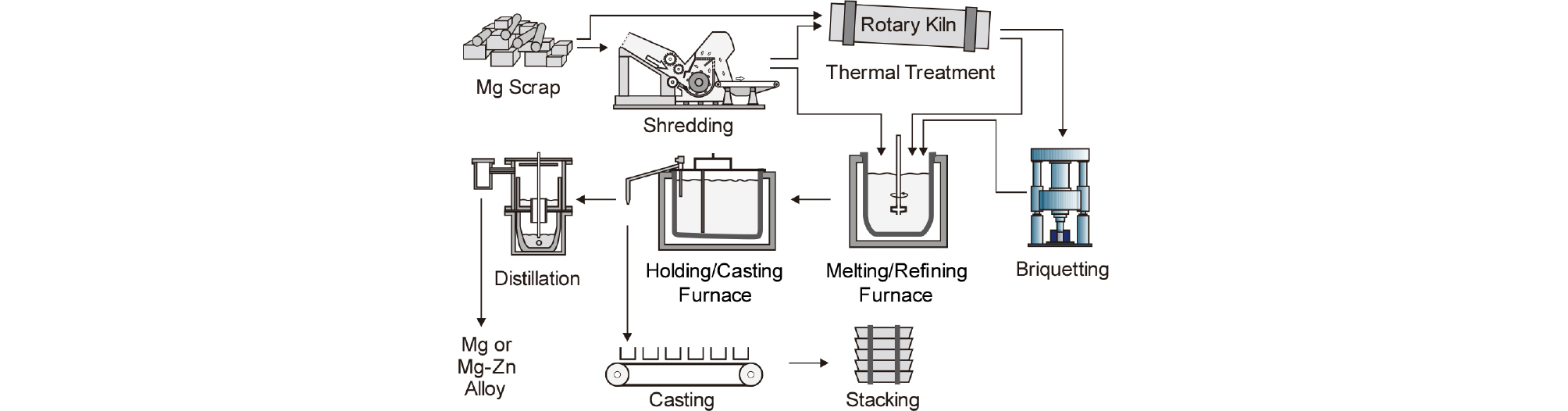
Fig. 6에는 Mg 합금 스크랩을 리사이클링하여 2차 지금 잉곳을 제조하는 공정을 나타내었다. 스크랩은 필요에 따라 슈레더 등으로 파쇄하거나 직접 로터리 킬른 등에서 도장층 등을 제거한다. 파쇄한 스크랩은 직접 용해로에서 용융하거나 도장층 등을 제거하는 전처리를 거친 후, 압축 성형하여 용해로 장입한다. 파쇄된 스크랩의 크기에 따라 압축 성형을 거치지 않고 용해하기도 한다. 용해로에서는 스크랩의 용해는 물론 불활성 가스에 의한 정련을 하는 것이 일반적이다. 용해한 스크랩은 주조하기 전에 유지로를 거쳐서 잉곳으로 주조하거나 증류 정련을 하기도 한다. 그 외에 자가 스크랩을 고상에서 처리하여 잉곳 등으로 재생하는 방법도 있다.
4.1. Mg 합금 중 불순물의 영향
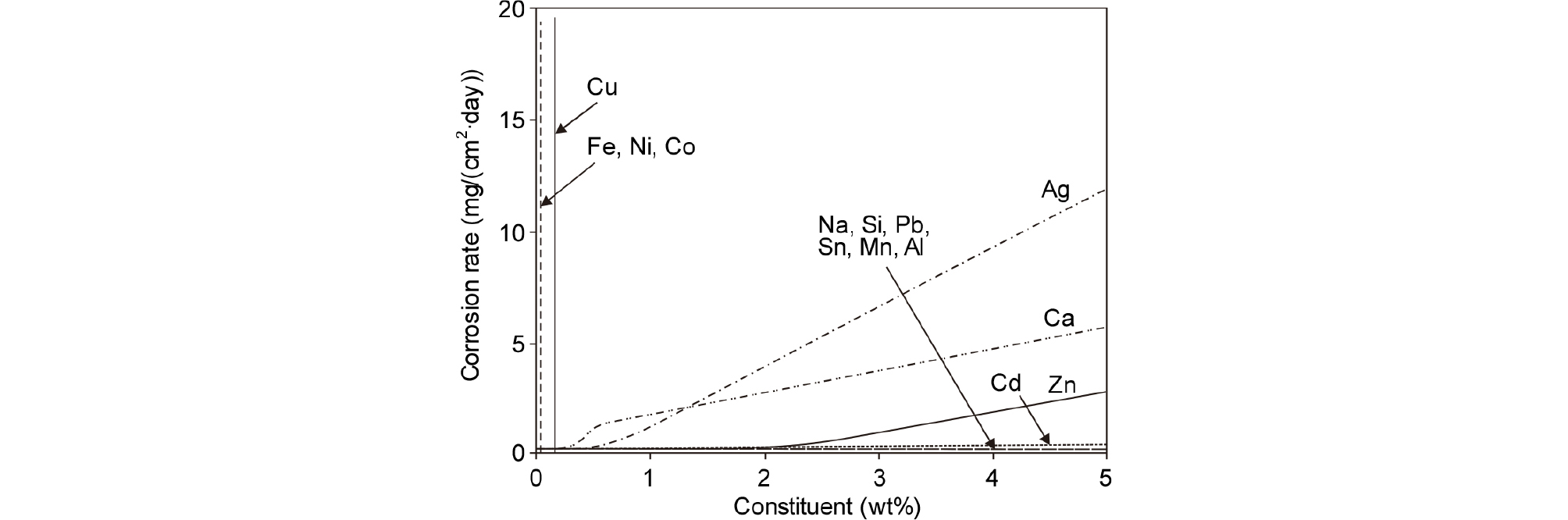
Mg 합금은 가공성, 내열성, 내식성 및 난연 성능이 나쁜 결점이 있다. 특히 Mg을 리사이클링하는 경우 혼입되는 불순물의 종류에 따라 내식성에 큰 영향을 미치고 있다. Fig. 7에는 2원계 Mg 합금에서 내식성에 미치는 첨가 원소 농도의 영향을 나타내었다15). Mg과 동일한 환경에서 사용되고 있는 Fe, Cu와 스테인리스강의 주요 성분인 Ni은 미량만 혼입되어도 내식성에 큰 영향을 미치는 것을 알 수 있다. Al의 경우 내식성에는 큰 영향을 미치지 않으나 다량으로 혼입되면 문제를 일으킬 수 있다. 따라서 Mg 합금을 리사이클링하기 위해서는 내식성과 관련하는 Cu, Ni, Si, Fe 등의 제거가 중요하다.
4.2. Mg합금 스크랩의 전처리
시중에서 발생된 스크랩은 Mg 합금 단독의 경우도 있으나 다른 금속과 혼합되어있는 경우가 많다. 따라서 Mg 합금을 분리하기 위해 슈레더 등으로 파쇄한 후, 자력 선별로 철강재를 분리한다. 그 후 습식 비중 선별 등으로 Mg 합금을 선별할 수 있다. 선별∙회수된 Mg 합금 스크랩의 표면에는 도장층 등의 유기물이 부착되어 있는 경우가 많으므로 이들을 제거하여야 한다. Mg은 쉽게 연소되므로 유기물이 고착된 상태로 대기 중에서 용해시키면 Mg 용탕이 폭발할 가능성도 있다. 용해된 경우에도 유기물과 Mg의 비중 차이가 크지 않아 비중 분리가 곤란하여 주조재의 실수율이나 품질, 내식성을 저하시키는 문제점을 가지고 있다16).
Mg 합금 제품의 도장층 박리에는 기계적인 방법과 화학적인 방법이 있다. 기계적인 방법으로는 샌드 블라스팅이 있으나 Mg 분진이 발생하여 폭발할 위험성이 있다. 물과 연마제를 동시에 분사하면 안전하게 도장층을 박리할 수 있는 가능성이 있으나, 피 박리품을 고정시켜야하므로 양산성이나 다양한 형상의 스크랩에 적용하기 곤란한 문제점을 가지고 있다.
화학적인 방법으로는 산이나 알칼리를 사용하는 용액 처리가 있다. 그러나 용액 처리로 도장층을 박리하는 경우, 스크랩에 따라 도장의 종류가 다양하므로 완전한 박리가 곤란한 경우도 있다. 다만 동일한 스크랩의 경우 적절한 용액을 선택하면 충분한 박리가 가능하다. Kimura 등은 노트북 케이스의 도장층을 수산화 칼륨과 수산화 나트륨의 혼합 알칼리 용액으로 노트북 케이스의 도장층을 팽윤시켜 박리하였다17). 한편 Koyanaka 등은 과열 수증기를 이용하여 Mg 시중 스크랩의 도장 부착물 제거를 시도하였다18). 400~410 ℃에서 40~50분간 처리하여 스크랩 표면의 도장층을 쉽게 제거한 것으로 보고되어 있다. 동일한 방법을 이용하여 Mg 절삭 분말에 부착된 절삭유를 제거하기도 하였다19). 그리고 단파장 레이저를 스크랩 표면에 조사하여 유기물이나 장시간 사용으로 발생한 부식 부위를 제거하여 청정한 표면을 얻은 예도 있다16).
4.3. Mg 합금의 용탕 처리
Mg 합금 스크랩을 용융한 후, 용탕 처리에 의해 불순물을 제거할 수 있다. 다만 Mg 자체가 활성 금속이므로 불순물의 선택적 산화 제거는 힘들다. 따라서 Mg에 용해도가 없으며 제거 대상 원소와 결합할 수 있는 제3 원소를 첨가하여 불순물을 제거한다.
4.3.1. 금속 불순물의 제거
Mg 합금의 내식성 저하를 방지하기 위해서 Fe는 50 ppm 이하가 필요하다. Mg 중에 혼입되어 있는 Fe 제거는, Mg과는 반응하지 않으면서 Fe와 화합물을 만들기 쉬운 원소를 첨가하여 화합물을 만들도록 한다. Fe는 C와 반응하여 Fe3C를 만들므로 밀도 차이로 침강시켜 제거할 수 있다. 특히 C와 Ca을 동시에 첨가한 경우 Fe 탄화물의 클러스터를 만들어 쉽게 침강시킬 수 있다. 그러나 Al을 함유하는 용탕에서는 C이 Al과 쉽게 반응하므로 제거효율이 낮아질 수 있다. 그리고 Mn을 첨가하여 Al-Fe-Mn 화합물을 형성시켜 Fe를 침전 제거하는 방법도 제안되어 있다20).
그리고 Mg과 Cu는 금속간 화합물을 만들기 쉬워 Fe와 같이 화합물을 만들어 제거하는 것이 곤란하다. 다만 Mg과는 반응하지 않으면서 Cu와 반응하는 원소인 Ti을 Mg 용탕에 침지시켜 Mg 용탕 중의 Cu를 고상의 Ti으로 확산시켜 제거하려는 시도도 있었다. 그리고 Mg 중의 Si은 ZnCl2나 CoCl2를 첨가하여 Fe와 Si의 복합 화합물을 만들어 침전제거할 수 있다. 한편 650 ℃의 Mg 용탕 중에 Al을 약 3 wt%만 첨가하여도 Ni의 용해도가 0.15 wt%까지 감소하여 Ni을 제거할 수 있으며, Mn을 첨가하면 더 낮은 수준까지 제거되는 것으로 알려져 있다21).
4.3.2. 가스 취입에 의한 용탕 처리
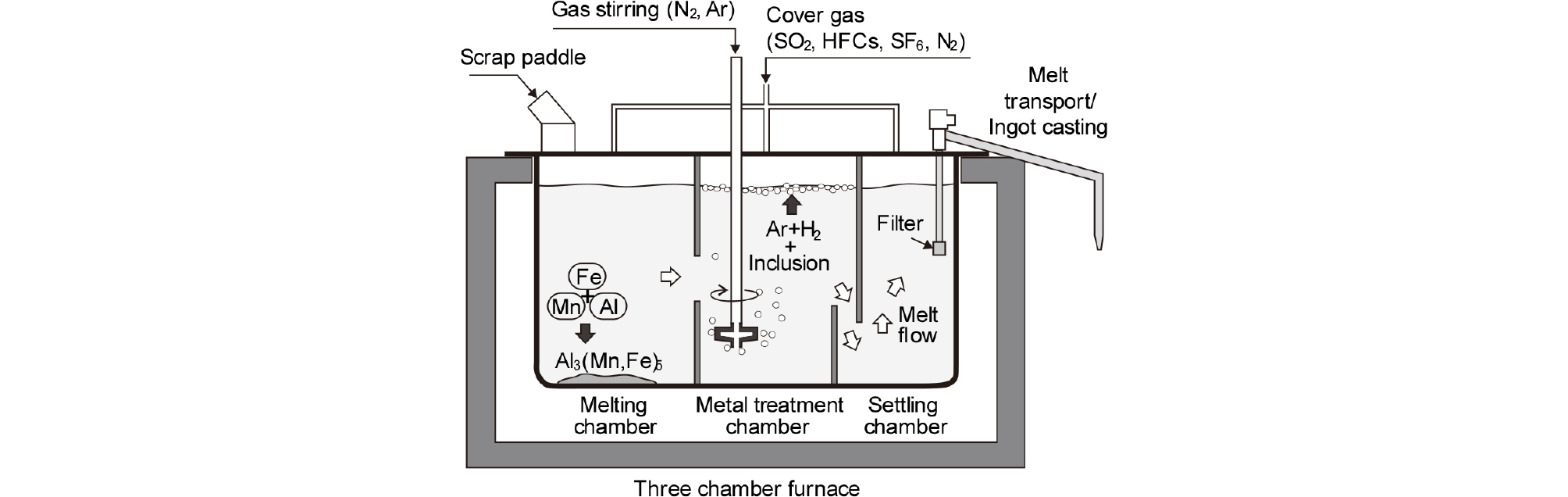
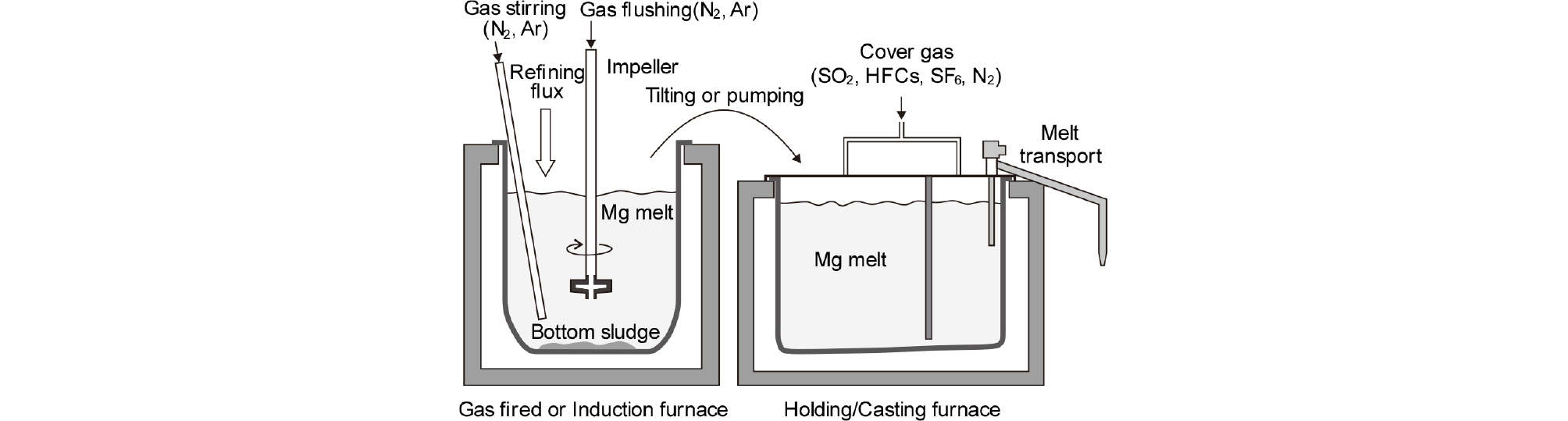
Mg 합금 주조품에 수소가 잔류하면 결함이 되므로 Al의 용탕 처리와 마찬가지로 불활성 가스를 취입하여 수소를 방출시켜 건전한 잉곳을 제조하고 있다. Mg 1차 지금과 함께 스크랩을 용해하여 Fe 등의 불순물은 침강 제거하고, 용탕 처리실에서 불활성 가스를 취입하여 수소 제거와 함께 개재물을 부상시켜 제거한다. Fig. 8에는 이러한 장치의 모식도를 재구성하여 나타내었다14,22). 한편 유지로에서는 용탕을 펌핑하여 주조기로 이송시킬 때 세라믹 필터를 설치하여 개재물 등을 제거하기도 한다23).
4.3.3. 플럭스에 의한 용탕 처리
Mg 스크랩을 재용해할 때, 플럭스를 사용하기도 한다. 플럭스는 MgCl2, KCl, BaCl2, CaCl2, CaF2 등으로 구성되어 있다24,25). MgCl2+KCl은 공정 조성으로 플럭스의 융점을 낮출 수 있으며, 불화물은 표면 젖음성과 MgO와의 반응성이 우수하다. BaCl2(밀도 3.85 g/cm3)는 밀도가 높아 플럭스가 Mg 용탕과 잘 혼합되도록 한 후 도가니 바닥에 쉽게 침강시키는 특징이 있다. 이러한 플럭스는 Mg 합금 종류에 따라 조성을 달리해야 한다. 특히 희토류가 함유된 합금의 경우 희토류 금속이 MgCl2와 반응하므로 CaCl2를 사용한다.
Fig. 9에는 플럭스를 사용하여 Mg 용탕을 정련하는 공정의 모식도를 나타내었다20). 스크랩을 장입하여 용융시키고, 플럭스를 첨가하여 산화를 방지한다. 산화 방지나 정련을 위한 플럭스로는 CaF2계를 많이 사용한다. 그리고 일반적으로는 Fig. 9에서와 같이 플럭스 단독보다는 불활성 가스와 함께 취입하여 정련하고 있다.
4.4. 진공증류에 의한 정제
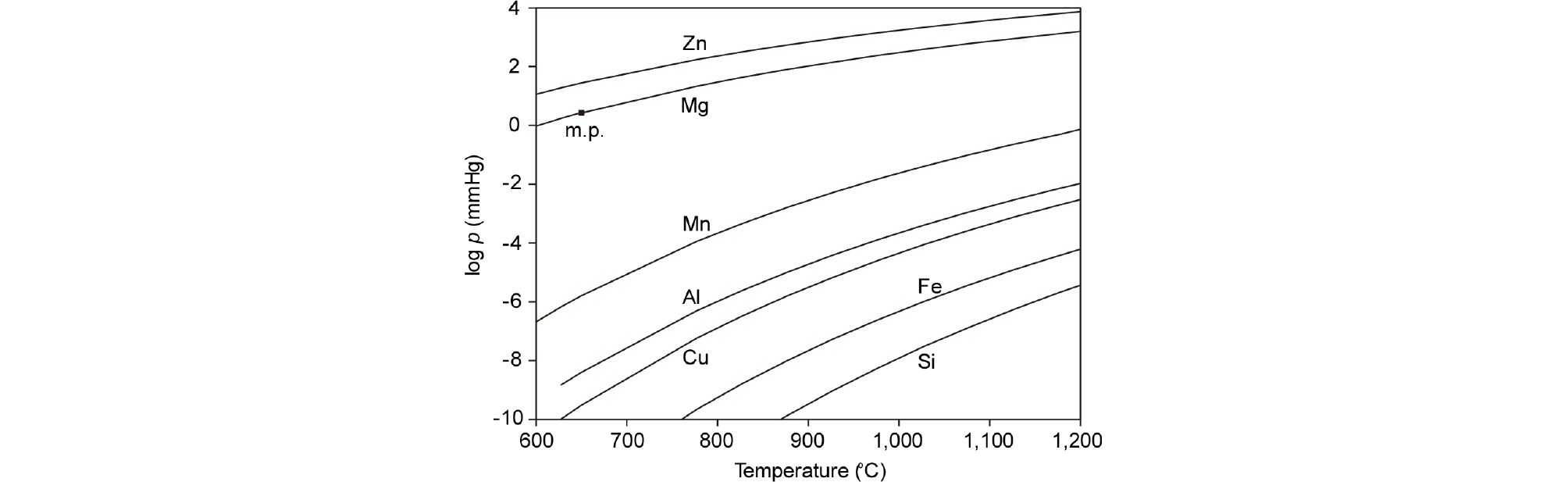
Mg은 증기압이 매우 높은 금속이므로, Mg 합금 스크랩을 용융하여 감압 상태에서 증류∙정제하면 고순도의 Mg을 얻을 수 있다. Fig. 10에는 Mg과 Mg 합금 원소 등의 온도에 따른 증기압을 계산하여 나타내었다. Zn는 동일한 온도에서 Mg보다 증기압이 높으므로 증류에 의해 제거할 수 없으나 AZ계 합금의 원료로 사용할 수 있다. 나머지 원소들은 증기압이 Mg보다 낮으므로 용탕에 잔류시켜 제거할 수 있다26). 실제로 Mg 합금 스크랩 용탕으로부터 고순도 Mg을 얻기 위해 많은 연구들이 수행되었다27,28,29).
4.5. Mg 절삭 칩의 고체 상태 리사이클링
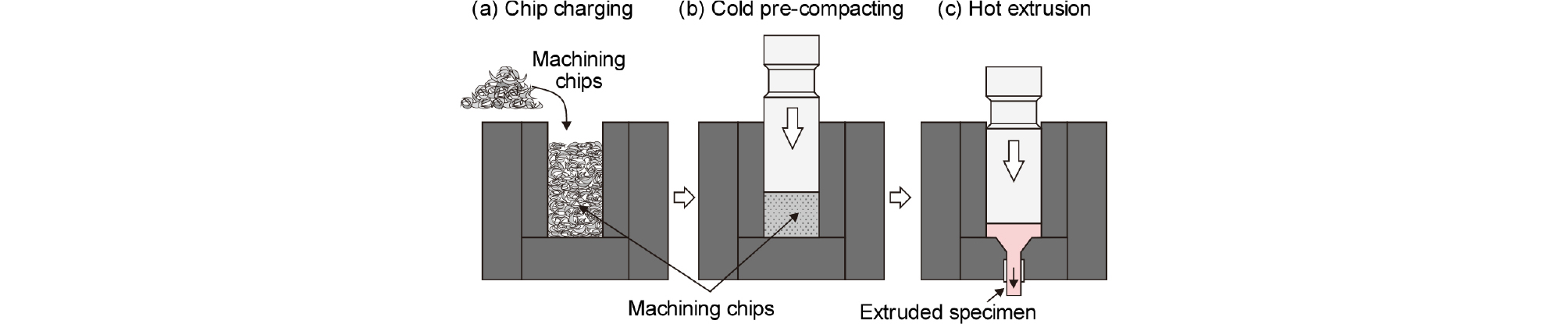
Mg 합금 부품을 제조하는 공정에서 발생하는 절삭 칩(chip)은 압축∙재용해하여 리사이클링하고 있으나, 고체 상태에서 빌릿 등을 제조하는 방법도 보고되어 있다30). 절삭 칩에 부착되어 절삭유 등은 사전에 제거한 후, 곧바로 열간 압출하거나, 미리 냉간 압축한 후 열간 압출에 의해 빌릿 등을 만들 수 있다. 특히 Mg 합금은 일정 온도에서 압력을 가하면 급격하게 결정립이 미세화되는 동적 재결정 현상이 일어나며, 고체 상태의 리사이클링은 이 원리를 이용하는 방법으로, Al31)이나 Ti32)에서도 유사한 리사이클링 방법이 보고되어 있다. Fig. 11에는 이러한 고체 상태의 리사이클링 방법을 모식적으로 나타내었다.
5. 종 합
본 연구에서는 Mg의 제련기술 현황과 Mg(합금) 스크랩의 리사이클링 기술 현황에 대하여 고찰하였다. Mg은 희소 금속으로 분류되고 있으나 전 세계 연간 생산량은 110만 톤이 넘으며, 지각 중 원소 존재도에서 7번째로 풍부한 원소이다. 우리나라는 Mg 1차 지금을 생산하지 않으나, 2018년 기준 우리나라의 Mg 1차 지금 수요는 약 24,400 톤이며, 리사이클링한 2차 지금 생산량은 11,800 톤 정도이다. 전 세계 Mg 생산량의 80 % 이상은 Si 열환원법인 Pidgeon법으로 만들고 있다.
Mg 스크랩 중 제품 제조공정에서 발생하는 자가 스크랩의 대부분은 리사이클링 되고 있으나, 기계 가공 중에 발생하는 절삭 칩이나 시중에서 발생한 노폐 스크랩은 아직 리사이클링 공정이 확립되지 못하고 있다. 자가 발생 스크랩은 재용해와 가스 취입, 플럭스 처리, 여과 등의 공정을 거쳐서 리사이클링 되고 있다. 다양한 합금 형태로 사용된 후 폐기된 노폐 스크랩은 여러 가지 합금이 혼합되어 있는 경우가 많으므로 합금 원소를 제거하는 것이 필요하며, 증류 정련으로 고순도의 Mg을 회수하기도 하지만, 불순물 원소를 쉽게 제거할 수 있는 정련기술 등이 확립된다면 리사이클링율이 상승할 것으로 기대된다. 절삭 칩은 유분 등을 제거한 후에 냉간 압축-열간 압출 등의 방법으로 고체 상태에서 리사이클링하는 방법이 보고되어 있다. 향후 Mg의 리사이클링을 활성화하기 위해서는 Mg의 용탕 처리 기술이나 고체 상태의 리사이클링 기술에 대한 연구∙개발이 필요할 것으로 사료된다.