1. 서 론
2. 탄탈럼의 생산량과 용도
3. 탄탈럼의 제련
3.1. 탄탈럼의 원료
3.2. 광석의 분해 및 Ta2O5와 Nb2O5의 분리
3.3. 탄탈럼 할로겐화물의 환원
3.4. 탄탈럼 산화물의 환원
3.5. 금속 탄탈럼의 정제
4. 탄탈럼의 리사이클링
4.1. Ta 커패시터 중 Ta 회수
4.2. 금속 Ta 및 합금 스크랩의 리사이클링
5. 종 합
1. 서 론
탄탈럼(tantalum, Ta)은 나이오븀(niobium, Nb), 바나듐(V)과 함께 주기율표의 5족에 속하는 전이금속으로 융점이 3,017 ℃인 대표적인 고융점 금속이다. Ta의 지각 중 원소 존재도는 2.0 ppm(52위)으로 Nb(20 ppm, 33위)의 1/10에 불과하며1), 전 세계 연간 생산량이 약 2,000 톤 수준에 불과한 희소금속이다. 특히 Ta은 Nb과 마찬가지로 반응성이 높아 소재화하기 힘든 희소금속이지만, 과학기술 및 산업적으로 매우 중요한 핵심 금속이다.
Ta은 희토류를 비롯하여 많은 원소가 발견된 스웨덴의 이테르비(Ytterby)에서 1802년에 에크베리(Anders Ekberg)가 발견하였다. 그러나 1801년에 발견된 Nb과 특성이 유사하여 1846년 독일의 로제(Heinrich Rose)가 Nb과 Ta을 분리할 때까지는 Nb과 혼동되었다2). 1903년 볼턴(Werner von Bolton)이 비교적 순수한 Ta을 만들어 전구의 필라멘트용으로 사용하였다. Ta의 명칭은 그리스 신화의 탄탈로스 왕에게서 유래하였다. 신화 속 탄탈로스 왕이 신들의 음식인 암브로시아를 훔쳐 인간에게 준 죄로 지옥에서 과일도 못 먹고 물도 마시지도 못하며 영원히 고통받는데, 많은 양의 산에도 녹지 않을 만큼 내산성이 강한 원소의 특징이 탄탈로스 왕과 비슷하다 하여 ‘탄탈럼(tantalum)’으로 명명하였다3). 또 Ta이 Nb과 오랫동안 혼동되었던 사정과 유사하게 탄탈루스가 지옥에서 먹거나 마시지 못하며 감질만 났었기 때문이라고도 한다. 실제로 영어 단어 ‘tantalize’는 ‘감질나게 하다’라는 뜻이 있다. Nb은 Ta과 한 몸이었기 때문에 탄탈로스의 딸인 니오베(Niobe)로부터 나이오븀(niobium)이라 명명하였다.
Table 1에는 Ta의 물리화학적 성질을 같은 족의 V, Nb과 비교하여 나타내었다. Ta은 백금과 유사한 은회색을 띠며, 밀도, 전성, 연성이 높고 매우 단단하지만 가공하기 쉬운 금속이다. 그리고 Ta은 왕수에도 용해되지 않는 등 백금과 동등한 내산성을 가지고 있으면서, 융점은 실용 금속 중에서 W(3,422 ℃) 다음으로 높아 내열성이 우수하다. 특히 Ta은 금속 중에서 가장 안정한 양극산화피막을 만들며, 이 피막의 유전율이 Al 피막의 2.7배에 달할 정도로 매우 높다. 따라서 Ta 커패시터(capacitor)는 Al 커패시터의 1/60 크기로도 동등한 성능을 나타내므로 휴대용 기기 등의 소형화에 크게 기여하였다. Ta은 이러한 특별한 성질들로 인해 생산량은 적으나 현대 산업의 핵심 금속이 되었다. 본 논문에서는 이러한 Ta의 생산량, 용도, 제련방법 및 리사이클링 현황 등에 관하여 고찰하였다.
Table 1
Physico-chemical properties of vanadium, niobium and tantalum
2. 탄탈럼의 생산량과 용도
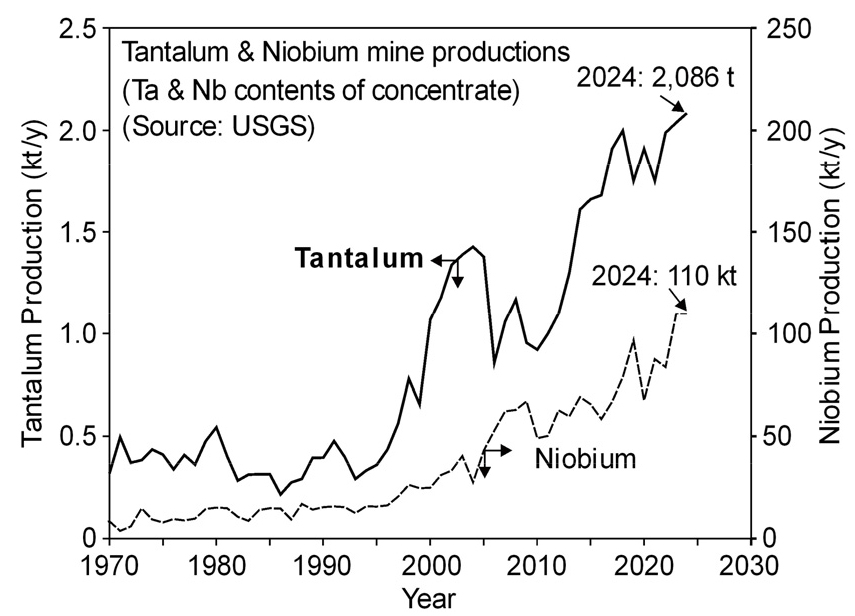
Fig. 1에는 Ta 함유량 기준 전 세계 광산 생산량의 변화를 Nb과 비교하여 나타내었다4,5). Ta과 Nb의 생산량은 1990년대 후반부터 급격하게 증가한 후 정체되었으나, 2010년부터 휴대용기기의 보급과 함께 다시 급격하게 증가하였다. 그러나 Ta의 생산량은 Nb의 1/50에도 미치지 못하며, 2024년 기준 연간 2,086톤이 생산되었다.
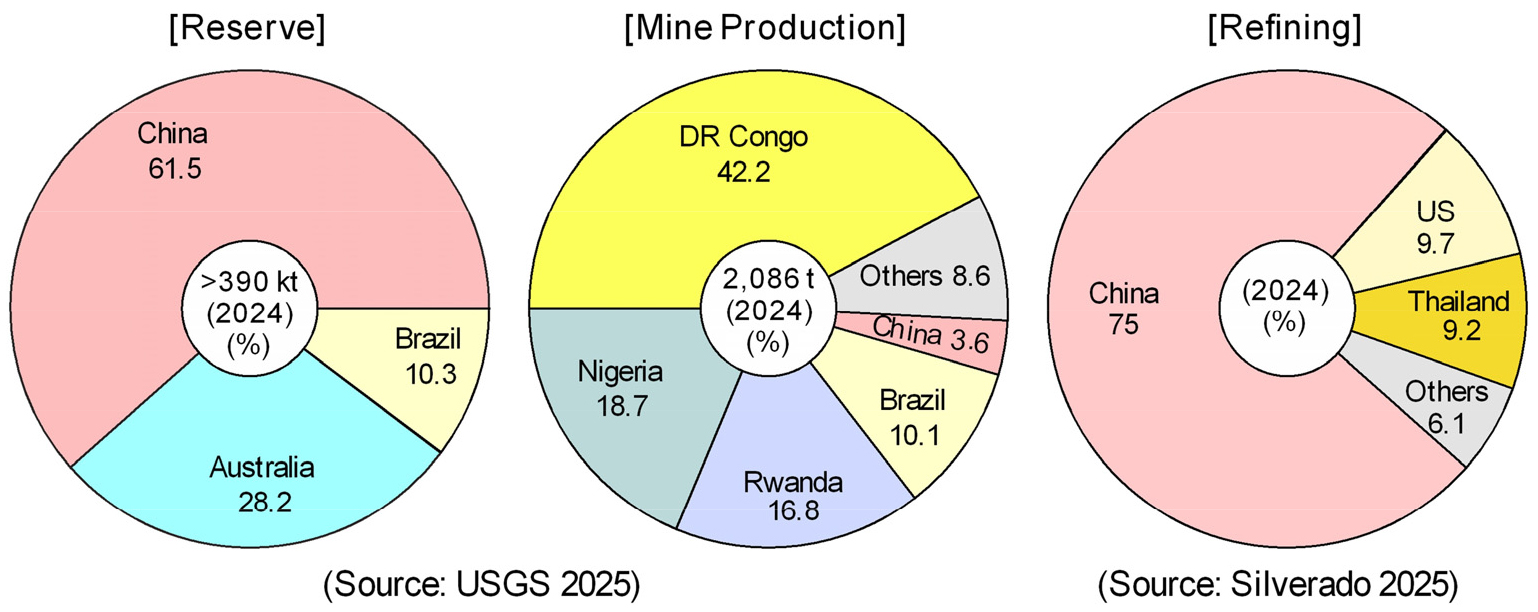
Fig. 2에는 2024년 기준 Ta의 국가별 매장량과 생산량 비율을 나타내었다6). Ta의 매장량은 USGS 자료에서 중국(61.5 %), 호주(28.2 %), 브라질(10.3 %)만 공개되어 있다. 생산 국가를 보면 콩고를 비롯한 아프리카에도 상당량이 매장되어 있는 것으로 추정되지만, 분쟁광물(conflict minerals)로 지정되어 공개되지 않고 있다. 2024년 기준 Ta 생산량은 콩고 공화국(42.2 %)이 가장 많고, 이어서 나이지리아(18.7 %), 르완다(16.8 %), 브라질(10.1 %) 등이며, 중국도 약 3.6 %를 생산하고 있다. 그러나 제련은 중국이 75 %를 차지하는 등 특정 지역에서만 생산되는 희소금속으로 현대 산업의 필수 핵심 금속이어서 안정적인 공급선의 확보가 중요하다.
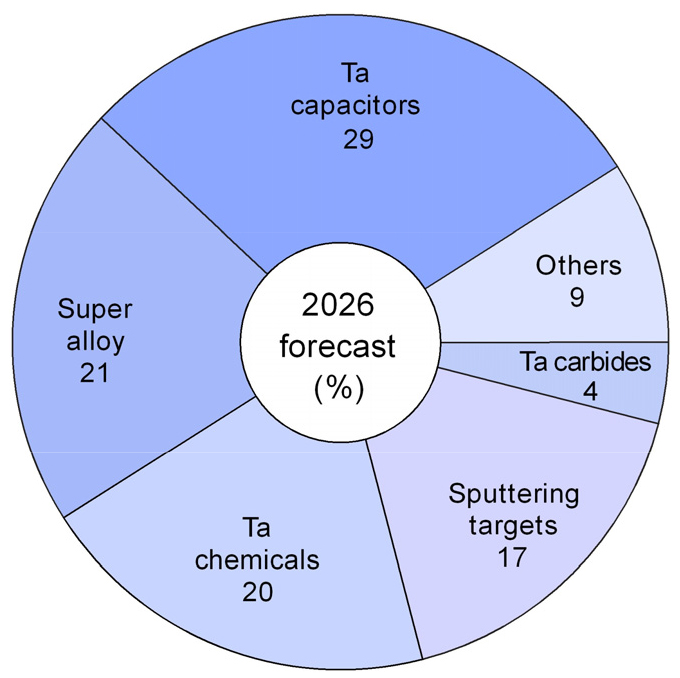
Fig. 3에는 2026년의 Ta 용도 비율을 예측한 결과를 나타내었다7). Ta은 커패시터용의 금속 Ta 분말 및 선재가 전 세계 수요의 약 30 %를 차지하며, 초합금, 화학장치, 반도체 등에 사용된다. 특히 Ta 커패시터는 노트북 PC, 태블릿 PC, 스마트폰 등 정보통신 기기의 소형화, 고성능화에 필수적이며, 그 외에도 액정 TV, 디지털 카메라, 비디오 카메라 등 디지털 가전이나 자동차 부품 등에 사용되고 있다. 또 Ta은 내열, 내식 재료, 내열 합금(superalloy)의 첨가원소, 스퍼터링 타깃(sputtering target) 등에 사용되고 있으며, Ta 산화물이나 탄화물 등의 화합물은 절삭공구, 광학렌즈 등에도 사용되고 있다. 그러나 분쟁광물인 Ta은 매장량과 생산량이 적고 고가여서 Ta 사용량을 줄이고, 화학적 성질이 유사한 Nb으로 대체하려 하고 있다.
3. 탄탈럼의 제련
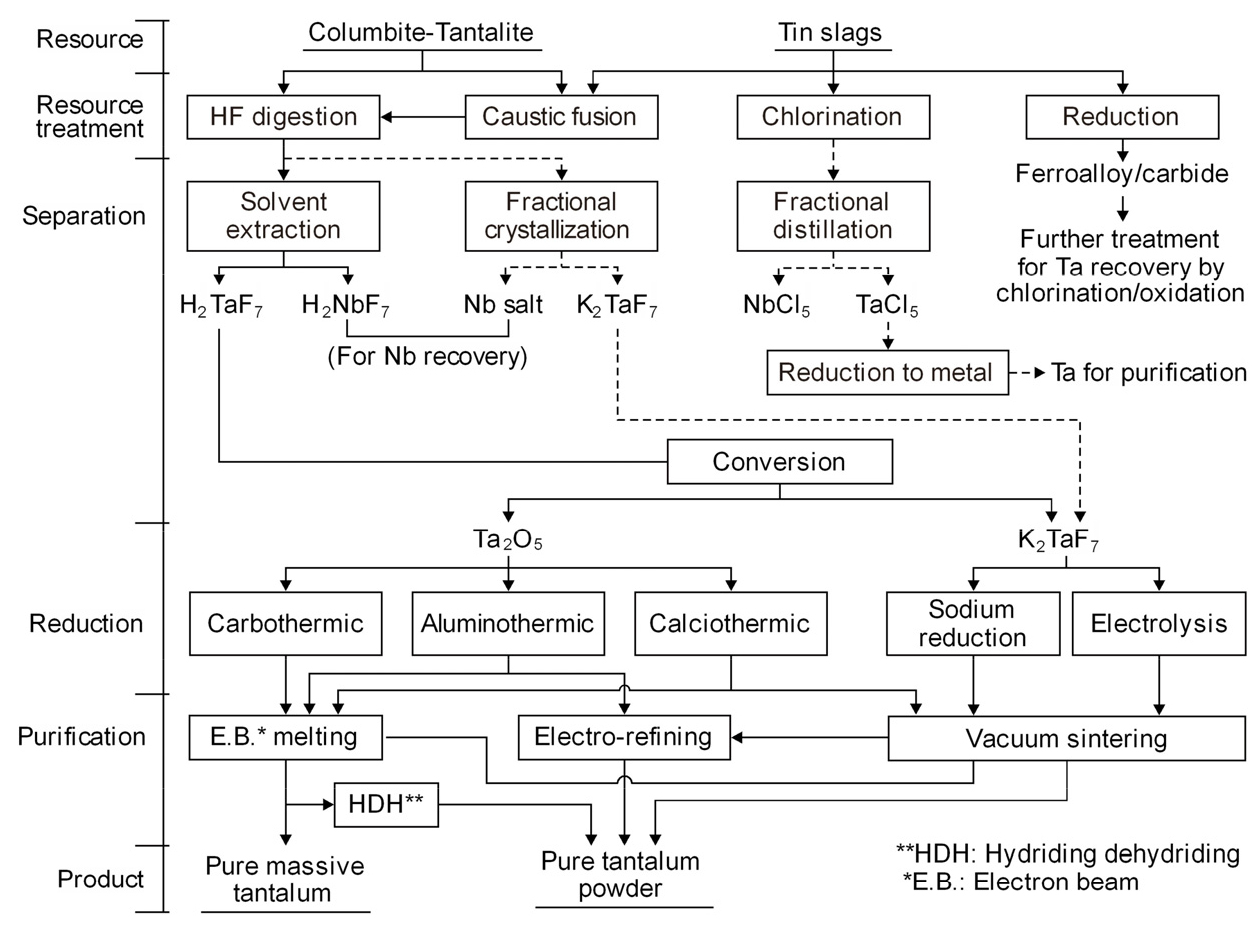
Fig. 4에는 Ta 원료에서 금속 Ta을 만드는 공정도를 나타내었다8). 금속 Ta의 원료에는 광석과 주석(Sn) 제련 슬래그가 있으며, 각각의 원료는 전처리 공정을 거쳐 용매 추출 등으로 Ta을 분리하여 추출한다. 이어서 Ta 산화물이나 Ta 불화물을 열환원, 용융염 전해 등으로 조금속을 만들고, 전자빔 용융, 전해정련, 고온 진공처리 등으로 정제하여 고순도 Ta을 만든다.
3.1. 탄탈럼의 원료
Table 2에는 Ta과 Nb의 주요 광물 및 조성 범위를 나타내었다2). Ta과 Nb은 화학적 성질과 원자 이온 반경이 유사하여 단독으로 존재하는 경우는 거의 없으며, Ta과 Nb의 산화물이 결합되어 있거나 다른 원소와 결합하여 탄탈라이트(tantalite)나 컬럼바이트(columbite)로 존재한다. Ta의 가장 중요한 광석으로는 columbite-tantalite, 파이로클로르(pyrochlore), Ta과 Nb을 함유한 주석광 등이 알려져 있다. Columbite-tantalite는 화학적으로 철망간 탄탈라이트-컬럼바이트((Fe,Mn)(Ta,Nb)2O6)로 이루어져 있다. Ta 함량이 높으면 탄탈라이트, Nb 함량이 높으면 컬럼바이트로 부르며, Ta과 Nb의 함량이 비슷하면 탄탈로컬럼바이트(tantalocolumbite)로 부른다9).
Table 2
Selected niobium and tantalum oxide minerals and their end-member Nb2O5 and Ta2O5 contents or compositional range2)
3.2. 광석의 분해 및 Ta2O5와 Nb2O5의 분리
Ta과 Nb은 항상 컬럼바이트와 탄탈라이트에 공존하므로 Ta2O5를 얻기 위해 광석을 분해하여야 한다. Table 3에는 용매에 따른 원료물질의 분해 및 침출 효율을 나타내었다10). Ta2O5는 HCl, HNO3, H2SO4, H3PO4, HCl+HNO3 등의 용액에서는 거의 용해되지 않으며, Nb2O5는 마이크로웨이브를 이용한 황산에 의한 분해와 B4Li2O7(lithium tetraborate)를 이용한 용융과 황산 침출에서 거의 100 % 가까이 용해되는 것을 알 수 있다. 따라서 Ta 광석은 불산 분해, 알칼리 용융, 염화 등으로 분해한 후 용매 추출법 등으로 분리한다.
Table 3
Summary of dissolution efficiency of niobium and tantalum using acid/alkaline leaching and acid/alkaline fusion followed by acid/water leaching10)
3.2.1. 불산 분해와 용매추출
대부분의 Ta-Nb 광석은 HF나 HF+HNO3/H2SO4에 쉽게 침출되지만, 일반적으로 불산을 사용하여 광석을 분해한다. Nb과 Ta의 분리는 분별 결정법을 이용하기도 하였으나, 현재는 불화물 함유 용액에서 MIBK(Methyl Isobutyl Ketone), DEHPA(di(2-ethylhexyl)phosphoric acid), 옥탄올(octanol), Alamine 336, TBP( tri-nbutyl phosphate), 시클로헥사논(cyclohexanone) 등을 이용한 용매 추출법으로 분리한다11).
한편 Ta과 Nb의 분리는 용매추출이 일반적이지만, 혼합산의 이온 강도를 조절하여 Nb을 수용액 중으로 추출할 수 있다. 또 암모니아를 용액에 첨가하여 Nb을 산화물로 침전시키거나, KF를 첨가하여 Nb을 불화칼륨 착체를 만들어 침전시켜 분리할 수도 있다12). Nb을 분리하여 정제한 H2(TaF7) 용액은 다음 식과 같이 암모니아 수용액으로 중화시켜 Ta2O5의 수화물로 만든 후 하소하여 Ta2O5를 얻는다.
또 다음 식과 같이 KF를 첨가하여 불화칼륨의 착체(potassium heptafluorotantalate)를 만들어 침전시키도 한다.
3.2.2. 알칼리 용융법
Ta 함유 정광을 NaOH나 Na2CO3, KOH 등과 함께 용융시켜 Ta과 Nb을 탄탈산소다(sodium tantalate)와 나이오븀산소다(sodium niobate)로 만든다13). 이어서 용융물을 수 침출하여 물에 가용성인 Si, Sn, W, Al 등의 불순물을 제거한다. 회수한 잔사를 가열하면서 20 % HCl로 침출시켜 Ta과 Nb을 각각 탄탈산과 나이오븀산으로 침전시키고, 산에 가용성인 나머지 불순물을 제거한다. 그리고 침전물을 불산으로 용해하여 용매 추출 등으로 Ta과 Nb을 분리한다11).
3.2.3. 염화법
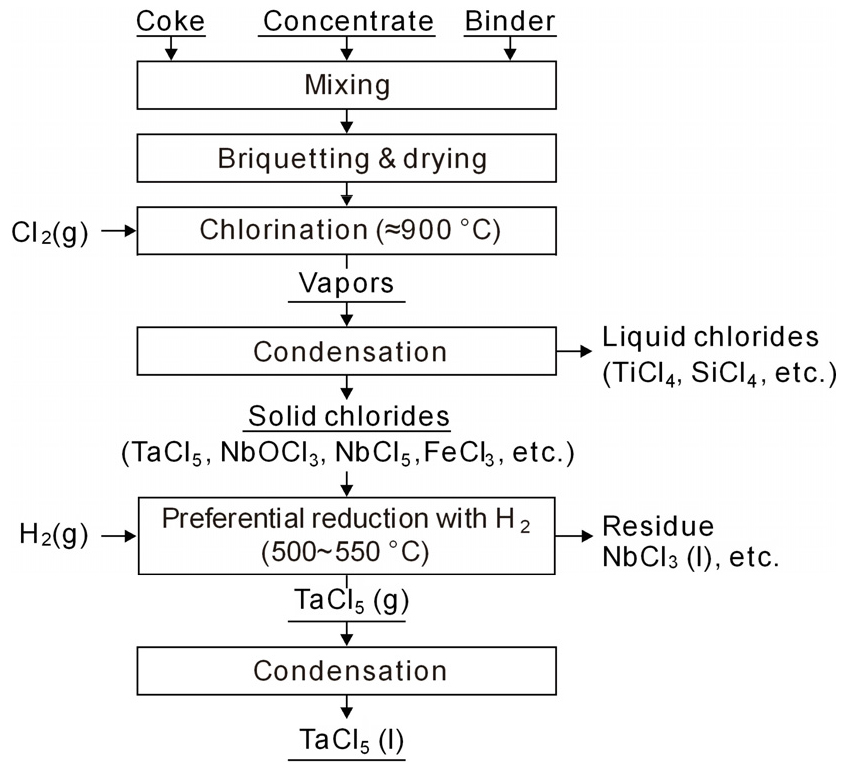
염화법은 Ti이나 Zr, Mg 등의 제련에서도 사용하는 것으로, 천연광석 등을 환원 염화하는 방법과 합금철인 FeTa을 염화하는 두 가지 방법이 있다11). Fig. 5에는 정광 염화법의 공정도를 나타내었다14). 정광의 염화 반응은 다음 식과 같이 산소를 제거하기 위한 C이 필요하다(Me: Ta, Nb etc.).
따라서 환원 염화를 위해서 천연광석이나 정광에 코크스와 피치를 혼합하여 단광으로 만들어 건조시킨 후, 약 900 ℃에서 염소 가스와 반응시킨다.
염화 과정에서 Si, Sn, Ti 등의 4염화물(tetrachloride)과 WOCl4도 함께 증류되므로 나머지 불순물들은 잔사에 남겨 제거할 수 있다. 그리고 TaCl5와 NbCl5의 분별증류는 불순물 제거에 효과적인 방법지만8), 각각의 끓는 점이 239 ℃와 249 ℃로 10 ℃밖에 차이가 나지 않아 다단계의 증류가 필요하다. 따라서 H2에 의해 TaCl5가 환원되지 않는 500~550 ℃에서 NbCl5만 선택적 환원으로 NbCl3(s)를 생성시켜 분리한다. 그리고 기체상태의 TaCl5(g)는 콘덴서로 흘러가 응축되므로 분리하여 회수할 수 있다13).
3.3. 탄탈럼 할로겐화물의 환원
금속 Ta은 할로겐화물을 금속열환원법과 용융염 전해법으로 환원하거나 산화물을 열환원법 등으로 환원하여 만들며, Table 4에 출발원료에 따른 환원 방법을 종합하여 나타내었다15).
Table 4
Comparison of reduction processes for tantalum metal15)
| Process | Reductant | Product | Post reduction | Remark | |
|
MTR* of K2TaF7 | Closed bomb | Na | Powder | Aq. leaching | Capacitor grade powder |
| Agitated bath | Na | Powder | Aq. leaching | Capacitor grade powder | |
|
Graphite Crucible | Al | Al3Ta |
Al removal by alloying with Cu followed by Cu-Al removal | Ta powder | |
|
FSE** of K2TaF7 | Halide containing melt | electron | Powder |
C removal followed by vacuum sintering | Capacitor grade Ta powder |
|
Oxide (Ta2O5) containing melt | electron | Powder |
C removal followed by vacuum sintering | Capacitor grade Ta powder | |
| Oxide Reduction | MTR in Ar | Ca-CaCl2 | Powder | Aq. Leaching, V/S | Higher Oxygen, yield 90 % |
| MTR in closed bomb | Ca with S | Massive | EB melt refining | Yield: 70~75 % | |
| Al with S | Massive | EB melt refining | Cheaper, yield 88 % | ||
| Al with Fe, Mn, Si | Massive | EB melt refining | Yield: 85~88 % | ||
| Open top reactor | Al-KClO3 | Massive | FS electrofining | Ta-4.7Al alloy, yield 84 % | |
| Carbothermic | C | Sponge | Vacuum sintering | Commercial process | |
|
Carbonitro- thermic | C-N2 | Sponge | Thermal decom. | Yield: +96 % | |
3.3.1. 불화물의 Na 환원
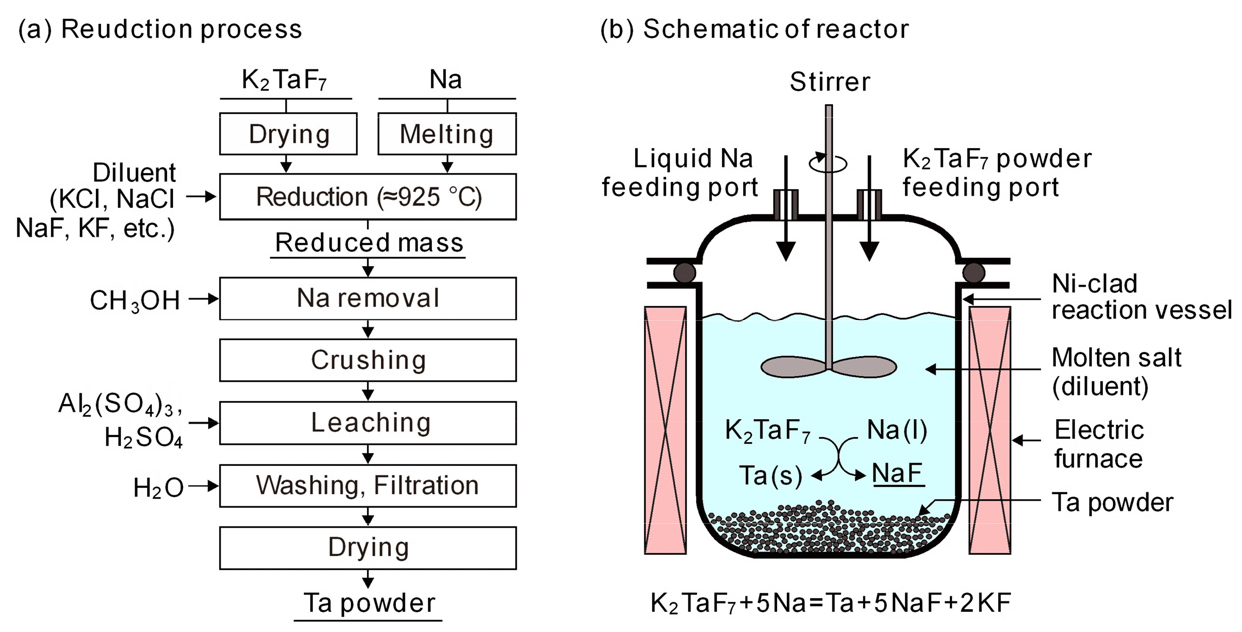
공업적인 금속 Ta 제조는 고체상태의 K2TaF7을 약 800 ℃에서 다음 식과 같이 액체 Na으로 환원하는 Hunter법을 사용하며16), Fig. 6에는 Na으로 환원하는 공정도와17), 환원 반응기의 모식도를 나타내었다18).
Na에 의한 K2TaF7의 환원은 매우 격렬한 발열반응이어서 KCl, NaCl, KF, NaF 등을 희석제로 첨가하며, 환원반응에서 생성된 NaF와 KF는 이러한 희석제(diluent) 중에 용해된다. 반응이 완료된 후 냉각시켜 용융염을 알콜이나 온수로 침출시켜 제거하면 분말상의 조금속 Ta이 얻어진다. 조금속 Ta은 산세 후 진공 열처리하거나, 전자빔으로 용융하여 Ta 잉곳으로 만든다. 또 Ta 분말은 조금속을 분쇄하거나 전자빔 용융한 잉곳을 수소화하여 분쇄한 후 진공 열처리로 탈수소하는 HDH(hydriding dehydryding)법으로 만든다. 한편 Kolosov 등은 Na 대신에 K으로 K2TaF7을 환원하였으나, 생성된 Ta이 스펀지상으로 응집되어 있었으며, 비표면적도 적어 커패시터로는 부적합한 것으로 보고하였다19).
3.3.2. 염화물의 Mg 환원
TaCl5의 금속 Mg에 의한 열환원 반응은 전기화학적으로 중성 화학종인 원료와 환원제가 확산하여 물리적 접촉에 의해 반응이 진행되며, 반응식은 다음과 같다.
한편 이러한 반응은 반응계 내에 이온과 전자를 운반하는 물질이 원료와 환원제의 물리적 접촉이 없어도 전기화학적 산화환원반응으로 진행할 수 있다. Park 등은 상기한 반응을 다음과 같이 금속 도전체를 매개한 반응(electronically mediated reaction, EMR)으로 나타내었으며20,21), 물리적인 접촉이 없어도 열환원 반응이 가능한 것으로 보고하였다.
3.3.3. 염화물의 수소환원
Park 등은 CVC(chemical vapor condensation) 원리로 1,400 ℃에서 TaCl5 증기와 H2를 반응시켜 14~56 nm 크기의 Ta 분말을 얻었다22). TaCl5의 수소에 의한 환원반응은 다음과 같다.
3.3.4. 탄탈럼 불화물의 용융염 전해
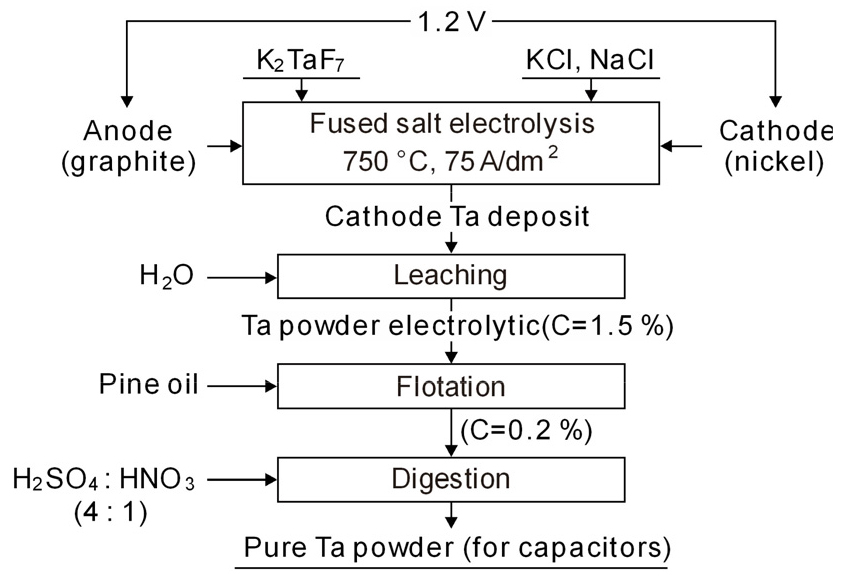
K2TaF7을 용융염 전해하여 커패시터용의 고순도 Ta 분말을 만들 수 있으며, Fig. 7에 공정도를 나타내었다15). 전해질은 KCl-NaCl의 공정 조성에 25 wt% K2TaF7을 첨가한 것이며, 흑연 도가니 중 700~800 ℃에서 K2TaF7의 분해전압인 1.2 V 이상에서 전해한다. 용융염 전해용 도가니가 흑연이므로 Ta 분말 중에 1~1.5 %C이 잔류하지만, pine oil을 이용한 부유 선별에 의해 0.2 %C까지 낮출 수 있다. 또 혼산(황산+질산)으로 침출하여 C을 23 ppm까지 낮추어 커패시터용 Ta 분말을 얻었다. 한편 Ta2O5를 55.0 % KCI, 27.5 %KF, 17.5 %K2TaF7의 전해욕 중에 첨가하여 용융염 전해를 하기도 하였다23).
3.4. 탄탈럼 산화물의 환원
산화물 원료는 할로겐화물보다 취급이 쉽고, 또 열환원 반응으로 환원할 수 있으므로 금속 Ta 제조에 적합한 출발원료이다. 환원제로는 C, Ca, Al, Mg 등이 있으나 일반적으로는 Ca과 Al을 많이 사용하며, Fig. 8에 산화물 환원법을 종합하여 나타내었다15).
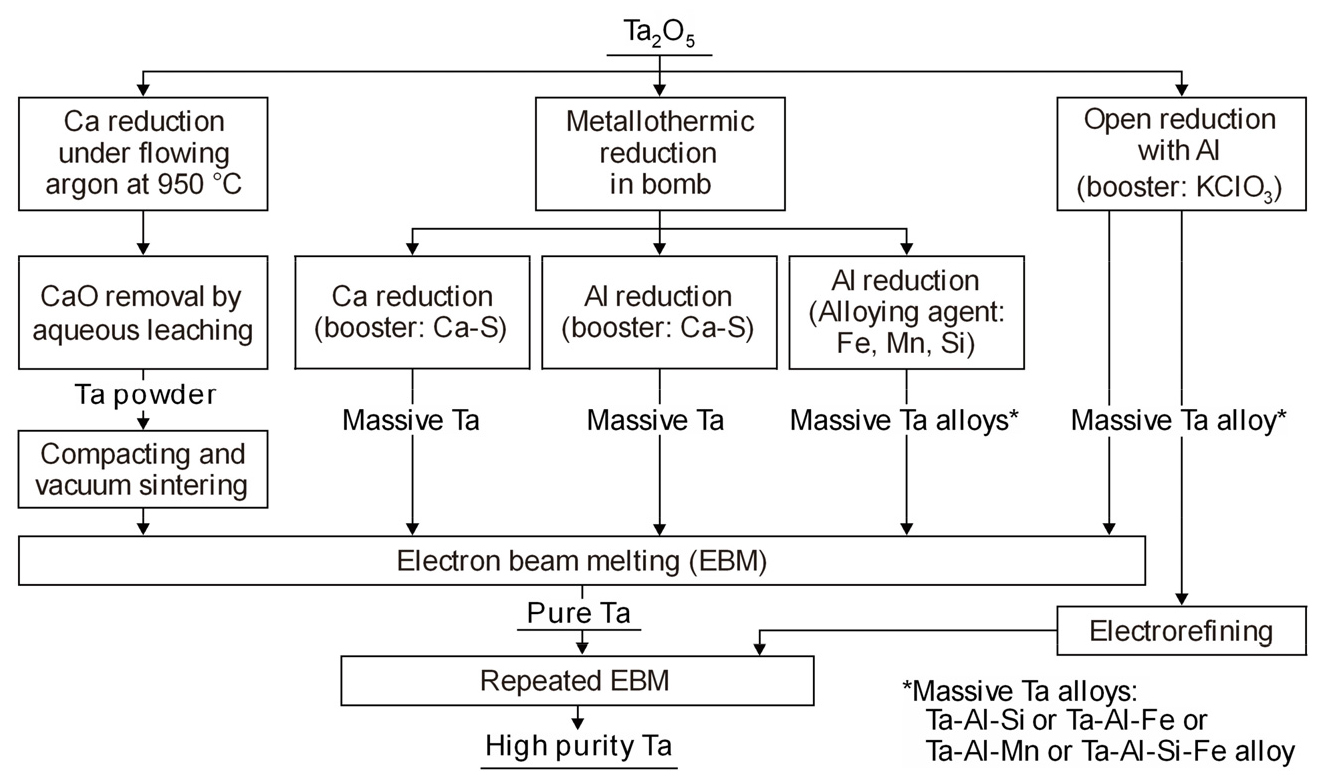
Fig. 8.
Comparison of various processes for the preparation of pure tantalum by the metallothermic reduction of oxide15).
3.4.1. 산화물의 Ca 열환원
Ta2O5의 Ca에 의한 열환원 반응은 다음과 같다24).
그러나 부산물인 CaO가 생성 Ta 입자들 사이에 갇혀 질산 침출에서도 제거되지 못하여 산소 농도는 1 wt% 정도를 나타내었다.
Ca 환원의 부산물인 CaO 제거를 위해 CaCl2-Ca 중에서 Ta2O5를 환원하여 CaO를 CaCl2에 용해시킨 예도 있다. 이러한 반응 후 CaCl2와 CaO는 물과 묽은 HCl로 침출시켜 제거하였으며, 생성 Ta 중 산소 농도는 약 6,000 ppm 수준이지만, 진공 열처리나 전자빔 용융으로 30 ppm 이하까지 낮출 수 있다25). 괴상의 Ta은 봄베형 반응기를 이용하지만, 보다 고온에서 반응시켜 금속-슬래그의 분리가 쉽도록 (Ca+S)를 heat booster로 첨가하여 반응시킨다.
3.4.2. 산화물의 Al 열환원
Ta2O5의 Al 열환원 반응은 다음과 같다.
Al 열환원 반응은 Ca 열환원보다 발열량이 부족하여 S을 첨가하여 Al2S3가 생성될 때의 열을 이용하며, 슬래그의 융점을 낮추는 효과도 있다15). 또 부족한 열량 보충을 위해 수소 플라즈마 반응기를 사용하거나, Al과 함께 KClO3를 촉진제로 첨가하고, Fe, Mg, Si 등으로 Ta의 2원계 및 3원계 합금으로 만들어 금속상의 융점을 낮추기도 한다. 생성된 합금은 전자빔으로 용융 정련하면 합금 성분을 제거할 수 있다.
3.4.3. 산화물의 C 열환원
Ta2O5를 C으로 열환원할 수 있으나, Ca이나 Al과 달리 3단계의 반응으로 금속 Ta이 얻어진다. 우선 Ta2O5와 C을 혼합하여 약 1,700 ℃의 10-3 torr 분위기에서 반응시켜 다음 식과 같이 TaC를 얻는다26).
1단계 반응에서 생성된 TaC를 Ta2O5와 혼합하여 펠릿으로 만들고, 2,100 ℃의 고진공(10-5 torr) 분위기에서 반응시키면 다음 식과 같이 Ta 스펀지가 만들어진다.
스펀지상의 Ta은 수소화시켜 파쇄하며, Ta 중 잔류 C 농도에 따라 성분 조정을 하고 최종적으로 진공 소결하거나 전자빔 용융으로 정련한다.
한편 금속 Nb과 마찬가지로 Ta 질화물을 경유하는 방법도 알려져 있다. TaN은 1,650 ℃ 이하의 질소 분위기에서는 안정하지만, 1,800 ℃ 이상의 진공 분위기에서는 분해된다. 따라서 Ta2O5를 C과 혼합하여 펠릿으로 만들어 질소 분위기 중에서 탄소 열환원 반응으로 TaN을 만들고, 이어서 0.01 Pa의 진공 분위기 중에서 약 2,150 ℃로 가열하면 TaN이 분해되어 금속 Ta 스펀지를 얻을 수 있다15).
3.5. 금속 탄탈럼의 정제
조금속 Ta 중 불순물은 침입형 원소와 치환형 원소로 구분할 수 있으며, 이러한 불순물은 고온에서의 진공 열처리나 전자빔 용융으로 정제할 수 있다. 또 용융염을 사용한 전해정제에 의해 고순도 Ta을 얻기도 한다.
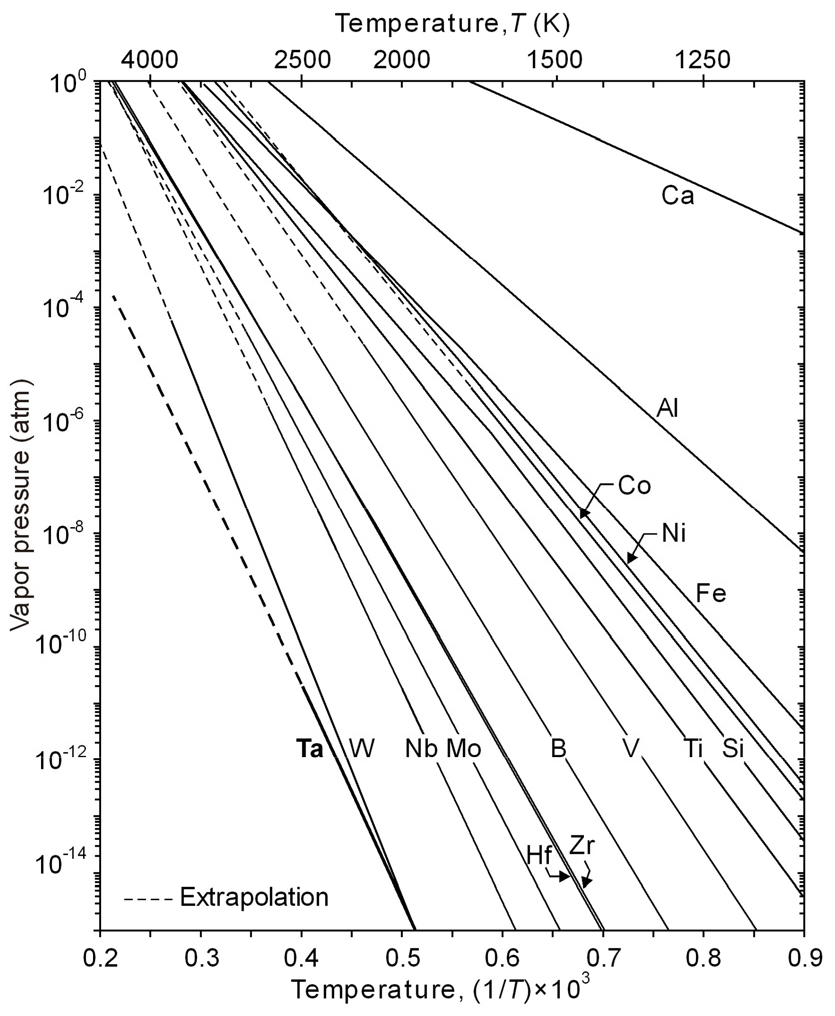
우선 Fig. 9에 몇 가지 순수 금속의 온도에 따른 증기압을 계산하여 나타내었다27). W을 제외하면 Ta의 증기압이 상대적으로 매우 낮다. 따라서 Ta보다 증기압이 높고 휘발성이 강한 Al, Mg, Ca, Fe, Si, Co, Ni 등의 금속 불순물은 고진공에서의 가열이나 용융에 의해 쉽게 제거할 수 있다. 그러나 불순물 Me의 제거 한계는 순수 상태의 증기압 는 물론 조금속 중 열역학적 농도인 활동도 도 매우 중요한 인자이다. 따라서 불순물 Me의 증발속도 는 다음과 같으며28), 와 는 각각 불순물 Me의 활동도계수와 몰분율, 는 순수 상태의 증기압(atm), 는 원자량(g/mol)이다.
따라서 순수 상태의 증기압이 높아도 조금속 중 불순물 농도와 활동도계수가 낮으면 제거 한계는 높아지므로 Ta 중 불순물의 열역학적 검토가 필요하다.
한편 Ta 중 대표적인 침입형 불순물 원소인 H, N, O, C 등은 고진공 중의 고온 열처리에 의한 증류나 탈가스에 의해 제거할 수 있다. 특히 H와 N은 2원자 분자 기체가 되어 비교적 쉽게 제거되는 것으로 알려져 있다11). 그러나 O는 고온의 진공 열처리에 의해 일부 감소되지만, Ta 중 O의 용해도가 높아 상당한 양이 조금속 중에 잔류한다. 또 고온에서도 산소분압이 Ta의 분압(증기압)보다 낮아 O2(g) 발생에 의한 탈산은 불가능에 가깝다. 따라서 Ta의 탈산은 Nb과 마찬가지로 복합 산화물의 생성과 증류에 의한 것으로 알려져 있다. 특히 불순물로 산소만 있을 때는 다음 식과 같이 저급 산화물 기체인 (TaO)를 생성하여 증류되는 희생 탈산(sacrificial deoxidation)이 일어나는 것으로 알려져 있다.
여기서 TaO의 증기압(atm)은 산소의 고용범위 내에서 다음과 같으며, 는 산소 농도(at.%)를 나타낸다29).
이러한 희생 탈산은 Ta과 Nb의 탈산에는 매우 효과적이지만, V과 Hf에서는 희생 탈산에 따른 조금속의 손실량이 많으며 Ti과 Zr 등은 희생 탈산의 적용이 곤란한 것으로 알려져 있다.
Ta 중 산소 농도가 높아 상당량의 Ta 증발로 희생 탈산의 적용이 곤란할 때는 C이나 Si, Al 등으로 탈산할 수 있다. 다만 탈산 생성물 기체인 RO(=CO, SiO, Al2O)와 TaO의 비율인 가 1 보다 훨씬 큰 값이어야 Ta의 손실을 줄일 수 있다. Ta-C-O와 Ta-Si-O계에서의 탈산 반응과 는 각각 다음과 같다29).
따라서 희생 탈산에 우선하여 C과 Si으로 Ta을 탈산할 수 있으며, 특히 Si 탈산은 매우 낮은 Si 농도에서도 C 보나 낮은 온도에서 탈산이 일어나며, 잔류하는 Si은 Fig. 9에서와 같이 증기압이 높아 진공 증류로 제거할 수 있다.
한편 Al에 의한 탈산에서는 와 함께 에 대해서도 고려하여야 하며 다음과 같다29).
따라서 Al 탈산에서는 이 중요하며, Al 농도가 높을수록 탈산에 유리하지만 Al 열환원 반응에서 잔류 Al 농도가 높으면 불순물이 되므로 제거 비용이 높아질 수 있다.
4. 탄탈럼의 리사이클링
Ta은 커패시터용의 금속 Ta 분말 및 선재가 전 세계 수요의 약 1/3을 차지할 정도로 많다. 또 Ta은 내열, 내식 재료, 합금 첨가원소, 스퍼터링 타깃 등에 사용되고 있으며, Ta 산화물이나 탄화물 등의 화합물은 절삭공구, 광학렌즈 등에도 사용되고 있다. 이러한 Ta의 다양한 용도는 결국 EoL 제품에 다양하게 분포되어 서로 다른 루트를 통하여 수집되므로 Ta 리사이클링의 장애로 작용하고 있다. 특히 커패시터나 기타 전자부품 중에 들어 있는 Ta의 농도가 매우 낮다는 점에서 Ta의 리사이클링이 더욱 복잡해지고 있다.
4.1. Ta 커패시터 중 Ta 회수
Ta 커패시터는 폐차, 폐전기·전자기기(WEEE, 전자 폐기물, 특히 휴대용 전자 제품, 컴퓨터, TV, 통신 인프라의 부품), 항공·우주 및 군사용 제품 등의 전자회로/인쇄회로 기판 등에 솔더링되어 있다. 일반적으로는 제품에서 커패시터의 작은 부분에만 Ta이 포함되어 있으므로 수명이 다한 전자부품에서 Ta의 리사이클링률이 낮은 것으로 알려져 있다. Ta 리사이클링의 핵심 과제는 다양한 부품에서 Ta을 함유하는 커패시터의 수집 및 분리와 함께 다양한 재료로 구성되어 있는 커패시터에서 Ta을 추출하는 기술을 개발하는 것이다.
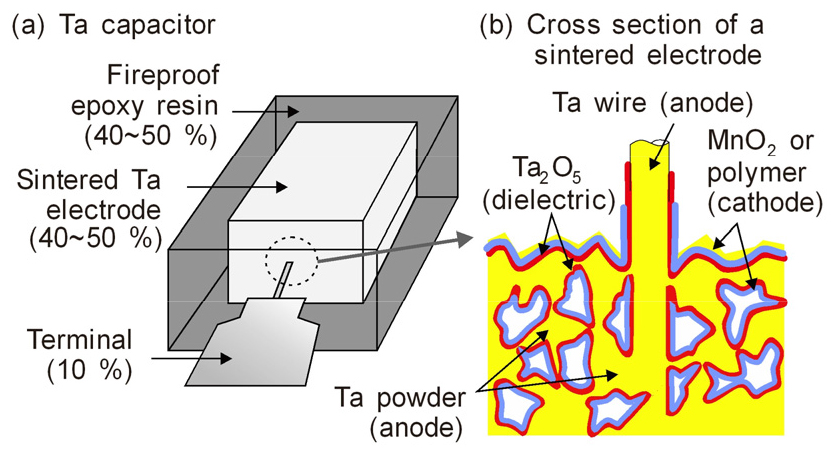
Fig. 10에는 Ta 커패시터의 구조를 나타내었다30). Ta 커패시터는 미세한 Ta 분말을 소결한 커패시터 전극, SiO2 분말을 배합한 고 난연성의 에폭시 수지제 케이스 및 전극에 연결된 단자로 구성되어 있다. Ta은 커패시터 무게의 40~50 % 정도를 차지하며, 전극인 소결체에 매우 높은 농도로 집중되어 있다.
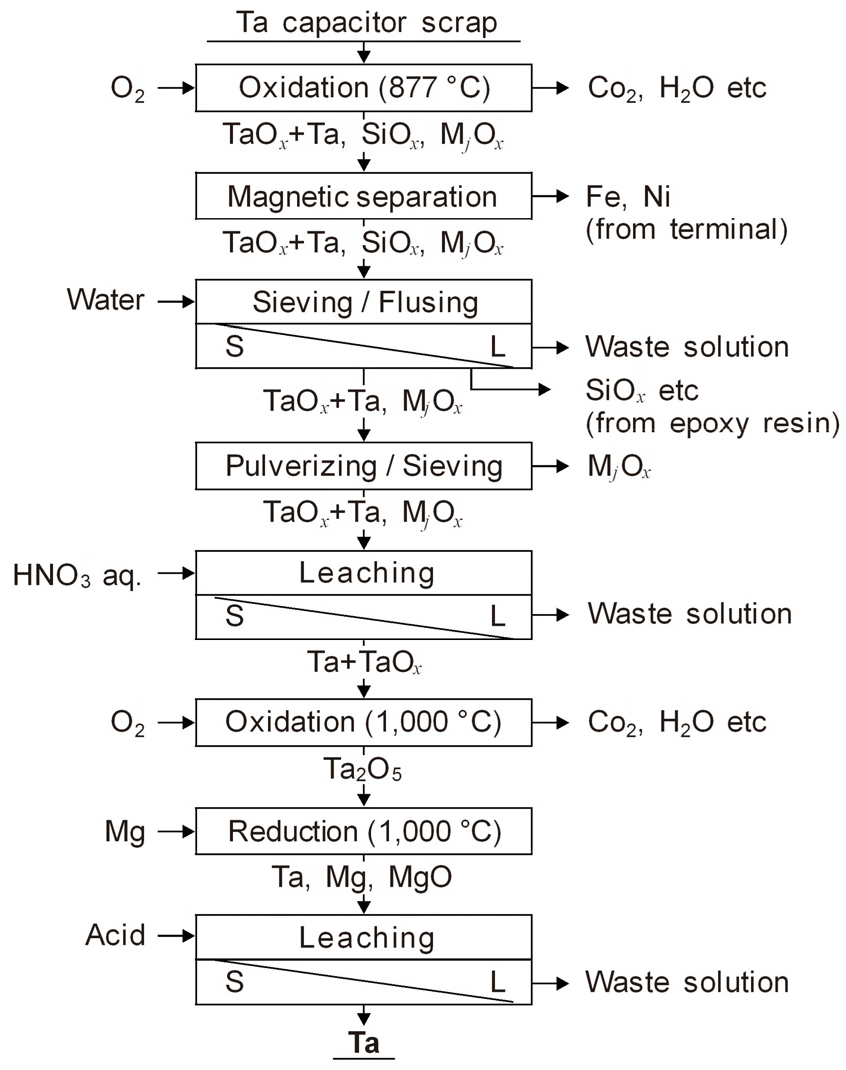
Okabe 등은 커패시터를 고온의 대기 중에서 산화시켜 내부의 Ta을 분리하였으며, Fig. 11에 Ta 커패시터에서 Ta을 회수하는 공정도를 나타내었다30). 커패시터를 약 877 ℃의 공기 중에서 산화시키면 에폭시 수지는 분말로 변하고 Ta 분말 소결체는 원형을 유지한 채 산화되어 체질에 의해 양자를 쉽게 분리할 수 있었다. 이후 자력 선별로 Fe, Ni 등의 자성체를 분리하고, Ta 외의 금속(Cu 등)은 질산으로 침출하여 제거하였다. 그리고 TaOx 및 Ta을 재산화시키거나 곧바로 Mg으로 환원하여 금속 Ta을 분말로 회수하였다. Ta 분말의 크기는 약 0.3 μm이고 순도는 99 % 정도였으며, 주요 불순물은 에폭시 수지 중의 Si이 혼입된 것으로 전자 재료용의 고순도 Ta을 얻기 위해서는 별도의 화학적 처리가 필요하다. 따라서 Okabe 등은 Ta을 고순도로 회수하기 위해 일메나이트(FeTiO3)의 선택염화 생성물인 FeCl2로 Ta 산화물 및 Ta을 염화시켜 Mg으로 환원하기도 하였다.
한편 Chen 등은 Okabe 등과 유사한 방법으로 Ta 커패시터의 에폭시 수지를 열분해하여 제거하고, Ta 이외의 금속 불순물을 자력 선별과 염산에 의한 선택 침출로 제거하였다. 그리고 회수한 Ta 잔사는 다음 식과 같이 염화시켜 TaCl5로 회수하였다31).
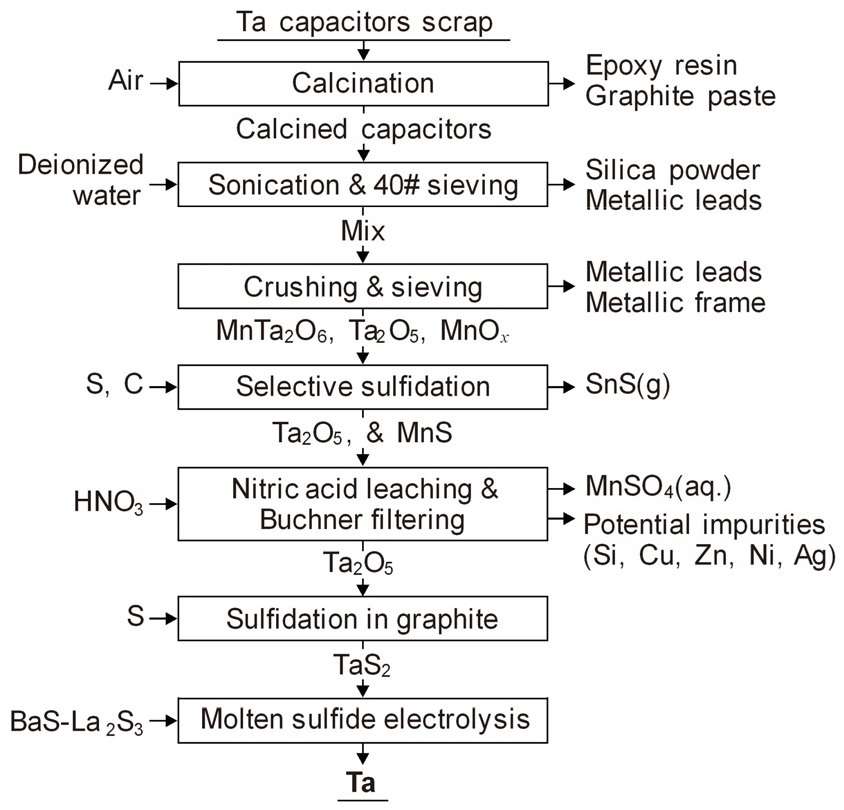
Katano 등은 질소 분위기 중 수증기와 NaOH로 Ta 커패시터의 에폭시 수지를 분해시켜 Ta 소결체를 회수하였다32). Boury 등은 Fig. 12와 같이 Mn, Fe 등과 Ta, Nb 등의 S 친화력 차이를 이용한 선택적 황화반응과 질산침출로 불순물을 제거하고, 회수한 Ta2O5를 다시 황화시킨 후 용융염 전해로 Ta을 회수하였다33). Ta 커패시터의 전처리는 Okabe 등과 동일하게 산소 분위기 중에서 가열하였으나, SiO2 분말 등을 제거하기 위해 수중에서 초음파를 인가하고 체질하였다.
4.2. 금속 Ta 및 합금 스크랩의 리사이클링
금속 Ta은 전자재료용 반도체 타깃으로 사용된 후 스크랩으로 배출되고 있다. 이러한 금속 Ta을 전자빔으로 용융하여 4N5급으로 고순도화한 예도 있다34). 그러나 전자빔 용융은 고가의 설비와 운용단가 문제 등의 문제가 있다. 따라서 Ta 선삭 스크랩을 수소화-탈수소화(hydride-dehydride, HDH)법을 이용하여 Ta 분말로 재생하기도 하였다35).
Ta을 함유한 슈퍼알로이 등의 합금은 Ta을 별도로 회수하지 않고 재용융하여 사용하는 것이 일반적이다. 그러나 Ta이 8 wt%까지 함유된 합금에서는 Ta을 회수하는 것이 경제적일 수 있다. 이러한 관점에서 Ta 함유 합금을 전기화학적으로 분해하여 Ta을 회수한 예도 있다36). 특히 슈퍼알로이의 직류 전해는 합금의 표면에 부동태 피막이 생성되어 분해가 쉽지 않아 음극과 양극 모두에 슈퍼 알로이를 사용하고 60~80 ℃의 15~25 wt%HCl 용액 중에서 낮은 주파수(0.1-1 Hz)로 PR(periodic reverse) 전해로 부동태 피막의 생성을 방지하여 용해시켰다. 합금 중의 Co, Ni, Cr 등은 용해되고 Ta, W, Hf 등은 고체의 산화물로 회수하였다.
한편 Olbrich 등은 슈퍼알로이를 60~95 %NaOH, 5~40 wt%Na2SO4 조성의 용융염으로 용해하여 유가금속을 회수하였다37). 산화제로 NaNO3나 K2S2O8을 첨가하고 900~1,050 ℃의 용융염에 공기나 산소를 주입하면서 슈퍼알로이를 용해하였다. 용융염을 냉각하여 파쇄하고 수 침출하여 Mo, W, Re 등을 수용액으로 제거하고, 잔사를 자력 선별하여 Ni, Co 등을 제거하였다. 남은 비자성체인 Al, Cr, Ti, Zr, Hf, Nb, Ta 등은 산화물로 회수하였으며, Ta은 약 15 % 정도이며 Ta 제련의 원료로 사용하였다.
WC 중 Ta을 회수하기도 하지만 대부분 W과 Co의 회수가 주목적이다. Kamimoto 등은 초경합금을 용융염 전해하여 W 등은 용해시키고 Ta은 산화물로 회수하였다38).
5. 종 합
본 논문에서는 Ta의 생산량, 용도 및 제련과 리사이클링 기술에 관하여 고찰하였다. Ta은 지각 중 원소 존재도가 2.0 ppm(52위)으로 연간 생산량도 약 2,000톤 수준에 불과한 희소금속이며 분쟁광물이지만, 현대 산업에 필수적인 핵심 금속이다. Ta 제련은 탄탈라이트와 컬럼바이트 등의 광석을 분해하여 Ta2O5와 Nb2O5를 분리해야 한다. 그리고 금속 Ta은 광석에서 분리한 Ta 불화물이나 염화물은 금속열환원법과 용융염 전해법으로 환원하며, 산화물은 Ca, Al, C 등을 환원제로 사용하는 열환원법 등으로도 만들 수 있다. 이러한 환원법으로 만든 조금속 Ta에는 금속 불순물과 함께 침입형 원소 등이 잔류하므로 고온의 진공 열처리, 전자빔 용융, 용융염 전해 등으로 정제한다. Ta 폐타깃이나 선삭 스크랩 등은 분류, 세척 공정을 거친 후 전자빔 용융 등으로 회수한다. 그러나 초합금 등에 합금원소로 첨가된 Ta의 리사이클링에 관해서는 잘 알려져 있지 않으나 별도로 회수하지 않으며, 원래의 합금 등으로 재용해하는 것이 일반적이다. 따라서 리사이클링율을 높이기 위해서는 세밀한 분류가 필요하다. 또 Ta은 커패시터에 사용된 것이 많아 이의 리사이클링에 많은 관심이 주어져 있으나, EoL 제품에 다양하게 분포되어 있고 Ta의 농도가 매우 낮아 리사이클링의 장애가 되고 있다. 이러한 Ta 커패시터는 열분해하여 Ta이나 산화물로 회수하여 Mg 환원이나 용융염 전해 등으로 회수하고 있다.