1. 서 론
2. LIB 전해액의 조성 및 상태
2.1. LIB 전해액 성분
2.2. 폐 LIB 전해액 상태
3. 폐 LIB의 분해 및 전처리(Disassembly and Pretreatment of Spent LIB)
3.1. 분류(Classification)
3.2. 방전(Discharge)
3.3. 해체(Dismantling)
3.4. 파쇄(Crushing)
3.5. 분리(Separation)
4. 폐 LIB의 전해질 재활용 방법
4.1. 전해액 수집( Electrolyte collection)
4.2. 전해액 정제(Electrolyte purification)
5. 결 론
1. 서 론
전 세계적으로 전기차, 휴대용 전자기기, 에너지 저장 시스템 등 다양한 분야에서 리튬이온배터리(LIB)의 사용이 급격히 증가함에 따라, 수명 종료 후 발생하는 폐 리튬이온전지(LIB) 문제가 심각한 사회·환경적 이슈로 대두되고 있다. LIB는 높은 에너지 밀도와 긴 수명을 갖춘 차세대 에너지 저장 장치로 현대 산업과 생활의 필수 요소가 되었으나, 폐 LIB에 포함된 유가금속 자원과 유해 물질의 적절한 처리 및 회수는 반드시 해결해야 할 과제이다.
특히 LIB의 전해질은 전체 배터리 무게의 약 10~15%를 차지하며, 유기 탄산염 혼합물과 리튬염으로 구성된 복합 화학물질로 높은 독성과 인화성을 지니고 있다. 따라서 폐 LIB 전해질을 무분별하게 처리할 경우 환경오염 및 인체 위해를 초래할 수 있으며, 신뢰성 있는 재활용 체계 구축에 큰 장애가 된다1,2). 기존 LIB 재활용 연구는 주로 양극재와 음극재 등 금속 자원의 회수에 집중되어 전해질 회수는 상대적으로 소외되어 왔다. 그러나 최근 연구에서는 전해질 회수의 중요성이 부각되고 있으며, 이는 자원 선순환과 환경 보전 측면에서 필수적이다. 전해질 내에 포함된 리튬과 유기 용매는 재사용이 가능하며, 특히 리튬은 전기차 및 에너지 저장 산업의 핵심 자원으로 공급 부족과 가격 변동성이 심각한 문제로 지적되고 있다. 효율적인 전해질 회수 기술이 확립될 경우 신규 원자재 수요 감소, 폐기물 처리 비용 절감, 지속 가능한 배터리 생태계 구축에 기여할 수 있다2,3). 그러나 전해질 회수 기술은 화학적 복잡성, 물리적 특성, 열적·화학적 안정성 차이로 인해 많은 기술적 도전 과제를 안고 있다. 대표적인 회수 방법으로는 저온 열처리, 진공 증류, 용매 추출, 초임계 이산화탄소 추출 등이 있으며, 각 방법은 회수율, 순도, 에너지 소비, 환경 영향 측면에서 고유한 장·단점을 가진다.
환경적 측면에서 전해질 회수의 필요성은 더욱 크다. 폐 LIB 내 유기 전해질은 자연적으로 분해되지 않고 잔류할 경우 토양과 수질을 오염시키며, 유해 가스 배출의 원인이 될 수 있다. 또한 전해질은 인화성과 폭발성을 내포하고 있어, 안전한 처리 기술 확보는 산업적 신뢰성과 사회적 안전을 보장하기 위한 필수 요소이다. 따라서 전해질 회수 기술은 단순한 자원 회수 차원을 넘어 배터리 산업의 환경 규제 대응과 순환 경제 실현을 위한 기반 기술로 기능할 수 있다4,5). 경제적 관점에서도 전해질 회수는 자원 재활용 효율성을 높이고 배터리 재생산 비용을 절감하는 데 기여한다. 회수된 유기 용매는 정제 과정을 거쳐 신규 전해질 제조에 재투입될 수 있어 원가 절감 효과가 크며, 리튬염 회수를 통한 공급 안정성 확보는 전지 산업 경쟁력 강화에 직결된다. 최근 전해질 회수 관련 산업은 일부 선진 기술을 보유한 기업을 중심으로 상용화 초기 단계에 진입하였으며, 향후 이러한 기술이 확산됨에 따라 글로벌 배터리 재활용 시장은 빠르게 성장할 것으로 전망된다2,6). 종합하면, 폐 LIB에서의 전해질 회수 기술 개발은 자원 고갈 문제 해결, 환경 보호, 산업 안전, 경제적 효율성 측면에서 필수 불가결한 과제이다. 이에 본 연구에서는 폐전해질 회수 기술의 최신 동향을 분석하고, 이를 기반으로 향후 친환경적이고 경제적인 전해질 회수 공정 개발 방향을 제시하고자 한다.
2. LIB 전해액의 조성 및 상태
2.1. LIB 전해액 성분
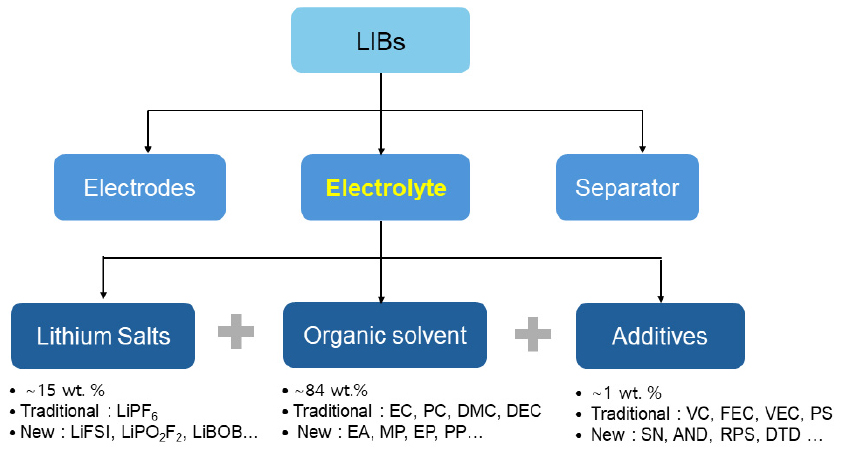
전해액은 LIB의 핵심 구성 요소로, Fig. 1에 나타낸 바와 같이 전해질염(lithium salts), 유기용매(organic solvents), 첨가제(additives)로 이루어져 있다. 전해액의 기본적인 역할은 양극과 음극 사이에서 리튬이온을 안정적으로 전도하고 전류 회로를 연결하는 것이다. 충·방전 과정에서 리튬염은 리튬이온을 제공하며, 유기용매는 이온의 전도 매개체로 작용한다.
현재 상용 LIB 전해액에서 가장 널리 사용되는 리튬염은 헥사플루오로인산리튬(LiPF6)으로, 전해액의 약 15 wt%를 차지한다(Table 1). LiPF6는 유기용매에 용해될 경우 대량의 리튬이온을 해리시켜 전해질에 높은 이온 전도성을 부여한다7,8). 유기용매는 전해액의 약 80-85 wt%를 차지하며, 고유전율을 갖는 고리형 카보네이트(ethylene carbonate, EC; propylene carbonate, PC)를 기본 용매로 사용한다. 또한 점도를 낮추기 위해 사슬형 카보네이트(dimethyl carbonate, DMC; ethyl methyl carbonate, EMC; diethyl carbonate, DEC 등)를 혼합하며, 일반적으로 3-5종의 용매를 조합하여 사용한다(Table 2).
Table 1.
Physical properties of different Lithium salts
Table 2.
Physical properties of different organic solvent
전해액의 전기화학적 성능을 향상시키기 위해 소량(약 1 wt%)의 첨가제가 사용되며, 대표적인 첨가제로는 비닐렌 카보네이트(VC)와 플루오로에틸렌 카보네이트(FEC) 등이 있다(Table 3)9).
Table 3.
Types of additives
2.2. 폐 LIB 전해액 상태
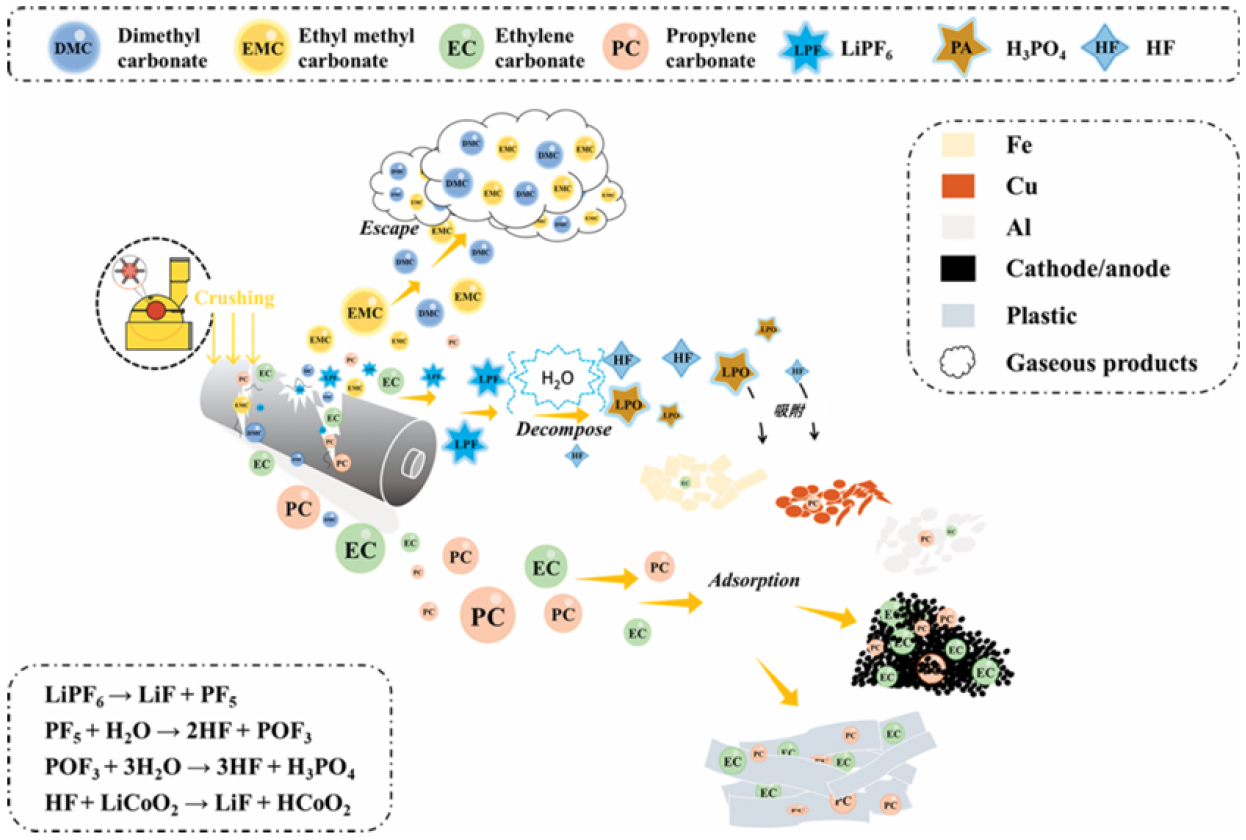
LIB의 전해액은 사용 과정에서 일부 성분이 전환될 수 있으나, 기본 조성은 크게 변하지 않는다. Henschel 등은10) 전 세계 5개 제조업체의 전기차용 LIB에 대해 사용 전·후 전해액을 분석하였다. 19개 배터리 시료를 분석한 결과, 전해액 내 DMC와 EMC는 사용 중 에스테르 교환 반응을 일으켜 소량의 DEC를 생성하는 것으로 나타났다. 또한 LiPF6는 시스템 내 수분과 반응하여 분해되면서 삼불화인(POF3)을 형성하고, 이는 다시 디플루오로인산(DFP)으로 전환된다. 이 과정에서 발생한 소량의 HF는 음극 표면에서 LiF 형태로 전환된다. LiPF6는 용매 분자와도 반응하여 디메틸 플루오로포스페이트(DMFP) 및 디에틸 플루오로포스페이트(DEFP)와 같은 부산물을 생성할 수 있다. 다른 연구에서는 리튬염이 용매의 미량 수분 및 용매 분자와 반응하여 유기(불소)인산염[O(F)Ps]을 형성하는 것으로 보고되었으며, 이러한 물질의 구조는 사린과 같은 화학무기와 유사하여 독성을 가질 것으로 추정된다11). 또한 LIB를 부적절하게 사용하면 전해액이 부분적으로 분해·소실될 수 있으며, 일부 폐 LIB의 전해액 함량은 초기 대비 약 50~70% 수준으로 감소하는 것으로 보고되었다12). 한편, Xiao 등은13) 폐 LIB 재활용 과정에서 유기 용매와 불화물을 포함한 독성 전해질의 이동 및 변형을 연구하였다. 폐 LIB를 기계적으로 처리한 후 각 성분의 이동 경로를 분석하고, 이를 기반으로 재활용 공정 방향을 제시하였다. Fig. 2에 따르면, 기계적 파쇄 시 DMC와 EMC는 비등점이 낮아 증발될 가능성이 크며, EC와 PC는 높은 유전상수로 인해 물에 잘 용해되어 리튬염이나 전극 물질에 흡착된 상태로 수상층에 존재하기 쉽다. 또한 LiPF6는 물과 반응하여 분해되며, 이 과정에서 리튬염, HF 및 H3PO4로 전환되는 것으로 보고되었다. 이러한 분해 산물은 환경오염뿐만 아니라 장비 부식의 원인이 될 수 있다. 이에 따라 연구진은 기계적 파쇄 및 분리 공정에서 발생하는 온도 상승을 억제하기 위해 냉각 시스템 및 습식 파쇄(wet crushing)를 도입하고, 알칼리성 용액을 분사하여 공정 중 생성되는 HF를 중화하는 방안을 제안하였다.
3. 폐 LIB의 분해 및 전처리(Disassembly and Pretreatment of Spent LIB)
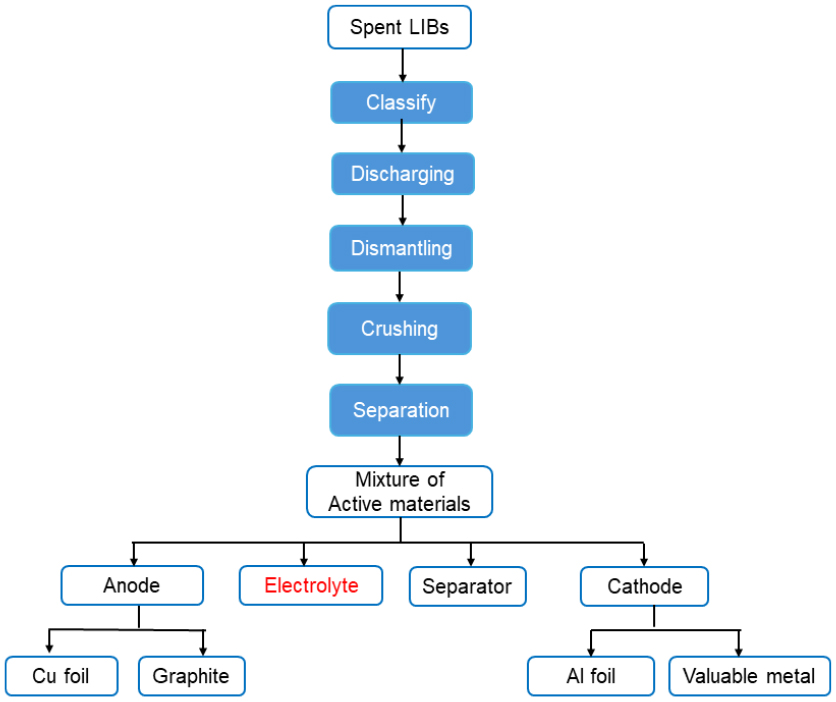
리튬이온배터리(Lithium-ion batteries, LIBs)는 일반적으로 약 5~8년의 사용 주기를 가지며, 이후 에너지 효율 저하로 인해 폐기 또는 재활용 단계에 진입한다. 폐 LIB에는 니켈(Ni), 코발트(Co), 망간(Mn) 등 고부가가치 중금속이 다량 함유되어 있으나, 부적절한 처리 시 토양·수질·대기 환경에 심각한 오염을 유발할 수 있다14). 특히 코발트(Co)는 발암물질로 알려져 있으며, 호흡기 및 소화기 질환 등 인체 건강에 중대한 영향을 미친다15). 폐 LIB의 전해질에는 중금속 외에도 리튬염(LiPF6), 유기용매(ethylene carbonate, dimethyl carbonate 등), 첨가제가 포함되어 있다. 주요 전해질 성분인 LiPF6는 수분과 반응하여 독성 및 부식성이 강한 POF3와 HF를 생성하며, 연소 시 P2O5를 방출하여 대기오염을 일으킬 수 있다12). 또한 유기용매는 휘발성과 난분해성 특성으로 인해 장기간 환경에 잔존하며, 토양 및 수질 오염의 주요 원인이 된다. 이러한 특성으로 인해 폐 LIB의 재활용은 단순 폐기보다 환경적·경제적 가치가 크다. 재활용 과정에는 금속 회수뿐만 아니라 전해질의 안전한 안정화·회수 및 재사용이 포함되며, 특히 전처리 공정은 전체 재활용 효율과 안전성을 결정짓는 핵심 단계로서 전해질 누출 방지, 회수, 그리고 화재·폭발 위험 저감이 중요하다. 폐 LIB 전처리는 일반적으로 분류(classification), 방전(discharge), 해체(dismantling), 파쇄(crushing), 분리(separation) 등의 순서로 수행된다(Fig. 3)16).
3.1. 분류(Classification)
배터리의 화학 조성(NCM, LFP 등)과 상태를 분석하여 적합한 처리 방법을 결정한다. 전기화학적 성능이 양호한 셀이나 모듈은 재활용 대신 ‘세컨드 라이프(second-life)’ 용도로 재사용할 수 있으며, 이는 비용 절감과 환경 부담 저감 효과를 동시에 가져온다.
3.2. 방전(Discharge)
폐 LIB는 폐기 시 일정한 잔존 전하를 보유하고 있어, 분해·파쇄 과정에서 양극과 음극이 접촉할 경우 단락이 발생하여 급격한 온도 상승, 전해액 발화, 유해 가스 방출 및 폭발로 이어질 수 있다17). 따라서 분해 전에 완전 방전을 수행하여 안전성을 확보하는 것이 필수적이다. 방전 방식은 물리적 방전과 화학적 방전으로 구분된다. 물리적 방전18)은 흑연, 금속 분말 등의 전도성 입자 또는 저항체를 이용해 양극과 음극을 직접 연결함으로써 전하를 소모하는 방법이다. 방전 속도가 빠르고 소형 배터리에 적합하다는 장점이 있으나, 발열이 심해 냉각 장치가 필요하고 전해액 누출 등 잠재적 위험이 존재한다. 또한 대용량 배터리의 경우 일부 에너지 회수가 가능하다. 화학적 방전19)은 염, 산, 알칼리 등의 전도성 용액에 배터리를 침적시켜 양극과 음극을 단락시키는 방법으로, 용액이 에너지를 흡수하기 때문에 상대적으로 안전성이 높다. 그러나 방전 과정에서 다양한 화학 반응이 발생하며, 배터리 파손 시 용액 오염 가능성이 있다. 대표적으로 NaCl 용액이 많이 사용되며, 45시간 침적 시 완전 방전이 가능하고, 10 wt% NaCl 용액을 사용할 경우 약 18시간 이내에 방전이 완료된다20). 한편, 유기용매나 산성·알칼리성 용액을 적용할 경우 배터리 손상을 최소화하여 방전 효율 저하를 방지하는 것이 중요하다.
종합적으로, 물리적 방전은 단시간 내 전하 소모가 가능하다는 장점이 있으나 열 및 폭발 위험이 크며, 화학적 방전은 처리 시간이 다소 길지만 대량 처리와 안전성 측면에서 유리하여 현재 산업 현장에서 널리 활용되고 있다.
3.3. 해체(Dismantling)
폐 LIB 처리 과정에서 해체(dismantling)는 핵심 단계이며, 현재 수동 해체와 로봇 해체의 두 가지 방식이 적용되고 있다. 수동 해체는 숙련된 작업자가 다양한 도구와 장비를 사용하여 배터리를 단계적으로 분해하는 방법으로, 높은 유연성과 정밀한 제어가 가능하여 배터리 구성 요소를 선택적으로 분리할 수 있다. 그러나 다량의 인력이 필요하고, 작업자의 안전 위험이 크다는 한계가 있다. 반면, 로봇 해체는 자동화 장비와 로봇 기술을 활용하여 기계식 팔 등 프로그램 제어 도구로 배터리를 분해·분리하는 방식으로, 고효율·고속 처리와 안전성 향상 측면에서 장점이 있다. 다만, LIB의 다양한 설계와 복잡한 구조를 효과적으로 처리하기에는 기술적 제약이 존재한다21).
3.4. 파쇄(Crushing)
폐 LIB 파쇄 공정은 유가금속 회수를 위한 전처리 단계로, 배터리를 기계적으로 분해하여 후속 분리 및 제련 공정의 효율을 향상시키는 역할을 한다22). 수작업 해체에 비해 처리 효율과 처리량이 우수하며, 일반적으로 다단계 파쇄를 적용하여 균일한 입도와 성분 분포를 확보한다23). 산업 현장에서는 주로 건식 파쇄(dry crushing)가 활용되며, 파쇄 전 배터리를 분류하여 입자의 일관성을 유지하고 선택적 파쇄를 통해 불필요한 분쇄를 억제함으로써 전극 소재의 순도와 분산성을 향상시킨다24). 건식 파쇄 공정은 분진 발생 억제를 위한 집진 설비가 필요하며, 고가의 장비가 요구된다. 또한 단락·산화·폭발 위험을 방지하기 위해 아르곤, 질소, 이산화탄소 등의 불활성 분위기와 저온 조건을 적용하여 플라스틱 케이스의 취성화를 유도하고 안전성을 확보한다25,26). 반면 습식 파쇄(wet crushing)는 물 또는 용액 내에서 파쇄를 수행하여 전해질과의 직접적인 반응을 차단하고, 폭발 및 화재 위험을 저감한다. 이 방식은 분진과 장비 막힘을 방지하며, 열을 흡수하여 난연 효과를 제공한다. 또한 고속·고압 수류 절단을 통해 소음과 에너지 소비를 줄이고 처리 속도를 향상시킬 수 있다27). 그러나 습식 파쇄는 결합제 및 전해질의 용출로 인해 폐수 처리 부담이 발생하고, 운영비가 증가한다는 단점이 있다. 파쇄 후 생성된 혼합물은 건식 제련을 통해 금속 원소 및 산화물을 직접 회수하거나, 습식 제련을 통해 양극재 내 개별 금속을 고순도로 분리·회수한다. 따라서 파쇄 공정은 안전성 확보와 환경영향 저감을 위해 설비 및 운전 조건의 최적화가 필수적이다.
3.5. 분리(Separation)
폐 LIB는 비활성화 과정을 거친 후, 농축된 양극재 분말을 회수하기 위해 성분 분리가 필요하다. 배터리는 플라스틱·금속 케이싱, 폴리머, 양극 집전체 및 음극 집전체 등으로 수동 분해가 가능하다. 현재 산업 현장에서는 파쇄 공정 후 자기 분리를 통해 금속 부품을 효과적으로 분리하여 처리 용량을 향상시키고 있다. 이후 미세 파쇄 및 선별 과정, 열처리 공정을 거쳐 양극 활물질이 농축된 블랙 파우더(black mass) 형태로 회수되며, 후속 분리 공정을 통해 고순도의 배터리 소재를 회수할 수 있다28).
4. 폐 LIB의 전해질 재활용 방법
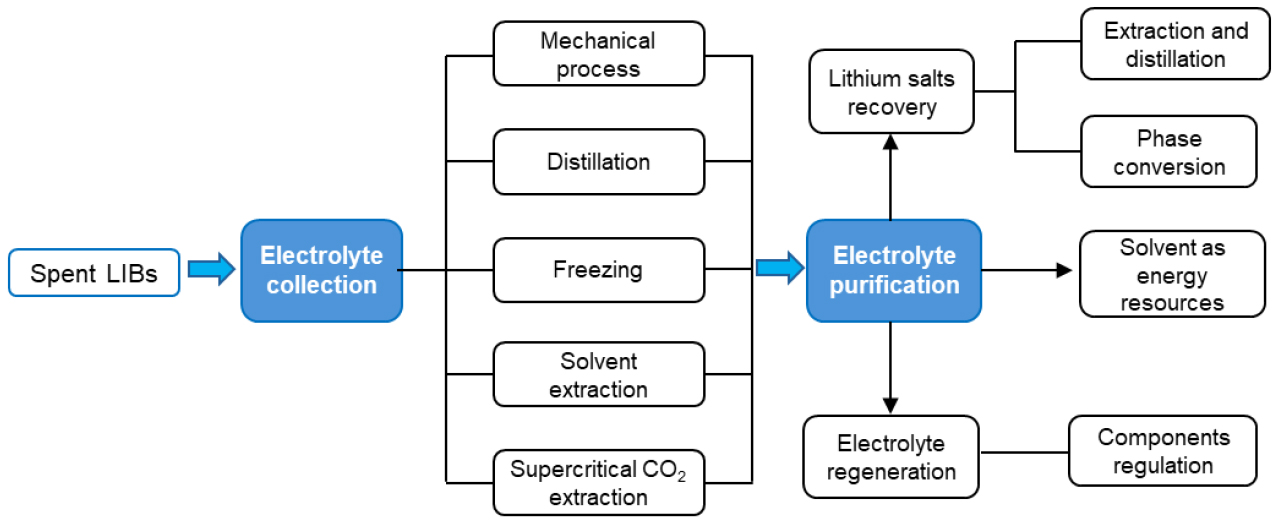
전해액 내 리튬염과 탄산계 유기용매는 회수 및 재활용이 가능한 중요한 자원이다. 회수된 유기용매는 대체 연료원으로 활용될 수 있으며, 재활용된 리튬염은 새로운 배터리 제조에 재사용할 수 있다. 급성장하는 LIB 시장은 이러한 자원의 수요를 증가시키고 있으며, 따라서 효율적인 전해액 재활용은 경제적·환경적 측면에서 높은 가치를 지닌다. 그러나 재활용 기술에 대한 연구가 지속되어 왔음에도 불구하고, 경제성이 확보된 공정 개발은 여전히 중요한 과제로 남아 있다. 폐 LIB의 전해액 재활용 공정은 Fig. 4에 나타낸 바와 같이 1) 해체·파쇄(dismantling and shredding), 2) 전해액 수집(electrolyte collection), 3) 전해액 정제 및 염 회수(electrolyte purification & salt isolation)의 세 단계로 구분할 수 있다2,29). 해체 및 파쇄 후 전해액을 수집하기 위해 기계적 공정, 증류, 동결, 용매 추출, 초임계 유체 추출 등의 기술이 적용되고 있다29). 전해액 정제 분야는 기술적 난제로 인해 연구가 미진하며, 산업 현장에서는 효율성과 비용 절감을 위해 수집 단계와 정제를 병행하기도 한다. 전해액 정제는 전해액 재생(electrolyte regeneration)과 리튬염 회수(lithium salts recovery)로 나눌 수 있다. 전해액 재생은 수집된 전해액을 거의 정제하지 않고 신배터리 제조에 직접 재사용하는 방식으로, 양극·음극 재활용과 달리 전해액은 충·방전 과정에서 전해질 분해와 불순물 축적이 발생하므로 동일한 성능을 확보하기 어렵다. 또한 상업용 전해액 수준으로 재생하기 위해서는 높은 비용이 요구된다30). 리튬염 회수는 불안정한 LiPF6를 Li2CO3와 같은 안정한 화합물로 전환하는 방법과, LiPF6 자체를 직접 회수하는 방법으로 구분된다. 전환 방식은 추가적인 화학 약품과 에너지가 필요하며31), 직접 회수 방식은 용매 추출 및 증류를 이용하나, 용매 중합, 고체전해질 계면(SEI) 용해, 전이금속 불순물 용출 등으로 인해 높은 순도와 회수율 확보가 어렵다. 현재까지 전해액 재활용을 위한 몇 가지 혁신적 방법이 보고되었으나, 대부분 상업화와는 거리가 멀다. 따라서 LiPF6와 유기용매를 고순도로 직접 회수할 수 있는 기술 개발이 전해액 재활용 분야에서 무엇보다 시급한 과제로 판단된다.
4.1. 전해액 수집( Electrolyte collection)
전해액 수집은 전해액 재활용 공정의 핵심 단계로, 끓는점, 용해도 등 전해액 성분의 물리적 특성을 활용하여 물리적 분리 과정을 통해 단계적으로 회수하는 방법이다. 대표적인 수집 방법으로는 기계적 공정, 증류 및 동결, 용매 추출, 초임계 CO2 추출 등이 있으며, 각 방법의 장단점은 Table 4에 정리하였다. 주요 기술의 세부 내용은 다음과 같다.
Table 4.
Comparison of Different Collecting Methods of Electrolyte2)
4.1.1. 기계적 공정(Mechanical process)
원심분리(centrifugation), 공기 분사(airflow purging), 진공 여과(vacuum filtration)와 같은 기계적 방법은 외력을 이용하여 전해액을 셀로부터 분리하는 방식이다. 폐 LIB는 분해 과정을 거친 뒤 전해액을 방출하게 되며, 이 과정은 일반적으로 전해액이 공기 또는 수분과 반응하는 것을 방지하기 위해 불활성 가스 또는 진공 분위기에서 수행된다. 예를 들어, Y. Wang 등은32) 전해액 회수를 위해 초고속 원심분리를 적용하였다. 폐 LIB를 먼저 N2 분위기에서 분해하여 셀 내 전해액을 배출한 후, 20,000 rpm 이상의 원심분리를 통해 전해액을 효과적으로 분리·회수하였다. 또한 J. Li 등은33) 파쇄 공정 이후 전해액 회수가 가능함을 보고하였으며, 수분 함량을 조절하고 원심분리와 반복적인 용매 역류 세척을 결합하여 전해액 회수 효율을 개선하였다. 공기 분사와 진공 여과는 각각 양압과 음압을 이용하여 전해액을 회수하는 방법이다. Lai Y. 등은34) 40~100 kPa의 음압에서 배터리를 분해·파쇄한 후, 전해질을 고온 가스로 휘발시켰다. 이후 휘발된 가스를 응축·여과 및 탈불소화하여 순수한 유기용매를 회수할 수 있었다. 본 기술은 저비용으로 전해질을 재활용할 수 있으며, 동시에 2차오염을 방지할 수 있다는 장점이 있다.
기계적 공정을 통한 전해액 수집 방법은 다른 물질을 첨가할 필요가 없고 전해액 조성을 변화시키지 않는다는 장점이 있다. 그러나 전해질은 전극 구조와 분리막에 침투하여 전극 표면에 고체 전해질 계면(SEI)을 형성하기 때문에, 기계적 방법만으로는 전해액을 완전히 분리하기 어렵다. 따라서 전해액을 완전하게 회수하기 위해서는 일반적으로 용매세척이나 기타 공정을 병행해야 한다.
최근에는 환경오염을 방지하고 전해액 회수 효율을 높이기 위한 방안으로 습식 파쇄(wet crushing) 공정이 주목받고 있다. 습식 파쇄는 폐 LIB 전처리 과정에서 일반적으로 사용되는 불활성 가스 분위기 하의 건식 파쇄(dry crushing)보다 안전성이 높으며, 전해액 회수에 효과적인 것으로 평가된다. Li B. 등은35) 수성 매체(물)를 이용한 파쇄 시 유해 전해액을 효과적으로 냉각시켜 폭발 위험을 억제하고 화재 예방에 기여한다고 보고하였다. 또한 습식 파쇄 과정에서 LiPF6의 약 90%가 4분 이내에 거의 분해되지 않고 용해되어 안전하게 처리될 수 있었다. 이 과정에서 불소(F) 및 인(P) 성분이 HF, PF5 등의 형태로 기체상으로 방출되지 않아 환경오염 저감에도 효과적이었다. 한편, 전해액 내 유기물은 빠르게 용해되지만 일부는 열 기화(thermal gasification)를 통해 재방출될 수 있으며, 이때 용액의 온도와 용존 전해질 농도가 유기물 방출에 중요한 영향을 미치는 요인으로 확인되었다. 이에 따라 연구진은 유해 전해액을 제어하기 위한 효과적인 방법으로 습식 파쇄 공정을 제안하였다. Yu H. 등은36) 폐 LIB의 전해액 회수를 위해 수중 파쇄 공정을 적용하였다. 이 방법은 먼저 배터리를 안전하게 방전한 후, 염수 또는 유기용매가 담긴 액체 환경에서 2단계로 파쇄하는 방식이다. 수중 파쇄는 파쇄 과정에서 발생할 수 있는 산소 축적과 스파크를 억제하여 화재 위험을 최소화하고, 배터리 내부 전해액이 액체 상으로 용출되도록 유도한다. 회수된 전해액은 진공 상태에서 70 ℃ 이하로 승온하여 증발시킨 뒤, 극저온 냉각 응축기를 통해 포집함으로써 고순도 전해액을 확보하고, 동시에 HF 및 LiF와 같은 유해 물질을 안전하게 분리·회수할 수 있다. 이후 불순물 정제 과정을 거쳐 재사용 가능한 전해액으로 재생이 가능하며, 이를 통해 환경오염 저감과 재활용 효율 및 안전성을 동시에 개선할 수 있는 방법으로 평가된다.
4.1.2. 동결 방식(freezing method)
폐 LIB 처리 과정에서 동결 방식(초저온 동결파쇄 공법)은 최근 주목받고 있는 안전하고 친환경적인 전처리 방법이다. 이 방식의 핵심은 폐 LIB 내부 전해액을 동결시켜 화재와 폭발 위험을 원천적으로 제거한 뒤, 해체·파쇄 등의 후속 공정을 수행하는 것이다. Fang Z. 등은37) 폐 LIB의 안전한 전처리를 위해 드라이 아이스와 액체질소를 활용한 초저온 동결(cryogenic freezing) 방식의 적용 가능성을 평가하였다. 전해질이 -80 ℃ 이하에서 고체 상태로 존재할 경우, 배터리에 물리적 충격을 가해도 열폭주(thermal runaway)가 발생하지 않았다. 그러나 상온으로 해동되면 위험성이 다시 증가하므로, 해체 및 파쇄 등 후속 공정은 동결 상태에서 신속히 수행해야 함을 제시하였다. 이를 통해 초저온 동결 처리가 폐 LIB의 열적 위험성을 원천적으로 차단할 수 있음을 실험적으로 입증하였으며, 안전하고 친환경적인 재활용 전처리 기술의 근거를 마련하였다. Sunderlin N. 등은38) 폐 LIB를 액체 질소(-197 ℃)로 동결하여 내부 전해질 고체화 시의 안전성, 해체 공정 중 화재·폭발 위험 경감, 내부 구조 분석 등의 결과를 보고하였다. Y. Zhao 등은39) 배터리 코어를 액체질소에 10-20분간 동결시켜 전해질을 입상 고체로 응축한 후, 가열 증류 장치로 95-120 ℃에서 증류하여 전해질을 회수하였다. 또한 일본 미쓰비시에서는 저온 조건에서 LIB를 분쇄하여 고체 전해질을 얻는 공정을 개발하였다40). Hongxiang CUI 등은41) 폐 LIB를 -30~-40 ℃ 환경에서 8~12시간 건조하여 수분을 제거한 뒤, 배터리를 분해하여 양극, 음극, 분리막 등의 구성 요소를 분리하였다. 이후 각 부품을 -10~-5 ℃에서 5~8시간 냉동시킨 후 분쇄하였다. 냉동된 분말은 20~45 ℃의 유기용매에 0.2~1시간 교반하고, 50~100 kHz 초음파 처리를 적용하여 전해액 성분이 용매에 용해되도록 하였다. 이어서 원심분리를 통해 고형물과 액체를 분리하고, -2~5 ℃ 저온에서 진공 여과를 통해 추가적인 고액 분리를 수행하였다. 여과액은 감압 증류 과정을 거쳐 유기용매를 회수하여 전해액 보충제로 재생하였다. 이 방법을 통해 전해액 회수율은 98% 이상에 도달하였으며, 전해액 손실과 환경오염 문제를 효과적으로 저감할 수 있음을 보고하였다.
이러한 동결 기반 전처리 방식은 안전성, 환경성, 분리 효율성 측면에서 우수한 친환경 기술로 평가된다. 그러나 액체질소 등 초저온 냉매를 사용해야 하므로 설비 및 운영비용이 높고, 에너지 소모가 크다. 또한 대규모 생산 라인 구축 시 초기 투자비와 냉각 유지비용이 부담으로 작용할 수 있다. 더불어 공정 자동화 및 대량 처리에 어려움이 있어, 향후 공정의 표준화·효율화 및 경제성 검증이 추가적으로 필요하다.
4.1.3. 증류(Distillation)
기화 또는 증류(distillation)는 전해질의 끓는점 차이를 이용하여 유기용매를 분리·회수하는 방법으로, 물질의 증기압, 온도, 압력에 큰 영향을 받는다. 이러한 특성으로 인해 폐 LIB에서 전해질 회수를 위해 다수의 연구가 수행되었다. Zachmann 등은42) tube furnace와 cold trap을 이용하여 90, 110, 130, 150 ℃의 네 가지 조건에서 저온 열처리에 의한 전해질 회수 기술을 연구하였다. 그 결과, 130 ℃에서 80분간 처리할 경우 DMC, EMC, EC를 성공적으로 회수할 수 있었으며, 동시에 배기가스에서 검출된 LiPF6, HF, POF3 등의 분해 생성물을 산성 용액 형태로 회수하였다. 이 기술은 단순하며 유기용매 회수가 가능하다는 장점이 있으나, LiPF6가 분해될 경우 불산과 인산 혼합물 및 유독 가스가 발생한다는 한계가 있다. Lai Y. 등은34) 240~260 ℃의 열풍(hot air)과 60~80 kPa의 감압 조건에서 전해질을 휘발시킨 후, 알칼리를 첨가하여 응축·여과 및 탈불소화 과정을 통해 순수한 용매와 고체 불소 화합물의 혼합물을 회수하였다. 이 방법은 전해질 유기용매를 단순하고 효율적으로 회수할 수 있으나, 용매 손실이 크고 LiPF6가 분해된다는 문제가 있다. 또한 Zhong 등은43) 열분해와 물리적 분리를 결합한 폐 LIB 재활용 공정을 개발하였다. 120 ℃의 저온 열분해를 통해 폐 LIB로부터 99.91%의 유기용매를 회수할 수 있었으며, LiPF6는 550 ℃에서 열분해하여 무해화 처리하였다. Wang Y. 등은44) 다단계 진공 감압 공비 증류(multistage vacuum azeotropic distillation)를 이용하여 전해액으로부터 탄산염 용매를 회수하고, 잔류 액체를 저온에서 결정화하여 LiPF6를 회수하였다. 이 공정은 연속 운전이 가능하며 LiPF6 회수율이 최대 75.1%에 달하는 높은 효율을 보였으나, 고가의 장비가 필요하다는 한계가 있다. Xu R. 등은3) DMC, DEC, EC가 혼합된 전해액을 대상으로 130 ℃, 진공 조건에서 120분간 증류를 수행하였다. 그 결과, DMC와 DEC는 혼합물 형태로 각각 100%와 79.40%의 회수율을 나타냈으며, EC는 증류 잔액으로 분리되었다. Zhou W. 등은45) 소프트팩 LIB의 단면을 절단한 후 진공 추출법으로 전해액을 추출하고, 응축법을 통해 회수하였다. 이 과정에서 95% 이상의 전해액 회수율을 달성하였으며, 대부분의 전해액을 손쉽게 회수할 수 있었고, 후속 처리 과정에서의 화재 및 폭발 위험을 효과적으로 저감할 수 있었다. 한편, 폐전해액에는 불소 이온이 포함될 수 있어 증류 과정 중 회수 용매로 쉽게 유입되어 순도를 저하시킬 수 있다. 이를 해결하기 위해 Dai H. 등은46) TiO 이온체-다공성 CaO 복합체를 사용하여 수집된 전해액을 흡착 처리한 뒤, 감압 증류를 통해 유기용매를 회수하였다. 이 방법으로 얻은 유기용매는 높은 순도를 보였으며, 이를 배합해 제작한 리튬이온전지는 우수한 사이클 성능을 나타냈다. Song C. 등은47) 저온 진공 증발 건조-응축 분리 공정을 활용하여 LIB의 전해질을 회수하였다. 해체된 배터리를 140 ℃ 진공 오븐에 4시간 처리한 후, 0, -20, -50, -75 ℃의 cold trap에서 증기를 순차적으로 응축·회수하였다. 그 결과, 최종 배기가스에서는 휘발성 유기화합물이 검출되지 않았으며, 회수된 전해액에는 비전해질 불순물이 존재하지 않았다. 저온 증류법은 조작이 간단하다는 장점이 있으나, LiPF6 용액은 가열 시 쉽게 분해되므로 증류 온도에 제한이 있으며, 일부 용매 성분 회수가 어렵다는 한계가 있다. Wu L. 등은48) 폐 LIB 에서 발생하는 잔류 전해질 처리를 위해 2단계 열처리 공정을 제안하였다. 1단계에서는 해체된 폐 LIB에 알칼리 용액(20% KOH 또는 Ca(OH)2)을 첨가한 후, 85 ℃ 저온 증류를 통해 Li2CO3와 오일상의 전해질 농축물을 얻었다. 이어서 2단계에서는 이 농축물을 300 ℃ 고온 열분해하여 보조연료와 NaF 및 Na3PO4 형태로 회수함으로써, 폐전해질의 안정적 처리 및 자원 회수 가능성을 제시하였다.
이와 같이 증류 기반 공정은 주로 유기용매 회수에 유리하지만, 전해액 내 LiPF6 및 기타 리튬염은 수증기와 함께 분해되어 LiF로 잔류한다. 또한 독성 및 부식성 물질인 HF, H3PO4 등을 제거·흡착할 수 있는 후처리 장비가 필요하다. 따라서 증류법은 전해질 재활용에서 고순도 용매 회수와 상업적 적용 가능성 측면에서 장점이 크지만, 에너지 소비, 환경 영향, 경제성 및 후처리 문제를 종합적으로 고려해야 하는 공정이다.
4.1.4. 용매추출법
용매 추출법은 전극 재료에 적절한 유기용매를 첨가하여 전해액을 유기용매층으로 이동시켜 수집하는 방식이다. 일반적으로 전해액(예: LiPF6 + DMC/EC/DEC 등 카보네이트계 용매)은 전극 재료 및 분리막 전체에 분포되어 있어, 이를 효과적으로 회수하기 위해서는 적절한 용매 선택이 필수적이다. 이러한 전해액을 유기용매로 추출한 후, 용액 내 각 성분을 증류(distillation) 공정을 통해 유기용매와 전해질로 분리·회수하는 방식이 적용된다. 특히 DMC 등의 탄산염(carbonate)이나 기타 전해질과 잘 혼합되는 유기용매를 활용한 연구가 보고되어 있으며, 이에 대한 개념도는 Fig. 5에 제시되어 있다49).
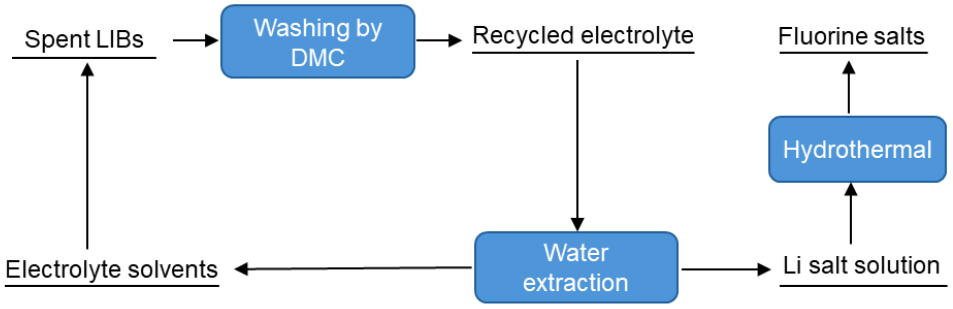
초기 연구로 Lain 등은50) 다양한 유기 액체를 활용하여 폐 LIB로부터 전해질을 추출하는 연구를 수행하였다. 이들은 추출 용매의 요건으로 감압 상태에서의 비등점이 리튬염 분해 온도보다 낮고, 무수 상태로 사용 가능한 재료여야 한다고 제시하였다. 이에 따라 디메틸 카보네이트(DMC)와 같은 탄산염계 용매가 주로 사용되었다. Tong D. 등은51) PC, DEC 및 DME(1,2-디메톡시에탄) 등의 용매를 사용하여 노후 전해질의 회수에 관한 연구를 진행하였으며, 특히 PC를 사용할 경우 가장 효과적이며 2시간 이내에 전해질을 완전히 제거할 수 있음을 보고하였다. Paul Haas 등은52) 용매 추출 공정을 통해 리튬이온배터리 내 전해질(LiPF6)과 고비점 유기성분(DMC, EC 등)을 분리함으로써 환경오염을 저감하고 자원 회수를 도모하였다. 이들은 DMC를 추출 용매로 사용하고 H2O를 혼합하여 다단 향류 추출 시스템을 적용함으로써 전해질과 유기 성분의 회수율을 향상시키는 동시에 잔여 불순물(HF)의 제거도 가능함을 확인하였다. Du, H. 등은53) 폐 LIB를 해체한 후 DMC를 이용하여 전해액을 세척 및 희석함으로써 기존 전해액 내 높은 유전상수(극성)를 가진 EC 성분을 제거하거나 저감하고자 하였다. EC는 물과 유사한 높은 유전상수(약 90)를 가지며, 이로 인해 전해액과 물의 분리가 어려운 특성이 있다. 반면 DMC는 유전상수가 3.1로 낮아, 이를 통해 EC 함량을 희석하면 물과의 분리가 용이해진다. 이후 EC-free 또는 EC 저감 전해액을 물과 혼합하여 리튬염(LiPF6)을 수상층으로 이동시키고, 이를 고온 수열법을 통해 안정한 LiF 및 Li3PO4 형태로 회수하는 방법이 제시되었다. 다만, 전해질 내 EC 성분이 완전히 제거되지 않을 경우 수층과 전해질의 분리가 어려워 추출 효율이 저하되며, 이에 따라 EC 함유 전해질은 반복적인 희석 및 추출 과정을 거쳐야 하는 한계가 존재한다(Fig. 6).
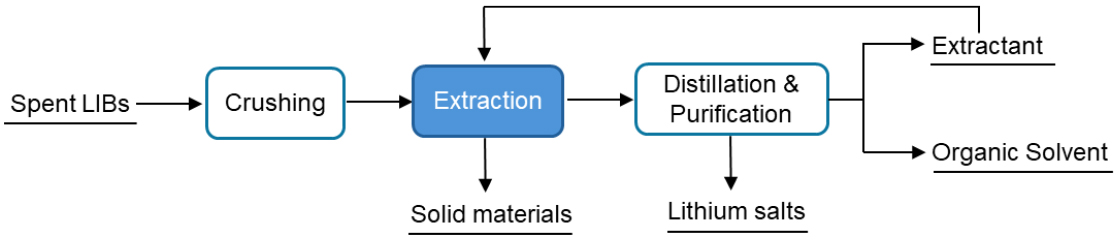
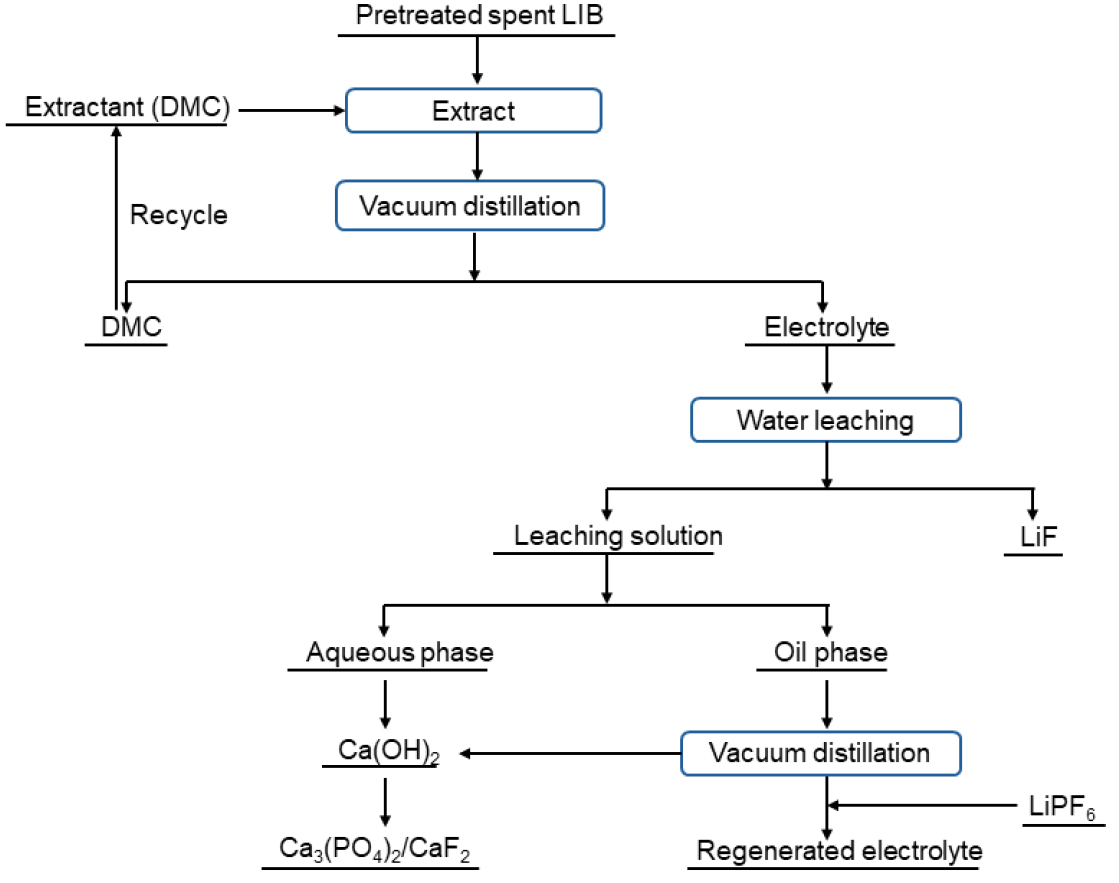
Zhu Y. 등은54) 폐 LIB 분해 과정에서 잔류 전해질을 무해하게 처리하기 위해 디메틸 카보네이트(DMC)를 용매로 사용하였다. 이들은 전극 및 분리막에 잔류된 LiPF6를 DMC로 침지(soaking)하여 용해시킨 후, 이를 반응기로 이송하였다. 반응기 내에서는 DMC와 1 M NaOH 수용액을 혼합하여 산성 전해질을 중화시키고, 동시에 Ca(NO3)2 수용액과 반응시켜 F⁻ 이온을 CaF2 결정으로 전환·회수하였다. 또한 EC, DMC, PC 등 유기용매는 수용액과 분리하여 재활용하는 기술을 제시하였다. Shi G. 등은55) DMC를 사용하여 폐전해질을 추출·수집한 후, 진공 증류를 통해 유기용매와 전해질을 분리하는 연구를 수행하였다. 증류에 의해 회수된 DMC는 폐전해질 추출에 재활용될 수 있으며, 분리된 전해질은 물로 침출시켜 유기오염물질을 제거하고 LiPF6를 가수분해하여 고순도 LiF, CaF2 및 Ca3(PO4)2를 회수하였다. 마지막 단계에서는 진공 증류와 분자체(molecular sieve)를 활용하여 유기용매 내의 수분(H2O)과 HF를 제거하였으며, 재생된 전해질은 적절한 비율의 리튬염과 유기용매를 첨가하여 재활용하는 방안을 제시하였다(Fig. 7).
Zhang S. 등은56) DMC를 사용하여 전해액을 추출하는 과정에서 초음파 및 교반 효과에 대해 고찰하였다. 수집된 추출액 중 DMC는 저온 감압 증류를 통해 회수되어 재사용되었으며, 증류 후 남은 전해질은 수 침출을 통해 LiPF6를 고부가가치 불화 리튬 또는 탄산 리튬으로 전환하여 회수하였다. 이때 용매의 회수율은 약 90%에 달하였다. Hu J. 등은57) DMC, EC, PC 등 탄산염계 용매를 활용하여 리튬이온배터리의 전해질을 추출하고, 증류를 통해 용매를 회수한 후 HF 가스를 통과시켜 고순도의 LiPF6 결정을 얻는 방법을 제시하였다. 분별증류로 회수된 용매는 전해질 추출에 재사용되었으며, 이 방법은 고가의 LiPF6를 효과적으로 회수할 수 있는 장점이 있으나, 부식성과 독성이 강한 HF 가스를 사용함에 따라 고가의 장비가 필요하고 안전상의 위험이 존재한다. Qiu Z. 등은58) EC를 추출 용매로 사용하여 폐 LIB의 양극, 음극 및 분리막 내부에 잔류된 전해질을 재활용하는 연구를 수행하였다. 수집된 전해액은 진공 분별증류를 통해 유기용매를 회수하였으며, 회수된 용매를 배터리에 재사용한 결과 우수한 성능을 나타냈다고 보고하였다. Liu L. 등은59) 폐 LIB를 불활성 가스 분위기에서 방전 처리하고 분해한 후, PC 또는 EC를 이용하여 전해질을 추출하는 재활용 장치를 고안하였다. 이 장치는 전해질의 분류 및 회수가 가능하며, 전해질 회수율을 개선할 수 있음을 확인하였다. Zhang J. 등은60) 용매 추출–LiPF6 전환–증류 분리 공정을 통해 리튬이온배터리 전해액 회수 기술을 제시하였다. 이들은 DMC 등 탄산염계 유기용매를 사용하여 배터리 분쇄물에서 전해액을 추출한 후, 후속 공정에서 유기용매와 헥사플루오로인산염(LiPF6)을 감압 증류를 통해 분리하였다. Zeng G. S. 등은61) 폐 LIB에서 전해질을 회수하기 위해 아세토니트릴과 탄산염으로 구성된 혼합 유기용매를 사용하였다. 이들은 LiPF6를 혼합 용매로 추출한 후 증류 공정을 통해 LiPF6를 회수하였으며, 회수율은 92% 이상으로 보고되었다. Chen X. Y. 등은62) 불활성 가스 분위기에서 탄산염 용매를 활용하여 전해질을 회수하는 연구를 수행하였다. 진공 증류를 통해 유기용매 및 증류 잔류물을 회수하고, 냉각 결정화를 통해 LiPF6를 얻었다. 리튬염의 조성을 분석한 후 전해질을 첨가하고 유기용매를 조절하여 전해질 생성물로 재생하였으며, 이 방법은 HF 오염이 없고 생산 장치의 내식성 요구가 낮으며 회수된 리튬염을 바로 사용할 수 있다는 장점이 있다.
탄산염계 용매 외에도 다양한 용매를 활용한 연구가 진행되었다. Wang X. 등은63) 에테르에서 LiPF6의 높은 용해도를 기반으로 폐 LIB를 침지하여 용액을 회수하고, 농축 결정화 및 재결정화, 여과, 건조 과정을 통해 LiPF6를 회수하였다. Lu X. 등은64) DCM(디클로로메탄), 클로로포름, 아세톤, 에탄올 등 극성 용매를 사용하여 폐LIB에서 전해질을 추출한 후, 80℃ 이하의 저온 증류로 용매를 회수하고, 증류 잔류물인 전해질은 알칼리성 수지를 통해 산을 제거하고 농도를 조절하여 배터리에 재사용하였다. Wan Y. 등은65) DCE(디클로로에탄)를 사용하여 리튬이온배터리 셀 조각에서 전해액을 추출하고, 저온(35~50℃) 상압 증류로 DCE를 분리한 후, 증류 잔류물을 저온(80℃) 감압 증류하여 전해액 용매와 LiPF6를 회수하였다. 이 방법은 공정이 간단하고 LiPF6의 분해를 방지할 수 있다는 장점이 있다.
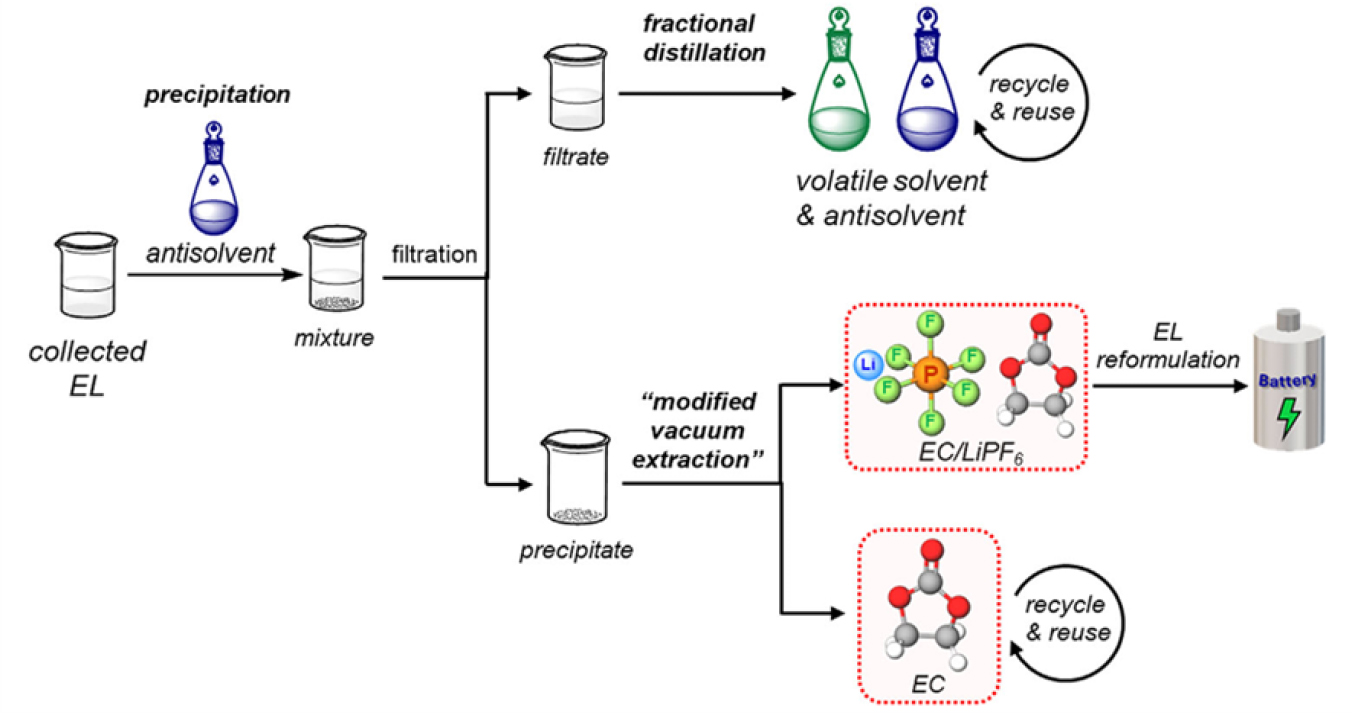
유기용매 기반 추출과 유사하게 수용액계 특수 용매를 활용한 기술도 제안되었다. He K. 등은66) AEES(Aqueous Exfoliating and Extracting Solution)라는 친환경 박리제를 사용하여 Al 및 Cu foil에서 전극 재료를 박리하고, 박리액 중 EC와 PC를 증류로 회수하였다. LiPF6는 AEES와 반응하여 수용성 염으로 전환되며, 이로부터 NaPF6 및 Li2CO3를 회수하였다. 최적화된 AEES 농도에서 Al foil, Cu foil, 전해질 및 전극 물질의 회수율은 각각 99%, 100%, 95.6%, 100%로 보고되었으며, 폐수 및 폐가스 배출이 없어 환경 친화적인 공정으로 평가된다. Zhao Y. 등은67) NaCl 수용액을 사용하여 리튬이온배터리 전해질을 추출하였다. 유기용매는 하부 유기상에서 회수하고, 상부 수용액에는 탄산염 및 인산염을 첨가하여 리튬을 회수하였다. 그러나 LiPF6의 가수분해로 인해 HF 및 인산이 발생하여 장비 부식 및 안전 위험이 존재한다. Zhang H. 등은68) 폐 LIB 전해질 회수를 위해 밀봉 저장, 증류, 진공 여과, 용매 회수 및 저장을 통합한 시스템을 개발하였다. 아세톤을 추출제로 사용하고, 증류를 통해 전해질과 분리함으로써 유기용매 및 불소의 누출을 효과적으로 방지할 수 있다. Ting W. 등은29) 폐전해질 재활용을 위해 2단계 분리·정제 공정을 제시하였다. 1단계에서는 역용매(antisolvent)로 톨루엔을 사용하여 EC/LiPF6 복합체를 선택적으로 침전시켜 분리하고, 증류를 통해 EMC 등 선형 탄산염 용매와 톨루엔을 분리하였다. 2단계에서는 에틸아세테이트(EA) 등 경쟁성 용매를 도입하여 진공 추출법으로 EC와 LiPF6의 결합을 약화시켜 EC를 고순도로 분리·정제하고 EC/LiPF6(몰비 1:1)를 회수하였다(Fig. 8 참조). 이 공정은 고순도 전해질 및 용매의 재활용이 가능하다는 장점이 있으나, 실제 산업 현장의 다양한 폐전해질 조성(첨가제, 대체염, 특수용매 등)에는 적용이 제한될 수 있으며, 용매 사용 및 회수 과정에서 추가 공정과 에너지가 소요되고, 수분 유입 시 LiPF6의 분해 및 유해 부산물 생성 위험이 존재한다.
이와 같이 용매 추출법은 폐 LIB로부터 전해질을 효과적으로 회수할 수 있으며, 전해질 분해로 인해 발생하는 유해 물질의 생성을 방지할 수 있는 장점이 있다. 그러나 이 공정은 상대적으로 낮은 회수율과 많은 양의 유기용매 소비, 그리고 추출 과정에서 새로운 유기 폐기물이 발생할 수 있다는 한계를 가진다. 또한 회수된 전해질은 추출 용매와의 혼합으로 인해 유기 불순물이 포함되어 있어, 정제 비용 증가 및 재사용 시 배터리 성능 저하를 초래할 수 있다. 그럼에도 불구하고, 최근 환경오염 방지를 위한 습식 파쇄(wet crushing) 기술이 주목받으면서 용매 추출법의 적용 가능성이 더욱 확대되고 있다. 습식 파쇄는 분진 발생을 억제하고 전해질의 손실을 최소화할 수 있어, 용매 기반 회수 기술과의 결합을 통해 보다 효율적이고 친환경적인 폐 LIB 재활용 공정으로 발전할 수 있는 가능성을 제시한다.
4.1.5. 초임계 추출법
초임계 유체는 임계 온도와 압력을 초과한 상태의 유체로, 기체와 유사한 낮은 점도 및 높은 확산 계수, 액체와 유사한 높은 밀도를 동시에 지니며 우수한 용해 특성을 나타낸다. 특히 CO2는 비교적 낮은 임계 조건(임계 온도 33.1 ℃, 임계 압력 7.38 MPa)에서 초임계 상태에 도달할 수 있어 활용이 용이하다. 초임계 CO2 추출은 압력과 온도 변화에 따른 용해도 조절이 가능하여 전해질의 선택적 분리 및 회수에 적합하며, 저온 조건에서 진행되므로 LiPF6와 유기용매의 분해를 효과적으로 억제할 수 있다. 또한 CO2는 구하기 쉽고 재활용이 가능하여 친환경적이고 효율적인 전해질 회수 매체로 주목받고 있다69).
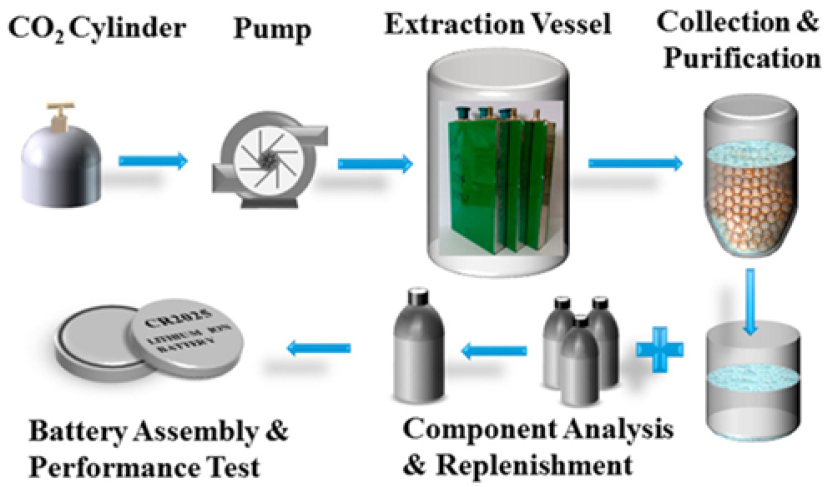
Grützke 등은70) 초임계 CO2 추출을 통해 리튬이온배터리에서 전해질(LiPF6 등)을 친환경적으로 회수하는 방법을 제시하였다. 액상 CO2(25°C, 60 bar)에서는 선형 카보네이트(DMC, EMC)가, 초임계 CO2(40°C, 300 bar)에서는 EC와 같은 극성 전해질이 효과적으로 추출되었다. 단순 CO2만으로는 리튬염 추출이 미미하였으나, CO2에 극성 용매(ACN, DEC, PC 등)를 혼합하면 모든 전해질의 추출률이 크게 향상되었으며, 특히 ACN과 PC를 3:1(부피비)로 혼합할 경우 최대 89% 이상의 회수율을 나타내었다. 이 방법은 온도, 압력, 용매 조성, 추출 유량 조절을 통해 효율 최적화가 가능하며, 배터리 소재 회수의 친환경적 대안임을 입증하였다. Liu Y. 등은71) 반응표면분석법(RSM)을 활용하여 초임계 CO2 추출 공정 변수를 최적화하고 회수율을 개선하였다. 최적 조건은 23 MPa, 40℃, 45분으로 설정되었으며, 이때 추출 회수율은 85.07±0.36%였고, 전해질의 유기용매 함량은 기본적으로 유지되었다. 회수된 생성물의 재사용을 위해 분자체(molecular sieves)와 약염기성 음이온교환수지를 사용하여 전해질 내 수분 및 HF를 제거하는 정제 연구도 수행되었다. Rothermel S. 등은72) 열처리, 아임계(subcritical) CO2, 초임계(supercritical) CO2 등 세 가지 추출 방법을 비교한 결과, subcritical CO2에 의한 전해질 추출 후 열처리를 통해 얻은 흑연의 전기화학적 성능이 가장 우수하였으며, 전해질 회수 효율은 90%에 달하였다. Mu D. 등은73) 초임계 CO2 추출을 이용하여 폐 LIB에서 전해질을 회수할 때, 압력, 온도 및 시간과 같은 공정 변수가 회수율에 미치는 영향을 분석하였다. 30℃ 조건에서는 압력 증가에 따라 추출 효율이 향상되었고, 시간 증가에 따라 효율은 최대치에 도달하였다. 반면, 7 MPa의 압력에서는 온도 상승에 따라 추출 효율이 감소하였다. 전해질 성분은 초임계 CO2에 용해되기 쉬우며, 최종 회수율은 90% 이상으로 보고되었다. Liu Y. 등은30) 배터리를 분해한 후 초임계 CO2 추출 시스템(40°C, 15 MPa)에 투입하여 먼저 10분간 정적으로 추출하고, 이후 2.0 L/min의 유속으로 20분간 동적으로 추출한 결과, 전해액 추출율은 약 85%였다. 선형 탄산염인 EMC 및 DEC에 대한 초임계 CO2의 추출 속도는 고리형 탄산염인 VC 및 EC보다 높았다. 회수된 전해액을 이온교환수지 및 분자체로 정제하고 성분을 보충한 결과, 재생된 전해액은 20°C에서 이온전도도 0.19 mS/cm를 나타내어 상용 전해액과 매우 유사한 특성을 보였다(Fig. 9).
Liu Q. 등은74) 저온에서 폐 LIB를 분해한 후 불활성 가스 분위기에서 초임계 CO2 추출을 수행하였다. 초임계 CO2는 강한 극성을 지니지 않기 때문에 극성 물질에 대한 추출 효과는 제한적이다. 이에 따라 초임계 CO2의 밀도 및 극성 물질 용해 능력을 개선하기 위해 첨가제로 아세톤을 함께 사용하여 전해질의 추출 효율을 향상시켰다. 추출 과정에서 발생하는 배기가스는 CaO 및 NaOH에 흡수되었으며, 추출물은 감압 증류를 통해 아세톤을 제거한 후 성분 분석을 통해 부족한 성분을 보충하여 전해질로 재생하였다. 이 방법은 10~40 MPa, 31~50℃의 조건에서 80% 이상의 추출 회수율을 달성하였다. Li A 등은75) 초임계 CO2 추출 시 고리형 탄산염과 N,N-디메틸포름아미드(DMF) 두 종류의 첨가제를 사용하여 전해질의 추출 효율을 96.24%까지 향상시켰다. 회수된 전해액은 다양한 분자체를 활용하여 수분과 HF를 제거한 후, 최종적으로 재활용 가능한 전해질로 재생하였다. Liu H. 등은76) 폐 LIB 전해질 회수를 위해 초음파를 활용한 반정적-반동적 조합의 초임계 CO2 추출 방법을 개발하였다. 초음파의 적용으로 추출율이 개선되었으며, 전해질 추출율은 약 82%까지 향상되었다. 한편, 국내의 Kim 등은77) 폐 LIB의 기계적 전처리를 통해 분리·회수한 양극재 분쇄물을 50~ 60℃, 50~130 atm의 압력 조건에서 CO2와 용매(아세토니트릴, 프로필렌카보네이트, 디에틸카보네이트) 및 계면활성제를 첨가제로 사용하여 초임계 추출을 수행하였다. 이후 양극재에 포함된 리튬 슬러리와 전해질 슬러리를 각각 분리·회수하고, 전기응집 처리를 통해 불순물을 제거하여 전해액을 회수하였다. 회수된 전해질은 탄산리튬(Li2CO3)으로 고순도화하여 회수하는 방법이 개발되었다.
초임계 CO2 추출법은 폐 LIB 전해질 회수에 적용 가능한 유망한 기술로 평가된다. 본 기술은 비극성 및 저극성 전해질(DMC, EMC 등)에 대해 우수한 회수 효율을 보이며, CO2 자체가 무독성이며 반응 후 잔류하지 않기 때문에 환경적 부담이 적다는 장점을 지닌다. 또한 인화성 유기용매를 사용하지 않으므로 화재 및 폭발 위험이 낮아 안정성 측면에서도 유리하다. 더불어 낮은 임계 온도와 압력에서 공정 운전이 가능하고, CO2를 공정 내에서 재순환하여 활용할 수 있어 친환경성과 자원순환성 측면에서도 강점을 가진다. 그러나 극성 전해질(예: EC, LiPF6)의 경우 CO2 단독 추출로는 회수 효율이 낮기 때문에, 극성 공동용매(co-solvent)를 병용해야 하는 등 공정 최적화가 요구된다. 또한 고압·고온 조건의 유지가 필수적이므로 설비 및 운전 비용이 증가할 수 있으며, 일부 조건에서는 공동용매의 첨가가 오히려 추출 효율을 저하시키는 경우도 있다. 더불어 현재까지 대규모 상업화 사례가 부족하여, 기존 유기용매 추출법 대비 경제성 측면에서 논란이 존재한다.
4.2. 전해액 정제(Electrolyte purification)
전해액은 일반적으로 유기용매(DMC, EMC, EC 등), 리튬염(LiPF6 등), 그리고 다양한 첨가제로 구성된 혼합물로, 수집 후에는 추가적인 정제 처리가 필요하다. 특히 리튬이온배터리(LIB)의 사용 과정에서 전해액과 전극(양극 및 음극) 사이의 반응으로 인해 새로운 화합물이 생성되며, 이로 인해 전해액의 조성이 더욱 복잡해진다. 전해액은 휘발성, 가연성, 독성, 민감성 등의 특성을 지니고 있어, 수집된 전해액을 효율적이고 안전하게 처리하는 것이 매우 중요하다. 이러한 전해액의 정제 방식은 크게 리튬염 회수와 전해액 재생으로 구분되며, 각각의 방식은 목적과 공정 조건에 따라 선택적으로 적용된다.
4.2.1. 리튬염 회수(Lithium salts recovery)
전해액에서 성분 분리의 핵심은 유기용매와 리튬염의 분리에 있다. 전해액 내 유기용매는 제조사마다 조성이 상이하며, 충·방전 과정에서 새로운 화합물이 생성되어 단일 성분의 분리가 어렵다. 또한, 비등점 차이를 이용한 분리 방식은 에너지 소비가 크고 공정 효율이 낮아 실용성에 한계가 있다. 리튬염인 LiPF6는 전통적으로 폐 LIB의 전처리 과정에서 분해되어 양극재와 함께 일부 회수되지만, 이 과정에서 독성 물질이 배출되는 문제가 여전히 존재한다. 최근에는 LiPF6의 경제적 가치가 부각되면서, 이를 직접 회수하거나 안정한 리튬염으로 전환하여 회수하는 방식에 대한 관심이 높아지고 있다. 리튬염 회수 방식은 크게 직접 회수법(direct recovery)과 전환 회수법(conversion recovery)으로 구분할 수 있으며, 각각의 방식은 공정 조건, 회수 효율, 환경 영향 측면에서 차별화된 특성을 지닌다.
4.2.1.1. LiPF6 직접회수법
LiPF6 직접 회수는 Fig. 4에 도시된 바와 같이 용매 추출, 증류, 초임계 추출 등의 방법을 통해 수집된 전해액에서 유기용매 성분을 분리함으로써 가능하다. 예를 들어, Zeng, G. 등은61) LiPF6를 직접 회수하기 위해 폐 LIB를 완전 방전시킨 후 건조하여 내부 습기를 제거하고, 분해를 통해 배터리의 코어를 회수하였다. 이후 해당 코어를 유기용매(아세토니트릴 및 탄산염으로 구성)와 혼합한 뒤 초음파를 적용하여 전해질, 즉 LiPF6를 용출시키고, 여과 과정을 거친 용출액을 감압 증류하여 LiPF6를 직접 회수하였다. 이 방법은 기존 회수법에 비해 환경적 위험성을 줄이고, 높은 회수 효율과 순도를 달성할 수 있음을 실험적으로 제시하였다. Hu, J. 등은57) 폐 LIB에서 LiPF6를 효율적으로 회수하기 위해 먼저 폐 LIB를 1 V 이하로 방전시키고, 세척 및 건조 전처리를 실시한 후 수분 1% 이하의 건조실에서 분해하였다. 이후 코어를 적절한 용매에 침지·교반(온도 10~50℃, 시간 5~60분)하여 LiPF6를 추출하고, 추출액을 여과 및 원심분리한 뒤 무수 HF 가스를 투입하여 순도를 향상시켰다. 마지막으로 증류를 통해 LiPF6를 회수하였으며, 이 방법은 공정이 간단하고 투자비 및 환경오염이 적으며, 높은 회수율과 우수한 순도를 확보할 수 있었다. Zhou, L. 등은78) 폐 LIB에서 전해질을 효율적으로 회수하기 위해 폐 LIB를 세척 및 완전 방전한 후, 불활성 가스가 채워진 건조실 또는 글러브박스에서 분해하여 전해질을 추출하였다. 추출된 전해질은 고진공 감압 조건에서 분별 증류를 통해 유기용매를 회수하고, 이를 정제하여 재활용하였다. 남은 LiPF6 염은 HF 수용액에 녹여 결정화 및 정제 과정을 거쳐 고순도 LiPF6를 얻었으며, 이 방법은 공정이 단순하고 효율적이며 환경 친화적이고, 회수된 재료는 리튬이온전지용 원료로 활용 가능하였다. Liu Q. 등은74) 폐 LIB를 액체 질소에 넣어 완전히 방전시킨 후, 글러브박스 내에서 배터리를 분해하여 초임계 CO2와의 접촉을 극대화하였다. 이후 배터리 셀과 냉동된 전해액 조각 및 전해액이 포함된 부품을 초임계 추출장치에 넣고, 아세톤(초임계 CO2의 2~10% 질량)을 첨가하여 80% 이상의 LiPF6를 추출하였다.
LiPF6 직접 회수법은 화합물의 구조를 유지한 채 회수할 수 있다는 장점이 있으나, 회수 과정이 복잡하고 전해액 회수(Electrolyte collection) 방식에 따라 효율이 크게 달라질 수 있다. 또한 회수된 LiPF6의 순도가 매우 중요하므로, 이를 개선하기 위해 HF를 활용한 추가 정제 공정이 요구된다.
4.2.1.2 .리튬염 전환법 (Lithium Salts Conversion)
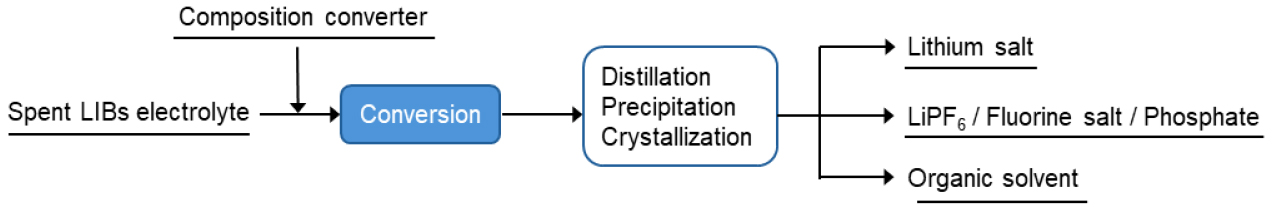
리튬이온배터리 전해액에 가장 일반적으로 사용되는 전해질인 LiPF6는 높은 화학적 활성을 지니고 있으며, 수분과 반응하거나 가열될 경우 독성이 강하고 부식성이 높은 물질로 쉽게 분해된다. 이러한 특성은 후속 분리 및 정제 과정에서 기술적 어려움을 초래한다. 상전환 회수법은 특정 시약을 첨가하여 LiPF6와 반응시킴으로써, 이를 화학적으로 안정한 리튬염, 불소염, 육불화인산염 또는 인산염으로 전환한 후, 이들 물질의 물리적·화학적 특성을 활용하여 단계적으로 회수하는 방식이다.
일반적으로 LiPF6는 수분에 의해 쉽게 분해되며, Li2CO3나 LiF와 같은 안정한 리튬염으로 전환할 경우 회수가 용이해질 수 있다. LiPF6에서 안정한 리튬염으로의 전환 과정을 도식하면 Fig. 10과 같다. 이러한 전환염 중에서 불용성이면서도 안정한 Li2CO3는 용액에서 쉽게 분리될 수 있으며, 양극재 원료로도 활용 가능하기 때문에 매우 유용하다. 전해액에 NaOH 및 Na2CO3 등을 첨가하여 알칼리성을 조절하면, LiPF6를 Li2CO3로 전환하여 회수할 수 있다. 전환 회수법에 의해 회수되는 주요 물질 및 반응식은 다음과 같다.
Jiang D. 등은79) LiPF6를 Li2CO3로 전환하는 통합 공정을 개발하였다. 먼저 폐 LIB를 분해한 후 알칼리 용액을 첨가하고, 초음파 침지를 거쳐 여과액을 얻은 뒤 환류 추출 및 증류 과정을 통해 유기상을 분리하였다. 이후 남은 여과액의 pH를 알칼리성으로 조절하고 Na2CO3를 첨가하여 Li2CO3를 침전시켜 회수하였으며, 용액 중의 F는 MgSO4를 첨가하여 MgF2 형태로 회수하였다. Wang W. 등은31) 전해액으로부터 습식 공정을 통해 고순도 Li2CO3를 회수하는 방법을 제안하였다. 먼저 LiF를 6% H2SO4로 침출하여 Li2SO4로 전환시키고, 80°C에서 액체-고체 비율 2:1로 반응시켜 98%의 리튬을 침출시켜 침출 용액을 얻었다. 이후 침출 용액의 pH를 NaOH로 11까지 조절하고, 에틸렌디아민테트라아세트산(EDTA) 3 g/L를 첨가하여 불순물을 제거하였다. 마지막으로 95°C에서 50분간 290 g/L의 Na2CO3를 첨가하여 침전 반응을 통해 99.5% 순도의 Li2CO3를 회수하였다. Chen Y. 등은80) KCl 및 NH4Cl과 같은 이온 반경이 큰 양이온을 포함하는 염화물 수용액을 사용하여 LiPF6와 반응시켜 불용성 NH4PF6 및 LiCl 용액으로 전환한 후, 용해성 알칼리 및 탄산염을 LiCl 용액에 첨가하여 86.7%의 회수율과 98.4%의 순도를 갖는 Li2CO3를 회수하는 방법을 제안하였다. Hiro H. 등은81) LiPF6 함유 폐액에 potassium bistrifluoromethanesulfonylimide(KTFSI)를 첨가하여 KPF6와 LiTFSI를 생성하고, 원심분리를 통해 KPF6 고체와 원심분리액을 분리하였다. 이후 회전 증발 건조를 통해 유기용매와 LiKTFSI 고체를 회수하였으며, 이 방법으로 99.5% 이상의 KPF6와 99% 순도의 리튬염을 얻을 수 있었다. He Kai 등은66) 나트륨 염을 포함하는 수용성 박리 추출제(AEES)를 사용하여 전극 및 분리막에서 전해질을 박리·추출하고, LiPF6를 NaPF6 및 리튬염으로 전환한 후 침전물 형태로 회수하였다. 증류를 통해 수용액을 제거하고 EC 및 PC를 회수하였으며, 최종적으로 NaPF6 및 Li2CO3를 얻었다. Wu Y. 등은82) 탄산염 용매를 사용하여 리튬이온배터리 분쇄물을 세척하고 전해액을 수집한 후, 감압 증류를 통해 유기용매를 회수하였다. 남은 고형물을 가열 분해하여 PF5 가스와 LiF 고체를 얻고, 산을 사용하여 LiF를 용해시킨 뒤 가용성 탄산염 또는 CO2를 첨가하여 Li2CO3를 제조하였다. 이 과정에서 생성된 PF5는 불안정하고 독성이 강하며, 수분과 쉽게 반응하여 HF를 형성한다. Y. Liu 등은83) 연속 흐름 반응기를 사용하여 폐전해질과 가용성 탄산염 또는 인산염 용액을 반응시켜 Li2CO3 또는 Li3PO4 침전물을 얻었다. 수상은 증발 및 결정화를 통해 육플루오르인산염(PF6)을 생성하였고, 유기상은 탈수 및 분자체 흡착 과정을 거쳐 유기용매로 회수하였다. 이 방법을 통해 리튬이온과 육플루오르인산염의 회수율은 각각 98.89%와 97.42%에 달하였다. Zhu H. 등은84) 폐 LIB 전해액에 Al(OH)3 또는 Al2(SO4)3를 첨가하고 pH를 1.3~1.5로 조절하여 AlPO4 침전물을 얻었다. 이후 여과 후액의 pH를 6.0~7.5로 조절하여 NaxAlF3₊ₓ 침전물을 얻고, 여액의 pH를 10.0~12.0으로 조절하여 Li 함유 여액을 확보한 후 K2CO3를 첨가하여 Li2CO3를 회수하였다. H. Yu 등은36) 폐 LIB를 액체 매질하에서 파쇄하여 전해질을 회수하는 방법을 개발하였다. 염화칼슘 혼합 용액을 파쇄기에 분사하면서 LIB를 파쇄한 후, 여과액을 저온 증류하여 유기상층과 수상층을 분리하였다. 수상은 사염화탄소로 추출하고, 유기상은 증류 공정을 통해 정제하였으며, 추출 잔류물은 나노여과막을 통해 리튬염 용액과 CaCl2 용액으로 분리하였다. 이 방법의 총 전해액 회수율은 91.2%였다. Y. Zhao 등은85) 폐 LIB에서 수집한 전해액을 진공 증류하여 유기용매를 분리하고, 잔류 전해질을 알칼리 용액(Ca(OH)2)으로 처리하여 CaF2 침전을 얻었으며, 전해질 내 리튬은 LiOH 용액 형태로 회수하였다.
4.2.2. 전해액 재생(Electrolyte regeneration)
폐 LIB의 모든 성분을 재활용하여 새로운 배터리에 사용하는 것은 폐 LIB 재활용의 궁극적인 목표이다. 양극 및 음극 소재의 재활용 기술은 활발한 연구와 함께 상용화가 이루어지고 있으나, 전해액의 재생은 그 특수한 물리·화학적 특성으로 인해 상대적으로 재활용이 어렵다. 특히 충·방전 과정에서 전해질과 전극 간의 화학 반응으로 인해 전해액의 조성이 다양하고 복잡하게 변화하며, 이로 인해 상용 전해질과 동등한 성능을 갖는 전해액으로 재생하는 것은 기술적으로 매우 어렵고 경제적으로도 부담이 크다. 전해액의 재생은 저온 증류, 용매 추출, 초임계 CO2 추출 등의 방법으로 수집된 용매에서 수분, 불순물, 전해질 잔여물, 분해 부산물 등을 제거하는 공정으로 구성된다. 주요 처리 방법으로는 탈수(Drying), 탈색, 여과(Filtration), 흡착(Adsorption), 분자체(Molecular sieve), 이온교환수지(Ion exchange) 등이 있으며, 필요에 따라 분별증류(Fractional distillation)를 통해 고순도의 용매를 선택적으로 추출할 수 있다.
예를 들어, Liu Y. 등은30) 폐 LIB를 분해하여 셀을 분리하고 원심분리를 통해 전해액을 회수한 후, 탈색 및 분자체 탈수 과정을 포함한 통합적인 전해액 재생 공정을 제안하였다. 해당 공정은 초임계 CO2 추출, 이온교환수지를 통한 탈산, 분자체를 이용한 정제 등으로 구성되었으며, 재생된 전해액은 20°C에서 0.19 mS·cm⁻¹의 이온 전도도를 나타내어 상용 전해액과 유사한 수준임을 확인하였다. 또한 LCO(LiCoO2)계 전지를 대상으로 전기화학적 특성을 비교한 결과, 재생 전해액은 초기 방전 성능은 양호하였으나 사이클 안정성은 상용 전해액에 비해 낮은 것으로 나타났다. KR 특허(10-2020-0040820)86)에 따르면, 전해액 중 불순물로 존재하는 플루오린산(HF)과 수분(H2O)을 각각 100~5 mg/ℓ, 100~10 mg/ℓ 수준에서 정제를 통해 HF는 10 mg/ℓ 이하, 수분은 15 mg/ℓ 이하로 저감시키는 기술이 소개되었다. 이 기술은 ⅰ) 약염기성 음이온교환수지를 이용한 1차 정제, ⅱ) 제올라이트를 활용한 수분 및 일부 HF 제거, ⅲ) 강산성 양이온교환수지를 통한 미량 양이온 제거 단계로 구성되며, 전해액의 송액에는 질소 가스 등 불활성 가스를 사용하였다. 정제된 전해액은 전극의 부식 및 전해질 분해를 억제하여 LIB의 수명 향상에 기여할 수 있다고 보고되었다. 또한 KR 특허(등록번호 10-1621124)87)에서는 합성 하이드로탈사이트류 흡착제를 이용하여 HF를 90% 이상 제거하여 10 ppmw(parts per million by weight) 미만으로 저감시키고, 합성 제올라이트 또는 활성 알루미나 흡착제를 통해 비수 전해액 내 수분 농도를 10 ppmw 이하로 감소시키는 정제 기술이 소개되었다. 이들 정제 방법을 연계하여 HF와 수분을 연속적으로 제거할 수 있는 정제 장치도 개발되었다. 이러한 평가 결과는 재생된 전해질 용매의 순도와 전기화학적 성능이 신품 수준에 근접하여 재사용이 가능함을 시사하며, 다단계 정제 공정을 통해 고순도 전해질 확보가 가능함을 보여준다. 이는 환경 부담 저감과 자원 재활용 측면에서 의미 있는 성과로 평가된다.
그러나 전해액 재생 공정은 매우 복잡하며, 폐루프(closed loop) 재활용의 개념을 충족하는 것처럼 보이지만, 초기 사이클에서의 용량 감소 등으로 인해 상용화에는 여전히 많은 기술적 장애가 존재한다. 산 결합 물질이나 불소화 인산염을 효과적으로 제거할 수 있는 고도 정제 기술의 개발이 필요하며, 폐전해액의 전체 조성을 정확히 파악하기 위해서는 고급 분석 기술이 필수적이다. Mönnighoff, X. 등의88) 연구에 따르면, 가스 크로마토그래피 및 화학 이온화 분석을 통해 폐전해액에서 17종의 휘발성 유기 노화 생성물이 검출되었으며, 실제로는 더 많은 유도체가 존재할 가능성이 있다.
이와 같이 폐전해액의 복잡한 재생 과정과 상용 전해액과의 비교가 어려운 특성을 고려할 때, 폐전해액 재생은 기술적으로 어려운 과제이다. 따라서 폐전해액 중 LiPF6을 직접 회수하거나 이를 안정한 리튬 기반 염으로 전환하여 회수하고, 전해액이나 추출제로부터 유래한 가연성 유기용매는 추가적인 정제 및 분리 과정을 거치지 않고 에너지 보조 연료로 활용하는 방안이 바람직한 방향으로 판단된다.
5. 결 론
1) 리튬이온배터리의 수요가 빠르게 증가하면서 폐 LIB의 발생량 역시 꾸준히 증가하고 있다. 이로 인해 자원 회수 및 환경 보호의 중요성이 전례 없이 강조되고 있으며, 그중에서도 전해액 재활용은 아직 연구와 산업 적용 모두에서 상대적으로 미흡한 분야로 남아 있다.
2) 전해액 내 염과 용매의 강한 배위 결합, 낮은 열 안정성, 수분과의 높은 반응성 등 여러 화학적 특성으로 인하여 기존 전해액 회수 및 전제 기술은 여전히 고비용, 저 효율성, 복잡한 공정 등으로 인해 상용화에 어려움을 겪고 있다.
3) 향후 전해액 재활용 기술의 상용화와 고도화를 실현하기 위해서는 여러 핵심적인 기술 개발이 필요하다. 즉, 상온 및 개방 환경에서 적용 가능한 간단한 전처리 기술 확보, 고효율적이며 저용매 소비형 추출 매체 설계, 유기용매와 LiPF6의 분해를 최소화하는 저온 증류 공정 확립, 그리고 LiPF6로부터 효과적이고 안정한 고순도 리튬 및 육불화인산염 회수 기술 개발 등이다.
4) 이러한 기술적 한계를 극복하고 전해액 재활용 효율을 극대화할 경우에 리튬이온배터리 자원 순환 체계의 완성도를 높이는 데 기여할 것으로 기대된다. 또한 차세대 배터리 기술과의 호환성을 고려한 연구가 병행될 경우, 전해액 재활용은 지속 가능한 배터리 산업의 핵심 기술로 자리매김할 수 있을 것으로 기대된다.