1. 서 론
최근 배출가스 및 연비 규제 강화와 탄소중립 정책 추진으로 인하여 자동차 배기가스 촉매 및 화학공업용 촉매 원료인 팔라듐 사용이 크게 증가하고 있다. 팔라듐을 포함한 백금족 금속은 남아프리카 공화국, 러시아, 미국, 캐나다, 짐바브웨 등 일부 나라에서 생산하고 있으며1), 우리나라는 현재 전량 수입에 의존하고 있다. 따라서 안정적인 팔라듐 수급을 위해서는 팔라듐 함유 폐자원으로부터 팔라듐 회수가 필요하다. 비교적 높은 팔라듐을 함유하고 있는 자동차 폐촉매는 해체 및 파․분쇄 후 침출공정을 통해 알루미늄을 분리시키고, 남은 침출액 내 백금족 금속을 환원시켜 회수한다1,2,3). 저품위 전자스크랩 및 전자폐기물은 건식공정을 통해 백금족 금속을 농축시킨 후 백금족 금속의 종류별 분리와 정제는 습식법을 이용하여 회수하고 있다2). 무전해 도금공정에서 사용되는 콜로이드 타입 촉매 폐액은 수산화나트륨을 첨가시켜 팔라듐과 주석을 석출시킨 후 필터링 공정으로 석출물을 회수한다. 석출물은 염산 침출 후 용매추출을 통해 팔라듐과 주석을 분리시켜 팔라듐을 회수하고 있다4). 또한, 저농도 수세수 내 팔라듐은 이온교환수지를 이용하여 흡착시켜 팔라듐을 회수하고 있다5). 현재 우리나라는 고품위 팔라듐을 함유하고 있는 폐촉매 및 도금폐액은 습식공정을 이용하여 팔라듐을 일부 회수하고 있으나, 저품위 전자스크랩 및 전자폐기물의 경우 폐기, 매립되고 있다. 저품위 전자스크랩 및 전자폐기물에서 팔라듐을 회수하기 위해서는 고온 환원용융 및 농축 공정을 통해 팔라듐 함유 조금속을 확보한 후 조금속 내 다량 함유하고 있는 구리, 니켈 등 금속을 분리시켜 손실 없는 팔라듐을 회수하는 전해공정이 필요하다. 슬라임(slime) 형태 회수 팔라듐을 왕수 또는 염산에 침출시킨 후 용매추출 공정을 통해 불순금속 분리․정제 공정을 통해 고순도 팔라듐을 회수할 수 있다. 본 연구에서는 팔라듐 함유 조금속으로부터 팔라듐 분리 및 고순도 동 회수가 가능한 전해공정을 연구하였다. 조금속 내 함유 금속별 산화특성을 평가하여 전해공정 시 불순금속 별 거동을 파악하여 분리․전해공정 최적 조건을 확보하고자 하였다.
2. 실험방법
고온 환원용융 공정 후 제조된 조금속 내 팔라듐과 다량 함유 불순금속(구리, 알루미늄, 철, 니켈)을 전해분리 시키기 위한 기초 연구로서 각 금속 성분별 산화전위를 potentiostat(VersaSTAT4, Prinston Applied Research)을 이용하여 선형주사전위법(Linear Sweep Voltammetry, LSV)으로 측정하였다. 1 L 크기의 부식전용 반응기를 사용하였으며, 1 cm × 1 cm 크기의 백금판 2개를 상대전극, 면적 1 cm2 의 팔라듐, 구리, 알루미늄 및 철 판을 각각 작업전극, 포화감홍전극(SCE, saturated calomel electrode)을 기준전극으로 사용하였다. 1~3 M 황산 전해액을 50 ℃ 유지시킨 후 평형상태전압(Open Circuit Potential, OCP)를 기준으로 0~1 V 전압을 1 mV/sec 속도로 인가하였다. 분리․전해공정에서 조금속 내 팔라듐 및 불순금속의 산화 특성을 평가하기 위해 0.7 M 황산구리(II) 5수화물(CuSO4·5H2O)를 각각 1~3 M 황산에 용해시킨 후 각 금속별 산화전위를 선형주사전위법으로 측정하였다. 고온 환원용융 공정 후 제조된 조금속에서부터 팔라듐 및 불순금속을 분리하기 위한 전해공정을 수행하였다. 전해액은 0.7 M 황산구리 및 2 M 황산을 용해시켜 사용하였고, glue 계열 유기첨가제 10 mg/L과 sulfide 계열 유기첨가제 5 mg/L을 첨가하였다. 전해액 온도는 40 ℃, 퍼들 교반기를 사용하여 60 rpm(revolution per minute) 속도로 교반하였다. 양극은 폐 PCB 스크랩에서부터 고온 환원용융 공정 및 농축공정을 거쳐 제조된 조금속을 사용하였고, 음극은 티타늄 판을 SiC 연마지로 연마하여 사용하였다. 전원공급장치(YPP15030, YAMAMOTO) 5 A/dm2 전류밀도를 인가하여 12.5 시간 공정을 수행하였다. 분리․전해공정 후 전해액, 슬라임 및 전착층 내 팔라듐과 불순금속에 대한 순도를 ICP-OES(Inductively Coupled Plasma Optical Emission Spectrometer, Integra XL, GBC Scientific)를 사용하여 분석하였다. 슬라임 및 전착층을 80~85 ℃로 가열된 왕수에 넣어 완전히 용해시켰고, 초순수(Deionized water)로 희석시켜서 ICP-OES 분석하였다.
3. 결과 및 고찰
3.1. 팔라듐 및 불순원소의 산화반응성 특성평가
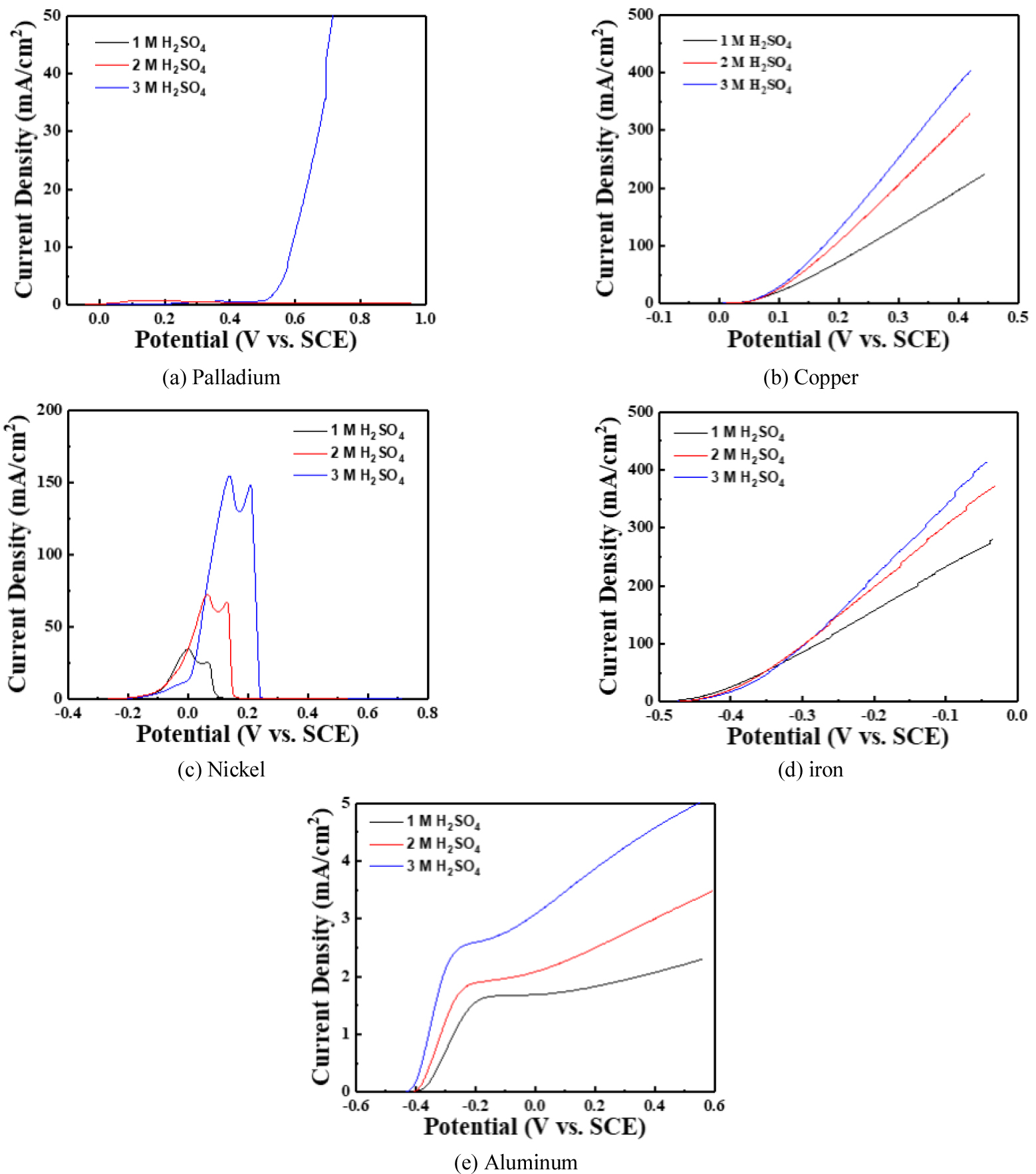
황산 전해액에서 불순금속의 산화전위 특성을 평가하기 위해 potentiostat을 사용하여 선형주사전위법으로 측정하였다. Fig. 1은 1~3 M 황산 전해액에서의 팔라듐과 구리, 니켈, 철 및 알루미늄의 주요 불순금속에 대한 산화 반응성을 분석한 결과이다. 팔라듐의 산화 반응성을 분석한 Fig. 1(a)에서 –0.15 V(vs. SCE)에서 산화가 발생하기 시작하였다. 1~2 M 황산 전해액에서는 인가전압이 증가함에도 팔라듐의 산화반응을 나타내는 전류밀도는 1 mA/cm2 이하의 값을 나타내었으며, 이는 산화반응이 거의 발생하지 않음을 의미한다. 하지만, 3 M 황산에서는 약 0.55 V (vs. SCE) 이상 인가전압에서 팔라듐 산화반응으로 전류밀도가 급격히 증가하는 경향이 발생하였다. 보고된 문헌에 의하면 팔라듐은 황산 전해액에서~1.4 V(vs. SHE)의 전압이 인가될 때 Pd(II) 상태의 양극의 전기화학적 산화반응이 발생하며, 반응식은 식 (1)과 (2)와 같다6). 따라서 3 M 황산에서 0.55~1 V(vs. SCE) 범위의 전압을 인가 시 팔라듐은 Pd(OH)2 또는 PdO의 산화물을 형성하며 Pd2+ 또는 Pd4+ 이온으로 용해는 되지 않을 것으로 판단된다.
Fig. 1(b)는 구리의 산화 반응성을 분석한 결과이며, 0.02 V(vs. SCE)에서 산화반응이 발생하기 시작하며, 인가전압이 증가할수록 전류밀도가 급격히 상승하는 경향을 나타내었다. 또한 황산 농도가 증가할수록 전류밀도도 증가하는 경향을 나타내었다. 전해공정 시 구리 양극에서는 O2- 이온과 반응하여 Cu2O 또는 CuO가 발생하게 되며 이후 아래 식 (3)과 (4)에 의해 황산구리로 용해가 발생한다. 황산 전해액에서 전해공정 시 구리는 CuSO4 반응물로 용해되고, 일부 Cu2O 또는 CuO 형태의 산화물을 형성할 것으로 판단된다.
Fig. 1(c)는 니켈의 산화 반응성을 분석한 결과이며, -0.48 V(vs. SCE)에서 산화반응이 발생하기 시작하며, -0.2~0.25 V 인가전압 범위에서 전류밀도가 급격히 상승했다가 감소하는 경향을 나타내었다. 이러한 현상은 앞서 보고된 문헌에 따르면7), 인가전압이 증가할 때 전류밀도가 상승하는 구간(i), 전류밀도가 감소하는 구간(ii), 전류밀도 값이 거의 없는 구간(iii), 다시 전류밀도가 급상승하는 구간(iv)이 발생한다고 보고되었다. 전압이 상승하는 구간(i)은 식 (5)에서 (7)까지 반응이 발생하여 양극에서 소량의 니켈이 전해액에 용해되는 반응이 발생한다.
전류밀도가 감소하는 구간(ii)은 식 (8)에서와 같이 전극 표면에서 약 2 Å 두께의 NiO 부동태 층을 형성하는 반응이 발생하게 되고, 그로 인하여 밀도가 감소하는 현상과 전류가 거의 흐르지 않는 구간(iii)을 발생시킨다. 이후 인가전압이 증가하게 되면 식 (9)에서와 같이 임계전압에서 NiO 부동태 층이 황산과 반응하여 니켈이 전해액에 용해되는 반응이 발생한다. 따라서 본 실험에서는 식 (5)~(7)과 같은 반응이 발생하는 구간(i) 반응이 발생하였고, 일부 니켈이 전해액으로 용출된 것으로 판단된다.
Fig. 1(d)는 철의 산화 반응성을 분석한 결과이며, -0.48 V (vs. SCE)에서 산화반응이 발생하기 시작하며, 인가전압 및 황산 농도가 증가할수록 전류밀도가 급격히 상승하는 경향을 나타내었다. 전해공정 시 양극에서는 철은 식 (10)에서와 같이 OH- 이온과 반응하여 Fe(OH)2가 생성되게 되며 이후 아래 식 (11)에 의해 황산철로 용해가 발생한다. 본 실험에서도 철은 황산철로 용해될 것으로 판단된다.
알루미늄의 산화 반응성을 분석한 Fig. 1(e)에서와같이 –0.43 V(vs. SCE)에서 산화가 발생하기 시작하였고, 인가전압 및 황산 농도가 증가할수록 전류밀도는 소폭 상승하는 경향을 나타내었다. 전해공정 시 양극에서는 알루미늄은 OH- 이온과 반응하여 Al2O3층의 생성되게 되며 전해액에 알루미늄 이온으로 용해되지 않을 것으로 판단된다.
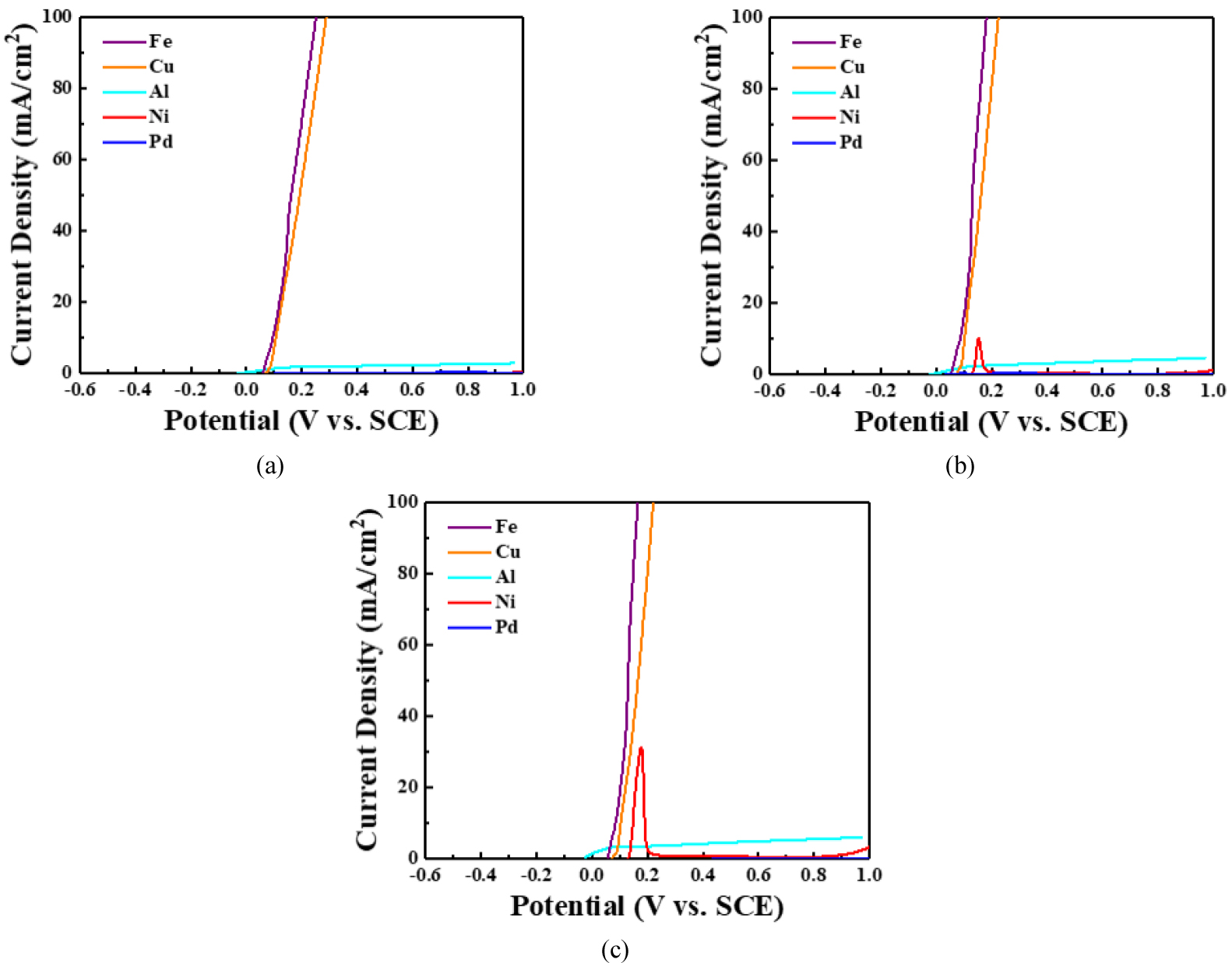
효율적인 분리․전해공정을 위해서는 황산구리가 용해된 황산 전해액을 사용하며, 황산 농도에 따른 불순금속의 산화전위 특성을 평가하여 Fig. 2에 나타내었다. Fig. 2(a)~(c)는 각각 1, 2, 3 M의 황산에 0.7 M 황산구리를 투여한 전해액에서 팔라듐 및 불순금속에 대한 산화 특성을 평가한 결과이며, 팔라듐의 산화반응은 약 0.05 V에서 시작하였고, 주요 불순금속 중 구리, 철, 니켈 및 알루미늄은 각각 약 0.07, 0.04, 0.12 및 -0.03 V(vs. SCE)에서 산화반응이 발생하기 시작하였다. 인가전압이 상승함에 따라 구리와 철의 전류밀도는 크게 증가하였고, 팔라듐, 니켈, 알루미늄은 매우 낮은 전류밀도를 나타내었다. 니켈은 황산 농도가 증가할수록 전류밀도가 점차 증가하는 경향을 나타내었다. 따라서 1 M 황산 및 0.7 M 황산구리 전해액에서 분리․전해공정을 수행 시 구리, 철은 용해되고, 팔라듐, 니켈 및 알루미늄은 산화물 형태 슬라임 회수가 가능할 것으로 판단된다. 2, 3 M 황산 및 0.7 M 황산구리 전해액에서 구리, 철, 니켈은 용해되고, 팔라듐 및 알루미늄은 산화물 형태 슬라임 회수가 가능할 것으로 판단된다.
3.2. 조금속으로부터 팔라듐 및 불순원소의 분리․전해공정
폐 전자폐기물에서 건식정련 및 팔라듐 농축공정으로 제조된 조금속을 사용하여 팔라듐 분리․전해공정을 수행하였다. 조금속의 성분을 Table 1에 나타낸 것과 같이 91.05 % 구리, 4.79 % 팔라듐, 2.27 % 철, 1.13 % 니켈, 0.64 % 실리콘과 수십~수백 mg/L 농도의 주석, 금, 은, 망간, 아연, 크롬을 함유하고 있었다. 40 ℃, 0.7 M 황산구리 및 2 M 황산 전해액에서 5 A/dm2 전류밀도를 인가하는 공정조건에서 분리․전해공정을 수행하였다. 인가전류밀도 조건은 potentiostat이용 금속의 산화반응 특성 결과에서 팔라듐 분리가 가능한 조건에서 전해공정의 과전압을 고려하여 선정하였다. 유기첨가제 분해 소모량을 고려하여 12.5시간, 6 cycle(총 75시간)을 수행하였고, 양극 부직포 및 반응기 바닥에 침전되어있는 슬라임을 잘 포집한 후 세척 및 건조시켜서 양극 슬라임 분말을 확보하였다. 분리․전해공정 12.5시간 수행하였을 때 전해액 내 금속 농도를 ICP-OES로 분석한 결과를 Table 2에 나타내었다. 전해액 내 구리 함량은 약 44.3 g/L이었고, 불순금속 중 철과 니켈의 함량이 각각 0.63 g/L 및 0.43 g/L으로 측정되었고 0.001 g/L의 극소량의 팔라듐이 용해되었다. 분리․전해공정을 12.5시간 수행한 후 전해액을 신액으로 교체하며 공정을 지속하였고, 용액 내 팔라듐 및 주요 불순금속 분석을 수행하였다. 분리․전해공정 시간 및 공정 cycle이 지속될수록 전해액 내 구리의 함량은 최초 약 45 g/L를 계속 유지하였으나, 주요 불순금속 중 철과 니켈 함량은 증가하는 경향을 나타내었고, 팔라듐도 소량 증가하는 경향을 나타내었다. 최초 196.57 g 조금속을 12.5시간, 6 cycle의 총 75시간 분리․전해공정을 수행한 후 잔여 조금속 무게는 64.43 g이었고, 회수된 슬라임 무게는 10.64 g이었다. 회수 슬라임의 팔라듐 및 불순금속의 성분을 ICP-OES로 분석한 결과를 Table 3에 나타내었고, 58.40 wt.%의 팔라듐, 1.43 wt.% 구리 및 수십~수백 mg/L의 철, 니켈 등의 불순금속들이 측정되었다. 조금속 슬라임 성분 분석결과로 용해된 조금속 및 회수 슬라임의 금속성분 별 중량을 계산한 결과 팔라듐 회수율은 97.46 %으로 손실이 거의 없는 팔라듐 회수가 가능하였다. 전해공정을 12.5시간 수행한 후 음극에서의 전착층의 성분을 분석한 결과를 Table 4에 나타내었다. 수~수십 mg/L의 팔라듐, 철, 니켈, 실리콘, 주석이 측정되었고, 99.990 wt.%의 4N급 구리를 회수하였다.
Table 1.
Quantitative analysis of impurity concentration in the crude metal by ICP-OES(wt.%)
| Elements | Pd | Cu | Fe | Ni | Si | Sn | Au | Ag | Mn | Zn | Cr |
| Crude metal | 4.79 | 90.81 | 2.27 | 1.13 | 0.64 | 0.0391 | 0.0356 | 0.0228 | 0.0152 | 0.0057 | 0.0010 |
Table 2.
Metal concentration in electrolyte after 12.5 hours the electrolysis process for Palladium separation
4. 결 론
폐 전자폐기물에서 건식정련 및 팔라듐 농축공정으로 제조된 조금속을 사용하여 팔라듐 분리․전해공정을 수행하여 다음과 같은 결론을 얻었다.
1. 황산구리 및 황산 전해액에서 불순금속의 산화전위 특성을 선형주사전위법으로 평가하였고, 구리, 철, 니켈은 용해되고, 팔라듐 및 알루미늄은 산화물 형태 슬라임 회수가 가능한 것으로 나타났다.
2. 조금속에서 팔라듐 분리 전해공정을 시 양극에서 철 및 니켈은 용출되어 전해액 내 철과 니켈의 함량은 점차 증가하였고, 팔라듐은 산화물 형태의 슬라임으로 분리되어 97.46 %의 손실이 거의 없는 팔라듐 회수가 가능하였다.
3. 팔라듐 분리․전해공정을 12.5시간 수행한 후 음극에서의 전착층에서는 99.990 wt.%의 4N급 구리를 회수하였다.