1. 서 론
2. 실험 방법
2.1. 샘플
2.2. 침출 정제
2.3. 알칼리 배소
2.4. 특성 분석
3. 결과 및 고찰
3.1. 침출 정제
3.2. 알칼리 배소
3.3. 재생 공정의 경제성 평가
4. 결 론
1. 서 론
전기자동차(Electric vehicle, EV)와 재생에너지 저장시스템(Energy storage system, ESS)의 급속한 보급은 고에너지밀도, 장수명, 고속 충전 특성을 가진 리튬이온전지(Lithium ion battery, LIB)의 수요를 폭발적으로 증가시키고 있다1). 전 세계 LIB 수요는 2030년까지 연평균 20%의 성장률(CAGR)을 보이며 약 4,700 GWh 규모에 이를 것으로 전망된다1). 그러나 LIB의 운용 수명이 일반적으로 3-5년에 불과하다는 점을 고려할 때, 향후 폐LIB 발생량이 급격히 증가할 것으로 예상된다2).
폐LIB는 리튬(Li), 니켈(Ni), 코발트(Co), 망간(Mn), 알루미늄(Al), 구리(Cu), 흑연(C) 등 다양한 유가금속과 비금속 자원이 함유되어 있으며3), 이러한 자원 확보 필요성과 더불어 환경 규제 강화에 따라 전 세계 LIB 재활용 시장은 빠른 속도로 확대되고 있다. 관련 문헌에 따르면 LIB 재활용 시장은 연평균 17% 이상 성장하여 2032년에는 약 569억 달러 규모에 이를 것으로 전망된다4,5).
현재까지의 폐배터리 재활용은 주로 건식 또는 습식 제련을 통해 양극재 금속((Li, Ni, Co, Mn)와 집전체(Al, Cu)를 회수하는 데 초점이 맞추어져 왔다1). 그러나 LIB 전체의 12-21 wt%, 특히 EV용 대형 배터리팩의 경우 최대 30 wt%를 차지하는 흑연은 상대적으로 재활용이 미흡한 실정이다6,7,8). 폐흑연(Spent graphite, SG)은 고온 제련 시 보조 환원제로 활용되거나 습식 제련 후 잔사 형태로 매립되는 경우가 많아, 자원의 비가역적 손실과 처리 비용, 환경 부담을 동시에 야기한다2,7).
배터리급 흑연의 신규 생산은 상당한 에너지와 비용을 필요로 한다. 천연 흑연은 부유선광, 산침출, 고온 열처리(2,000 °C 이상) 등의 다단계 공정을 거쳐야 하며, 인조 흑연은 흑연화 공정(2,500-3,000 °C)을 요구하기 때문에 생산단가는 톤당 8,000-13,000 달러에 이른다2). 반면 폐흑연은 일정 수준의 결정성을 유지하고 있어, 신규 흑연화 단계를 부분적으로 생략할 수 있다. 따라서 재활용을 통해 약 3,000 달러/톤 수준의 비용으로 배터리급 흑연 생산이 가능하며, 전량 수입에 의존하는 국가에서는 전략적 이점이 크다9).
흑연은 전 세계적으로 중국 생산 의존도가 높은 자원으로, 유럽연합(EU)은 이를 전략적 핵심 원료로 지정하였다4). 수요 또한 2030년까지 4배, 2040년까지는 25배 이상 증가할 것으로 전망되어5), 폐흑연의 효과적인 재활용 기술 개발이 시급하다. 따라서 폐흑연의 회수와 재생은 자원순환과 탄소중립 실현, 배터리 제조 경쟁력 확보를 위한 중요한 대안으로 부각된다.
그러나 폐흑연 재활용 기술은 양극재 회수 기술에 비해 상대적으로 연구와 적용이 부족하다2). 이는 폐흑연이 전극 구조 특성상 잔류 양극재, 바인더, 전해질 분해물, 고체전해질계면(SEI) 등이 혼입되어 있고, 장기간 충·방전 과정에서 구조적 열화가 진행되기 때문이다5). 또한, 회수 경로에 따라 불순물 조성과 결함 특성이 달라진다. 예를 들어 집전체에서 직접 회수한 흑연, 부유선광으로 얻은 블랙매스 분리물, 습식 제련 잔사에서 회수된 흑연은 각각 상이한 불순물과 구조적 특성을 보인다9). 블랙매스 유래 흑연은 Al·Cu 잔류물과 분리막 열분해 잔사 등을 포함하고3), 침출 잔사는 황산 침출 시 형성되는 금속 황산염 및 산화물이 다량 존재한다. 따라서 폐흑연의 재생 공정은 회수 경로에 따라 달라지는 오염 특성과 구조적 안정성을 고려하여 설계되어야 한다.
최근에는 폐흑연의 재생을 위해 저온 불소화 로스팅10), 산 침출4,8,11,12,13,14), 알칼리 침출4), 알칼리 배소11), 고온 열처리4,5,14), 표면 재구성5,8) 등 다양한 방법이 제안됐다. 이러한 공정들은 불순물 제거와 결정성 회복을 통해 상용 음극재에 준하는 전기화학적 성능을 구현하였으며, 낮은 불순물 함량, 축소된 층간거리(d002), 낮은 ID/IG 비 등의 성과가 보고되었다. 이는 전통적인 고온 흑연화 공정에 의존하지 않고, 순환형 배터리 경제 구축에 기여할 수 있음을 보여준다.
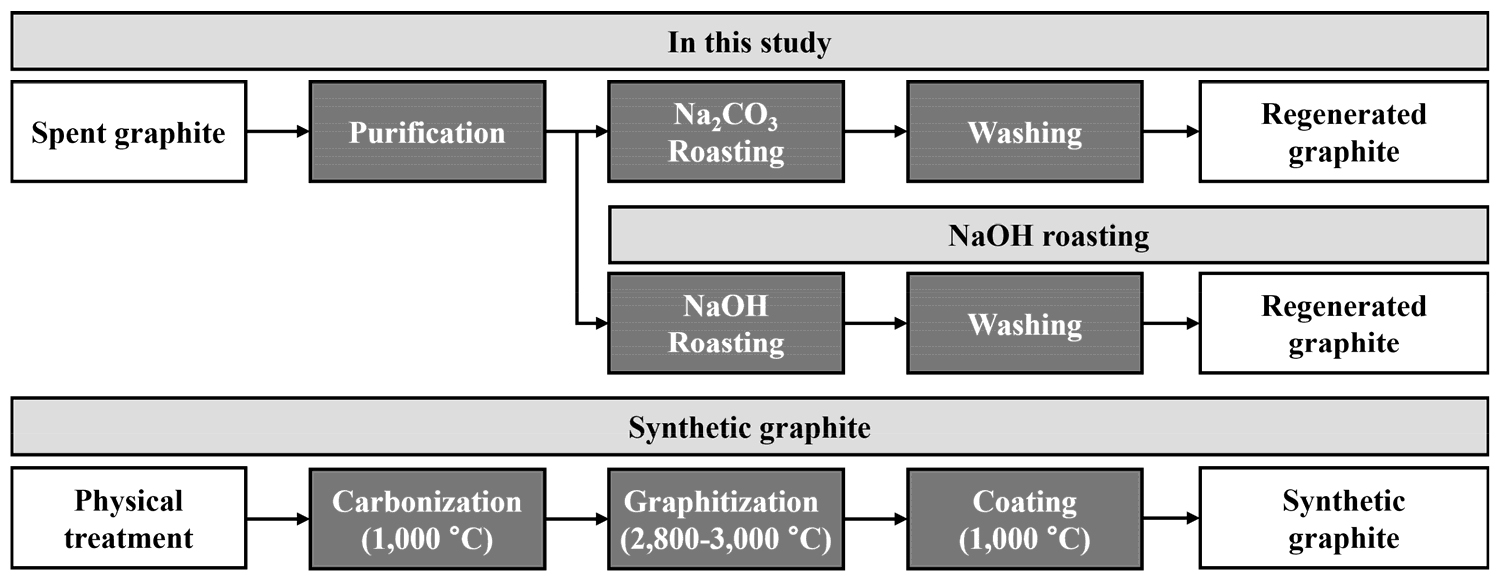
본 연구에서는 Fig. 1과 같이 습식 제련 침출 잔사에서 회수한 폐흑연에 대해 2단계 정제 공정을 적용하였다. 구체적으로 수침출과 800 °C에서 Na2CO3 배소를 통해 표면 불순물을 선택적으로 제거하고 흑연 구조를 회복하였다. 본 공정은 강산과 불소계 시약 사용을 배제하여 작업 안전성을 높였으며, 재생 흑연의 물리·화학적 특성 분석을 통해 순도, 결정성, 결함 수준이 원료 폐흑연 대비 향상됨을 확인하였다.
2. 실험 방법
2.1. 샘플
본 연구에 사용된 침출 잔사는 국내 폐배터리 습식 제련 재활용 기업인 성일하이텍에서 제공받았다. 해당 시료는 약 500 °C에서 열처리하여 바인더와 전해질을 제거한 블랙매스를 황산 침출한 후, 여과 과정을 거쳐 얻어진 케이크 형태의 잔사이다. 초기 시료의 수분 함량은 약 30 wt% 수준이었으며, 이를 80 °C에서 24시간 건조하였다. 또한, 전처리 과정에서 유입된 셀 케이싱이나 포장재 등 큰 불순물을 제거하기 위하여 100 μm 체를 이용한 체거름 과정을 수행하였다. 흑연 시료의 원소 조성은 유도결합플라즈마-광학방출분광기(ICP-OES, iCAP Pro XP, ThermoFisher, USA)를 이용하여 분석하였으며, 그 결과를 Table 1에 제시하였다. 이때, 탄소 매트릭스 내 포함된 무기 불순물을 완전히 용해하기 위해 350 °C 이상의 조건에서 황산을 이용한 열분해 과정을 거친 후, 왕수로 용해하였다15).
Table 1
Elemental compositions (ppm) of spent graphite samples by ICP-OES
2.2. 침출 정제
습식 정제는 고체 함량 20wt%(고체/펄프) 조건에서 80 °C에서 2시간 동안 교반(400 rpm)하면서 수행하였다. 이 과정에서 얻어진 흑연을 정제 흑연(PG, Purified graphite)으로 표기하였다. 또한, 단순 수침출만 진행한 시료는 WG(Water leached graphite)로 구분하였다. 비교를 위하여 동일한 조건에서 5 M 황산과 35 wt% 과산화수소를 이용한 산 침출을 수행하였으며, 해당 시료는 AG(Acid leached graphite)로 명명하였다. AG 시료는 수침출 정제 효율을 평가하기 위한 기준 시료로 활용하였다.
2.3. 알칼리 배소
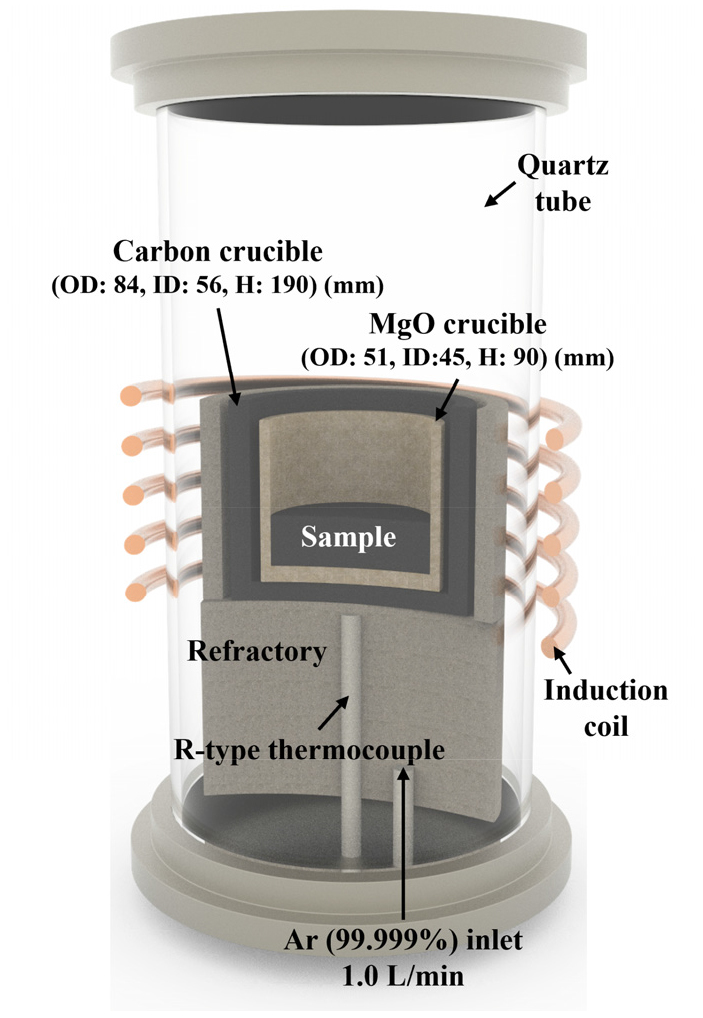
각 PG 시료(30g)에 대해 10 wt% Na2CO3를 혼합한 뒤, 5 mm 크기의 지르코니아 볼(300 g)을 사용하여 볼밀링으로 1시간 동안 혼합하였다. 혼합된 시료는 MgO 도가니에 넣고, 승온 속도 10 °C/min 조건으로 800 °C까지 가열하여 2시간 동안 아르곤(Ar, 1.0 L/min) 분위기에서 배소하였다. 실험은 R 타입 열전대를 이용해 온도를 보정한 유도가열로에서 탄소 도가니를 통해 열처리를 진행되었으며, 구체적인 장치는 Fig. 2에 제시하였다. 배소가 끝난 후 시료는 80 °C에서 2시간 동안 400 rpm으로 교반하면서 수침출을 진행하였고, 이후 진공 여과와 증류수 세척을 거쳤다. 이렇게 얻어진 시료는 RG(Roasted graphite)로 표기하였으며, 배소 전 처리 방식에 따라 각각 R-WG와 R-AG로 구분하였다.
2.4. 특성 분석
SG, PG, RG의 열적 거동은 열중량분석(TGA, STA 449 F5, Netzsch, Germany)을 이용하여 공기 분위기(250 ml/min)에서 승온 속도 10 °C/min으로 1000 °C까지 평가하였다. 잔류 회분(ash)은 X-선 형광분석(XRF, ZSX PrimusIV, Rigaku, Japan)을 통해 확인하였으며(Table 2), 별도로 동일 조건에서 1000 °C 열처리를 수행하여 질량 손실 기반으로 정량화 하였다(Table 3).
Table 2
Oxide compositions (wt%) of spent graphite ashes by XRF
Table 3
Ash content of spent graphite samples
흑연의 미세 구조와 원소 분포는 전계방출 주사전자현미경(FE-SEM, Mira 3, Tescan, Czech Republic)과 에너지 분산형 X선 분광법(EDS, XFlash® 6|30, Bruker Nano GmbH, Germany)을 이용하여 관찰하였다. 결정 구조는 X-선 회절(XRD, SmartLab SE, Rigaku, Japan)으로 평가하였으며, 흑연화 정도와 구조적 무질서는 라만 분광법(RAMAN Touch, Nanophoton, Japan)을 이용하였다. 또한, 표면 화학 상태는 X-선 광전자 분광법(XPS, ESCALAB, VG Scientific, Thermo Fisher Scientific, USA)을 통해 수행하였다.
3. 결과 및 고찰
3.1. 침출 정제
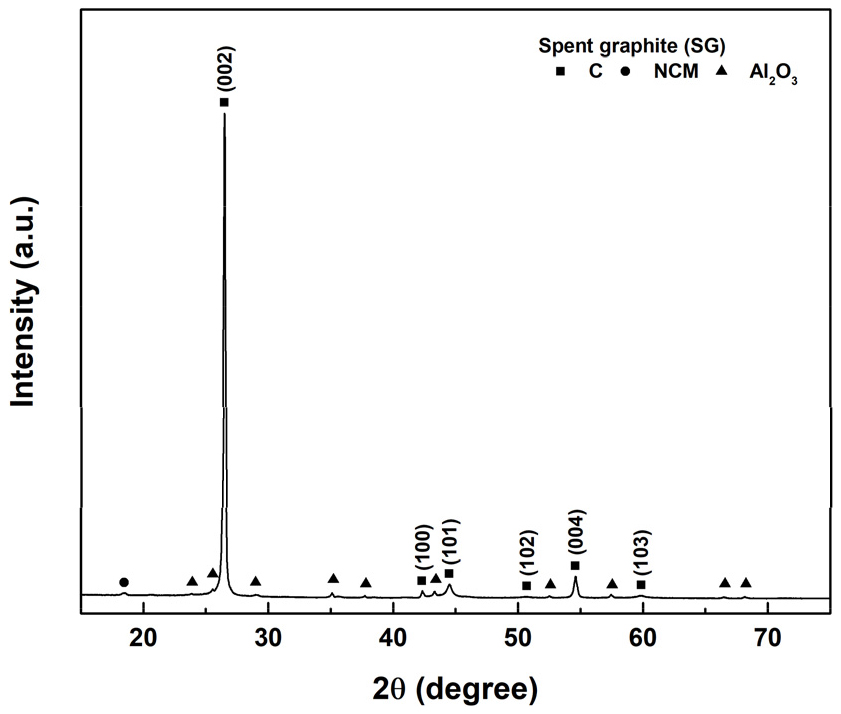
Fig. 3(a)와 Fig. 3(b)는 폐흑연의 SEM 관찰 결과와 EDS 원소 분포를 보여준다. 이미지에서 확인되는 바와 같이, 흑연 표면에는 양극재로부터 유래한 전이금속, Al2O3, 및 불소화 화합물 등이 잔존하여 심각한 오염이 발생하고 있음을 알 수 있다. 이러한 불순물은 Fig. 4의 XRD 분석 결과에서도 일부 나타나는데, 2θ=26.5°, 42.3°, 44.5°, 50.7°, 54.6°, 60.0° 부근에서 나타나는 회절 피크는 각각 흑연의 (002), (100), (101), (102), (004), (103) 결정면에 해당한다4,8,10,13,16,17). 또한, Ni-Co-Mn (NCM) 상과 Al2O3와 관련된 미약한 회절 신호가 관찰되어, 양극재 및 집전체 열화 과정에서 기인한 무기 잔재물이 남아 있음을 확인하였다.
Table 1의 ICP 분석에 따르면, 수침출 후 Ni, Co, Mn과 같은 전이금속 불순물은 대부분 제거된 반면, Al은 농도 변화가 크지 않았다. 이는 전이금속이 황산 침출 과정에서 수용성 황산염으로 전환되어 제거되기 쉬운 반면, Al은 상대적으로 안정한 형태(Al2O3)로 존재하기 때문이다. 특히, 산을 외부에서 첨가하지 않고도 황산염 잔류물의 수침출 시 용액이 산성화(pH=약 1.5)되는 현상이 나타났다.
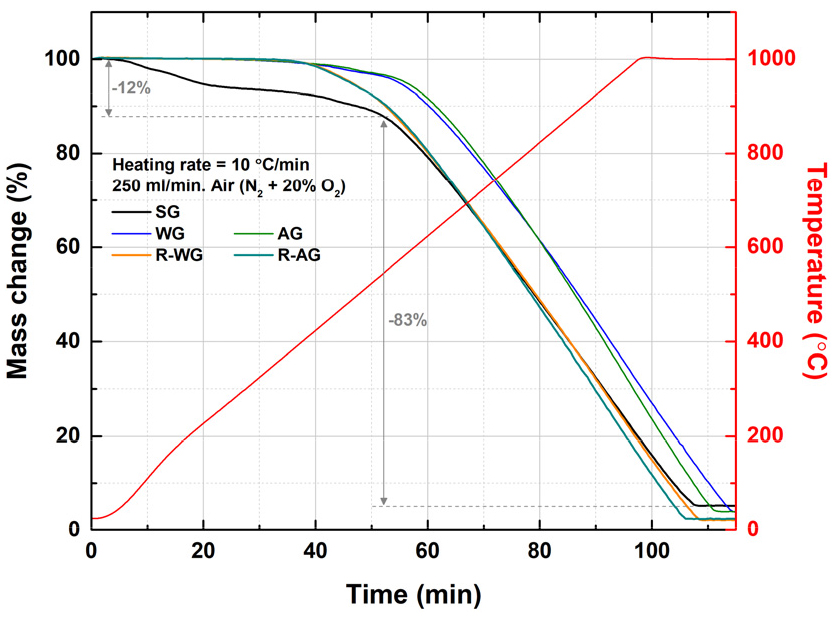
열중량분석 결과(Fig. 5, Table 3)에 따르면, 침출잔사는 휘발분(약 12%), 고정탄소(약 83%), 회분으로 이루어져 있으며, 이는 상용 흑연 음극재(고정탄소 약 99% 이상)에 비해 많은 불순물을 포함한 것으로 알 수 있다. 정제에 따른 회분 함량을 비교하였을 때, 폐흑연의 회분(ash) 함량은 5.42 wt%였으나, 수침출 처리한 WG 시료에서는 4.02 wt%, 산침출 처리한 AG 시료에서는 3.93 wt%로 감소하였다. 이를 통해 침출 정제가 불순물(특히 NCM 성분) 제거에 효과적임을 확인할 수 있었다.
3.2. 알칼리 배소
폐흑연에서 Al 불순물은 주로 집전체 및 양극 소재의 도펀트 등에서 기인한다18). 황산 침출 과정에서 과산화수소가 존재할 경우 금속 Al은 Al2O3로 산화되며, 이는 화학적으로 안정하여 황산 침출만으로는 제거하기 어렵다16). 또한 SiO2 등 산에 불용성인 무기물이 함께 존재할 수 있어, 이들 불순물을 효과적으로 제거하기 위해서는 다른 정제 전략이 필요하다.
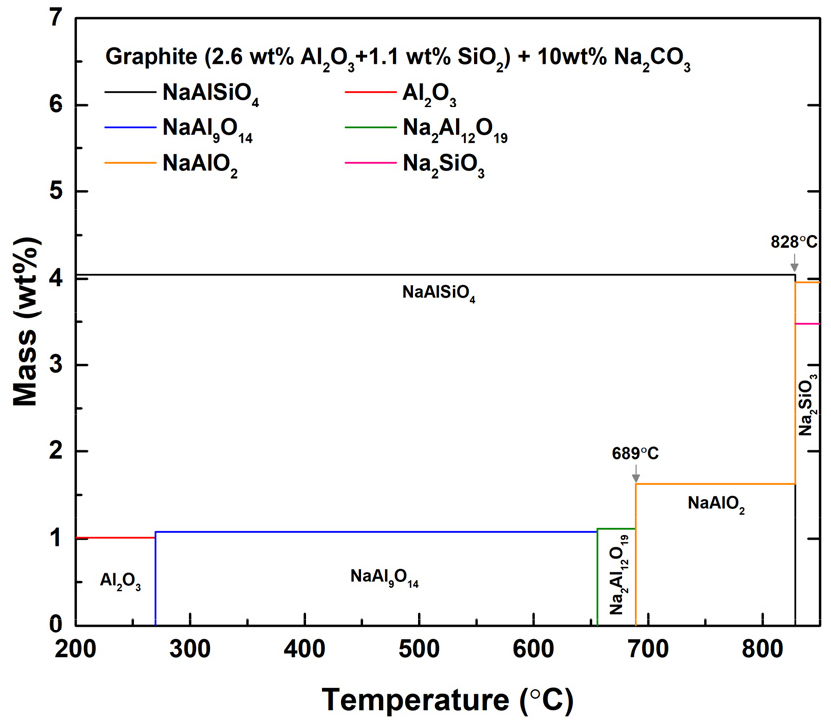
기존 연구에서는 NaOH와 같은 알칼리를 이용한 고온 배소가 Al2O3와 SiO2를 각각 수용성 알루민산염(NaAlO2)과 규산염(Na2SiO3)으로 전환할 수 있음이 보고되어 있다. 그러나 반응 조건에 따라 NaAlSiO4와 같은 수불용성 화합물이 함께 형성되기도 한다19). 본 연구에서는 부식성이 강한 NaOH 대신 Na2CO3를 사용하였으며, 반응성과 안전성을 고려하여 800 °C에서 배소를 수행하였다. 열역학 계산(Table 4, 반응식 (4)-(9))에 따르면, 이 조건에서 Al2O3와 SiO2가 NaAlO2와 Na2SiO3 형태로 전환되는 반응이 우세하였다20,21,22). 또한 ZrO2, WO3 등의 도펀트 역시 수침출이 가능한 형태로 전환될 수 있는 것으로 보고되어 있다23,24). 실제 FactSageTM 계산 결과에서도 NaAlO2와 함께 일부 NaAlSiO4의 형성이 확인되었으며(Fig. 6), 이로 인해 수침출만으로는 불순물이 완전히 제거되지 않을 가능성이 제기되었다.
Table 4
Representative thermodynamic reactions during alkali roasting
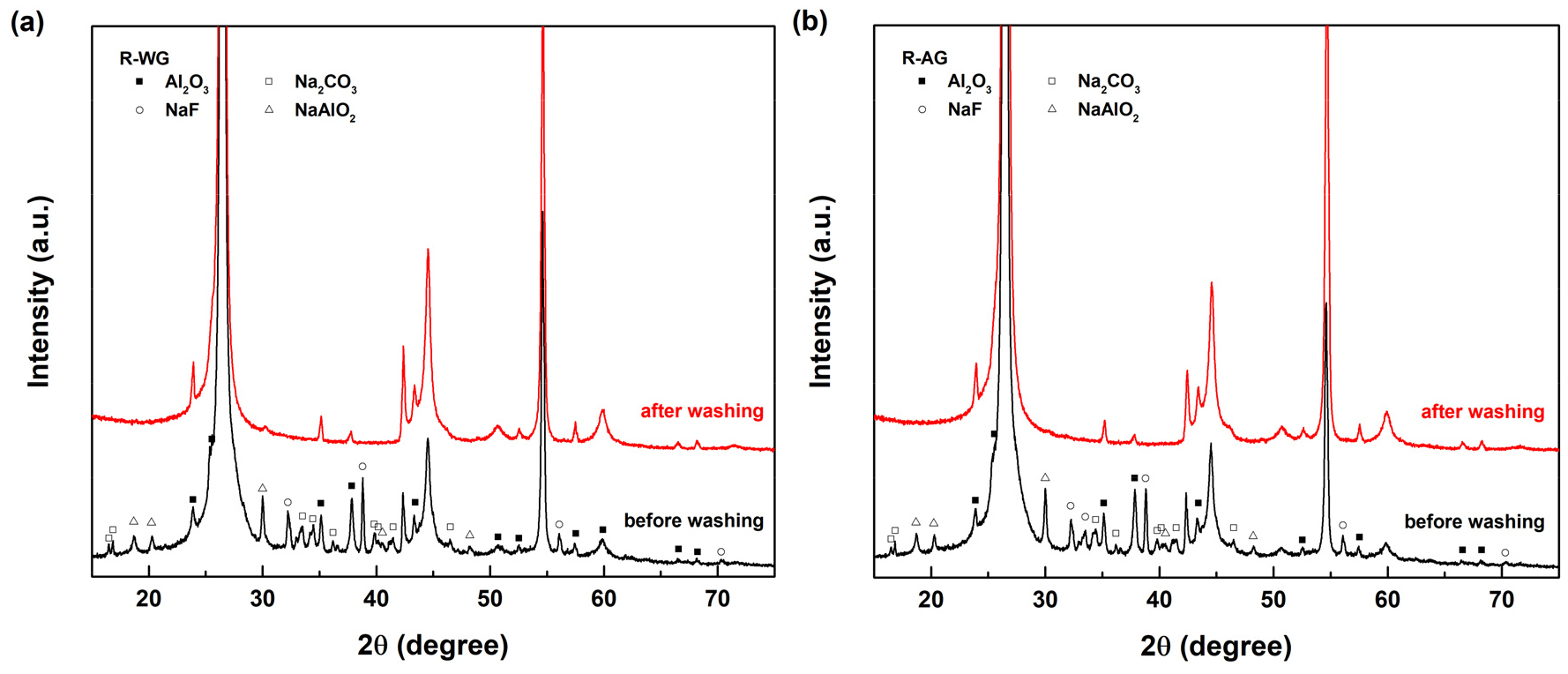
XRD 분석 결과(Fig. 7)에서는 배소 후 NaAlO2와 NaF의 특성 피크가 관찰되었으며25,26,27), 이후 수침출 과정을 거치면서 이들 상이 효과적으로 제거됨을 확인하였다. 이는 배소 부산물이 수용성 형태로 변환되어 후처리 정제를 통해 쉽게 제거될 수 있음을 의미한다. 열중량분석에서도 PG 대비 R-WG와 R-AG 시료의 회분 함량이 각각 2.23 wt%, 2.36 wt%로 감소하였으며, Al2O3, SiO2, ZrO2, WO3 등 주요 무기 불순물이 효과적으로 제거된 것을 알 수 있었다. 다만, Na2O 잔류가 관찰되어 일부 불용성 화합물(예: NaAlSiO4)이 형성된 것으로 추정된다. 이러한 상은 전극에서 절연층을 형성하여 리튬 이온 이동을 방해하거나 계면 저항을 증가시킬 수 있는 것으로 알려져 있어28), 고순도 흑연 회수를 위해서는 후속 산 침출 공정이 필요할 것으로 판단된다.
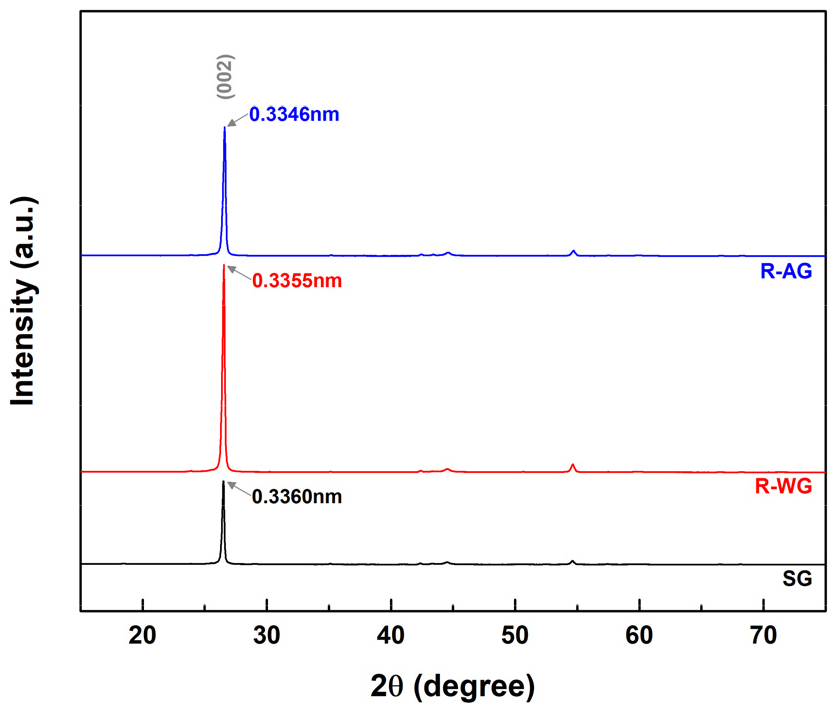
한편, XRD, 라만, XPS 분석을 통해 알칼리 배소가 흑연 구조 회복에도 기여함을 확인하였다. XRD 분석에서 (002) 피크의 강도와 선명도가 향상되었으며(Fig. 8), 아래의 Bragg 법칙에 따라 계산된 면간 거리(d002)는 폐흑연 0.3360 nm에서 R-WG 0.3350 nm, R-AG 0.3346 nm로 감소하여 층간 구조가 회복된 것을 알 수 있었다(상용 흑연 음극재 면간 거리(d002는 0.3354 nm))4).
면간 간격(d002)는 아래의 Bragg 법칙 (1)에 의해 계산된다4).
여기서 λ는 0.15406 nm(Cu Kα radiation), θ는 (002)면에 해당하는 Bragg 각도 값이다.
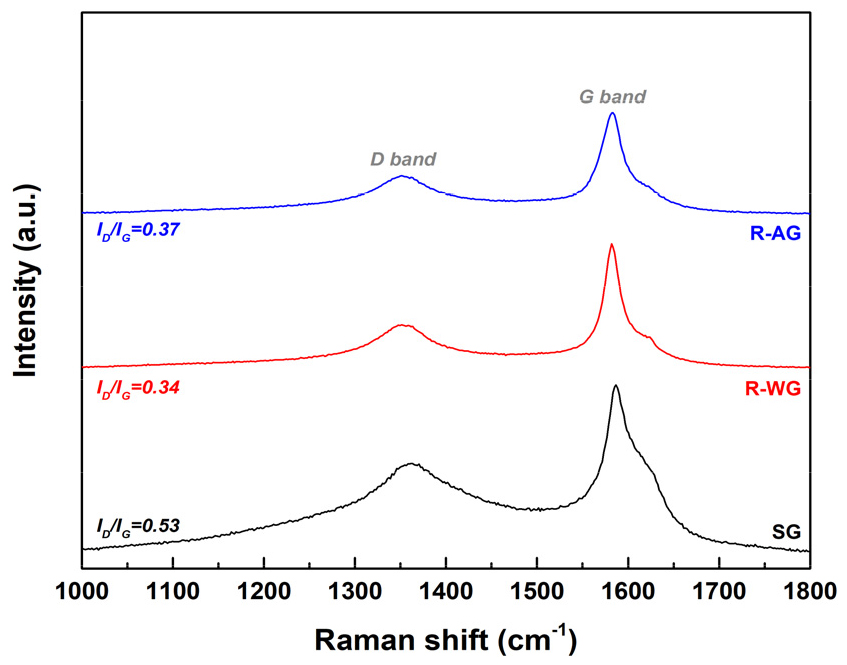
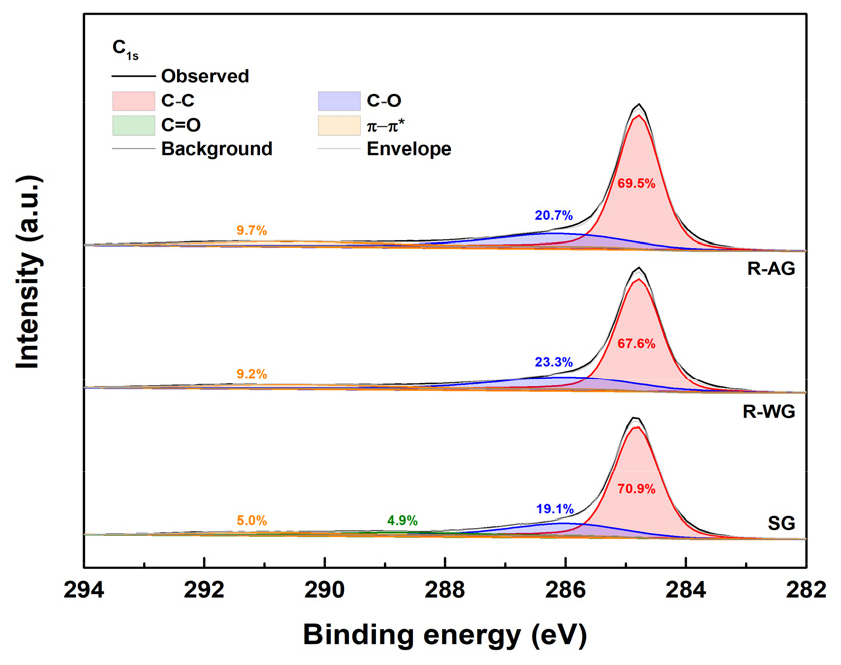
라만 분석(Fig. 9)에서는 ID/IG 비가 폐흑연 0.53에서 R-WG 0.34, R-AG 0.37로 감소하여 결함 밀도가 줄고 결정성이 개선되었음을 확인하였다(상용 흑연 음극재 ID/IG 비는 0.04)4,5,16,17). 또한, XPS C 1s 스펙트럼(Fig. 10)에서는 sp2 결합 영역과 관련된 π-π* 피크 면적 비율이 폐흑연 5.0%에서 RG 시료에서 9% 이상으로 증가하였다. 반대로, 열화에 기인하는 C=O 피크(~288.7 eV)는 사라지고, C–O 피크(~286.0 eV)는 일정 수준(20.7-23.3%)을 유지하였다. 이는 알칼리 배소를 통해 산소계 작용기가 효과적으로 제거되고, 흑연의 sp2 구조가 회복되었음을 뒷받침한다4,6,16,17).
종합하면, Na2CO3 알칼리 배소 공정은 폐흑연의 무기 불순물 제거, 층상 구조 회복, 표면 화학 상태 개선을 동시에 달성할 수 있는 효과적인 방법임을 확인하였다. 이러한 결과는 재생 흑연을 리튬이온전지 음극재로 재활용하는 데 있어 실질적인 가능성을 제시한다. 전략은 불순물 제거, 구조 질서 회복, 표면 제어를 동시에 달성하여, 재생 흑연의 LIB 소재로의 적용에 대한 가능성을 높인다.
3.3. 재생 공정의 경제성 평가
본 연구에서는 제안된 흑연 재생 전략의 경제적 타당성을 검토하기 위하여, 재활용 흑연과 인조흑연을 대상으로 비교 비용 분석을 수행하였다. Fig. 11과 Table 5에 제시한 바와 같이5), 각 공정 단계별 시약 사용량과 열처리에 필요한 에너지 소모량을 기준으로 Na2CO3 배소, NaOH 배소, 그리고 인조흑연 제조 공정을 비교하였다.
Table 5
Economical evaluation with different processes
Process (/1 ton of Carbon) |
Used chemical reagent |
Unit price* ($/kg) |
Quantity used (kg) |
Cost ($) (chemical reagent) |
Processing temperature (°C) |
Amount of heat needed** (kWh) |
Total cost ($/ton) (electricity cost*** = 0.12 $/kWh) |
| In this study | Na2CO3 | 0.228 | 100 | 22.8 | 800 | 168.14 | 42.98 |
| NaOH roasting | NaOH | 0.926 | 100 | 92.6 | 500 | 103.05 | 104.97 |
|
Synthetic graphite | - | - | - | - |
2,800-3,000 (carbonization, coating: 1,000) |
645.21 (carbonization, coating: 211.52) | 77.43 (50.76) |
* Unit price of the chemical reagents from https://stat.kita.net/
인조흑연 제조 공정의 경우, 2,800-3,000 °C에 달하는 고온에서 이루어지는 흑연화(graphitization) 공정이 전체 생산비용의 약 35%를 차지하는 가장 비용 집약적인 단계로 알려져있다5). 이는 극도로 높은 에너지 소비가 요구되기 때문이다. 반면, 재생 흑연의 경우 원료 측면에서 사용되는 폐흑연 자체가 저비용이라는 점과 더불어, 탄화(carbonization) 및 흑연화와 같은 고에너지 공정을 생략할 수 있다는 점에서 공정 단순화와 비용 절감 효과를 동시에 기대할 수 있다.
특히, Na2CO3 배소 공정은 NaOH 배소 대비 시약 단가가 낮아 약 59.0% 수준의 비용 절감 효과를 보였으며, 인조흑연 제조 공정과 비교할 경우에도 약 66.4% 낮은 총 비용을 기록하였다. 이는 주로 공정 온도가 크게 낮아 에너지 소모가 줄어든 결과이다. 이러한 분석을 종합하면, Na2CO3 기반의 재생 공정은 경제성 측면에서도 경쟁력 있는 대안임을 확인할 수 있다.
4. 결 론
본 연구에서는 습식 제련 과정에서 발생한 침출 잔사로부터 회수된 폐흑연을 대상으로, 수침출과 알칼리 배소를 연계한 2단계 정제·재생 공정을 적용하였다. 수침출 단계에서는 잔류 황산염과 전이금속 계열 불순물이 효과적으로 제거되었으며, 이어서 800 °C에서 Na2CO3를 이용한 알칼리 배소를 수행한 결과, Al2O3, SiO2, ZrO2, WO3와 같은 산불용성 성분이 수용성 화합물로 전환되어 잔재 함량이 40% 이상 감소시켰다. XRD, 라만 분광, XPS 분석을 통해 층간 간격 수축, 결함 밀도 저감, π-π* 전이 강도 증가가 확인되어 흑연 구조의 질서 회복 및 sp2 결합 영역의 복원이 이루어진 것을 확인할 수 있었다. 다만, NaAlSiO4 등과 같은 수불용성염이 일부 형성되는 것으로 예상되어 후속 산침출 공정의 필요성도 제기되었다.
이와 같은 결과는 강산이나 불소계 시약을 사용하지 않고도 불순물 제거와 구조 회복, 표면 화학 제어를 동시에 달성할 수 있음을 보여준다. 따라서 본 연구에서 제안한 공정은 경제성 있는 재생 흑연을 리튬이온전지 음극재로 활용할 수 있는 가능성을 제시하며, 향후 순환형 배터리 경제 실현에 기여할 수 있는 유망한 방법으로 평가된다.