1. Introduction
2. Experimental
3. Result and discussion
3.1. Effects of intial pH
3.2. Influence of temperature
3.3. Isotherms
3.4. Kinetic
3.5. Desorption
4. Conclusion
1. Introduction
희유금속은 지각 내 부존량이 적거나 매장량이 많지만 고품위 또는 순수한 금속으로의 추출이 어려운 금속자원으로 현재 산업적인 사용이 있거나 수요의 증가가 예상되는 바나듐, 텅스텐, 몰리브덴, 리튬, 마그네슘, 희토류 등 35종의 금속원소를 말한다.
바나듐과 텅스텐은 희유금속에 속하는 원소들로 바나듐은 철강 및 특수강용으로 합금에 첨가되어 항장력과 내열성을 높이기 위해 사용되거나 촉매의 용도로 석유의 탈유, 알코올 산화 황산제조, 프로필렌수지의 합성, 탈질∙탈황 촉매 등에도 널리 이용되고 있으며, 텅스텐은 금속의 경도 및 내열성이 강하여 합금, 공구강, 전자기기, 화학 원료, 촉매, 무기, 화약 및 금속 그 자체로 산업 전반에 걸쳐 널리 이용되고 있다. 그러나 국내 매장량이 희박하거나 미비하여 자체적인 수급이 어려우며 국내 수요의 대부분을 수입에 의존하고 있다. 따라서 국제 희유금속 공급량이나 국제시세에 매우 민감하여 수급에 어려움을 겪고 있다. 이에 따라 폐기물 등에 함유되어 있는 바나듐 및 텅스텐 원소를 회수하여 이를 재사용 가능한 형태로 재생산 하는 연구가 진행되고 있다. 특히 최근 급격히 발생량이 증가하고 있고 향후 그 발생량이 크게 늘 것으로 예측되고 있는 폐촉매에서 바나듐과 텅스텐 등의 희유금속을 회수하려는 연구가 주목받고 있다. 2015년부터 유로6가 적용됨에 따라 보다 강화된 환경규제로 인하여 자동차용 탈질촉매의 수요 및 폐촉매의 발생량이 크게 증가할 것으로 예상되어 이를 위한 연구의 필요성이 더욱 절실하다.
폐촉매에서 바나듐, 텅스텐과 같은 금속원소는 침전법, 용매추출법, 이온교환 흡착법 등 다양한 방법으로 회수할 수 있다. 침전법에 의한 바나듐과 텅스텐의 회수에 관한 연구로 Luo 등은 tungsten alloy scrap으로부터 86.96%의 ammonium metavanadate와 85~90wt%의 ammonium tungstate를 회수하였다고 보고하였다1). 침전법은 수용액 또는 비수용액 상태에서 침전제를 첨가하여 용액 내 금속이온을 침전시켜 분리하는 방법으로 조작이 간단하고 신속한 반면에 공정 중 여러 가지 원소들이 함께 침전되어 이에 따른 불순물의 처리가 어려워 고순도의 제품을 얻어내지 못하므로 이를 활용한 제품의 성능 및 효율에 좋지 않은 영향을 미치게 되므로 활용분야에 한계성을 가지게 된다. 용매추출법은 금속이온을 함유하고 있는 수용액상에 산성추출제 또는 염기성 추출제 등을 첨가하여 추출 및 분리하는 방법으로 D2EHPA, PC-88A, Aliquat336 등의 산성 추출제와 Alamine336 등의 염기성 추출제가 가장 널리 사용되고 있다. Lozano는 황산염 수용액으로부터 Primene R81과 Alamine 336을 사용한 바나듐 회수 및 추출 특성을 규명하는 연구에서 용액의 pH에 따른 바나듐의 상태에 대하여 보고하였다2). Ahn 등은 Alamine 336을 사용한 바나듐과 티타늄의 용매추출 연구를 통하여 바나듐의 추출거동에 대하여 규명하였는데, pH 1.0에서 40% 정도의 낮은 추출률을 보였지만 2.5 이상으로 유지할 경우 추출률이 96% 이상 증가하고 4.0 이상에서는 99.8%까지 추출이 가능하다고 하였다3). Gerhardt 등은 광석침출액으로부터 텅스텐, 몰리브덴, 레늄을 추출 및 분리하는 연구에서 diisododecylamine(DIDA)을 사용하여 99.9%의 텅스텐을 추출하였다고 보고하였다4). 이러한 용매추출법에 의한 금속이온의 분리 및 회수는 용액의 pH 등의 조건에 따른 추출제 선택의 제약이 있으며, 특정 조건에서 상분리 반응속도가 현저히 저하되고 추출과정에서 발생하는 부유물 및 침전물을 분리하기 어려운 단점을 가지고 있다.
한편 이온교환 수지를 이용한 금속이온의 분리 및 회수는 용액 내 금속이온과 이온교환 수지 사이에서 같은 전하를 가지는 이온들이 가역적인 교환을 하게 되므로 이온의 특성에 따른 분리가 가능하고 용액 내 미량의 금속원소를 선택적으로 분리하거나 용액의 오염 없이 불순물의 제거가 용이한 장점을 가지고 있어 최근 이온교환 수지를 이용한 흡착법이 주목받고 있다. 또한 탈착공정 이후에 재생이 가능하여 재사용에 의한 경제적 측면으로도 유용하며, 흡착 및 탈착을 위한 공정준비과정이 간단한 장점을 가지고 있다.
이온교환 수지를 이용한 연구로 Hu는 molybdate solutiuon으로부터 강염기성 음이온교환 수지 D296을 이용하여 바나듐을 제거하는 흡착실험을 통하여 용액 내 바나듐을 99.5% 제거하였다고 보고하였으며, Ahn 등은 몰리브덴과 텅스텐 혼합용액으로부터 합성 킬레이트 수지를 사용한 흡착실험을 통하여 pH 1~6 범위에서 흡착에 의한 몰리브덴과 텅스텐의 효과적인 분리가 가능함을 보고하였다5,6).
바나듐, 텅스텐 회수에 관한 연구는 선행되어 왔으나, SCR 탈질폐촉매와 같이 바나듐과 텅스텐을 동시에 함유하고 있는 폐기물로부터 이온교환법에 의한 회수 및 분리에 관한 연구는 미비하다. 또한 이온교환 수지를 이용한 바나듐과 텅스텐의 흡∙탈착 메커니즘의 규명과 반응식에 대한 구체적인 연구가 미흡한 실정이다.
따라서 본 연구에서는 SCR 탈질 폐촉매 침출액과 같은 바나듐, 텅스텐 혼합용액으로부터 흡∙탈착 메커니즘을 규명하고 반응에 영향을 미치는 인자들에 대하여 고찰하고자 한다. 본 연구에 사용된 이온교환 수지는 겔 타입의 강염기성 음이온교환 수지로 용액 내 금속이온의 흡착에 효과적인 것으로 알려져 있다.
2. Experimental
이온교환 수지에 대한 바나듐과 텅스텐 이온의 흡착 및 탈착 특성의 규명을 위하여 ammonium metavanadate(SAMCHUN, 99%)와 ammonium tungstate pentahydrate(KANTO, 90%)를 증류수에 용해시켜 모의용액을 제조하였다. 반응기는 회분식 실험을 위해 50mL conical tube 및 250mL pyrex 반응조를 사용하였으며, HCl 및 NaOH 수용액을 이용하여 용액의 산도를 조절하였다.
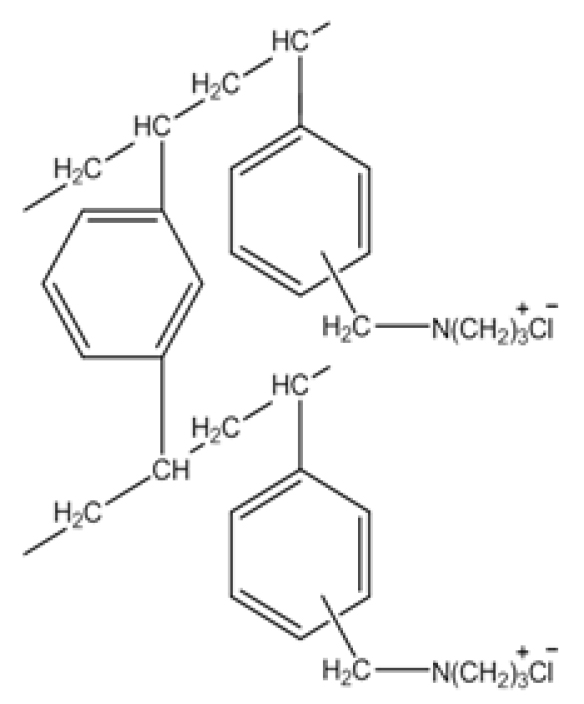
흡착실험에 사용된 이온교환 수지는 Cl-기를 교환기로 갖는 겔 타입의 음이온교환 수지 Lewatit Monoplus M600(Lanxess, Germany)으로, 분자식은 Fig. 1과 같으며 물리∙화학적 특성은 Table 1에 나타내었다.
Table 1.
The physical and chemical characteristics of Lewatit monoplus M600
이온교환 수지에 대한 바나듐 및 텅스텐 이온의 흡∙탈착 특성을 평가하기위해 ammonium metavanadate와 ammonium tungstate pentahydrate를 증류수에 용해시켜 혼합한 모의용액을 사용하여 용액의 흡착평형실험, 흡착속도실험을 진행하였으며, 흡착을 마친 이온교환 수지를 수거하여 HCl 및 NaOH의 몰농도에 따른 탈착실험을 진행하였다.
흡착평형실험은 항온진탕기를 이용한 회분식 실험으로 진행되었으며, 이온교환 수지의 첨가량을 고정하고 용액의 초기산도에 따른 흡착률 비교실험 및 흡착질의 농도에 따른 등중량 흡착등온실험을 진행하였다. 용액의 초기산도에 따른 흡착률 비교실험은 바나듐, 텅스텐 각각 500mg/L 농도의 모의용액 50mL를 각각 pH 1.0~13.0으로 적정한 후 이온교환 수지 0.3g을 첨가하고 303K, 200rpm에서 24시간 교반하여 실시하였다. 흡착등온실험은 50~500mg/L 농도의의 바나듐 및 텅스텐 이온을 함유하는 모의용액에 이온교환 수지 0.5g을 첨가하여 303K, 200rpm에서 24시간 교반하여 진행하였다.
흡착속도실험은 바나듐, 텅스텐 각각 500mg/L 농도의 모의용액 100mL에 이온교환 수지 0.5g을 첨가하여 1~1440분 동안 교반하여 각 시간별로 시료를 채취하는 방법으로 실시하였다.
탈착실험은 탈착용액의 초기산도 및 HCl과 NaOH의 농도에 따른 탈착능 평가실험을 진행하였다. 탈착실험을 위해 바나듐, 텅스텐 각각 500mg/L 농도의 모의용액에 이온교환 수지 0.5g을 첨가하고 24시간 교반하여 최대흡착에 도달한 이온교환 수지를 수거하여 세척∙건조시켜 준비된 이온교환 수지에 1M, 2M, 3M의 HCl 및 NaOH 수용액 100mL를 각각 첨가하고 303K, 200rpm에서 1~240분 동안 교반하여 각 시간별로 시료를 채취하는 방법으로 실시하였다.
이온교환 수지에 의한 바나듐, 텅스텐 이온의 흡착량은 흡착반응 종료 후 잔류 바나듐, 텅스텐의 농도를 측정하고 이를 용액의 부피 및 이온교환 수지의 첨가량에 대하여 식 (1)을 이용하여 도출하였다.
여기서 는 흡착평형 상태에서 흡착제 단위질량(g)당 흡착된 흡착질의 양(mg/g), 는 흡착질의 초기농도(mg/L), 는 흡착질의 평형농도(mg/L), 는 흡착질을 함유하는 용액의 부피(L), 는 첨가된 흡착제의 투여량(g)을 나타낸다. 용액 내 바나듐과 텅스텐 이온의 농도는 ICP-OES(Optima 2000 DV, Perkinelmer)를 사용하여 측정하였다.
3. Result and discussion
3.1. Effects of intial pH
용액의 초기산도는 회분식 반응기에서의 흡착공정에서 용액 내 금속이온의 형태 또는 흡착제의 흡착 성능에 매우 중요한 영향을 미치는 변수로 작용한다. 이온교환 수지의 가용 pH 범위 내에서 최적의 흡착환경을 조성하여 성능의 최적화를 이루어 낼 수 있으며 용액의 산도에 따른 금속이온의 결합형태 또한 흡착반응에서 큰 변수로 작용하게 된다. 회분식 반응기에서는 흡착반응 중 용액의 pH가 변함에 따른 상태변화에 대하여 이를 조절하기 어렵다. 따라서 용액의 초기산도가 흡착성능에 미치는 영향을 규명하기 위하여 초기산도를 pH 1.0~13.0, 바나듐과 텅스텐의 농도 500mg/L의 혼합용액 50mL에 이온교환 수지를 0.3g 첨가하여 실험을 진행하였다. 용액의 pH 조절을 위해 HCl과 NaOH 수용액을 사용하였다.
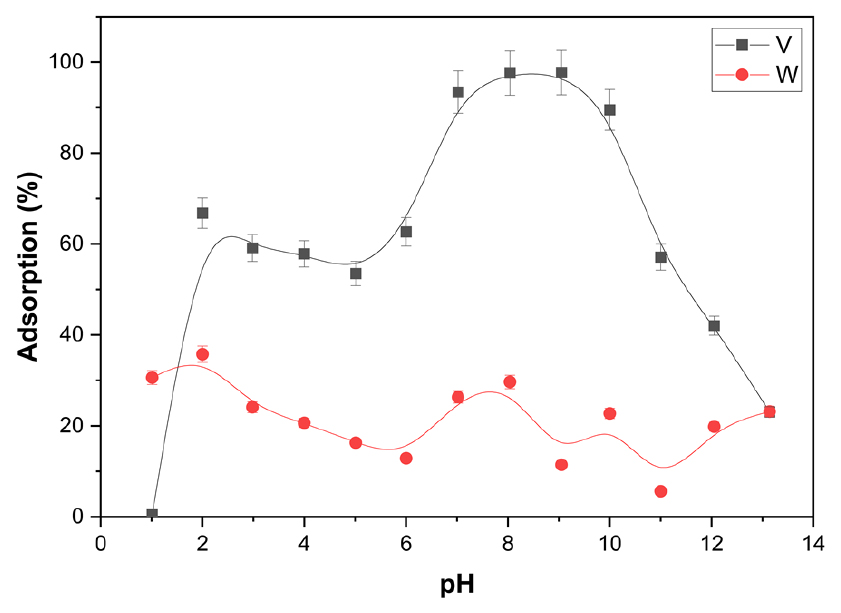
Fig. 2와 같이 용액의 초기산도에 따른 바나듐과 텅스텐의 흡착거동은 상이하게 나타났다. 바나듐은 용액의 초기산도에 따른 흡착거동의 편차가 크게 나타났으나 텅스텐은 흡착거동의 편차가 크지 않았다. 바나듐은 pH 1.0 및 2.0에서 흡착이 거의 이루어지지 않는 것을 알 수 있으며, 두 이온 모두 pH 6.0 이상에서 흡착률이 감소하며, 강염기성 환경에서는 흡착률이 크게 감소하는 것을 알 수 있다. 바나듐은 pH에 따른 이온의 형태가 달라지는데, pH 1.5 미만에서 양이온으로 존재하며, pH 1.5이상에서 음이온의 형태로 존재하여 pH 2.0~10.0에서 이온교환 수지에 흡착이 용이한 안정한 형태의 음이온으로 존재하는 것으로 판단된다. 텅스텐은 모든 pH 영역에서 낮은 흡착률을 나타내었다. 일반적으로 텅스텐은 용액의 산성도가 증가함에 따라 여러 가지 형태의 폴리옥소메탈레이트(polyoxometalate) 음이온을 형성하는데 pH 1.0~2.0에서는 [W10O32]4-, pH 2.0~4.0에서는 [H2W12O40]6-, pH 5.0~9.0에서는 [W7O24]6-, [H2W12O42]10-와 같은 형태로 존재하며 pH 1.0 미만의 강한 산성에서는 WO3∙2H2O로 침전이 된다7). 이러한 형태 변화로 인해 산성 용액에서의 텅스텐의 흡착률이 증가하나 다공성 타입의 이온교환 수지에 비해 비표면적이 작은 겔 타입의 이온교환 수지에서는 영향을 미치지 않는 것으로 사료된다.
3.2. Influence of temperature
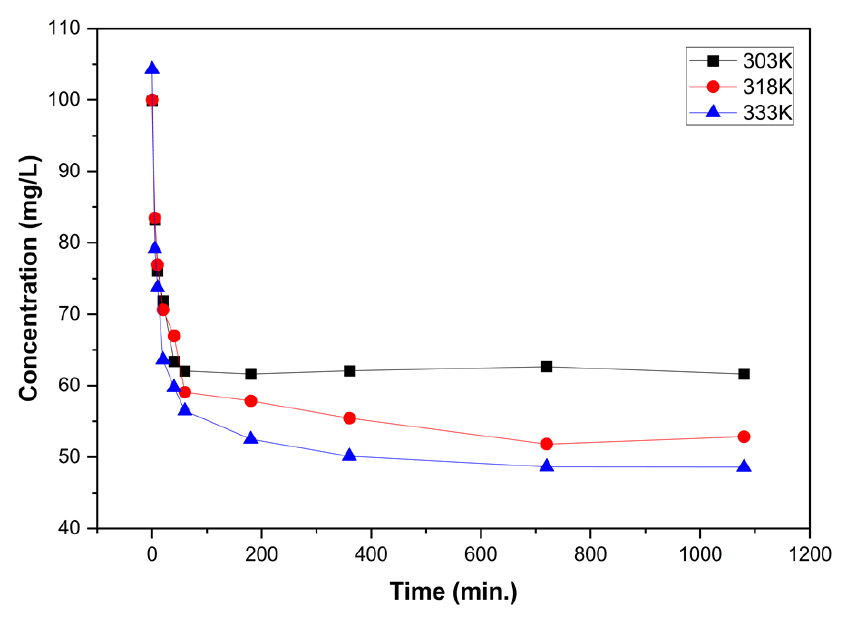
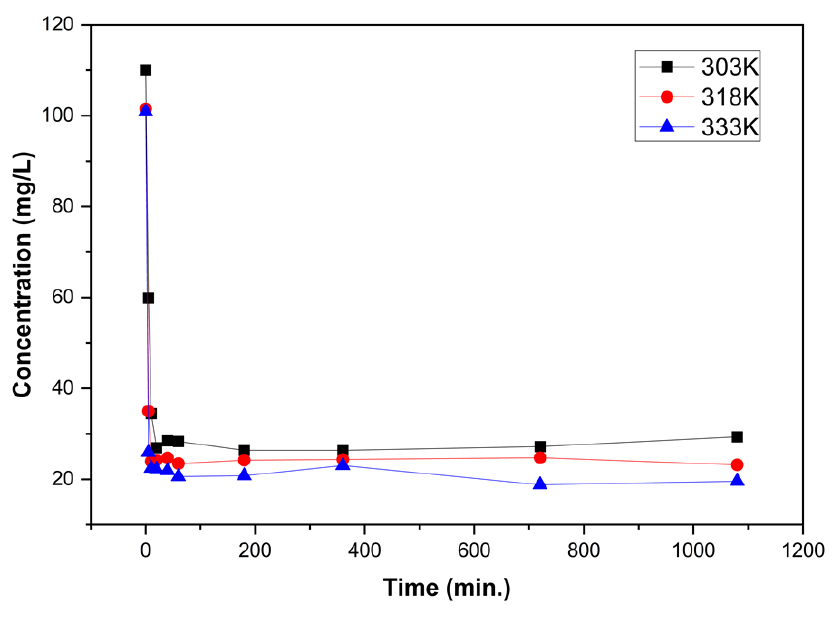
흡착반응에서 반응온도는 반응속도 및 최대흡착량 등에 영향을 미치는 변수로 작용한다. 반응온도는 용액 내 흡착질의 활성화 에너지를 상승시켜 흡착제와의 반응속도를 증가시켜준다. 303, 318, 333K의 반응온도에서 실시된 실험에서 Figs. 3, 4과 같이 온도상승에 따라 반응속도와 최대흡착량이 증가하는 것으로 나타났다. 그러나 반응속도의 증가는 흡착평형에 도달하기 전 흡착량의 증가에는 영향을 미쳤으나 평형에 도달하는 시간에는 큰 차이가 나타나지 않았다. 이는 반응온도가 증가함에 따라 흡착속도가 증가하였으나 최대흡착량의 차이로 인하여 흡착평형에 도달하는 시간의 차이가 미미하게 나타난 것으로 사료된다.
3.3. Isotherms
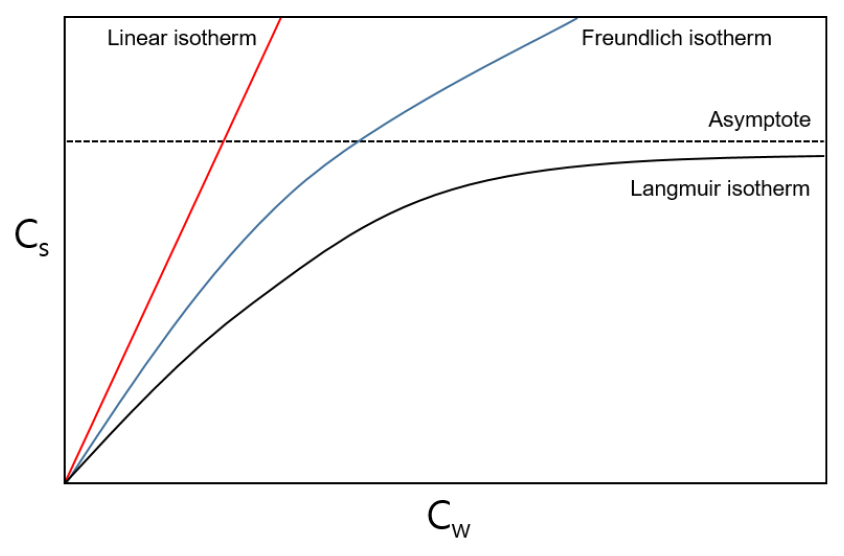
흡착질에 대한 흡착제의 흡착평형특성을 기반으로 하여 다양한 형태의 흡착등온식에 적용함으로써 흡착 매커니즘을 규명할 수 있는 식으로 흡착제에 의하여 제거되는 흡착질의 양을 나타낼 수 있는 Langmuir 및 Freundlich 흡착등온모델 등이 있으며, Fig. 5과 같이 흡착등온선의 형태에 따라 Langmuir형과 Freundlich형을 구분할 수 있다. Langmuir와 Freundlich 흡착등온식은 Table 2와 같이 표현된다.
Langmuir 흡착등온식은 흡착질 표면에 흡착질이 단분자층을 형성하며 흡착이 이루어지는 것을 가정하며, 는 흡착평형 상태에서 흡착제 단위질량(g)당 흡착된 흡착질의 양(mg/g), 는 흡착질의 평형농도(mg/L)를 나타내며, 와 는 흡착용량과 흡착속도와 관련된 Langmuir 상수이다.
Freundlich 흡착등온식은 흡착제 표면이 불균일한 표면에너지를 가지고 흡착된 금속이온 사이의 인력에 의해 다분자층으로 흡착이 이루어지는 것을 가정하며, 는 흡착질의 평형농도(mg/L), 는 흡착제 단위질량(g)당 흡착된 흡착질의 양(mg/g), 와 은 흡착공정의 적합도를 나타내는 상수로, 는 흡착용량, 은 기울기 값으로 0~1의 범위에서 흡착강도 및 불균일성을 나타내며 불균일성이 높아질수록 0에 가까워진다.
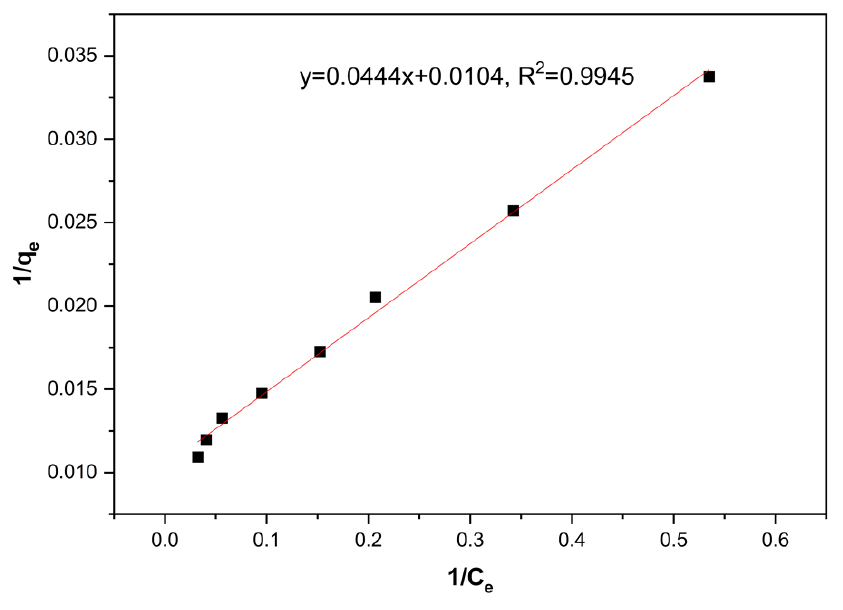
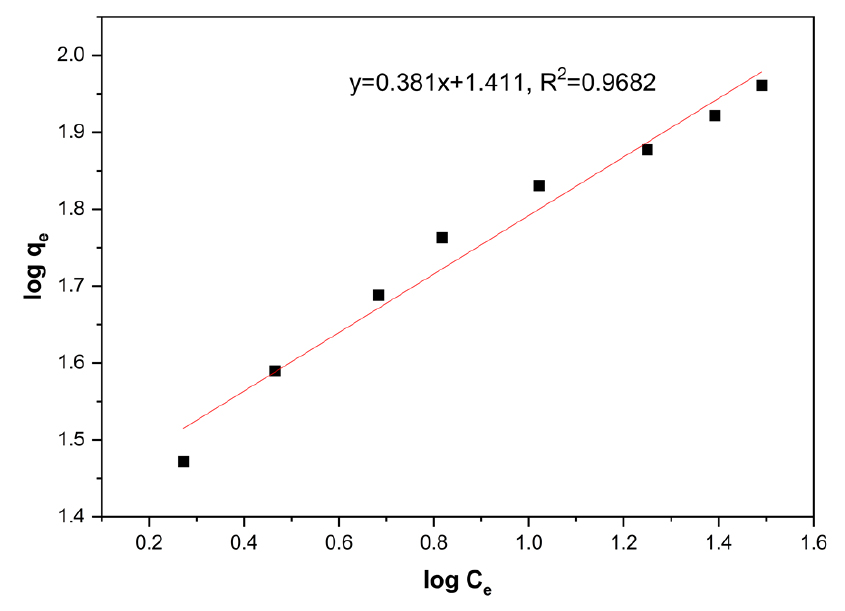
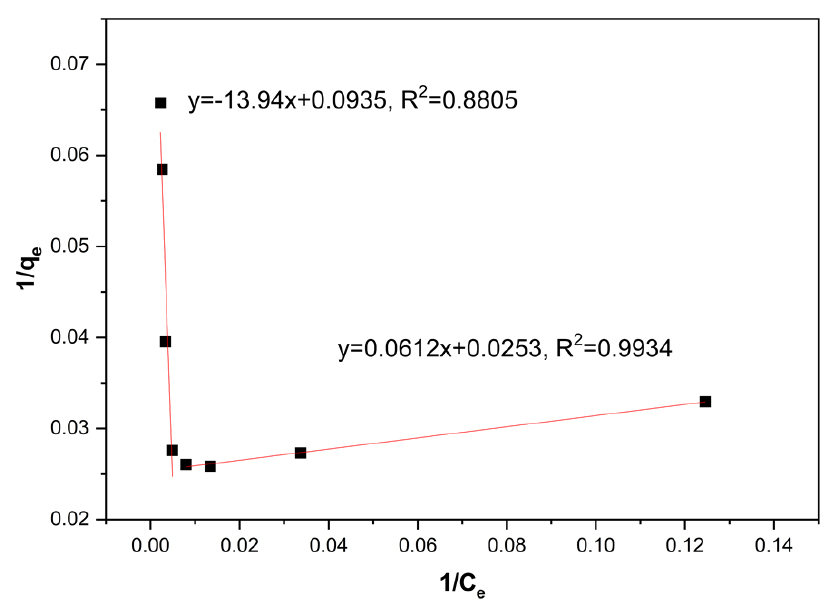
Langmuir 흡착등온선과 Freundlich 흡착등온선을 각각 Figs. 6, 7, 8, 9에 도시하였으며, 각각의 흡착등온식에 따른 상수 값을 Table 3에 나타냈다.
Table 3.
Langmuir and Freundlich isotherm constant
| Langmuir | Freundlich | |||||
| q(mg/g) | b(L/mg) | R2 | KF ((mg/g) (L/mg)1/n) | 1/n | R2 | |
| V | 96.15 | 0.234 | 0.9945 | 25.763 | 0.381 | 0.9682 |
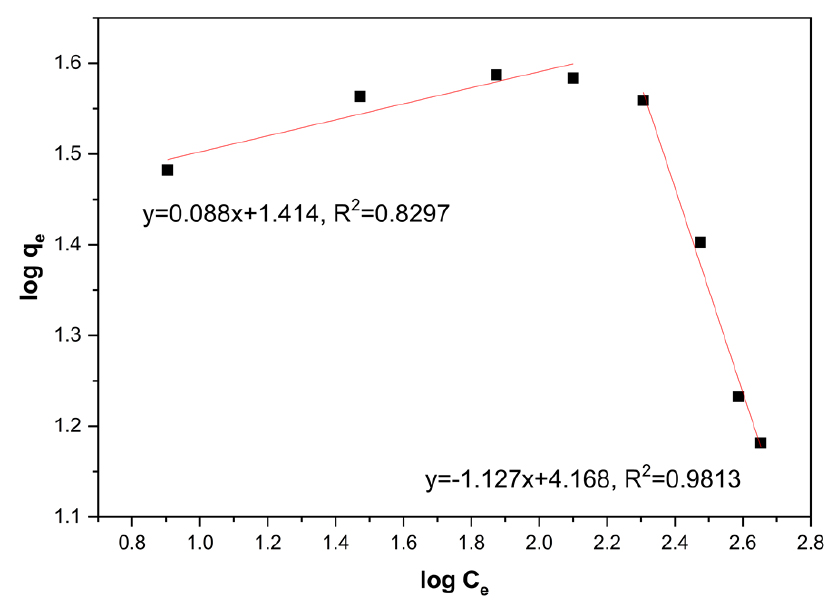
| W | 39.53 | 0.413 | 0.9934 | 25.942 | 0.088 | 0.8297 |
음이온교환 수지에 의한 바나듐 텅스텐 이온의 등온흡착실험을 통하여 Langmuir와 Freundlich 흡착등온식의 적합도를 분석한 결과 바나듐의 Langmuir 흡착등온식 상관계수는 0.9945, Freundlich 흡착등온식 상관계수는 0.9682이며, 텅스텐의 Langmuir 흡착등온식 상관계수는 0.9934, Freundlich 흡착등온식 상관계수는 0.8297로 두 이온 모두 Langmuir 흡착등온식에 더 적합한 것으로 나타났다. 바나듐의 경우 Freundlich 흡착등온식에도 따르는 특성이 나타났는데, 이는 겔 타입의 흡착제를 구성하는 망상구조의 가교 내부에서 바나듐 이온의 응축이 나타나는 것으로 사료된다. 텅스텐 이온은 다공성 타입의 이온교환 수지를 이용한 연구에서 텅스텐 이온의 흡착등온선이 Freundlich 흡착등온식 형태를 따르는 경향을 나타내었으나 겔 타입의 이온교환 수지에서는 나타나지 않았는데, 이는 겔 타입 이온교환 수지의 망상구조에 의한 micro pore에는 텅스텐 이온의 침투가 이루어지지 않고, 다공성 타입 흡착제 내부의 macro pore 내에서 텅스텐이온의 침투 및 폴리옥소메탈레이트화에 의한 응축반응의 영향으로 흡착제 내부로의 사료된다. 텅스텐 이온은 용액의 산도에 따라 여러 가지 형태의 폴리옥소메탈레이트를 형성하게 되는데, Eh-pH diagram에 따르면 용액의 염기도가 증가할수록 WO42-의 용액 내 비율이 증가하며, pH 1~2에서는 [W10O32]4-, pH 2~4에서는 [H2W12O40]6-, pH 5~9에서는 [W7O24]6-와 [H2W12O42]10-가 생성되며, 강한 산성일 경우에는 WO3∙2H2O로 침전된다7).
Langmuir 흡착등온식에 의한 공정 적합성 여부는 Hall 등이 제안한 분리계수()의 분포에 따라 판단할 수 있는데, R > 1은 부적합, R = 1은 선형(linear), R = 0일 때 비가역이며, 0 < R < 1일 때 적합한 것으로 알려져 있다8,9,10,11).
본 실험에서 얻어진 Table 3의 결과 값을 식 (2)에 적용한 결과 바나듐은 0.2731, 텅스텐은 0.1723으로 나타났다. 결과 값에 의하면 모두 Langmuir 흡착등온식에 적합한 것으로 나타나나 용액 내 금속이온간의 친화력 등에 의하여 흡착특성에 차이가 나타나는 것으로 사료된다.
Freundlich 흡착등온식에 의한 공정 적합성 여부는 Fukukawa가 제시한 1/n값의 분포에 따라 판단할 수 있는데, 1/n의 값이 0.1~0.5일 때 효과적인 흡착이 가능하다고 하였다. 본 실험에서는 바나듐의 1/n 값은 0.381로 Fleundlich 흡착등온선에 적합한 것으로 나타났으며, 텅스텐의 1/n 값은 0.088로 Freundlich 흡착등온식에 적합하지 않은 것을 알 수 있다12,13).
3.4. Kinetic
흡착 반응속도식은 이온교환 수지에 대한 바나듐과 텅스텐 이온의 흡착 반응속도를 정량적으로 분석하기 위한 것으로 유사 1차 반응속도모델(pseudo-first-order) 및 유사 2차 반응속도모델(pseudo-second-order)을 사용하였다. 유사 1차 반응속도모델은 수용액 상에서 흡착제와 흡착질간의 반응속도와 평형상태에서의 흡착량과의 관계를 규명하기 위한 가장 널리 사용되고 있는 반응속도식으로 다음과 같다.
식 (3)은 선형화를 통해 다음과 같이 정리할 수 있다.
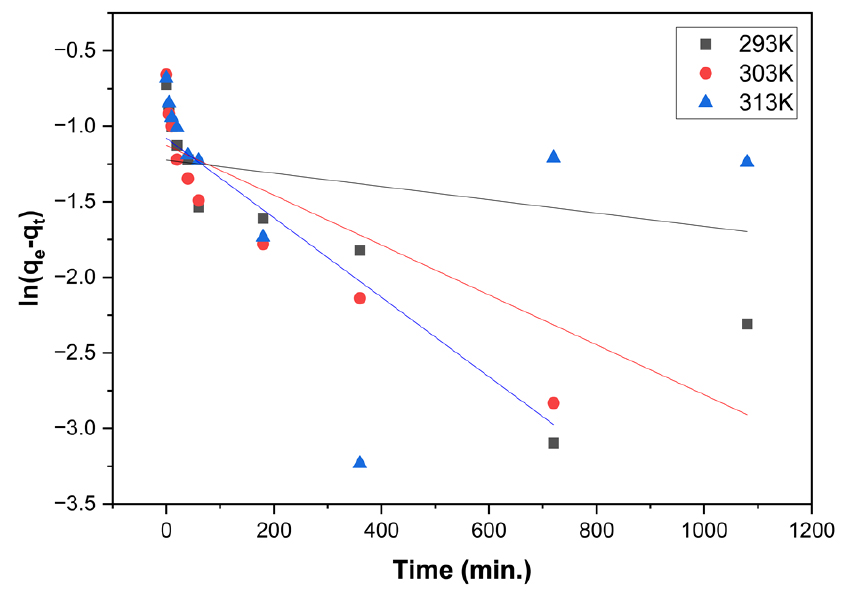
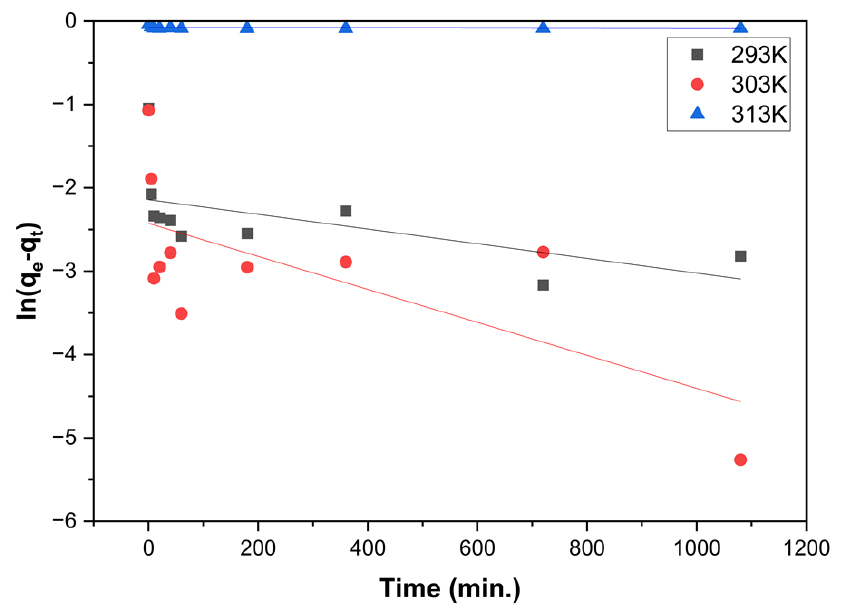
여기서, 은 1차 반응속도 상수(min-1), 는 흡착평형 상태에서 흡착제 단위질량(g)당 흡착된 흡착질의 양(mg/g), 는 반응시간 에서 흡착제 표면에서의 흡착량(mg/g), 는 시간(min)을 나타낸다. 흡착속도실험에서 얻어진 값을 식 (5)에 적용하여 Figs. 10, 11에 나타내었으며, 직선식으로부터 산출한 , 및 값을 Table 4에 나타내었다.
Table 4.
Pseudo-1st-order and pseudo-2nd-order rate constant
유사 2차 반응속도모델은 고체상에서 흡착평형능력을 바탕으로 Ho와 Mckay에 의해 다음과 같은 식으로 제시되었다14).
식 (6)은 선형화를 통해 다음과 같이 정리할 수 있다.
여기서, 는 2차 반응속도 상수(g/mg∙min), 는 흡착평형 상태에서 흡착제 단위질량(g)당 흡착된 흡착질의 양(mg/g), 는 반응시간 에서 흡착제 표면에서의 흡착량(mg/g), 는 시간(min)을 나타낸다.
위 직선식의 기울기와 절편으로부터 , 및 값을 구할 수 있으며, 여기서 (mg/g∙min)는 흡착반응에서의 초기 흡착률로 다음 식 (8)과 같다.
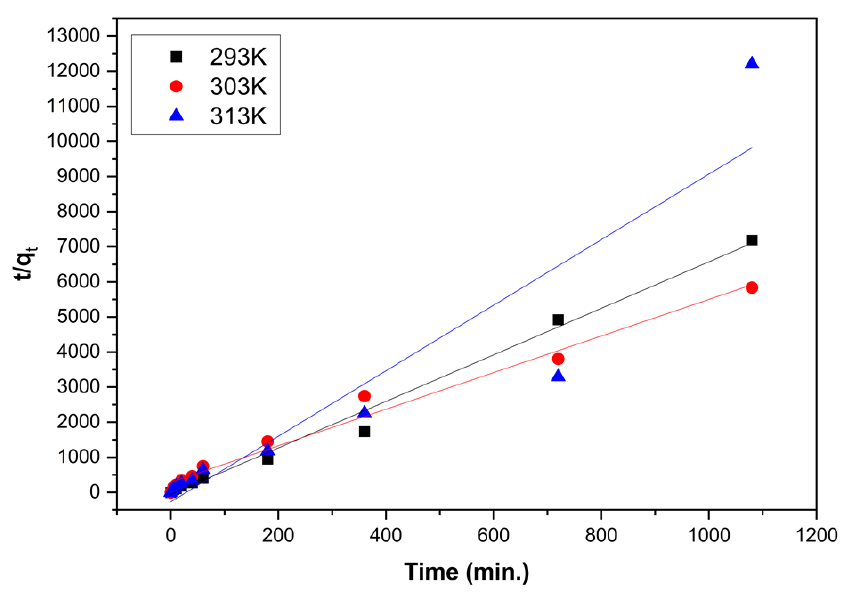
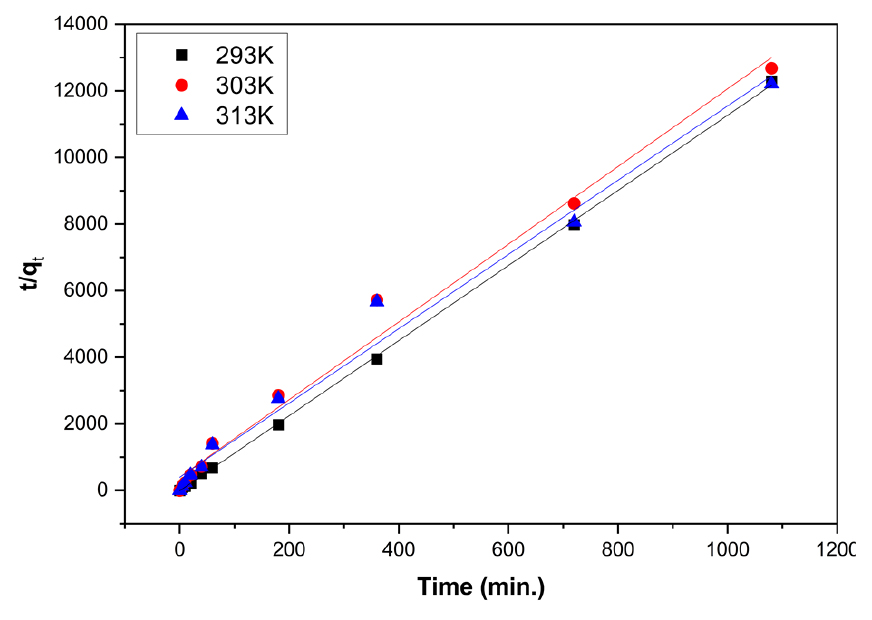
흡착속도실험의 결과를 식 (7)에 적용하여 Figs. 12, 13에 나타내었으며, 직선식으로부터 산출한 , , 및 값을 Table 4에 나타내었다.
Table 4에서 유사 1차 반응속도식과 2차 반응속도식으로부터 얻은 평형흡착량 와 실제 실험을 통하여 얻은 평형흡착량 를 비교하였을 때, 유사 2차 반응속도식으로부터 얻은 에 보다 근사 값으로 일치하는 것을 알 수 있으며, 또한 유사 2차 반응속도식에 적합한 것을 알 수 있다.
3.5. Desorption
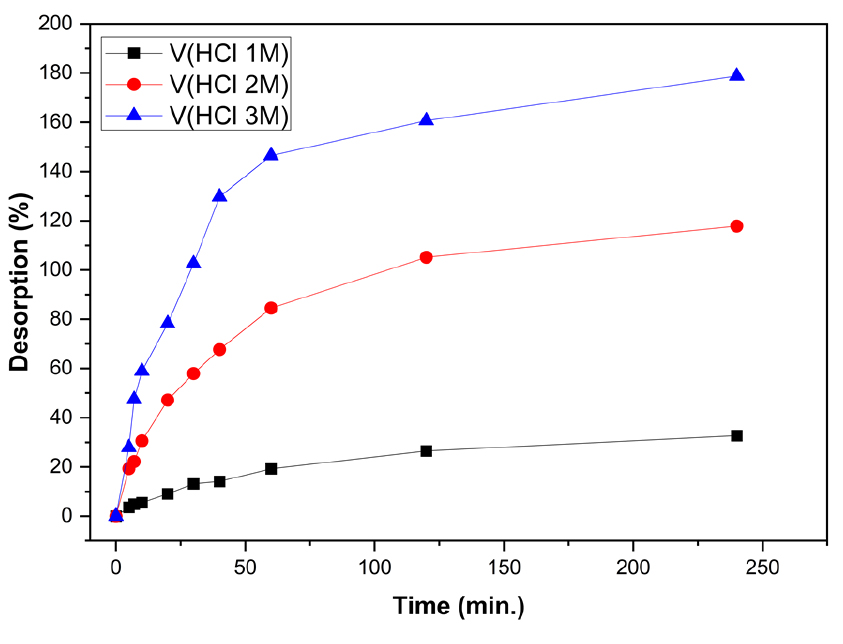
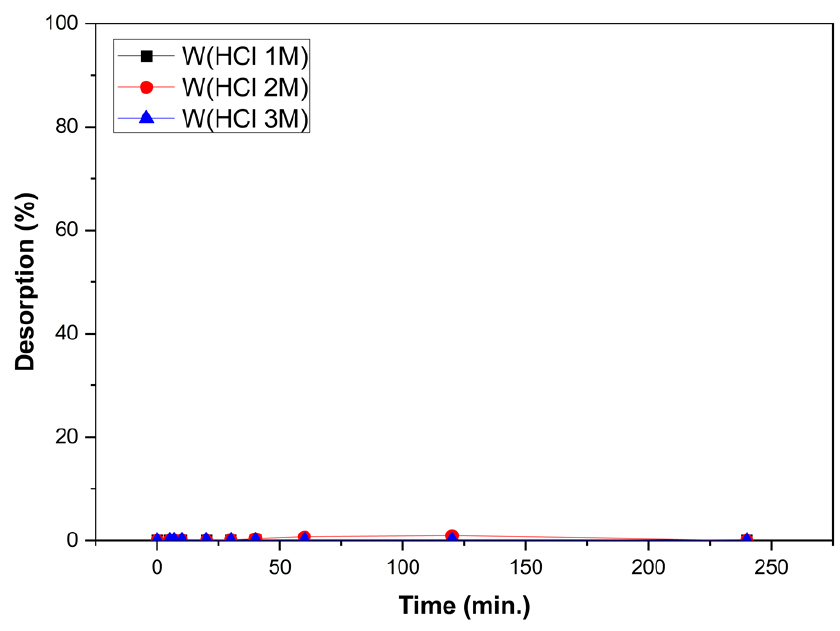
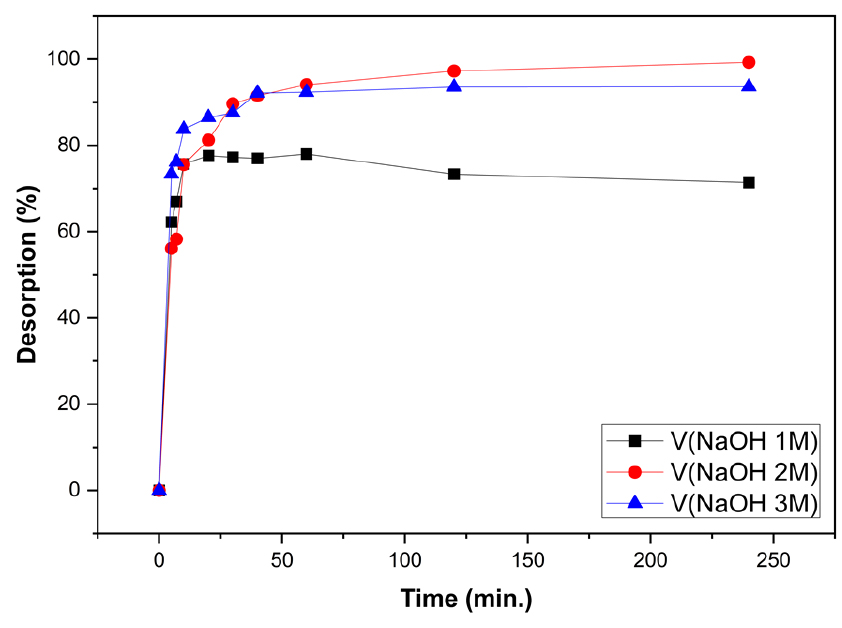
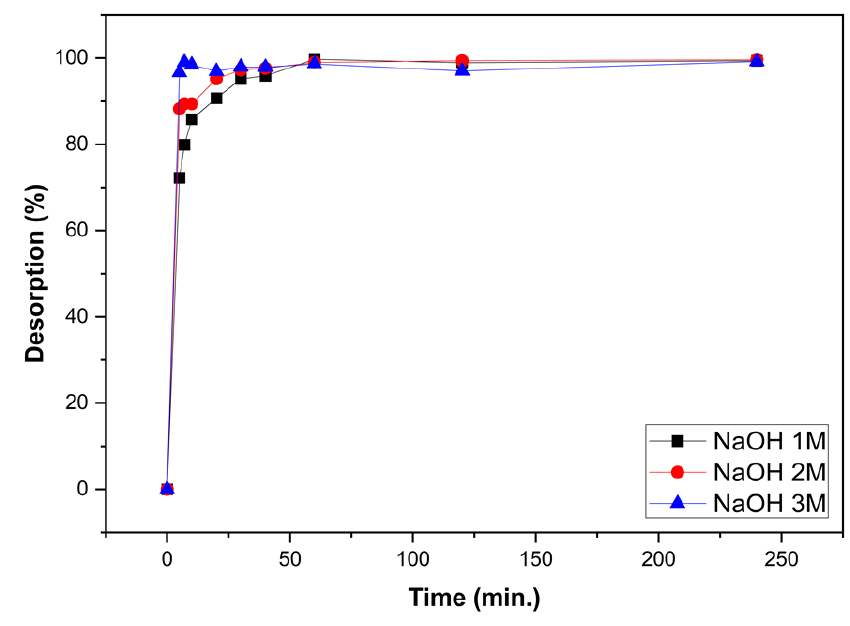
탈착용액의 종류 및 농도에 따른 탈착률 비교를 위하여 각각 1M, 2M, 3M의 HCl 및 NaOH 수용액을 사용한 탈착실험을 진행한 결과를 Figs. 14, 15, 16, 17에 도시하였다. HCl 수용액에서 바나듐 이온은 농도의 증가에 따른 탈착률의 증가가 확연히 차이가 나타나며 탈착반응 개시 후 60분 까지 빠르게 탈착이 이루어지고 이 후 속도가 감소하는 경향을 나타내었다. 그러나 HCl 수용액에서 텅스텐 이온의 탈착률은 극히 미미하였다. NaOH 수용액에서 바나듐과 텅스텐 이온 모두 반응개시 30분 까지 빠르게 탈착이 이루어졌으며, 60분 이후 평형에 도달하였다. 텅스텐 이온은 NaOH 수용액의 농도증가에 따른 탈착률과 속도에서 큰 차이를 보이지 않았으나 바나듐은 농도에 따른 탈착률의 차이를 보였으며, 특히 2M의 NaOH 수용액에서 가장 탈착이 잘 이루어 지는 것으로 나타났다. 이는 두 이온의 용액의 초기산도에 따른 흡착특성과 연관이 있는 것으로 사료되는데, 바나듐은 pH 1.0의 강산성 및 pH 13.0의 강염기성에서 흡착률이 크게 낮아졌으며, 텅스텐은 pH 13.0의 강염기성에서 흡착률이 매우 낮게 나타났다. 이와 같은 바나듐과 텅스텐의 탈착 특성을 이용하여 두 이온의 완전한 분리가 가능함을 규명하였다.
4. Conclusion
바나듐과 텅스텐 이온의 혼합용액으로부터 겔 타입의 음이온교환 수지를 이용한 초기산도, 흡착등온실험, 반응온도실험, 반응속도실험 등을 통하여 흡착특성을 규명하였다. 또한 탈착실험을 통하여 바나듐과 텅스텐 이온의 탈착 특성 및 분리 조건을 규명하였다.
용액의 초기산도가 흡착에 미치는 영향을 비교하기 위한 실험에서 바나듐은 산도 또는 염기도가 강할수록 흡착률이 낮았는데, 특히 pH 1.0의 강산성 및 pH 13.0의 강염기성에서 흡착률이 크게 낮아졌으며, 텅스텐은 겔 타입의 이온교환 수지에서는 다공성 타입의 이온교환 수지에 비하여 흡착률이 크게 낮은 것으로 나타났고, 염기도의 증가에 따라 흡착이 감소하는 경향을 보이며 pH 13.0의 강염기성에서 흡착률이 매우 낮게 나타났다. 반응온도가 흡착반응에 미치는 영향은 293, 303, 313K의 반응온도에서 실시된 실험에서 바나듐은 온도상승에 따라 반응속도와 최대흡착량이 증가하는 것으로 나타났으나 흡착평형에 도달하기 전 흡착량의 증가에는 영향을 미치지만 평형에 도달하는 시간에는 큰 차이가 나타나지 않았다. Langmuir 및 Freundlich 흡착등온식에 적용한 흡착등온실험의 결과 바나듐과 텅스텐 모두 Langmuir 흡착등온식에 잘 부합하는 것으로 나타났는데, 바나듐의 경우 Freundlich 흡착등온식에도 따르는 특성이 나타났다. 이는 겔 타입의 흡착제의 망상구조 가교 내부에서 바나듐 이온의 응축으로 인하여 나타나는 것으로 사료된다. 유사 1차 반응속도모델(pseudo-first-order)과 유사 2차 반응속도모델(pseudo-second-order)에 적용한 반응속도실험 결과 두 이온교환 수지 모두에서 유사 2차 반응속도모델에서 잘 모사되는 것을 알 수 있었으며, 이론값과 실험값이 거의 일치한 것으로 나타났다. 탈착용액의 종류 및 농도에 따른 탈착특성실험에서 바나듐은 HCl 수용액과 NaOH 수용액 모두 탈착이 이루어졌고, 텅스텐은 NaOH 수용액에서만 탈착이 이루어졌다. 따라서 탈착용액에 따른 바나듐과 텅스텐의 탈착특성을 이용하여 두 이온의 완전한 분리가 가능하며, 탈착용액의 농도가 증가할수록 탈착률 또한 증가하는 것을 알 수 있었다. 또한 탈착반응 개시 후 30분 이내에 평형에 도달하여 90% 이상의 회수가 가능함을 규명하였다.