1. Introduction
탄소 중립을 위해 전 세계적으로 전기자동차의 보급률은 증가하고 있으며, 국제에너지기구(IEA, International Energy Agency)의 통계 자료에 따르면 전 세계 전기자동차는 2010년 약 1만 4천대에서 2019년 716만 7천대까지 연평균 약 116.3% 증가하였다1). 이러한 전기자동차의 핵심 부품인 배터리는 높은 에너지 밀도, 빠른 충방전 속도 및 고온과 저온에서의 안정적인 성능 등의 장점으로 리튬이온배터리가 주로 채택되고 있다2). 리튬이온배터리의 종류는 양극의 구성에 따라 NCM(니켈코발트망간), LFP(리튬인산철), LCO(리튬코발트산화물), LMO(리튬망간산화물) 등이 있으며, 기존에는 배터리의 용량 및 주행가능 거리 등을 고려하여 3원계인 NCM 배터리가 주를 이루었다. 최근 안정적인 원자재 공급 및 낮은 생산 비용 대비 우수한 성능으로 LFP계 배터리에 대한 수요도 증가하고 있는 실정이다3,4). Electric Vehicle Tank의 발표 자료에 의하면 전 세계 LFP 배터리 출하량 비중은 2020년 18.3%에서 2021년 30.6%(172.1 Gwh)로 급증해 급속한 확대 추세를 예상하고 있다5,6). 이처럼 기존에 많이 채택되던 NCM 배터리의 재활용 기술은 많은 연구가 진행된 바 있지만, 아직 LFP 배터리의 재활용 기술에 대한 연구는 미비하다6,7,8,9).
LFP 배터리 재활용 시 가장 경제적으로 가치 있는 원소는 리튬이며, 높은 회수율로 얼마나 효율적으로 회수할 수 있는가가 중요하다. 크게 건식제련, 습식제련 및 환경친화적 방법인 기계화학적 방법, 전기화학적 방법으로 분류가 가능하다. 먼저, 건식제련을 통해 리튬을 휘발시켜 더스트 형태로 회수하는 경우 높은 에너지 소비와 탄소 배출이 문제가 될 수 있으며, 회수 효율은 Holzer et al.(2021)의 연구에 의하면 건식제련을 통해 리튬을 약 68.4% 휘발시켜 회수하였다10).
또한 산업에서 많이 시행되고 있는 다단의 습식 제련은 침출과 침전 반응으로 이루어지며 공정 도중 리튬이 손실되어 손해가 발생할 수 있으며 폐수 처리가 필요하다11). Zheng et al.(2016) 연구에 의하면 고액비 100 g/L로 60℃에서 4시간 동안 황산을 사용하여 리튬 약 97%, 철 약 98% 침출하여 Li2CO3 및 FePO4·H2O 형태로 회수하는 연구를 수행하였다12). 또한 Huang et al.(2016)은 염산과 과산화수소를 첨가하여 고액비 200 g/L 및 반응온도 60℃ 조건으로 2시간 동안 리튬 약 92%, 철 약 97% 침출하여 인산리튬(Li3PO4) 및 염화철(FeCl3) 형태로 회수하였다13).
최근 이러한 습식제련의 무기산 사용양을 줄여 환경 부하를 감소시키기 위한 기계화학적 및 전기화학적 방법을 사용하여 리튬을 회수하고자 하는 연구도 수행되고 있다14,15). 기계화학적 방법은 화학 반응 시 전단, 마찰, 충격 등 기계적 힘을 추가하여 물리적/화학적 특성 변화를 유도한다. 주로 옥살산과 같은 유기산, Na2EDTA와 같은 킬레이트제, 염화나트륨 등을 사용하여 LFP 배터리로부터 리튬을 추출한다. 전기화학적인 방법에는 이온교환 및 전기투석이 해당된다16,17). 전기화학적 방법은 화학 시약을 사용하지 않아 자연친화적이지만 고가인 이온교환막과 유지 및 보수가 번거로운 단점이 있다.
이에 본 연구에서는 이전 연구18) 결과를 기반으로 리튬을 폐LFP 양극재로부터 선 추출하기 위해 무기산이 아닌 과황산계산화제 과황산나트륨을 사용하여 선택적으로 리튬만 침출시키고자 하였으며, 이에 일반적인 침출 방법에서는 고액비의 영향을 확인하였으며, 기계화학적 침출 방법에서는 과산화수소의 영향을 확인하여 두 메커니즘에 대하여 리튬의 선침출 효율을 비교하고자 하였다.
2. Experimental
폐LFP(Lithium iron phosphate) 양극재를 전단응력을 사용하여 파쇄 후 -150 μm로 분급한 블랙파우더(Black powder)를 원료로 사용하였다. Fig. 1과 같이 +1,000 μm, -1,000+500 μm, -500+150 μm, -150 μm으로 4개의 구간으로 분급하였으며, 알루미늄 박판의 기계적 특성으로 인해 구겨지며 상대적으로 큰 입도 구간인 +1,000 μm 구간에 밀집되었다. 이에 본 연구에서는 -150 μm 구간의 블랙파우더를 원료로 사용하였다.
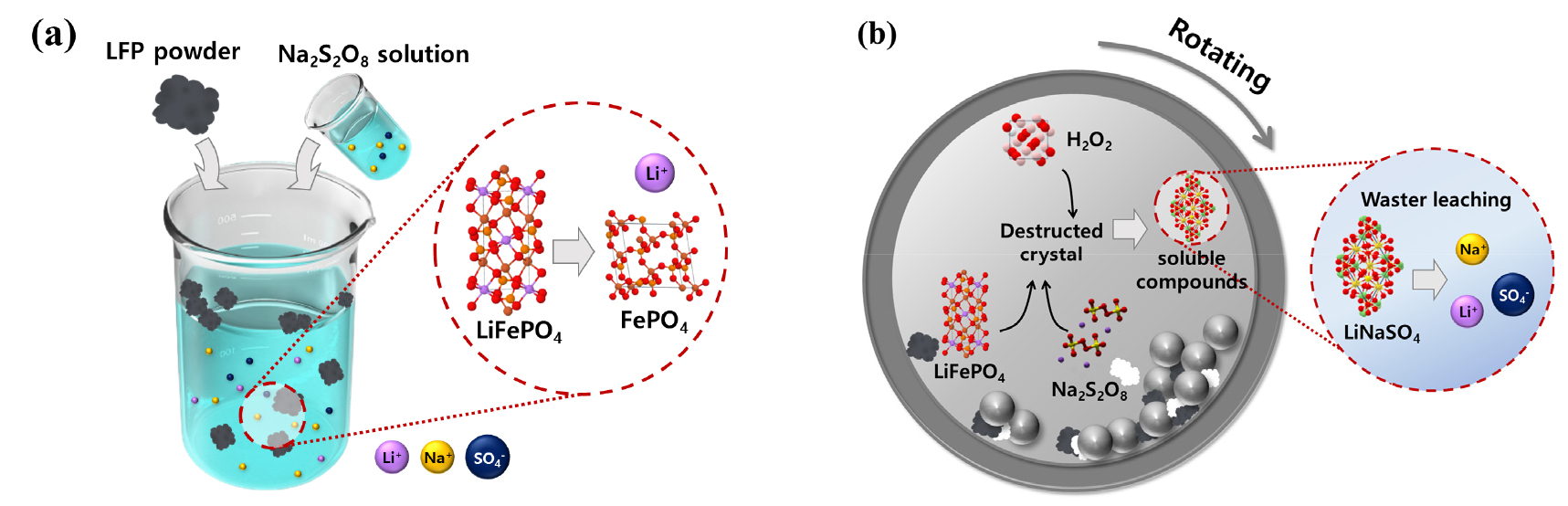
폐LFP 양극재 분말로부터 리튬을 선침출하기 위해 2가지 방법을 사용하였으며 침출 메커니즘은 Fig. 2에 각각 나타내었다. Fig. 2의 (a)는 일반침출법으로 과황산계산화제인 과황산나트륨(Na2S2O8, Sodium persulfate, Sigma-Aldrich)을 폐LFP 양극재 분말 5 g과 반응식을 고려하여 이론적 함량의 1.1배의 농도로 약 4.15 g의 과황산나트륨으로 수용액을 제조하여 침출 용매로 사용하였다. 상온에서 폐LFP 양극재 분말과 과황산나트륨 수용액을 3시간 동안 250 rpm의 속도로 교반하며 고액비에 따른 리튬의 선택적 침출 반응을 진행하였다.
Fig. 2의 (b)는 과황산계산화제인 약 4.15 g의 과황산나트륨을 분말 상태로 폐LFP 양극재 분말 5 g과 (a) 실험인 일반 침출 방법의 조건과 동일한 농도 비율로 고상 상태로 Ball mill(HAN TECH, HBM-Mini-3R)에 투입하여 기계화학적 반응을 유도하였다. 볼밀 반응 조건은 직경 5 mm, 10 mm의 지르코니아 볼을 혼합하여 약 40% 충진하였으며, 3시간 동안 상온에서 임계속도를 고려하여 산출한 160 rpm으로 밀링하였다. 이때 과황산나트륨과 폐양극재 분말의 반응은 Zhang et al.(2019)의 연구에도 언급되었듯이 식 (1)과 같이 진행된다19). 또한 과산화수소의 첨가량에 따른 리튬의 선택적 침출 효율을 확인하고자 하였다. 밀링 반응 후 고액비 50 g/L의 증류수를 투입하여 1 시간 동안 추가 밀링 반응으로 리튬을 선택적으로 침출시켰다.
각각의 방법으로 리튬을 선택적으로 액상에 침출시키고자 하였으며, 침출 반응 후 액상과 고상으로 분리하여 액상은 유도결합플라즈마분광기(inductively coupled plasma optical emission spectroscopy, ICP-OES, iCAP Pro XP, ThermoFisher)로 주요 원소의 함량 변화를 확인하였으며, 고상은 XRD(X-ray diffraction spectroscopy, XRD, XRD-6100, Shimadzu) 분석을 통해 결정상 변화를 확인하였으며, SEM(Scanning Electron Microscope, SEM, Mira3, TESCAN)으로 형상 변화를 분석하였다.
3. Results and discussion
본 연구에서 사용한 원료는 폐LFP 배터리의 양극재 스크랩으로 -150 μm 구간의 파쇄산물을 사용하였다. 양극재 분말의 함량은 Table 1에 나타내었으며, 리튬은 약 4.2% 함유되어 있다. 철은 약 22.5%, 인은 약 15.8% 혼합되어 있었으며, 양극재 박막의 소재인 알루미늄은 파쇄 과정에서 블랙파우더에 일부 혼입되어 약 0.2% 함유되어 있다. Yang et al.(2018)의 연구에 사용된 양극재 스크랩의 함량은 리튬 약 3.46%, 철 약 26.45%, 인 약 15.88% 그리고 알루미늄이 약 16.85%이 포함되어 있었으며20), Chen et al.(2023) 연구에서는 리튬이 약 4.22%, 철 약 32.57%, 인 약 18.72%로 언급되었다21). 대부분의 폐LFP 배터리의 양극재에는 리튬이 약 3.5~4.5% 정도 함유되어있는 것으로 확인된다.
Table 1.
Chemical composition of wasted LFP cathode powders(mg/kg)
| Elements | Li | Fe | P | Al |
| wasted LFP powder | 42,272 | 225,115 | 157,661 | 2,736 |
폐LFP 양극재 분말로부터 리튬을 분리 회수하기 위한 실험 조건은 본 저자들의 이전 연구 내용을 기반으로 리튬의 선택적 침출을 위해 과황산계산화제 3종인 과황산나트륨(Na2S2O8), 과황산칼륨(K2S2O8) 및 과황산암모늄((NH4)2S2O8) 중 비교하여 과황산나트륨을 선택하여 진행하였다. 과황산칼륨의 경우 물에 대한 용해도가 다른 산화제에 비해 현저히 낮아 수용액 제조 시 시간 소모 및 고액비의 영향을 가장 많이 받으며, 과황산암모늄의 경우 리튬의 침출율은 높지만, 철에 대한 침출율도 미량이지만 증가하여 과황산나트륨으로 선정하였다18). 따라서 과황산나트륨을 사용한 일반 침출 방법에서는 고액비에 따른 영향을 확인하였으며, 볼밀을 사용한 기계화학적 침출 방법은 과산화수소(H2O2)를 첨가하지 않은 조건과 일반 침출 방법을 비교하고자 하였으며, 기계화학적 반응에서는 과산화수소 0.5~2 ml까지 첨가하며 이에 대한 영향을 확인하였다.
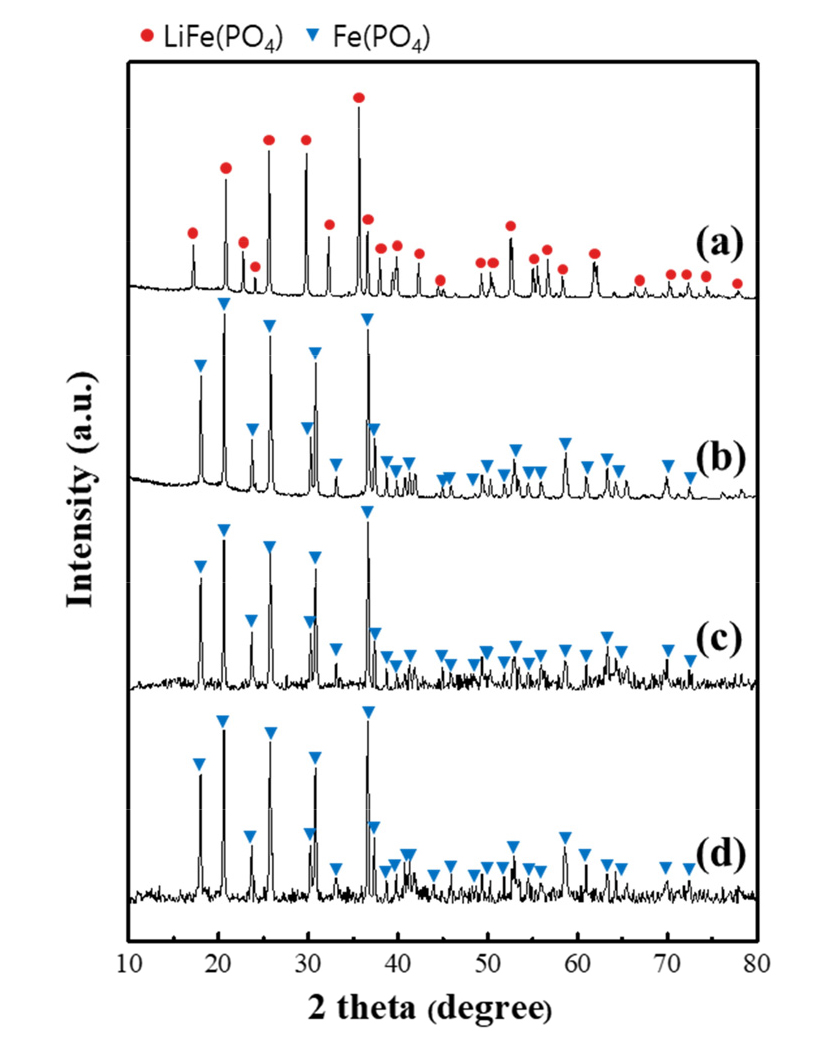
먼저, Fig. 3에 일반 침출법을 사용하여 고액비 50 g/L, 100 g/L 및 200 g/L 별 침출 잔사의 XRD 그래프를 나타내었다. 원료인 폐LFP 양극재 분말의 XRD peak는 올레빈 구조의 LiFePO4와 일치하였고, 고액비에 상관없이 침출 잔사는 FePO4 결정상으로 분석되었다. 이는 원료 내 리튬의 함량이 약 4.2%로 고액비 200 g/L 조건에서 리튬의 침출율은 약 76.01%이므로 잔사에는 약 20% 이상의 리튬이 남아있지만, 전체 분말에서의 리튬 함량은 약 1% 이하로 XRD 분석 방법에서의 검출 한계로 리튬에 대한 peak는 검출되지 않은 것으로 사료된다.
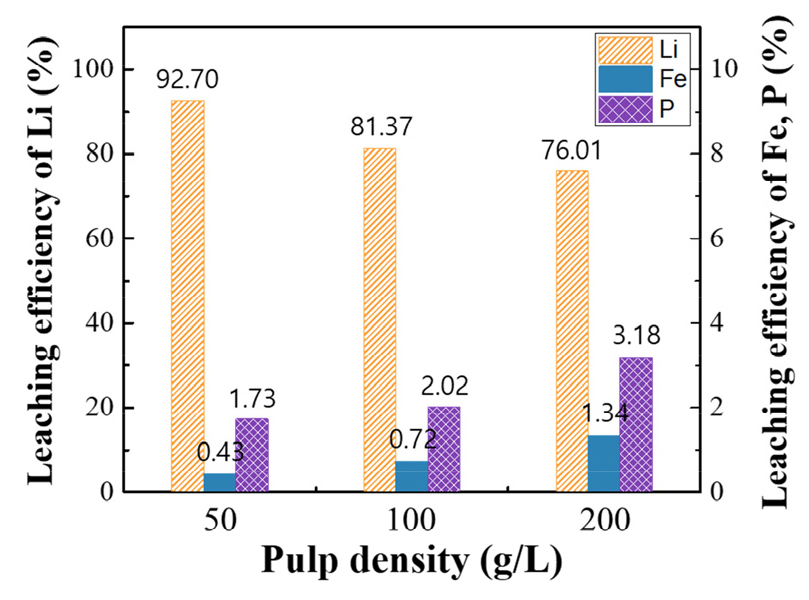
Fig. 4는 일반 침출의 리튬, 철 및 인의 고액비에 따른 침출율이다. 고액비가 50 g/L, 100 g/L 및 200 g/L로 증가할수록 리튬 이온의 침출율은 92.70%, 81.37% 및 76.01%로 감소하였다. 반면 철은 0.43%에서 1.34%로 인은 1.73%에서 3.18%까지 각각 증가하는 경향을 나타내었다. 양극재 소재인 LiFePO4 물질 자체의 전기전도도가 다른 양극재에 비해 10-9~10-10 S/cm 수준으로 양극재 표면에 카본으로 코팅하여 전기전도도를 향상시킨다22,23). 이로인해 일반 침출 방법으로 폐LFP 양극재 분말로부터 리튬 침출 시, 카본은 소수성을 나타내어 양극재 분말을 과황산나트륨 수용액과 혼화성이 낮아 반응 초반에는 합침 되지 않고, 용매 위로 뜨는 현상이 나타나 침출 반응 종료 후에도 용매에 젖지 않은 분말이 일부 확인된다. 이에 과황산나트륨 분말을 고상으로 LFP 양극재 분말과 기계적화학적 방법으로 LFP 양극재 분말 내 리튬을 물로 쉽게 용출이 가능한 Li2SO4, NaLiSO4 등과 같은 수용성 화합물로 전환하고자 하였다.
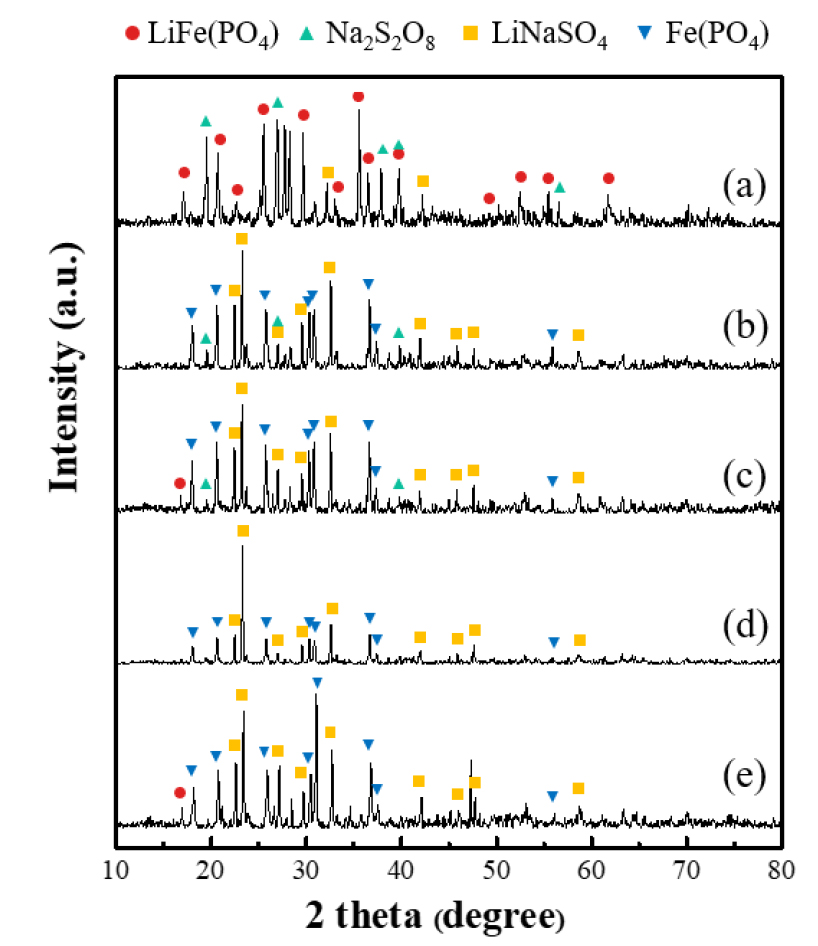
일반 침출 방법과 기계화학적 방법으로 폐LFP 양극재 분말로부터 리튬의 선택적 침출을 비교하고자 하였으며, 기계화학적 방법에서는 추가로 과산화수소가 미치는 영향을 확인하였다. 폐LFP 양극재 분말과 과황산나트륨은 일반 침출법과 동일 조건으로 양극재 분말과의 화학반응식을 고려하여 이론 함량의 1.1배의 농도로 두 분말 모두 고상의 형태로 볼밀에 투입하여 기계화학적 반응을 유도하였다. Fig. 5의 (a)부터 (e)는 과산화수소 투입량을 0 ml부터 2 ml까지 각각 조절하여 3 시간의 기계화학적 반응 후 분말의 XRD 분석 결과이다. (a)의 과산화수소를 첨가하지 않은 조건에서는 양극재 분말과 과황산나트륨이 반응되지 않고 각각의 분말 그대로 확인되었다. 과산화수소를 첨가한 조건에서는 LFP 결정상이 LiNaSO4와 FePO4의 결정상으로 분리되었다. 과산화수소 0.5 ml 및 1 ml 첨가한 샘플은 미세하더라도 Na2S2O8의 결정상이 확인되며, 1.5 ml 조건에서는 LiNaSO4와 FePO4의 결정상만 나타났다. 이는 볼 밀링의 기계적 힘이 구동력이 되어 전기 에너지를 대체하여 리튬 추출을 유도하고, 산화제인 Na2S2O8와 LiFePO4 결정상에서 추출된 리튬의 화학적 산화반응으로 LiNaSO4와 FePO4의 생성물로 전환된 것이다16). 또한 Li et al.(2019) 연구에 따르면 과산화수소의 첨가는 리튬의 용출을 향상시키고, Fe의 용해도를 감소시킨다는 연구 결과가 있으며, 본 연구에서도 과산화수소를 첨가하에 따라 리튬 용출에 용이하게 분해 및 상전환된 것을 확인할 수 있었다.
2-theta 23.3°는 LiNaSO4의 주 피크이며, 36.6°는 FePO4의 주피크로 과산화수소의 첨가량이 증가할수록 해당 피크의 검출 세기가 상대적으로 증가하였다. 특히 과산화수소 1.5 ml 첨가한 샘플의 XRD 결과에서는 다른 조건의 분말에 비해 LiNaSO4가 상대적으로 주피크로 확인되며 이를 수치적으로 비교하고자 LiNaSO4의 대비 FePO4의 주피크의 세기 비율을 확인했다. 과산화수소 0.5 ml 첨가한 샘플은 1.68, 1.0 ml는 1.57, 1.5 ml는 4.06 그리고 2 ml에서는 1.80으로 특히 과산화수소 1.5 ml를 첨가하여 반응한 조건의 XRD 결과에서 유독 LiNaSO4 결정상의 세기가 상대적으로 높게 나타나는 것을 확인할 수 있었다.
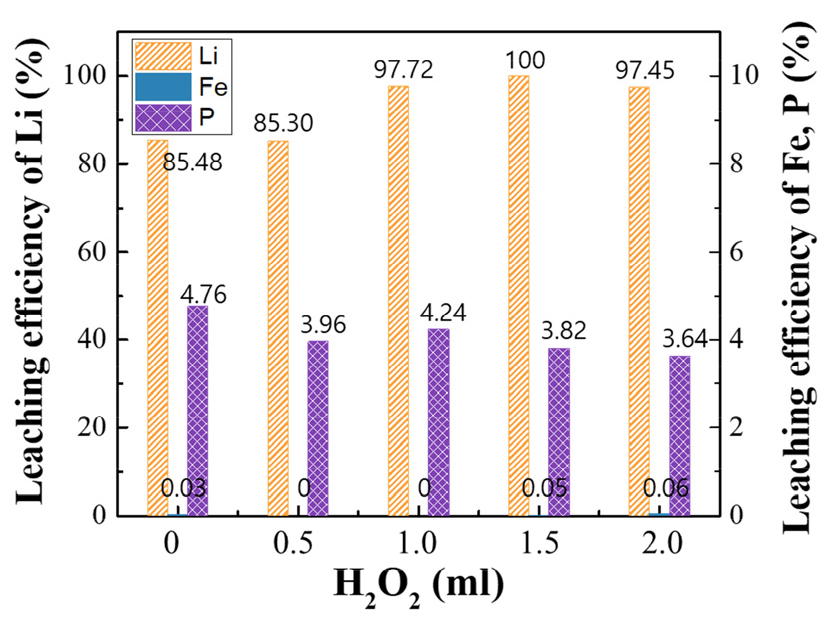
상기 기계화학적 반응 후 각 고액비 50 g/L 조건으로 증류수를 추가하여 3 시간 수침출 반응을 진행하였다. 침출 반응 후 고액을 분리하여 액상은 ICP 분석을 통해 리튬, 철, 인의 침출율을 산출하여 Fig. 6에 나타내었으며, 고상은 XRD 분석을 통해 결정상 변화를 확인하여 Fig. 7에 나타냈다. Fig. 6의 침출율 결과에서 기계화학적 반응 후 수침출 시 철의 침출율은 약 0~0.06%이며, Fig. 4의 일반 침출 시 철의 침출율은 약 0.43~1.34%이다. 따라서 기계화학적 반응 시 과산화수소를 첨가함으로써 철 2가를 3가로 산화시켜 FePO4 형성에 유리하여 철의 침출을 저하시키는 효과를 확인할 수 있었다. 리튬 침출액으로부터 침전 반응을 통해 리튬화합물 형태로 회수 시, 침출액 내 철의 함유량이 약 3,000 ppm 이상일 경우 리튬화합물의 순도를 위해 철 제거 공정의 추가가 필요하다24). 이에 과산화수소를 첨가함으로써 철 제거 공정을 제외할 수 있어 공정 간소화가 가능하다. 또한 기계화학적 반응에서 수침출 용액 내 리튬의 침출율은 과산화수소를 첨가하지 않은 조건과 0.5 ml 첨가한 조건은 별반 차이가 없었으며, 1.0 ml 첨가한 샘플부터 약 97% 이상의 침출율이 나타났으며, 1.5 ml 첨가했을 때 약 100% 가까이 리튬이 선택적으로 침출되는 조건임을 확인하였다. 이는 Fig. 5에서 기계화학적 반응 후 XRD 결과에서도 유독 LiNaSO4 결정상의 세기가 상대적으로 높게 검출된 것과 관련된 것으로 사료된다. 반면 인은 일반 침출보다 상대적으로 미량 높게 침출되었다.
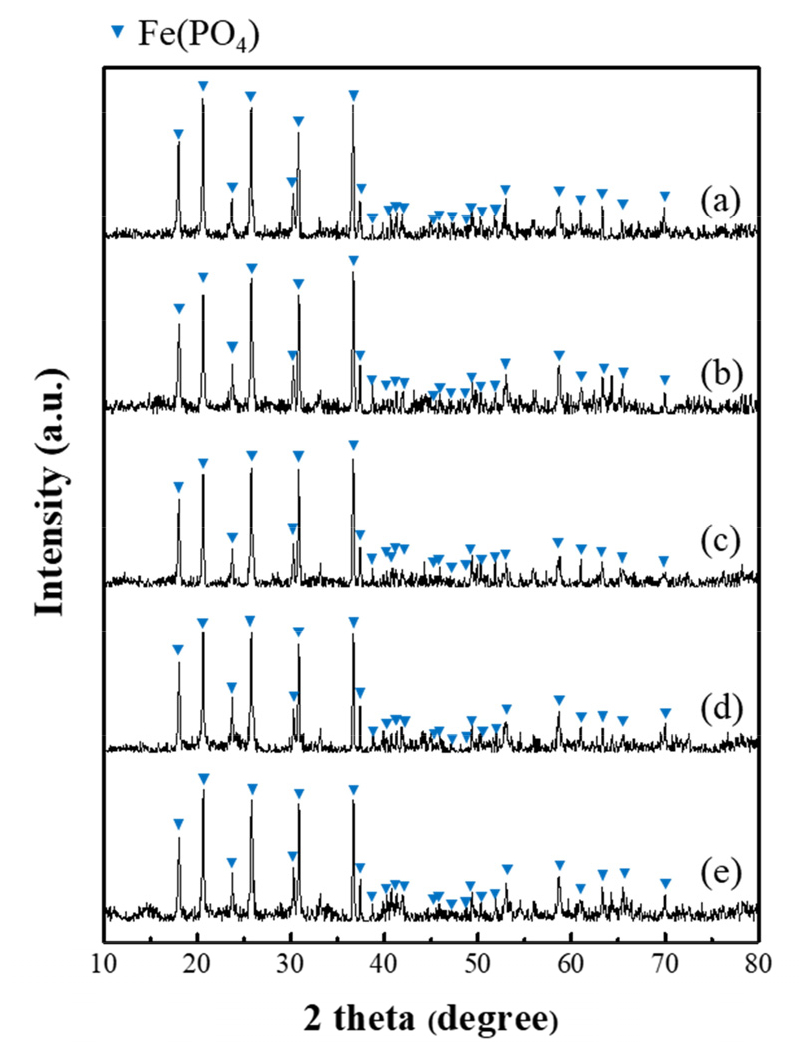
Fig. 7에는 기계화학적 반응 후 수침출한 침출잔사의 XRD 분석 결과이다. 과산화수소 첨가 유무 및 함량에 관계없이 모두 FePO4 결정상과 일치하였다. 이는 모든 조건에서 리튬이 약 85~100% 침출된 침출 잔사로 추출되지 않은 잔사 내 미량의 리튬은 검출한계로 인해 리튬에 해당하는 피크는 상대적으로 검출되지 않았다.
기계화학적 반응 후 침출 잔사의 SEM 이미지를 Fig. 8에 나타냈다. (a)는 원료인 폐LFP 양극재 분말 이미지이며, (b)부터 (f)는 볼밀을 사용하여 과산화수소 함량에 따른 침출 잔사이다. 원료 폐LFP 양극재 분말은 균일한 크기의 입자들이 치밀하게 뭉쳐있으며, 이에 비해 볼밀링으로 기계화학적 반응한 분말의 침출 잔사는 입자 간의 크랙과 공극이 증가한 것을 확인할 수 있다. 이로 볼밀링에 의해 리튬이 추출되며 이와 같이 형상 변화가 발생하였음을 간접적으로 유추할 수 있다.
4. Conclusions
폐LFP 배터리 양극재를 파분쇄하여 -150 μm 분말로부터 리튬을 선추출하고자 하였다. 분말에는 리튬이 약 4.2% 포함되어 있었으며, 현재 상용화되어 있는 폐배터리로부터 리튬 회수공정은 후단에서 리튬을 회수하여 손실과 순도에 문제가 발생하며, 과량의 산(acid) 사용으로 환경 문제도 야기한다. 이에 과황산계 산화제 중 과황산나트륨 수용액을 사용하는 일반 침출 방법과 과황산나트륨 분말을 고상의 상태로 반응시키는 기계화학적 침출을 사용하여 리튬을 선택적으로 선추출하여 비교하였다.
1. 일반 침출방법을 사용할 경우 고액비가 낮을수록 리튬의 선택적 침출율이 높으며, 고액비 50 g/L 조건에서 리튬은 약 92.70%, 철은 약 0.43%, 인은 약 1.73%의 침출율을 나타냈다.
2. 기계화학적 방법에서는 과산화수소의 영향을 확인하였는데, 과산화수소의 첨가는 폐LFP 배터리 양극재의 리튬과 과황산나트륨의 반응에서 NaLiSO4 형성 시 리튬의 화학적 산화반응 및 철의 산화를 촉진시켜 리튬의 선택적 침출의 효율이 향상되었다. 기계화학적 반응 시 과산화수소 1.5 ml 첨가했을 때, 리튬은 약 100%, 철은 약 0.05% 및 인은 약 3.64% 침출 결과를 나타냈다.
본 연구를 통해 동일한 조건으로 일반 침출과 기계화학적 반응을 비교하면, 과산화수소를 첨가하지 않은 기계화학적 반응의 리튬 침출율은 약 85.48%로 일반 침출 방법의 리튬 침출율 약 92.70%에 비해 효율이 떨어진다. 하지만 일반 침출 방법의 철 이온이 약 4,300 ppm 침출되지만, 기계화학적 방법에서는 약 300 ppm으로 리튬의 선택성을 향상시킬 수 있었다.