1. 서 론
2. 하프늄의 생산량과 용도
3. 하프늄의 제련
3.1. Hf 원료와 분리 추출
3.2. Kroll법에 의한 하프늄 제조
3.3. 용융염 전해에 의한 하프늄 제조
3.4. HfO2의 금속열환원에 의한 하프늄 제조
3.5. 금속 하프늄의 정제와 용융
4. 하프늄의 리사이클링
5. 종 합
1. 서 론
하프늄(Hf, hafnium)은 주기율표상에서 타이타늄(titanium, Ti), 지르코늄(zirconium, Zr)과 같은 족에 속하는 금속이지만, 지각 중 원소 존재도는 3 ppm(45위)으로 Ti의 0.57 %(9위), Zr의 0.02 %(18위)1)에 훨씬 못 미치며, 전 세계 연간 생산량도 약 80 톤에 불과한 희소금속이다. 이러한 Hf은 Zr 광석인 지르콘(zircon, zirconium silicate, ZrSiO4) 중 Zr을 치환 고용하는 형태로 존재하며, 원자력용 고순도 Zr의 정련 과정에서 부산물로 생산되고 있다.
Hf은 같은 족 원소인 Zr과 원자가가 같고 이온 반경(Hf 0.085 nm, Zr 0.086 nm)이 거의 같은 등 화학적·물리적 성질이 유사하고2), 상호 분리가 어려워 천연 원소로서는 마지막에서 세 번째인 1923년에 발견되었다. 그러나 멘델레예프(Dmitri Mendeleev)는 그 이전인 1869년에 화학 원소 주기 법칙에 관한 보고서에서 Ti과 Zr보다 더 무거운 유사 물질이 존재하는 것을 예측했다. 멘델레예프는 1871년에 Zr 아래 위치에 란타넘(La, 57)이 있다고 믿었다3). 그 후 1922년 덴마크의 보어(Niels Bohr)가 당시 미발견이었던 72번 원소는 란타노이드가 아니라 Zr과 유사한 것이라고 예언하면서 닐스 보어 연구소에서 X-선 회절분석과 분별 결정을 반복한 끝에 1923년에 Hf을 발견하였다. 하프늄이란 원소명은 이 원소의 존재를 확인한 보어의 고향인 코펜하겐의 라틴어 이름인 하프니아(Hafnia)에서 유래하였다4).
Table 1에는 Hf의 물리화학적 성질을 주기율표의 같은 족인 Ti, Zr과 비교하여 나타내었다5). Hf은 회백색의 전이금속으로 Ti이나 Zr 보다 고융점(융점 2,233 ℃)이며, 상온에서의 밀도는 Zr보다 2배 이상 큰 중금속이다. 또 Hf은 1,760 ℃ 이하에서는 hcp 구조를, 그 이상에서는 bcc 구조를 갖는다. Hf은 전성과 연성이 풍부하며, 산화력이 있는 산에는 용해되지만, 알칼리에는 용해되지 않는다. 또 Hf은 고온에서 산소, 수소, 질소, 할로겐 원소 등과 반응하여 화합물을 만들며, 기본적으로는 Zr과 물리화학적 성질이 유사하다.
Table 1
Physico-chemical properties of titanium, zirconium and hafnium
금속 Hf의 열중성자 흡수 단면적이 105 barn/atm으로 Zr의 약 570배 정도로 중성자를 매우 잘 흡수하여 원자로 내부에서 핵분열의 연쇄반응을 억제하는 제어봉(nuclear reactor control rods)으로 이용되며, 초합금용 첨가 원소로도 사용되는 등 현대사회의 핵심 금속이다. 본 논문에서는 이러한 Hf의 제련과 리사이클링 기술에 관하여 고찰하였다.
2. 하프늄의 생산량과 용도
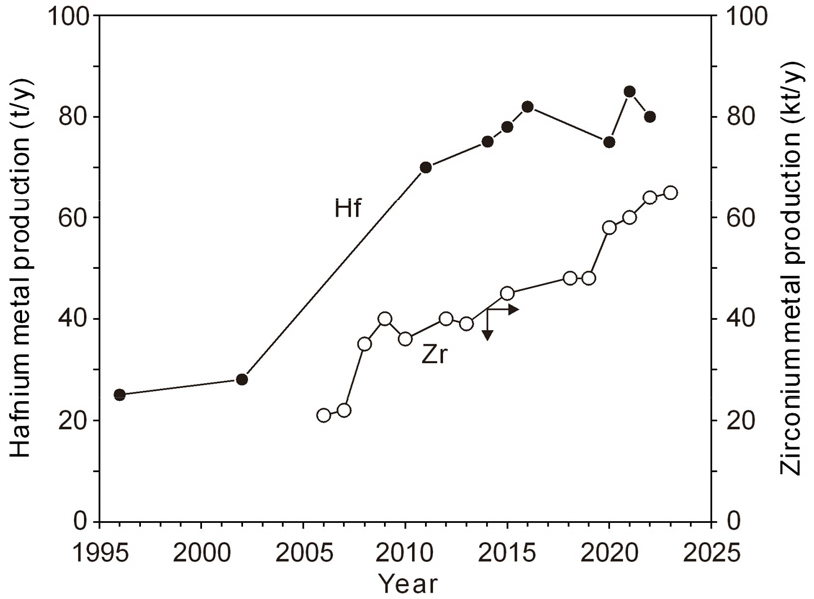
Hf은 지르콘 중에 함유되어 있으므로 USGS(U.S. Geological Survey)6) 등에서도 Hf은 Zr과 함께 나타내고 있다. 지르콘 중 Zr:Hf이 약 50:1이며, 바델라이트(baddeleyite)에는 약 73:1로 함유되어 있다7). 2024년 기준 전 세계 Zr 정광 생산량은 약 150만 톤 수준이며, ZrO2 기준으로는 약 98만 톤이다.5) 그러나 원자력용 금속 Zr의 수요가 약 5,000 톤이므로 지르콘 중 Hf 함유량으로 추정하면 연간 약 100 톤 미만이 생산될 수 있으며, Fig. 1에 연간 금속 Hf 생산량을 Zr과 비교하여 나타내었다8). 2000년대 초반까지 Hf의 연간 생산량은 30 톤에도 미치지 못하였으나, 2010년 이후부터 약 70 톤 이상이 생산되고 있으며, 2022년에는 약 80 톤의 금속 Hf이 생산되었다. 2024년의 하프늄 시장 규모는 89.10 톤으로 추정하며, 2029년에는 115.85 톤에 달하여 연평균 5.39%의 성장률을 나타낼 것으로 전망하고 있다9). 특히 고온용 초합금 수요가 증가하여 2026년의 금속 Hf 수요는 112~151톤에 달할 것으로 예상하고 있다10,11).
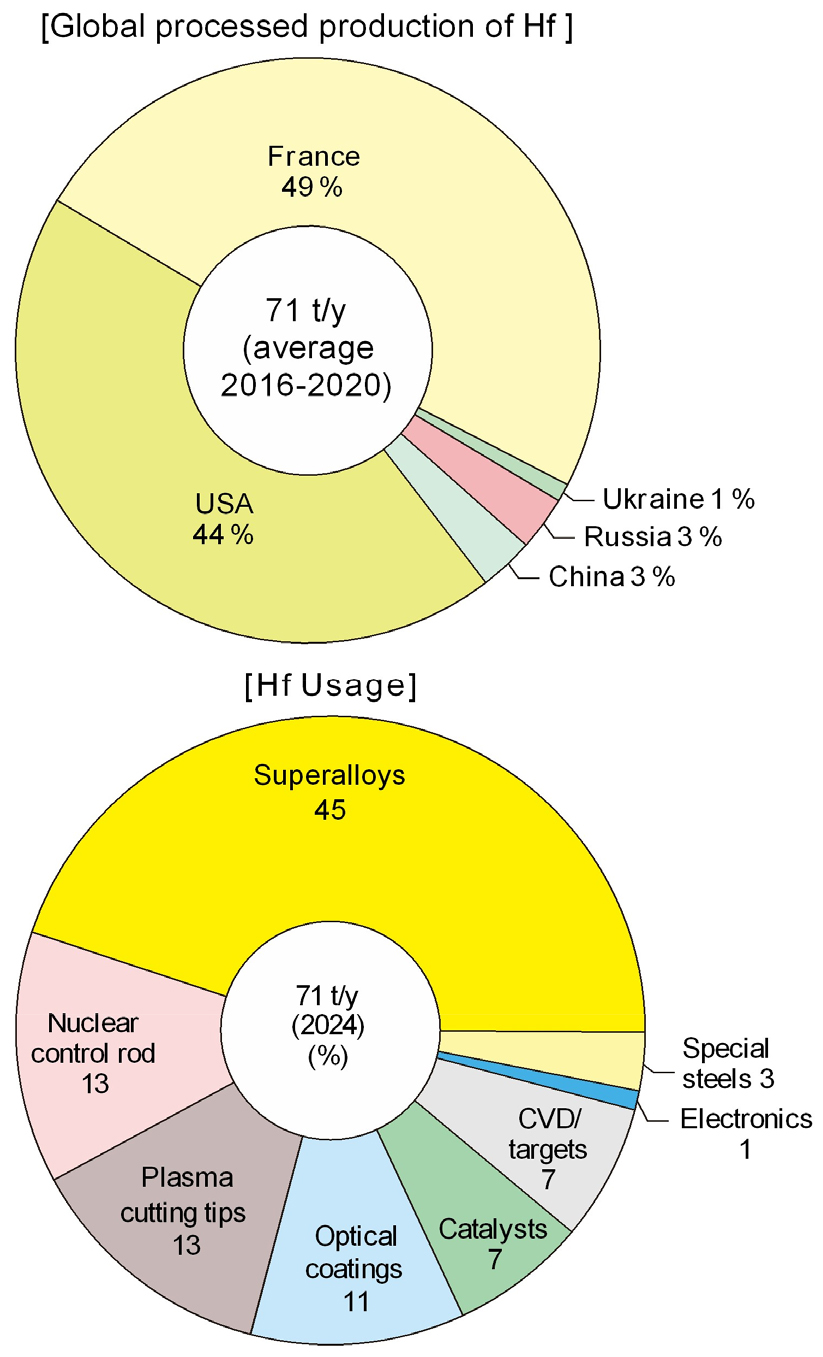
Fig. 2에는 Hf의 국가별 생산 비율(a)과 용도(b)를 나타내었다12). 전 세계 금속 Hf 생산량의 약 83 %는 프랑스와 미국에서 생산되고 있으며, 중국과 러시아에서 각각 3 %를 생산하고 있는 수준으로 원자력용 금속 Zr을 생산하는 나라에 국한되어 있는 전략 금속이다.
Hf은 높은 강도와 초고온에서의 안정성으로 인해 항공우주 및 산업용 터빈 용도의 초합금(45 %)이나 특수강(3 %) 등의 합금원소로 사용되고 있다. Hf은 로켓 엔진의 노즐에 사용되는 Nb 기반 합금의 약 10 %를 차지한다. 특히 Hf은 MAR-M-247 초합금(1.2~1.8 wt% Hf)에 필수적이며, 제트 엔진의 고온 부위(터빈 블레이드와 베인)에 사용되고 있다. 그리고 Hf 초합금은 주로 발전에 사용되는 산업용 터빈 등에도 사용되지만 Hf 함량은 0.1~0.2 wt% 수준이다.
또 Hf은 공작기계에서 금속 재료 등의 절단을 위한 스로어웨이(throw away) 팁이나, 금속 절단용 플라스마 아크용 노즐, 플라스마 전극(탄산하프늄, 질화하프늄), 고온용 세라믹에도 사용되고 있지만 Hf 함유량은 1 wt% 미만에 불과하다. 그 외에도 불화하프늄은 광파이버에, Hf-Nb 카바이드는 초경공구용 재료로 사용되고 있으며, 내식 재료로 화학플랜트 등에 사용되기도 한다.
한편 Hf은 Zr과 반대로 열중성자 흡수 단면적이 커서 원자력 발전소나 원자력 잠수함의 비등수형 원자로(boiling water reactor, BWR)의 제어봉(13 %)에 고순도 Hf(99.6~99.8 wt%)이 사용되고 있다. 그 외에도 Hf 산화막은 유전율이 높아 반도체 집적회로 gate의 전극 재료로도 일부 사용되고 있으므로13) 향후 톤 단위 이상의 Hf 수요가 예상된다.
3. 하프늄의 제련
3.1. Hf 원료와 분리 추출
광물학적으로 Hf은 Zr과 함께 존재하여 Hf과 Zr이 함유된 광물은 40여 종에 이른다. 이 중에서 지르콘 샌드와 바델라이트가 주요 원료이지만, 대부분 지르콘 샌드를 Hf과 Zr의 원료로 사용한다. Table 2에는 각 원료의 조성 예를 나타내었으며14), Hf은 지르콘 광상 중에 Hf/(Zr+Hf)≒1/50의 비율로 함유되어 있으므로15) Zr 제조 과정에서 Hf을 분리하여 추출하고 있다.
Table 2
Chemical composition of zircon and baddeleyite (wt%)
| Components | ZrO2 | HfO2 | SiO2 | TiO2 | Fe2O3 | Al2O3 | Others |
| Australian zircon | 66.90 | 0.4~17 | 32.60 | 0.12 | 0.04 | 0.43 | 0.037 |
| S. African baddeleyite | 96.00 | 0.5~2.1 | 1.5 | 1.0 | 1.0 | - | 0.2 |
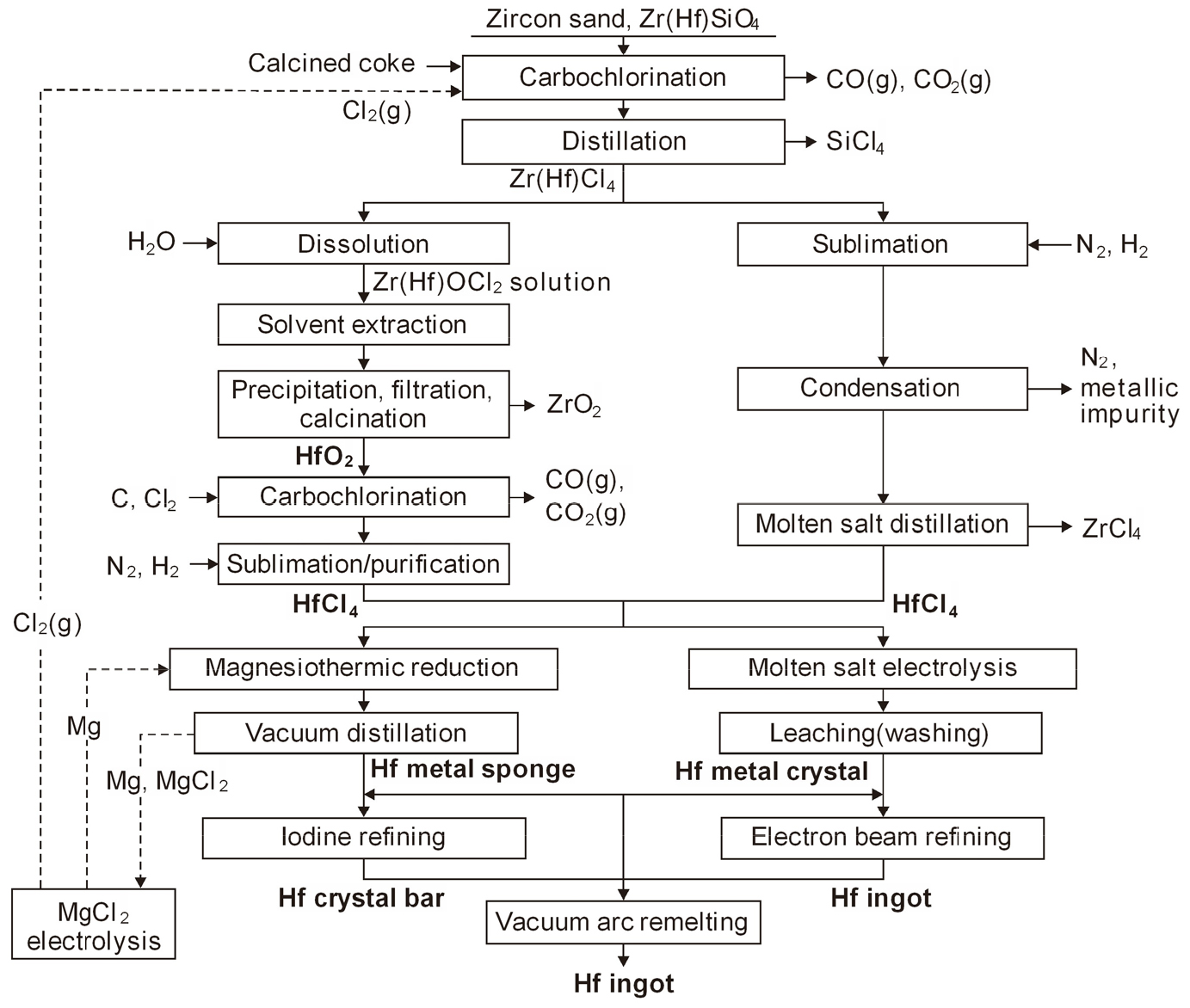
Fig. 3에 지르콘 샌드에서 금속 Hf을 제조하는 공정도를 나타내었다16,17). Hf과 Zr의 화학적 성질이 유사하여 상호 분리가 매우 어렵지만 용매 추출법, 분별 결정법, 분별 증류법, 이온 교환법, 흡착법 등을 이용하여 분리하고 있다. 용매 추출법에는 사용하는 용매에 따라 MIBK(Methyl Isobutyl Ketone)-Thiocyanate Process, TBP(Tributyl Phosphate)-Nitric Acid Process 및 N235(Alamine 336) 공정18) 등이 있으나 공업적으로 MIBK법을 많이 사용하고 있다.5)
MIBK법은 지르콘을 염화시켜 만든 Hf과 Zr의 혼합 염화물을 출발원료로 사용하며, 지르콘의 염화반응은 다음과 같다.
상기한 반응의 Zr과 Hf의 염화물(Zr(Hf)Cl4)을 물에 용해시키고 염산 용액에서 가수분해하여 지르코늄-하프늄 옥시크로라이드(Zr(Hf)OCl2)를 만든다. 이어서 Zr(Hf)OCl2를 NH4CNS와 혼합하고 MIBK와 접촉시켜 Hf은 유기상(MIBK)으로, Zr은 수상(NH4CNS)으로 분배시켜 각각 HfO2와 ZrO2로 회수한다.18) 그 외에도 염산 용액이나 황산 용액 중 Hf과 Zr의 용매추출에 의한 분리에 관하여 많은 연구가 이루어져 있다19,20).
한편 Kroll법에 의한 Hf이나 Zr 스펀지 제조는 각각의 염화물을 출발원료로 사용하므로 염화물 상태로 분리하는 것이 유리하다. HfCl4와 ZrCl4는 Table 3과 같이 물리화학적 성질이 유사하지만21) 증기압 차이를 이용하여 분리할 수 있으며, 각각의 증기압(mmHg)은 다음과 같다22).
Table 3
Physical constants tetrachlorides of hafnium and zirconium
이러한 증기압 차이를 이용한 분리 공정에는 (i) 대기압에서의 박막 승화 공정, (ii) 사염화물과 추가 화합물 생성 후 해당 화합물의 환류, (iii) 고압에서의 사염화물 분별 증류, (iv) 1기압에서의 용융염 증류 등이 알려져 있다.
박막 승화법(thin film sublimation process)은 523 K에서 HfCl4의 휘발성이 ZrCl4 보다 1.7배 정도 높은 것을 이용한 분리법이다. 상압의 523 K에서 ZrCl4와 HfCl4의 증기압은 각각 27.60, 59.58 mmHg이지만, 완전한 환류 조건에서 원하는 분리도를 얻기 위한 이론적인 판(plate) 수가 약 30 개로 계산되는 등21) 수십 번 반복해야 원하는 순도를 얻을 수 있다.
박막 승화법의 문제점을 해결하기 위해 여러 가지 혼합 용융염 중에서 HfCl4와 ZrCl4를 분리하고자 하였다. 특히 프랑스 CEZUS사에서는 KCl-AlCl3 용융염 중에서 추출 증류공정(extractive distillation process)을 사용하여 용융염 중 HfCl4를 증류시켜 분리하였으며, 1회 분리로 HfCl4가 30~50 %까지 농축되는 것으로 알려져 있다.18) Gupta 등은 KCl-AlCl3 용융염 중 ZrCl4의 분리에 대해 상세하게 검토하기도 하였다23). 분리 정제한 HfCl4는 Kroll법이나 용융염 전해법을 이용하여 금속으로 환원한다.
3.2. Kroll법에 의한 하프늄 제조
Kroll법은 염화물을 Mg으로 환원하는 방법이므로, 용매추출 등으로 분리한 HfO2를 다음 식과 같이 산소를 제거하기 위한 탄소질 환원제를 이용한 염화반응에 의해 HfCl4로 만든다.
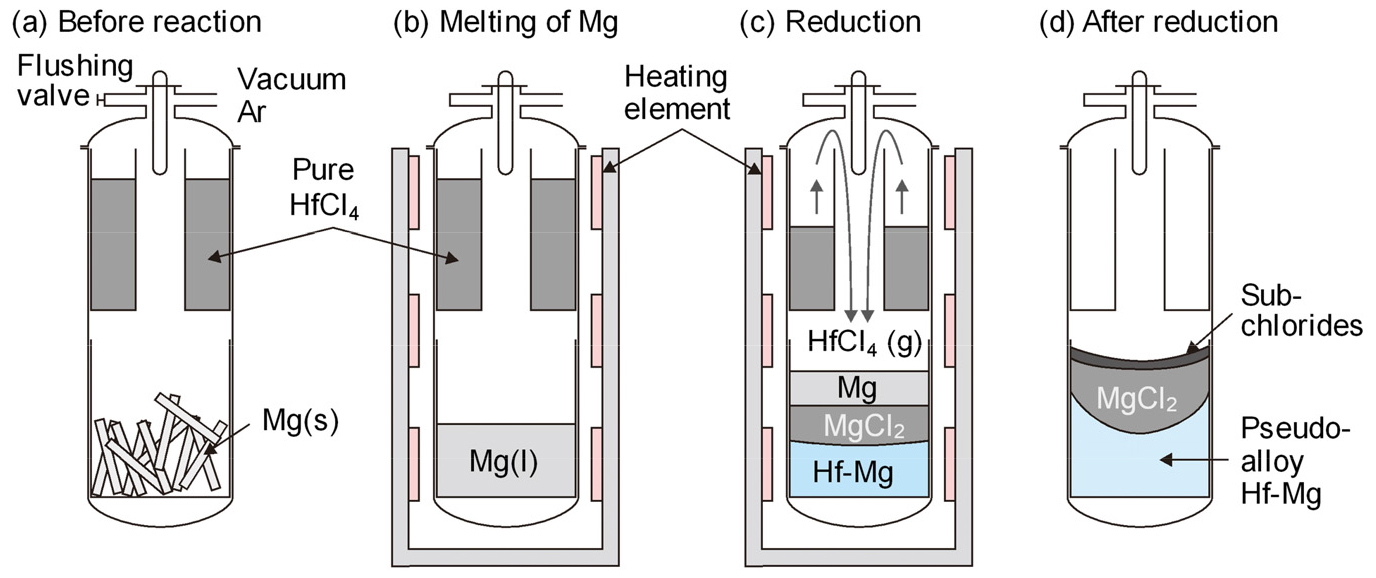
정제한 HfCl4를 Ti이나 Zr 제련과 마찬가지로 다음 식과 같이 고순도 Mg으로 환원하여 금속 Hf으로 제조하며, Fig. 4에 Kroll법에 의한 Hf 제조 공정도를 나타내었다24).
생성물의 반응성이 높아 공기와 수분이 없는 불활성의 양압 분위기에서 환원한다. 우선 Fig. 4(a)와 같이 환원반응 전에 반응물질인 HfCl4와 Mg을 내열강제 반응조에 장입한다. Fig. 4(b)와 같이 상하 온도가 다른 노 내에 반응조를 장착하고, 노의 하부에서 Mg을 용융시킨다. 그리고 Fig. 4(c)와 같이 HfCl4는 노의 상부에서 승화하여 반응조의 하부로 내려가 용융 Mg의 표면에서 식(5)와 같이 환원된다. 생성된 구형의 Hf은 침강하여 용융 Mg이 있는 반응조 바닥에 모이며, 이것을 Hf-Mg 의합금(pseudoalloy)이라 부른다.
환원이 완료된 후 900~1,000 ℃의 고진공 분위기에서 Ti이나 Zr의 Kroll법과 마찬가지로 과잉의 Mg과 생성물인 MgCl2 및 기타 휘발성 물질을 증류하여 제거하면 스펀지상의 Hf이 남는다. 스펀지 Hf은 극도로 발화성이 강하여 파쇄한 후 Ar 분위기 중에 보관한다. 한편 Kroll법으로 제조한 Hf은 Ti이나 Zr과 달리 순도가 높지 않으며, 특히 산소나 질소 함유량이 높다. 냉간 가공 등을 하려면 400 ppm 이하의 산소 농도가 요구되지만, 일반적으로 500~1,000 ppm 정도의 산소가 함유되어 있으므로 정제 공정을 거쳐야 한다.
3.3. 용융염 전해에 의한 하프늄 제조
CEZUS사에서 Kroll법보다 효율적인 Hf 제조법으로 HfCl4를 직접 용융염 전해하는 방법을 개발하였다. 용융염은 소량의 NaF를 함유한 등몰의 NaCl-KCl이며, 기체상의 HfCl4를 전해조의 용융염 중에 주기적으로 주입하여 보충하면서 750~850 ℃에서 전해한다25). 전해 Hf은 결정상이나 플레이크 형상을 하고 있으며 순도가 매우 높다.
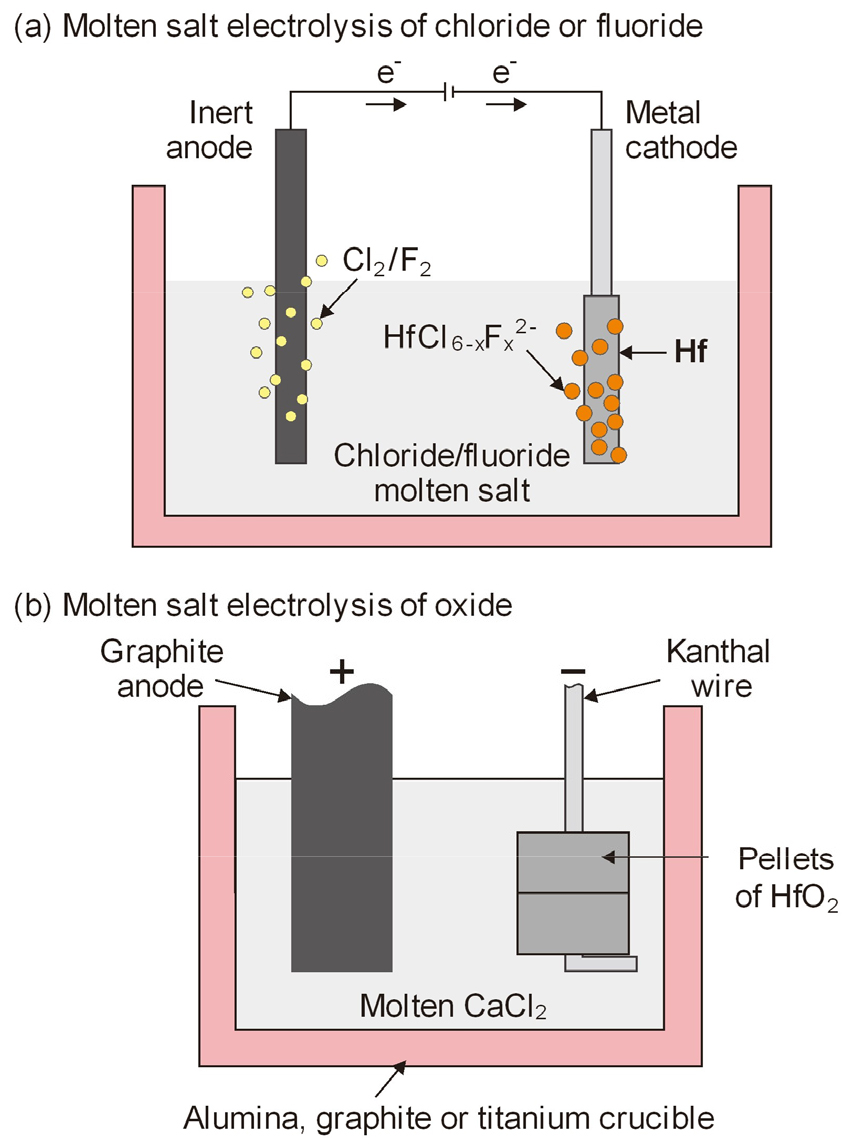
Wu 등은 NaCl–KCl–NaF–K2HfF6 용융염 중 HF(IV)의 전해 환원에 관해 검토하여 NaF 농도가 낮을 때(0<[F-/Hf4+]≤17.39)는 Hf(IV)→Hf(II)와 Hf(II)→Hf의 2단계에 걸쳐서 환원이 일어나며, NaF 농도가 높을 때(17.39<[F-/Hf4+]<23.27)는 Hf(IV)→Hf으로 환원되는 것으로 보고하였다26). Fig. 5(a)에는 Hf 염화물이나 불화물의 용융염 전해를 모식적으로 나타내었다27). Mukhachov 등은 KCl-KF계에서 HfF4를 용융염 전해하고 아이오딘법으로 정제하여 고순도의 Hf 결정을 얻었다28).
한편 Ma 등은 NaCl-KCl-NaF(0.35:0.35:0.3) 용융염 중에 HfO2를 용해시켜 Hf의 전기화학적 거동에 대해 검토하여 TiO2 등의 용융염 전해와 마찬가지로 HfO2를 용융염 전해하여 Hf을 제조할 수 있는 것으로 보고하였다29). 그리고 Fray 등은 TiO2의 용융염 전해30)와 마찬가지로 Fig. 5(b)와 같이 HfO2를 용융염 중에서 직접 탈산하여 금속 Hf이나 합금을 제조할 수 있는 것으로 보고하였으나31) 아직 생산성 등 해결해야 할 문제점이 있어서 상용화되지는 못하고 있다. 이와 같이 다양한 출발원료를 사용한 Hf의 용융염 전해에 관하여 연구되고 있으나27) 생산량 자체가 적어 연구결과의 예는 많지 않다.
3.4. HfO2의 금속열환원에 의한 하프늄 제조
염화물보다 산화물의 취급이 간편하므로 HfO2를 Mg, Ca 등의 환원제로 환원하는 금속열환원법에 관한 연구도 이루어지고 있다. HfO2의 금속 열환환원법의 기본 반응은 다음과 같으며, 수소 분위기 중에서 환원하면 수소화물을 만들 수 있다32).
그러나 Zr의 금속열환원 반응과 마찬가지로33) 식(6)에서 부산물인 MgO나 CaO를 완전히 제거하여야 한다. Sehra 등은 HfO2를 960 ℃에서 Ca으로 2시간 동안 환원시키고, 환원 생성물을 곧바로 얼음으로 냉각시킨 물에 넣어 과잉의 Ca을 제거하였으며, 부산물인 CaO는 냉각시킨 묽은 염산으로 침출시켜 제거하였다. 얻어진 조금속 Hf을 아이오딘법으로 정제하여 약 93 %의 실수율로 금속 Hf을 제조하였다34).
Abdelkader 등도 HfO2를 800 ℃에서 3시간 동안 Ca으로 환원하였으나, 부산물인 CaO 제거를 위해 30 mol%NaCl–70 mol%CaCl2 중에서 환원하여 산소농도가 1,000 ppm 이하인 금속 Hf을 얻었다. 그러나 산소 농도를 더욱더 낮추기 위해서는 과잉의 용융염을 사용하여 CaO를 제거하는 것이 필요하며, 용해된 CaO를 연속적으로 전해하는 등의 방법도 필요한 것으로 보고하였다35). 특히 HfO2는 Zr 제련공정의 용매추출 등 Hf 분리 공정에서 부산물로 산출되므로 금속 열환환원법은 염화물을 경유하지 않는 친환경적인 제련법이 될 수 있어서 향후 많은 연구 결과가 나올 것으로 기대되고 있다.
3.5. 금속 하프늄의 정제와 용융
Kroll법이나 용융염 전해, 금속열환원 등으로 제조한 Hf은 정제공정을 거쳐 고순도 Hf으로 된다. 금속 Hf의 정제에는 전해정련법, 아이오딘법, 전자빔용융법의 세 가지가 알려져 있다. 우선 Hf의 전해정련은 Nettle 등이 Kroll법으로 만든 스펀지 Hf을 90%NaCl-10%KCl-7%HfCl4, 55% LiCl-45%KCl-3%HfCl4, 55%NaCl-45%KCl-9%K3HfCl7의 세 가지 용융염으로 약 830 ℃에서 실시하여 O 130 ppm, Fe<10 ppm, N<10 ppm 등의 고순도 Hf을 얻었다36). 그러나 Hf의 전해정련은 Ti이나 Zr의 정련보다 어려워서 잘 적용하지 않는 것으로 알려져 있지만, 불순물 제거에 매우 효과적이어서 향후 새로운 전해정제법의 개발이 기대되고 있다.
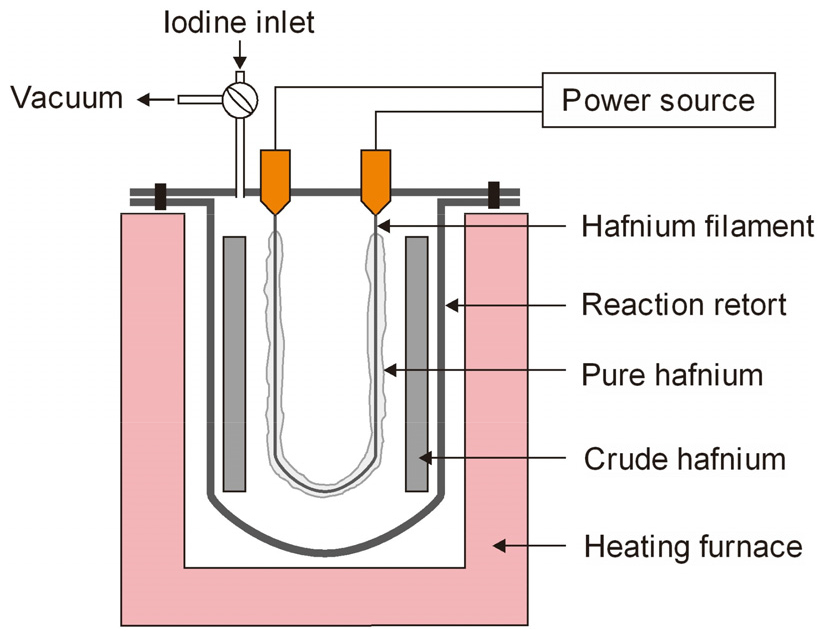
아이오딘(I)법(Van Arkel법)은 1925년 Van Arkel 등37)이 개발한 것으로 CVD(chemical vapor deposition)법을 응용한 Ti, Zr, Hf 등의 정제법으로 알려져 있으며, Fig. 6에 반응 장치를 모식적으로 나타내었다. 아이오딘법은 고체 금속(Me)과 아이오딘(I) 사이의 가역반응을 이용한 것으로, 조Hf을 200~300 ℃의 비교적 낮은 온도에서 I2(g)와 반응시키면 다음 식과 같이 HfI4가 만들어진다38).
HfI4의 융점은 445 ℃이지만 394 ℃에서 승화하므로 1,300~1,600 ℃로 가열된 필라멘트와 만나 열분해되어 순수한 Hf 결정이 얻어진다. 아이오딘법으로 조Hf을 정제하면 산소와 질소가 50 ppm 이하인 고순도의 Hf을 얻을 수 있으나, 일정 수준 이하의 Fe은 제거할 수 없으므로 미리 제거해 두어야 한다. Tian 등은 반응기 재료, 필라멘트 온도, 반응시간 등의 영향을 검토하여 필라멘트 온도를 전류()와 전압()을 제어하여 이 높을수록 Fe, Ni 등의 제거에 효과적인 것으로 보고하였다39). 다만 Ti이나 Zr과 마찬가지로 생산성이 낮아 정제 비용이 매우 높은 문제점이 있다.
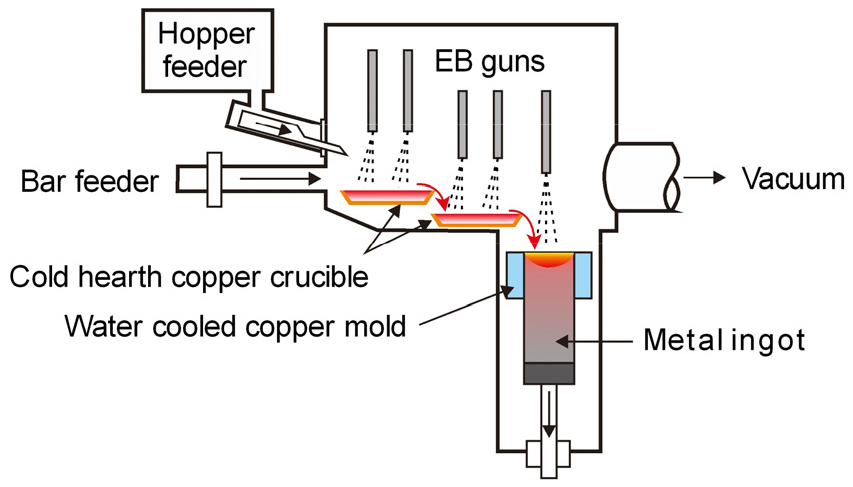
한편 Hf은 융점(2,233 ℃)에서의 증기압이 매우 낮아 고 진공 분위기의 전자빔용융(electron beam melting, EBM)에서 Hf보다 증기압이 높은 불순물 원소들을 휘발시켜 제거할 수 있다. 특히 EBM은 스펀지 Hf의 정제나 스크랩의 리사이클링에서도 매우 유효한 방법이며, Fig. 7에 전자빔 용융 장치의 모식도를 나타내었다.
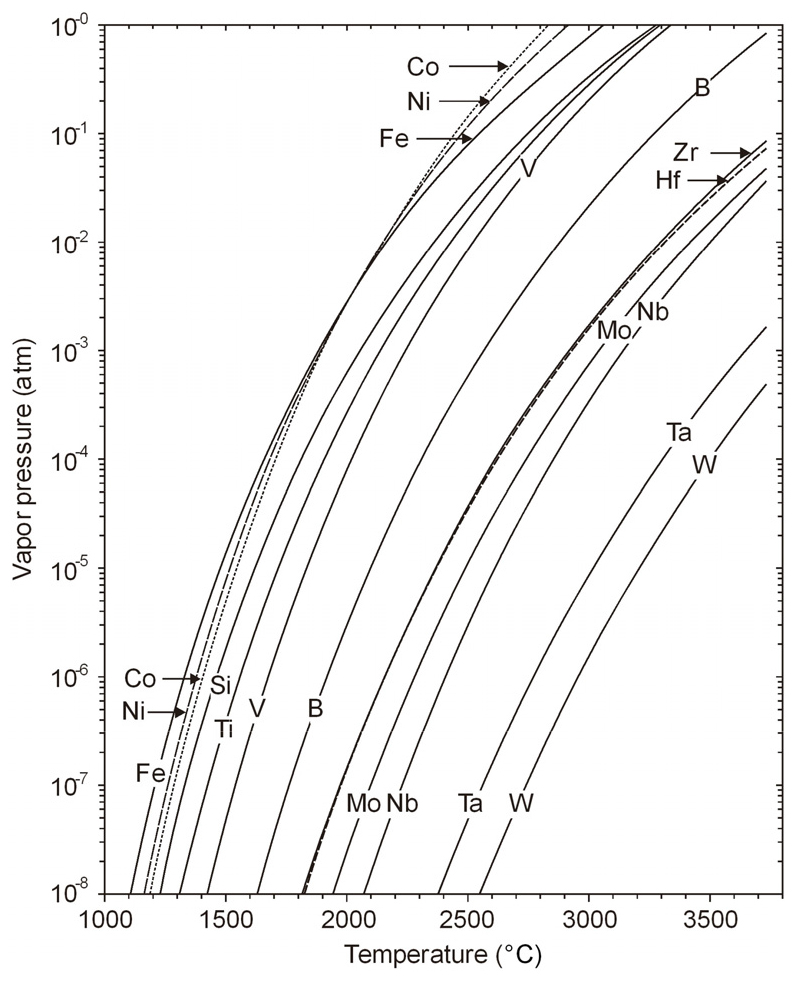
Fig. 8에는 Hf, Zr을 비롯한 몇 가지 원소의 온도에 따른 증기압을 계산하여 나타내었다40). 그림으로부터 EBM에 의해 고융점 금속인 W, Ta, Nb, Mo 등을 제외한 V, Ti, Si, Fe, Ni, Co 등의 금속 불순물을 제거할 수 있지만, Zr은 Hf과 증기압이 유사하여 제거할 수 없다. 그리고 질소는 제거되지 않으며, 산소는 용융 속도를 낮추면 400 ppm 이하까지 제거할 수 있다.24)
이러한 조금속의 증류 정제에 의한 불순물 제거 한계는 순수 상태의 증기압만으로는 구할 수 없으며, Hf과 불순물의 2원계나 다성분계에서의 증기압을 열역학적으로 검토하여야 한다. Hf-B 2원계에서 불순물 B의 증기압은 다음과 같다.
따라서 순수한 불순물의 증기압 가 순수 Hf의 증기압인 보다 높아도 조금속 중 불순물 B의 활동도()에 따라 제거 한계가 결정되므로 불순물 B의 증기압은 순수상태의 증기압 , 조금속 중 활동도 와 활동도계수 가 필요하다. 이러한 자료를 바탕으로 조금속 중 미량으로 함유되어 있는 불순물 B의 제거 한계를 구하여야 한다.
한편 평형상태의 용융 금속 표면에서 불순물 B의 증발속도()는 기체분자 운동론에 의한 다음의 Langmuir식으로 나타내며41), 는 불순물 B의 원자량(g/mol)을 나타낸다.
그러나 대부분의 증발 제거는 증발속도에 의해 율속되는 것은 아니며, 오히려 액체 금속 표면에서 불순물 기체의 물질이동에 의해 율속된다. 그리고 평형상태에서는 증발과 응축 속도가 같으므로 이 식은 용탕에서 가스상으로의 원자나 분자의 이동 속도를 나타내며, 임의의 온도에서 용매 A 중 용질 B의 상대적인 증발속도는 다음과 같다.
따라서 증발속도 비율인 가 높을수록 용매 금속 A의 손실을 줄이고 용질 B의 증발량을 증가시킬 수 있며, 로 가정할 수 있으므로 와 함께 에 관한 검토가 필요하다.
4. 하프늄의 리사이클링
Fig. 2에서 설명한 바와 같이 Hf은 항공우주 및 산업용 터빈의 초합금(45 %)이나 특수강(3 %) 등의 합금원소로 사용되며, 원자로의 제어봉(13 %)으로도 사용되고 있다. 원자로 제어봉 Hf은 고순도이지만 EoL 제품의 상세는 알려져 있지 않으며, 방사성 폐기물이어서 방사능이 소멸할 때까지 장기간 보관해야 하므로 사실상 리사이클링이 불가능하다. 그러나 제어봉 제조 공정에서 발생하는 스크랩은 리사이클링이 필요할 것이다.
한편 제트엔진이나 발전용 가스터빈에 사용되는 고온 재료인 Ni계 합금은 Hf의 함유율(0.1~0.2 wt%)이 낮아 Hf으로는 리사이클링되지 않으나 스크랩 자체가 고가이므로 Ni계 합금으로 리사이클링되는 것으로 추정된다. 1,300 ℃ 이상의 고온에서 사용할 수 있는 제3세대 고온 재료인 Ir-Hf계 합금은 Hf의 함유율(15 at%)도 높고 Ir이 고가의 귀금속이어서 향후 리사이클링이 필수적이지만, 고온 내열성 코팅재42) 등으로 사용된 것은 리사이클링이 곤란할 것이다. 공작기계용으로 이용된 EoL 제품도 Hf의 함유율이 낮아 Hf으로는 리사이클링되지 못하고 있다.
반도체 집적회로용의 Hf 산화막 제조시 CVD법에 사용한 폐타깃(waste target)은 EBM을 이용하여 리사이클링할 수 있다. 그러나 플라스마 전극으로 사용된 것은 탄화하프늄, 질화하프늄 등으로 Hf 함유량은 높으나 리사이클링 실태에 대해서는 잘 알려져 있지 않다43). 이와 같이 현재로서는 대부분의 Hf이 리사이클링 대상이 못 되고 있으나, 가격이나 수집 여하 및 사용량 확대에 따라 리사이클링 대상이 되는 스크랩이나 합금 등이 나올 것으로 생각된다.
한편 Hf 스크랩도 다른 금속들과 마찬가지로 제품 생산 공정에서 절삭 칩(chips)이나 반도체 산업에서 사용된 Hf 타깃 등을 리사이클링하기 위해서는 수집, 분류, 세척에 이어서 용융 및 정제가 필요하다. 그러나 Hf은 고융점(2,233 ℃) 금속이므로 Fig. 7에 나타낸 전자빔을 이용한 용융과 정제가 필요하다. Vutova 등은 Hf 절삭 칩을 전자빔 용융하여 정련 시간과 출력에 따라 Sn, Al, Mo, Fe, Ni 등을 제거하였다. Zr은 Hf보다 융점이 낮지만 Fig. 8에 나타낸 바와 같이 증기압이 유사하여 제거하지 못하였다44,45). Sehra 등은 Ca 열환원으로 제조된 규격외 Hf을 NaCl-NaF-HfCl4 혼합 용융염 중에서 전해정련하여 산소농도를 6,900 ppm에서 126 ppm으로 탈산하는 등 고순도 Hf으로 재생하기도 하였다46).
5. 종 합
금속 하프늄은 연간 생산량이 약 80 톤에 불과하며, 미국과 프랑스 등 일부 국가에서만 생산되는 핵심 희소금속이다. 이러한 Hf은 원자로의 제어봉, Ni계 초합금, 플라즈마 아크 금속 절단용 노즐, 반도체 집적회로 등 첨단산업에 필수적인 금속으로 향후 생산량 증대가 예상된다. Hf은 Zr 광석인 지르콘 중에 소량 함유되어 있어서 원자력 산업용의 고순도 금속 Zr을 생산하는 과정에서 부산물로 회수하고 있다. 금속 Hf은 지르콘을 분해한 후 회수한 Hf 염화물(HfCl4)을 Mg으로 환원하는 Kroll법이나 염화물의 용융염 전해법으로 제조하고 있으나, 산화물의 용융염 전해와 금속열환원법에 관해서도 연구되고 있다. 조금속 Hf은 아이오딘법이나 융용염 전해정련 및 전자빔 용융정제를 거쳐 고순도 Hf으로 정제한다. 특히 Hf의 전자빔 용융정제는 스펀지 Hf의 용융과 공정 스크랩의 리사이클링에 매우 유효한 방법이다. Ni계 초합금 등에 사용된 Hf은 함유량이 낮아 리사이클링 대상이 되지 못하지만 동일 합금으로 리사이클링 되는 것으로 추정된다. 기타 기계 가공용 등의 용도로 사용된 것도 함유량이 낮아 리사이클링 실태에 관하여 잘 알려져 있지 않다. 특히 원자력용으로 사용된 Hf은 방사성 폐기물이어서 리사이클링 대상이 되지 못하고 있다. 그러나 반도체용의 타깃 금속이나 가공 과정에서 발생하는 칩 등은 전자빔 용융 및 정제를 통하여 리사이클링하고 있다. 이러한 Hf은 전 세계 생산량 자체가 매우 적고 스크랩 발생에 관해서도 잘 알려져 있지 않아 리사이클링의 걸림돌이 되고 있다.