1. 서 론
2. 실험방법
2.1. 시료 준비
2.2. 침출 및 용매추출 실험
3. 결과 및 고찰
3.1. 시료 특성
3.2. 제강분진 침출
3.3. 제강분진 내 아연의 분리정제 공정
4. 결 론
1. 서 론
제강분진은 Electric Arc Furnace Dust라고 불리우며, 철강 생산 시 고온의 전기로혹은 전로에서 발생되는 분진을 일컫는다. 철을 생산 시 생산량의 약 1.5%의 분진이 발생하며 고철 원료의 종류나 처리공법에 따라 다소 차이가 있으나 약 20~40%의 아연, 10~25%의 철을 함유하고 있으며 이 밖에 납, 망간, 구리, 카드뮴등의 중금속을 비롯해 염소, 불소 등과 같은 음이온들도 함유하고 있다1,2,3,4). 이러한 분진류는 주요국가에서는 지정 유해폐기물로 정하고 폐기물 처리/관리에 규제를 두고 있다. 하지만 우리나라는 제강분진을 도로포장용 아스콘 충진재나 건설자재로도 활용할 수 있도록 허용하고 있으며 이럴 경우 중금속과 염소, 불소등의 이온들로 인한 토양 및 수질 오염을 발생할 수 있어 이에 대한 재활용 공정 개발이 요구되고 있다5). 제강분진을 재활용하는 공정은 주로 고온의 건식제련법을 적용하고 있다. 대표적인 공정인 Waelz kiln 법은 분진을 코크스 breeze와 혼합하여 로터리 킬른 내에서 환원해 조산화 아연을 회수한다. 하지만 해당 공정은 아연 농도가 60% 이상의 고농도 원료를 사용하고 있으며 조산화아연 뿐만 아니라 염화아연으로도 회수되어 제품의 순도를 떨어뜨린다. 또한 제강 분진 내 염소, 불소 성분에 의해 로내 내화벽돌 침식이 심해 킬른의 보수 및 유지비가 많이 소요되는 단점이 있다. 또 다른 건식제련 공정은 RHF(Rotary Hearth Furnace)로 알려진 공정이다. 원형의 회전로에서 고온 환원 반응을 진행하며, 철 산화물과 폐기물을 미분탄으로 환원하여 철은 직접환원철로 회수한다. 그리고 아연의 경우 분진으로 발생하여 Bag filter에서 회수를 하며 이때 아연의 품위는 약 79%이다. 하지만 5% 미만의 아연을 함유한 제강분진만 처리가 가능하다. 이는 공정 중 산화아연에 따른 blockage가 발생하기 때문이다. 또한 조업 면에서도 kiln 법에 비해 높은 온도인 1250℃이상에서 반응을 하여 고에너지가 필요한 단점이 있다1,6,7). 이 밖에도 Waelz kiln 법을 변형한 HTR 공정, Plasma를 활용한 공정, 용융환원 공정등이 있다. 제강분진을 습식 제련으로 재활용하는 공정은 매우 드물다. 대표적으로 EZINEX 공정이 있는데, 이는 침출액으로 염화암모늄을 사용하여 아연, 카드뮴, 구리, 니켈, 은, 납 등을 염화암모늄 복합물의 형태로 침출한다. 춤출 후 아연은 전해채취를 통해 고순도의 아연을 금속으로 회수하는 공정이나 아연 회수율이 50% 전후로 매우 낮은 단점이 있다8). 이 밖에 강산을 사용하여 침출을 하거나, 고온고압에서 아연을 전량 침출하는 공정은 있으나 철이 같이 침출되기 때문에 철을 과다한 알칼리 용액을 이용해 제거하는 공정이 필요한 단점이 있다. 이러한 점을 극복하기 위한 다양한 습식제련에 대한 연구가 진행되었으나 대부분 침출에 대한 내용만 언급하고 아연을 고순도로 회수하는 공정까지 이야기하고 있지 않는다. 따라서 본 연구에서는 제강분진으로부터 아연을 선택적으로 회수하여 가축 사료, 비료, 가죽/목재용 방부제, 정수, 부유선별 공정, 탈황 공정 등 다양한 산업에 적용 가능한 고순도의 황산아연까지9) 고부가가치화하는 일괄 습식 공정에 대해 소개하고자 한다.
2. 실험방법
2.1. 시료 준비
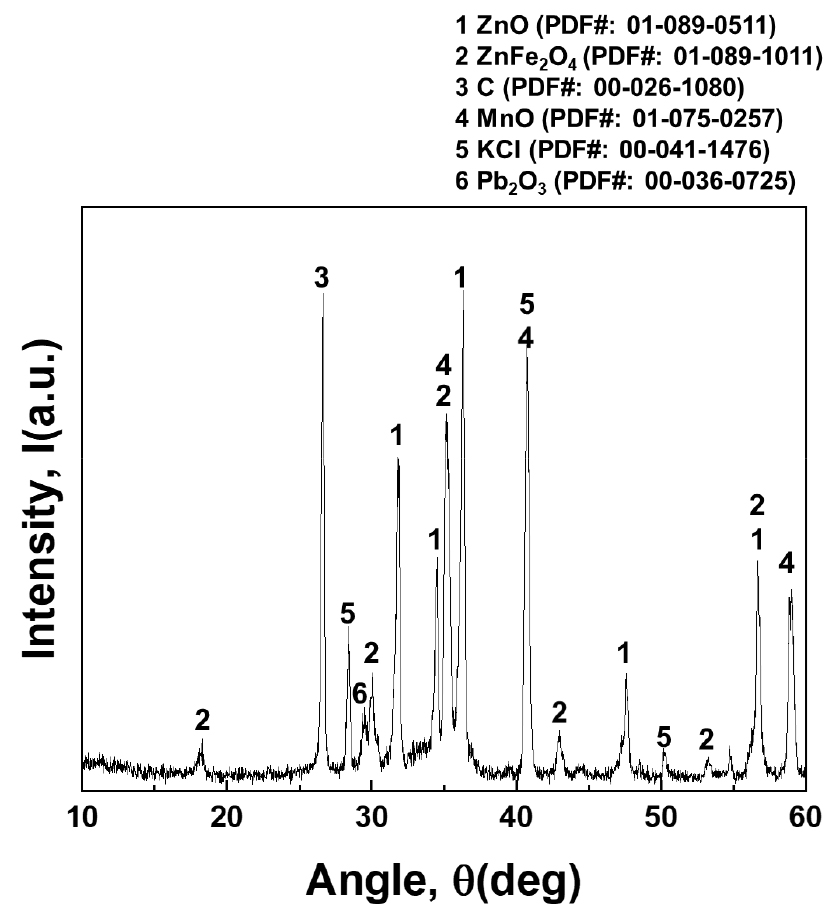
본 연구에서 사용한 국내 발생 제강분진은 육안상 짙은 갈색의 분말로 이루어져 있었다. 제강 분진이긴 하나 일부 분진이 뭉쳐서 딱딱한 덩어리로 되어 있는 부분들도 있어서 로드밀을 이용해 75μm 이하로 분쇄하여 사용하였다. 사용한 제강분진을 유도결합플라즈마(ICP, Inductively Coupled Plasma, Optima 8300, PerkinElmer, USA)를 이용하여 함유하고 있는 원소를 분석하여 Table 1에 나타내었다. 또한 XRD(X-ray diffraction, SmartLab, RIGAKU, JAPAN) 분석을 통해 시료의 결정 구조를 살펴보았으며, 그 결과를 Fig. 1에 나타내었다.
Table 1.
The content of elements in electric arc furnace dust (%)
| Elements | Zn | Fe | Mn | Pb | Ca | Mg | Cd | Na | K |
| Content (%) | 22 | 9.9 | 19 | 0.96 | 5.3 | 0.6 | 0.04 | 1.3 | 4.3 |
2.2. 침출 및 용매추출 실험
아연의 선택적인 회수를 위한 습식제련 공정으로 본 연구에서는 산침출공정과용매추출 공정을 수행하였다. 침출공정은 75μm 이하로 분쇄된 제강분진을 Heating mantle에 고정한 5 neck round bottom flask에 Sulfuric acid(H2SO4, Samchun, Korea)와 혼합하여 수행하였다. 변수실험으로 황산 농도, 침출 온도, 고액비에 따라 수행하였으며 교반속도는 250rpm으로 조건을 고정하였다. 용매추출 공정은 용매로 Di-(2-ethylhexyl) phosphoric acid(상업명 D2EHPA)를 정제없이 Kerosene(Junsei, Japan)으로 희석하여 사용하였으며, Sodium hydroxide(NaOH, Duksan, Korea)를 이용하여 용매를 비누화(Saponification)하였다. 변수 실험으로 O/A 비율에 따른 실험을 수행하였다. 아연과 공동추출된 금속이온들의 세정을 위하여 H2SO4를 이용해 pH를 1~5.5로 조정한 수용액을 사용하였다. 불순물을 세정한 후 아연은 1.5M H2SO4를 이용하여 탈거하여 ZnSO4 용액을 제조하였으며, 제조된 ZnSO4 용액은 Vacuum evaporator(R-215, BÜCHI, Switzerland)를 이용하여 90℃에서 ZnSO4 분말을 얻었다. 실험 중 획득한 용액의 분석은 모두 ICP를 활용하여 분석하였다.
3. 결과 및 고찰
3.1. 시료 특성
본 연구의 사용된 제강분진은 기존 제강분진에 비해 특이점이 있다. 기존에 알려진 제강분진의 경우 주 성분이 아연과 철로 이루어져 있어 아연이 15~30%, 철이 20~40% 함유되어 있다10,11,12,13,14,15). 하지만 Table 1에서 보다 시피 본 제강분진에는 아연이 22%, 철은 10% 함유되어 있으며, 다른 제강분진과 다르게 망간이 19% 함유되어 있었다. 이러한 망간이 제강분진에 많이 함유되어 있는 것은 제강 공정에서 사용되는 고철 중 망간을 함유한 스크랩을 활용하거나, 페로망간 제조 공정에서 발생되는 함 망간 분진이 같이 포함되어 있을 것으로 사료된다16,17). Fig. 1의 제강분진 XRD 결과에서도 제강분진 내에 ZnO, ZnFe2O4 외에 MnO, C, KCl, Pb2O3도 함유되어 있는 것을 볼 수 있다. 또한 원료 내에 C도 같이 관찰이 된다. 이는 페로 망간 공정 중 전기로(Elacric furnace)에서 발생된 망간 분진에 Carbon이 많이 함유되어 있기 때문이다17). 즉 해당원료는 제강분진과 페로 망간 제조 공정 중 전로(Converter)가 아닌 전기로에서 발현된 망간분진의 혼합물로 판단이 된다. 따라서 앞으로 제강분진의 원료가 망간분진과의 혼합물이 될 수 있기 때문에 변화하는 제강분진 내 금속 함유량을 정확히 파악하고 이에 적합한 공정의 개발이 필요할 것이다.
3.2. 제강분진 침출
3.2.1. 제강 분진 침출의 열역학적 평가
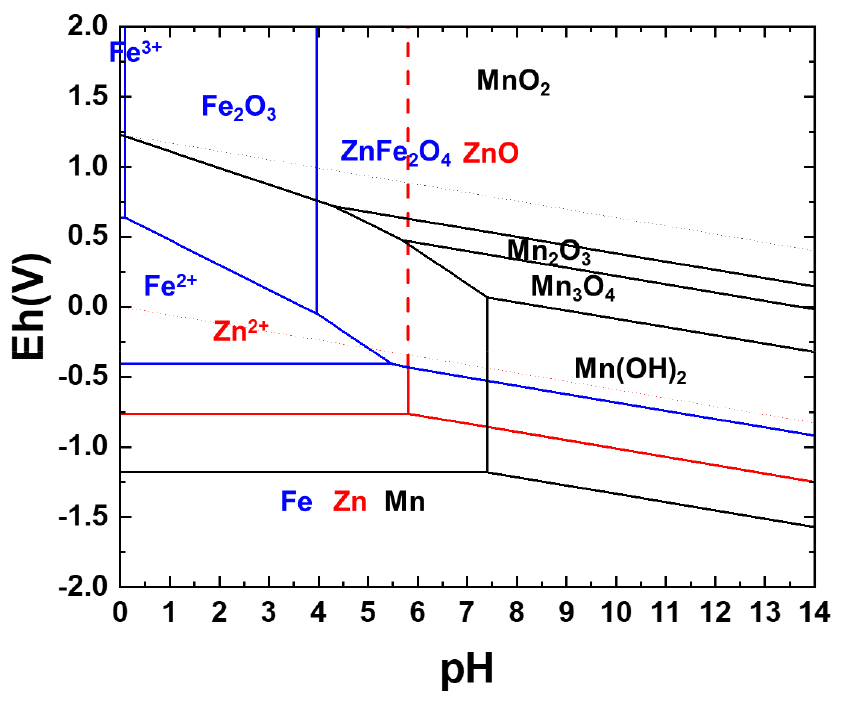
Fig. 2에 Zn-Fe-Mn-S-H2O의 25℃에서 Eh-pH diagram을 나타내었다. ZnFe2O4의 경우 열역학적으로 pH 4이하에서 황산에 의한 아연의 용해가 가능할 것으로 사료되며 철의 경우 pH를 낮추어 ferric ion으로 용해하거나 Eh를 낮추어 ferrous ion으로 용해가 가능할 것으로 보인다. 하지만 ZnFe2O4의 침출 반응속도가 느리거나 침출액의 pH가 4이상으로의 변화에 따라서는 ZnFe2O4가 용해되지 않을 수도 있다. 제강분진 시료내에 ZnO의 경우 pH 5.8이하로 유지될 경우 아연이 황산에 열역학적으로 용해될 수 있다. 다만 pH가 5.8 이상에서는 ZnO로의 침전이 될 수 있기 때문에 침출액의 pH를 적정하게 유지하는 것이 중요하다. Mn의 경우 주로 MnO로 존재하기 때문에 황산에 안정적으로 용해가 될 것으로 판단된다. 아래 제강 분진 내 화합물들의 침출 반응을 나타내었다.
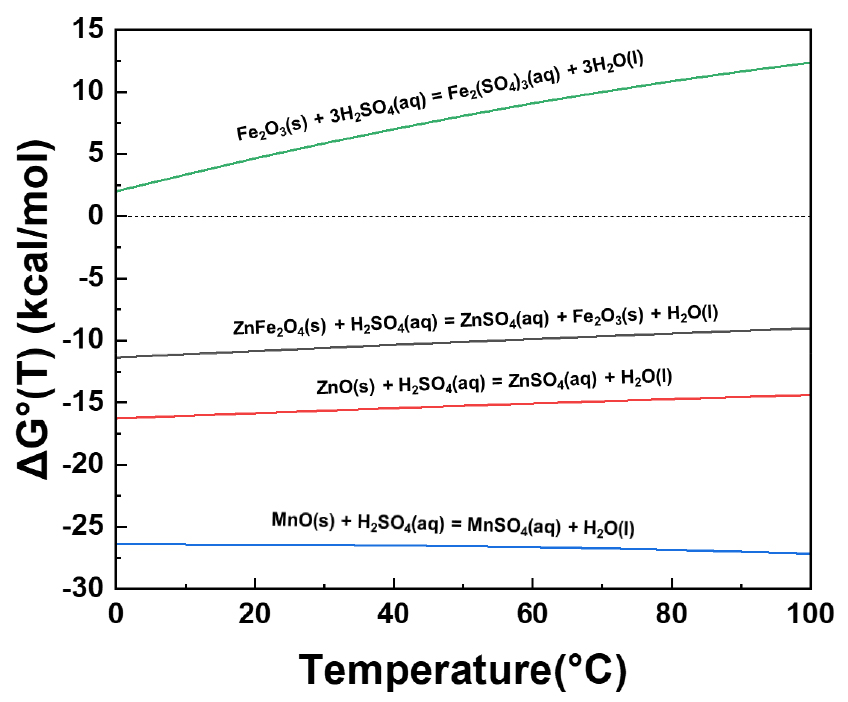
위 반응식에 대해 온도에 따른 Gibbs free energy(ΔG°)을 구하여 그래프로 표현하면 Fig. 3과 같다. Fe2O3의 용해반응은 열역학적으로 어려우며, Fig. 2에서와 같이 황산의 농도를 높혀 pH를 낮출 경우 ferric ion(Fe3+)로 용해될 수 있을 것이다. 반대로 ZnFe2O4, ZnO, MnO 는 황산에 의해 각각 아연, 망간이 용해가 될 것으로 사료되나 ZnFe2O4의 경우 앞에서 언급한 바와 같이 pH가 4이하이거나 반응 속도에 영향을 받을 것으로 사료된다. Fig. 2와 Fig. 3을 살펴보았을 때 아연의 침출률을 높이기 위해서는 pH를 낮추어서 ZnFe2O4의 아연을 같이 침출하여야 하지만 이 때는 철도 불순물로 같이 침출될 수 있기 때문에 철의 침출을 억제하기 위해서는 침출액의 pH를 4~5.8로 제어할 필요가 있다.
3.2.2. 제강 분진 침출 실험
제강분진을 1M 황산을 이용하여 고액비 10%, 20%에서 6시간 침출을 진행하였으며, 금속의 침출률과 침출액의 pH를 Table 2에 나타내었다.
Table 2에서 살펴보듯이 고액비 10%에서의 침출액의 pH는 1.69로 낮은 pH를 나타내었다. 이에 따라 아연과 망간의 침출률이 각각 96%이었다. 또한 철의 침출률은 22% 이었다. 이는 앞서 Eh-pH diagram에서 보듯이 낮은 pH에서의 ZnFe2O4 내의 아연, 철의 용해가 동시에 이루어 졌음을 나타낸다. 반면에 고액비를 20%로 높일 경우 침출액의 pH는 6이며 이 때 철의 침출은 이루어 지지 않는다. 고액비를 증가할 경우 pH의 증가는 제강분진의 아연과 망간의 침출에 따라 물분자를 형성, 즉 수용액 중의 수산화이온(OH-)이 증가하기 때문으로 사료된다. 또한 10% 고액비 보다 pH 증가량이 20% 고액비에서 더 높은 것은 시료내 침출되는 아연과 망간의 절대 농도가 높음과 동시에 발생되는 수산화이온이 증가하기 때문으로 사료된다. 실제 10% 고액비 침출에서의 아연, 망간의 농도는 각각 20.7g/L, 20.0g/L임에 반해 20% 고액비 침출에서의 아연, 망간의 농도는 각각 31.5g/L, 30.3g/L로 증가하였다. 다만 고액비를 증가할 경우 침출액의 pH 증가에 의해 철의 침출률은 억제할 수 있으나 아연의 침출률은 감소시켰으며, 이 때의 아연 침출률은 75% 이었다. 이는 pH 영향으로 침출 중 아연이 ZnO로 재침전이 되었거나 시료 내의 ZnFe2O4의 침출이 완전히 이루어지지 않았기 때문이다. 두번째는 온도에 따라 침출 실험을 진행하였다. 온도는 50, 60, 70, 80℃에서 6시간 동안 1M 황산을 이용하여 고액비 20%에서 진행하였으며 그 침출률 결과를 Table 3에 나타내었다. Table 3에서 살펴보듯이 60℃ 이상에서 침출 온도가 증가할수록 아연의 침출률이 감소하였다. 이는 pH의 증가와 관련이 있는데, 침출 온도가 증가할수록 망간의 침출률이 증가하여 pH의 증가에 기여한 것으로 판단된다. Eh-pH diagram 상 아연의 ZnO로의 침전이 망간의 침전 범위보다 pH 값이 더 낮음을 알 수 있다. 이에 따라 pH 증가 시 아연의 ZnO로의 침전이 발생하는 것으로 사료된다. 50℃의 결과는 이와는 반대로 아연의 침출률이 60℃에 비해 더 감소한다. 이 역시 50℃ 실험에서의 pH와 관련이 있는데, 60℃ 침출액의 pH 보다 높음을 알 수 있다. 이 때의 망간의 침출률이 상대적으로 높았으며, 이에 따라 50℃의 침출에서 아연이 ZnO로 침전이 발생하는 것으로 판단된다. 온도에 따른 제강분진의 아연, 망간의 침출 경향은 일정하지 않았으나, 1M 농도의 황산을 사용하여 침출 할 경우 망간, 아연의 침출에 따라 침출액의 pH 제어에 매우 민감함을 알 수 있었다. 따라서 침출에 따른 pH의 제어를 하기 위하여 황산의 농도를 높여 침출 실험을 진행하였다.
Table 2.
The leaching efficiency of elements with S/L ratio (%)
| S/L ratio | Zn | Fe | Mn | Pb | Cd | pH |
| 10% | 96 | 22 | 96 | 1 | 96 | 1.69 |
| 20% | 73 | 0 | 72 | 0.8 | 85 | 6.00 |
Table 3.
The leaching efficiency of elements with temperature (%)
| Temperature | Zn | Fe | Mn | Pb | Cd | pH |
| 50℃ | 30 | 0 | 81 | 0.8 | 87 | 6.38 |
| 60℃ | 73 | 0 | 72 | 0.8 | 85 | 6.00 |
| 70℃ | 10 | 0 | 68 | 0.7 | 88 | 6.59 |
| 80℃ | 5 | 0 | 66 | 0.6 | 89 | 6.76 |
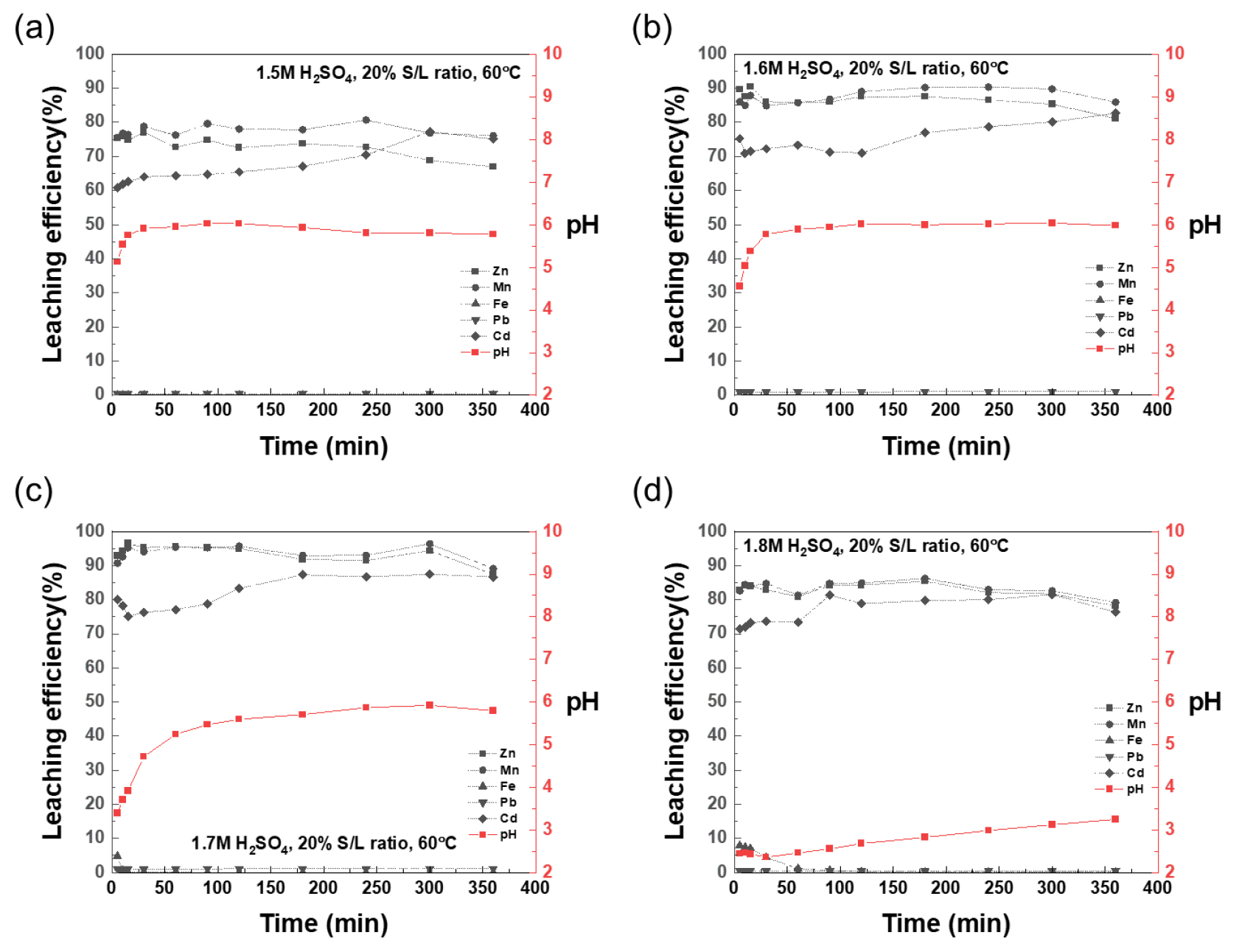
황산 농도에 따른 침출 실험의 경우 황산 농도를 1.5, 1.6, 1.7, 1.8 M 로 조정하여 실험을 진행하였다. 1.8M 이상으로 황산의 농도를 높이지 않은 것은 침출액의 pH가 낮아져 철을 침출 시키기 때문이다. 황산 농도에 따른 시간별 금속의 침출률을 Fig. 4에 나타내었다. Fig. 4를 살펴보면 대부분 침출 반응이 반응초기에 이미 완료됨을 알 수 있다. 30분에 침출 반응이 완료된 후 이후에 360분까지 침출률은 크게 증가하지도 감소하지도 않았다. 제강분진 산 침출 시 반응시간을 6시간 이상 침출하는 것은 비효율적이다. 이에 따라 적정한 침출 시간을 설정할 필요가 있을 것이다. pH의 변화는 1.5, 1.6, 1.7M 황산 실험의 경우 점차 증가하여 6부근에서 안정한 영역을 나타내며, 1.8M 황산 실험에서는 3.5 이하로 낮은 값을 나타내었다. 철의 침출의 경우 1.8M에서 반응 초기 10%까지 침출 되었다가 점차 침전하여 낮아지기는 하였으나 침출이 끝날 때까지 침출액 내에 수십 ppm의 철이 잔류하였다. 1.7M 황산 실험에서는 높은 아연의 침출률을 획득할 수 있었으나 반응 초기에는 pH가 낮아 침출액 내 철이 잔류하였다. 침출액 내 철이 존재하지 않을 때 시간은 4시간 침출을 수행하였을 경우이다. 반면에 1.6M 황산 침출의 경우 침출 초초부터 철은 침출되지 않았으며 아연의 침출률 역시 85%를 유지하였다. 침출 시간의 경우 반응 효율과 pH의 안정함을 유지하기 위하여 1시간을 최적 조건으로 설정하였다. 최종적으로 1.6M 황산, 고액비 20%, 침출 온도 60℃, 1시간 반응을 통해 아연의 침출률 85%, 망간의 침출률 85%를 얻었으며, 이 때 철은 침출되지 않았다.
3.3. 제강분진 내 아연의 분리정제 공정
3.3.1. 아연의 용매추출
침출 실험에서 획득한 침출액의 조성을 Table 4에 나타내었다. 아연이 38.6g/L,망간이 41.4g/L 함유되었으며 그밖에 Pb, Cd, K, Na 등이 존재하고 pH는 5.98이었다. 침출액에서 아연을 선택적으로 회수하기 위해 용매추출 공정을 적용하였다. 아연 외 최대 불순물이 망간이므로 망간으로부터 아연을 선택적으로 추출하는 용매를 선택하여야 하며, 대표저인 양이온 추출제인 D2EHPA를 사용하였다. D2EHPA에 따른 금속 양이온의 추출 경향은 다음과 같이 잘 알려져 있다; Zn2+>Mn2+>Cd2+18).
Table 4.
The concentration of elements in leaching solution and feed solution (mg/L)
| Elements | Zn | Fe | Mn | Pb | Cd | Na | K | pH |
| Leaching solution (mg/L) | 38600 | 0 | 41400 | 15.2 | 34 | 8210 | 1591 | 5.98 |
| Feed solution (mg/L) | 19110 | 0 | 24060 | 4.8 | 25.7 | 5058 | 1116 | 5.75 |
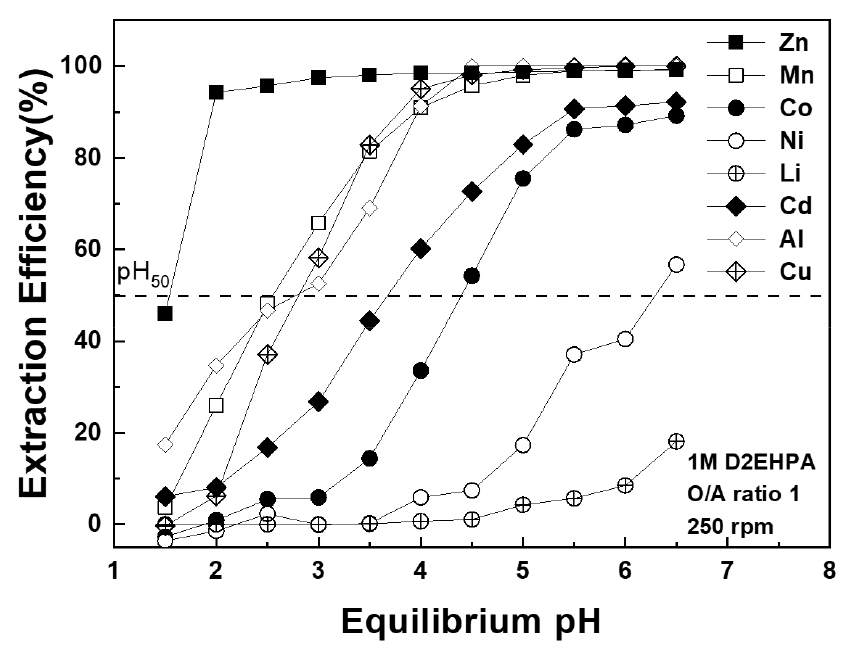
Fig. 5에 나타낸 1M D2EHPA의 pH isotherm 실험 결과에 따르면 아연과 망간의 분리 경향을 나타내는 ΔpH50 값이 1임을 알 수 있다19). 이러한 결과에 의해 D2EHPA를 추출제로 하여 평형 pH를 1.5~2 사이에서 아연과 망간의 분리가 가능할 것으로 사료된다. D2EHPA에 의한 추출반응식은 아래와 같다.
위 반응을 살펴보면 수상(aueous phase)의 금속이온을 추출하면 용매의 수소이온이 수용액상으로 이동하는 것을 알 수 있다. 즉, 금속이온을 추출하면 할수록 수상 내 수소이온의 농도가 증가하게 되고 이는 수상의 pH를 낮추는 원인이 된다. 수상의 pH가 낮아지게 되면 Fig. 5에서 살펴보듯이 금속의 추출률은 낮아지게 된다. 따라서 수상의 pH를 낮아지지 않게 하기 위해서 용매를 수산화나트륨으로 비누화하였다. 아래 용매의 비누화도 반응식을 나타내었다.
[NaOH]는 비누화 반응에 사용한 수산화나트륨의 농도(M), [D2EHPA]는 용매의 농도(M), VNaOH와 VD2EHPA는 각각 비누화 반응에 사용한 수산화나트륨과 용매의 부피(L)를 나타낸다. 이러한 용매의 비누화 반응을 통해 용매의 수소이온의 일부를 나트륨 이온으로 대체하게 된다. 이럴 경우 금속이온을 추출할 때 수소이온 대신 나트륨 이온을 수상으로 이동시켜 수상의 pH 감소를 막게 된다. 비누화된 용매의 금속 추출 반응식은 아래와 같다.
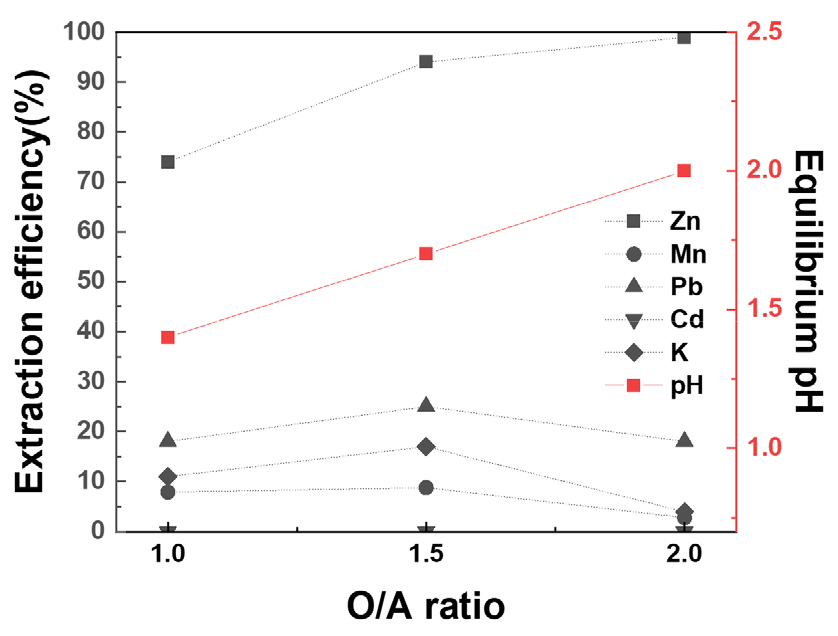
본 실험에서는 0.8M D2EHPA에 32% 비누화도를 적용하여 O/A 비율를 조정하여 용매추출을 진행하였다. 용매추출에 사용한 모액(Feed solution)은 금속 농도를 일정하게 유지하기 위해 3차 증류수를 이용하여 희석하였으며 그 농도를 Table 4에 나타내었다. O/A 비는 1, 1.5, 2로 조정하고 향류 3단에서 실험을 진행하였다. 그 실험 결과를 Fig. 6에 나타내었다. 아연은 O/A 비가 높아질수록 추출률이 증가한다. 이는 raffinate의 평형 pH 증가와 관련이 있다. 반면 망간은 추출률이 O/A 비 증가에 따라 감소한다. 이는 D2EHPA에 의한 추출 경향이 아연이 망간에 비해 높기 때문에 향류 다단 추출이 진행되는 동안 추출된 망간이 수상 내의 아연과 교환을 통해 추출이 이루어지기 때문으로 사료된다. 기타 공동 추출되는 납은 추출률은 높으나 모액내 농도가 매우 낮기 때문에 추출된 농도는 상당히 낮은 0.45mg/L이다. 최종적으로 O/A 비 2에서 아연은 99% 추출이 되었으며, 망간은 2.8% 공동 추출이 되었다.
3.3.2. 불순물 세정 및 황산아연 제조
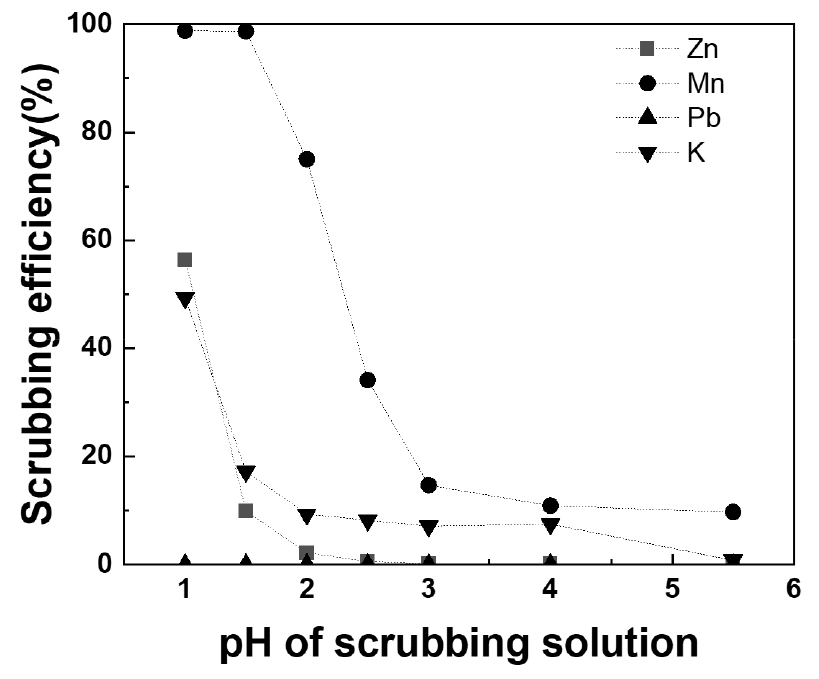
공동추출된 망간을 제거하기 위해 pH를 조정한 황산 수용액을 사용하여 세정 실험을 수행하였다. pH는 1~5.5로 조정한 황산 수용액이며 O/A 비율은 1이며 5회 연속 세정을 수행하였고 5회 세정 후의 세정률을 Fig. 7에 나타내었다. 망간의 경우는 pH 1과 pH 1.5 두 세정액에서 모두 세정되고 pH가 상승하면 세정률은 감소하였다. 아연과 칼륨 역시 마찬가지 이며 pH 1 세정액에서는 아연의 세정률이 58%이므로 망간이 전량 세정되더라도 적정한 세정은 아닐 것으로 판단된다. 따라서 세정액은 pH 1.5로 조정한 황산 수용액을 적정 세정액으로 판단하였으며, 이 때 아연의 세정률은 10% 이다. 하지만 해당 세정액은 망간의 함유량이 330mg/L로 낮으므로 침출액에서 모액을 제조할 때 희석 용액으로 충분히 재사용이 가능할 것으로 사료된다.
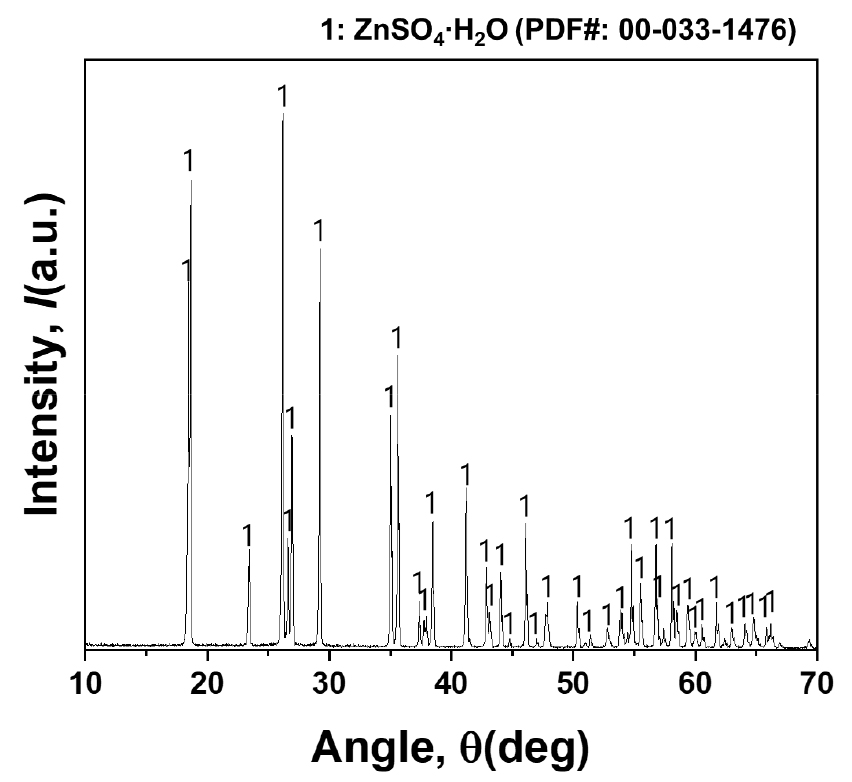
세정 후 Loaded organic으로부터 1.5M 황산을 이용하여 향류 3단 탈거 실험을 수행하였다. 이 때 O/A 비는 4로 고정하였으며 O/A 비를 높인 것은 탈거액에 아연을 농축하기 위함이다. 최종적으로 아연은 99% 탈거되었으며, 탈거액에는 40g/L의 아연, 1.2mg/L의 망간이 함유되어 있었다. 회수한 탈거액으로부터 90℃에서 감압증류를 실시하였으며 얻어진 산물은 필터 후 90℃ 오븐에서 건조하였다. 건조 후 분말의 성상을 XRD를 통해 분석하였으며 그 결과를 Fig. 8에 나타내었다. 성분은 ZnSO4∙H2O(Zinc sulfate hydrate) 이었으며 순도는 99.9% 이었다.
4. 결 론
본 연구에서는 제강 분진으로부터 습식제련 공정울 통해 아연을 선택적으로 회수하였다. 먼저 제강분진은 아연의 함량은 22%이나 기존의 잘 알려진 제강분진과 다르게 철의 함량이 9.9%로 상대적으로 낮고, 망간의 함량이 19% 높았다. 따라서 이에 적합한 습식제련 공정을 설계하였으며, 1.6M 황산, 고액비 20%, 60℃, 1시간 반응을 통해 아연과 망간을 85% 침출하였다. 이 때 침출액의 pH는 자연스럽게 5 이상으로 높아지므로 철은 침출되지 않았다. 망간으로부터 아연을 선택적으로 회수하기 위해 D2EHPA를 이용하여 용매추출 실험을 수행하였으며, 0.8M D2EHPA, 32% 비누화도, O/A 비 2, 향류 3단 추출을 통해 아연을 99% 추출하였다. 이 때 공동추출된 망간은 pH 1.5로 조절한 황산 수용액으로 5회 세척하여 모두 세정할 수 있었다. 최종적으로 아연은 1.5M 황산, O/A 비 4, 향류 3단 탈거를 통해 농축, 탈거하였으며 탈거액에는 40 g/L 아연을 함유하고 있었다. 탈거액으로부터 감압증류를 통해 황산아연 1수화물을 제조하였으며, 순도는 99.9%이었다.