1. 서 론
글로벌 온실가스 감축 정책으로 인하여 전기자동차(Electronic Vehicle, EV) 시장이 크게 성장하고 있으며, 연료전지, 태양광, 풍력 등 신재생 에너지와 연계된 에너지저장장치(Energy Storage System, ESS)의 사용이 크게 증가함에 따라 리튬이온전지 사용이 급증하고 있다1,2). 그로 인해 리튬이온전지의 리튬, 니켈, 코발트, 망간 등 핵심 금속소재의 가격이 급등하는 문제와 전량 수입에 의존하고 있는 가운데 최근 코로나19로 인한 노동 수급 이슈, 운송 차질, 공장 가동 중단, 봉쇄 장기화 등으로 인해 수급이 불안정한 상황이다3). 일반적으로 EV나 ESS에 사용되는 전지는 대략 10년정도 사용하면 전지의 용량이 감소하여 폐기되며, 향후 폐전지 발생량이 급증할 것으로 예상되므로 폐전지에서 리튬, 니켈, 코발트, 구리 등 유가금속을 회수하여 재사용하는 기술이 필요하다. 현재 전기자동차나 에너지저장장치에서 발생하는 폐리튬이온전지 내 유가금속 종류 및 조성은 매우 다양하나 대략 25.8 ~ 29.1 %의 니켈, 3.5 ~ 8.4 % 코발트, 3.9 ~ 4.7 % 리튬, 3.6 ~ 4.1 % 알루미늄, 3.0 ~ 3.3 % 구리, 0.03 ~ 0.8 % 망간 등의 유가금속을 함유하고 있으며, 방전 및 해체공정을 통해 양극활물질을 분리하여 이후 파쇄, 침출, 용매추출, 분리·정제, 증발·결정화 공정을 통해 황산코발트, 황산니켈 및 탄산리튬 또는 인산리튬으로 회수하고 있다4,5,6,7). 회수된 유가금속화합물은 양극활물질 재사용을 위한 연구가 계속되고 있으며, 일부 재활용 황산니켈의 경우 전해도금액 제조에 사용되고 있다. 코발트는 절삭공구 및 초경합금 소재로 많이 사용되고 있고, 니켈은 세계 시장에서 주로 스테인리스강, 특수강, 도금, 주물, 화학 등에 사용되며, 특히 스테인리스용 수요가 약 60 %, 기타 합금 제조부문의 수요가 약 30 %를 차지하기 때문에 다양한 산업에 사용되기 위해서는 고순도 잉곳과 같은 금속 소재화 공정이 필요하다8). 본 연구에서는 코발트, 니켈 및 구리 소재화를 위한 전해채취(electrowinning) 공정에 대한 전기화학적 반응속도론적 연구를 수행하였다. 회전원판전극(Rotating Disc Electrode, RDE)를 사용하여 전해액 온도 및 교반속도에 대한 전해조건의 반응율속단계를 규명하고자 하였다.
2. 실험방법
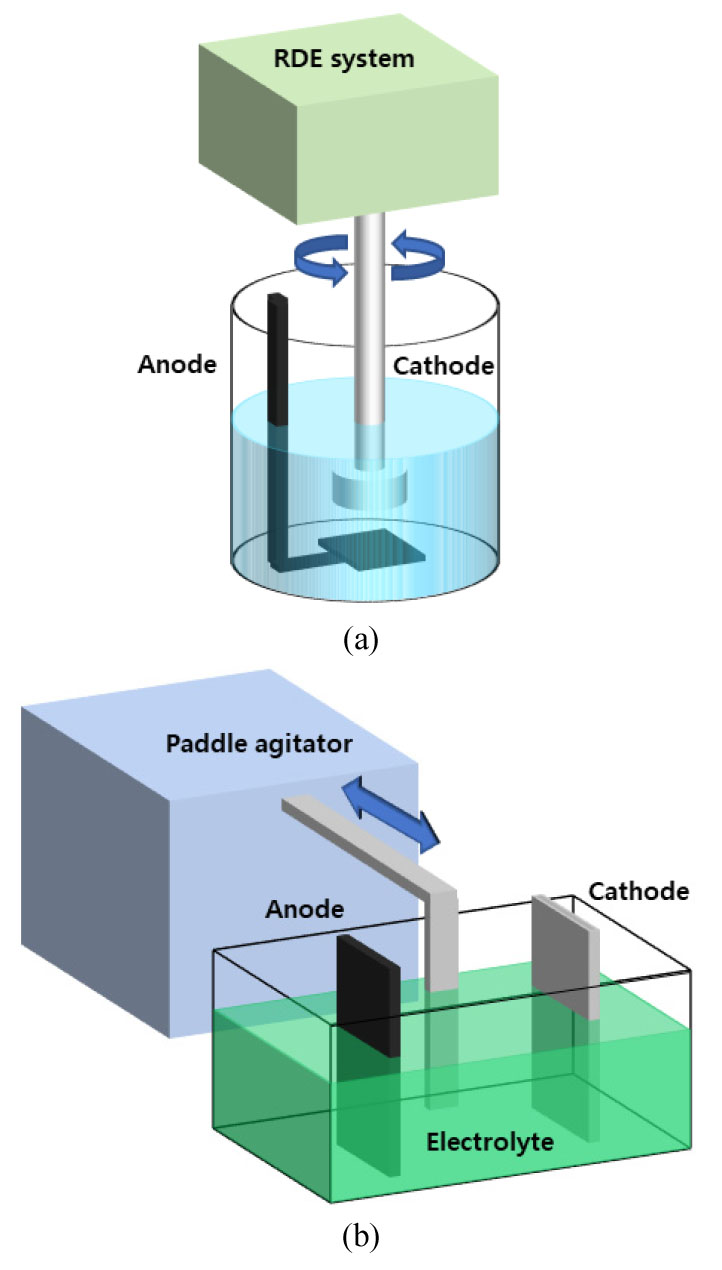
Fig. 1(a)와 같은 RDE시스템을 이용하여 전기화학적 실험을 수행하였다. 고순도 분리‧정제액 성분을 기준으로 제조한 니켈, 코발트 및 구리의 모의 제조용액을 각각 40, 50, 60 및 70 ℃ 온도에서 치수안정성 전극(DSA, Dimentionally Stable Anode)을 counter 전극으로 사용하였다. 99.9 % 이상 순도를 가지는 1 mm 두께의 티타늄판을 면적 1 cm2의 원형으로 가공하여 working 전극으로 사용하였고, Ag/AgCl saturated KCl을 reference 전극으로 사용하였다. Potentiostat(Princeton Applied Research社, VersaSTAT 4) 장비로 니켈 전해채취 2.85 V, 코발트 전해채취 2.5 V 및 구리 전해채취 2.75 V의 전압을 각각 10, 20, 30, 40, 50분간 인가하여 실험하였고, 이후 전해액 내 니켈, 코발트 및 구리의 함유량 감소량을 측정하였다. RDE 시스템을 이용하여 구한 반응율속단계 결과를 전해채취 공정인자 중 전해액 온도와 교반속도 변화에 따른 전해채취층의 전류효율 변화 결과와 비교를 통해 검증하고자 하였다. 전해채취 공정에 사용한 전해액은 현장의 폐리튬이온전지로부터 분리, 파쇄, 침출, 분리‧정제 및 농축 공정으로 회수하고 있는 고순도 유가금속 용액의 금속 농도 및 pH를 동일하게 제조하고자 하였다. 황산니켈, 황산코발트 및 황산구리를 사용하여 전해액을 제조하였고, pH는 황산을 사용하여 보정하였다. 전해액의 주요조성을 Table 1에 나타내었다.
Fig. 1(b) 모식도에서와 같은 구조의 전해장치에 있어서 양극은 치수안정성 전극을 사용하였고, 음극은 티타늄 판을 SiC 연마지로 연마하여 사용하였다. 전원공급장치(YPP15030, YAMAMOTO)를 이용하여 Table 1에 언급한 전류밀도를 인가하여 3 시간 공정을 수행하였다. 전해채취 후 전착층의 무게를 정밀저울로 측정하여 아래 식 (1)과 식 (2)를 이용하여 전류효율을 구하였다.
- 이론 전착량(Theoretical Quantity of Electrodeposition)
WT = Mass of metal (g)
A = Atomic weight of metal (g/mol)
I = Current (A)
t = Time
n = Number of electrons transferred
F = Faraday’s constant (C/mol)
Z = Electrochemical equivalent (A/nF)
- 전류효율(Current efficiency)
Table 1.
Concentration of chemical reagents in electrowinning electrolyte
3. 결과 및 고찰
전해채취 반응은 물질전달(mass transfer)과 전기화학반응(electrochemical reaction)을 포함하는 비균질반응으로 이루어지며, 전해액과 전극의 계면에서 대류 확산, 전자 이동 및 전기화학반응과 같은 여러 가지 반응이 순차적으로 발생한다. 안정적인 전해채취 공정을 유지하기 위해서는 반응기구를 규명하여 공정인자 제어가 필요하다. 이러한 반응기구는 RDE를 이용하여 Koutecký-Levich법으로 규명이 가능하다9). 일반적으로 hydrometallurgy 반응에서의 활성화에너지값이 3 ~ 4 kcal/mol인 경우 물질전달율속, 11 ~ 12 kcal/mol인 경우 화학반응율속, 중간값은 혼합율속이라고 알려져 있다. 니켈, 코발트 및 구리의 전해채취에 관한 반응기구(reaction mechanism)를 규명하기 위해 RDE 시스템을 이용하여 니켈, 코발트 및 구리 전해채취를 수행하였다. 전해채취 공정시간이 지속될수록 코발트, 니켈 및 구리의 전착량이 증가하고, 이에 전해액 내 금속농도가 감소하였다. 이때 감소량 추이의 기울기를 통해 반응속도 계수를 구하였다. 반응속도 계수와 온도의 역수 관계를 Arrhenius 식으로 나타내었고, 식 (3)에 의해 니켈, 코발트 및 구리의 활성화에너지를 구하여 니켈, 코발트 및 구리의 전해채취 공정의 반응율속단계를 규명하였다.
k = Chemical reaction rate
A = Pre-exponetial factor
Ea = Activation energy
R = The gas Constant (1.987 cal⋅mol−1⋅K−1)
T = Temperature in Kelvin
3.1. 니켈 전해채취 반응속도론적 고찰
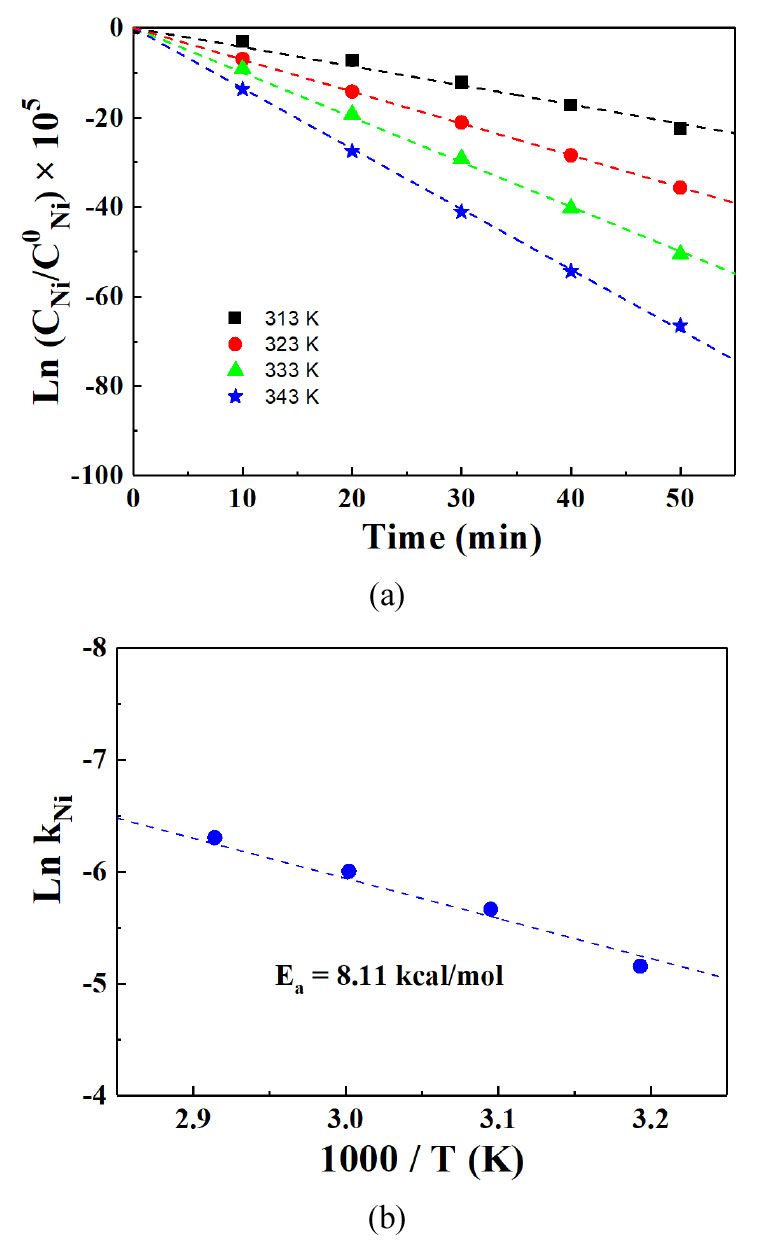
Fig. 2는 전해액 온도 40 ~ 70 ℃ 구간에서 니켈 전해채취 시 전해액 내 니켈 농도 감소량과 Arrhenius plot을 나타내었고, 계산된 활성화 에너지 값은 8.11 kcal/mol 이었다. 이는 물질전달과 전기화학반응이 동시에 전체 반응속도를 율속하는 혼합율속으로 판단된다. 따라서 니켈 전해채취 공정에서 반응온도 및 교반속도는 모두 중요한 공정인자로 보다 면밀한 제어 필요하다. 니켈 전해채취 시 전해액 온도 및 교반속도 변화가 전류효율에 미치는 영향을 알아보기 위해 전해액 온도가 각각 40, 50 및 60 ℃, 교반속도 30, 60 및 90 rpm 조건에서 50 mA/cm2 전류밀도를 인가하여 3시간 전해채취를 수행였고, 이때의 니켈 전해채취층의 전류효율을 Fig. 3에 나타내었다. Fig. 3(a)는 교반속도 60 rpm에서 전해액 온도 변화에 따른 니켈 전해채취 전류효율을 나타낸 그래프이고, 전해액 온도가 증가함에 따른 니켈 전해채취 전류효율은 각각 86.14 %, 88.48 % 및 90.83 %이었다. Fig. 3(b)는 전해액 온도 50 ℃에서 교반속도 변화에 따른 니켈 전해채취 전류효율을 나타낸 그래프이고, 전류효율은 각각 86.97 %, 88.48% 및 91.24 %이었다. 이 결과에서, 니켈 전해채취 시 온도 및 교반속도가 증가하면 전류효율은 소폭 상승하였고, 앞서 속도론적 연구 결과인 물질전달과 전기화학 반응이 동시에 나타나는 혼합율속 결과와 일치하였다. Fig. 3(c)는 인가전류밀도 증가에 따른 니켈 전해채취 전류효율 변화를 나타낸 그래프이고, 전류밀도가 증가할수록 니켈 전해채취 전류효율을 92.91 %에서 86.68 %으로 감소하는 경향을 나타내었다.
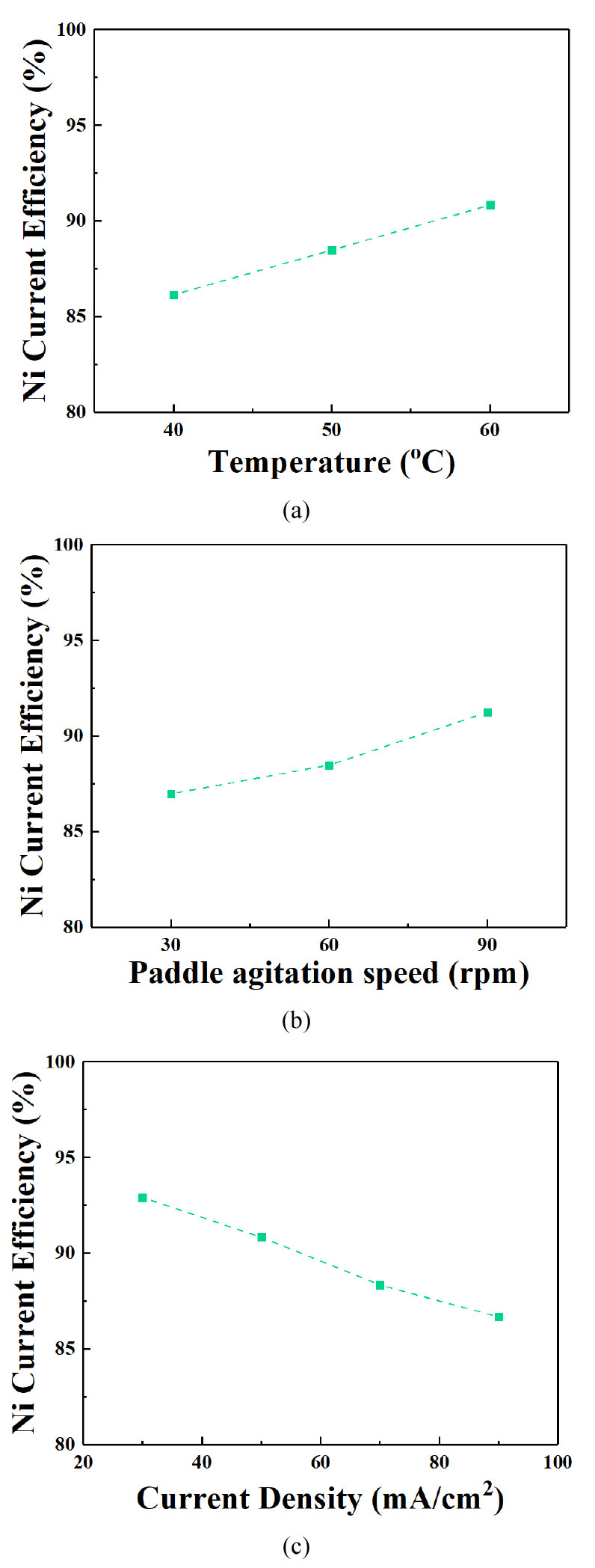
Fig. 3.
Evaluation of the effect of nickel electrowinning on process factors: (a) Current efficiency of nickel electrowinning as function of temperature of the electrolyte, (b) Current efficiency of nickel electrowinning as function of paddle agitation speed, (c) Current efficiency of nickel electrowinning as function of applied current density.
3.2. 코발트 전해채취 반응속도론적 고찰
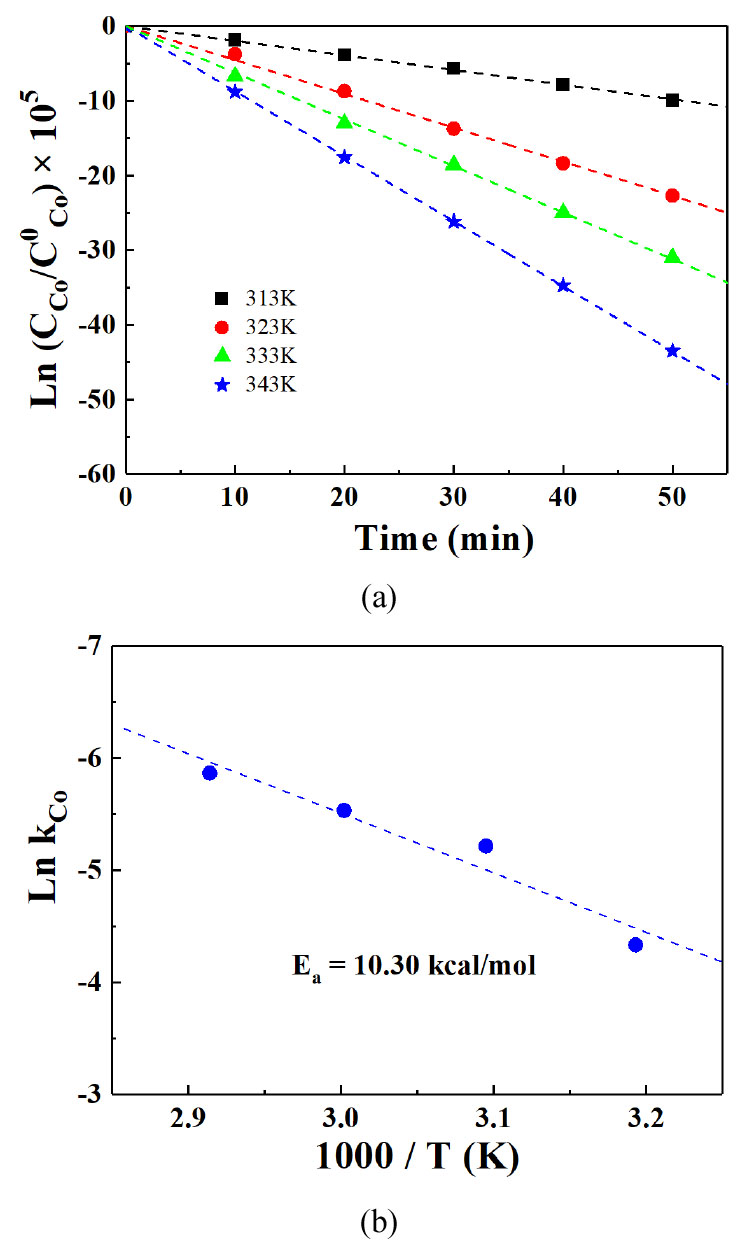
전해액 온도 40 ~ 70 ℃ 에서 코발트 전해채취 시 전해액 내 코발트 농도 감소량을 Fig. 4(a), Arrhenius plot을 Fig. 4(b)에 나타내었고, 계산된 활성화 에너지 값은 10.30 kcal/mol으로 화학반응율속인 것을 확인하였다. 이 온도구간에서의 코발트 전해채취 공정은 전기화학반응에 관여하는 공정인자 중 하나인 전해액 온도가 주요 제어해야할 공정인자로 생각된다. 전해액 온도 및 교반속도 변화가 전류효율에 미치는 영향을 확인하기 위해 앞서 실험한 것과 같은 40, 50 및 60 ℃, 교반속도 30, 60 및 90 rpm 조건에서 50 mA/cm2 전류밀도를 인가하여 3시간 전해채취를 수행였하여 Fig. 5에 나타내었다. 전해액 온도가 증가할 때 코발트 전해채취 전류효율은 각각 87.61 %, 92.05 % 및 93.42 %이었고, 전해액 교반속도가 증가할 때의 전류효율은 각각 90.99 %, 92.05 % 및 92.13 %이었다. 코발트 전해채취 시 전해액 온도가 증가할 때 전류효율도 증가하는 추세를 나타내었으나, 전해액 교반속도가 증가함에도 전류효율은 91 ~ 92 %으로 변화의 정도가 미미하였다. 화학반응율속인 코발트 전해채취 반응속도론적 연구결과와 일치함을 확인하였다. Fig. 5(c)는 인가전류밀도 증가에 따른 코발트 전해채취 전류효율 변화를 나타낸 그래프이고, 전류밀도가 30, 50, 70 및 90 mA/cm2으로 증가할수록 코발트 전해채취 전류효율을 93.15, 92.05 및 92.27 %으로 유지하다가 88.43 %으로 감소하는 경향을 나타내었다.
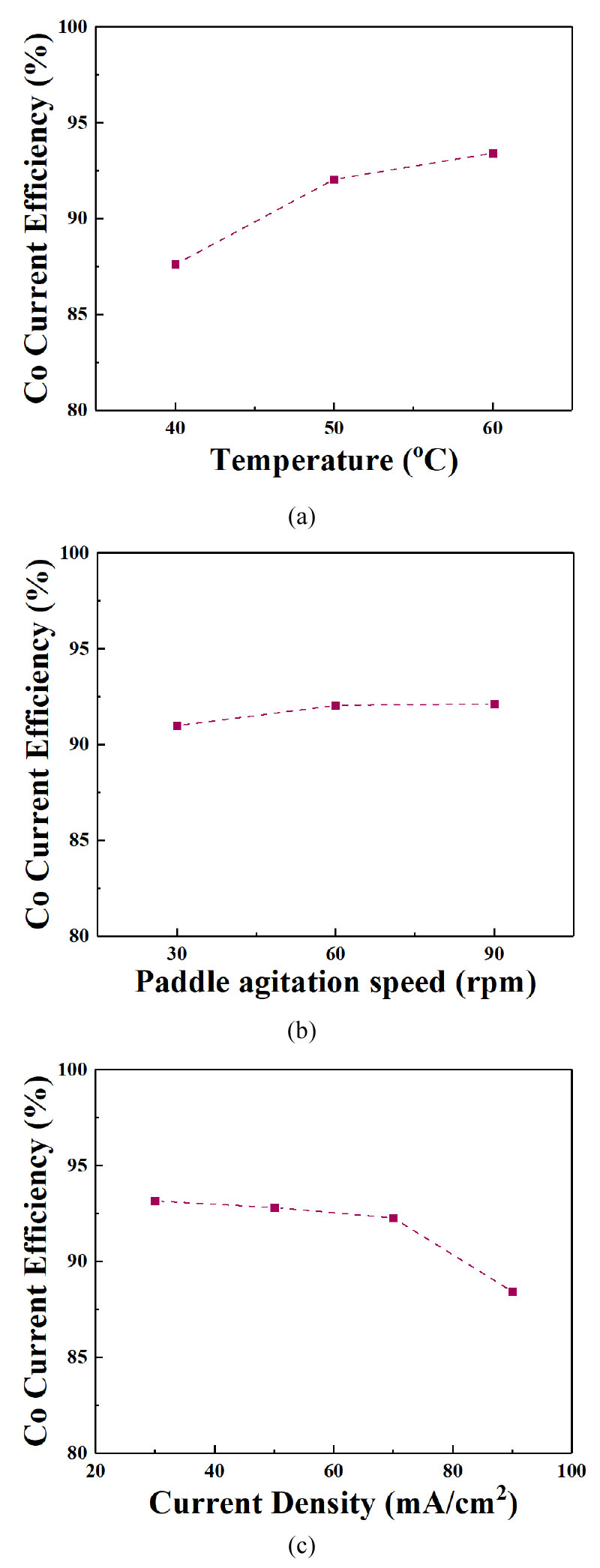
Fig. 5.
Evaluation of the effect of cobalt electrowinning on process factors: (a) Current efficiency of cobalt electrowinning as function of temperature of the electrolyte, (b) Current efficiency of cobalt electrowinning as function of paddle agitation speed, (c) Current efficiency of cobalt electrowinning as function of applied current density.
3.3. 구리 전해채취 반응속도론적 고찰
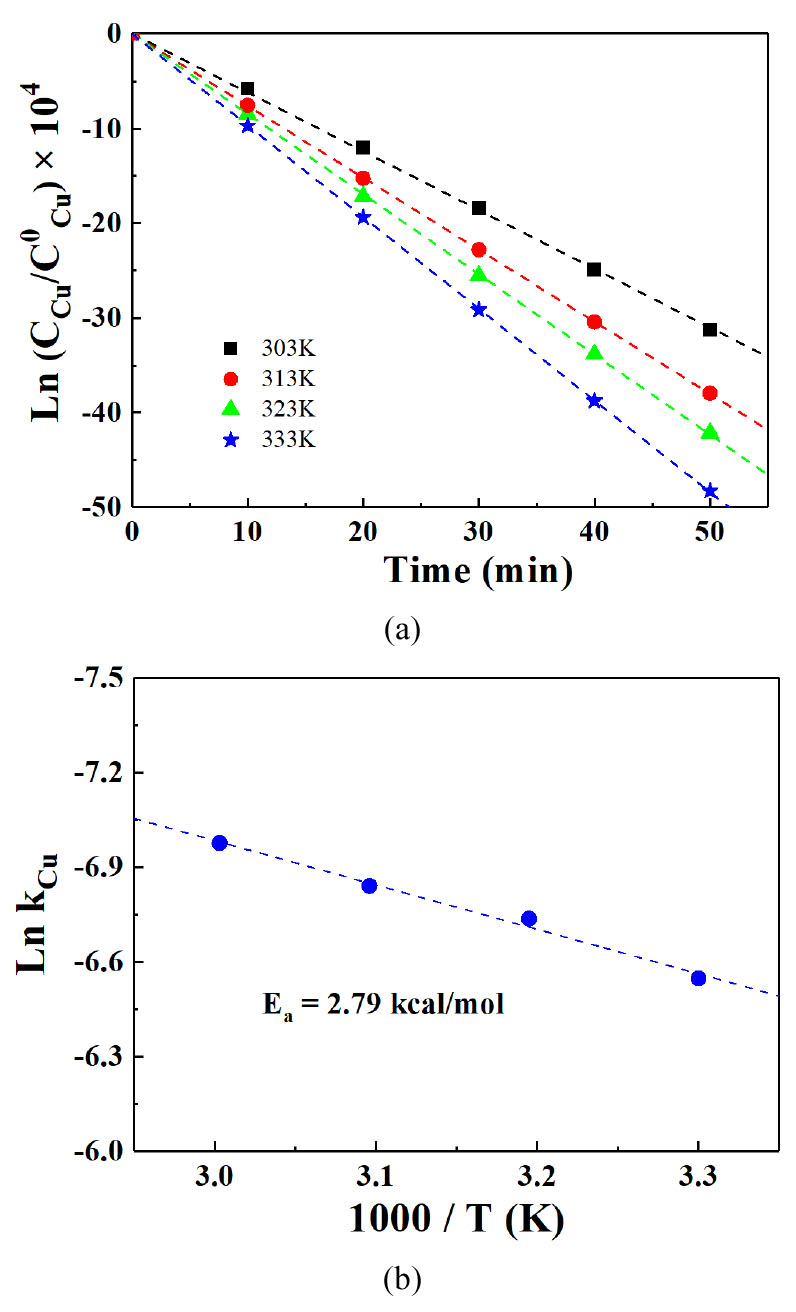
RDE 시스템으로 구리 전해채취를 수행하여 Fig. 6에 나타내었다. 전해액 온도 30 ~ 60 ℃에서 구리 전해채취 시 전해액 내 코발트 농도 감소량을 Fig. 6(a), Arrhenius plot을 Fig. 6(b)에 나타내었고, 계산된 활성화 에너지 값은 2.79 kcal/mol으로 물질전달율속(mass transfer)으로 판단된다. 이러한 온도구간에서의 구리 전해채취 공정에서는 교반속도 제어를 고려해야 할 것으로 생각된다.
전해액 온도 및 교반속도 변화가 구리 전해채취 전류효율에 미치는 영향을 확인하기 위해 앞서 실험한 것과 같은 전해액 온도 각각 40, 50 및 60 ℃, 교반속도 각각 30, 60 및 90 rpm에서 100 mA/cm2 전류밀도 조건에서 3시간 전해채취를 수행하여 아래 Fig. 7에 나타내었다. 전해액 온도가 증가함에도 구리 전해채취 전류효율은 각각 97.45 %, 97.8 % 및 97.88 %으로 차이가 거의 없었으나, 교반속도가 증가 시 구리 전해채취 전류효율은 각각 94.62 %, 97.8 % 및 97.53 %으로 소폭 상승하다가 약 97 %에서 유지하였다. 구리 전해채취의 속도론적 연구 결과인 물질전달율속 결과에 의하면 교반속도가 증가하면 전류효율이 증가하여야 하나, 구리는 전해공정효율이 아주 높은 금속 중 하나로 높은 전해채취 효율을 가지기 때문에 일정한 교반속도 이상에서는 효과가 낮은 것으로 판단된다. Fig. 7(c)는 인가전류밀도 증가에 따른 구리 전해채취 전류효율 변화를 나타낸 그래프이고, 전류밀도가 증가할수록 구리 전해채취 전류효율을 98.92 %에서 92.78 %으로 감소하는 경향을 나타내었다.
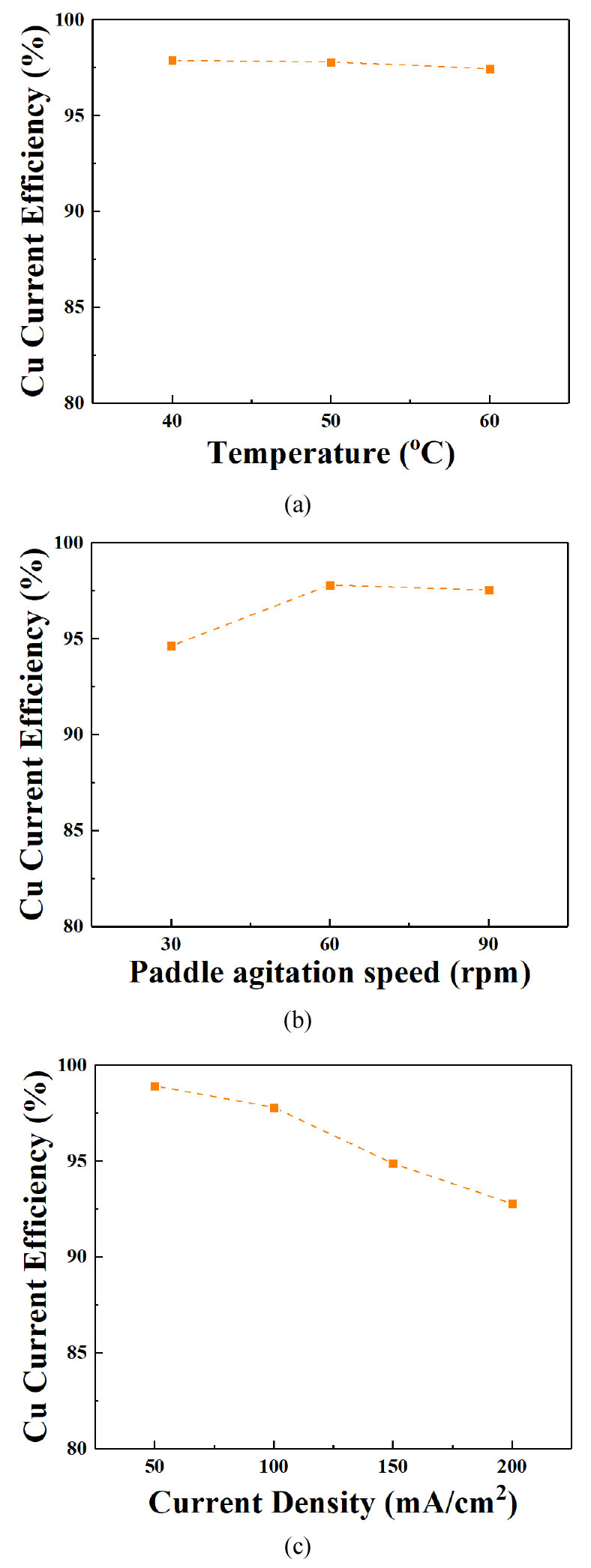
Fig. 7.
Evaluation of the effect of copper electrowinning on process factors: (a) Current efficiency of copper electrowinning as function of temperature of the electrolyte, (b) Current efficiency of copper electrowinning as function of paddle agitation speed, (c) Current efficiency of copper electrowinning as function of applied current density.
4. 결 론
폐리튬이온전지로부터 제조된 고순도 분리․정제액으로 RDE 시스템을 사용하여 전해액 온도 및 교반속도 공정조건에 대한 니켈, 코발트 및 구리 전해채취의 반응율속단계를 규명하였고, 유가금속 소재화를 위한 전해채취 공정을 수행하여 다음과 같은 결론을 얻었다. 니켈 전해채취의 반응율속단계는 혼합율속으로 반응온도 및 교반속도 모두 영향을 미치는 공정인자로 보다 면밀한 제어 필요하다. 코발트 전해채취의 반응율속단계는 화학반응율속으로 전기화학반응에 관여하는 공정인자 중 하나인 전해액 온도제어가 필요하다. 구리 전해채취의 반응율속단계는 물질전달율속으로 교반속도 제어를 고려하여야 한다.