1. 서 론
2. 실험방법
2.1. 시료 및 시약
2.2. 실험방법
3. 실험결과 및 고찰
3.1. 티탄철석 정광 내 유가금속 비율
3.2. 티탄철석 정광의 황산 침출 실험
3.3. 산화 및 환원 침출용액으로부터 분리 정제공정에 의한 유가금속의 회수 가능성
4. 결 론
1. 서 론
바나듐은 멕시코 광물학자 델리오(Andres M. del Rio, 1764-1849)에 의해 갈연석에서 처음 발견되었다. 자연 상태에서는 화합물로만 존재하며 은회색의 전이금속이다. 높은 인장 강도 및 경도 그리고 내 피로성과 같은 특성으로 인해 전체 바나듐 생산량의 85% 이상이 철강 산업에서 철 그리고 비철금속의 합금 원료로 널리 사용되고 있으며 촉매로써도 널리 사용되고 있다. 또한 수용액 내 에서 바나듐은 +2, +3, +4, +5가 등의 산화가로 존재할 수 있는데 이 전위차이의 원리를 이용하여 에너지 저장장치로써 리튬이온 배터리를 대체할 수 있는 차세대 전지인 바나듐 흐름 전지(vanadium redox-flow batteries) 의 전해액으로 사용될 수 있다1,2,3,4).
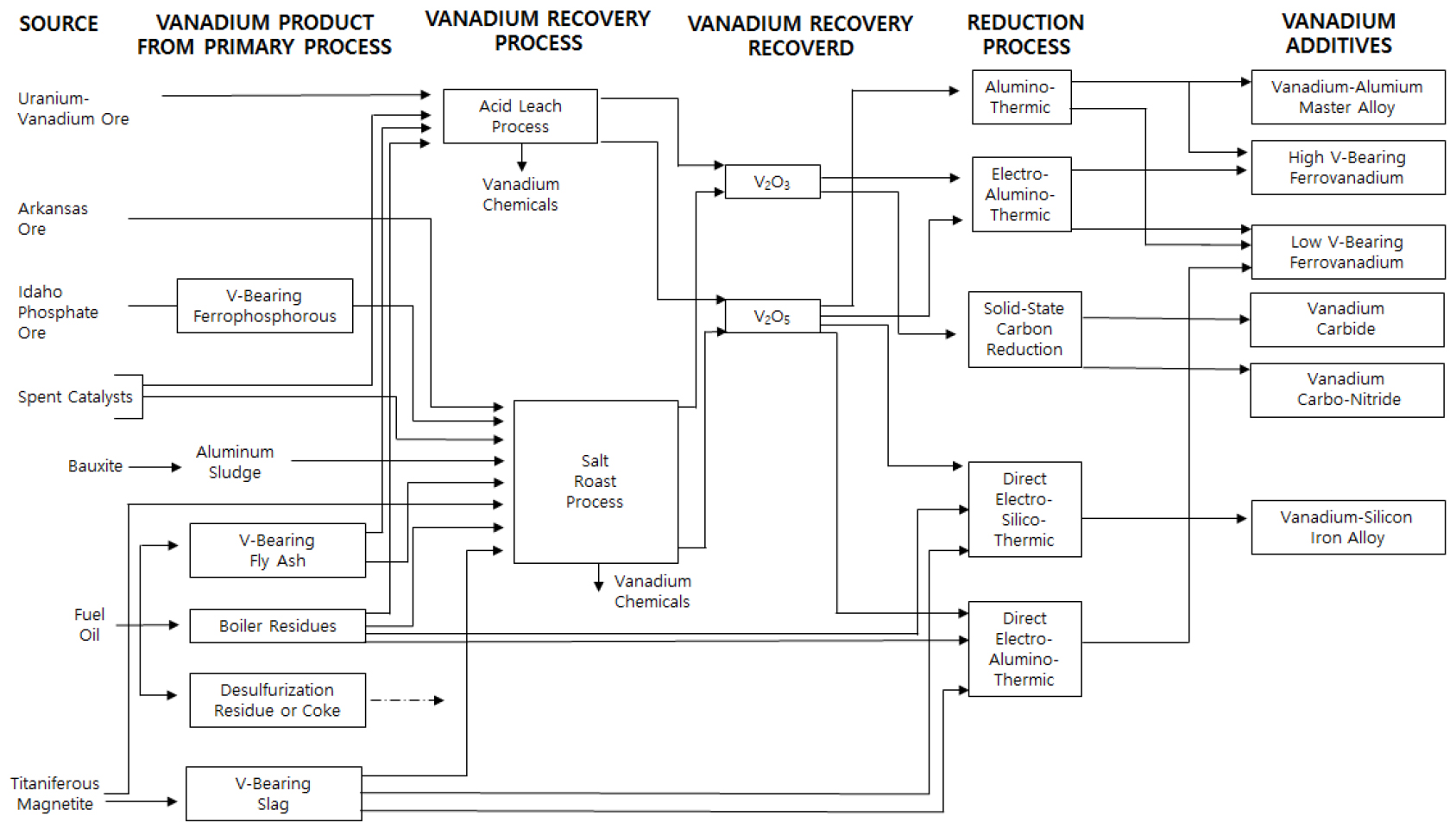
세계 바나듐 자원량은 6300만톤 이상으로 추산되며 매장량은 2000천만 톤으로 추산된다. 중국 46%, 러시아 26%, 남아프리카공화국 18% 등 3개국에 약 90% 매장되어 있어 지역적 편재가 심하다5). 하지만 일반적으로 바나듐은 주 광물종이 없고 주로 철광석 광물종인 자철석(magnetite) 티탄철석(ilmenite) 크롬철석(Chromite) 내 1-2% 소량 존재하며 Fe, Ti 금속의 제련과정에서 부산물로 회수하고 있다. 특히 자철석 내 Fe3+ 자리에 바나듐이 V3+ 형태로 치환되어 존재하는 것으로 알려져 있다6,7,8,9,10,11,12,13). 또한 V2O5 기준으로 Bauxite 내에서 0.05%-0.1% 그리고 phosphate 광물 종 내에서도 0.5% 이하로 존재하며 crude petroleum에 약 350 ppm 정도 존재하는 것으로 알려져 있다. 바나듐의 제련 및 회수공정을 Fig. 1에 나타내었다. 바나듐의 제련 공정이 각 원료물질마다 차이를 보이는데 이는 앞서 설명하였듯이 주 광물이 없어 다른 광물 종 내 낮은 함유량으로 존재하여 부산물로써 바나듐을 얻고 있기 때문이다. 따라서 일반적으로 바나듐을 회수할 시 농축공정이 필요하며 자철석(magnetite) 및 티탄철석(ilmenite)에서는 슬래그법을 통해 약 6-24%까지 농축하여 회수하고 Bauxite에서는 Aluminium sludge의 염 배소 공정을 통해 약 6-20%정도, V-Bearing Ferro-phosphorous의 FeP 회수 공정으로부터 5-10% 정도로 V2O5 형태로 농축하여 회수하고 있다. 이러한 농축공정은 산 침출 공정 및 알칼리 염 배소 공정 후 침출을 통해 V을 침출시킨 후 다시 암모니아를 투입시켜 메타암모늄 헝태로 침전시키는 공정을 포함하며 메타암모튬바나데이트를 열처리하여 V2O5 및 V2O3의 형태로 바나듐을 회수하고 Alumino-Thermic 환원공정을 통해 철강 산업의 원료로 투입한다. 즉 V2O5 및 V2O3를 얻기 위해 많은 분리정제 공정이 필요하다. 반면 Direct Electro-Alumino-Thermic 반응을 통해 곧 바로 바나듐을 직접적으로 회수할 수 있지만 바나듐의 함유량이 낮은 ferro vanadium의 원료로만 사용한다14).
반면 국내의 경우 1990년대부터 바나듐 함유 광상을 확인하고 바나듐 연구가 지속적으로 진행되어 왔으며 최근 연천지역에서 티탄철석 광산에 부존되어 있는 자철광에 바나듐이 부존되어 있는 것을 확인하였다15,16,17). 따라서 국내 바나듐 함유 티탄철석으로부터 V2O5 및 바나듐 회수공정 개발연구가 활발히 진행되고 있으나18,19,20,21) 직접 산 침출법에 의한 바나듐 함유 티탄철석으로부터 유가금속 회수연구 보고는 찾아보기 힘들다. 그러므로 바나듐의 복잡한 회수 공정을 단순화 시키고자 국내 함 바나듐 티탄 철석으로부터 염 배소 없이 직접 황산 침출법을 통해 바나듐의 침출거동을 알아보았고 이와 동시에 회수가능성을 본 연구에서 알아보고자 한다.
2. 실험방법
2.1. 시료 및 시약
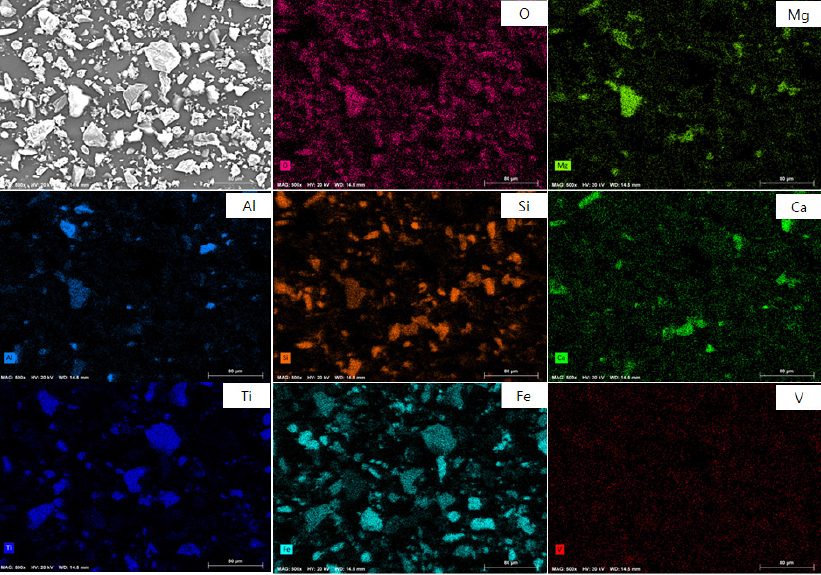
본 연구에서 사용한 시료는 경기 연천지역에 위치한 관인광산에서 제공받은 티탄철석 광상의 정광이다. ICP-AES(Inductively coupled plasma Atomic Emission Spectroscopy)분석을 통해 정광 내 화학적 성분을 Table 1에 나타내었고 Fig. 2와 Fig. 3에 XRD와 SEM-mapping 분석 결과를 각각 나타내었다. 침출에 사용한 황산은 순도 95%, 산화제로는 Na2S2O8 그리고 환원제로는 NaS2O3를 사용하였다.
Table 1.
Composition of valuable metals in concentrate of vanadium bearing titano-magnetite (unit: wt.% by ICP)
| Element | V | Ti | Fe | Ca | Mg | Al |
| VTM concentrate | 0.46 | 8.26 | 49.6 | 0.56 | 2.19 | 4.8 |
2.2. 실험방법
본 연구에서 사용한 침출장치는 반응온도 조절을 위해 히팅맨틀 위에 1L 크기의 5구 바닥이 둥근 파이렉스 플라스크를 얻어 놓았으며 실험 도중 증기로 인한 액상의 손실을 방지하고자 응축기를 장착하였다. 침출 실험은 설정한 반응온도 상에서 고액비 1:10의 조건하에서 시료를 투입하였으며 교반속도는 200 RPM으로 동일하게 설정하였다. 침출 실험 도중 시간에 따라 일정한 시료를 채취하였으며 채취한 시료로부터 ICP 분석을 통해 유가금속의 침출량을 분석하였다. 침출 실험종료 후 고액 분리를 통해 침출 잔사를 획득하였고 무게 측정 후 알칼리 퓨전을 수행하였다. 그리고 왕수 처리하여 잔사 내 유가금속의 함량을 분석하였다. 유가금속의 침출량과 잔사 내 유가금속의 함유량을 기준으로 침출율을 계산하였다.
3. 실험결과 및 고찰
3.1. 티탄철석 정광 내 유가금속 비율
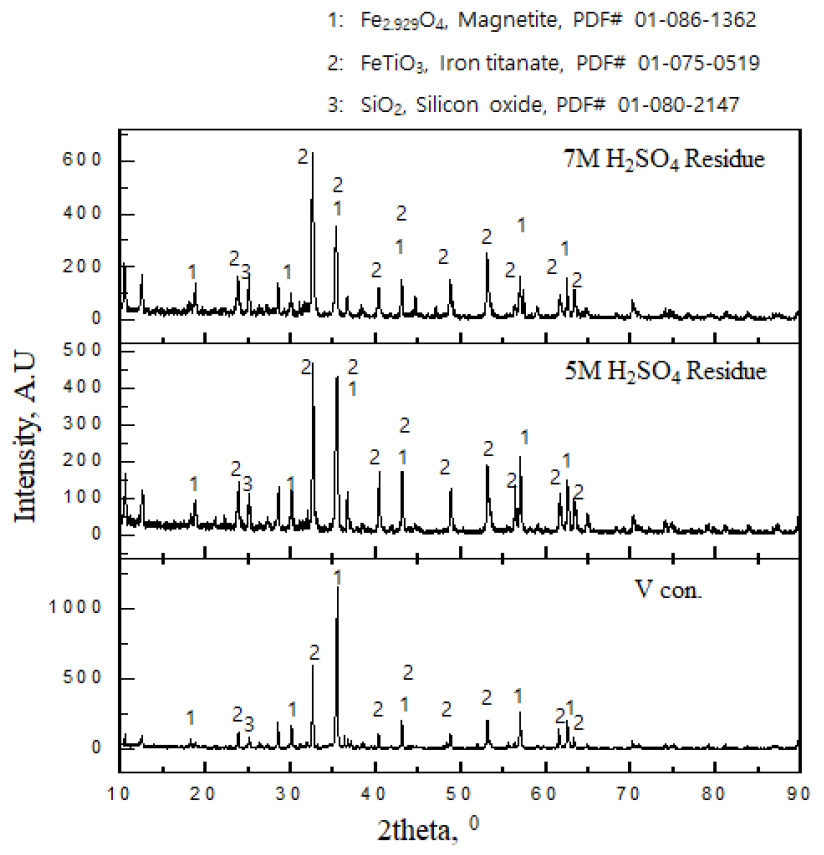
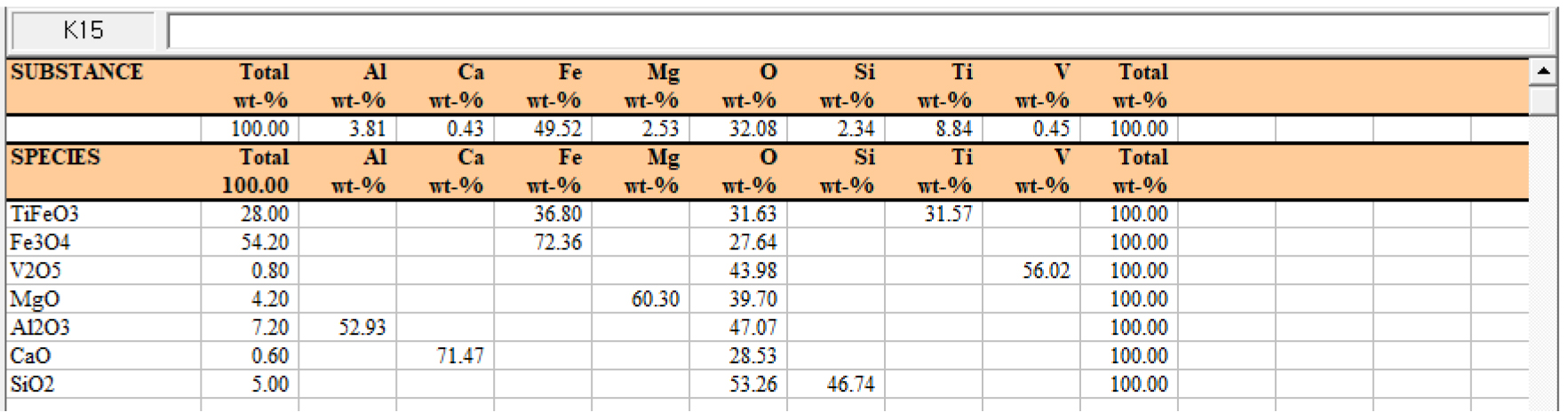
Table 1에서 알 수 있듯이 시료 내 V은 약 0.46%, Fe는 49.6%, Ti은 8.26%, Ca은 0.56%, Mg은 2.19%, Al은 4.8% 함유되어 있는 것을 볼 수 있으며 XRD 및 SEM-mapping을 통해 시료 내 주성분은 Fe3O4와 FeTiO3로 이루어져 있는 것을 알 수 있다(Fig. 2, Fig. 3). FeTiO3와 Fe3O4의 대략적인 함유량을 알아보기 위해 HSC 프로그램을 이용하여 VTM 원광 내 magnetite와 ilmenite의 조성비를 비교하여 보았다. 비교 기준은 VTM 정광 내 총 Fe의 함량이 49%, V의 함유량이 0.45%, Ti 8.8% 라는 Table 1의 ICP 분석 자료를 근간으로 HSC 프로그램에 data를 삽입하였다. 그 결과 ilmenite인 FeTiO3는 약 28% 함유되어 있으며, magnetite인 Fe3O4는 약 54%, 그리고 V2O5는 0.8% 정도 함유되어 있는 것으로 계산되었다(Fig. 4). 즉 magnetite와 ilmenite의 비율이 약 1.9:1의 비율인 것으로 판단하였다.
3.2. 티탄철석 정광의 황산 침출 실험
3.2.1. 황산 농도별 실험에 따른 유가금속의 침출거동
VTM 정광을 원료로 하여 5M H2SO4과 5M HCl을 이용하여 유가금속의 침출율을 비교하였을 때 5M H2SO4를 사용하였을 시 8시간동안 V이 64.2%, 5M HCl을 사용하였을 때 57.1% 침출되었다(Table 2). 따라서 이후의 모든 실험은 V 침출에 관해 황산이 염산보다 효율적이었기에 황산 농도에 따른 실험을 진행하였다.
Table 2.
Leaching efficiency of valuable metals from VTM Con. by H2SO4 and HCl (80°C, 200RPM, 8hr, unit: %)
| Element | V | Fe | Ti | Si | Ca | Mg | Al |
| 5M H2SO4 | 64.2 | 59.8 | 11.1 | 2.4 | 60.2 | 90.7 | 60.8 |
| 5M HCl | 57.1 | 51.4 | 5.7 | 4.0 | 69.1 | 90.1 | 89.7 |
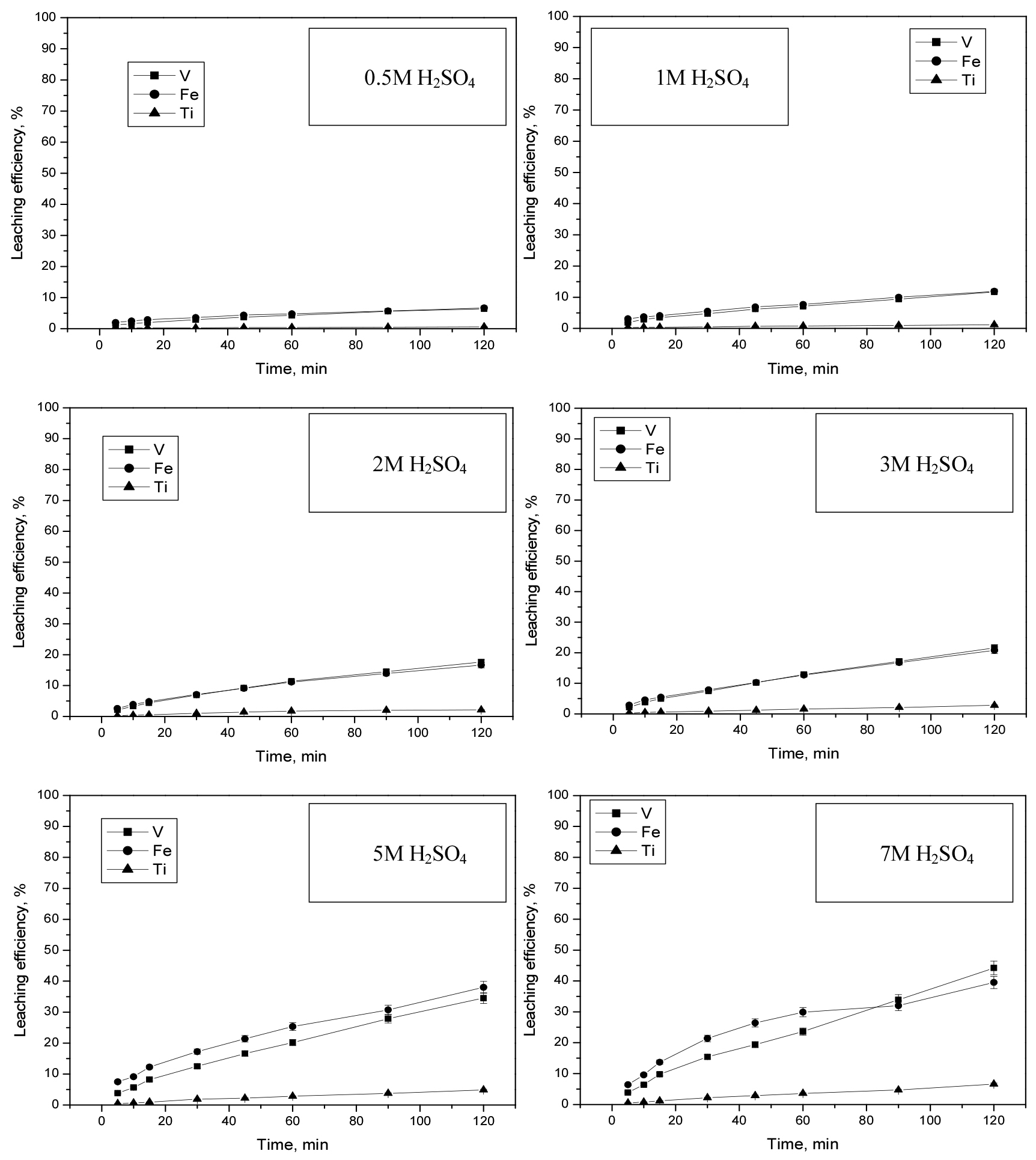
황산농도에 따른 침출 실험조건은 60°C, 고액비 1:10, 200 RPM의 조건하에서 진행하였고 그 결과를 Fig. 5에 나타내었다. 황산을 이용한 직접침출 결과 예상되는 바와 같이 황산 농도가 증가할수록 V의 침출율이 증가하는 것을 관찰 할 수 있었다. 0.5, 1M H2SO4에서는 2시간 동안 V이 5% 이하로 침출되었고 2M, 3M H2SO4에서는 2시간 동안 V이 20% 이하로 침출되었으며 5M, 7M H2SO4에서는 2시간 동안 V이 40% 이하로 침출되었다. Fe의 경우 V과 유사하게 0.5M, 1M H2SO4에서는 2시간 동안 Fe가 5% 이하로 침출되었고 2M, 3M H2SO4에서는 2시간 동안 Fe가 20% 이하로 침출되었고 5M, 7M H2SO4에서는 2시간 동안 Fe가 40% 이하로 침출되었다. 즉 Fe와 V의 침출율이 매우 유사하였으며 침출곡선의 형태 또한 매우 유사하였다. 이는 Fe가 침출되어야지 V이 침출될 수 있음을 보여준다. 즉 VTM 정광의 magnetite 내 V이 Fe3+ 이온격자 대신 V3+로 치환되어 있다는 연구결과와 일치한다6,7,8,9,10,11,12,13). 또한 침출곡선이 매우 linear 한데 이는 초기 침출속도가 매우 느리다는 것을 의미한다. 따라서 V의 침출율을 높이기 위해서는 Fe가 침출되어야 하며 Fe의 침출속도를 증가시킬 필요가 있다. Ti의 경우 Fe와 V의 침출율과 비교하여 60°C조건하에서 1M–7M H2SO4까지 침출이 5% 이하로 거의 일어나지 않았다. Ti이 ilmenite 광내에 존재함으로써 FeTiO3가 알려진 대로 상당히 난용성 물질이기 때문이다. 최종적으로 7M H2SO4에 44.2% V, 39.5% Fe, 6.6% Ti이 각각 침출되었다. XRD 분석을 통해 VTM 정광 내 주요광물이 magnetite 그리고 ilmenite임을 보여주고 있다. 그리고 황산 침출 후 잔사 분석을 통해 5M H2SO4와 7M H2SO4의 잔사에서 main peak가 magnetite가 아니라 ilmenite임을 확인하였다(Fig. 2). 이는 H2SO4의 침출을 통해 VTM 정광 내 ilmenite보다 magnetite가 효율적으로 침출될 수 있음을 보여준다.
3.2.2. 침출온도에 따른 유가금속의 침출거동
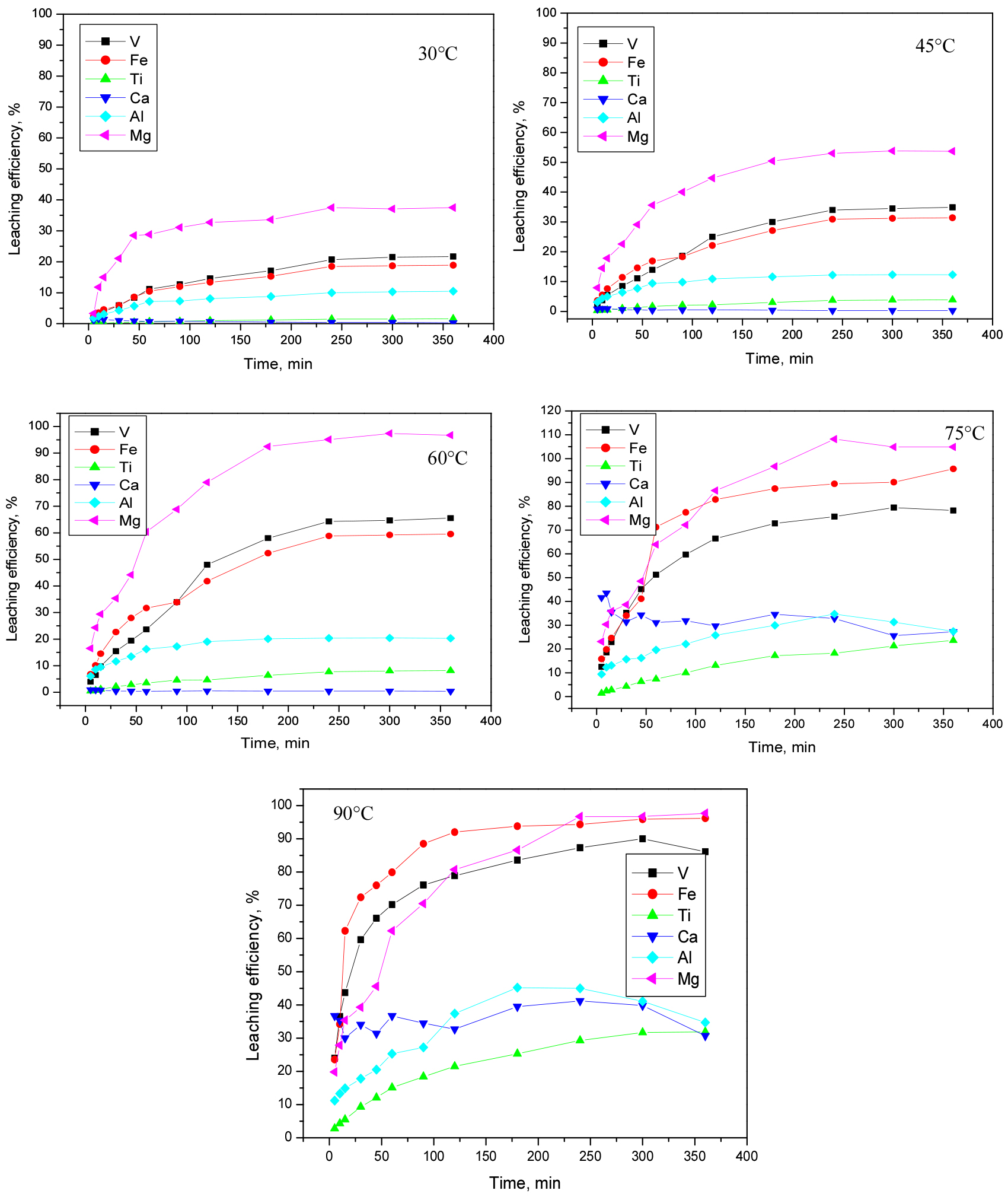
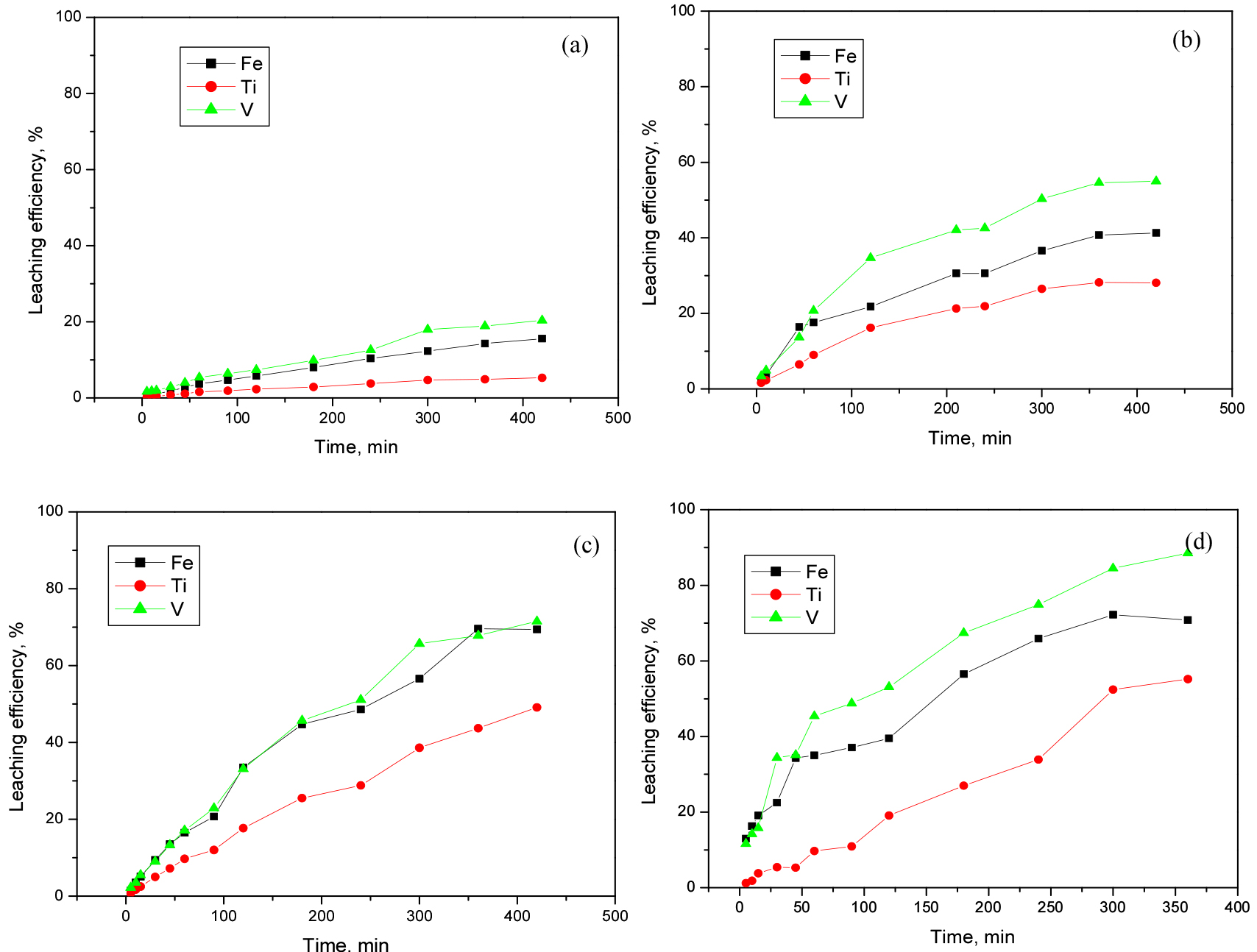
VTM 정광으로부터 7M H2SO4에서 V과 Fe의 침출율이 가장 효율적이었으므로 7M H2SO4에 대한 온도별 실험을 수행하였다. 침출 실험 온도는 30, 45, 60, 75, 90°C에서 수행하였으며 고액비 200RPM, 그리고 반응시간을 420분으로 두었다. 420분으로 둔 이유는 황산 농도별 실험에서 2시간 동안 반응시킬 경우 Fe와 V의 침출곡선이 계속해서 증가하였기 때문이다. 따라서 침출반응이 종료되는 시점, 즉 침출곡선이 완만해 지는 지점을 알아보기 위해 420분 동안 침출실험을 수행하였다. 그 결과를 Fig. 6에 나타내었다. Fig. 6에서 볼 수 있듯이 30°C실험에서 V과 Fe는 침출곡선이 매우 유사하였으며 약 20% 정도 침출되었고 그리고 Ti의 경우 침출이 거의 이뤄지지 않았다. 반면 나머지 유가금속의 경우 Mg이 약 35% 정도 침출된 것을 볼 수 있다. Ca의 경우 침출이 거의 일어나지 않았는데 그 이유는 침출제로 황산을 사용함으로써 Ca이 CaSO4로 침전되기 때문에 침출이 일어나지 않은 것으로 사료된다. 45°C실험에서도 V과 Fe는 침출곡선이 매우 유사하여 약 30% 정도 침출되었으며 Ti은 역시 침출이 거의 이뤄지지 않았다. 반면 나머지 유가금속의 경우 Mg이 약 50% 이상 침출된 것을 볼 수 있다. Ca의 경우 CaSO4로 침전되기 때문에 해당 조건에서도 침출이 일어나지 않았다. 60°C실험에서도 역시 V과 Fe는 침출곡선이 매우 유사하였으며 약 60% 이상 침출되었고 그리고 Ti의 경우 침출이 약 5% 정도 이뤄졌다. Mg의 경우 전량 침출되었으며 Ca은 CaSO4로 침전되기 때문에 역시 침출이 일어나지 않았다. 75 °C 실험에서부터 V과 Fe의 침출곡선의 간격이 벌어지는 것을 확인할 수 있다. 초기 50분까지는 침출거동이 매우 유사하다가 그 이후부터 Fe의 침출율이 V의 침출율보다 증가하는 것을 관찰할 수 있다. 이때 Ti의 침출은 시간이 지남에 따라 liner 하게 꾸준히 증가하여 420분 시점에서 약 20% 이상 침출된 것을 확인할 수 있다. 즉 75°C 부터는 VTM 정광 내 ilmenite가 침출되어 Fe의 침출율이 V 보다 높아진 것이다. 따라서 75 °C 부터 ilmenite가 침출되기 시작한 것으로 사료된다. 그러므로 침출 반응온도에 따라 침출율이 낮더라도 VTM 정광 내 ilmenite로부터 magnetite를 침출시킬 수 있음을 보여준다. Mg의 경우 전량 침출되었고 Ca은 이전 30-60°C의 결과에서는 침출되지 않았지만 75°C부터는 약 30% 정도 침출되었다. CaSO4는 물에 대한 용해도가 약 0.21g/100ml(20°C)인 난용성 물질로써 널리 알려진 사실이다. 본 연구에서는 침출제로 7M H2SO4에 침출시켜 이론적인 SO42-의 농도가 7M 임에도 불구하고 Ca가 75 °C부터는 CaSO4 형태로 침전되지 않고 침출된 이유는 온도의 영향 때문이 아니다. 앞서 설명하였듯이 CaSO4의 용해도는 온도가 증가할수록 소폭 감소하거나 상의 종류(α-CaSO4·0.5H2O, β-CaSO4·0.5H2O, CaSO4·2H2O) 또는 결정수에 따라 온도가 증가할 시 용해도는 감소한다22). 75°C부터 Ca이 침출된 이유는 Ca이 CaSO4로 침전되기 않았기 때문이며 그 이유는 침출제의 H2SO4의 SO42-가 ilmenite 의 Ti 침출에 관여하였기 때문이다23,24). 따라서 ilmenite 의 침출반응식을 아래 식 (2)와 같이 나타낼 수 있다.
최종적으로 90°C의 반응온도에서 Fe는 약 95%, V은 85% 이상 침출되었다. Fe, V, Mg, Ti 등의 유가금속들은 온도가 증가함에 따라 침출율이 증가한 것을 볼 수 있다. 이는 Fe, V, Mg, Ti 등의 유가금속들의 침출은 반응온도에 상당히 민감하다는 의미이며 즉, 반응 율속단계가 chemical reaction 임을 간접적으로 나타낸다. Ca의 경우 반응온도가 증가하기 때문에 Ca의 침출율이 증가한 것이 아니라 앞서 설명하였듯이 SO42-가 Ca의 침전보다 침출반응온도가 증가함에 따라 ilmenite의 Ti 침출반응에 보다 기여하기 때문에 Ca이 침출된 것으로 판단하였다.
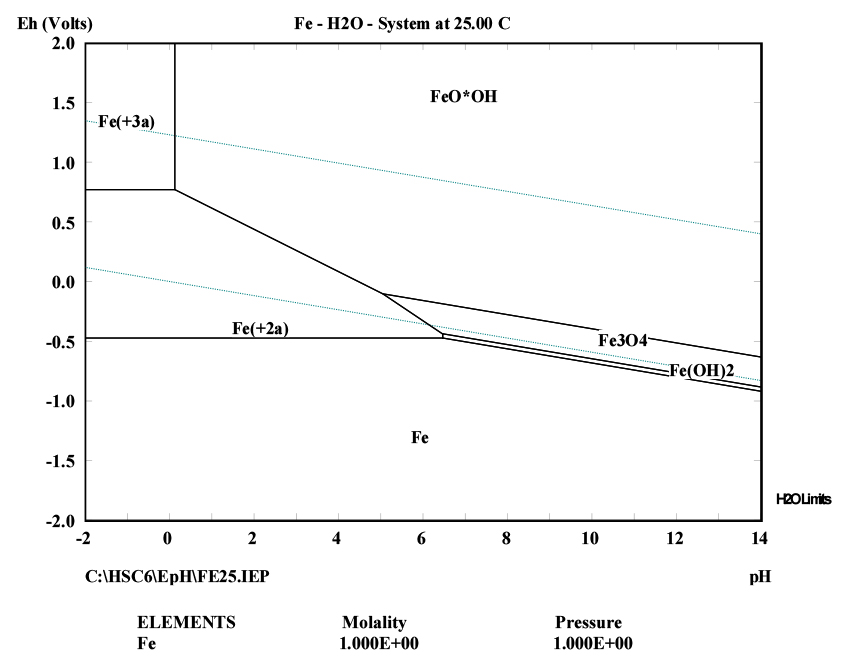
황산 농도별, 반응온도별 침출실험을 통해 VTM 정광 내 V을 침출시키기 위해선 magnetite 내 Fe의 침출율 및 침출속도를 증가시켜야 한다는 것을 알 수 있었다. 아래 Fig. 7에 Fe에 대한 Eh-pH diagram을 HSC 프로그램을 이용하여 작도하였다. Fig. 7에서 볼 수 있듯이 Fe3O4는 pH 5이상 Eh –1.0 – 0 mV 사이의 범위에서 안정하다. 이때 V을 침출시키기 위해 Fe3O4 내 Fe를 환원시켜 Fe2+ 이온 종으로 침출시키는 것이 효율적인지 또는 Fe3+ 이온종이 효율적인지 알아보기 위해 산화 및 환원 침출실험을 수행하였다. 산화제로는 Na2S2O8을 첨가하였으며, 환원제로는 Na2SO3를 첨가하였다. 침출실험 전 황산침출과 황산·산화침출 그리고 황산·환원침출의 gibbs free energy 값을 비교해 보았다. Table 3에서 볼 수 있듯이 직접 황산 침출 시 Gibbs free energy 값은 –27.6 kJ인데, 황산·산화 및 황산·환원 침출 시 gibbs free energy 값은 각각 –283.8 kJ, -195.1 kJ로 상당히 증가한 것을 볼 수 있다. 따라서 황산·산화 및 황산·환원 침출을 통해 Fe의 침출율을 상승시킴으로써 V의 침출율도 증가시킬 수 있을 것이라 판단하였다.
Table 3.
Gibbs free energy for different leaching system at 20°C
3.2.3. 황산·산화 및 황산·환원 침출에 따른 유가금속의 침출거동
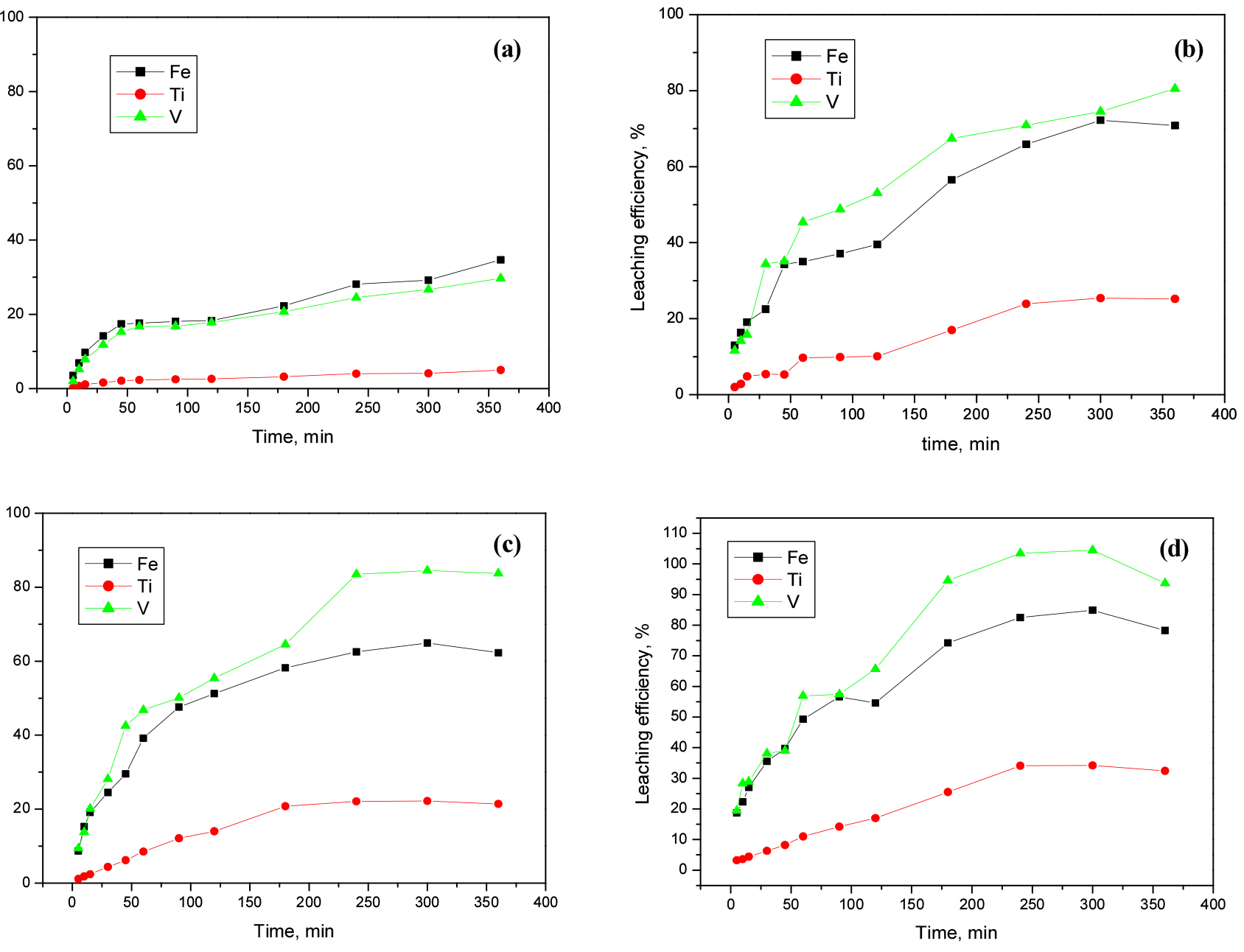
1M, 5M, 7M H2SO4 농도별 그리고 산화제인 Na2S2O8을 1M 투입, 200 RPM, 60°C 조건하에서 황산·산화침출 실험을 수행하였다(Fig. 8). 그 결과 Na2SO3를 이용한 황산·산화침출에서 1M H2SO4에서는 Eh값이 1060 mV, 5M H2SO4에서는 Eh값이 1120 mV, 7M H2SO4에서는 Eh값이 1135 mV, 7M H2SO4, 75°C에서는 Eh값이 1180 mV로 측정되었다. Fe와 V은 1M H2SO4 황산·산화침출에서 침출거동이 매우 유사하였으며 약 34.7%, 29.7% 각각 침출되었고 1M 직접황산침출 실험과 비교하였을 시 120분 시점에서 V과 Fe의 침출율이 각각 6.6%, 6.4% 더 증가하였다. 이때 Ti은 침출되지 않았다. 5M H2SO4 황산·산화침출에서 V과 Fe의 침출곡선은 유사하나 전 영역에서 V의 침출율이 Fe보다 상대적으로 소폭 높은 것을 볼 수 있다. 이때 V은 약 80.5%, Fe는 최대 70.8% 침출되었다. 5M H2SO4 직접침출실험과 비교하면 120분 시점에서 침출율은 V의 경우 18.6% 더 상승되었고 Fe는 약 1.5% 정도 더 상승되었다. 또한 Ti이 최종적으로 20% 정도 침출되어 황산·산화침출은 magnetite 뿐만 아니라 ilmenite에도 영향을 미침을 알 수 있다. 7M H2SO4 황산·산화침출에서 V은 약 83.7%, Fe는 64.9% 침출되었다. 7M H2SO4 60°C의 직접침출 조건과 비교할 시 V의 침출율은 유사하였고 Fe는 14.3% 침출율이 감소하였다. 7M H2SO4 75°C 황산·산화 조건에서는 V이 거의 전량 침출된 것을 볼 수 있고 Fe는 84.9% 까지 침출율이 증가하다 최종적으로 360분 시점에서 소폭 감소한 78.3% 정도 침출되었다. 황산·산화침출의 경우 5M H2SO4 황산·산화침출에서부터 V과 Fe의 침출곡선의 간격이 벌어지는 것을 확인할 수 있는데 흥미로운 것은 직접황산침출에서는 이 간격의 차이가 Fe의 침출율이 높았다면 황산·산화침출에서는 V의 침출율이 높다는 것이다. 또한 Fe의 침출율이 황산의 농도가 증가할수록 소폭 감소하는 것을 볼 수 있다. 이러한 결과를 바탕으로 5M H2SO4부터 Ti이 침출되기 시작하며 산화분위기 상에서는 침출된 Ti 이온이 다시 고온에서 반응함으로써 가수분해25)되고 Ti이 가수분해 될 때 Fe가 불순물로 작용하여 침전된 것으로 사료된다. Ti에 대한 가수분해 반응을 반응식 3에 나타내었다.
1M, 5M, 7M H2SO4 농도별 그리고 환원제인 Na2SO3를 1M 투입, 200 RPM, 60°C 조건하에서 산화 침출 실험을 수행하였다(Fig. 9). Na2SO3를 이용한 황산·환원 침출의 경우 1M H2SO4에서는 Eh값이 600.2 mV, 5M H2SO4에서는 Eh값이 694 mV, 7M H2SO4에서는 Eh값이 694 mV, 7M H2SO4, 90°C에서는 Eh값이 소폭 상승한 705 mV로 측정되었다, 1M H2SO4 황산·환원침출 실험에서 Fe는 15.6%, V은 20.4% 침출되었다. 1M H2SO4 침출의 120분 시점과 비교하였을 시 Fe와 V의 침출율이 약 6.1%, 4.3% 정도 감소하였으며 Ti은 최종적으로 Ti은 5.3% 침출되었다. 5M H2SO4 황산·환원침출에서는 V이 약 55%, Fe가 41.3%, 그리고 Ti이 28.1% 정도 침출되었다. 5M 직접황산침출 실험과 비교하였을 시 V의 침출율은 매우 유사하였고 Fe는 약 16.2% 정도 침출율이 감소하였다. Ti의 경우 침출율이 11.2% 이상 증가하였다. 7M H2SO4 황산·환원침출의 경우 V이 71.5%, Fe가 69.4%, Ti이 약 49.1%로 침출되었다. 7M H2SO4 직접황산 침출과 비교하였을 시 V은 26.5% 침출율이 감소하였고 Fe는 32% 침출율이 감소하였다. 7M H2SO4 황산·환원침출 90°C의 조건에서 Fe는 70.8%, V은 88.5%, Ti은 55.2% 최종적으로 침출되었다. 황산·환원침출의 경우 V의 침출율은 직접황산침출과 유사하나 Fe의 침출율이 황산·산화침출과 동일하게 감소한 것을 확인할 수 있다. 하지만 황산·산화침출과의 차이점은 황산·산화 침출에서는 Fe의 침출율이 증가하다가 감소하는 것이고 황산·환원침출에서는 Fe의 침출율이 직접황산침출과 비교하였을 시 단순히 낮다는 것이다. 또한 Ti의 침출율이 상당히 증가하였다. 이는 환산·환원 침출의 경우 VTM 정광 내 magnetite보다 ilmenite의 침출에 상당한 영향을 끼침을 알 수 있다.
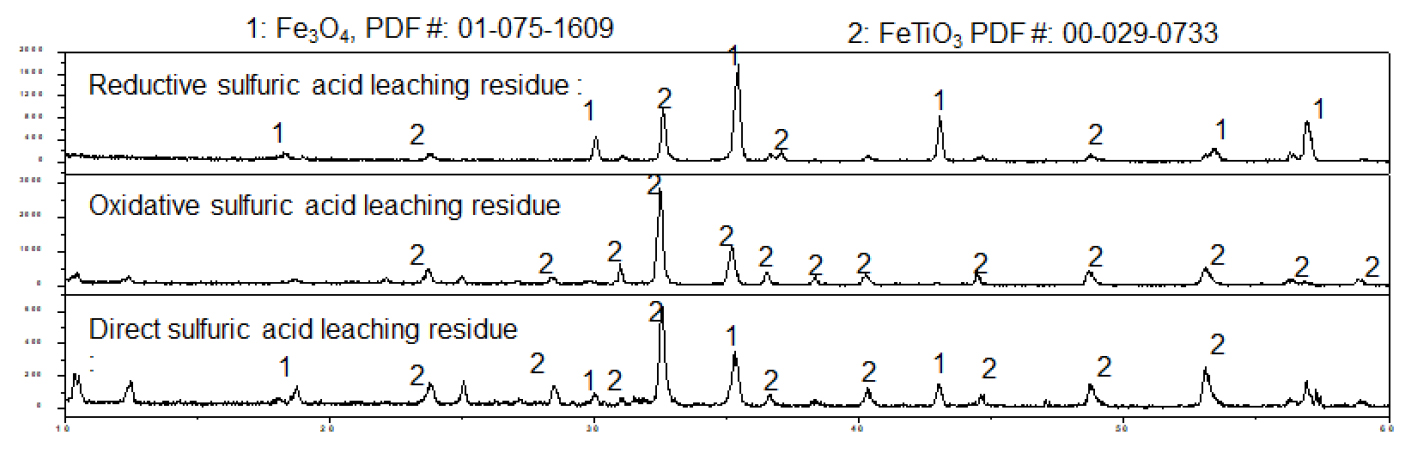
직접황산침출과 황산·산화 침출 그리고 황산·환원 침출 후 발생한 잔사를 XRD 분석하였고 이를 Fig. 10에 나타내었다. Fig. 10에서 보면 알 수 있듯이 환원 침출과 직접황산침출의 경우 ilmenite와 magnetite 모두 관측이 되었고 차이점은 황산·환원침출에서는 main peak로써 magnetite 관측된 것을 볼 수 있다. 즉 황산·환원침출은 VTM 정광 내 magnetite보다 ilmenite의 침출에 영향을 끼친 것을 볼 수 있다. 반면 황산·산화침출의 경우 main peak로써 ilmenite만 관측된 것을 볼 수 있는데, 이는 VTM 정광 내 대부분의 magnetite는 침출되었다고 판단할 수 있으며 따라서 V 역시 전량 침출되었다.
3.3. 산화 및 환원 침출용액으로부터 분리 정제공정에 의한 유가금속의 회수 가능성
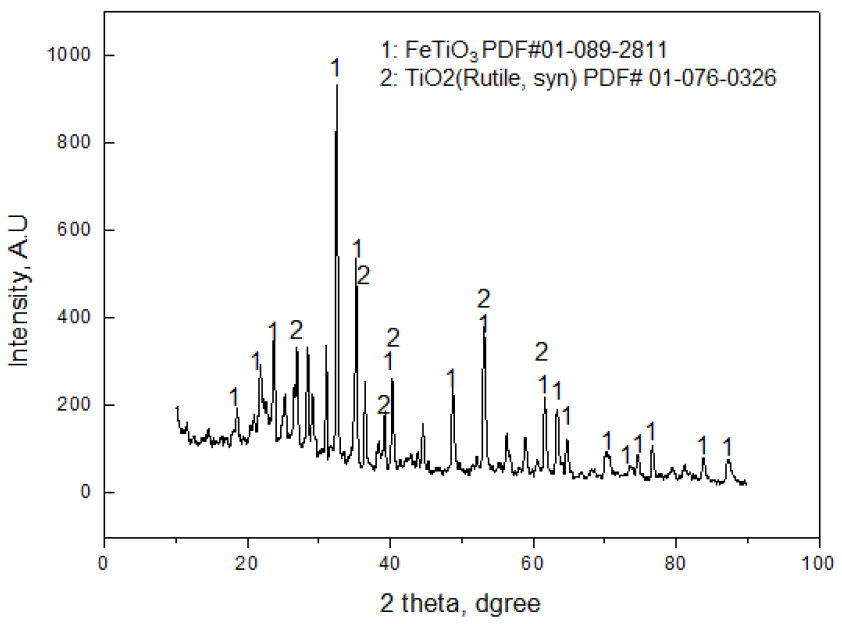
산화침출 및 환원침출의 침출용액을 비교하였을 시 육안 상 산화 침출용액에는 시간이 경과함에 따라 침전물이 형성되고 환원 침출용액은 침전물이 전혀 형성되지 않았다(Fig. 11). Fig. 12에서 볼 수 있듯이, 산화침출용액 내 침전물을 XRD 분석하였을 때 main peak가 ilmenite(FeTiO3) 와 rutile(TiO2)로 분석되었다. 즉, 산화 침출동안 Ti이 침출되며 침출반응이 고온에서 반응하거나 시간이 경과하면 침출된 Ti이 가수분해 되어 rutile(TiO2)이 된다. 이때 Ti이 가수분해 될 때 Fe도 함께 가수분해 되어 ilmenite(FeTiO3)로 침전되는 것이다. 즉 분리정제 공정단계에서 침출용액을 빨리 처리하지 못할 시 용액 내 침전이 발생하기 때문에 산화침출용액은 적합하지 않다.
황산·산화 침출용액, 황산·환원침출 용액을 이용하여 용매추출 실험을 수행하였다. 사용된 용매는 양이온교환 추출제인 D2EHPA, 음이온교환 추출제인 Alamine 336, 용매화 추출제인 Cyanex 923을 사용하였다. 그 결과를 Table 4와 Table 5에 나타내었다. 산화침출용액으로부터는 그 어떤 유가금속도 선택적으로 추출 할 수 없었다. 하지만 환원 침출용액으로부터는 Cyanex 923에 의해 Ti이 선택적으로 추출되는 것을 볼 수 있다26). 단 1단 추출만으로 Ti이 약 94.5%가 추출되었다. Fe의 경우 환원 침출에서는 전혀 추출되지 않은 것을 볼 수 있다. 이는 Fe가 Fe2+로 존재하기 때문에 낮은 pH 영역에서 추출되지 않은 것으로 판단하였다27).
Table 4.
Solvent extraction efficiency of valuable metals from oxidative sulfuric acid leaching solution (unit: %)
Table 5.
Solvent extraction efficiency of valuable metals from reductive sulfuric acid leaching solution (unit: %)
| Reductive sulfuric acid leaching solution | V | Fe | Ti | Ca | Al |
| Feed, mg/L | 471 | 43400 | 1230 | 250 | 520 |
| 50% saponification 1M D2EHPA | 9.2 | 8.8 | 76.3 | 0 | 7.3 |
| 1M Alamine336 | 0 | 0 | 0 | 0.0 | 0 |
| 1M Cyanex 923 | 0.2 | 9.3 | 94.5 | 0 | 0 |
4. 결 론
황산 직접 침출법을 통해 유가금속의 침출거동을 알아보았고 특히 V은 Fe가 침출되어야 침출됨을 알 수 있었다. 이는 magnetite 내 Fe3+ 자리에 V3+가 치환되어 있음을 간접적으로 보여준다. 따라서 V의 침출율을 향상시키기 위해 Fe의 침출속도 및 침출율을 증가시킬 필요가 있었으며 이를 위해 산화 및 환원침출 실험을 수행하였다. 산화 침출 실험 시 V이 전량 침출됨을 확인하였지만 황산 침출용액과 산화 침출용액은 시간이 경과함에 따라 침전물이 발생하였고 침전물은 XRD 분석을 통해 FeTiO3 및 TiO2로 확인하였다. 또한 분리정제 실험 시 산화 침출용액에서는 선택적으로 유가금속을 회수할 수 없었다. 반면 환원침출의 경우 V의 침출율이 88.5%에 도달하였지만 시간이 경과함에 따라 그 어떤 침전물도 발생하지 않았다. 또한 분리정제 공정에서 Ti을 Cyanex 923을 사용하여 선택적으로 회수할 수 있었다. 따라서 이후의 용액의 안정성 및 분리정제 공정을 위해 황산 침출 그리고 산화침출보다 환원침출을 수행하는 것이 보다 바람직할 것이다.