1. 서 론
2. 실험 방법
2.1. 시료
2.2. 방법
3. 실험 결과 및 고찰
3.1. 파분쇄 전처리
3.2. 산 침출
3.3. 분리정제
3.4. 니켈 증발농축 결정화
3.5. 니켈금속 전해채취
4. 결 론
1. 서 론
니켈은 전통적으로 스테인레스강, 니켈계 내열합금의 주요 구성원소가 되는 중요한 자원이다. 또한 최근 전기자동차용 고용량 리튬이차전지의 양극활물질로 국내 수요가 크게 늘면서 국가적 차원에서 공급망 관리가 필요한 핵심광물로 여겨지고 있다1,2). 국내 산업에 미치는 중요도에 비해 국내 부존자원이 없는 니켈은 전량 수입에 의존하고 있으며3), 이에 따라 페리튬이차전지로부터 니켈의 회수와 관련된 재활용기술 개발은 매우 활발한 편이다4,5). 그러나, 내열, 내식, 고온강도 등이 우수해 자동차, 화학공업, 발전소, 항공기 등 일반 산업용 및 고온 부품소재로 널리 사용되고 있는 니켈계 내열합금의6) 경우에는 그 중요성에 비해 원료의 수급이나 사용 후 제품의 재활용에 대한 국내 연구는7) 상대적으로 미미한 실정이다. 특히 정확한 국내 통계자료는 없지만 니켈계 내열합금은 주조제품 제조 시 투입량의 절반 정도가 공정스크랩으로 발생하고 정밀가공품 제조의 경우에는 대부분이 오염된 가공칩이나 가공스크랩 형태의 폐자원이 되는 것으로 알려져 있다. 오염이 되지 않은 공정스크랩의 경우에는 간단한 전처리 과정을 거쳐 제품 제조 시 필요한 모합금 제조의 원료로 활용이 가능하나 오염이 심한 가공칩이나 스크랩의 경우에는 습식제련 기반 재활용공정을 거쳐 각 원소별로 회수하고 부가가치를 높이는 방법이 필요하다. 이러한 니켈계 합금 스크랩의 활발한 재활용을 위해서 건식, 습식, 그리고 건습식 혼합 등의 필요에 맞는 다양한 공정에 대한 연구가 필요하다8). 모합금 제조에 혼합 투입하는 단순한 건식 방법으로 재활용되지 못하는 오염된 합금 스크랩은 대부분의 경우 침출을 용이하게 하기 위한 화학조성의 변화, 파분쇄의 용이성 부여 등을 위해 황화배소나 알칼리 배소 같은 전처리 단계를 거친다. 전처리 단계 산물은 산침출, 용매추출, 침전분리, 결정화, 전해채취 등의 일반적인 습식제련 기술을 필요에 따라 조합한 재활용공정을 거친다.
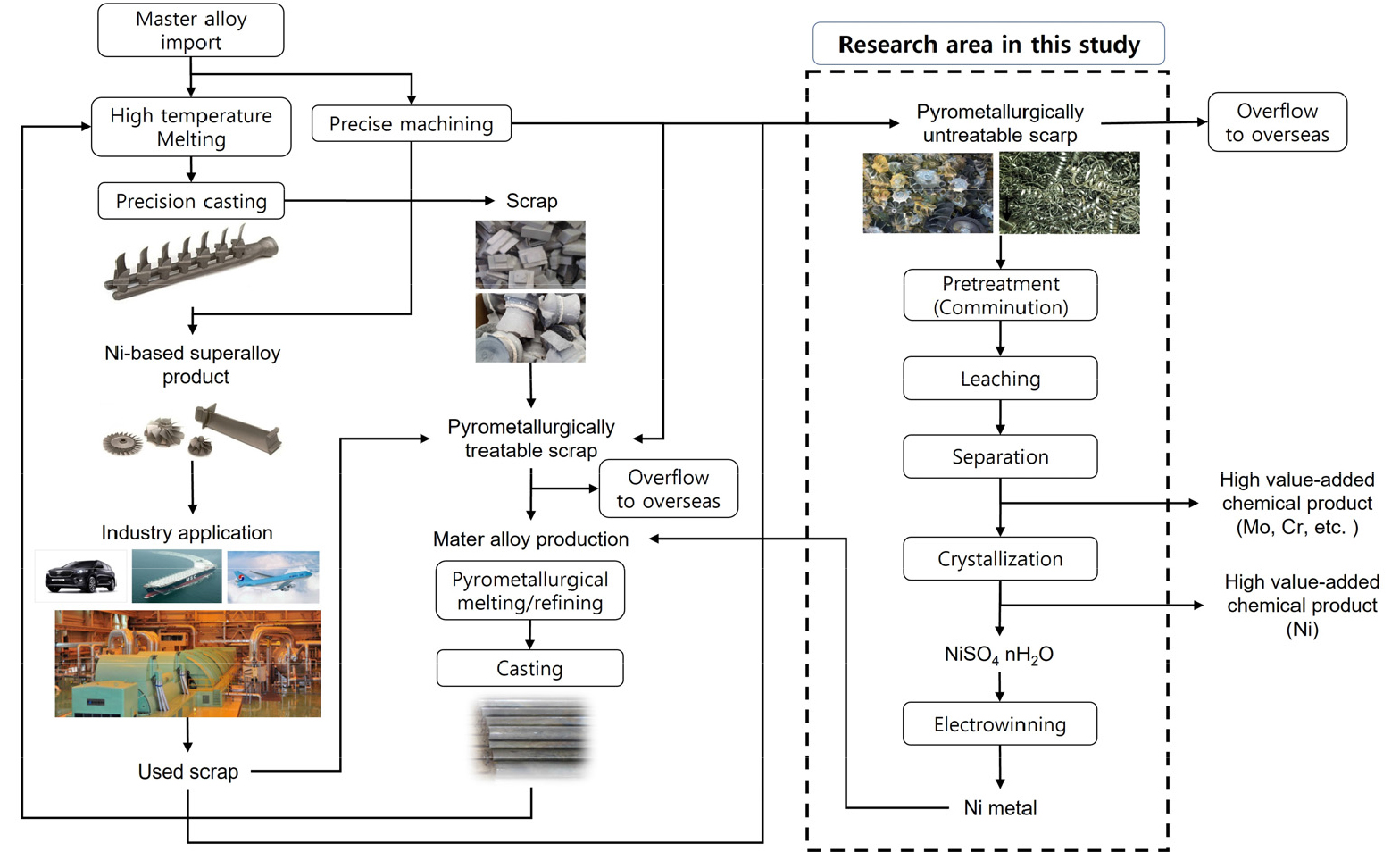
Fig. 1은 이러한 니켈계 내열합금의 국내 물질흐름과 단순 건식 재용해로 재활용할 수 없는 니켈계 내열 합금 스크랩에 대한 본 재활용 연구의 영역을 나타낸 개념도이다. 현재 국내의 인코넬계 모합금 잉곳 제조는 연구개발을 통해 상업적으로 이루어지고 있으나 건식처리가 불가한 오염된 스크랩의 상업적인 재활용은 아직 이루어지고 있지 않다.
Fig. 1에서 보듯이 니켈계 내열합금 스크랩의 재활용을 위해 니켈계 내열합금 중에서도 자동차용 터보차져의 고온 부품 소재로 널리 사용되고 있는 인코넬 713C를6) 대상으로 구성 원소들을 각각 분리하고 정제하는 습식제련 단위 기술들을 이용해 전체 재활용공정을 구성하였다. 파분쇄 전처리는 내식성이 높은 원료의 침출에 필요한 반응 표면적 확보를 위한 단계이며, 침출은 본 연구의 핵심 대상 원소인 니켈과 몰리브데늄 등의 희유금속을 효과적으로 침출하는 단계이다. 또한 침출액으로부터 각각의 희유금속을 분리하기 위한 용매추출 단계를 거쳐 침전법이나 증발결정화법을 이용해 고순도 희유금속 화합물과 황산니켈수화물을 제조하여 부가가치를 향상시킨다. 황산니켈은 리튬이차전지 양극활물질의 원료로 활용 가능하고 전해채취를 통해서 제조된 니켈 금속은 내열 모합금 제조에 사용 가능하다. 이러한 단위기술들을 결합하여 하나의 전체 공정으로 만들 때 각 단위기술 단계를 수행하기 위해 필요한 기술수준과 전체 공정의 효율성이라는 관점에서 기술과 공정이 균형을 이루는 것이 중요할 것이다. 본 연구에서는 인코넬 713C에 함유된 많은 희유금속들 중 우선 니켈을 중심으로 재활용에 필요한 각 단계의 단위기술을 개발하고 이를 이용하여 습식 재활용 공정을 구성하였다. 그리고 이에 대한 기술적 효율성에 대한 평가를 통해 개발된 습식 재활용 공정의 문제점과 다양한 가능성을 함께 제시하고자 하였다.
2. 실험 방법
2.1. 시료
본 연구에서는 인코넬 713C 스크랩을 시료로 사용하였으며, Table 1은 실험에 사용된 인코넬 713C의 주요 조성 분석 결과를 나타낸 것이다. 67.1 % 정도의 니켈 베이스에 크롬, 몰리브데늄, 알루미늄, 니오븀 등을 주요 합금원소로 포함하고 있다.
Table 1.
Major chemical composition of Inconel 713C used in this study
| Element | Cr | Mo | Al | Nb | Ni |
| Content (wt.%) | 13.4 | 4.23 | 5.93 | 2.17 | Bal |
2.2. 방법
2.2.1. 파분쇄 전처리
인코넬 713C 스크랩을 1 cm3 크기로 절단하여 시약급 알루미늄 그래뉼(Junsei, Chemical pure, 8~10 mm)과 일정 무게비로 혼합 후 흑연 도가니에 넣고 유도로를 사용하여 1500 °C에서 90분간 유지한 후 노냉하였다. 상온 냉각 후 알루미나 유발을 사용하여 파분쇄하고 체질을 통해 75 μm 이하 입도의 분말 시료를 얻었다. 분말 시료의 물성은 X-선 회절분석을 실시하여 조사하였다.
2.2.2. 산 침출
Fig. 2는 침출 실험에 사용된 반응기로서 500 mL pyrex 재질의 반응조를 사용하였고 용액 온도조절을 위한 히팅맨틀, 온도조절기 그리고 교반을 위한 교반모터 등으로 이루어져 있다. 니켈의 침출을 위해 침출반응이 좀 더 안정적으로 이루어지는 것으로 판단되는 인코넬 713C: 알루미늄 그래뉼 = 1: 0.681인 시료를 사용하여 침출을 실시하였다. 침출 실험은 농도가 조절된 황산 침출액을 반응기에 넣고 300 rpm의 속도로 교반하면서 설정된 침출 온도에 도달하도록 가열한 뒤 침출시료를 장입하고 침출을 실시하였다. 시료내 주요 금속 성분인 니켈, 알루미늄, 크롬, 몰리브데늄의 침출온도에 따른 침출율을 조사하기 위하여 75 μm 이하의 파분쇄 분말 5.00 g을 2 mol/L 황산 농도, 10 g/L 고액비에서 반응온도를 달리하여 90분간 침출율을 측정하였다. 침출액 및 침출잔사 내 성분은 ICP-OES(Inductively Coupled Plasma Optical Emission Spectroscopy) 정량분석(한국지질자원연구원)을 통해 확인하였다. 침출시간별 주요 금속 성분의 침출율은 식 (1)에 의해 계산하였다.
또한 75 μm 이하의 파분쇄 분말 10.0000 g을 2 mol/L 황산 농도, 20 g/L 고액비, 80 °C 반응 온도에서 2시간 동안 침출 후 고액분리하여 니켈, 알루미늄 등이 용해된 침출액과 몰리브데늄 등이 농축된 침출잔사를 얻었다. 침출시료, 침출액, 그리고 침출잔사내 성분은 ICP-OES 정량분석(한국화학융합시험연구원)을 통해 확인하였다.
2.2.3. 분리정제
니켈 추출을 위해서 먼저 i) 침출액으로부터 잔여황산과 몰리브데늄을 용매추출하여 용액의 pH를 높이는 단계, ii) 알루미늄을 용매추출 하는 단계, iii) 침전법으로 크롬을 추출하는 단계를 거쳐 최종적으로 니켈이 함유된 분리정제액을 얻었다. i) 단계 실험을 위해서는 음이온 추출제 Alamin 336 165 g/ TBP(tributyl phosphate) 30 mL/ bal. Kerosene 으로 이루어진 유기상 300 mL와 침출액 150 mL를(O/A = 2/1) 500 mL 볼륨플라스크에 장입하고 10분간 흔들어 혼합한 뒤 유기상과 수상이 분리될 때까지 두었다. 이후 수상을 채취하여 용액의 pH를 측정하였다. ii) 단계 알루미늄 제거는 초순수로 i) 단계액을 5배 희석하고 추출제로 Cyanex 273x 30 mL/ TBP 5 mL/ bal. Kerosene으로 이루어진 유기상 100 mL와 5배 희석한 수상을 O/A = 1/1인 조건에서 1회 120분/평형 pH 3.13, 2회 36분/평형 pH 3.67의 조건으로 2회 반복하였다. iii) 단계로 Al 추출후 얻어진 수상으로부터 크롬을 제거하기 위하여 NaOH를 첨가하여 용액 pH 4.7에서 크롬 수산화물로 크롬을 제거하였으며 최종적으로 니켈 분리정제액을 얻었다. 각각의 용액내 금속성분의 정량분석은 ICP (한국화학융합시험연구원) 정량분석을 통해 확인하였다. 크롬의 제거율은 식 (2)에 따라 계산하였다.
2.2.4. 니켈 증발농축 결정화
Fig. 3은 분리정제 단계에서 얻어진 니켈 분리정제액으로부터 황산니켈(NiSO4)을 제조하기 위한 진공증발농축 결정화 실험장치를 나타낸 것이다. 분리정제액이 장입되는 회전형 원형 플라스크와 가열을 위한 실리콘오일 배스가 오른쪽에 위치하고 가열 증발된 용액이 응축되어 포집되는 응결장치가 가운데, 그리고 증발농축 결정화 과정에서 시스템의 기압을 제어하는 진공펌프, 응결콘덴스의 냉각수를 공급하는 냉각 배스 등이 중앙에서 좌측으로 위치하고 있다. 전단계인 분리정제과정에서 얻어진 분리정제액을 장입하고 100 °C, 300 mbar, 20 rpm 조건에서 4시간동안 증발농축 과정을 실시한 후 상온으로 냉각하며 결정화를 진행하였다. 생성된 결정화물은 초순수로 세척 후 상온에서 건조하였다. 얻어진 건조산물은 유발로 분쇄 후 X-선 회절분석과 유도결합 ICP 정량분석(한국화학융합시험연구원)을 실시하여 생성물의 상(phase)과 성분 함량을 조사하였다.
2.2.5. 니켈금속 전해채취
금속니켈 전해채취는 Fig. 4와 같이 양극실과 음극실이 아사히 글라스사의 음이온교환막(Selemion AMV)으로 분리된 전해채취 시스템을 사용하여 실시하였다. 전해조는 전극당 유효반응면적이 240 cm2 인 티타늄 음극 2매와 Pb-5% Sb 양극 3매가 각각 음이온교환막으로 분리되는 단위셀 5개가 교대로 맞물리는 구조이다. 양극실과 음극실은 내화학성 순환 펌프에 의해 0.5 mol/L 황산용액 (anolyte)과 황산니켈을 용해하여 제조한 catholyte가 순환할 수 있도록 되어 있다. 그림의 중앙에 위치한 전해조를 중심으로 좌측에 전류를 인가하기 위한 전원공급기와 황산니켈 투입을 위한 교반기 및 투입조, catholyte 순환펌프, 그리고 불순물 여과용 필터 등이 있고 우측에 전해액 온도조절기, anolyte 순환펌프 등이 있다. 그리고 중앙의 전해조에는 전해액 온도조절을 위한 히터와 열전대가 위치하고 있다. Catholyte는 니켈농도 80 g/L, 붕산(boric acid, Junsei GR급) 15 g/L, pH 2.5로 제조하였다. Catholyte 제조에 사용된 황산니켈은 결정화에서 얻어진 것을 사용하였다. 전해채취는 25 mA/cm2 정전류인가, 전해액 온도 60 °C의 조건에서 이루어졌다. 전해채취 시 금속 니켈로 회수되고 빠져나간 전해액 내의 니켈 성분은 황산니켈로 지속적으로 보충하였다. 한편 catholyte의 pH를 실시간으로 측정하여 일정 이하값으로 낮아지면 황산니켈 투입조에 수산화나트륨을 투입하여 pH를 유지하고자 하였다. 전해채취 후 얻어진 금속니켈의 물성은 순도분석(한국화학융합시험연구원)과 X-선 회절분석을 통해 조사하였다.
3. 실험 결과 및 고찰
3.1. 파분쇄 전처리
인코넬 713C 스크랩은 내식성이 높아 벌크상태 스크랩의 산침출은 속도론적으로 매우 비효율적이다. 따라서 적당한 크기로 자른 인코넬 713C 스크랩과 알루미늄을 일정한 비율로 혼합, 고온용융 후 상온냉각을 통해 파분쇄가 용이한 금속간화합물 형성을 유도하였다(Fig. 5). 니켈 내열합금을 알루미늄과 섞은 뒤 고온용융을 통해 니켈-알루미늄 금속간화합물을 형성시키고 이를 파분쇄하여 침출에 용이한 분말로 만드는 것이 보고된 바 있다9).
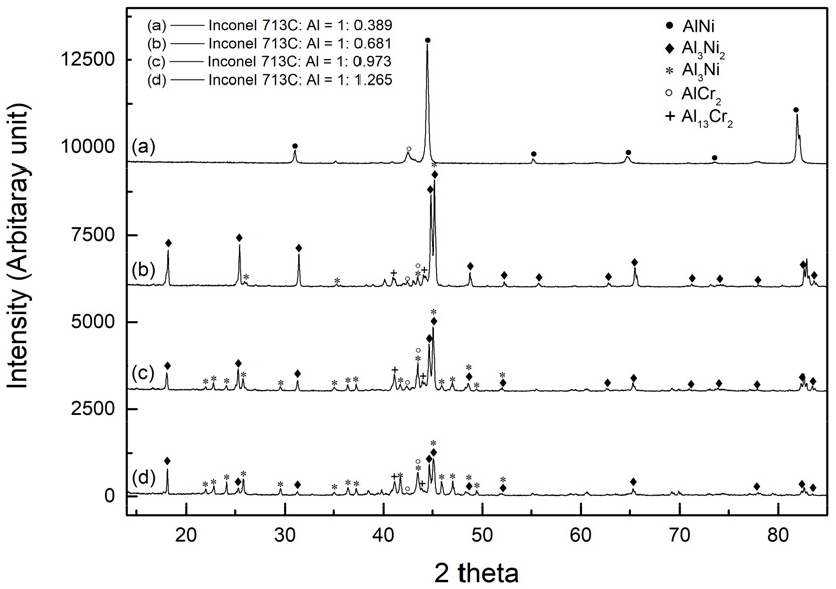
금속간화합물 제조 시 인코넬 713C 스크랩과 알루미늄 그래뉼의 무게비는 1:1.265, 1:0.973, 1:0.681, 1:0.389, 1:0.097, 1:0.055로 변화시켰다. 1:1.265~1:0.389의 비율에 의해 제조된 고온용융 산물은 알루미나 유발에 의해 파쇄가 되었으며, 수작업을 통하여 75 μm 이하로 파분쇄할 수 있었다. 1:0.097 이하의 낮은 알루미늄 함량에서는 인코넬 713C 스크랩의 고온용해가 완전하지 않았으며, 유발에 의한 파분쇄가 되지 않았다. Fig. 6에 파분쇄된 고온용융산물 분말의 XRD 분석 결과를 나타내었다. 혼합비율 1:0.389 조건에서 형성된 고온용융산물은 NiAl 금속간화합물이었으나 1:1.265로 알루미늄의 비율이 높아짐에 따라 Ni2Al3를 거쳐 NiAl3 금속간화합물이 주된 생성물이었다.
3.2. 산 침출
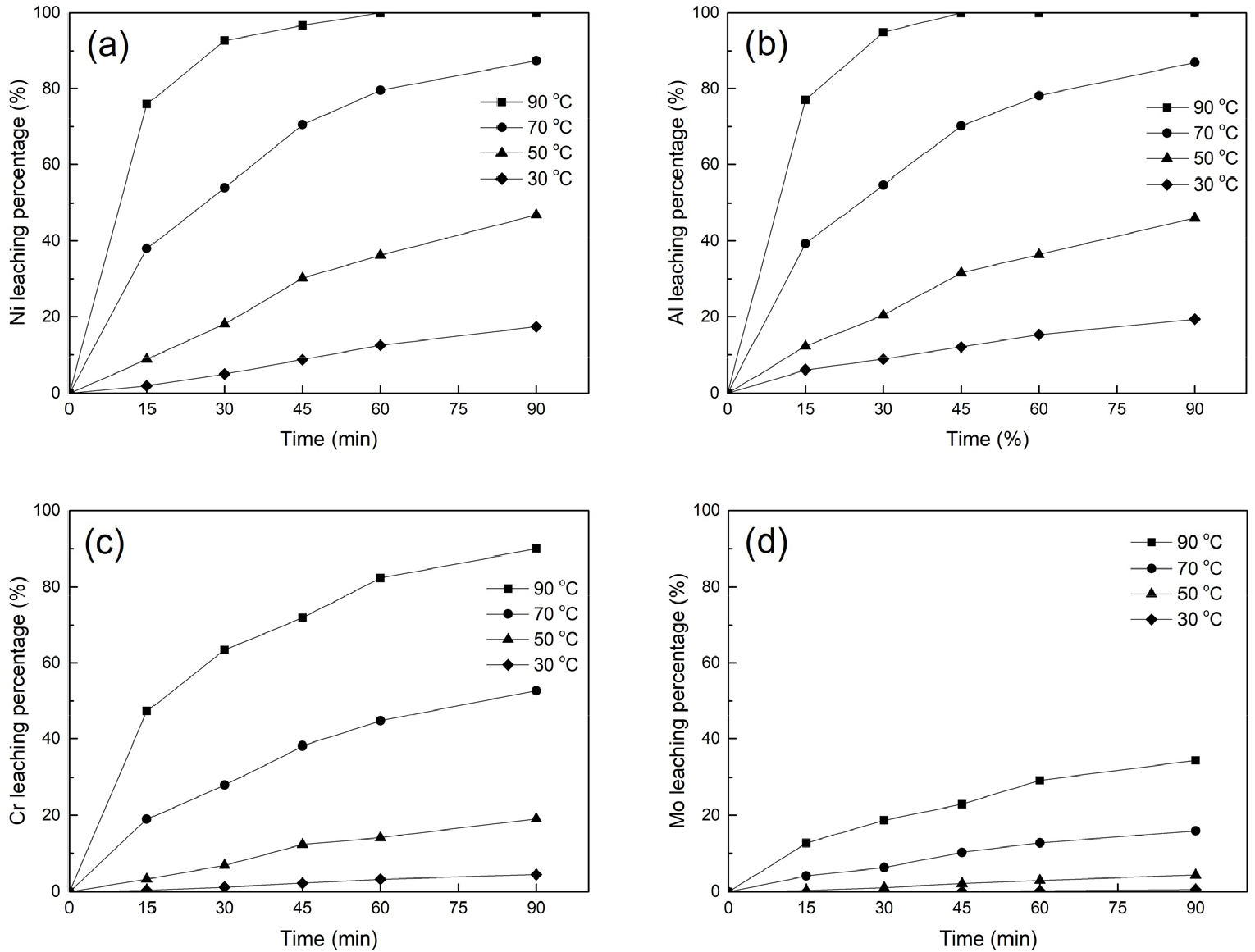
파분쇄의 효율성과 침출의 용이성을 동시에 고려하여 인코넬 713C 스크랩:알루미늄 그래뉼 = 1:0.681 조건에서 얻어진 고온용융/파분쇄(≤ 75 μm) 시료를 침출실험에 사용하였다. Fig. 7은 2 mol/L 황산용액에서 침출온도에 따른 주요 금속 성분의 침출율을 나타낸 것이다. 니켈의 경우 90 °C에서 60분 경과 시 99 % 이상의 침출율에 도달하였으며, 침출온도가 낮아짐에 따라 침출율은 점점 둔화되어 30 °C, 60분 경과 시 12.5 %의 침출율을 나타내었다. 니켈과 금속간 화합물을 형성한 알루미늄은 니켈의 침출과 비슷한 양상을 나타내었으며, 크롬은 전반적으로 약간 낮은 침출율을 나타내었다. 그러나 몰리브데늄은 90 °C, 60분 경과 시에도 29.1 %의 낮은 침출율을 보이고 30 °C, 60분 경과 시는 0.3 %로 거의 침출되지 않는 양상을 나타내었다.
Table 2는 인코넬 713C 스크랩:알루미늄 그래뉼 = 1:0.681 파분쇄 시료 10 g을 2 mol/L 황산 농도, 20 g/L 고액비, 80 °C 반응 온도에서 2시간 동안 침출한 뒤 얻은 침출액과 침출잔사의 성분분석 결과이다. Table 2의 침출시료내 주요 성분의 함량과 침출액과 침출잔사내 성분의 합의 성분분석치 차이는 니켈 3.26, 알루미늄 -1.06, 크롬 4.45, 몰리브데늄 -11.24 %로 몰리브데늄을 제외하고 모두 5% 미만이었다. 니켈은 97 % 이상 침출되었고 몰리브데늄은 대부분 침출잔사에 농축되었다. 잔사내 알루미늄의 경우 분석기관의 고체시료내 해당성분 분석서비스 불가로 분석을 하지 못하였다. 파분쇄를 용이하게 하기 위해 혼합된 알루미늄은 높은 발열 반응으로 침출반응을 격렬하게 만들었으며, 이는 공정 규모가 커질 때 적절한 반응속도 조절이 필요하고 산 소모를 추가로 크게 증가시키는 부분에서 불리한 측면이 있다.
Table 2.
Major chemical composition and its amount of leaching sample, solution and residue
| Sample | Amount of leaching solution and residue | unit | Ni | Al | Cr | Mo |
| Leaching sample | 10.000 g | g | 4.159 | 3.780 | 0.633 | 0.249 |
| Leaching solution | 500 mL | mg/L | 8,410 | 7,480 | 1,010 | 125 |
| %1) | 97.9 | - | 76.4 | 28.3 | ||
| Leaching residue | 1.0132 g | g | 0.0895 | NA3) | 0.1562 | 0.1585 |
| %2) | 2.1 | NA | 23.6 | 71.7 |
3.3. 분리정제
3.3.1. 잔여황산 및 몰리브데늄 추출
Table 3은 침출액, A 용액(잔여황산 및 몰리브데늄 추출 후 수상(aqueous phase)), B 용액(A의 5배 희석액), C 용액(Al 추출 후 수상), D 용액(Cr 침전 제거 후 최종적으로 얻어진 Ni 정제액)의 성분 분석 결과를 나타낸 것이다.
Table 3.
Quantitative analysis of metal content in various solutions
| Sample | Unit | Ni | Al | Cr | Mo |
| Leaching solution | mg/L | 8,410 | 7,480 | 1,010 | 125 |
| A solution | mg/L | 11,000 | 9,720 | 1,190 | ND |
| B solution | mg/L | 2,350 | 2,070 | 250 | ND |
| C solution | mg/L | 2,350 | ND1) | 212 | ND |
| D solution | mg/L | 2,340 | ND | 14 | ND |
용액 pH < 0인 침출액의 잔여황산을 추출 회수하는 단계에서 음이온 추출제인 Alamin 336 을 사용하여 추출을 행한 결과 상분리 후 수상의 부피가 초기 대비 72.7 %로 감소하였고 에에 따라 각 성분의 농도는 증가하였다. 몰리브데늄의 경우에는 황산과 함께 추출되어 유기상으로 이동하였으며, 수상에서는 검출되지 않았다. 황산이 추출되고 얻어진 수상의 pH는 2.23으로 황산이 성공적으로 추출되었음을 알 수 있었다. 황산과 함께 추출된 몰리브데늄은 별도의 분리정제 단계를 거치게 된다10).
3.3.2. 알루미늄 추출
알루미늄을 추출하기 위해 Table 3의 A 용액을 3상 형성 방지를 위해 초순수로 5배 희석한 다음 양이온 추출제인 Cyanex 272x를 사용하여 pH 3~3.5 사이의 조건에서 실험을 실시하였다. 알루미늄의 경우 ICP 분석치의 오차가 크게 발생하여 신뢰성이 떨어지나 본 연구에서는 알루미늄의 거동 이해 정도로 본 실험을 실시하였다. 5배 희석액인 B 용액의 니켈 농도는 2,350 mg/L으로 A 용액 값으로의 환산 시 11,750 mg/L이고 침출액으로부터 유추된 A 용액의 농도가 11,584 mg/L인 것으로 계산되어 니켈의 농도 분석은 오차범위 내에서 정확히 이루어지고 있음을 알 수 있다. 동일 실험을 2회 반복한 뒤 얻어진 수상 C 용액에서 농도변화가 없는 니켈과 달리 알루미늄은 모두 추출되어 검출되지 않았고 크롬도 농도가 약간 감소하였다.
3.3.3. 크롬 추출
알루미늄 추출 단계로부터 얻어진 C 용액 내의 크롬은 212 mg/L으로 크롬 추출을 위해 추출 시 평형 pH를 높이면 니켈이 유기상으로 일부 같이 추출되었다. 이는 니켈의 분리정제 목적에 바람직하지 않다. 따라서 본 연구에서는 크롬과 니켈의 수산화물 생성 pH의 차이를 이용한 침전법으로 크롬을 제거하였다. C 용액의 pH를 4.7로 조절하고 크롬 수산화물 침전을 생성하였다. 고액분리 후 얻어진 용액인 D 용액의 크롬 성분 농도는 14 mg/L으로 크롬의 93.4%가 제거되었다.
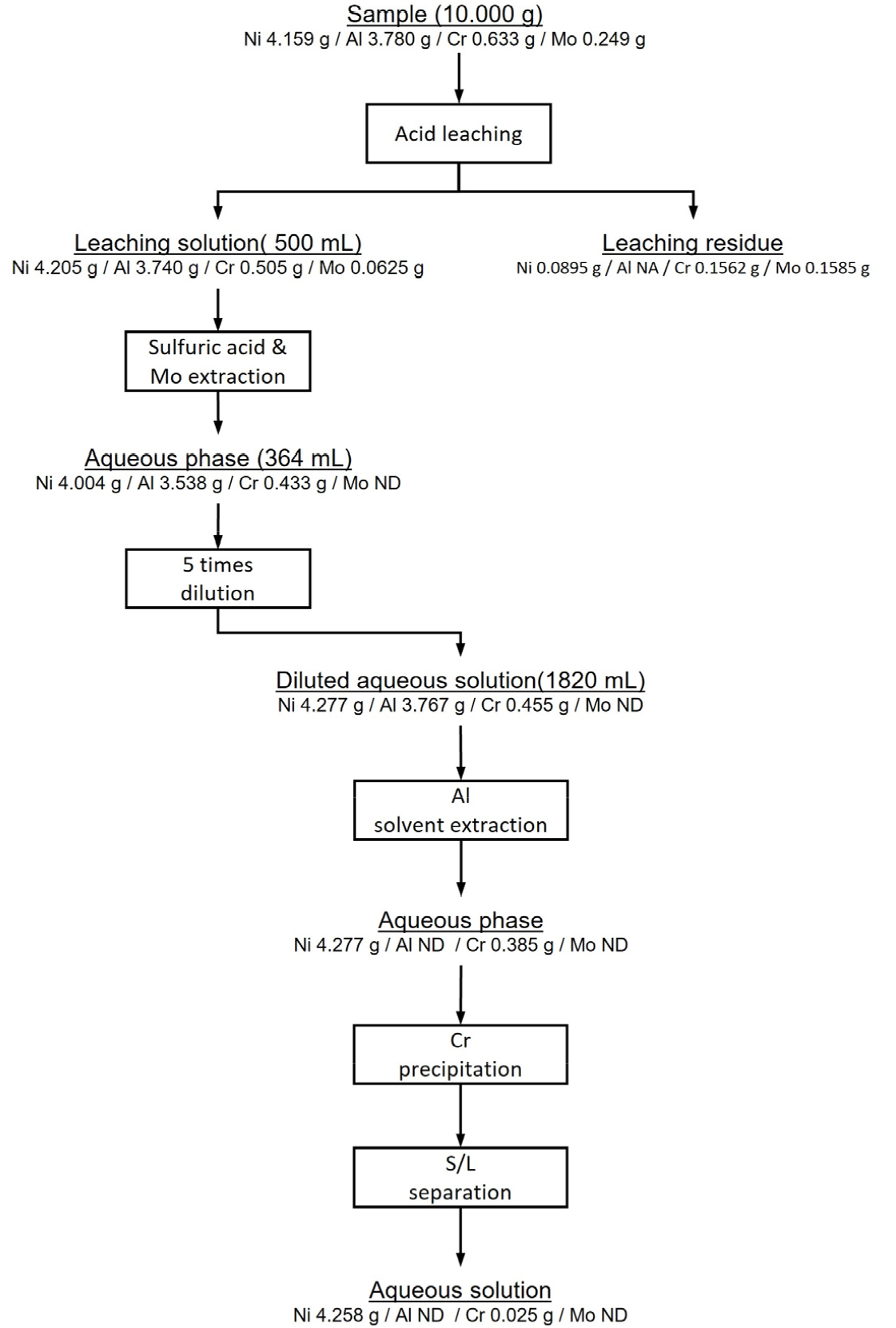
침출부터 크롬추출까지 단계의 물질 흐름을 Fig. 8에 나타내었다. 각 단계의 물질량은 초기 침출시료내 물질량 대비 각 단위공정에서 남은 물질량은 나타낸 것으로 침출잔사 및 크롬 추출후 최종적으로 남은 용액내 니켈의 함량의 합은 침출시료내 니켈량과 4.5 % 차이를 보인다. 이러한 변동은 분석 및 실험 오차를 고려할 때 허용 가능한 범위로 생각된다.
3.4. 니켈 증발농축 결정화
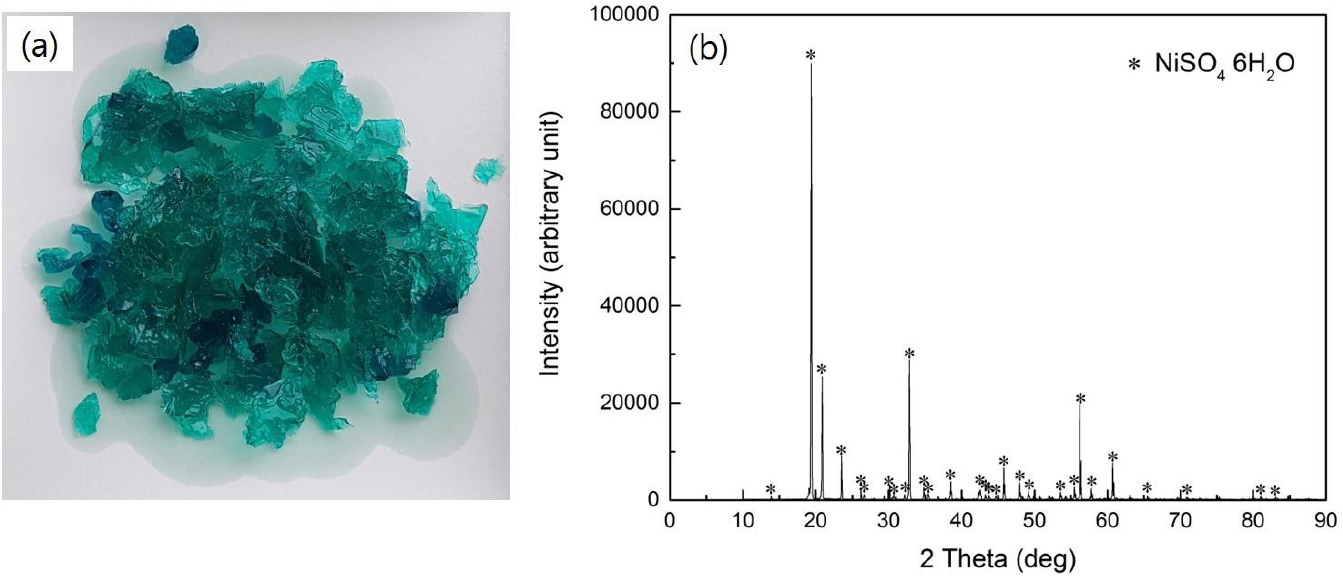
Fig. 9은 증발농축결정화 과정에서 얻어진 석출물의 사진과 X-선 회절분석 결과이다. 청록색의 결정성 석출물과 결정수를 함유한 황산니켈의 X-선 회절 피크가 잘 나타나고 있다. 본 증발농축결정화 과정은 석출된 결정을 회수하고 회수된 양만큼을 다시 분리정제액으로 보충하여 반복함으로 이론적으로는 회수율이 100 %이다. 실질적인 손실은 결정을 세척하는 과정에서 미량 발생하나 세척수를 결정화 플라스크로 공급하여 재회수 가능하다. 제조된 황산니켈은 결정성이 우수한 황산니켈수화물의 X-선 회절분석 결과를 나타내었고 ICP 정량분석을 실시한 결과 크롬은 검출되지 않았다.
3.5. 니켈금속 전해채취
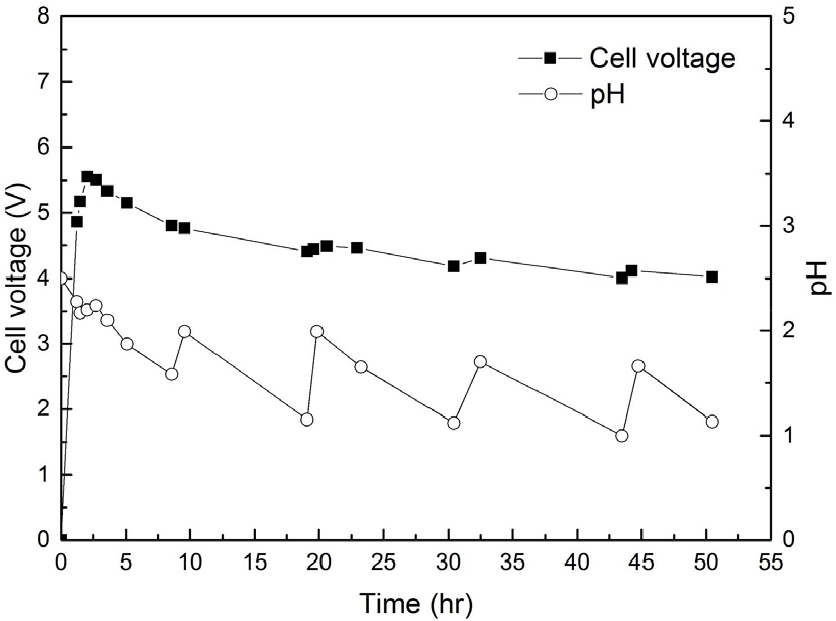
Fig. 10은 정전류 인가 시 측정된 셀전압과 전해액의 pH 변화를 나타낸 것이다. 총 50.48 시간의 전해채취를 실시하였으며, 486 g의 금속 니켈을 얻었다. 이때 셀전압은 초기 5.5 V까지 상승하였다가 서서히 감소하여 4.5 V 수준에 도달하였다. 전해액 catholyte의 pH 변화를 보면 지속적으로 감소하는 경향을 보이고 용액의 pH 유지를 위해 수산화나트륨을 투입할 때 올라가고 다시 감소하는 것을 알 수 있다. 니켈은 표준전극전위가 수소발생전위보다 낮아 용액의 pH가 낮을수록 전류효율이 낮아지게 되고 이를 방지하기 위해 pH 2.5 전후로 유지하는 전해액에서 전해채취를 실시하게 된다. Fig. 8의 전해액의 pH 변화 측정값은 본 연구에서 도입한 음이온 교환막에 의한 양극에서 생성된 수소이온의 음극으로의 이동 차단이 효과적이지 않음을 의미한다. Ren Xiu-lian 등에 따르면 니켈 전해채취 시 양극실과 음극실을 나누는 음이온 교환막을 사용하면 니켈 농도와 pH가 조절된 catholyte를 음극실로 공급하는 전통적인 방식과 달리 양극에서 생성된 수소이온의 니켈 전해채취 반응으로의 영향을 차단할 수 있어 전해액의 pH 조절로부터 자유로운 장점이 있다고 하였다11). 이론적으로는 양극에서 물 분해에 의한 산소발생 시 생성된 수소이온이 음극실로 넘어오지 못하고 음극실에서 전해채취 시 존재하는 수소이온은 수소가스로 환원되어 제거된다. 실질적으로는 양극실에서 소량의 수소이온이 완전하지 않은 음이온교환막의 양이온 차단 성능에 따라 음극실로 이동하여 일정 수준의 pH를 유지하는 것으로 보고하였다. 그러나 본 연구에서 사용된 음이온교환막의 수소이온차단 효과는 필요한 이론적 고려만큼 되지 않아 catholyte의 pH가 지속적으로 감소하는 것으로 나타났다. 이에 따라 catholyte의 pH를 유지하기 위해 수산화나트륨을 지속적으로 투입해야 하였지만, 이온교환막을 사용하도록 설계된 전해셀 구조로 인해 실시간 pH 유지에 효율적이지 못하였다. 따라서 주기적으로 catholyte의 pH를 높여서 공급하는 기존의 방식으로 전해채취를 진행하였고 catholyte의 평균 pH는 1.7 정도이었다. 본 전해채취 실험에서는 5.417 kWh/kg의 전력소모가 측정되었고 이때 전류효율은 73.3 %이었다. 통상적인 상용 니켈 전해채취 공정의 전류효율은 95 % 이상으로 알려져 있다12,13). 전류효율이 낮은 것은 음이온교환막의 기대성능이 예상처럼 되지 않아 전해채취 시 평균 pH가 낮기 때문으로 생각된다.
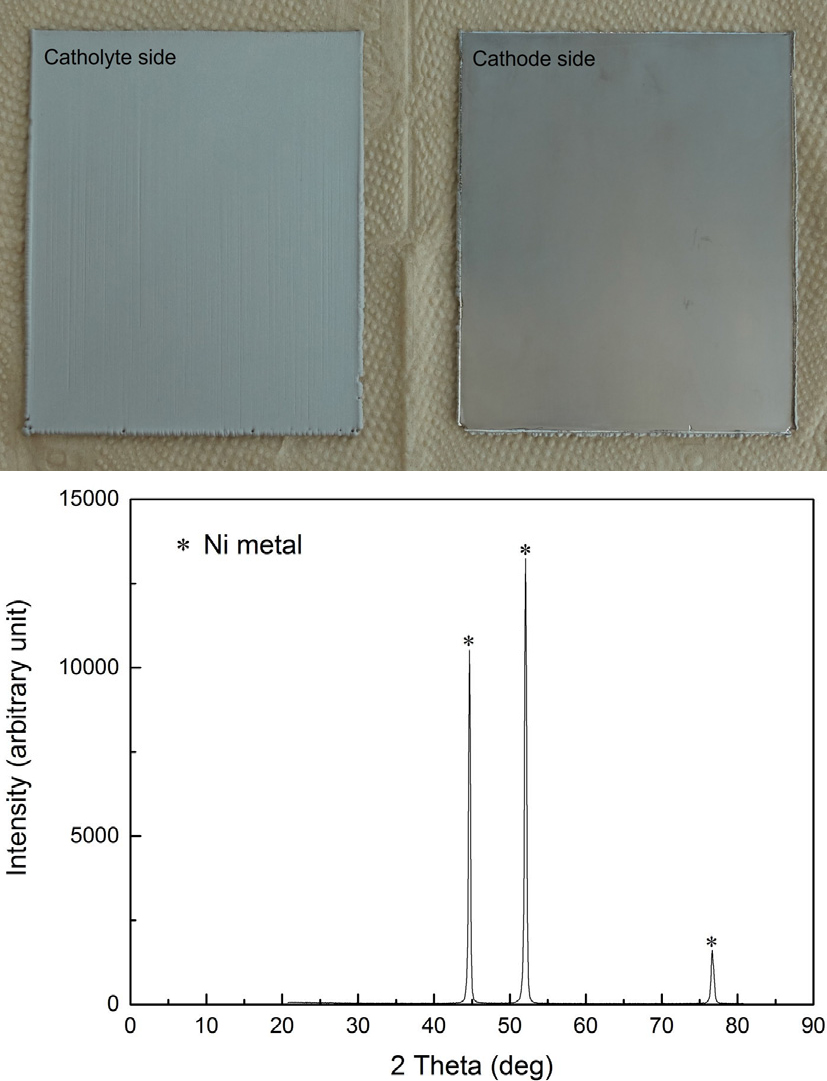
Fig. 11과 Table 4는 상기 전해채취를 통해 얻어진 금속 니켈의 사진과 X-선 회절분석 결과 및 순도 분석을 위한 ICP 분석(한국화학융합시험연구원) 결과를 나타낸 것이다. X-선 회절 분석 결과로부터 결정성이 잘 발달된 금속 니켈임을 알 수 있었으며 99.9 % 순도를 나타내었다. Table 4의 순도 분석으로부터 주요 불순물은 납, 아연, 코발트, 안티몬 등으로 나타났으며, 납과 안티몬은 양극으로부터 기인한 것으로 생각된다.
Table 4.
Quantitative analysis of impurity elements in electrowinned nickel
| Element | Unit | Percentage |
| Pb | % | 0.030 ± 0.01 |
| Co | % | 0.057 ± 0.0808 |
| Cr | % | 0.000 |
| Fe | % | 0.009 ± 0.0095 |
| Cu | % | 0.000 |
| Zn | % | 0.010 |
| B | % | 0.000 |
| Na | % | 0.000 |
| Al | % | 0.000 ± 0.00057 |
| Sb | % | 0.010 |
| Ni | % | 99.881) |
4. 결 론
본 연구에서는 인코넬 713C 사용 후 스크랩으로부터 니켈을 회수하기 위하여 파분쇄, 황산침출, 용매추출, 진공증발농축결정화, 전해채취 등의 단위기술들로 이루어진 공정을 제안하고 평가하였다. 파분쇄 공정을 용이하게 하기 위해 인코넬 713C를 알루미늄과 혼합, 고온용융을 통해 니켈-알루미늄 금속간화합물을 형성시킬 때 니켈:알루미늄 혼합비는 1:0.389 이상에서 파분쇄가 잘 되었다. Ni2Al3가 주 금속간화합물로 형성되는 니켈:알루미늄 = 1:0.681 파분쇄 분말의 황산침출 시 98 % 정도의 니켈 침출율을 얻었으나 혼합된 알루미늄의 용해를 위해 추가로 산이 과다 소모되는 단점이 있었다. 니켈 추출을 위한 전 단계로 황산과 몰리브데늄, 알루미늄 용매추출은 순차적으로 Alamin 336, Cyanex 272x를 사용하여 성공적으로 진행하였다. 크롬의 침전분리, 황산니켈의 결정화 단계를 거쳐 얻어진 황산니켈수화물을 이용한 니켈 전해채취 공정에서는 음이온교환막을 적용한 catholyte pH 자동조절방식을 도입하였다. 그러나 음이온교환막에 의한 양극 생성 수소이온의 차단이 성공적으로 작동하지 않아 음극실의 pH가 조절하한선보다 낮아졌고 이에 따라 낮은 니켈 전착전류효율을 나타내었다. 이때 얻어진 전해채취 니켈의 주요 불순물로 양극으로 사용된 Pb-5 % Sb로부터 기인한 것으로 생각되는 납과 안티몬이 검출되었으나, 순도는 평균 99.9 %로 만족스러운 수준이었다.