1. 서 론
2. 실험방법
3. 실험결과 및 고찰
3.1. SrSO4의 carbothermic 반응에 의한 SrS 제조
3.2. SrS의 수침출에 의한 Sr(OH)2 수용액 제조
3.3. 탄산화(carbonation) 반응에 의한 Sr(OH)2 수용액으로부터 SrCO3 제조
4. 결 론
1. 서 론
스트론튬(Sr) 광물자원은 크게 셀레스타이트(SrSO4) 및 스트론티아나이트(SrCO3)로 나누어지나 생산량 관점에서 볼 때 셀레스타이트가 주요한 광물이다1). Sr은 주로 정광 또는 다양한 화합물 형태로 산업에 사용되는데 이 중 탄산스트론튬(SrCO3)이 가장 많이 사용되고 있으며 컬러 텔레비전 튜브용 유리, 페라이트 자석, 세라믹, 폭죽 등에 사용된다1). Sr의 국내 생산은 전무하며 전량 수입에 의존하고 있다. 희유금속 원재료 수출입 통계에 따르면 2019년 SrCO3 수입규모는 약 13,528톤으로 10,939천불 정도이다2).
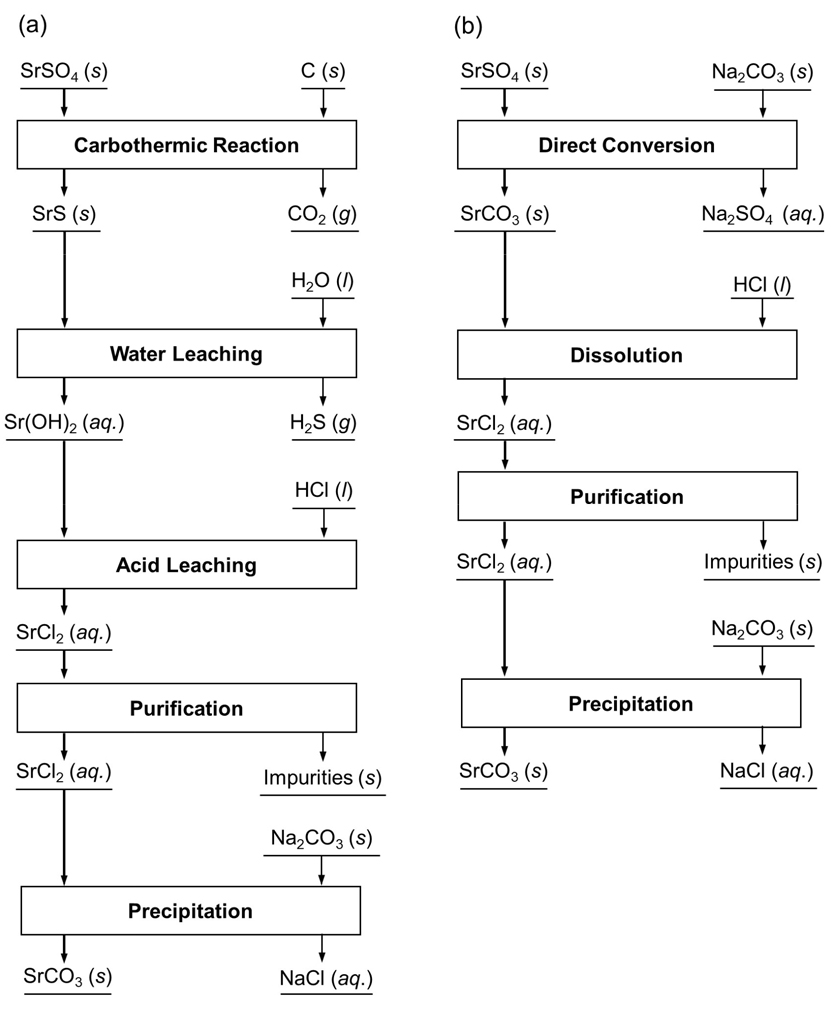
셀레스타이트 광석으로부터 SrCO3을 제조하는 방법으로 Fig. 1에서 볼 수 있는 것과 같이 Black Ash법과 Direct Conversion (또는 Double decomposition)법이 사용된다1,3,4,5,6). Black Ash법은 1373 K에서 탄소 (C)를 이용한 셀레스타이트의 환원 반응에 의해 제조된 황화스트론튬(SrS)을 수침출 시킨 후, 이를 이산화탄소(CO2) 또는 탄산나트륨(Na2CO3)과 반응시켜 침전에 의해 SrCO3을 제조한다. 반면 Direct Conversion법은 셀레스타이트를 Na2CO3 수용액과 368 K에서 반응시켜 SrCO3을 제조한다. 이때 제조된 SrCO3의 순도에 따라 추가적 정제 과정이 필요하며 SrCO3의 염산 침출 후 생성되는 염화스트론튬(SrCl2) 수용액과 CO2 또는 Na2CO3과의 반응에 의해 SrCO3을 제조한다.
Black Ash법은 SrS 이외의 불순물이 수침출 시 용해가 어렵기 때문에 최종 제품 내 불순물 저감에 효과적인 장점이 있으나 고온 환원 반응이 요구되기 때문에 높은 에너지가 소모되는 단점이 있다1,7,8). 반면 Direct Conversion법은 Black Ash법과 비교하여 매우 낮은 온도에서 반응이 일어나기 때문에 에너지 관점에서 유리하나 추가적 정제 공정을 통한 순도 향상이 필요하다는 단점이 있다1).
국외 SrCO3 제조 연구의 경우 기존 Black Ash법의 높은 에너지소모를 낮추기 위해 촉매제 및 활성탄을 사용한 환원온도 저감, 마이크로웨이브 및 mechanochemical법을 이용한 셀레스타이트로부터 SrS 제조 등 다양한 연구결과가 보고되고 있다9,10,11,12). 국내 SrCO3 제조 연구의 경우 한국지질자원연구원에서 해수 내 Sr을 회수하고자 고선택성 Sr 흡착 소재, Sr 농축액 제조공정, 및 Sr 농축액 분리정제 및 화합물화 공정을 개발하였다13). 이를 통해 해수로부터 순도 99.2 %의 SrCO3을 제조하였다고 보고하였다.
국내 Sr 자원의 경우 비단 해수에만 국한되는 것이 아니라 육상 광물 내에도 부존하고 있는 것으로 보고되고 있다. 대표적으로 홍천 자철광의 경우 철 함량이 약 38 mass% 정도로 일반적 철광석 대비 품위가 낮으나 총희토류(T-REO) 함량이 2.4 mass%, Sr 함량이 7.0 mass%로써 다양한 유가금속을 함유하고 있다14). 따라서 한국지질자원연구원에서는 국내 미활용 자원으로부터 유가금속 회수를 통한 자원 자급도 향상을 위해 홍천 자철광으로부터 유가금속 회수 공정을 개발하였다14).
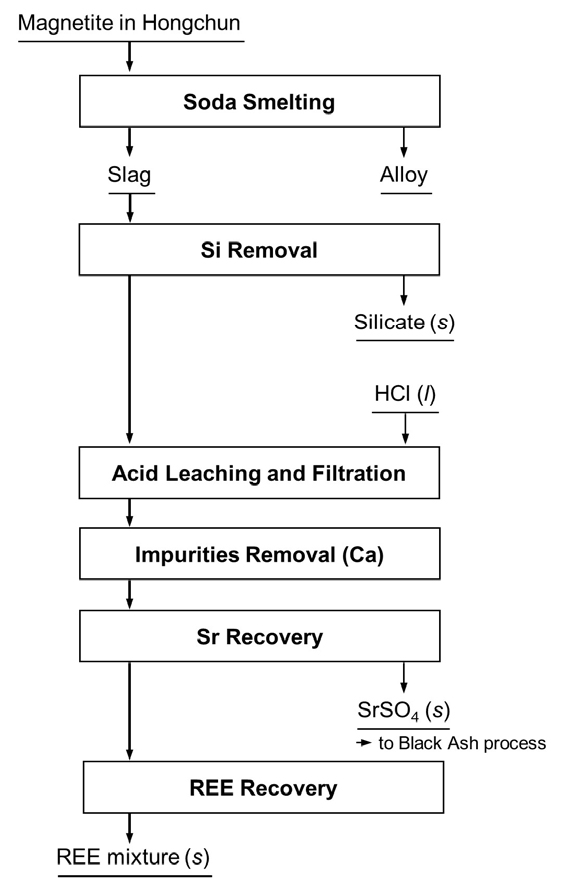
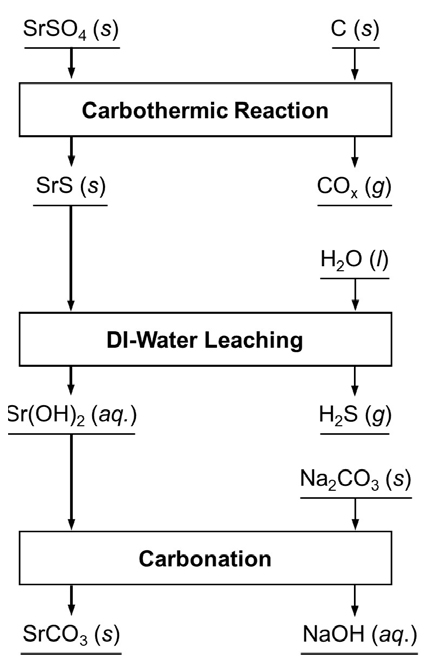
Fig. 2는 홍천 자철광으로부터 유가금속 회수를 위한 공정 흐름도로써 홍천 자철광의 용융환원을 통해 철 및 망간 등의 금속상과 규소, 칼슘, 마그네슘, Sr, 및 희토류 산화물 등으로 이루어진 슬래그를 제조하고 슬래그로부터 희토류 및 Sr을 회수한다. 이와 같은 전체 공정 중 본 연구에서는 Fig. 3에서와 같이 국내산 홍천 자철광으로부터 회수된 고순도 SrSO4로부터 SrCO3의 제조 가능성을 확인하기 위해 Black Ash 법을 적용한 기초 실험을 수행하였다. 본 연구에서는 Fig. 2의 공정을 통해 제조된 SrSO4가 고순도의 원료이기 때문에 Fig. 1(a)의 산침출 및 정제공정이 생략되었다.
2. 실험방법
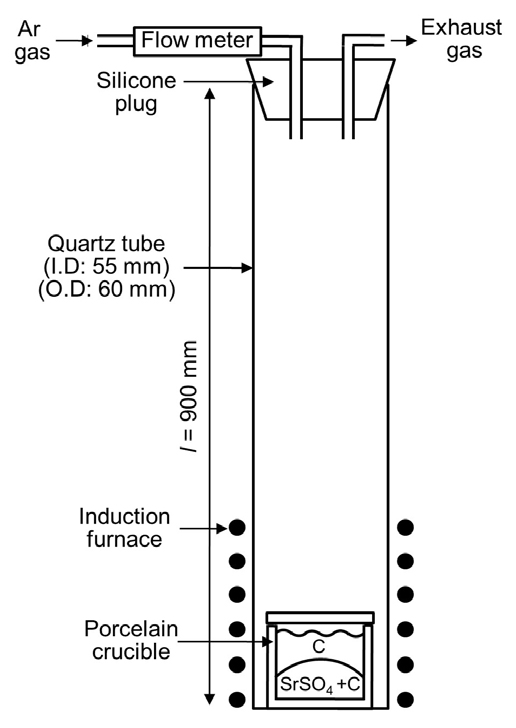
Fig. 4는 Black Ash법의 첫번째 단계인 carbothermic 반응에서 사용한 실험 장치의 모식도를 나타내며 Table 1은 carbothermic 반응의 실험 조건을 나타낸다.
Table 1.
Experimental conditions of the carbothermic reaction of SrSO4
|
Exp no.a |
Reaction Temp., T / K |
Weight of C, wC / g |
Weight of SrSO4, wSrSO4 / g |
Reaction time, tr / h |
| 141030 | 1273 | 1.973 | 2.971 | 3 |
Carbothermic 반응에서 사용한 SrSO4는 혼합광 슬래그로부터 약산 침출 – pH 조절 – 수산화물의 선택적 침출 – SrSO4 회수의 과정에 의해 만들어진 고순도 SrSO4를 사용하였으며14), 건조 오븐을 이용하여 350 K에서 72 시간 이상 건조 후 실험에 사용하였다.
Carbothermic 반응 실험을 위해 Fig. 4에서 볼 수 있는 것과 같이 석영 반응관에 SrSO4 및 탄소 분말(Kojundo Chemical Lab. Co., Ltd., purity ≥ 99.9 %)의 혼합물과 그 위를 탄소 분말로 채운 자재 도가니(porcelain crucible)를 장입하였다. 이후 석영 반응관의 내부 분위기를 아르곤(Ar) 가스로 치환 시켰으며 실험 중 유량계를 이용하여 Ar 가스를 2 l/min로 흘려주었으며 반응관 내부 압력은 1 atm으로 유지하였다.
시료 준비가 끝난 후 석영 반응관을 유도로(induction furnace)에 설치하고 50 K/min.으로 승온 후 1273 K에서 3 시간 반응시켰다. 반응이 끝난 후에는 반응관을 유도로에서부터 즉시 제거한 후 반응관 온도가 상온에 도달할 때까지 자연 냉각시켰다.
Carbothermic 반응 후 얻어진 반응 생성물은 Table 2의 조건에 따라 353 K에서 0.5 시간 수침출을 실시하였다. 침출이 끝난 후 침출액과 미용해 고체 잔사는 여과지를 사용하여 분리하였으며 여과지에 남은 고체 잔사는 건조 오븐을 이용하여 350 K에서 0.5 시간 건조시켰다.
Table 2.
Experimental conditions of water leaching of the residues obtained after the carbothermic reduction
|
Exp no.a |
Reaction Temp., T / K |
Volume of water, vwater / ml |
Weight of feedstock, wfeedstock / g |
Leaching time, tl / h |
| 141030 | 353 | 200 | 0.996 | 0.5 |
Table 3은 carbonation 반응의 실험 조건을 나타낸다. Carbonation 반응을 통해 SrCO3을 제조하기 위해 298 K에서 Na2CO3과 수침출 및 여과를 통해 얻어진 침출 정제액을 0.5 시간 반응시켰다. Carbonation 반응 후 용액 중 생성된 흰색의 반응 생성물은 테플론 필터를 사용하는 electric aspirator(JEIO TECH. CO., LTD., model: VE-11)를 이용하여 분리한 후 건조 오븐을 이용하여 350 K에서 6 시간 건조시켰다.
Table 3.
Experimental conditions of carbonation of the leachate obtained after the water leaching
|
Exp no.a |
Reaction Temp., T / K |
Reaction time, t’r / h |
Volume of water, vwater / ml |
Weight of Na2CO3, wNa2CO3 / g |
Volume of leachate, vleachate / ml |
| 141030 | 298 | 0.5 | 200 | 3.527 | 190 |
각 단계의 반응에서 얻어진 샘플의 조성은 inductively coupled plasma optical emission spectrometer(ICP-OES: PerkinElmer, Optima 5300DV / Thermo Scientific, iCAP 6000 series)를 사용하여 분석하였다. 또한 샘플의 결정상은 X-ray diffraction(XRD: RIGAKU, RINT 2200, Cu-Kα raditation)을 이용하여 분석하였으며 샘플의 미세조직 및 조성은 scanning electron microscopy/energy dispersive X-ray spectroscopy(SEM/EDS: JEOL, 6380A)을 사용하여 분석하였다.
3. 실험결과 및 고찰
3.1. SrSO4의 carbothermic 반응에 의한 SrS 제조
Fig. 5(a)는 SrSO4의 carbothermic 반응이 끝난 후 회수한 반응 생성물의 사진이다. 사진에서 볼 수 있듯이 반응 후 회색빛을 띄는 반응 생성물이 얻어졌으며 반응 생성물을 회수 시에 석영 반응관으로부터 유황 냄새가 나는 것을 확인할 수 있었다.
Fig. 6(a), (b), 및 (c)는 각각 background, carbothermic 반응에 사용한 고순도 SrSO4 원료, 및 SrSO4의 carbothermic 반응 후 얻어진 반응 생성물의 XRD 분석 결과를 나타낸다. 또한 Table 4는 carbothermic 반응에 사용한 고순도 SrSO4 원료와 carbothermic 반응 생성물의 성분분석 결과를 나타낸다. 본 실험에 사용된 원료 및 각 단계에서 제조된 샘플의 경우 기 보고된 분석 결과14) 및 EDS 분석 시 금속 원소로써는 Sr 및 구리 (Cu)만 분석된 결과를 바탕으로 Sr, Ca, 및 Cu에 대해서 ICP-OES 성분분석을 실시하였다.
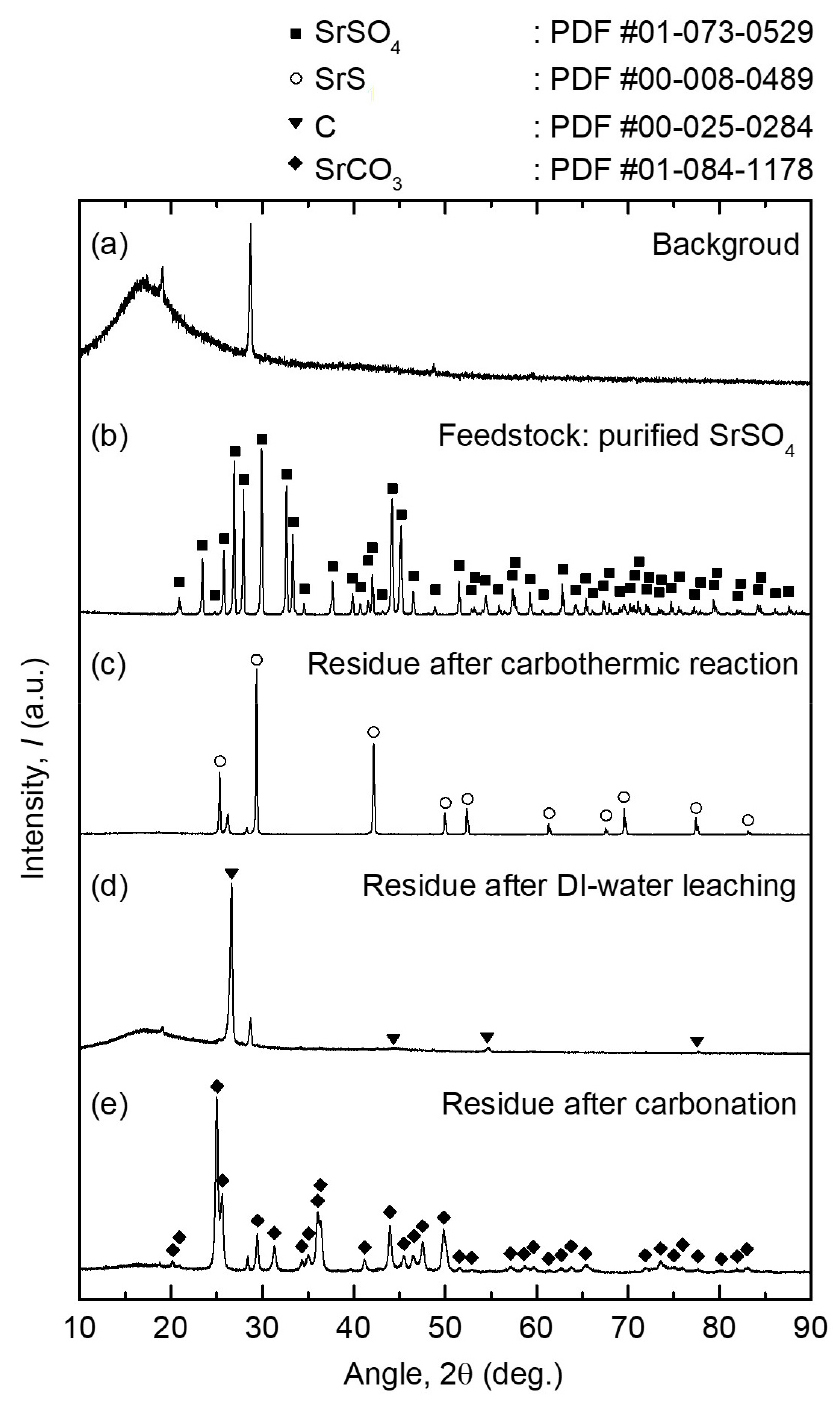
Fig. 6.
XRD analysis results of (a) background, (b) high-purity SrSO4 feedstock, (c) residues obtained after carbothermic reaction of SrSO4, (d) residues in a filter paper obtained after water leaching obtained after water leaching, (e) residues obtained after carbonation reaction of purified Sr(OH)2.
Table 4.
Analytical results of the feedstock and residues after each experiment
Fig. 6(b) 및 (c)와 Table 4의 결과에서부터 식 (1)과 같은 SrSO4의 carbothermic 반응에 의해서 고순도 SrS이 생성되었음을 알 수 있다. Fig. 7(a) 및 (b)는 각각 carbothermic 반응에 사용된 SrSO4 원료 및 반응 생성물의 SEM 이미지이다. SEM 이미지에서 볼 수 있는 것과 같이 carbothermic 반응 전 후, 원료 및 생성물의 입자 크기 및 표면 형상에는 큰 차이가 나타나지 않았다.
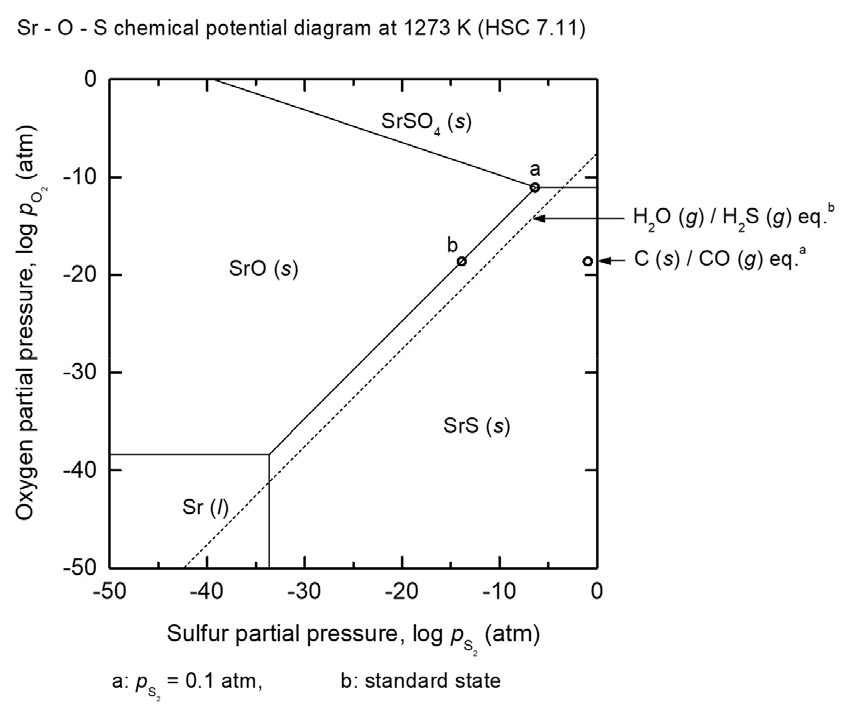
SrSO4의 carbothermic 반응을 열역학적으로 고찰하는 경우 SrSO4, SrS, 및 SrO간의 반응을 고려 할 필요가 있으며, 따라서 Sr-O-S계의 화학포텐셜 다이어그램(chemical potential diagram)을 이용한 열역학적 검토가 필요하다. Fig. 8은 1273 K에서 Sr-O-S계의 화학포텐셜 다이어그램을 나타낸다15). Fig. 8에서 x축은 황 화학포텐셜(sulfur chemical potential, pS2)이며 y축은 산소 화학포텐셜(oxygen chemical potential, pO2)을 나타낸다. 본 다이어그램에서 각 화합물이 위치하는 2차원 평면 영역은 1273 K에서 반응계 내의 pS2 및 pO2의 값이 해당 영역 내에 위치할 경우 영역 내 화합물이 안정상임을 의미한다.
Carbothermic 반응의 경우 탄소를 사용하기 때문에 Fig. 8에서 볼 수 있는 것과 같이 반응계 내 pO2은 C (s) / CO (g) eq.에 의해서 제어되며 값이 결정된다. 그러나, Fig. 8에서 볼 수 있는 것과 같이 SrSO4로부터 SrS를 생성하기 위해서는 반응계 내의 pO2뿐만 아니라 pS2도 제어되어야 함을 알 수 있다.
우선, 반응계 내의 pS2가 Fig. 8 내 a 점의 x축 값인 5.09 × 10-7 atm보다 큰 값을 가질 경우 반응계 내의 pO2 값이 9.53 × 10-11 atm 보다 작다면 SrSO4로부터 SrS가 생성가능함을 알 수 있다. 따라서 pO2가 C (s) / CO (g) eq.에 의해서 제어되고 pS2가 5.09 × 10-7 atm보다 크다면 SrSO4로부터 SrS가 생성된다. 또한 pO2가 C (s) / CO (g) eq.에 의해서 제어되고 반응계 내의 pS2가 Fig. 8 내 b점의 x축 값인 1.69 × 10-14 atm보다 클 경우 SrSO4로부터 SrS가 식 (1)에 의해 생성되게 된다. 그러나, 실험 조건에 따라 반응계 내 pS2가 1.69 × 10-14 atm 보다 작을 경우, SrSO4로부터 SrO가 식 (2)에 의해서 생성될 가능성이 있음을 알 수 있다.
M.M. Hessien은 1273 K에서 SrSO4의 carbothermic 반응에 의해 SrO가 일부 생성되었음을 보고하였다5). 따라서 Black Ash법을 적용하여 SrSO4로부터 SrCO3의 생성 가능성을 검증한 본 실험에서는 Fig. 6(c)의 결과와 같이 SrO의 생성없이 SrS을 얻을 수 있었지만 열역학적으로 SrS만을 얻기 위해서는 반응계 내의 pS2를 적극적으로 제어할 필요가 있음을 알 수 있다. SrO 생성 시 원료 내 함유된 산화물 불순물에 따라 복합산화물 형성에 의한 Sr 회수율 저감의 원인이 될 수 있으며 또한 환경유해성의 SO2 가스 발생 등 제조공정 상 난점이 발생한다.
3.2. SrS의 수침출에 의한 Sr(OH)2 수용액 제조
Fig. 5(b) 및 (c)는 각각 SrSO4의 carbothermic 반응으로 제조된 SrS을 포함한 반응 생성물을 수침출 시킨 후 여과지를 사용하여 걸러진 용액 및 여과지에 남아있던 잔사의 사진이다. 사진에서 볼 수 있는 것과 같이 침출액 여과 시 투명한 수용액과 흑색의 잔사로 분리되었다. Fig. 6(d)는 여과지에 남아있던 잔사의 XRD 분석 결과이다. XRD 분석결과에서 알 수 있는 것과 같이 잔사의 경우 탄소로 분석되었다.
SrS의 수침출 시 총합반응은 식 (3)과 같다1,4,5). 식 (3)의 경우 ∆G°r이 작은 양의 값을 가지고 있고 반응에 의해서 생성되는 H2S 가스가 반응계 내에서 제거되기 때문에 정방향의 반응이 진행된 것으로 사료된다. 따라서 353 K에서 SrS의 수침출 시 Sr(OH)2 수용액 제조되고 탄소 분말 등의 미용해 고체 불순물의 경우 여과에 의해 제거 가능함을 알 수 있다. 이때 Sr(OH)2의 물에 대한 용해도는 273 K에서 0.41 g/100 mL, 373 K에서 21.83 g/100 mL이기 때문에 수침출 시 높은 침출률을 위해서는 침출온도가 중요함을 알 수 있다16). 또한 식 (4)에서 볼 수 있는 것과 같이 수침출 시 SrO로부터 Sr(OH)2 수용액이 제조되는 것을 알 수 있다. 따라서 SrSO4의 carbothermic 반응 시 SrS로 전환되지 않고 SrO로 일부 전환되었다고 하더라도 수침출 시 Sr(OH)2 수용액으로 제조 가능함을 알 수 있다.
3.3. 탄산화(carbonation) 반응에 의한 Sr(OH)2 수용액으로부터 SrCO3 제조
탄산화 반응에 의해 Sr(OH)2 수용액으로부터 SrCO3의 제조를 위해 CO2 가스 또는 Na2CO3을 탄산화제(carbonating agent)로 사용할 수 있는데 본 연구에서는 Na2CO3을 사용하였다.
상온에서 Na2CO3을 Sr(OH)2 수용액에 용해시켜 반응시킨 결과 Fig. 5(d)와 같은 흰색의 분말이 즉시 생성되기 시작하였다. Fig. 6(e)는 탄산화 반응으로 생성된 침전물의 XRD 분석 결과를 나타내며 Table 4는 생성된 침전물의 성분 분석 결과를 나타낸다. Fig. 6(e) 및 Table 4의 결과로부터 SrCO3가 식 (5)의 반응에 의해 생성되었음을 알 수 있다. Table 4에서는 순도 평가를 위한 전원소 분석은 이루어지지 않았지만 제조된 SrCO3 분말 내 Cu만 불순물로 존재할 경우 순도는 약 99.96 %이다. Fig. 7(c)는 탄산화 반응에 의해서 제조된 SrCO3의 SEM 이미지이다. 탄산화 반응에 의해 용액 내 Sr2+ 이온이 석출되어 SrCO3가 제조되었기 때문에 1차 입자(primary particle)의 크기가 Fig. 7(a) 및 (b)의 SrSO4 원료 및 SrS 대비 작음을 알 수 있다.
4. 결 론
본 연구에서는 Black Ash법을 이용하여 국내산 홍천 자철광으로부터 회수된 SrSO4로부터 SrCO3가 제조 가능함을 실험적으로 증명하였다. 1273 K에서 SrSO4의 carbothermic 반응을 통해 SrS가 생성되며 열역학적으로 고찰을 통해 SrS의 제조를 위해서는 반응계 내의 황 화학포텐셜의 적극적 제어가 필요함을 밝혔다. 353 K에서 생성된 SrS 함유 잔사의 수침출 및 여과 시 Sr(OH)2 수용액이 제조되었다. 이를 298 K에서의 Na2CO3를 이용한 탄산화 반응에 의해 SrCO3가 생성됨을 증명하였다.