1. 서 론
2. 마그네슘 열환원법을 이용한 TiO2으로부터 저산소 Ti 제조를 위한 열역학적 고찰
3. 실험방법
3.1. TiO2 원료 분급 및 환원 반응을 위한 전처리
3.2. Mg 금속을 이용한 열환원
3.3. 환원 반응 산물의 HCl 침출
3.4. 분석 방법
4. 결과 및 고찰
4.1. 건식 체질한 TiO2 입도가 환원 후 Ti 산물의 산소 농도에 미치는 영향
4.2. H2 분위기에서 Mg 금속을 이용한 열환원법에 의한 TiO2로부터 저산소 Ti 금속 제조 메커니즘
4.3. TiH2 산물의 산소 농도 저감의 한계 원인 분석
4.4. TiO2 원료의 분급 방식이 Ti 산물의 산소 농도에 미치는 영향
5. 결 론
1. 서 론
타이타늄(Ti) 및 Ti 합금은 높은 비강도 및 내식성 등 우수한 물리·화학적 특성을 가지고 있어 항공우주, 해양, 군사 등 다양한 산업 분야에서 널리 사용되고 있다1,2,3,4,5,6). 또한, Ti은 생체적합성이 우수하여, 인공 관절이나 치과용 임플란트 등 의료용 소재로도 널리 사용되고 있다6,7). 이에 따라 Ti에 대한 수요가 지속적으로 증가하고 있다8).
그러나 Ti은 지각 내 아홉 번 째로 풍부한 원소임에도 불구하고, 고순도 금속으로의 제조가 어렵기 때문에 희소금속으로 분류되고 있다4,5,9). 특히, Ti은 산소와의 친화력이 크며 Ti의 산소 농도 증가 시 인성 및 연성 등 다양한 기계적 특성이 저하된다10,11). 따라서 Ti 금속 내 불순물 함량에 따라 Commercially Pure(CP) 등급을 구분하고 있는 국제표준(ASTM, American Society for Testing and Materials)에서는 Ti 금속 내 산소 함량이 주요 지표로 사용되고 있으며, Grade(Gr.) 1은 0.18 mass% 이하, Gr. 2는 0.25 mass% 이하로 규정하고 있다12).
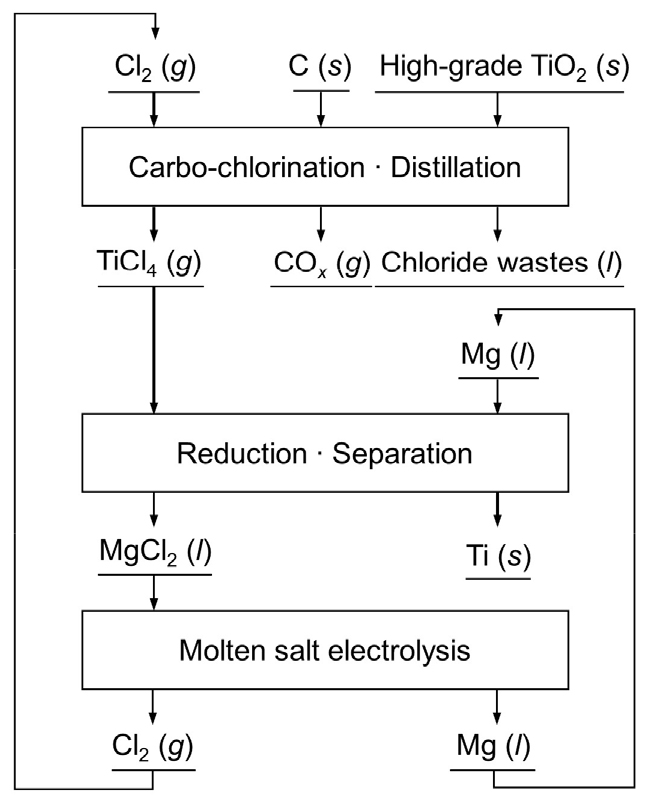
Ti의 높은 산소 친화력으로 인해 현재 Ti 금속은 Fig. 1과 같이 염화물 기반의 Kroll법에 의해 상용 생산되고 있다. Kroll법의 첫번째 단계는 carbo-chlorination으로, 1273 K의 탄소(C)가 존재하는 반응기 내에서 순도 95 % 이상의 고품위 이산화타이타늄(TiO2)과 염소(Cl2) 가스와의 반응에 의해 사염화타이타늄(TiCl4)을 생성한다. 이후 1073 K에서 마그네슘(Mg) 금속을 이용한 TiCl4의 환원 반응에 의해 고용 산소 약 500 ppm의 고순도 Ti 금속이 제조된다. 이때 부산물로 생성된 염화마그네슘(MgCl2)은 1273 K에서의 진공증류에 의해 Ti 금속 산물로부터 분리·회수된다. 분리·회수된 MgCl2은 925 – 943 K의 고온에서 용융염전해를 통해 Mg 금속과 Cl2 가스로 회수되며 이는 각각 TiCl4의 환원과 고품위 TiO2의 carbo-chlorination 반응에 사용된다4,13,14,15,16,17,18,19).
그러나 Kroll법은 고순도 Ti 금속을 생산할 수 있는 장점이 있는 반면 환경부하가 크다는 단점도 존재한다. 예를 들어, carbo-chlorination 반응의 경우 다량의 온실가스(COx)가 배출되며 독성의 Cl2 가스가 사용된다. 또한, 환원 반응은 큰 발열반응이며 회분식(batch)으로 조업이 이루어지고 있어 반응기(retort) 당 1 톤/일로 낮은 생산성을 나타내고 있다16,17,18).
이러한 종래 기술의 한계를 극복하고자 고순도·저산소 Ti 금속 제조를 위한 신 제련법 개발이 활발히 이루어지고 있다. 특히, TiO2으로부터 직접적으로 Ti 금속을 제조하기 위해 Ti 금속보다 산소에 대한 친화력이 큰 금속 환원제(M)를 이용한 TiO2의 금속 열환원법이 주목받고 있다. 이러한 신규 제련법은 TiO2의 TiCl4으로의 전환이 생략됨으로써 제련공정이 단순화되며, Cl2 가스를 사용하지 않기 때문에 환경부하를 줄이고 공정 안전성을 향상시킬 수 있다2,20,21).
TiO2의 금속 열환원법에 의한 Ti 제조 시, 사용되는 금속 환원제에 따라 Ti 금속 내 한계 고용 산소 농도가 결정된다. TiO2으로부터 Ti 금속을 직접 제조할 수 있는 대표적인 금속 환원제로는 Mg, 칼슘(Ca), 이트륨(Y) 등이 있다. 이 중 Ca과 Y은 매우 강한 환원제이며, 1200 K에서 환원 시 Ti 내 고용 산소를 약 100 ppm까지 낮출 수 있다. 그러나, Ca과 Y은 고가의 환원제로써 이를 이용한 열환원법의 경우 공정의 경제성 확보에 어려움이 따른다. 반면, Mg은 상대적으로 저렴한 환원제이나 1200 K에서 환원 시 Ti 내 고용 산소가 약 2.00 mass%으로, ASTM Gr. 1 기준인 1800 ppm까지 낮출 수 없다는 단점이 있다21).
그러나 최근 Mg 금속을 환원제로 사용한 저산소 Ti 금속 제조에 대한 연구가 활발히 진행되고 있다. 이는 크게 환원 반응 부산물인 산화마그네슘(MgO)의 활동도(activity)를 낮추는 방법과 Ti 내 고용 산소의 활동도 계수(activity coefficient)를 높이는 방법으로 나눌 수 있다22,23,24). 이 중 Ti 내 고용 산소의 활동도 계수를 높이는 방법의 경우 수소를 활용하고 있어 비교적 공정이 간단하며 MgO의 활동도를 낮추기 위한 전자(electron) 또는 시약의 사용이 없어 공정비용 측면에서 유리하다.
수소 가스(H2) 분위기에서 Mg 금속을 이용한 환원 후 탈산반응을 통해 TiO2으로부터 저산소 Ti을 제조하는 공정이 주로 보고되었으나21,25,26,27), 최근 단일단계 환원 반응에 의한 0.21 mass% 산소를 함유한 Ti 제조 결과가 보고되었다24). H2 분위기에서 Mg 금속을 이용한 TiO2의 단일단계 환원 반응의 경우 환원 후 생성된 최종 Ti 산물의 산소 함량에 환원 시간, TiO2 원료 입도, 수소 화학포텐셜(hydrogen chemical potential, pH2) 등 다양한 공정변수가 영향을 미친다.
이 중 TiO2 원료 입도의 경우, 환원 전 TiO2 원료의 입도가 Mg 금속을 이용한 환원 후 Ti 산물의 최종 산소 농도에 미치는 영향이 보고된 바 있다. Zhang et al.(2016) 은 nano-sized, 10 μm 및 20 – 45 μm의 입도 범위를 갖는 TiO2 원료를 각각 993 – 1173 K에서 환원하여 Ti 산물의 산소 농도를 비교한 결과, nano-sized TiO2을 사용했을 때 Ti 산물의 산소 농도는 1.28 mass%를 나타냈으며, 20 – 45 μm의 입도 범위에서는 가장 낮은 산소 농도인 0.78 mass%를 얻었다21). 그러나, 45 μm 이상의 입도를 갖는 TiO2 원료를 Mg 금속으로 환원하여 제조한 Ti의 산소 농도에 대한 평가는 아직 보고된 바 없다. 또한, 최근 Song et al.(2025)은 습식 체질로 분급된 TiO2의 입도 범위가 973 K의 H2 분위기 내 Mg 금속을 이용한 환원 반응 후 생성된 수소화타이타늄(TiH2) 분말의 산소 농도에 미치는 영향을 조사하였으며, 입도 범위가 45 – 75 μm 인 TiO2 원료를 사용한 경우 산소 함량이 0.21 mass%인 TiH2이 제조되었다고 보고하였다24). 그러나, 환원 반응에 사용되는 원료의 입도 분급법에 따른 TiO2의 입도 범위가 환원 반응 후 생성된 Ti 내 고용 산소 농도에 미치는 영향에 대해서는 보고된 바 없다.
따라서 본 연구에서는 건식 체질로 분급한 TiO2 원료의 입도 범위가 환원 반응 후 생성된 TiH2 분말의 산소 농도에 미치는 영향을 조사하였다. 또한 습식 체질로 분급한 TiO2 원료의 환원결과와 비교함으로써 TiO2 원료의 입도 분급법이 환원 후 생성된 TiH2 분말의 산소 농도에 미치는 영향을 분석하였다. 또한, H2 분위기 내 Mg 금속을 이용한 열환원법에 대한 열역학적 분석을 통해 TiO2으로부터 저산소 Ti의 제조 메커니즘을 고찰하였다.
2. 마그네슘 열환원법을 이용한 TiO2으로부터 저산소 Ti 제조를 위한 열역학적 고찰
본 연구에서는 실험에 앞서 Mg 금속을 이용한 Ti 내 산소의 환원 반응식으로부터 반응 메커니즘을 분석하고, 이를 통해 Mg 금속을 이용한 열환원법의 단점인 Ti 내 고용 산소 농도 저감 한계를 극복하고자 하였다. 즉, 열역학적 분석을 바탕으로 TiO2의 Mg 금속을 이용한 열환원을 통해 저산소 Ti 금속의 직접 제조 가능성을 고찰하였다.
반응계 내 Mg 금속을 이용한 열환원 반응은 식 (1)에 따라 진행되며, Mg과 MgO 간의 평형 조건 하에서 MgO의 활동도(aMgO) 및 Mg의 활동도(aMg)를 각각 1로 가정할 시, 주어진 온도에서 반응계 내 평형 산소 분압(pO2)은 일정한 값으로 고정된다.
이때, 973 K에서 TiO2은 Mg에 의해 환원되어 Ti으로 존재하며, 해당 Ti에 고용된 산소는 식 (2)의 Sievert의 법칙을 따른다. 즉, 반응 온도(T)와 해당 온도에서의 표준 깁스 자유에너지 변화(∆G°r)가 주어지면, 열역학적 평형 조건 하에서 Ti 내 고용 산소의 활동도(a[O] in Ti)는 반응계의 pO2에 의해 고정된다. 이때, 식 (3)과 같이 a[O] in Ti는 산소의 활동도 계수(γO)와 Ti 금속 내 고용 산소의 몰분율(NO)의 곱으로 계산할 수 있다. 따라서 Ti 내 고용된 산소의 농도는 식 (3)으로부터 구할 수 있다23).
식 (1)과 식 (2)를 종합하면, Ti 내 고용 산소의 Mg 금속을 이용한 열환원 반응을 식 (4)와 같이 나타낼 수 있다. 이때, a[O] in Ti는 주어진 온도에서 Mg과 MgO 간의 평형에 의해 고정되는 pO2에 따라 결정되기 때문에, Mg 금속을 이용한 열환원 반응에 의해 제조된 Ti 내 고용 산소 농도는 식 (5)와 같이 나타낼 수 있다.
식 (5)로부터 Ti 내 산소 농도는 exp (∆G°r / RT), (aMgO / aMg), 및 (1 / γO)에 의해 결정되기 때문에 이를 제어함으로써 TiO2의 Mg 금속을 이용한 열환원법을 통해 Ti 내 산소 농도 저감 한계를 극복할 수 있는 방안을 도출할 수 있다21,22,24,25,26,27,28,29,30,31,32,33,34,35,36,37).
첫 번째로, exp (∆G°r / RT) 항으로부터 공정 온도를 낮추는 방법이 고려될 수 있다. 그러나 Mg 금속을 환원제로 사용하는 경우, 고체 TiO2과 Mg이 균일하게 혼합되어 환원 반응이 진행되기 위해서는 Mg 금속이 반응계 내 액상으로 존재해야 한다. 따라서 환원 반응은 Mg 금속의 융점 이상, 또는 용융염을 이용할 경우 용융염 조성에 따른 융점 이상에서 수행되어야 하므로, 공정 온도를 낮춤으로써 Ti 내 고용 산소 농도를 저감하는 방법은 제한적이다.
두 번째로 (aMgO / aMg) 항의 경우, Mg 금속을 이용한 열환원 반응 후 생성된 부산물인 MgO의 aMgO를 감소시킴으로써 Mg 금속의 환원력을 증가시키는 방법이다. aMgO를 감소시키기 위한 열역학적 접근은, 환원 반응으로 생성된 MgO를 제거 또는 변환하여 반응계 내 MgO의 몰분율을 낮추는 것이 핵심이며, 이를 위한 대표적인 방법은 다음 두 가지로 구분된다.
첫 번째 방법은, 용융염을 이용한 환원 반응 중 용융염에 용해된 MgO을 전기화학적으로 제거하여 MgO의 몰분율을 감소시키는 방법이다22,28,29). 두 번째 방법은, 용융염을 이용한 환원 반응 시 생성된 MgO을 화학반응을 통해 MgCl2으로 전환시켜 MgO의 몰분율을 감소시키는 방법이다. Mg 금속을 이용한 열환원법에서는 MgCl2이 용융염의 주요 성분으로 사용된다. 이때 희토류 염화물(RECl3)을 용융염에 첨가 시, 환원 반응 중 생성된 MgO은 식 (6)과 같은 반응에 의해 MgCl2으로 전환되며 부산물로 희토류 oxychloride(REOCl)가 생성된다. 이와 같은 반응을 활용하여 반응계 내 MgO 몰분율 감소를 통해 aMgO를 감소시킬 수 있다. 이와 같이 Mg / MgCl2 / REOCl / RECl3 (RE = Y, La, Ho, Ce 등) 간의 평형을 활용하여 aMgO를 낮추는 연구가 최근 활발히 진행되고 있다30,31,32,33).
마지막으로, 식 (5)의 세 번째 항인 (1 / γO)의 경우, Ti 내 고용 산소의 γO를 증가시켜 Ti 내 산소 농도를 감소시키는 방법이다. Utah 대학의 Fang 교수 연구팀은 H2 분위기에서 TiO2의 Mg 금속을 이용한 환원 및 환원산물의 탈산 반응 시 Ti 내에 수소(H)를 고용시켜 γO를 증가시킴으로써 저산소 TiH2이 제조됨을 보고하였다21,24,25,26,27).
그러나 1023 K의 H2 분위기에서 Mg 금속을 이용한 TiO2의 환원 반응만 고려 시 0.78 mass% 산소를 함유한 TiH2의 제조는 보고되었으나26), ASTM 규격에 부합하는 저산소 TiH2을 제조한 사례는 아직까지 보고되지 않았다. 이러한 한계는 Ti의 높은 산소 친화도에 의해 반응 중 산소 오염이 쉽게 일어나기 때문이다. 특히, 최종 Ti 산물의 산소 농도는 고용 산소 뿐만 아니라 표면에 형성되는 산화피막도 영향을 미치기 때문에 고용 산소 농도를 낮게 유지하고 산화피막 형성을 최소화하는 것이 저산소 Ti 제조의 핵심이다38,39).
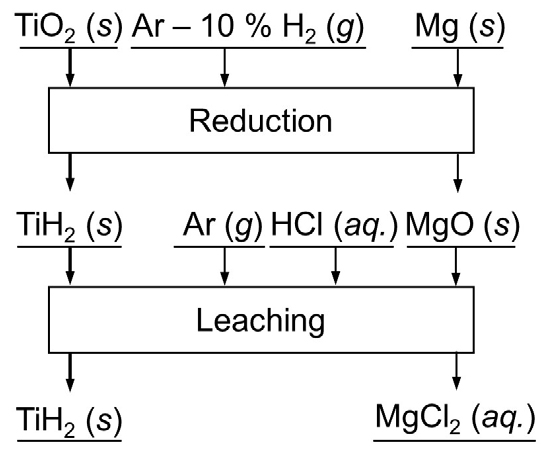
Fig. 2은 본 연구에서 수행된 전체 공정의 흐름도를 나타낸 것이다. 본 연구에서는, H2 분위기에서 Mg 금속을 이용한 TiO2의 환원 반응 시 수십 μm의 입도를 갖는 TiO2 원료를 사용하여 제조된 Ti의 단위 질량당 산화피막이 차지하는 부피분율을 감소시킴으로써 단일 환원 공정만으로 저산소 Ti 분말을 제조하고자 하였다. 특히, TiO2 원료의 입도는 입도 분급법에 영향을 받기 때문에 본 연구에서는 입도 분급법이 최종 Ti 산물의 산소 농도에 미치는 영향을 조사하였다.
3. 실험방법
3.1. TiO2 원료 분급 및 환원 반응을 위한 전처리
본 연구에 사용된 TiO2은 황산법을 이용한 상용 제련공정에서 소결 후 분쇄 전 단계에서 회수된 중간 원료이며, 코스모화학(주)으로부터 제공받았다.
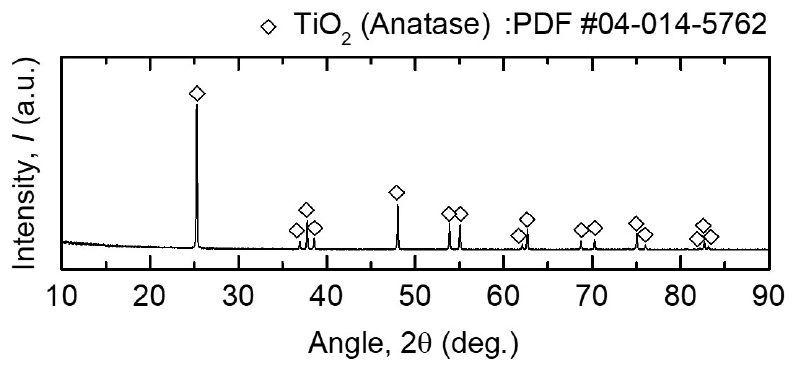
Fig. 3는 본 연구에서 사용된 TiO2 원료의 XRD 분석 결과를 나타내며, 아나타제(anatase) 상의 TiO2으로 확인되었다. 해당 원료를 진동식 체질기(Vibratory sieve shaker, J-PVS, JISICO)를 이용하여 45 – 75 μm, 75 – 106 μm, 106 – 150 μm, 및 150 – 300 μm의 입도 범위로 분급하였다. 분급된 시료는 453 K의 진공오븐(VOS-602SD, EYELA)에서 24 시간 이상 진공 건조 후 환원 실험에 사용하였다.
환원 전 반응물 내 잔류 수분을 완전히 제거하기 위해 TiO2 원료와 염(salt)의 균일 혼합물을 예비 용융(pre-melting) 하였다. 사용된 염은 무수 MgCl2 (순도: > 97.0 %, Wako Pure Chemical Corporation)과 무수 염화칼륨(KCl, 순도: > 99.0 %, KOJUNDO Chemical Laboratory Co., Ltd.)이며, 사용 전 시약 내 잔류 수분을 최소화하기 위해 453 K의 진공 오븐에서 72 시간 동안 건조하였다. 건조한 MgCl2 및 KCl은 질량비 3 : 1로 혼합하여 사용하였다. 분급된 TiO2 원료와 MgCl2–KCl 혼합염은 글러브박스(MB-Unilab Max, MBraun Inc.) 내에서 막자사발을 이용해 혼합하였다. 혼합된 시료는 철(Fe) 도가니(외경(ϕ) = 29 mm, 두께(t) = 1 mm, 높이(h) = 70 mm)에 장입하였다.
동일한 질량의 MgCl2 – KCl 혼합염 및 서로 다른 입도 범위를 가지는 동일한 질량의 TiO2 원료 혼합물이 장입된 두 개의 Fe 도가니를 글러브박스에서 꺼내어 Fe 재킷(ϕ = 89 mm, t = 2 mm, h = 200 mm)에 위치시켰다. 이후 Fe 재킷을 스테인리스 스틸 반응기 내부에 장입하고, 상부 플랜지를 조립하였다. 플랜지 조립 후, 반응기 내부를 아르곤(Ar) 가스(순도: > 99.999 %)로 치환하였으며, 질량 유량 제어기(MFC, MODEL 3660, KOFLOC Corporation)를 사용하여 반응 중 반응기 내부 압력이 1 atm이 되도록 Ar 가스를 지속적으로 유입하였다. 그 후, 반응기를 전기로에 삽입하여 1053 K에서 1 시간 동안 예비 용융을 실시하였다.
3.2. Mg 금속을 이용한 열환원
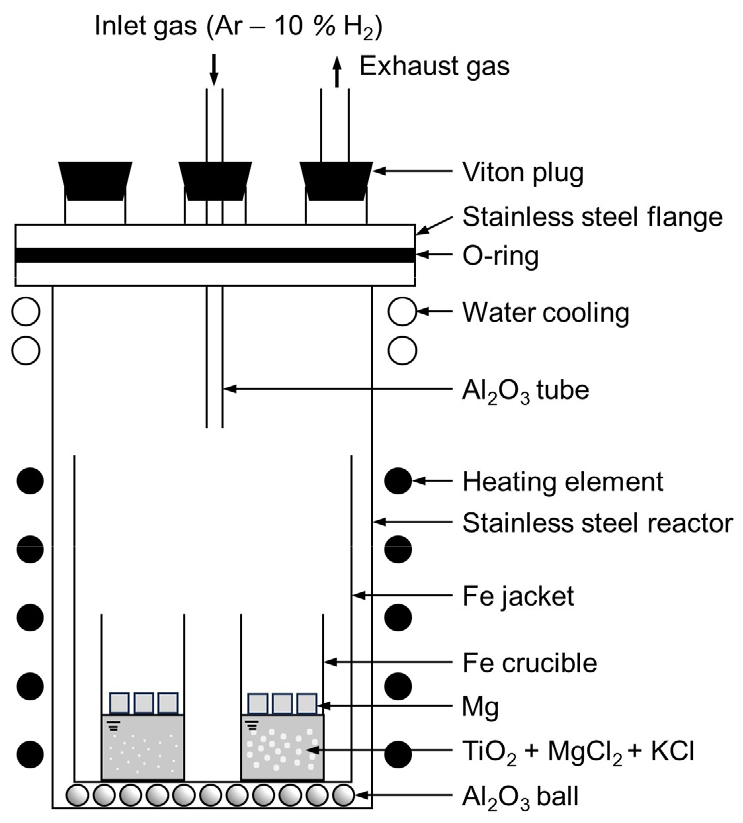
예비 용융이 완료된 후, 반응기 온도가 상온에 도달 시 플랜지를 열고 사전에 칭량한 Mg 금속 큐브(가로 × 세로 × 높이 = 10 mm × 10 mm × 10 mm, 순도: 99.99 %, RNDKOREA Corporation)를 Fig. 4와 같이 Fe 도가니 내부에 장입하였다. 이후 플랜지를 조립한 후 반응기 내부를 Ar – 10 % H2 가스로 치환하였으며, MFC를 사용하여 반응 중 반응기 내부 압력이 1 atm이 되도록 Ar – 10 % H2 가스를 지속적으로 유입하였다. 이후 반응기를 전기로에 장입하고, 973 K까지 승온 후 해당 온도에서 24 시간 동안 환원 반응을 진행하였다. 환원 반응 종료 후, 반응기를 상온까지 냉각하였다.
3.3. 환원 반응 산물의 HCl 침출
환원 반응 후 회수한 산물에 포함된 잔류 Mg, MgCl2, KCl 및 반응 생성물인 MgO을 제거하기 위해 염산(HCl) 침출을 수행하였다. 침출은 이중 자켓 반응기를 이용하였으며, 반응기에 10 % HCl 용액 500 mL (순도: 35.0 – 37.0 %, JUNSEI Chemical Co., Ltd.)를 장입하였다. 침출 온도는 항온수조기(CW3-10, JEIO TECH Co., Ltd.)를 이용해 293 K로 유지하였다. 또한 HCl 용액은 magnetic bar를 이용하여 400 rpm으로 교반하였으며, 산물 투입 전 Ar 가스를 1 L/min으로 30 분 동안 주입하여 HCl 용액을 버블링하였다. 이후, 환원 반응 산물을 반응기 상부 플랜지 neck을 통해 투입하였으며 Ar 가스를 주입하면서 30 분 동안 침출하였다.
1차 HCl 침출 후, 반응기 내 내용물을 여과지(pore size: 0.45 μm)를 이용해 감압 여과하였고, 여과 후 회수한 분말을 증류수로 세척 후 아세톤으로 세척하였다. 2차 HCl 침출을 위해 293 K에서 동일한 반응기에 10 % HCl 용액 500 mL를 투입하고 300 rpm으로 교반하면서 Ar 가스를 1 L/min으로 주입하여 10 분 동안 버블링하였다. 이후 회수된 분말을 투입하였으며 Ar 가스를 주입하면서 30 분 동안 침출하였다. 침출 후 반응기 내 내용물을 감압 여과하여 분말을 회수하였으며 이를 증류수 및 아세톤으로 세척하였다. 최종적으로 얻은 분말은 상온의 공기 중에서 30 분 동안 건조한 후, 진공 데시케이터(dessicator)에서 30 분 동안 건조하였다. 이후 다시 상온 공기 중에서 30 분 동안 건조하여 최종 산물을 확보하였다.
3.4. 분석 방법
HCl 침출 후 회수한 산물의 산소 농도는 N/O/H 분석기(TCH600, LECO Co.)를 사용하여 분석하였다. 최종 산물의 결정상은 X선 회절 분석기(XRD: MiniFlex 600, Rigaku)를 이용하여 분석하였다. TiO2 원료의 입도 및 미세구조는 주사전자현미경(FE-SEM: JSM 7800F Prime, JEOL Ltd.)을 이용하여 분석하였다.
4. 결과 및 고찰
4.1. 건식 체질한 TiO2 입도가 환원 후 Ti 산물의 산소 농도에 미치는 영향
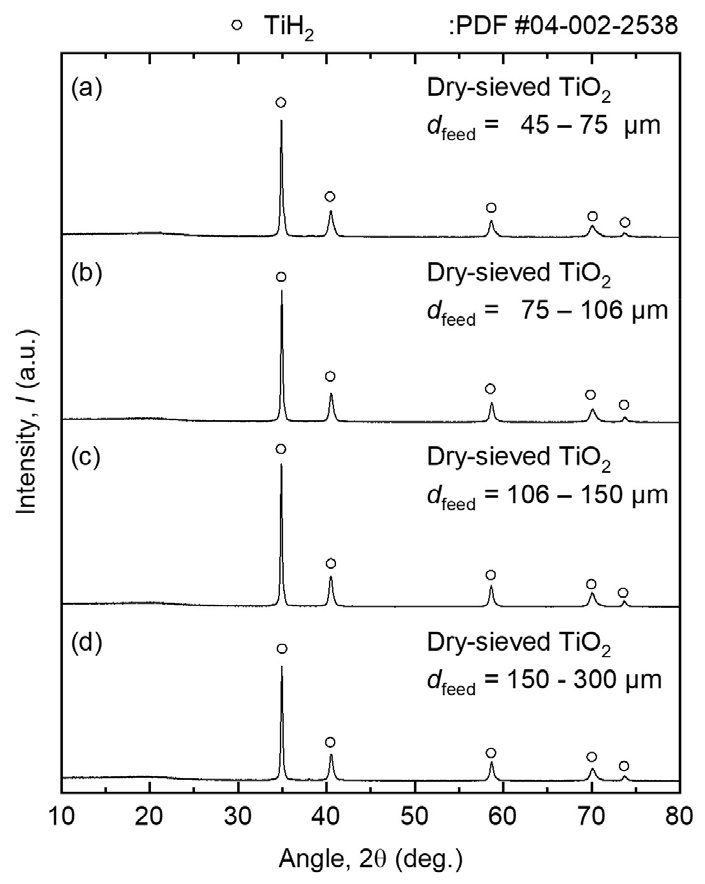
Fig. 5는 건식 체질로 분급된 TiO2 원료의 입도에 따른 환원 반응 후 최종 Ti 산물의 XRD 분석 결과를 나타낸다. 973 K의 Ar – 10 % H2 가스 분위기에서 24 시간 동안 Mg 금속을 이용한 열환원 반응 결과, 모든 입도 범위에서 최종 Ti 산물이 TiH2 상으로 확인되었다. 이는 Ar – 10 % H2 가스 분위기에서 Ti 내 수소의 고용이 TiO2 원료의 입도와 관계없이 충분히 이루어졌음을 나타낸다. 즉, 973 K의 10 % H2 혼합 가스 분위기에서 Mg 금속을 이용한 열환원 반응이 높은 pH2 조건에서 진행되었음을 의미한다.
Table 1은 건식 체질로 분급된 TiO2 원료의 입도에 따른 환원 반응 후 최종 Ti 산물의 산소 농도 분석 결과를 나타낸다. Table 1에서 볼 수 있는 것과 같이 TiO2 입도가 45 – 75 μm, 75 – 106 μm, 106 – 150 μm, 및 150 – 300 μm일 때 TiH2 내 산소 농도는 각각 0.415 mass%, 0.441 mass%, 0.463 mass%, 및 0.480 mass%를 나타내었다. 따라서 TiO2 원료의 입도가 증가할수록 TiH2 내 산소 농도가 점차 증가하는 경향을 보이는 것을 확인할 수 있다. 본 연구에서 제조된 TiH2의 산소 농도는 0.415 – 0.480 mass%로, ASTM Gr. 1 또는 Gr. 2의 산소 농도 기준보다 다소 높다. 그러나 Park et al.(2025)의 연구에 따르면37), 973 K의 Ar 가스 분위기에서 Mg 금속을 이용한 TiO2을 열환원한 경우 생성된 최종 Ti 산물의 산소 농도는 3.78 – 3.90 mass%으로 보고된 바 있다. 이는 본 연구에서 수행한 높은 pH2에서의 열환원 반응을 통해 최종 Ti 산물의 산소 농도를 0.415 – 0.480 mass%까지 효과적으로 저감할 수 있었음을 시사한다.
Table 1
Experimental conditions and results of magnesiothermic reduction of TiO224)
|
Particle size of feed, dfeed / μm | Using dry-sieved TiO2 feed in this study | Using wet-sieved TiO2 feed24) | ||||
| Final productb |
Mean particle size, dproduct / μmc |
Concentration of O, CO (mass%)d | Final productb |
Mean particle size, dproduct / μmc |
Concentration of O, CO (mass%)d | |
| 45 – 75 | TiH2 (s) | 25.41 | 0.415 ± 0.032 | TiH2 (s) | 26.97 | 0.212 ± 0.028 |
| 75 – 106 | TiH2 (s) | 23.13 | 0.441 ± 0.028 | TiH2 (s) | 34.37 | 0.248 ± 0.018 |
| 106 – 150 | TiH2 (s) | 23.47 | 0.463 ± 0.031 | TiH2 (s) | 25.75 | 0.244 ± 0.059 |
| 150 – 300 | TiH2 (s) | 24.69 | 0.480 ± 0.021 | TiH2 (s) | 26.75 | 0.282 ± 0.032 |
4.2. H2 분위기에서 Mg 금속을 이용한 열환원법에 의한 TiO2로부터 저산소 Ti 금속 제조 메커니즘
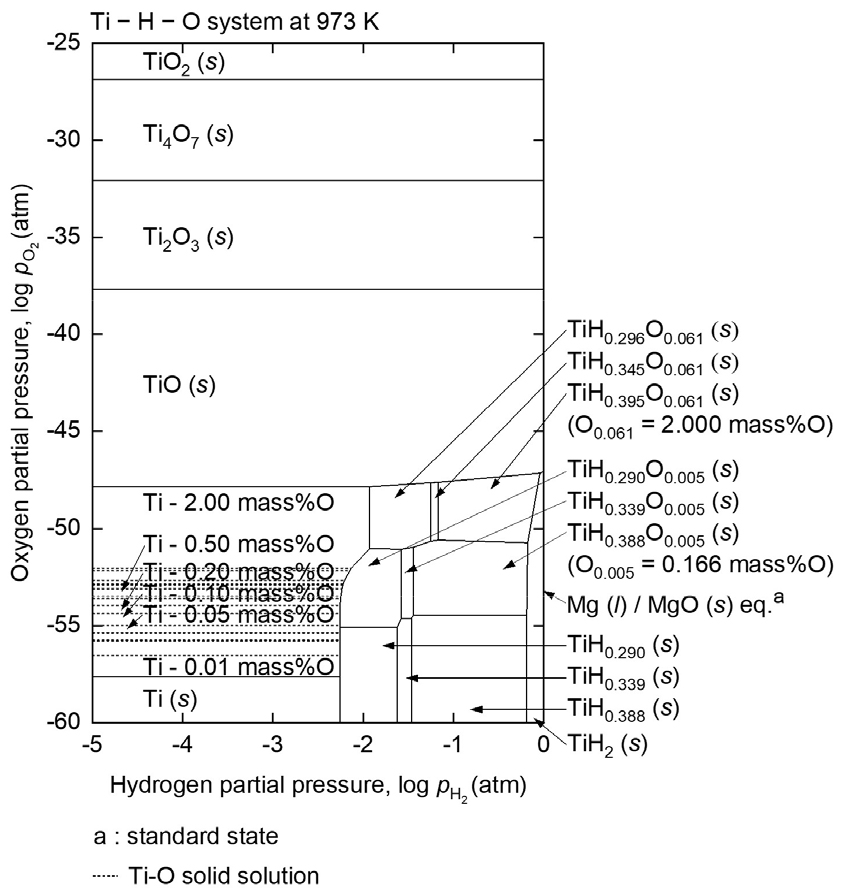
973 K의 10 % H2 혼합 가스 분위기에서 Mg 금속을 이용한 TiO2의 열환원 반응을 통해, 약 0.4 mass% 산소가 함유된 TiH2이 제조되었다. Ti 내 수소 고용에 의한 저산소 Ti 생성 메커니즘은 Ti – H – 산소(O) 삼원계 내 고용체(solid solution)간 평형 및 그에 따른 안정상(phase)을 기반으로 설명할 수 있다. Fig. 6은 973 K에서의 Ti – H – O 계의 화학포텐셜 다이어그램(chemical potential diagram)을 나타낸다24,25,40,41). 다이어그램의 x축은 반응계 내 pH2, y축은 반응계 내 pO2을 나타내고 있기 때문에, Fig. 6은 973 K에서 pH2 및 pO2에 따른 Ti – H – O 간의 가장 안정된 고용체와 각 상 간 평형을 모식화 한 것으로 이해할 수 있다.
먼저, 반응계에서 H2의 사용 없이 Mg을 이용한 열환원을 수행하는 경우, 식 (1)에 따라 반응계 내 평형 pO2은 Mg (l) / MgO (s) 평형에 의해 5.75 × 10–54 atm으로 고정된다. 이 값은 Ti 내 고용 산소 농도 0.5 mass%의 Ti – O 고용체 상의 안정 영역(3.21 × 10–54 atm < pO2 < 7.33 × 10–54 atm)에 해당한다. 이는 pH2이 적극적으로 제어되지 않는 조건에서 Mg을 이용한 TiO2의 열환원 반응 시 Ti 내 고용 산소 농도가 0.5 mass%까지 낮아질 수 있음을 의미한다. 그러나 이 산소 농도는 ASTM 규격과 비교하면 다소 높은 값에 해당한다.
반면, H2를 분위기 가스로 사용함으로써, 반응계 내 pH2이 높게 유지되는 경우, Ti – H – O 고용체 상의 형성을 고려해야 한다. 이 조건에서도 973 K에서 반응계 내 pO2은 Mg (l) / MgO (s) 평형에 의해 동일하게 5.75 × 10–54 atm으로 유지된다. Fig. 6에서 볼 수 있듯이, 이와 같이 고정된 pO2 조건 하에서, Ti – O 고용체 상으로부터 Ti – H – O 고용체 상으로의 상전이가 발생하는 pH2은 5.75 × 10–3 atm으로 계산된다. 반응계 내 pH2이 5.75 × 10–3 atm 이상으로 유지되는 경우, 해당 조건에서는 pH2 및 pO2 모두 0.166 mass%의 산소를 함유한 TiHxO0.005(x = 0.290, 0.339, and 0.388) 상의 안정 영역 내에 위치하게 된다. 따라서, pH2이 5.75 × 10–3 atm 이상으로 유지되는 H2 분위기에서 Mg 금속을 이용한 열환원을 수행하는 경우, 0.166 mass% 산소를 함유한 Ti 제조가 가능함을 알 수 있다.
이는 식 (5)에서 제시된 바와 같이, 동일한 a[O] in Ti 조건에도 불구하고 H2를 분위기 가스로 사용함으로써 Ti 내 γO를 증가시켜 Ti 내 고용 산소 농도를 더욱 낮출 수 있음을 시사한다.
이러한 열역학적 메커니즘에 기반하여, H2 분위기에서 Mg 금속 열환원을 통해 TiO2으로부터 저산소 Ti을 제조하기 위해서는 Ti 내 수소의 고용이 중요하며, 이를 위해 반응계 내 pH2을 충분히 높은 수준으로 유지하는 것이 필수적이다. 본 연구의 경우, 973 K에서 반응계 내 pH2이 5.75 × 10–3 atm 이상으로 유지되도록 Ar – 10 % H2 가스를 분위기 가스로 사용한 결과 Fig. 5에서 나타난 바와 같이 본 실험의 조건 하에서는 TiO2 원료의 입도와 무관하게 최종 산물에서 TiH2 상이 생성되었다.
4.3. TiH2 산물의 산소 농도 저감의 한계 원인 분석
본 실험을 통해 제조된 TiH2 분말의 산소 농도는 0.415 – 0.480 mass%로, Fig. 6에서 논의된 산소 농도인 0.166 mass%와는 다소 큰 차이를 보였다. 이러한 차이는 산소 농도 저감의 한계를 뜻하며, 이는 Ti의 산소 농도를 결정하는 두 가지 요인인 고용 산소와 비표면적에 기인한 산화피막의 부피분율로 나누어 고찰할 수 있다.
먼저, 고용 산소의 관점에서 살펴보면, 본 실험에서는 반응계 내 pH2이 충분히 높게 유지되어 TiH2이 회수되었으나 사용된 TiO2 원료 입도가 수십 μm 수준으로 비교적 크기 때문에, 입자 내 환원이 충분히 진행되지 않았을 가능성이 있다. 즉, Mg (l) / MgO (s) 평형에 따른 환원 반응에 의해 Ti 내 산소가 제거되었으나, 해당 평형에 도달하기에는 본 실험의 반응시간이 충분하지 않았을 가능성이 있다.
Song et al.(2025)의 연구 결과에 따르면24), 973 K의 10 % H2 혼합 가스 분위기에서 Mg 금속을 이용한 TiO2의 열환원 반응을 여러 TiO2의 입도 범위 및 반응시간에서 수행한 결과, TiO2 원료 입도 범위 45 – 75 μm 및 150 – 300 μm의 열환원 반응시간을 12 시간에서 24 시간으로 증가시킬 경우 환원 후 최종 TiH2 산물의 산소 농도는 각각 0.238 mass% 및 0.492 mass%에서 0.212 mass% 및 0.282 mass%로 감소하였다. 이는 환원 시간이 부족할 경우, 입도 차이에 따른 산소 농도 격차가 더욱 현저히 나타날 수 있음을 나타내고 있다.
그러나 본 연구의 Table 1에서 볼 수 있는 것과 같이 건식 체질 후 회수된 TiO2 원료 입도 범위 45 – 75 μm 및 150 – 300 μm의 경우, 최종 TiH2 산물의 산소 농도는 각각 0.415 mass% 및 0.480 mass%로 두 산소 농도 간 차이는 650 ppm으로 상당히 작은 차이를 보였다.
따라서, 본 연구의 실험 조건에서는 TiO2 입도에 따른 환원 반응 정도에 일부 차이가 존재하지만, 전반적으로 고용된 수소 및 산소의 농도가 포화 상태에 근접한 것으로 사료되며, 이에 따라 반응시간 증가에 의한 더욱 낮은 산소 농도를 함유한 TiH2의 제조는 제한적일 것으로 사료된다.
이러한 점을 고려할 때, 본 연구의 실험 조건에서 산소 농도 저감의 한계는 Ti 내 고용 산소 외에도 다른 요인에 기인할 수 있으며, 앞서 제시한 바와 같이 환원 후 회수된 TiH2 산물의 표면에 형성된 산화피막의 부피분율이 이에 영향을 미쳤을 가능성이 있다. Fig. 7(a) – (d)는 본 연구에서 건식 체질을 통해 분급된 TiO2 원료의 입도 별 SEM 이미지를 나타내며, 모든 입도 범위에서 체눈 크기보다 작은 미세 입자의 혼입이 뚜렷하게 관찰되었다.
미세 입자 생성은 사용한 TiO2 원료 내 함유된 미세 입자 뿐만 아니라, 진동식 체질기를 이용한 건식 체질 시 발생하는 미세 입자도 고려할 수 있다. Fig. 7(i)와 같이 본 실험에서 사용된 TiO2은 나노 크기의 1차 입자들이 응집된 μm 크기의 2차 입자로서, 다공성 미세조직을 갖는 것으로 관찰된다. 이러한 구조적 특성으로 인해, 체질 과정에서의 기계적 진동이나 충격에 의해 입자가 부분적으로 분해되었을 가능성이 있다. 이와 같이 생성된 미세 입자는 이상적으로는 체눈 크기에 따라 분급되어야 하나 체눈 막힘 등 다양한 요인에 의해 분급효율이 감소되어 혼입된 것으로 예상된다. 이러한 혼입된 미세 입자는 단위 질량당 비표면적을 증가시켜 표면 산화피막의 부피분율을 증가시키는 원인이 되었을 것으로 사료된다. 따라서, 더 낮은 산소 농도의 Ti을 제조하기 위해서는 정밀한 원료 분급 기술의 적용이 필수적임을 알 수 있다.

Fig. 7.
SEM images of dry-sieved TiO2 feed particles in the ranges of (a) 45 – 75 μm, (b) 75 – 106 μm, (c) 106 – 150 μm, and (d) 150 – 300 μm and wet-sieved TiO2 feed particles in the ranges of (e, i) 45 – 75 μm, (f) 75 – 106 μm, (g) 106 – 150 μm, and (h) 150 – 300 μm at following resolutions: (a – h) at low resolution (×100); (i) at high resolution (×5000).
4.4. TiO2 원료의 분급 방식이 Ti 산물의 산소 농도에 미치는 영향
TiO2 원료 분급 방식이 Mg 금속을 이용한 열환원 반응 후 최종 TiH2 산물의 산소 농도에 미치는 영향을 정량적으로 평가하기 위해, 본 연구에서 수행한 건식 체질에 의해 분급된 TiO2을 사용한 환원 결과와, 동일한 환원 조건 하에서 습식 체질에 의해 분급된 TiO2을 사용한 Song et al.(2025)의 연구 결과를 비교 분석하였다. Table 1에 각각의 TiO2 원료를 이용한 환원 반응 후 얻어진 TiH2의 산소 농도 분석 결과를 나타내었다24).
습식 체질은 주로 약 50 μm 이하로 미세 입자인 경우 등에 효과적인 분급 방식으로, 액체의 유동을 따라 입자가 체를 통과하도록 유도함으로써 정밀한 분급이 가능해진다42,43,44). Song et al.(2025)의 연구에서는 진동식 체질기를 사용하지 않고, 중력에 의한 증류수의 유동만을 이용하여 습식 체질을 수행하였으며, 본 연구와 동일하게 45 – 75 μm, 75 – 106 μm, 106 – 150 μm, 및 150 – 300 μm의 입도 구간으로 분급하였다24). Fig. 7(e) – (h)는 습식 체질을 통해 분급된 TiO2 원료의 SEM 이미지를 나타낸 것으로, Fig. 7(a) – (d)의 본 연구에서 사용된 건식 체질을 통해 분급된 TiO2 원료와 비교하여 미세 입자 혼입이 현저히 적은 것을 확인할 수 있다.
습식 체질한 TiO2 원료를 973 K의 Ar – 10 % H2 가스 분위기에서 Mg 금속을 이용한 열환원 반응을 24 시간 수행한 결과, Table 1과 같이, TiO2의 입도 구간인 45 – 75 μm, 75 – 106 μm, 106 – 150 μm, 및 150 – 300 μm에서 각각 0.212 mass%, 0.248 mass%, 0.244 mass%, 및 0.282 mass%의 산소를 함유한 TiH2 분말이 제조되었다. 이는 본 연구의 건식 체질한 TiO2 원료의 Mg 금속을 이용한 열환원 반응 후 최종 TiH2 산물의 산소 농도 분석 결과와 비교 시 모든 입도 구간에서 약 0.2 mass%의 낮은 산소 농도를 나타냈다. 이는 Fig. 7에서 관찰된 바와 같이, 습식 체질 방식이 보다 정밀한 입도 분리를 가능하게 함으로써 미세 입자의 혼입이 감소하여 비표면적 증가가 억제되고, 이에 따라 산물의 표면 산화피막의 부피분율이 감소했기 때문인 것으로 사료된다.
특히 주목할 점은, 습식 체질을 통해 45 – 106 μm 범위로 정밀하게 분급된 TiO2 원료를 사용할 경우, 973 K의 10 % H2 혼합 가스 분위기 하에서 Mg 금속을 이용한 환원 반응을 24 시간 동안 수행하면 별도의 탈산 반응 없이도 ASTM Gr. 2의 산소 농도 기준(≤ 0.25 mass%)을 만족하는 저산소 TiH2 제조가 가능했다는 점이다. 저산소 TiH2은 분말야금 공정에서 원료로 직접 사용 가능하다37). 또한 탈수소화 공정을 통해 Ti 금속분말로 제조할 수 있으며, 이때 공정 조건에 따라 산소 농도에 추가적인 영향을 미칠 수 있다45). 본 결과는 황산법에 의해서 제조되는 다공질 TiO2의 분급 방식이 H2 혼합 가스 분위기에서 Mg 금속을 이용한 단일 단계 환원 반응에 의해 제조되는 TiH2의 산소 농도에 큰 영향을 미치는 주요 요인임을 시사한다.
5. 결 론
본 연구에서는 TiO2 원료의 분급법 및 입도가 Mg 금속을 이용한 열환원 반응 후 제조된 Ti 산물의 산소 농도에 미치는 영향을 조사하였다. 열역학적 분석 결과, 973 K에서 Mg 금속을 이용한 TiO2의 열환원 반응에 의한 저산소 Ti 제조를 위해서는 높은 pH2을 유지하는 것이 중요함을 밝혔다. 건식 체질로 분급한 TiO2의 Mg 금속을 이용한 열환원 반응을 973 K의 Ar – 10 % H2 가스 분위기에서 24 시간 동안 수행하였다. 그 결과, 모든 입도 구간에서 TiH2이 제조되었으며 TiO2 원료의 입도 범위가 45 – 75 μm에서 150 – 300 μm으로 증가 시 TiH2의 산소 농도는 0.415 mass%에서 0.480 mass%로 증가하였다. 또한, 습식 체질로 분급된 TiO2 원료를 사용한 환원 결과와의 비교분석을 통해 저산소 TiH2 제조를 위해서는 TiO2 원료의 정밀한 입도 분급이 중요함을 밝혔다.