1. 서 론
지속적으로 발전하는 에너지 저장장치 기술과 증가하는 수요로 인해 에너지 저장장치 관련 시장은 계속해서 확대되고 있다. 특히 가전제품의 동력원 및 전기 자동차(EVs)를 포함한 운송 분야 등의 소비가 크게 증가하고 있으며, 이에 사용되는 에너지 저장장치인 리튬 이차전지(LIB; Lithium Ion Battery)의 중요성이 부각되고 있다. 리튬 이차전지는 높은 에너지와 전력 밀도, 긴 수명 및 환경 친화성 등의 특성으로 인해 중요한 에너지 저장장치로 각광받고 있지만 이에 결과적으로 발생하는 이차전지 폐기물에 함유되어 있는 유해금속 및 희소금속들 또한 증가하게 됨에 따라 처리 등의 문제가 발생한다1,2,3).
에너지 저장장치 자체의 특수 폐기물을 처리할 수 있는 처리장의 공간은 제한적이며 처리 비용도 매우 높은 편에 속하며 수거, 제거 또는 재활용에 관하여 배출되는 폐기물에 비해 상대적으로 구체적이고 체계적이지 않아 처리가 어렵다. 따라서 리튬 이차전지를 구성하고 있는 주요 요소인 희소금속 등을 재활용하여 재사용하는 것은 환경 오염 및 원자재 소비를 방지할 수 있다4,5). 특히 리튬 이차전지 중에서도 고성능 리튬 이차전지의 수요가 계속해서 증가하고 있으며 리튬 전구체로 사용되는 주 원재료인 수산화리튬의 경우에는 요구되는 수요에 비해 한정적인 자원에 속해 있으므로 폐기물로부터의 수산화리튬 재활용 기술이 필요하다. 또한, 수산화리튬을 수입에 의존하고 있는 국내의 경우에는 리튬 이차전지를 포함한 폐자원에서의 리튬 회수가 자원의 안정적 확보 차원에서 중요하므로 수산화리튬 제조 기술 및 이를 통한 리튬의 재자원화가 필요하다6,7,8,9,10).
리튬 이차전지 폐기물에서 선택적으로 리튬을 회수하기 위해 전처리 공정 후에 침출되지 않은 잔사 및 Ni, Mn, Co 등이 포함된 불순물을 제거하고 선택적으로 리튬 회수 및 확보하기 위해 습식 공정, 제련 공정, 건식제련 공정 등의 재활용 공정을 통해 수산화리튬을 제조하고 있다11,12,13,14). 최근에는 리튬 이차전지 폐기물로부터 수산화리튬을 제조함에 있어서 원료 수급이 원활하며 공정이 단순하고 불순물을 최대한 제거하기 위해 습식 공정을 통한 리튬 회수 관련 연구 위주로 진행되고 있다15,16). 특히 습식 공정을 통해 재활용되어 얻어진 수산화리튬이 리튬 이차전지로의 재사용하기 위해서는 Na, Ca, Cl 등 불순물 농도가 매우 낮은 수준으로 요구되므로 알칼리성 수산화물을 사용하여 수산화리튬을 제조한다. 알칼리성 수산화물을 통해 수산화리튬으로의 변환 효율을 최대로 높임과 동시에 불순물(K+, Na+ Ca2+, Mg2+, Cl-, SO42+ 등)은 용해 과정에서 제거되면서 불순물의 잔사와 리튬염 수용액 형태로 존재하는 수산화리튬으로 분리할 수 있다17). 따라서 이와 같이 리튬 이차전지에서 선택적으로 리튬을 회수하는 전처리 공정을 통해 회수한 후, 습식 공정을 이용하여 고순도 수산화리튬을 제조하려는 연구가 활발하게 진행되고 있다. 수산화리튬 분말 제조를 위한 습식 공정인 DRR(Double Replacement Reaction) 공정은 반응에 수반되는 에너지의 활용이 가능하여 합성에 필요한 에너지가 적으며 빠른 반응속도와 균일한 반응 제어를 수행할 수 있다. 위와 같은 공정을 이용하여 비교적 낮은 온도에서의 침전되는 불순물 제거를 쉽게 수행할 수 있으며, 침전 공정에 필요한 알칼리성 수산화물을 이용하여 수산화리튬 수용액 제조 및 최종적인 분말을 수득할 수 있다.
본 연구에서는 폐리튬이차전지로부터 황산리튬 형태로 회수된 리튬염 용액을 원료로 사용하였으며, 알칼리성 침전제 종류에 따라 선택적으로 황산이온을 침전을 시키는 공정을 사용하여 제조된 수산화리튬의 제조 거동을 평가하는 연구를 수행하였다. 수산화리튬의 제조 거동 평가를 위한 합성공정의 조건 변수로 침전제 종류, 침전제 농도 제어를 두어 본 연구를 진행하였다. 또한 2차 침전법의 합성온도에 따른 침전제 종류별 수산화리튬의 제조거동을 비교하기 위해 합성온도를 조건 변수로 두어 연구를 진행하였다. 고순도 수산화리튬 제조를 위해 2차 침전법인 DRR 공정을 이용하였으며, 최종적으로 제조된 분말의 결정성 확인을 통해 설정 조건에 따른 수산화리튬의 제조 거동을 평가하고자 하였다18).
2. 실험 방법
2.1. 실험 원료
수산화리튬 분말을 DRR 공정으로 제조하기 위한 출발 물질로는 리튬 이온이 함유되어 있는 폐리튬이차전지로부터 회수되어 얻어진 황산리튬(Li2SO4·H2O)을 본 연구의 원료로 사용하여 진행하였다.
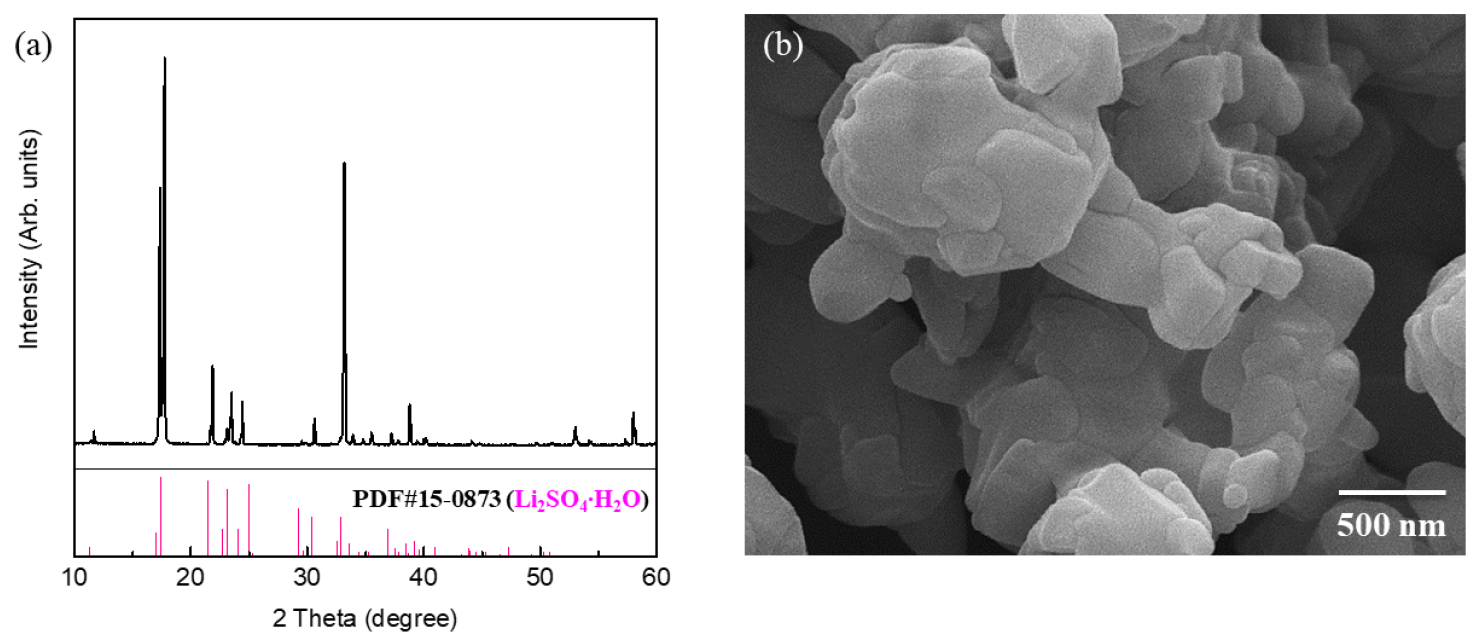
이차전지 폐기물로부터 리튬 회수 후 얻은 황산리튬 분말의 결정상과 크기 및 미세구조 확인을 위해 Fig. 1의 (a) X-선 회절(XRD; X-ray diffraction spectroscopy, XRD-6100, Shimadzu)과 (b)주사전자현미경(SEM; Scanning Electron Microscope, Mira3, TESCAN)을 통해 회절 패턴과 표면을 확인하였다. DRR 공정에 사용된 리튬 원료 분말은 마이크로 이하 크기의 입자로 구성된 단일상의 황산리튬(Li2SO4∙H2O, JCPDS no.15-0873)임을 확인하였다. 또한, 회수된 황산리튬 원소 함량을 확인하기 위해 유도결합플라즈마분광기(ICP-OES; Inductively Coupled Plasma Optical Emission Spectroscopy, Perkin Elmer 5300DV)를 통해 성분 분석을 진행하였으며, Table 1과 같이 분석 결과를 통해 99.92%의 황산리튬임을 확인하였다.
Table 1.
Summary of ICP analysis of as-synthesized Li2SO4 powder
| Element | Concentration of Li2SO4 (%) |
| Li+ | 10.63 |
| Na | 0.01 |
| P | 0.063 |
| Al | 0.001 |
| Mg | - |
| Cu | - |
| Fe | - |
| As | - |
| Ca | - |
| Co | - |
| Ni | - |
| Mn | - |
| Pb | - |
| Zn | - |
| Cd | - |
| Cr | - |
| Purity | 99.92 |
2.2. 알칼리성 침전제 종류에 따른 수산화리튬 제조
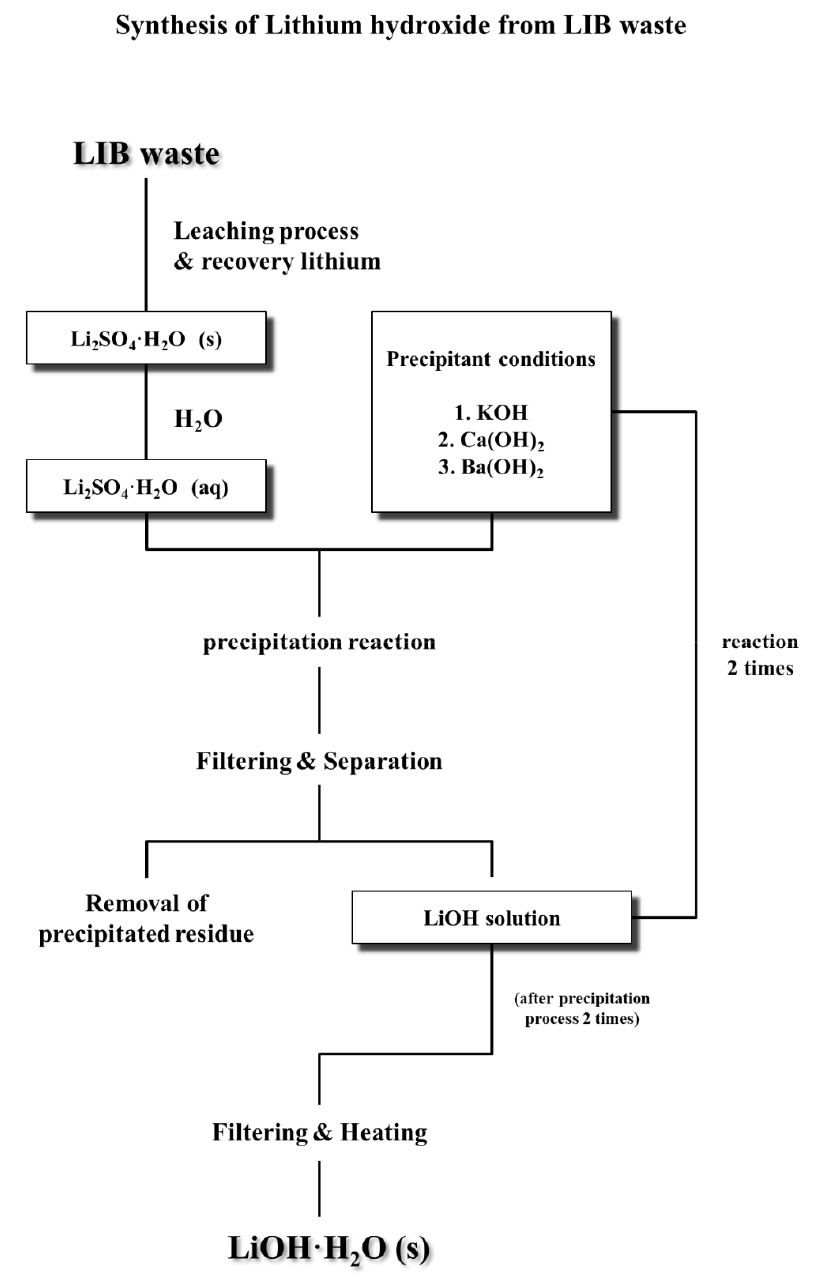
원료로 사용되는 황산리튬으로부터 DRR 공정을 통해 알칼리성 침전제 종류에 따라 합성되는 수산화리튬의 제조 거동을 확인하는 연구로, 개략적인 공정도를 Fig. 2에 나타내었다. 회수된 리튬염인 황산리튬 원료로부터 알칼리성 침전제 종류에 따른 수산화리튬 제조 거동을 확인하기 위해서 수산화칼륨(KOH, 95%, SAMCHUN), 수산화칼슘(Ca(OH)2, 95%, Sigma Aldrich), 수산화바륨(Ba(OH)2, 95%, Sigma Aldrich)의 총 3가지의 알칼리성 침전제 종류를 이용하였고, 2차 침전법인 DRR공정으로 실험을 실시하였다.
알칼리성 침전제 종류에 따른 수산화리튬 제조 거동을 확인하기 위하여 이전에 수행하였던 황산리튬을 이용한 수산화리튬 합성 최적 조건(DRR 공정, 합성온도 40 ℃, 합성시간 2 hr, [Li]/[OH]=1:1)을 포함한 합성 조건을 두고서 실험을 수행하였다19). 수산화리튬 분말의 제조 거동 평가를 위해 각 조건에서의 합성시간은 2 hr로 고정하였으며 알칼리 종류(KOH, Ca(OH)2, Ba(OH)2), 합성온도(40 ℃, 80 ℃), 리튬 전구체와 침전제와의 몰비([Li]/[OH]=1:0.5~4)의 조건을 두어 실험을 수행하였다. 우선 황산리튬 분말 0.02 mol을 200 ml의 초순수에 투입하여 300 rpm에서 충분히 용해될 때까지 녹여 액상의 리튬 전구체를 준비하였으며 균일한 온도 조절을 위하여 액상의 리튬 전구체 가열 속도는 5 ℃/분으로 반응 용액을 단계별로 승온시켰다. 정해진 합성온도 조건에 도달하면 알칼리성 침전제 종류에 따라 투입하여 침전반응을 실시하였다. 침전반응 종료 후 잔사-용액의 분리를 위해 필터페이퍼를 이용한 1차 고/액 분리와 불순물 최소화를 위해 분리된 용액을 200 nm 크기 기공을 가진 마이크로필터가 장착된 실린지를 이용하여 최종적으로 불순물을 제거하였다. 이후 잔사가 제거된 용액을 증발시켜 수분을 제거하여 합성된 분말을 수득하였다. 1차 침전공정에서 수득한 합성분말의 순도를 높이기 위해 같은 조건으로 DRR 공정을 실시하였으며, 앞서 실시했던 불순물 제거 및 수분 제거 공정까지 실시하여 최종적으로 결정화된 수산화리튬 분말을 회수하였다.
3. 결과 및 고찰
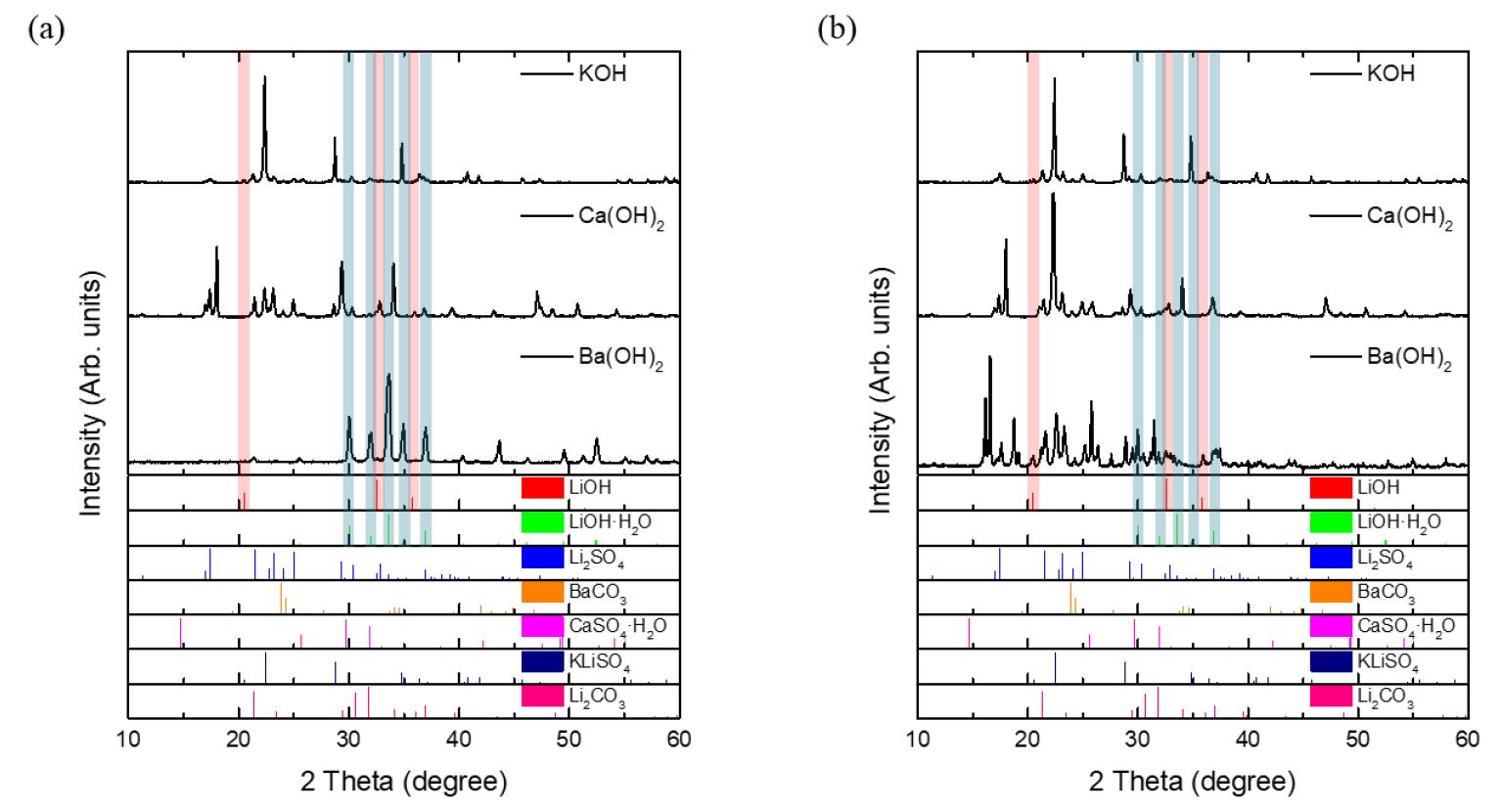
알칼리성 침전제 종류에 따른 수산화리튬 제조 거동을 알아보기 위해 (KOH, Ca(OH)2, Ba(OH)2) 총 3 가지의 침전제를 사용하였으며, 연구 원료에는 폐리튬이차전지에서 회수된 황산리튬을 사용하였다. 또한 각 조건에서의 균일하고 순도 높은 수산화리튬 분말의 합성을 위하여 이전의 연구와 같이 2차 침전법인 DRR공정을 통해 수산화리튬을 제조하였다. Fig. 3는 수산화리튬 제조 거동을 확인하기 위하여 (a) 40 ℃, (b) 80 ℃의 합성온도에서 실험을 실시한 결과이며, 합성온도를 제외한 공정의 합성시간, 침전제 몰비, 공정 횟수는 2 hr, [Li]/[OH]=1:1, DRR 공정으로 고정하였다. 침전제로 사용하는 KOH, Ca(OH)2, Ba(OH)2 각각의 수산화리튬 반응은 식 (1), (2), (3)과 같으며 aq는 수용액상(aqueous solution), s는 고체상(solid phase)을 나타낸다(KSP: K2SO4= 1.32, CaSO4=2.4×10-5, BaSO4, 1.1×10-10).
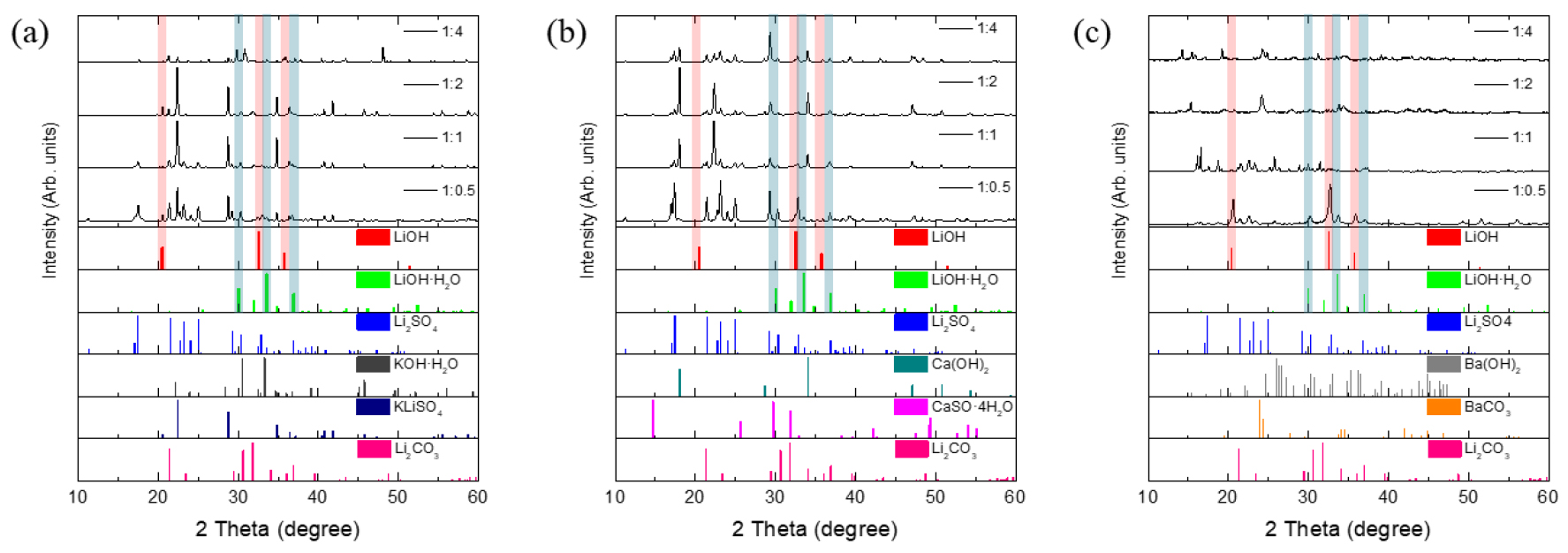
알칼리성 침전제 종류별 합성온도에 따라 합성된 분말의 결정성을 확인하기 위해 X-선 회절 분석을 진행하였다. 합성된 분말의 회절패턴에서 불순물을 제외하고 크게 수산화리튬과 수산화리튬 제일수화물이 동시에 분석되었으며 이에 따라 두 합성물이 혼재되어 있다고 판단하였다(LiOH, JCPDS no. 75-0777, LiOH∙H2O, JCPDS no. 76-1047). KOH의 경우에는 합성온도 40 ℃, 80 ℃에서 모두 LiOH∙H2O 피크를 희미하게 확인할 수 있었지만 대부분 불순물인 KLiSO4의 피크임을 확인하였다. 이는 황산리튬이 녹아 있는 황산염 용액에 포함되어 있는 황산염 이온이 침전제로 투입되는 KOH와의 반응을 통해 KLiSO4과 같은 복합염의 형성으로 인한 리튬 이온 유실로 수산화리튬 합성률이 낮다고 판단하였다20). Ca(OH)2를 투입하였을 때의 합성 분말은 합성온도 40 ℃, 80 ℃에서 모두 LiOH∙H2O 상을 확인할 수 있었으며, 합성온도 80 ℃일 때 보다 40 ℃일 때의 LiOH∙H2O 결정상이 더 강하게 나타남을 확인하였다. 불순물로는 CaSO4·H2O 상을 확인할 수 있었으며 이는 KOH와 마찬가지로 Ca 복합염이 형성되었다고 판단하였다. 또한, 원료로 사용된 황산리튬 피크가 강하게 나타남을 보아 황산리튬이 미반응물로써 수산화리튬과 혼재하여 존재하고 있음을 확인하였다.
세 종류의 알칼리성 수산화물 중에서 Ba(OH)2 사용하여 수산화리튬 합성을 진행하였을 때가 가장 수산화리튬 결정성이 높음을 확인할 수 있었으며, Ca(OH)2를 투입하였을 때와 마찬가지로 합성온도 40 ℃일 때 강하고 균일한 LiOH∙H2O의 결정상을 나타내었다. 합성온도에 따른 실험을 우선적으로 실행한 후, 전구체 몰비 변수 조절을 통하여 제조되는 수산화리튬의 제조 거동을 평가하였다. 알칼리성 수산화물과의 몰비에 따른 수산화리튬 제조 거동 및 전구체 농도가 수산화리튬 합성이 미치는 영향을 파악하기 위하여 [Li]/[OH]의 몰비를 1:0.5, 1:1, 1:2, 1:4로 두어 침전제 농도에 따른 분말의 제조 거동을 확인하였다. 수산화물 농도에 따른 농도 의존성 확인을 위해 합성온도는 선행연구와 같이 40 ℃, 80 ℃에서 합성시간 2 hr, DRR 공정을 이용하여 수산화리튬을 합성하였다.
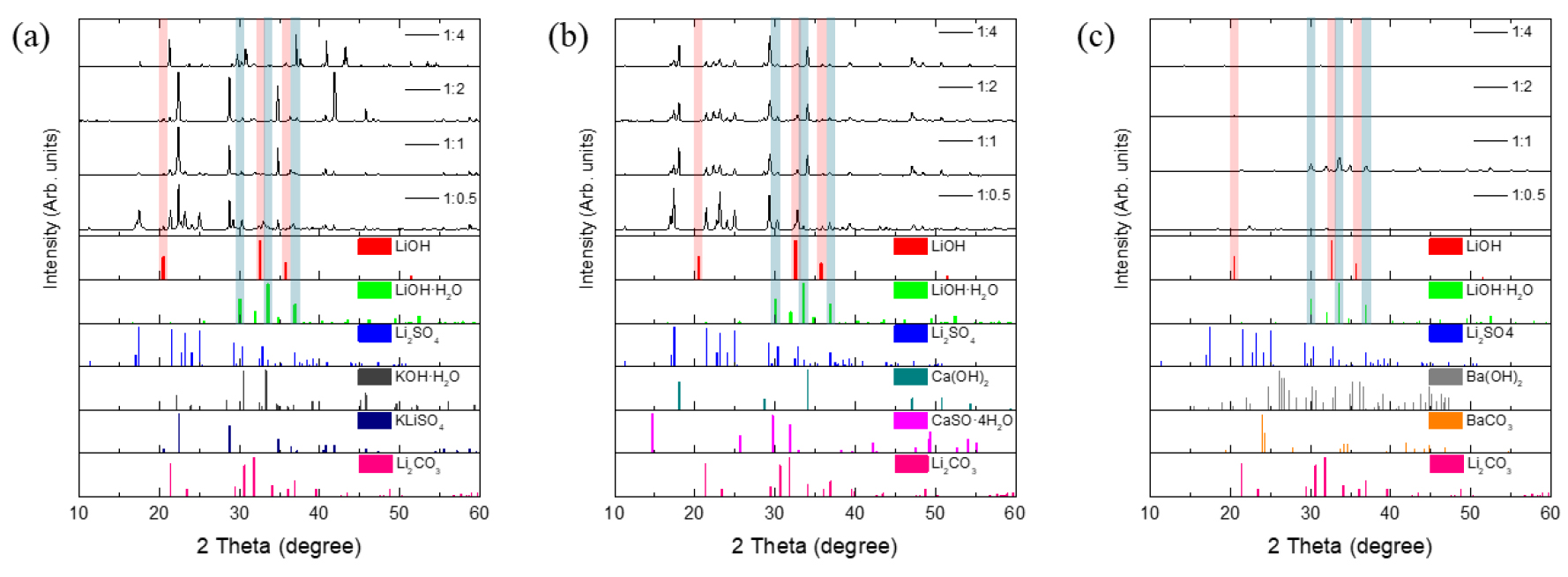
Fig. 4는 합성온도 40 ℃에서 [Li]/[OH]=1:0.5~4로 침전제의 농도를 달리하여 합성한 분말의 회절패턴을 분석한 결과를 나타냈다. 침전제 종류로 KOH를 선택하여 수산화리튬 합성공정을 진행하였을 때는 LiOH을 포함하여 LiOH∙H2O의 결정상 또한 거의 나타나지 않음을 확인할 수 있었으나 KOH의 투입 농도가 높을수록 LiOH∙H2O 상이 낮을 때보다는 강하게 나타남을 확인할 수 있다. 마찬가지로 [Li]/[OH]=1:0.5, 1:1, 1:2의 전구체 몰비에서 KLiSO4의 복합염의 결정상이 강하게 나타남을 Fig. 4(a)에서 확인할 수 있었다. Ca(OH)2를 침전제로 사용하여 합성을 진행한 결과, KOH보다는 LiOH∙H2O 상의 형성이 상대적으로 잘 되었음을 알 수 있었다. 또한 [Li]/[OH]=1:0.5의 몰비에서는 LiOH의 결정상을 확인할 수 있었으며, 이 외의 다른 전구체 몰비([Li]/[OH]=1:1~4)에서도 희미하게 나타남을 Fig. 4(b)에서 확인할 수 있었다. 특히, Ca(OH)2를 침전제로 사용할 경우에는 난용해성의 특징을 가지고 있는 Ca+이 황산리튬이 녹아 있는 전구체 용액에 해리되면서 SO42-과의 반응을 통해 CaSO4(s)의 침전물로 가라앉으면서 해당 불순물을 제거해야 한다. 하지만, Ca(OH)2는 물에 대한 용해도가 낮아 수용액 상에 이온으로 존재하는 것이 아닌 고체인 결정상으로 그대로 남기 때문에 반응이 어렵다. 침전제로 Ba(OH)2를 사용하여 수산화리튬을 제조한 결과는 Fig. 4(c)에 나타냈으며, 전구체 몰비가 [Li]/[OH]=1:1일 때, LiOH∙H2O의 피크 형상이 강했고 일부는 LiOH∙H2O의 상도 확인할 수 있었다. 특히, 몰비가 [Li]/[OH]=1:2 이상으로 침전제 농도가 높아지면 반응 후 잔사와 용액 간의 고/액 분리를 진행할 때, 용액에 Ba(OH)2을 포함한 불순물이 수산화리튬 용액에 잔류함에 따라 수득한 분말에 불순물이 다수 포함되어 있다고 판단하였다.
Fig. 5는 합성온도 80 ℃에서 [Li]/[OH]=1:0.5~4로 침전제의 농도를 달리하여 합성한 분말의 회절패턴을 분석한 결과를 나타냈다. 특히, 앞서 합성온도가 40 ℃일 때 가장 균일하고 결정성 높았던 Ba(OH)2의 경우에 [Li]/[OH]=1:0.5으로 전구체 몰비를 두어 진행한 결과가 상대적으로 가장 높은 수산화리튬 결정성을 갖는 것을 확인하였다. 또한, 합성온도가 높아짐에 따라 LiOH∙H2O의 결정상 보다는 일수화물이 붙지 않은 LiOH의 결정상을 나타내었다. 나머지 알칼리성 침전제인 KOH, Ca(OH)2의 경우에는 Ba(OH)2에 비해 상대적으로 거의 합성반응을 하지 못하였지만, Ba(OH)2에서의 변화와 같이 반응온도 40 ℃이었을 때 희미하게 띄던 LiOH∙H2O의 결정상은 합성온도가 80 ℃로 높아짐에 따라 거의 보이지 않고, 희미하지만 일수화물이 붙지 않은 LiOH의 결정상 피크를 확인할 수 있었다.
알칼리성 침전제 종류에 따라 제조한 분말의 미세조직을 확인하기 위하여 제조한 수산화리튬 분말의 SEM 분석을 진행하였다. 모든 합성조건(합성온도, 침전제와의 농도비)에서 알칼리성 침전제가 Ba(OH)2일 때, 상대적으로 높은 수산화리튬 결정성을 나타냈으며 해당 조건에서의 미세조직 확인 및 비교분석을 위해 SEM 결과를 Fig. 6에 나타냈다. 가장 높은 LiOH과 LiOH∙H2O의 결정상을 보인 두 합성조건에서의 수산화리튬 입자 분석을 진행한 결과, 대체로 100 nm의 입자 크기를 가진 둥근 형태의 입자를 형성했음을 확인할 수 있었다((a): 합성온도 40 ℃, [Li]/[OH]=1:1, (b): 합성온도 80 ℃, [Li]/[OH]=1:0.5). Fig. 7은 같은 조건에서의 알칼리성 침전제 종류에 따라 합성된 분말의 미세조직을 비교하기 위해 분석한 결과이다(전구체 몰비 [Li]/[OH]=1:1 합성온도 40 ℃, 합성시간 2 hr). 제조된 수산화리튬 분말의 입자는 각 조성에 따라서 모양과 크기가 다르게 형성되었으며, 침전제의 조성마다 입자 크기는 상이했지만 대체로 1 μm 이하의 입자들로 구성되어 있는 것을 확인할 수 있었다. 특히 KOH를 침전제로 사용하여 제조된 분말의 입자의 경우에는 입자 형상과 크기 또한 불균일하고, 다른 침전제를 사용했을 때에 비해 입자 크기가 크게 제조되었음을 확인하였다. 또한 제조된 수산화리튬의 입자 크기는 합성온도 40 ℃, 합성시간 2 hr, [Li]/[OH]=1:1 조건일 때, (a) KOH, (b) Ca(OH)2, (c) Ba(OH)2로 갈수록 입자 크기가 작게 형성되었으며, Ba(OH)2일 때 가장 균일하고 결정성 높은 수산화리튬을 제조하였다. 이를 통하여, 알칼리성 침전제 종류에 따라 수산화리튬 분말 결정성을 포함하여 입자의 크기에도 영향을 미침을 알 수 있었다.
최종적으로 알칼리성 침전제 종류에 따라 합성된 분말의 LiOH∙H2O과 LiOH 합성 정도를 확인하기 위하여 XRD로 분석한 분말 결정성의 결과를 Table 2에 정리하여 나타냈다. 알칼리성 수산화물 조성에 따라 합성된 분말은 결과적으로 LiOH∙H2O와 LiOH의 두 가지 수산화리튬 분말 합성이 가능하기는 하지만, Ba(OH)2를 침전제로 사용하였을 때가 가장 결정성 높은 분말을 합성할 수 있음을 확인하였다.
Table 2.
Synthesized result of LiOH powder prepared according to alkaline hydroxide composition
4. 결 론
본 연구에서는 알칼리성 침전제 종류에 따라 제조되는 수산화리튬 결정화 정도를 확인하였다. 폐리튬이차전지로부터 회수된 황산리튬을 출발 원료로 사용하여 수산화리튬 제조 거동을 확인하였으며, 합성 진행 간 불순물 제거 및 높은 수산화리튬 결정성을 위해 2차 침전법인 DRR공정을 사용하였다. 알칼리성 침전제 종류에 따른 수산화리튬 제조 거동 평가를 위해 알칼리성 침전제 종류(KOH, Ca(OH)2, Ba(OH)2)를 포함하여 전구체 몰비 및 합성온도 조건 설정을 두어 실험을 진행하였다. 합성온도 조건에서는 합성온도가 높을수록 LiOH∙H2O보다 수화물이 제거된 LiOH 분말의 결정성을 확인할 수 있었으며, 알칼리금속 수산화물 조성에 따라 제조한 수산화리튬은 특히 Ba(OH)2 일 때 온도에 상관없이 가장 균일한 LiOH∙H2O 혹은 LiOH 분말을 합성하였다. Ca(OH)2의 경우에는 물에 대한 용해도가 낮아 수산화이온이 용액 상에 적게 존재하기 때문에 리튬이온과의 반응이 어려워 수산화리튬 합성이 어렵다고 판단하였다. 최종적으로는 회수된 리튬염인 황산리튬 분말을 이용하여 침전제로 알칼리금속 수산화물 Ba(OH)2를 사용했을 때, 합성시간 2 hr, 전구체 몰비가 [Li]/[OH]=1:1의 합성조건에서 가장 최적으로 수산화리튬 분말을 합성하였다. 또한, 합성온도 40 ℃일 때는 LiOH∙H2O(s)를, 합성온도 80 ℃일 때는 수화물이 제거된 LiOH(s)를 합성하였음을 확인할 수 있었다.