1. 서 론
리튬이차전지(Li-ion battery)는 1991년 최초로 상용화되었으며, 현재에는 친환경 전기자동차의 전원공급을 위해 사용된다1). 전기자동차 산업은 전 세계적으로 빠르게 발전하고 있으며, 2040년에 2020년 대비 약 32배 증가한 1억 400만대의 전기차가 판매될 것으로 전망되며, 배터리의 시장규모 또한 2019년 대비 약 33% 증가하여 급속도로 성장하고 있다2). 리튬계 이차전지의 이론 수명은 6~8년으로 2020년까지 연간 10.2만 톤이 폐기되었으며, 2030년까지 1.100만 톤 이상에 이를 것으로 예상된다3,4).
그 중 올리빈형 구조를 가진 리튬인산철계(LiFePO4, LFP) 배터리는 1997년 Goodenough가 제안한 이래로 주목을 받아 리튬계 이차전지의 양극재로 사용되어왔으며, 현재 전 세계 시장의 약 36%를 점유하고 있어 향후 수많은 폐배터리가 발생할 것으로 예상되고 있다5,6,7,8). 이러한 LFP 배터리는 저렴한 비용과 높은 안전성으로 인해 리튬계 이차전지의 시장 점유율에 기여하였으며, 급격한 시장규모의 성장에 따라 리튬자원의 공급부족으로 이루어질 수 있다7). 그러므로 세계적인 리튬의 가격 변동성과 국내 리튬 원자재 수입 의존성이 높기 때문에 재활용의 관심이 높아지고 있다. 폐배터리는 희소금속과 유해금속을 포함할 뿐만 아니라, 처리가 제한적이고 처리 비용이 높기 때문에 환경문제 해결과 더불어 자원순환의 일환으로 폐배터리 재활용 연구를 통한 리튬 금속의 회수는 필수적이다9). 또한, 리튬계 이차전지의 시장이 확대됨에 따라 공정에서의 스크랩을 필두로 하여 사용 후 폐배터리의 재활용 연구가 활발히 진행되고 있다10,11,12,13,14,15,16).
폐LFP 배터리의 재활용 연구의 경우, 크게 직접 재생법17,18,19,20)과 습식 침출 및 재합성을 통한 하이브리드형 공정법21,22,23,24,25,26,27,28)으로 나눌 수 있다. 또한, 열처리를 통해 다시 재사용하는 직접 재생법이 가지고 있는 단점을 보완하기 위하여 습식 침출 및 재합성의 하이브리드형 공정법이 제안되었다. 하이브리드형 공정법은 강산, 약산 및 과황산계 산화제와 같은 침출제를 이용하여 폐LFP 에서 리튬을 선택적으로 회수할 수 있다고 보고하였다26,32,33). 약산을 이용한 연구는 포름산23), 아세트산25), 시트러스산29,30) 및 옥살산31)을 이용하여 리튬을 선택적으로 회수하는 연구가 수행되었다. 과황산계 산화제인 과황산나트륨을 이용하여 리튬을 약 99% 침출하였으며26), 과황산나트륨을 이용하여 기계적인 침출로 리튬을 99% 이상 침출하였다는 연구결과도 보고되었다32). 또한, 과황산계 산화제인 과황산암모늄을 이용하여 침출한 연구 결과도 보고되었다33). 이와 같이 최근 과황산계 산화제를 이용한 연구들이 수행되었지만, 동일한 조성의 폐LFP 분말 및 동일한 침출 조건에서 실험을 진행하지 않았으며, 자세한 과황산계 산화제와 리튬의 반응을 통한 침출 메커니즘을 설명하지 않아 각 산화제의 종류별 리튬의 침출율 및 특성의 비교 분석이 어렵다.
본 연구에서는 폐LFP 양극재 분말에서 과황산계의 산화제 사용하여 리튬의 선택적 침출 및 침출율을 비교 분석하고자 하였다. 비교 분석을 위하여 화학적 반응식을 고려하여 열역학적 계산을 통한 고찰과 함께 3종류의 과황산계 산화제[과황산나트륨(Na2S2O8), 과황산칼륨(K2S2O8), 그리고 과황산암모늄((NH4)2S2O8)]를 이용하여 이에 따른 전체적인 침출율과 리튬에 대한 선택적 침출에 대하여 평가하였다.
2. 실험 방법
본 연구에서 사용된 폐LFP 분말은 L사에서 공급된 LFP 양극재 스크랩으로 분쇄공정을 거친 후 150 µm 이하로 분급되어진 분말을 사용하였다. 분급된 폐LFP 분말은 유도결합플라즈마 분광기(Inductively Coupled Plasma Optical Emission Spectroscopy, ICP-OES, Liberty RL Sequential, Varian)를 이용하여 분석한 결과, 리튬이 약 4.01% 함유되어 있으며, 양극재 기판의 주 성분인 알루미늄이 약 0.08% 혼합되어 있었다. 폐LFP 분말의 주요 성분에 대한 화학조성 및 기존에 진행된 연구진들이 사용한 폐LFP 분말의 주요 성분을 포함하여 Table 1에 나타내었으며, 주사전자현미경(Scanning Electron Microscope, SEM, Mira3, TESCAN) 및 X-선 회절분석법(X-ray diffraction spectroscopy, XRD, XRD-6100, Shimadzu)을 이용하여 분말의 표면 형상 및 결정상을 분석하였다. Table 1의 주요 성분을 보면 리튬의 함량은 문헌들과 비슷한 약 4.01%로 확인되었고, 철 및 인의 함량은 각 문헌별로 약간의 차이가 있었다.
Table 1.
Chemical composition of waste LiFePO4 cathode powders (%)
| Li | Fe | P | Al | etc | Ref. |
| 4.01 | 31.77 | 5.43 | 0.08 | - | This study |
| 3.46 | 26.45 | 15.88 | 16.85 | - | Yang et al.25) |
| 4.63 | 33.69 | 19.47 | - | 0.20 | Zhang et al.26) |
| 3.69 | 28.80 | 16.50 | 0.35 | 0.28 | Tao et al.34) |
| 3.89 | 29.63 | 12.85 | 11.58 | 7.7 | Ji et al.35) |
폐LFP 분말에서 리튬의 선택적 침출을 위하여 과황산계 산화제를 사용하였으며, 사용된 산화제는 시약급으로 과황산나트륨(Sodium persulfate, Na2S2O8, Sigma-Aldrich), 과황산칼륨(Potassium persulfate, K2S2O8, Sigma-Aldrich) 그리고 과황산암모늄(Ammonium persulfate, (NH4)2S2O8, Sigma-Aldrich)과 같이 3종류를 사용하여 침출효과를 비교하고자 하였다.
리튬의 선택적 침출은 상기 3종류의 과황산계 산화제를 폐LFP 분말 대비 반응 몰 비를 계산하여 증류수에 용해한 용액을 사용하였다. 먼저, 과황산계 산화제가 LiFePO4에 대하여 이론적 몰 비의 1.1배로 증류수에 용해된 용액에 각각 광액농도 50 g/L, 100 g/L, 및 200 g/L로 폐LFP 분말을 투입하여 실험하였다. 이때, 교반속도 및 침출시간은 250 rpm 및 3시간으로 고정하였다.
과황산계 산화제의 농도 및 광액농도에 따른 리튬의 선택적 침출 후 침출 잔사를 필터페이퍼(Qualitative Filter Paper 150 mm, ADVANTEC)를 이용하여 고액 분리하였으며, 고상은 건조 후 분말 특성을 살펴보았다. 액상의 경우에는 ICP를 통하여 침출된 리튬의 양 및 성분을 분석하여 리튬의 침출율을 계산하였으며 식 (1)에 나타내었다.
여기서 ni는 성분 i의 침출율(%)이며, ci는 침출수 내 성분 i의 농도(g/L), 는 침출수의 부피, m0는 투입한 폐LFP 분말의 질량(g), wi는 투입 분말 내 성분 i의 함량(%)이다.
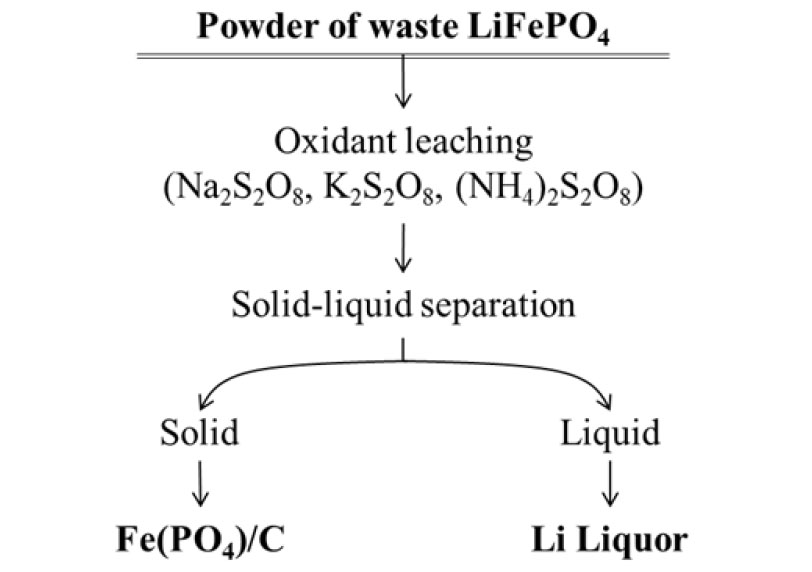
본 실험의 공정 흐름도는 Fig. 1에 나타내었으며, 최종적으로 회수된 분말은 SEM 및 XRD를 통해 침출 잔사의 형상 및 결정상을 분석하였다.
3. 결과 및 고찰
3.1. 폐LFP 분말
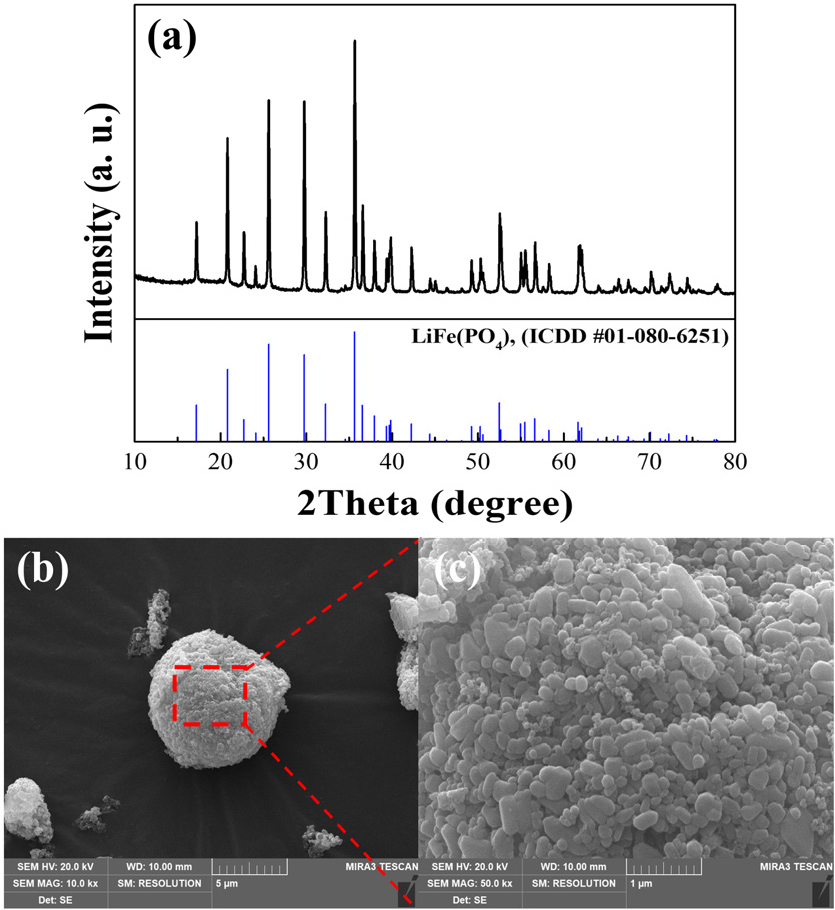
본 연구에서 사용한 폐LFP 분말의 표면 형상 및 결정상을 확인한 SEM 및 XRD 결과를 Fig. 2에 나타내었으며, 리튬의 선택적 침출 이후 표면 및 결정상을 비교하였다. 폐LFP 분말의 XRD 분석 결과 LiFePO4(ICDD #01-080-6251) 결정상으로 확인되었다.
먼저 폐LFP 분말에서 리튬을 선택적으로 침출하기 위해, 3종류의 과황산계 산화제와 폐LFP 분말과의 화학적 반응식을 하기 (2), (3), 및 (4)에 나타내었다. 이러한 화학적 반응이 열역학적으로 가능한지 고려하기 위하여 반응식을 HSC Chemistry 10(Metso:Outotec, Finland)을 사용하여 계산하였다.
사용된 HSC Chemistry 프로그램에서 LiFePO4의 직접적인 계산이 불가하기 때문에 상기의 반응을 계산하기 위해서, 출발물질인 LiFePO4는 아래 식 (5)와 같이 우선적으로 도출하여 반응식에 적용하였다36).
위와 같은 반응에 대하여, 3종류의 과황산계 산화제와 화학적 반응식은 다음과 같이 생성되고 Gibbs free energy() 기반의 열역학적 계산을 통해 자발적인 반응 유무의 예측이 가능하다.
상온에서 식 (6), (7) 및 (8)로부터 생성된 리튬황산염이 존재하는 수용액에 인산철이 침전하는 반응의 는 각각 -282.2 kJ/mol, -282.4 kJ/mol, -281.9 kJ/mol로 3종류의 과황산계 산화제 모두 유사한 자발적인 반응임을 확인하였다. 열역학적 계산을 기반으로 하여 3종류의 과황산계 산화제 영향에 따른 리튬의 선택적 분리 및 침출율을 비교하였다.
3.2. 폐LFP 분말의 침출
폐LFP 분말의 침출에 과황산계 산화제는 상기 반응식 (2), (3) 및 (4)에 따라 LiFePO4에 대하여 이론적 몰 비 대비 1.1배로 증류수에 용해시켜 투입하였다. 광액농도에 따른 침출율을 살펴보기 위하여 광액농도를 50 g/L, 100 g/L 및 200 g/L로 조절하여 비교하였다. 침출 실험의 고정 변수는 폐LFP 분말이 침출용액과 충분히 반응할 수 있도록 교반속도, 반응 온도 및 시간은 각각 250 rpm, 30℃으로 유지하면서 3시간으로 진행하였다. 이는 기존의 연구결과에서 과황산계 산화제인 과황산나트륨(Na2S2O8)에 의한 리튬의 선택적 침출 시, 리튬 침출율은 침출 온도 및 시간에 대한 영향이 매우 적으며, 과황산계 산화제의 양은 이론적 양 대비 1.05배 이상이면 리튬의 침출율이 거의 일정하다는 보고에 따라 본 연구의 기본 실험 조건을 결정하였다26). 침출 후에는 잔사와 용액을 필터페이퍼를 사용하여 분리하였으며, 용액의 경우 리튬을 비롯한 함유 성분을 ICP 분석을 통하여 성분을 분석하였고 침출 잔사는 SEM 및 XRD를 통하여 표면 형상 및 결정상을 분석하였다.
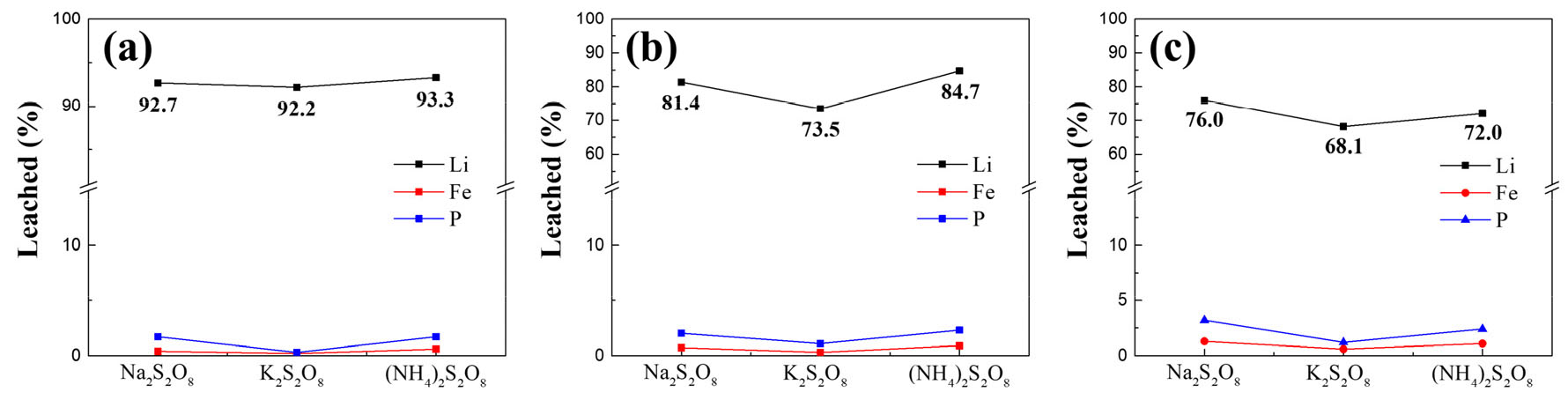
광액농도 50 g/L, 100 g/L 및 200 g/L 조건에서 3종류의 과황산계 산화제(Na2S2O8, K2S2O8, (NH4)2S2O8)를 사용하여 리튬을 선택적으로 침출하고자 하였다. 각 조건의 광액농도에서 침출 후 얻은 침출 잔사물은 반응 후 표면 형상의 변화 및 결정상 확인을 위한 SEM 및 XRD는 Fig. 3에 나타내었으며, 침출 후 침출용액에 함유된 각 성분의 농도와 리튬 침출율을 Table 2 및 Fig. 4에 나타내었다.
Table 2.
Chemical composition of reaction leachate using oxidant agents from waste LiFePO4 cathode powder (pulp density = 50 g/L, 100 g/L, 200 g/L)
Fig. 2(a)의 XRD 분석결과 본 연구에서 사용한 폐LFP 분말은 전형적인 LFP 이차전지 양극재 결정상인 LiFePO4를 나타내었고, 3종류의 과황산계 산화제를 사용하여 리튬을 선택적으로 침출한 후 회수된 침출 잔사의 결정상은 Fig. 3(a)에 나타내었다. 위에서부터 (1)은 폐LFP 분말의 피크인 LiFePO4 결정상이며, (2)는 과황산암모늄, (3)은 과황산포타슘, (4)는 과황산나트륨을 사용하여 침출한 후 회수된 침출 잔사의 XRD결과이다. 각 과황산계 산화제를 사용하여 침출 한 침출 잔사의 XRD 결과, 리튬이 제거된 FePO4(ICDD #01-074-9600)결정상으로 분석되었다. 이는 과황산계 산화제를 이용한 리튬 침출 후의 결정상은 orthorhombic olivine LiFePO4 구조에서 결정성이 높은 orthorhombic FePO4 결정상으로 바뀌었다는 기존의 연구결과와 일치하는 경향을 보였다26,32,37). 또한, Fig. 3(b)-(c)의 SEM 분석결과 침출 전의 폐LFP 분말과 비교하였을 때 표면형상 차이는 보이지 않았다. 폐LFP 분말과 과황산계 산화제가 반응하여 리튬이 침출되었고, 이에 침출 잔사의 결정상이 변화하였지만 표면 형상은 변하지 않았다. 따라서, 과황산계 산화제와의 반응은 폐LFP 분말의 형상에 큰 영향을 미치지 않는 것으로 보인다.
Table 2의 ICP 분석 결과에서 3종류의 과황산계 산화제를 사용하여 광액농도 50 g/L로 침출한 경우, 리튬의 침출 농도는 약 1,800 ppm 정도로 분석되었다. 침출 실험 시 초기 pHi와 최종 pHa를 측정하였으며, 최종 pHa는 광액농도가 증가함에 따라 약간 감소하는 경향을 보였다. 과황산계 산화제를 이용하여 침출 후 침출수의 ICP 분석 결과를 토대로 식 (1)을 이용하여 폐LFP 분말의 리튬 농도 대비 침출율을 계산하였으며, 약 92% 이상으로 과황산계 산화제 종류에 상관없이 거의 비슷한 결과를 나타내었다. 광액농도 100 g/L 및 200 g/L의 경우에 3종류 과황산계 산화제 모두 광액농도가 늘어날수록 리튬 침출율이 감소하였다. Na2S2O8의 경우에는 92.7%에서 81.4%(감소율 12.2%) 및 76.0%(감소율 6.6%)로 감소하였고, K2S2O8의 경우에는 92.2%에서 73.5%(감소율 20.3%) 및 68.1%(감소율 7.3%)로 감소하였고, (NH4)2S2O8의 경우에는 93.3%에서 84.7%(감소율 9.2%) 및 72.0%(감소율 15.0%)로 감소하였다. 특히 100 g/L 이상의 광액농도에서는 과황산계 산화제인 K2S2O8의 경우, Na2S2O8 및 (NH4)2S2O8에 비하여 동일한 광액농도 조건에서 리튬의 침출율이 제일 낮았다.
Table 3에서 나타낸 과황산계 산화제의 물에 대한 용해도를 보면 K2S2O8은 Na2S2O8 및 (NH4)2S2O8에 비하여 용해도가 현저하게 낮은 것을 확인할 수 있다38,39,40). 따라서 K2S2O8이 다른 산화제에 비해 낮은 용해도로 인하여 완전 용해가 되지 않고 슬러리 상태로 남아 있어 폐LFP 분말과 반응을 하지 못하였기 때문에 리튬의 침출율이 낮은 것으로 판단된다.
Table 3.
Solubility of persulfate-based oxidant agents in 100 ml of water by temperature from 0℃ to 50℃38,39,40)
| g/100 ml water | |||
| Temperature (℃) | Na2S2O8 | K2S2O8 | (NH4)2S2O8 |
| 0 | 53.4 | 1.7 | - |
| 10 | 54.1 | 2.9 | - |
| 20 | 54.7 | 4.7 | 55.9 |
| 25 | 74.8 | 5.9 | 85.0 |
| 40 | 82.9 | 11.3 | - |
| 50 | 85.0 | 16.8 | 116.0 |
폐LFP 분말에서 부터 리튬의 선택적 침출을 위하여 과황산계 산화제인 Na2S2O8을 사용한 Zhang et al.의 연구 결과를 보면, 침출 온도 25℃, 침출 시간 20분, Na2S2O8의 이론 양 대비 1.05배 및 광액농도 300 g/L의 조건에서 리튬의 침출율이 약 99% 이상이라고 보고하였다26). 또한, 광액농도가 200 g/L에서 500 g/L까지 증가하여도 리튬의 침출율이 모두 약 90% 이상이라고 보고하였다. 본 연구에서는 50 g/L일 때, 리튬의 침출율이 92.7% 이지만 광액농도가 200 g/L까지 증가하였을 때 76.0%로 약 16.7% 감소하여 매우 상반된 결과를 보였다. 또한, (NH4)2S2O8를 사용한 Peng et al.의 연구에서는 침출 온도 30℃, 침출 시간 300분, (NH4)2S2O8의 이론 양 대비 1.4배 및 광액농도 50 g/L의 조건에서 97.7%의 리튬 침출율을 나타내었으며, 광액농도 100 g/L에서는 리튬의 침출율이 45.4%로 53.5% 정도로 급격히 감소하였다33). 본 연구에서는 (NH4)2S2O8을 이용하여 광액농도 50 g/L의 침출조건에서 리튬의 침출율이 93.3%로 유사한 결과를 나타내었지만, 광액농도 100 g/L에서는 리튬의 침출율이 84.7%로 Peng et al.의 연구에서 45.4%에 비해 39.5%의 큰 차이를 보였다.
Table 2의 ICP 분석 결과를 토대로 과황산계 산화제를 이용한 침출 시 광액농도 별 리튬에 대한 타 성분의 분리효율을 보고자 하였으며, 분배계수 식을 바탕으로 아래와 같은 식으로 계산하였다. 다음의 계산식을 식 (9) 및 식 (10)에 나타내었다.
여기서 Di는 성분 i의 분배 계수이며, ci-L은 침출수 내 성분 i의 농도(g /L), ci-S은 침출 반응 후 침출 잔사 내 성분 i의 농도(g/L)이다. 여기서 침출 잔사 내 성분 i의 농도는 투입한 원료 내 성분 i의 농도에서 침출수의 성분 i의 농도를 빼서 계산하였다. 그 다음 리튬과 철 및 인의 분리효율을 확인하기 위해 다음과 같은 식으로 계산하였다.
식 (9)에서 계산된 Di를 이용하여 β를 계산하였으며, β(Li-Fe)는 리튬과 철의 분리효율, β(Li-P)는 리튬과 인의 분리효율을 표현하여 Table 4에 표시하였다. Table 2의 리튬의 침출율은 과황산포타슘이 92.2%로 가장 낮았으나 분리효율은 다른 원소들에 비하여 약 1.6배 높은 것으로 확인되었다. 침출 시 광액농도가 증가함에 따라 리튬의 침출율은 감소하였는데 분리효율 또한 감소하는 것으로 확인되었다. 따라서, 본 연구에서는 광액농도가 가장 낮은 50 g/L에서의 침출이 가장 적합한 것으로 판단된다.
Table 4.
Chemical composition of reaction leachate using oxidant agents from LiFePO4 cathode powder (pulp density = 50 g/L, 100 g/L, 200 g/L)
4. 결 론
폐리튬인산철 배터리의 양극재 분말에서 리튬을 선택적으로 회수하기 위하여 과황산계 산화제를 사용하였다. 과황산계 산화제의 비교 분석을 위하여 과황산나트륨, 과황산포타슘, 과황산암모늄의 3종류 산화제를 사용하였으며, 리튬의 선택적 침출율 및 각 성분 간 분리효율을 평가하였다.
1) 폐LFP 분말의 XRD 결과는 올리빈 구조의 LiFePO4 결정상으로 분석되었으며, 리튬의 침출 후 XRD 결정상은 Fe(PO4) 결정구조로 변하였다.
2) SEM 분석 결과, 폐LFP 분말과 과황산계 산화제를 이용하여 침출 후 잔사의 분말의 형상은 특별한 차이가 없었다.
3) 사용된 모든 과황산계 산화제에서 광액농도 50 g/L의 조건에서는 전체적으로 92% 이상의 침출율을 나타내었으며, 특히 과황산암모늄이 93.3%로 가장 높은 침출율을 보였다.
4) 광액농도를 100 g/L 및 200 g/L로 증가시켰을 때, 모든 과황산계 산화제에서 리튬의 침출율이 감소하였으며, 특히 과황산포타슘의 경우 92.2%에서 68.1%로 24.1%의 최대 감소율을 보였다. 이는 과황산포타슘의 경우 물에 대한 용해도가 다른 과황산계 산화제에 비해 현저히 낮기 때문에 폐LFP 분말과 충분히 반응하지 못하여 침출율이 낮은 것으로 판단된다.
5) 리튬과 타 성분과의 분리효율 측면에서는 과황산포타슘이 다른 산화제에 비해 제일 효과적임을 알 수 있었다.