1. 서 론
2. 실험 방법
3. 결과 및 고찰
3.1. 스크랩 활용 Ti 분말의 입도별 산소 제어
3.2. Ti3AlC2 MAX 상 합성에 미치는 DOSS-Ti 분말의 입도의 영향
3.3. Ti3AlC2 MAX 상분율에 미치는 Al 함량의 영향
3.4. 최적 조건에서 합성된 Ti3AlC2 MAX 상의 미세구조, 형상 및 나노구조
4. 결 론
1. 서 론
MAX 상은 일반식 Mn+1AXn 을 갖는 층상 구조의 삼원 탄화물, 질화물 및 탄질화물이며, 여기서 M은 초기 전이 금속이며, A는 A족 원소(13족 또는 14족 원소)이며, X는 탄소 또는 질소이며, n은 1 ~ 3의 정수이다1). MAX 상은 저밀도, 우수한 전기 전도성과 같은 고유한 금속 및 세라믹과 같은 특성으로 인해 점점 더 많은 관심을 받고 있다2). MAX 상의 가장 흥미로운 특성은 전기화학 커패시터에 이상적인 2차원 물질로 알려진 MXene 합성의 전구체로 사용될 수 있다는 점이다. MXene의 합성을 위한 다양한 MAX 상이 있지만 Ti3AlC2가 우수한 전기화학적 성능으로 인해 가장 널리 사용되어 오고 있다3).
일반적으로 MAX 상은 원소 분말을 혼합하고 고온의 불활성 분위기에서 가열하여 합성되므로, MXene의 전구체는 흑연으로 제조되는 그래핀과 같은 다른 2차원 물질에 비해 상대적으로 높은 비용이 요구된다. 저렴한 MAX 상을 제조하는 접근 방식 중 하나는 스크랩을 전구체로 사용하는 것이다4,5). 특히 금속 타이타늄(Ti)은 난가공성으로 인해 생산 공정에서는 많은 양의 스크랩이 발생하며, MAX 상의 전구체 중 하나로써 이러한 Ti 스크랩을 활용하는 것은 MAX 상의 합성 비용과 그에 따른 MXene의 합성에 소요되는 비용을 줄이는 데 도움이 될 수 있다. Ti 스크랩을 재활용하는 경제적인 방법 중 하나는 수소화-탈수소화(Hydrogenation-DeHydrogenation, HDH) 공정이 알려져 있다. HDH 공정은 Ti를 수소 분위기에 노출시켜 수소화물을 형성시킨 뒤, 수소화물의 취성을 이용하여 파쇄하여 수소화물 분말을 제조할 수 있다. 이 후 진공 열처리를 통하여 쉽게 저비용의 Ti 분말을 제조할 수 있다6,7). 하지만 분말화 과정에서 Ti의 높은 산소 친화력로 인해 산소 함량의 증가가 불가피하여, 후속적인 탈산 공정이 요구된다. 이러한 Ti의 잔류 산소는 Ti3AlC2 MAX 상의 합성 과정에서 악영향을 미칠 수 있다. Ti3AlC2 MAX 상의 합성 과정에서 잔류 산소는 Al의 높은 산소 친화도로 인해 MAX 상의 층 사이에 Al2O3를 형성하여 Al 손실로 인한 TiC의 형성을 야기할 수 있다. 또한, MAX 상에서 형성된 Al2O3 및 TiC는 MXene 제조를 위한 selective etching과정에서 multilayered MXene에 남아 개재물로 작용할 수 있다8). 따라서 산화 개재물의 형성을 억제하기 위해선 MAX 상 전구체 또는 MAX상의 산소 함량을 제어하는 것이 중요하며, 동시에 TiC의 함량을 최소화하여 Ti3AlC2의 상분율을 향상시키는 것이 요구된다.
이전 연구에서 Ti 스크랩으로부터 HDH 및 고상탈산(DeOxidation in Solid-State, DOSS) 공정을 통해 준비된 저산소 Ti , Al, graphite 분말을 3:1:2의 몰비로 혼합하여 무압 소결 방식으로 Ti3AlC2 MAX상을 합성하였다9). 이 때의 합성된 25 ~ 45 μm의 DOSS-MAX상 분말의 산소 함량은 3,875 ppm이었다. Ti 스크랩으로부터 제조된 DOSS-MAX 분말은 상용 Ti3AlC2 MAX 분말보다 높은 Ti3AlC2의 상분율 및 낮은 산소 함량을 보여주었으며, Ti 분말의 산소 저감을 통하여 TiC불순물의 함량을 감소시킬 수 있었다. 그러나, 합성된 MAX상 분말에서 여전히 일부의 TiC가 잔존하였다. 따라서 본 연구는 전구체 Ti 분말의 입도 및 Al 함량을 제어하여 Ti 스크랩을 활용한 Ti3AlC2 MAX상의 상분율 향상을 위한 합성 조건의 최적화를 수행하였다.
2. 실험 방법
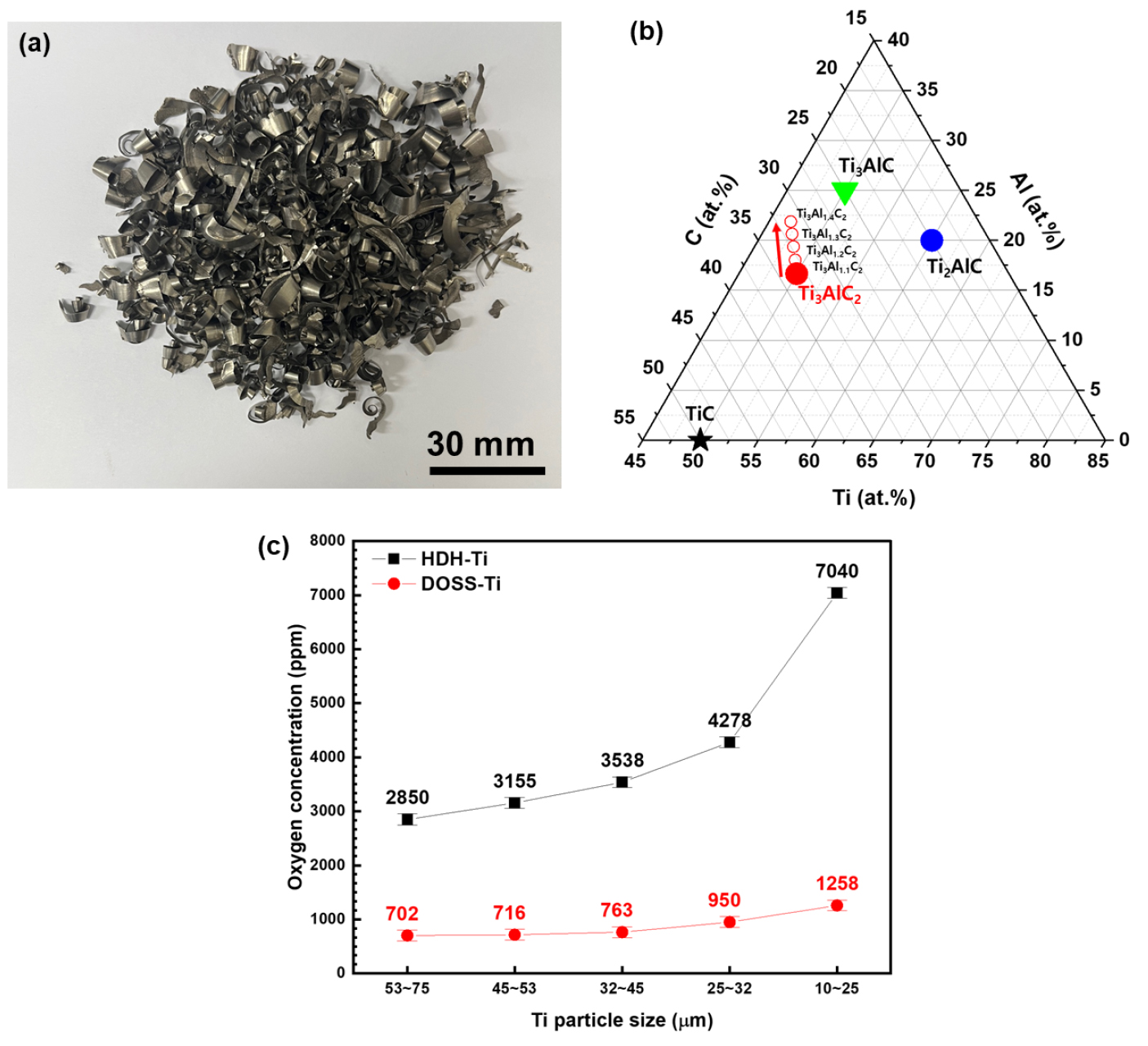
Ti 스크랩을 활용하여 Ti3AlC2 MAX 상을 합성하기 위해, Ti 스크랩에 대한 HDH 및 DOSS 공정이 수행되었다. Fig. 1(a)는 실험에 사용한 Ti 스크랩의 모습을 나타내었으며, 기계 가공 과정에서 발생한 터닝 스크랩을 사용하였으며, 에탄올과 아세톤으로 세척하였다. 세척된 Ti 터닝 스크랩은 6 × 105 Pa의 수소 분위기에서 700 °C에서 3 시간 동안 수행되었다. 수소화된 Ti 스크랩은 기계적 분쇄를 통해 분말로 만든 다음 7.3 × 10-2 Torr의 진공 분위기에서 700°C에서 3시간 동안 탈수소화하였다. 그 후, 탈수소화된 Ti(HDH-Ti) 분말은 10 ~ 75 μm의 입도 범위에서 입도별로 체질하였다. 이후, DOSS 공정은 상압 Ar 분위기 하에서 수행되었다10). 상압 Ar 분위기하에서 수행된 DOSS 공정은 고체 상태의 Ti와, 탈산제로 사용한 Ca 사이의 반응을 통하여 산소의 제어가 이루어진다.
Ti 분말의 표면과 Ca 그래뉼이 접촉한 영역에서 고체 상태의 Ca와 산소가 반응하며, 접촉하지 않는 영역에서는 일부 기화된 Ca와 산소가 반응하여 CaO를 형성하게 된다. 이 때의 반응 부산물인 CaO는 묽은 염산을 통해 산 세를 진행하면 쉽게 제거가 가능하다6).
이전 연구6,10)에서 확립된 최적조건에서 산세를 진행한 결과, 표면에서 Ca 성분이 완전이 제거되는 것을 확인됨에 따라 최종 MAX 상 합성체에 미치는 영향은 미미할 것으로 예상되었다. HDH-Ti 분말은 Ca 그래뉼(calcium granule, JUNSEI, 99.5%)과 함께 2:1의 질량비로 스테인리스 용기에 장입하였다. Super Kanthal furnace를 이용하여 800 °C에 300 분 동안 열처리를 진행하였다. 이때 승온 속도는 10 ℃/min이며, Ar을 1 기압을 유지하며 1,000 sccm씩 흘려주었다. 탈산 열처리 이후 분말은 10%의 묽은 염산과 증류수를 이용해 세척 후 진공 건조하여 회수하였다. 이후 Ti 스크랩을 활용한 Ti 분말을 사용하여 Ti3AlC2 MAX 상 분말의 합성을 수행하였다.
Ti3AlC2 MAX 상의 합성을 위해, DOSS-Ti 분말, Al (<45 μm powder size, 99% purity, SAMCHUN Pure Chemical Co., Ltd.) and graphite 분말(<45 μm powder size, 99.9995%, Alfa aesar Co., Ltd)이 출발 물질로써 사용되었다. 출발 물질 DOSS-Ti, Al 및 graphite 분말은 3 : 1 ~ 1.4 : 2의 몰 비율로 dry mixer에서 24 시간동안 혼합되었다. 출발 물질의 혼합 조건에 대하여 Ti-Al-C system에 대한 3원계 상태도에 나타내어 Fig. 1(b)에 도시하였다. 이어서 혼합된 분말은 스테인리스 몰드(ϕ 16 mm × 5 mm)에서 40 MPa의 압력 하에서 일축으로 압축시켰다. Ti3AlC2 MAX 상의 합성은 Super Kanthal furnace에서 Ar 분위기 하에서 무압 소결을 통하여 수행되었다. 승온 속도는 10 ℃/min으로 제어하였으며, 합성 온도는 1450 ℃에서 5시간 동안 유지하였다. 합성된 MAX 상은 마노 유발에서 분쇄하여 분말화하였다. 이후, Ti 스크랩으로부터 합성된 Ti3AlC2 MAX 상 분말에 대한 특성 분석이 진행되었다.
합성된 Ti3AlC2 MAX 상 분말의 결정 구조는 45 kV 및 40 mA에서 Cu Kα source를 사용한 X선 회절분석(X-ray diffraction, XRD, Shimadzu Co., XRD-6100)을 통하여 분석하였다. XRD는 step scan 모드를 사용하여 측정하였으며, 2θ는 5° ~ 80°, step size는 0.01°에서 step당 3초동안 데이터를 수집하였다. Rietveld refinement을 사용한 상에 대한 정량 분석은 PROFEX 소프트웨어를 사용하여 수행되었다11). 합성된 Ti3AlC2 MAX 상 분말의 산소 함량은 solid-state infrared absorption방식의 산소/질소 분석기(ON-900, Eltra Corp., Germany)를 사용하여 측정하였다. 합성된 Ti3AlC2 MAX 상의 미세조직과 분말의 형상은 전계방계 주사전자현미경(Field Emission Scanning Electron Microscope, FE-SEM, Hitachi Co., SU-70)을 통해 관찰하였다. 합성된 Ti3AlC2 MAX 상 분말의 표면 산화층 및 나노 구조는 구면수차 보정 투과전자 현미경(Cs corrected-Field Emission Transmission Electron Microscope, STEM, JEM-ARM200F)을 통해 분석하였다.
3. 결과 및 고찰
3.1. 스크랩 활용 Ti 분말의 입도별 산소 제어
Fig. 1(c)는 Ti 스크랩의 HDH 및 DOSS 공정 이후의 입도에 따른 산소 함량의 변화를 보여준다. HDH 공정으로 제조된 Ti 분말의 산소 함량은 입도 53 ~ 75 μm에서 2,850 ppm으로 측정되었다. 입도가 감소함에 따라 산소 함량은 지속적으로 증가하였으며, 입도가 10 ~ 25 μm까지 감소 시 7,040 ppm으로 산소 함량이 급격하게 증가하였다. 이후 HDH-Ti 분말에 대하여 DOSS 공정을 수행한 Ti 분말의 산소 함량은 입도 53 ~ 75 μm에서 705 ppm으로 측정되었으며, 입도가 감소함에 따라 산소 함량은 점차 증가하여 입도 10 ~ 25 μm에서 1,255 ppm으로 측정되었다. DOSS 공정은 Ti 내부의 고용된 산소를 제거할 뿐만 아니라 표면 산화층의 두께 또한 감소시키는 것으로 알려져 있다6). 따라서 DOSS 공정에 의해 Ti 스크랩으로부터 제조된 HDH-Ti 분말의 산소 함량은 효과적으로 감소시킬 수 있었다.
3.2. Ti3AlC2 MAX 상 합성에 미치는 DOSS-Ti 분말의 입도의 영향
Fig. 2(a)는 DOSS-Ti 분말의 입도에 따른 1450℃에서 5시간동안 합성한 MAX 상 분말의 XRD 결과를 보여준다. 입도 53 ~ 75μm의 DOSS-Ti 분말로 합성된 MAX 상 분말에서는 Ti3AlC2 및 TiC 상뿐만 아니라 Ti2AlC 상의 피크가 관찰되었다. DOSS-Ti 분말의 입도가 감소함에 따라 Ti2AlC 상의 (002) 피크의 강도가 점차 감소하였으며, 입도 25 ~ 32 μm 및 10 ~ 25 μm의 DOSS-Ti 분말로 합성된 MAX 상 분말에서는 Ti2AlC 상이 사라진 것으로 확인되었다. DOSS-Ti 분말의 입도가 감소함에 따라 MAX 상 합성 반응이 효과적으로 일어난 것으로 보인다. 일반적으로 MAX 상 합성에서 효과적인 합성 반응이 일어나기 위해서 분말 혼합물의 비표면적은 최대화되어야 한다고 알려져 있으며12), 이는 전구체 분말의 입도가 감소할수록 합성 반응이 효과적으로 이루어진다는 것을 의미한다. 한편, N. Usha Kiran 등13)은 Ti3SiC2 MAX 상 합성 과정에서, Ti 금속 전구체의 입자 크기가 상의 순도를 결정하는 데 중요한 역할을 한다고 보고하였다. 분말의 입자 크기가 작고, 유효 표면적이 높을수록 비화학양론적 TiO를 형성하여 MAX 상 형성을 방해하는 것을 확인하였다. Ti 분말 입도가 감소할수록 비표면적은 증가하고, 표면 산화층으로 인한 순수한 MAX 상 형성에 악영향을 미칠 수 있다. 하지만, 본 연구에서 DOSS-Ti 분말의 입자 크기가 감소함에 따른 순도 저하가 발생하지 않았으며, Ti2AlC 상의 사라지면서 Ti3AlC2 및 TiC 상만이 관찰되었다. 이는 DOSS 공정으로 인한 Ti 분말의 산소 저감 및 표면 산화층의 두께 감소14)의 영향과 분말 입자 크기의 감소에 따른 합성 반응 속도 향상12)이 기인한 것으로 판단된다.
원소 분말을 혼합한 무압 소결 시의 Ti3AlC2 MAX 상 합성 메커니즘은 다음과 같다15). 초기 혼합 분말은 Al의 융점(660°C) 이상에서 다량의 Al 원자가 빠르게 확산되고, 900°C 부근에서 Ti 입자 표면에 축적되어 Al이 풍부한 금속간 화합물을 형성한다. Al이 풍부한 금속간화합물의 외곽 층에서 Ti의 내부로 Al의 확산이 일어나고 입자는 Ti3Al을 형성하게 된다. AlxTi 금속간화합물 층은 Al3Ti와 TiAl의 구성요소가 각각 1387°C와 1460°C에 해당하는 분해 온도에 도달할 때까지 성장한다15). 1300°C 부근에서 Ti3Al 입자 표면의 일부 영역에서 다음과 같은 두 가지 반응이 일어난다.
1400°C 부근에서 Ti2AlC는 TiC와 반응하여 Ti3AlC2를 형성한다.
이러한 합성 메커니즘에 따라, 분말 입도가 증가하면 Al 원자가 Ti 입자의 표면에서 내부까지 확산되는 거리가 증가하게 된다. 이로 인해 32 μm 이상의 입도 범위에서 합성된 MAX 상들은 반응이 완료되지 못한 Ti2AlC 상이 잔류한 것으로 판단된다.
Fig. 2(b)는 DOSS-Ti 분말의 입자 크기에 따른 1450℃에서 5 시간동안 합성한 MAX 상의 산소 함량 변화를 보여준다. 입도 53 ~ 75μm의 DOSS-Ti 분말을 전구체로 사용한 MAX 상 합성체의 산소 함량은 3,428 ppm으로 나타났다. 전구체 DOSS-Ti 분말의 입자 크기가 감소함에 따라 합성된 MAX 상 분의 산소 함량은 점차 증가하였으며, 입도 10 ~ 25 μm의 DOSS-Ti 분말을 사용한 MAX 합성체의 산소 함량은 다소 증가한 수치인 3,682 ppm으로 나타났다. 이러한 산소 함량의 증가 경향은 DOSS-Ti 분말의 입자 크기 감소에 따른 산소 함량의 증가 경향과 일치하였다. 합성 반응이 충분히 이루어져 Ti3AlC2 상과 미량의 TiC 만이 잔류하며, 상대적으로 낮은 산소 함량을 나타내는 전구체 DOSS-Ti 분말의 입자 크기는 25 ~ 32 μm이었다. 따라서, 25 ~ 32 μm의 DOSS-Ti 분말을 사용하여 Al의 함량을 조절하여 추가적인 Ti3AlC2 MAX 상분율의 향상을 위한 조건을 조사하였다.
3.3. Ti3AlC2 MAX 상분율에 미치는 Al 함량의 영향
Fig. 3는 1450℃에서 5시간동안 합성한 MAX를 Rietveld refinement 수행 후 Al 함량에 따른 MAX 상의 XRD 패턴 분석 결과를 보여준다. 합성된 모든 Ti3AlC2 MAX 상 분말에서는 주로 Ti3AlC2 상과 미량의 TiC 및 Al3Ti에 해당하는 피크만이 관찰되었다. Al 함량에 따른 TiC 및 Al3Ti 피크의 미소한 강도의 변화가 관찰되었다. 이에 따른 상분율 변화를 계산한 결과를 Fig. 4(a)에 나타내었다. Al 함량이 1에서 1.1로 증가함에 따라 TiC의 상분율 3.58%에서 0.93%로 감소하였다. 이후 Al 함량이 1.2로 증가했을 때, TiC의 상분율은 1.7%로 증가하였으며 이후 Al 함량이 증가할수록 TiC의 상분율은 지속적으로 증가하였다. 한편, Al3Ti의 상분율은 Al 함량이 1에서 1.1로 증가함에 따라 0.53%에서 1.82%로 증가하였다. Al 함량이 증가함에 따라 Al3Ti의 상분율은 지속적으로 증가하는 경향을 나타내었다. 종합적으로 합성된 Ti3AlC2 MAX 상의 상분율은 Al 함량이 1에서 1.1로 증가하였을 때 97.25%의 가장 높은 상분율을 나타내었으며, 이후 Al3Ti와 TiC가 증가함에 따라 다시 Ti3AlC2의 상분율이 감소하는 경향이 확인되었다. Al 함량을 1.1로 소량 증가시키는 경우, Al 증발15,16)에 의한 TiC의 형성을 일부 억제시킬 수 있었다. 반면, Al 함량이 더욱 증가하는 경우, 앞선 합성 메커니즘 초기 단계에서 언급된 Al이 풍부한 금속간화합물 층이 과잉 분포하여 충분히 분해되지 못함에 따라 Al3Ti가 잔류하게 되어 화학양론적 불균형이 발생하여 오히려 TiC의 함량이 증가된 것으로 판단된다.
Fig. 4(b)는 Al 함량에 따른 Ti3AlC2 상의 (002) 면의 면간 거리 d(002)의 변화를 보여준다. Al 함량이 1에서 1.1로 증가함에 따라 d(002)는 0.9293 nm에서 0.9296 nm로 증가하였다. 이 후 Al 함량이 증가함에 따라 Ti3AlC2 상의 (002) 면의 면간 거리 d(002)는 지속적으로 증가하는 경향이 확인되었다. Fig. 4(c)는 Al 함량에 따른 Ti3AlC2 상의 격자 상수의 변화를 나타내었다. Al 함량이 1에서 1.1로 증가함에 따라 격자 상수 a는 0.3075 nm에서 0.3077 nm로 증가하였으며, 격자상수 c는 1.8587 nm에서 1.8593 nm로 증가하였다. Al 함량이 증가함에 따라 Ti3AlC2 상의 격자 상수 a 및 c는 모두 증가하였으며, 격자 상수 c의 증가량이 격자 상수 a의 증가량보다 크게 나타났다. 이는 축 비 c/a의 변화와 연관되며, 초기 축 비 c/a의 변화량은 크지 않았지만 Al 함량이 1.3으로 증가함에 따라 급격히 감소하였다. Al 함량의 증가에 따른 (002) 면 및 격자 상수의 증가 현상은 T.S. Mathis 등16)의 연구에서도 유사한 현상이 관찰되었다.
Fig. 4(d)는 Al 함량에 따른 1450℃에서 5시간동안 합성한 Ti3AlC2 MAX 상의 산소 함량의 변화를 보여준다. DOSS-Ti, Al, graphite 분말을 3:1:2의 몰 비율로 합성된 Ti3AlC2 MAX 상 합성체의 산소 함량은 2,720 ppm으로 나타났으며, Al 함량이 증가함에 따라 서서히 증가하여 3:1.4:2의 몰 비율로 합성된 Ti3AlC2 MAX 상 합성체의 산소 함량은 3,010 ppm으로 나타났다. 이 때 최적 합성 조건인 DOSS-Ti, Al, graphite 분말을 3:1.1:2의 몰 비율로 합성된 MAX 상 합성체의 산소 함량은 2,775 ppm이었다. 이어서 Ti3AlC2 MAX 상 합성체를 분말화한 경우 평균적으로 약 1,200 ppm가량 산소 함량이 증가하였다. 분말화한 Ti3AlC2 MAX 상 합성체 또한 Al 함량이 증가함에 따라 산소 함량이 유사하게 증가하는 경향이 확인되었으며, 최적 합성 조건인 3:1.1:2의 비율로 합성된 Ti3AlC2 MAX 상 분말의 산소 함량은 3,990 ppm으로 나타났다.
3.4. 최적 조건에서 합성된 Ti3AlC2 MAX 상의 미세구조, 형상 및 나노구조
이후, 최적 조건에서 합성된 Ti3AlC2 MAX 상의 미세구조 및 분말의 형상을 FE-SEM을 통하여 확인하였다. Fig. 5은 DOSS-Ti, Al, graphite 분말을 3:1.1:2의 몰 비율로 혼합하여 합성된 Ti3AlC2 MAX 상 합성체 및 분말의 FE-SEM 이미지를 보여준다. 합성된 Ti3AlC2 MAX 상의 미세조직은 Fig. 5(a)와 같이 주로 판상형 결정립으로 구성되어 있으며 전형적인 MAX 상의 미세조직을 보여주고 있었다. Fig. 5(b)는 파쇄를 통해 분말화된 Ti3AlC2 MAX 상의 형상을 보여주며, 분말화 이후에도 전형적인 MAX 상의 층상구조를 나타내고 있었다.
또한, 최적 조건에서 합성된 Ti3AlC2 MAX 상의 표면 산화층 및 나노 구조를 확인하기 위해 TEM 분석을 수행하였다. Fig. 6은 DOSS-Ti, Al, graphite 분말을 3:1.1:2의 몰 비율로 혼합하여 합성된 Ti3AlC2 MAX 상 분말의 TEM 이미지를 보여준다. Fig. 6(a)는 합성된 Ti3AlC2 MAX 상 분말의 표면 산화층은 약 2 nm의 두께로 확인되었으며, Fig. 6(b)의 EDS 분석 결과에 따라 Ti, Al 성분이 공존하는 산화물 층으로 식별되었고 이는 이전 연구들과 일치하는 결과를 보여주었다17). 해당 산화물층 영역 바로 아래에 해당하는 결정면은 면으로 확인되었으며 이 때의 면간 거리는 0.2447 nm로 확인되었다. 앞선 Rietveld refinement에서 도출된 3:1.1:2의 비율로 합성된 MAX 상 분말의 면의 면간 거리는 0.2448 nm로 계산되었으며 TEM의 측정 결과와 거의 일치하는 값을 보여주었다.
4. 결 론
본 연구에서는 Ti 스크랩을 활용하여 Ti3AlC2 MAX 상의 상분율을 향상시키기 위한 합성 조건 최적화를 조사하였다. Ti 스크랩으로부터 HDH 및 DOSS 공정을 통해 저산소 Ti를 제조하고, 이를 이용하여 Ti3AlC2 MAX 상을 합성하였다. DOSS 공정에 의해 Ti 스크랩으로부터 제조된 HDH-Ti 분말의 산소 함량은 효과적으로 감소되었다. Ti3AlC2 MAX 상의 합성에서 DOSS-Ti의 입도가 감소할수록 Ti3AlC2 상의 합성 반응이 효과적으로 일어났지만, Ti3AlC2 MAX 상의 산소 함량은 증가하였다. Al 함량에 따른 Ti3AlC2 MAX 상의 합성에서, Al 함량이 1.1일 때 최대 상분율을 나타냈으며, 이후 Al3Ti 및 TiC의 함량이 증가하는 경향이 확인되었다. 최종적으로 최적 합성 조건은 25 ~ 32 μm의 DOSS-Ti, Al, graphite 분말을 3:1.1:2의 몰 비율로 혼합하여 합성되었다. 이 때의 Ti3AlC2, TiC 및 Al3Ti의 상분율은 각각 97.25%, 0.93%, 1.82%로 나타났으며, 25 ~ 45 μm의 Ti3AlC2 MAX 분말의 산소 함량은 4,210 ppm으로 확인되었다. 최적 조건에서 합성된 Ti3AlC2 MAX 상은 주로 판상형 결정립과 전형적인 층상구조를 이루고 있었으며, 약 2 nm의 두께의 표면 산화층을 나타냈다. 결과적으로, 전구체 DOSS-Ti 분말의 입도 및 Al 함량을 제어하여, 저산소 Ti3AlC2 MAX 상 분말의 상분율을 성공적으로 향상시킬 수 있었다.